ОБМЕН ЛИПИДОВ НОВЫЙ.ppt
- Количество слайдов: 113
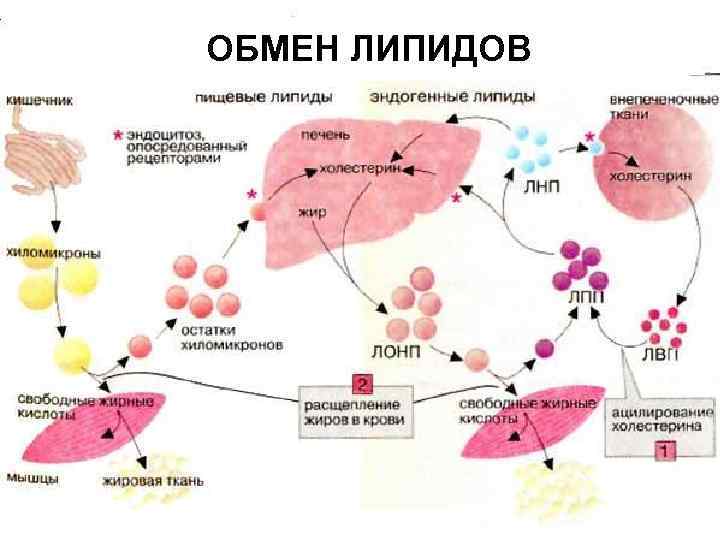
ОБМЕН ЛИПИДОВ Обмен липидов.

Липиды – вещества органической природы, обладающие общим свойством – нерастворимостью в воде, но существенно отличающиеся по структуре и функциям.

Классификация липидов По химическому строению: 1. Высшие жирные кислоты (ВЖК) 2. Глицеринсодержащие липиды • Нейтральные жиры (ТАГ) • Фосфолипиды (ФЛ) 3. Липиды, не содержащие глицерин • Сфинголипиды (СФ) • Стероиды – холестерол (ХС) 4. Липиды, связанные с веществами других классов • Липопротеины (ЛП) • Липополисахариды

По физиологическому значению: 1. Структурные, участвующие в построении мембран (2 -3 кг), например: ФЛ, ХС, СФ и др. 2. Резервные – откладывающиеся в виде ТАГ в подкожно-жировой клетчатке, служащей формой депонирования энергии. 3. Бурый жир – имеющий значение в терморегуляции у грудных детей.

Высшие жирные кислоты. ВЖК - это соединения с длинной неразветвленной цепью углеродных атомов, имеют на одном конце СООН. Наиболее часто встречаются ж. к. с 16, 18, 20 углеродными атомами. В организме насыщенных жирных кислот - 25%, ненасыщенные - 75%. Атомы углерода нумеруются, начиная с карбоксильной группы, ω 3 2 1 СН 3……. СН 2 – СООН а углерод концевой метильной группы – ω (омега) углерод.

Для указания = связей, их положения, было принято такое обозначение: ω – 3 это значит, что двойная связь между 3 и 4 атомами углерода, если их отсчитывать с ω(омега) конца.
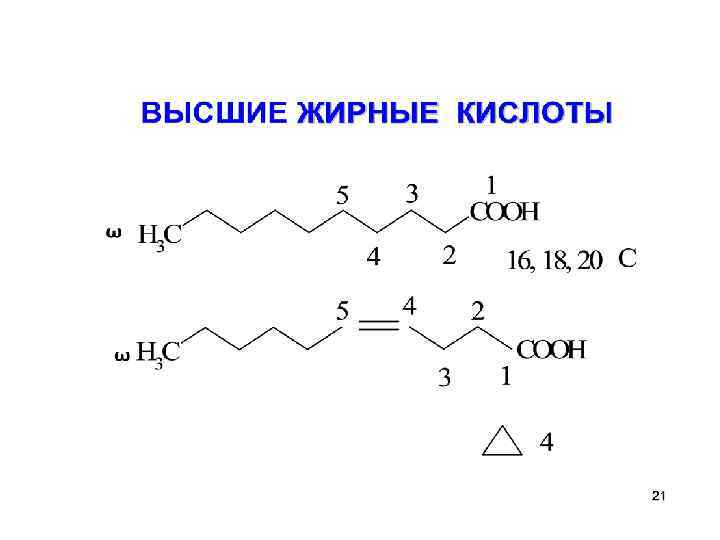


Роль высших жирных кислот 1. Энергетическая. Благодаря окислению ВЖК ткани организма получают более половины всей энергии, только эритроциты и нервные клетки не используют их в этом качестве. Как энергетический субстрат используются, в основном, насыщенные и мононенасыщенные ВЖК.

2. Структурная. ВЖК входят в состав ФЛ, ТАГ, СФ и ЭХС. Наличие полиненасыщенных ЖК (ПНЖК) определяет биологическую активность ФЛ, свойства биологических мембран, взаимодействие ФЛ с мембранными белками и их транспортную и рецепторную активность.

3. Эйкозановые ВЖК являются субстратом для синтеза эйкозаноидов – биологически активных веществ, изменяющих количество ц. АМФ и ц. ГМФ в клетке, модулирующих метаболизм и активность как самой клетки, так и окружающих клеток. Иначе эти вещества называют местные или тканевые гормоны.

4. ПНЖК повышают растворимость ХС, активируя превращения ХС в желчные кислоты и копростанол. 5. Обеспечивают нормальное состояние кровеносных сосудов (способствуют образованию большого количества простациклинов). 6. Стимулируют иммунитет (повышают устойчивость к инфекционным заболеваниям, рентгеновскому облучению).

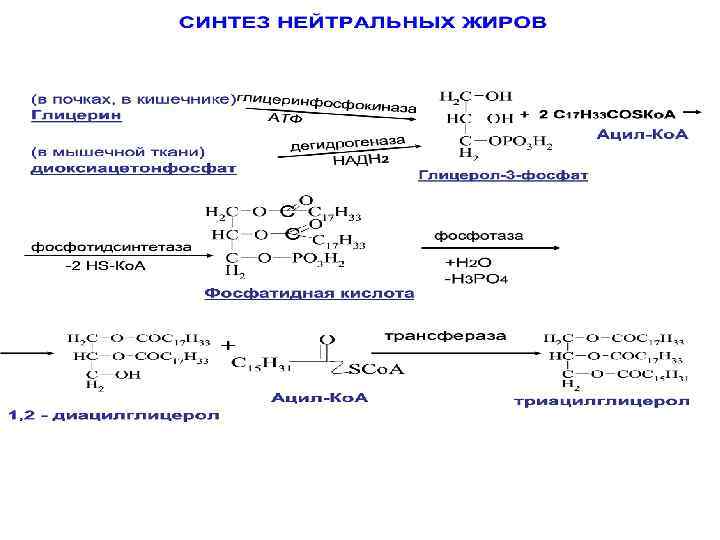
Триацилглицеролы ТАГ являются наиболее распространенными липидами в организме человека. В среднем их доля составляет 16 -23% от массы тела взрослого. В их состав входит 3 -х атомный спирт глицерол и ВЖК: олеиновая кислота 55%, пальмитиновая 20%, линолевая 10%.

ТАГ

Функции ТАГ: • резервно-энергетическая; • теплорегуляторная; • механическая защита тела и внутренних органов; • образование Н 2 О
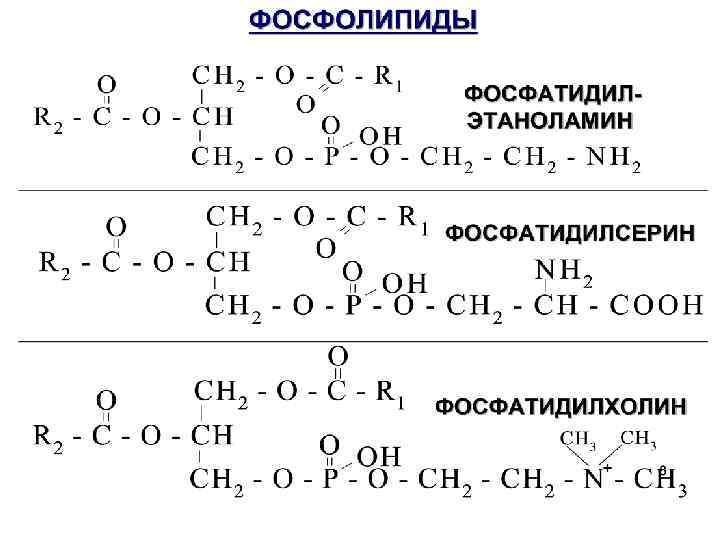

Биологическая роль ФЛ. 1. Входят в состав в мембран, участвуя в их избирательной проницаемости. 2. Дипальмитоилфосфатидилхолин (до 80%), является компонентом сурфактанта, выстилающего альвеолы легких и препятствующей слипанию стенок альвеол во время вдоха.

3. Фосфатидилэтаноламин и фосфатидилхолин мембран взаимодействует с ферментами, образуя комплексы, которые активируют факторы свертывания крови. Фосфатидилсерин активирует процессы фибринолиза. 4. Обладают липотропным действием, препятствуя отложению ТАГ в печени. 5. Продукты их распада участвуют в патогенезе бронхиальной астмы, атеросклероза. 6. Ф-серин влияет на освобождение гистамина.

Холестерол ХС – стероид, характерный только для животных организмов. 50% синтезируется в печени, 15 -20% в тонком кишечнике, остальной – в коже, коре надпочечников, половых железах. В сутки синтезируется 1 г ХС. С пищей поступает 300 -500 мг. N в крови = 3, 9 -5, 2 ммоль/л У новорожденных ХС – 1, 3 -2, 6 ммоль/л В 12 -14 лет – достигает нормы.

Биологическая роль 1. Входит в состав мембран, обуславливая их вязкость и жесткость. 2. Субстрат для синтеза желчных кислот, стероидных гормонов, витамина Д 3. 3. Поддерживает тургор кожи.

ХС

С пищей ежедневно в организм поступает от 80 до 100 г липидов. У грудных детей основной пищей служит молоко, содержащее жиры в эмульгированном виде и переваривание липидов начинается в желудке, под влиянием лингвальной липазы и липазы желудочного сока, которая активна, т. к. р. Н = 5, 0 -5, 5.

Переваривание и всасывание липидов. Переваривание у взрослых в ротовой полости и в желудке не происходит вследствие: - р. Н слюны = 7, 1 -7, 2; р. Н желудочного сока = 1, 5 -2, 5; - жиры в данных отделах ЖКТ не подвергаются эмульгированию. В 12 -перстную кишку (р. Н=8 -9, 0) поступает панкреатический сок, содержащий парные желчные кислоты и ферменты, расщепляющие различные липиды.

В печени из ХС синтезируются первичные желчные кислоты (холевая, дезоксихолевая), затем они образуют конъюгаты с глицином (гликохолевая) или с таурином (таурохолевая). Роль желчных кислот: - усиливают перистальтику кишечника; - эмульгируют жиры; - участвуют в образовании мицелл, способных всасываться.

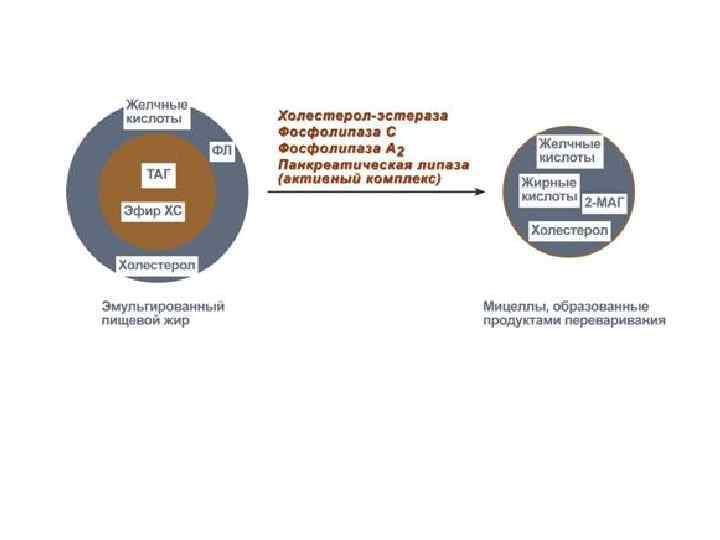
В кишечнике ТАГ-липаза расщепляет ТАГ до 2 моноацилглицеролов (2 -МАГ) и ВЖК, холестеролэстераза - ЭХС до ХС и ВЖК, фосфолипаза – ФЛ до глицерина, ВЖК, Н 3 РО 4 и азотсодержащие соединения.

Образование мицелл Образовавшиеся 2 -МАГ, ВЖК и ХС, формируют гидрофобное ядро мицеллы. В ядро также входят жирорастворимые витамины. Снаружи ядра находятся молекулы желчных кислот (гидрофильная часть). Глицерол всасывается в кровь. Образовавшиеся мицеллы помогают всасываться нерастворимым липидам.

Кишечно – печеночная циркуляция Мицеллы диффундируют внутрь клеток подвздошной кишки. Липидные компоненты остаются в просвете кишечника. Желчные кислоты попадают через воротную вену в печень, из печени вновь секретируются в желчный пузырь и далее опять в 12 -перстную кишку. Этот путь желчных кислот называют кишечно – печеночной циркуляцией. Каждая молекула желчных кислот за сутки проходит 58 циклов, и около 5% желчных кислот выделяется с фекалиями. Новые молекулы желчных кислот синтезируются из ХС.
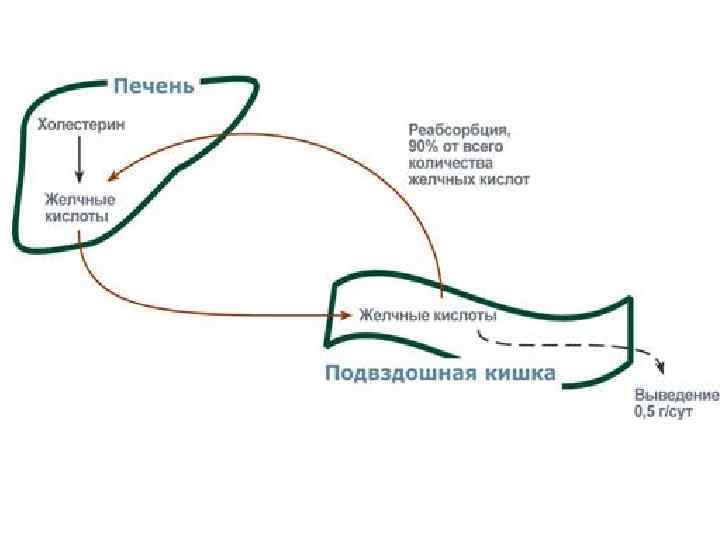

Ресинтез липидов в энтероцитах. Ресинтез жиров – это синтез липидов в стенке кишечника из поступающих экзогенных жиров, иногда могут использоваться и эндогенные ВЖК. Основная задача – адаптировать состав жиров пищи к составу жиров организма и связать поступившие с пищей средне- и длинноцепочечные ВЖК со спиртом – глицеролом или ХС. Это ликвидирует их детергентное действие на мембраны, и осуществляют транспорт по крови в ткани.

Нарушения переваривания и всасывания жиров. В результате нарушения переваривания и всасывания жиров – возникает стеаторея (жирный стул). В норме содержание жиров в фекалиях составляет не более 5%. При стеаторее нарушается всасывание жирорастворимых витаминов (авитаминозы) и незаменимых жирных кислот).

Причины возникновения стеатореи. 1. Снижение желчеобразования в результате недостаточного синтеза желчных кислот и ФЛ при болезнях печени, гиповитаминозах. 2. Снижение желчевыделения (цирроз, желчнокаменная болезнь и др. ). У детей часто причиной может быть перегиб желчного пузыря, который сохраняется и во взрослом состоянии. 3. При недостатке панкреатический липазы (острый и хронический панкреатит, острый некроз). 4. Недостаточность синтеза пищеварительных ферментов и ферментов ресинтеза липидов в энтероцитах при белковой и витаминной недостаточности.

Транспорт липидов Поскольку липиды являются гидрофобными молекулами, то они транспортируются по крови в составе особых частиц –ЛП. Все типы ЛП имеют сходное строение: гидрофобное ядро, состоящее из ТАГ и ЭХС и гидрофильной поверхности, образованной белками, ФЛ и ХС.


Белки в ЛП обычно называются апобелками, выделяют несколько их типов – А, В, С, D, Е. В каждом классе ЛП находятся соответствующие ему апобелки, выполняющие структурную, ферментативную и кофакторную функции.

Хиломикроны и ЛПОНП. Транспорт ТАГ из кишечника в ткани (экзогенные ТАГ) осуществляется в виде хиломикронов (ХМ), от печени к тканям (эндогенные ТАГ) – в виде липопротеинов очень низкой плотности (ЛПОНП). В крови ХМ подвергаются действию липопротеинлипазы (ЛПЛ) эндотелия, которая отщепляет ВЖК от ТАГ. ВЖК соединяются с альбуминами (ЛПОВП) и разносятся в различные ткани. В результате количество ТАГ в ХМ резко снижается и образуются остаточные ХМ, которые транспортируются в гепатоциты.

В жировой ткани в абсорбтивный период ВЖК депонируются в виде ТАГ, в сердечной мышце работающих скелетных мышцах используются как источник энергии. В печени образуются ЛПОНП, которые поступают в кровь, где также взаимодействуют с ЛПЛ эндотелия, которая расщепляет ТАГ. ВЖК переходят в ткани или, связываясь с альбуминами (ЛПОВП), разносятся по организму. В результате образуются остаточные ЛПОНП, которые поступают либо в печень, либо после воздействия на них печеночной ТАГ-липазы превращаются в липопротеины низкой плотности (ЛПНП).

Мобилизация ТАГ (липолиз). Активируется: - при физиологических ситуациях – стресс, мышечная работа, голодание; - при патологических – сахарный диабет (СД) 1 -го типа, Базедова болезнь, стероидный диабет и др.

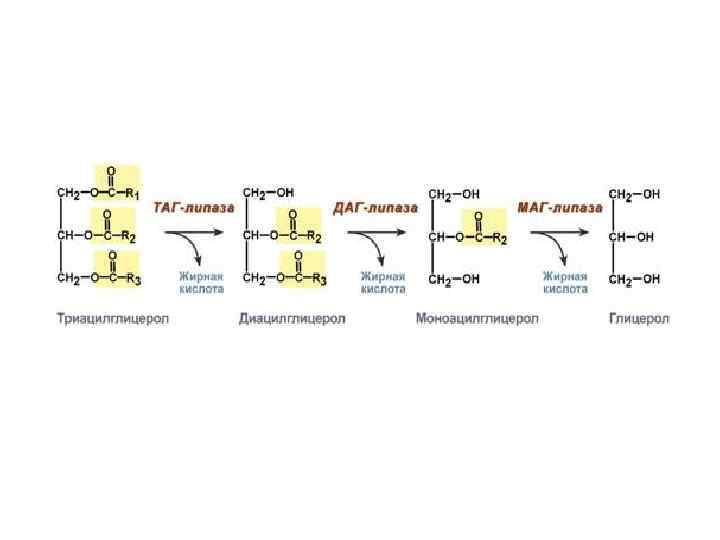
Под влиянием гормончувствительной ТАГлипазы происходит отщепление первой ВЖК от ТАГ с образованием диацилглицерола (ДАГ). ДАГ под влиянием ДАГ-липазы расщепляется до моноацилглицерола (МАГ), являющегося субстратом для МАГ-липазы. В результате образуются ВЖК и глицерол, которые покидают клетку.
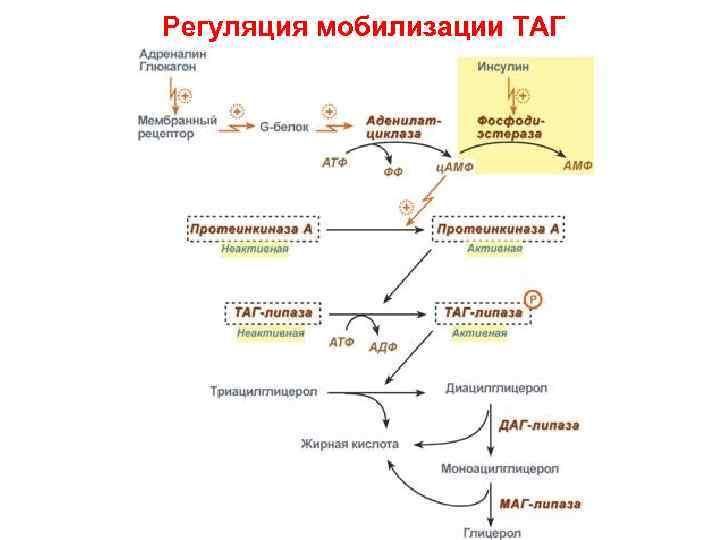
Регуляция мобилизации ТАГ

СТГ увеличивает количество АЦ. Глюкокортикоиды способствуют синтезу ТАГ- липазы по внутриклеточному механизму; Инсулин тормозит липолиз: - активирует фермент фосфодиэстеразу; - дефосфорилирует ТАГ-липазу, ингибируя ее активность.

Глицерол с кровью доставляется в печень и почки, где фосфорилируется и окисляется в метаболит гликолиза диоксиацетонфосфат (ДАФ) В зависимости от условий ДАФ может включаться в реакции глюконеогенеза (при долгосрочном голодании, интенсивной мышечной нагрузке) или окисляться в гликолизе до ПВК.
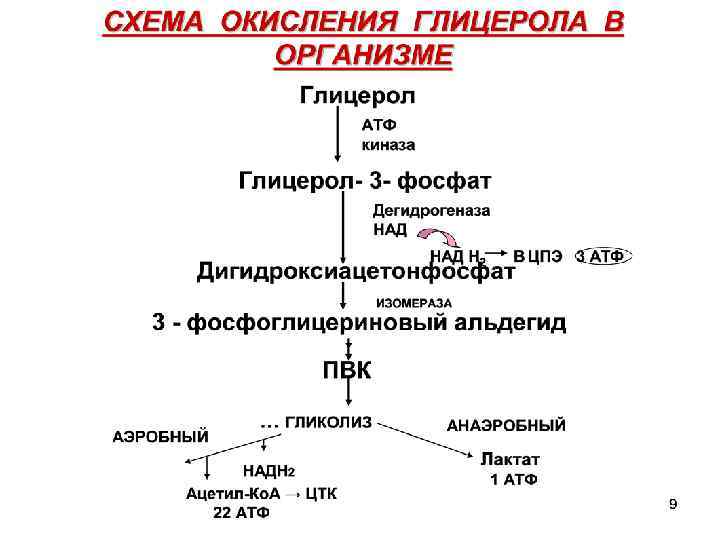

Метаболизм ВЖК. β-окисление ВЖК. Для преобразования энергии, заключенной в ВЖК, в энергию связей АТФ существует метаболический путь окисления ВЖК до СО 2 и воды, тесно связанный с ЦТК и дыхательной цепью. Этот путь называется β-окисление, т. к. происходит окисление 3 -го углеродного атома ВЖК (β-положение).

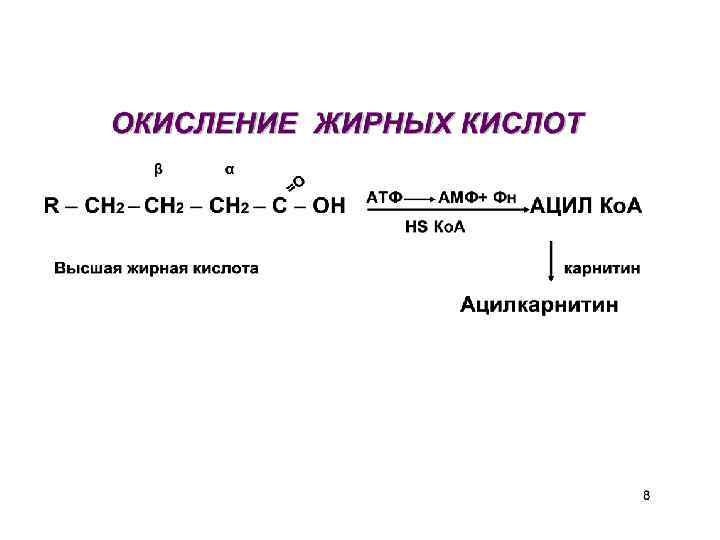
Этапы окисления жирных кислот I этап – подготовительный, протекает в цитозоле. В результате происходит активирование ВЖК с образованием ацил- SКо. А. II этап - Ацил-S-Ко. А соединяется с витаминоподобным веществом карнитином.

Карнитин синтезируется в печени и почках и затем транспортируется в остальные органы. Во внутриутробном периоде и в первые годы жизни значение карнитина для организма чрезвычайно важно. Энергообеспечение нервной системы детского организма и, в частности, головного мозга осуществляется за счет двух параллельных процессов: карнитинзависимого окисления ВЖК и аэробного окисления глюкозы.

Карнитин необходим для роста головного и спинного мозга, для взаимодействия всех отделов нервной системы, ответственных за движение и взаимодействие мышц. Существуют исследования, связывающие с недостатком карнитина детский церебральный паралич и феномен "смерти в колыбели".

Процесс собственно β-окисления состоит из 4 -х реакций, повторяющихся циклически. Реакции протекают в митоходриях. В них последовательно происходит: - Дегидрирование - Гидратация - Второе дегидрирование - Тиолиз

В последней реакции от ВЖК отщепляется ацетил-SКо. А. К оставшейся (укороченной на два углерода) ВЖК присоединяется HS-Ко. А, и она возвращается в первую реакцию (дегидрирование). Все повторяется до тех пор, пока в последнем цикле не образуются две молекулы ацетил-SКо. А.
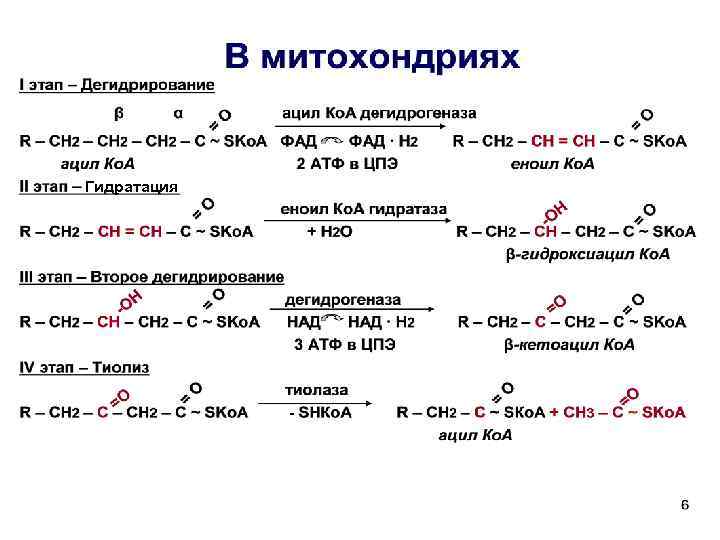
Гидратация


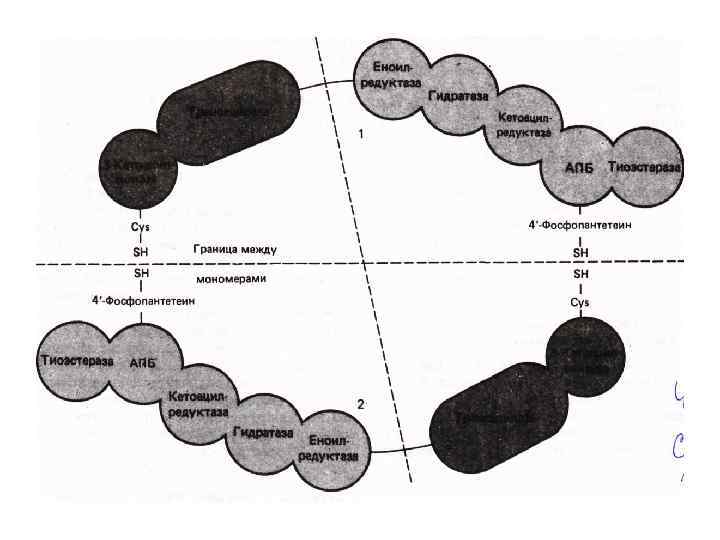
Синтез жирных кислот (липогенез). Синтез наиболее активно происходит в цитозоле клеток печени, кишечника, жировой ткани, в состоянии покоя или после еды. Особенности: 1. Протекает в цитоплазме. 2. Происходит синтез только пальмитиновой кислоты. 3. Принимает участие АПБ – полиферментный комплекс, состоящий из 6 ферментов. 4. Необходимо участие реакций карбоксилирования, СО 2, АТФ, НАДФ∙Н 2.
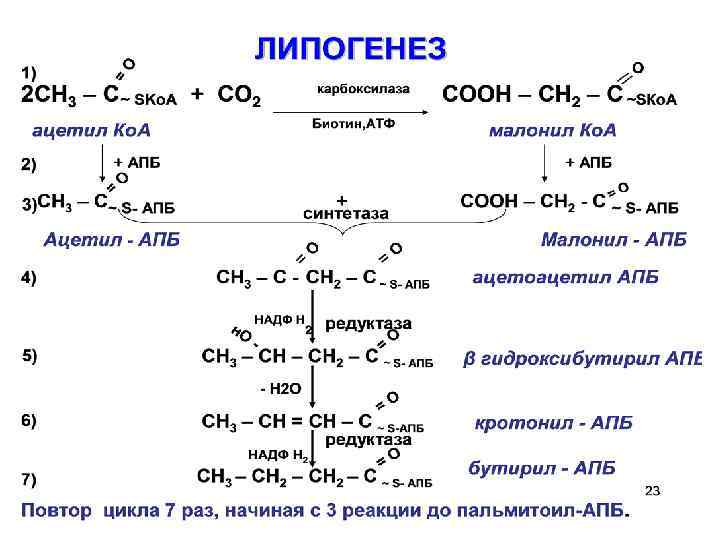

Удлинение пальмитиновой кислоты происходит с участием ацетил-Ко. А, с образованием стеариновой кислоты. В печени и в тканях мозга из стеариновой кислоты образуются ВЖК с длинной углеродной цепью от С 20 до С 24, необходимых для образования глико- и сфинголипидов. Из ненасыщенных ВЖК в организме синтезируется только олеиновая в результате дегидрирования стеариновой кислоты (десатурация) – под влиянием ферментов десатураз, которые могут образовывать двойные связи только у 9 углеродного атома, ω-3 и ω -6 не синтезируются в организме и обязатель-но должны поступать с пищей.

Гормональная регуляция Ключевым ферментом синтеза ВЖК – карбокси- лаза, активность которого регулируется: - глюкагон, адреналин, по аденилатциклазному механизму вызывают ее фосфорилирование, она становится неактивной и липогенез тормозится; - инсулин вызывает дефосфорилирование карбоксилазы, которая становится активной и стимулируется липогенез; по внутриклеточному механизму инсулин - индуктор синтеза карбоксилазы.

Ожирение – полигенное заболевание, сопро- вождающееся накопление ТАГ в адипоцитах, которое является фактором риска развития инфаркта миокарда, инсульта, СД, гипертонической и желчнокаменной болезни. Первичное – развивается в результате алиментарного дисбаланса – избыточное калорийное питание по сравнению с расходованием энергии. Причины: - генетические нарушения до 80%; - состав и количество потребляемой пищи; - система питания в семье; - уровень физической активности; - психологические факторы.

У людей, склонных к ожирению, имеется более прочное сопряжение дыхания и окислительного фосфорилирования, т. е. более эффективный метаболизм. Возможно разное соотношение аэробного и анаэробного гликолиза. Анаэробный гликолиз (как менее эффективный) «сжигает» гораздо больше глюкозы, в результате снижается ее превращение в жиры.

У человека обнаружен ген ожирения. Продуктом экспрессии этого гена служит белок лептин, который содержит 167 аминокислотных остатков, взаимодействует с рецептором гипоталамуса, в результате снижается секреция нейропептида У, подавляя пищевое поведение. У 80% больных концентрация лептина в крови тучных людей больше в 4 раза чем у нормы. У 80% лиц с первичным ожирением гипоталамус нечувствителен к лептину, у 20% - дефект структуры лептина.

Вторичное – развивающееся в результате какого-либо основного заболевания, чаще эндокринного. Например, б-нь Иценко-Кушинга и др.
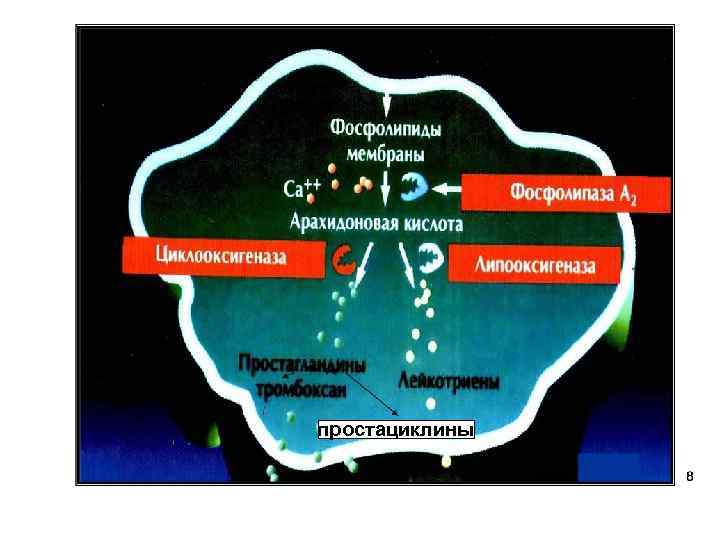
простациклины
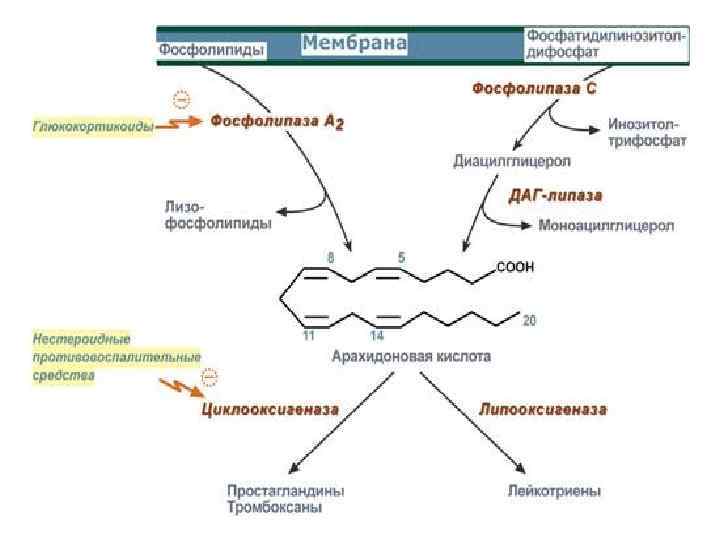

От ФЛ мембран под действием фосфолипазы А 2, отщепляется арахидоновая кислота, которая используется для синтеза эйкозаноидов. Активируют фосфолипазы: гормоны, гистамин, цитокины, гипоксия, иммунные воздействия и др. В клетках имеется 2 основных пути превраще-ния арахидоновой кислоты: 1 – циклооксигеназный, приводящий к синтезу простагландинов – предшественников тромбоксанов и простациклинов; 2 – липооксигеназный, заканчивающийся образо -ванием лейкотриенов.

Простагландины 1. Влияют на сокращение гладких мышц. 2. Способствуют секреторной функции желудка. 3. Участвуют в воспалительных реакциях. 4. Модулируют действие гормонов. 5. Влияют на гемодинамику почек. 6. Автономно регулируют нервное возбуждение.

Простациклины– образуются в стенках кровеносных сосудов сердца, матки, слизистых желудка. 1. Расслабляют гладкую мускулатуру 2. Способствуют фибринолизу, и тем самым препятствует свертыванию крови.

Тромбоксаны являются антагонистами простациклинов, образуются в тромбоцитах, в мозге, способствуют свертыванию крови: - вызывают агрегацию тромбоцитов; - оказывают сосудосуживающее действие. Накопление служит причиной тромбоза, атеросклероза.

Лейкотриены в лейкоцитах, макрофагах. 1. Вызывают сокращение гладких мышц дыхательных путей. 2. Стимулируют секрецию гликопротеинов, увеличивают количество слизи в дыхательных путях. 3. Участвуют в аллергических и иммунологических реакциях. 4. Повышают проницаемость сосудов. Затрудненное дыхание при бронхиальной астме связано с действием лейкотриенов.

Жировое перерождение печени. Гепатоциты переполняются ТАГ, разрушаются, образуются кисты, вокруг них разрастается соединительная ткань, развивается жировая дистрофия. Главной причиной является нарушения синтеза ЛПОНП. Так как ЛПОНП включают разнородные соединения, то блок может возникнуть на разных уровнях синтеза:

• недостаток апобелков – нехватка белка или незаменимых аминокислот в пище, воздействие токсинов и ингибиторов синтеза белка; • снижение синтеза ФЛ – отсутствие липотропных факторов (витаминов, метионина, ПНЖК, холина), из-за чего не формируется оболочка ЛП; • нарушение секреции ЛП в кровь – патология мембран гепатоцитов при активации ПОЛ вследствие недостаточности антиоксидантных систем (гиповитаминозы С, А, Е, нехватка цинка и железа).

Процесс синтеза ХС происходит в цитозоле клеток, это один из самых длинных метаболических путей в организме человека, включает около 100 последовательных реакций.
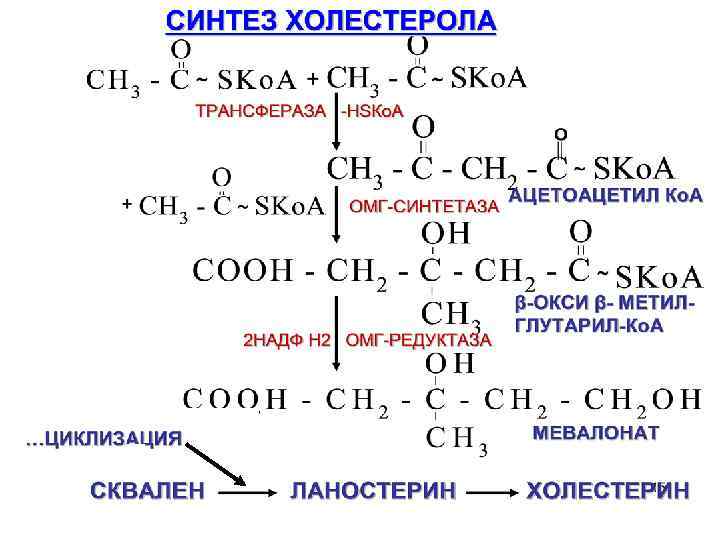
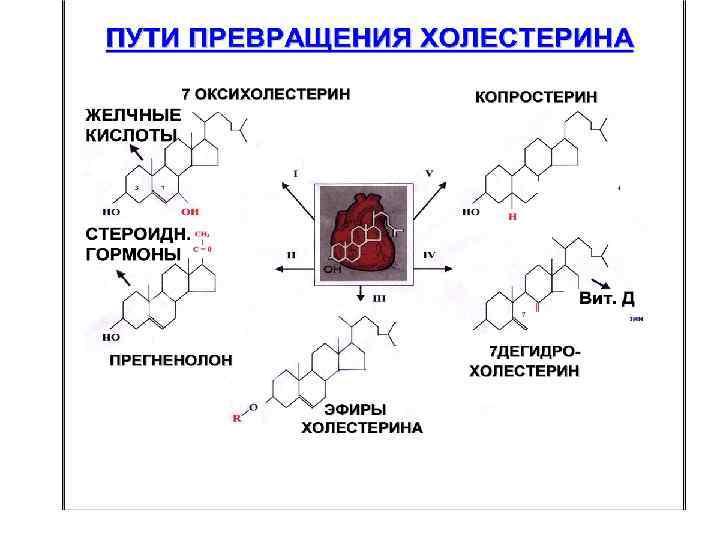

Пути превращения ХС. 1. Окисление. В печени ХС окисляется в желчные кислоты (80%), в коре надпочечников в стероидные гормоны (3%). В результате - в молекуле ХС появляются полярные группы, гидроксилы, карбоксилы, повышается его растворимость в воде, что способствует выведению из организма.

2. Этерификация. Образование эфиров ХС. ЭХС составляют около 10% от общего количества ХС в организме. При этом растворимость уменьшается и это приводит к его накоплению. У новорожденных относительно низкий коэффициент этерификации по сравнению с более старшим возрастом детей = 0, 58 -1 ммоль/л, что связано с дефицитом ПНЖК. 3. Дегидрирование. В положении 7, 8 образуются двойные связи, что приводит к образованию 7 -дегидрохолестерола (предшественника витамина Д 3).

Выведение холестерола. Чтобы поддерживать постоянный уровень его в организме необходимо выводить 1, 5 г в сутки. 1 г в сутки окисляется в желчные кислоты, 200 -300 мг в сутки с калом в виде копростанола, 100 мг со слущенным эпителием, 40 мг - на синтез стероидных гормонов, с мочой 1 -2 мг в сутки.

Транспорт холестерола и его эфиров в организме. Транспорт холестерола и его эфиров осуществляется липопротеинами низкой и высокой плотности.

Липопротеины низкой плотности - образуются в гепатоцитах de novo и в сосудистой системе печени под воздействием печеночной ТАГ-липазы из ЛПОНП, - основным апобелком является апо. В-100, - нормальное содежание в крови 3, 2 -4, 5 г/л, - самые атерогенные.

Функции 1. Транспорт холестерола в клетки половых желез, коры надпочечников, кожы, печени. 2. Транспорт ПНЖК в виде эфиров ХС в некоторые клетки рыхлой соединительной ткани (фибробласты, тромбоциты, эндотелий, гладкомышечные клетки), в эпителий гломерулярной мембраны почек, в клетки костного мозга, в клетки роговицы глаз, в нейроциты, в базофилы аденогипофиза.

Клетки рыхлой соединительной ткани активно синтезируют эйкозаноиды. Поэтому им необходим постоянный приток ПНЖК, что осуществляется либо переходом фосфолипидов от оболочки ЛПВП в мембраны клеток либо поглощением ЛПНП, которые несут ПНЖК в виде эфиров холестерола. Особенностью всех этих клеток является наличие лизосомальных кислых гидролаз, расщепляющих эфиры ХС. У других клеток таких ферментов нет.

Обмен 1. В крови первичные ЛПНП взаимодействуют с ЛПВП, отдавая свободный ХС и получая этерифицированный. В результате в них происходит накопление эфиров ХС, увеличение гидрофобного ядра и "выталкивание" белка апо. В 100 на поверхность частицы. Таким образом, первичный ЛПНП переходит в зрелый. 2. На всех клетках, использующих ЛПНП, имеется высокоафинный рецептор, специфичный к ЛПНП – апо. В-100 -рецептор. При взаимодействии ЛПНП с рецептором происходит эндоцитоз липопротеина и его лизосомальный распад на составные части – фосфолипиды, белки (и далее до аминокислот), глицерол, жирные кислоты, холестерол и его эфиры.

• ХС превращается в гормоны или включается в состав мембран; • при невозможности удалить ХС часть его этерифицируется с олеиновой кислотой ферментом ацил-SКо. А: холестерол-ацилтрансферазой (АХАТ). ПНЖК, образованные при распаде ЭХС используются для синтеза эйкозаноидов или фосфолипидов. Остаточный ХС удаляется из клеток с составе ЛПВП.

Липопротеины высокой плотности. - образуются в печени de novo, в плазме крови при распаде хиломикронов, некоторое количество в стенке кишечника; - основным апобелком является апо А 1, содержат апо. Е и апо. СII.

Функции 1. Осуществляют транспорт свободного ХС от тканей к печени. 2. Фосфолипиды ЛПВП являются источником полиеновых кислот для синтеза клеточных фосфолипидов и эйкозаноидов.

Метаболизм. 1. Синтезированный в печени ЛПВП первичный) содержит в основном фосфолипиды и апобелки. Остальные липидные компоненты накапливаются в нем по мере метаболизма в плазме крови. 2. В ЛПВП активно протекает реакция при участии лецитин: холестерол-ацилтрансферазы (ЛХАТ-реакция). В этой реакции остаток полиненасыщенной жирной кислоты переносится от ФХ на свободный ХС с образованием лизофосфатидилхолина (л. ФХ) и эфиров ХС.

3. Взаимодействует с ЛПНП и ЛПОНП, которые являются источником свободного ХС для ЛХАТреакции, в обмен ЛПВП отдают эфиры ХС. 4. Взаимодействуя с ЛПОНП и ХМ, получают ТАГ и отдают им апо. Е- и апо. СII-белки. 5. При посредстве специфических транспортных белков получают свободный ХС из клеточных мембран. 6. Взаимодействует с мембранами клеток, отдает часть фосфолипидной оболочки, доставляя таким образом полиеновые жирные кислоты в клетки. 7. Накопление свободного ХС, ТАГ, лизо. ФХ и утрата фосфолипидной оболочки преобразует ЛПВП 3 (условно его можно назвать "зрелый") в ЛПВП 2 ("остаточный"). Последний захватывается гепатоцитами при помощи апо. А-1 -рецептора.

Регуляция метаболизма холестерола. Регуляторным ферментом является ОМГ- редуктаза, активность которой может изме-няться в 100 и более раз.

1. Метаболическая регуляция – по принципу обратной отрицательной связи фермент ингибируется конечным продуктом реакции – холестеролом. Это помогает поддерживать внутриклеточное содержание холестерола постоянным. Избыток ХС по приципу обратной связи подавляет образование новых рецепторов к ЛПНП, их количество уменьшается и клетка связывает меньше ЛПНП.

2. Гормональная регуляция. Глюкагон и адреналин посредством аденилатциклазного механизма активируют протеинкиназу А, которая фосфорилирует фермент и переводит его в неактивную форму, синтез ХС тормозится. Глюкагон подавляет количество рецепторов к ЛПНП. Инсулин фосфорилирует ОМГ-редуктазу, способствуя переходу в активное состояние, синтез ХС стимулируется. Инсулин, Т 3, половые гормоны увеличивают количество рецепторов.

Патология обмена ХС. Гиперхолестеринемия – повышение уровня ХС в крови при норме 3, 9 -5, 2 ммоль/л. Факторы риска: 1. Гиперкалорийное питание (избыточное поступление углеводов, жиров) 2. Гиподинамия 3. Курение 4. Сопутствующие заболевания (гипертоническая болезнь, сахарный диабет, гипотиреоз, ожирение) 5. Стресс (адреналин приведет к синтезу ацетил. Коа → ХС).

Атеросклероз. Заболевание, связанное с накоплением холестерола и его эфиров, в ЛПНП, в эндотелии сосудов.


В области бляшки часто образуются тромбы, суживающие просвет сосуда, что приводит к острому нарушению кровообращения и развитию инфаркта миокарда, инсульта.


Желчнокаменная болезнь. Патологический процесс, при котором в желчном пузыре образуются камни, основу которых составляет ХС. Выделения ХС в желчь должно сопровождаться пропорциональным выделением желчных кислот и ФЛ, удерживающих гидрофобные молекулы ХС в желчи в мицеллярном состоянии. Если эти пропорции нарушены, то ХС начинает осаждаться в желчном пузыре, образуя вязкий осадок, который постепенно становится твердым. Камни могут состоять не только из холестерола (белого цвета), но и из смеси ХС, билирубина, белков, кальция – смешанные (коричневого цвета).

Причины: гиперкалорийное питание, избыток ХС в пище, застой желчи, нарушение энтерогепатической циркуляции желчных кислот, а также их синтеза, инфекции желного пузыря.

Дислипопротеинемии Нарушения обмена липопротеинов – дислипопротеинемии. Причины: изменение активности ферментов обмена липопротеинов, снижение рецепции липопротеинов на клетках, нарушения синтеза апобелков.

Тип I. Гиперхиломикронемия. Обусловлена генетической недостаточностью липопротеинлипазы. Клинически проявляется в раннем возрасте ксантоматозом и гепатоспленомегалией в результате отложения липидов в коже, печени и селезенке.

Тип II. Гипер-β-липопротеинемия Подтип IIа (семейная гиперхолестеролемия) Причин существует много. Различные мутации затрагивают синтез ЛПНП, апо-В-100, рецепцию. Уровень ХС-12 -20 ммоль/л. Клинически проявляется атеросклеротическими нарушениями. Первичная гипер-β-липопротеинемия встречается более часто и наблюдается уже в раннем возрасте, в случае гомозиготной формы заканчивается летальным исходом от инфаркта миокарда в молодом возрасте.

Метаболизм кетоновых тел. К кетоновым телам относятся: • Ацетоуксусная кислота • β оксимасляная (β окси-бутират) • Ацетон В норме 0, 9 -1, 7 ммоль/л (1 -3 мг/дл)

Функции кетоновых тел: 1. Источник энергии (ацетоацетат 33 АТФ, β оксибутират 21 АТФ). 2. Регуляторная (регулирует скорость липолиза в жировых клетках). Образование кетоновых тел идет в печени.
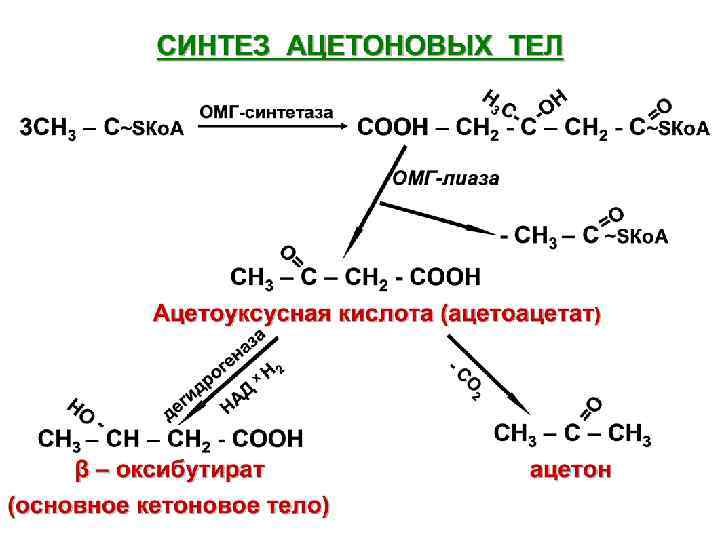

Из печени они поступают в периферические ткани: скелетные мышцы сердца. Мозг потребляет кетоновые тела только при недостатке глюкозы. В периферических тканях кетоновые тела окисляются с образованием энергии. У детей они служат дополнительным энергетическим материалом в период активного роста.

Но часто из-за несовершенства регуляции обменных процессов, диетических ошибок (кетогенная пища), переутомления могут привести к накоплению большого количества кетоновых тел 20 -30 ммоль/л (при Ν – 1, 7 ммоль/л). При этом возникает ацидоз на ранней стадии, кетоз – поздней. Понижается р. Н крови, ацетонемическая рвота, запах ацетона при дыхании. Об этой – детской патологии должно быть известно каждому педиатру. Развитие этого состояния может перейти в кому и вызвать смерть. Кетоз может возникнуть при сахарном диабете, при голодании, при беременности, при токсикозе.
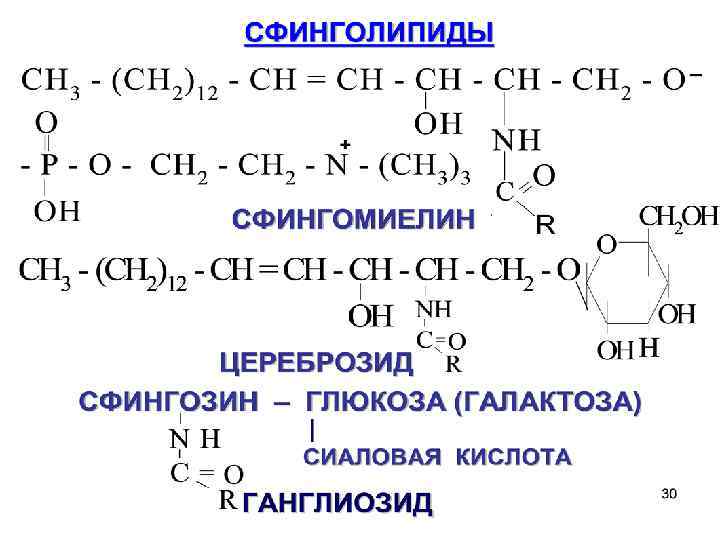

Биологическая роль. 1. Структурная функция, входят в наружный слой плазматической мембраны, участвует в межклеточных контактах. 2. Карбоксильная группа сиаловых кислот, придает мембране отрицательный заряд и эти соединения способны связывать Νа, К изменяя их распределение в мозговой ткани. 3. Сфингомиелины- в передаче нервного импульса.

Сфинголипидозы. Это генетические наследственные заболевания, когда из-за отсутствия ферментов происходит неполное расщепление сфинголипидов.
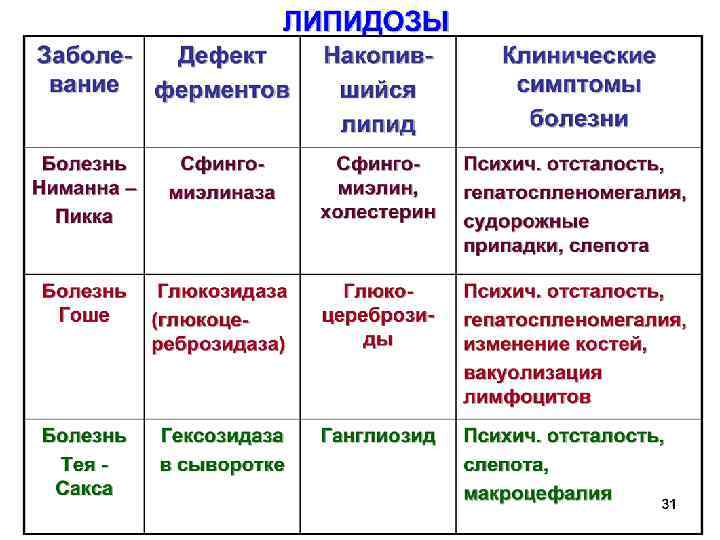

Нимана – Пика редко встречается заболевание 6 типов. Накопление сфингомиелина, во внутренних органах и нервных тканях. Нет фермента сфингомиелиназы. А - форма. (В грудном возрасте) клиника: задержка роста, умственного развития, гепатоспленомегалия, частые респират. инфекции и слепота (вишнево красное пятно на сетчатке глаз в 50% случаев). Смерть в возрасте 3 -4 х лет.

Гоше часто встречающейся липидоз 3 формы накопления цереброзидов: 1. Инфантильная. В первые месяцы задержка роста, нервнопсихические нарушения, неврол Неврологические расстройства, заканчивающиеся смертью до 1 год 2. Ювенильная. На втором году - умственное оставани, гепатоспленомегалия, неврологические расстройства (судороги, мышечная гипотония), заболевание костей, погибают с 6 -лет. 3. Взрослая (висцеральная). Отложение во внутренних органах и костях. Нет или редко умственные отставания и неврологические расстройства.

Болезнь Тея-Сакса у евреев в 4 -6 месяцев – ганглиозидоэ Клиника: мышечная гипотрофия, неврологические изменения, полная слепота. У детей 1 года жизни чаще наблюдается болезнь Нимана-Пика, а после года – болезнь Гоше.
ОБМЕН ЛИПИДОВ НОВЫЙ.ppt