52abb27fc0df4fda245f1d740471d3b2.ppt
- Количество слайдов: 33

ОБЕСПЕЧЕНИЕ ПОЛНОЦЕННОГО ЭТИОТРОПНОГО ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА С. Е. Борисов, Т. И. Иванушкина, Д. А. Иванова, Н. В. Литвинова, Ю. Ю. Гармаш Московский городской научно-практический Центр борьбы с туберкулезом Департамента здравоохранения города Москвы Российская медицинская академия последипломного образования, терапевтический факультет, кафедра фтизиатрии г. Екатеринбург, 12 апреля 2012 г.

ХИМИОТЕРАПИЯ — лечение инфекционного, паразитарного или злокачественного заболевания с помощью ядов или токсинов, губительно воздействующих на инфекционный агент — возбудитель заболевания, на паразитов или на клетки злокачественных опухолей при сравнительно меньшем отрицательном воздействии на организм хозяина Яд или токсин при этом называется химиопрепаратом, или химиотерапевтическим агентом

• ЦЕЛЬ ФАРМАКОТЕРАПИИ В ОБЩЕМ СМЫСЛЕ - коррекция тех или иных нарушений жизнедеятельности организма, восстановление или улучшение функций пораженных органов и систем. • ЦЕЛЬ ХИМИОТЕРАПИИ - уничтожение, убийство или, по крайней мере, торможение размножения паразитов, инфекционных агентов или злокачественных клеток, по возможности с меньшим повреждающим действием на организм хозяина. Нормализация жизнедеятельности и улучшение функций пораженных органов и систем при этом достигаются вторично, как следствие уничтожения или ослабления причины, вызвавшей заболевание — инфекции, опухоли или паразитарной инвазии.

ВОЗБУДИТЕЛИ ТУБЕРКУЛЕЗА Класс: Schizomycetes Порядок: Actinomicetalis Семейство: Mycobacteriaceae Род: Mycobacterium (включает более 140 видов) M. tuberculosis complex Ø M. tuberculosis humanus Ø M. tuberculosis bovis (в том числе M. bovis-BCG) Ø M. tuberculosis africanum Ø M. tuberculosis microti Ø M. tuberculosis canetti Ø M. caprae ØM. pinnipedii
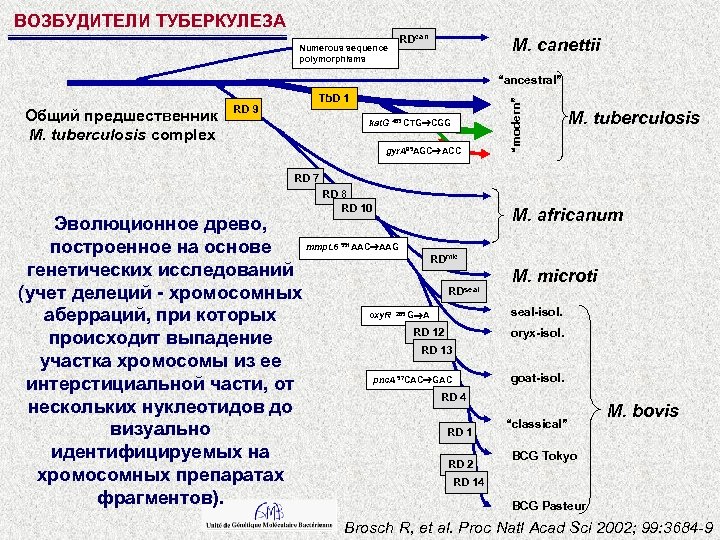
ВОЗБУДИТЕЛИ ТУБЕРКУЛЕЗА RDcan Numerous sequence polymorphisms M. canettii Общий предшественник M. tuberculosis complex RD 9 Tb. D 1 kat. G 463 CTG CGG gyr. A 95 AGC ACC “modern” “ancestral” M. tuberculosis RD 7 RD 8 RD 10 Эволюционное древо, mmp. L 6 построенное на основе генетических исследований (учет делеций - хромосомных аберраций, при которых происходит выпадение участка хромосомы из ее интерстициальной части, от нескольких нуклеотидов до визуально идентифицируемых на хромосомных препаратах фрагментов). M. africanum 551 AAC AAG RDmic RDseal oxy. R M. microti seal-isol. 285 G A RD 12 oryx-isol. RD 13 goat-isol. pnc. A 57 CAC GAC RD 4 RD 1 RD 2 “classical” M. bovis BCG Tokyo RD 14 BCG Pasteur Brosch R, et al. Proc Natl Acad Sci 2002; 99: 3684 -9

ВОЗБУДИТЕЛИ ТУБЕРКУЛЕЗА Грам-положительные микроорганизмы Грам-отрицательные микроорганизмы Липидный бислой клеточной мембраны большинства Грам+ микроорганизмов покрыт пористым пептидогликановым слоем, который не вполне защищает от антимикробных агентов липидный бислой; Имеют две мембраны. Внешняя мембрана функционирует как эффективный барьер проницаемости, так как состоит из липополисахаридов (ЛПС) и транспортных каналов. липиды вместе с ЛПС; миколаты пептидогликан; арабиногалактан каналы глицериды липоарабиноманнан Микобактерии продуцируют многослойную толстую клеточную оболочку, богатую миколовыми кислотами и исключительно эффективно выполняющую барьерные функции.
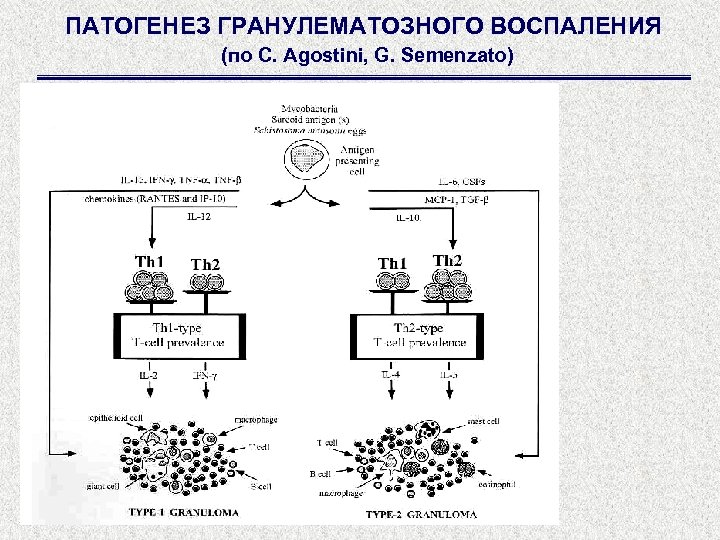
ПАТОГЕНЕЗ ГРАНУЛЕМАТОЗНОГО ВОСПАЛЕНИЯ (по C. Agostini, G. Semenzato)
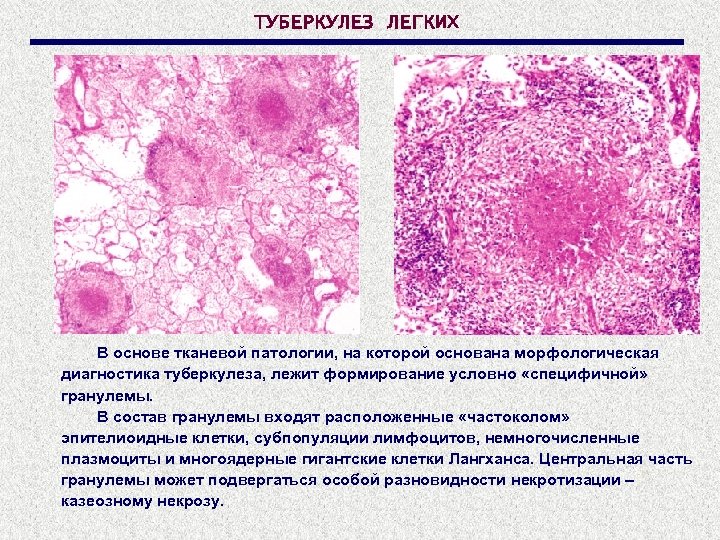
ТУБЕРКУЛЕЗ ЛЕГКИХ В основе тканевой патологии, на которой основана морфологическая диагностика туберкулеза, лежит формирование условно «специфичной» гранулемы. В состав гранулемы входят расположенные «частоколом» эпителиоидные клетки, субпопуляции лимфоцитов, немногочисленные плазмоциты и многоядерные гигантские клетки Лангханса. Центральная часть гранулемы может подвергаться особой разновидности некротизации – казеозному некрозу.

ОСОБЕННОСТИ МИКОБАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ Ø Способность возбудителя к внутриклеточному существованию (персистенции) и размножению Ø Превращение предназначенных для выполнения защитных функций фагоцитов в «фармакологические убежища» для микобактерий Ø Трансформация фагоцитов и превращение их в источник дисбаланса иммунной системы
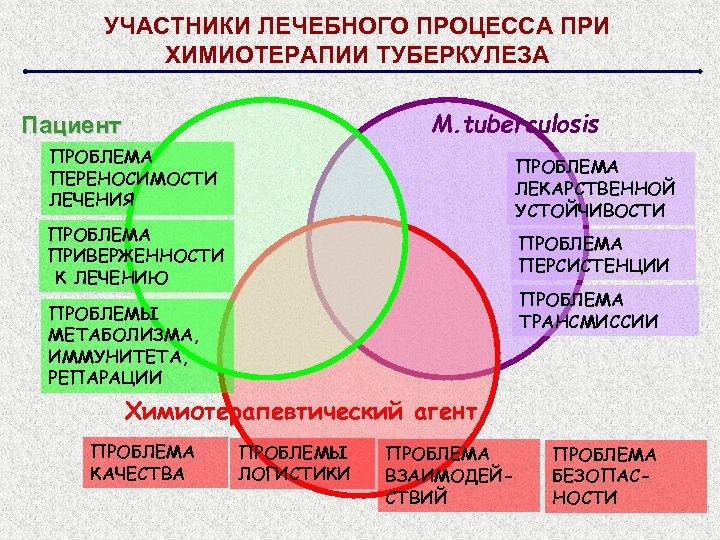
УЧАСТНИКИ ЛЕЧЕБНОГО ПРОЦЕССА ПРИ ХИМИОТЕРАПИИ ТУБЕРКУЛЕЗА M. tuberculosis Пациент ПРОБЛЕМА ПЕРЕНОСИМОСТИ ЛЕЧЕНИЯ ПРОБЛЕМА ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТИ ПРОБЛЕМА ПРИВЕРЖЕННОСТИ К ЛЕЧЕНИЮ ПРОБЛЕМА ПЕРСИСТЕНЦИИ ПРОБЛЕМА ТРАНСМИССИИ ПРОБЛЕМЫ МЕТАБОЛИЗМА, ИММУНИТЕТА, РЕПАРАЦИИ Химиотерапевтический агент ПРОБЛЕМА КАЧЕСТВА ПРОБЛЕМЫ ЛОГИСТИКИ ПРОБЛЕМА ВЗАИМОДЕЙСТВИЙ ПРОБЛЕМА БЕЗОПАСНОСТИ

ПРОБЛЕМЫ ЭТИОТРОПНОЙ ТЕРАПИИ ТУБЕРКУЛЕЗА • Получение новых знаний о МБТ в ходе Возбудитель заболевания фундаментальных исследований • Совершенствование методов определения лекарственной чувствительности МБТ • Совершенствование химиотерапевтических Химиотерапевтический агентов и режимов этиотропной терапии • Повышение приверженности пациентов к лечению Пациент • Стимуляция защитных сил организма больного и репаративных процессов, модулирование инволюционных изменений

СОВЕРШЕНСТВОВАНИЕ ХИМИОТЕРАПЕВТИЧЕСКИХ АГЕНТОВ И РЕЖИМОВ ЭТИОТРОПНОЙ ТЕРАПИИ ü Оптимизация использования имеющихся противотуберкулезных препаратов ü Создание новых лекарственных форм существующих противотуберкулезных средств, включая комбинированные препараты ü Создание аналогов имеющихся противотуберкулезных средств ü Использование существующих антибактериальных препаратов широкого спектра действия ü Создание новых препаратов с избирательной антимикобактериальной активностью ü Сочетание антимикобактериальной терапии с иными видами лечения
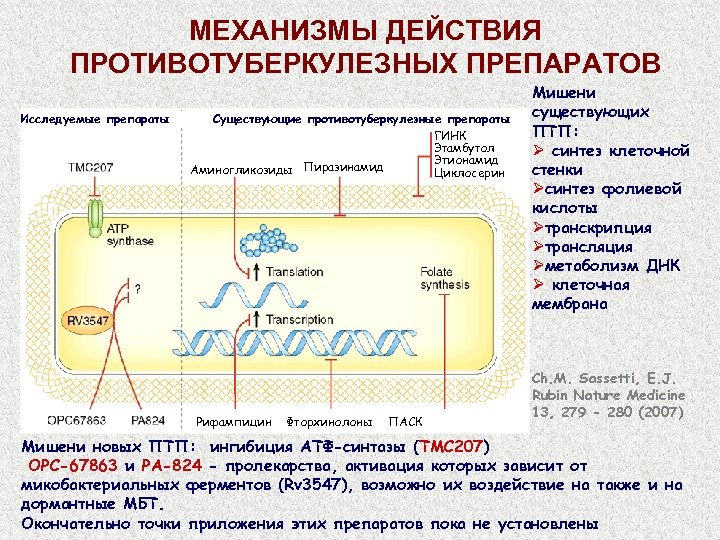
МЕХАНИЗМЫ ДЕЙСТВИЯ ПРОТИВОТУБЕРКУЛЕЗНЫХ ПРЕПАРАТОВ Исследуемые препараты Существующие противотуберкулезные препараты ГИНК Этамбутол Этионамид Аминогликозиды Пиразинамид Циклосерин Рифампицин Фторхинолоны ПАСК Мишени существующих ПТП: Ø синтез клеточной стенки Øсинтез фолиевой кислоты Øтранскрипция Øтрансляция Øметаболизм ДНК Ø клеточная мембрана Ch. M. Sassetti, E. J. Rubin Nature Medicine 13, 279 - 280 (2007) Мишени новых ПТП: ингибиция АТФ-синтазы (TMC 207) OPC-67863 и PA-824 - пролекарства, активация которых зависит от микобактериальных ферментов (Rv 3547), возможно их воздействие на также и на дормантные МБТ. Окончательно точки приложения этих препаратов пока не установлены
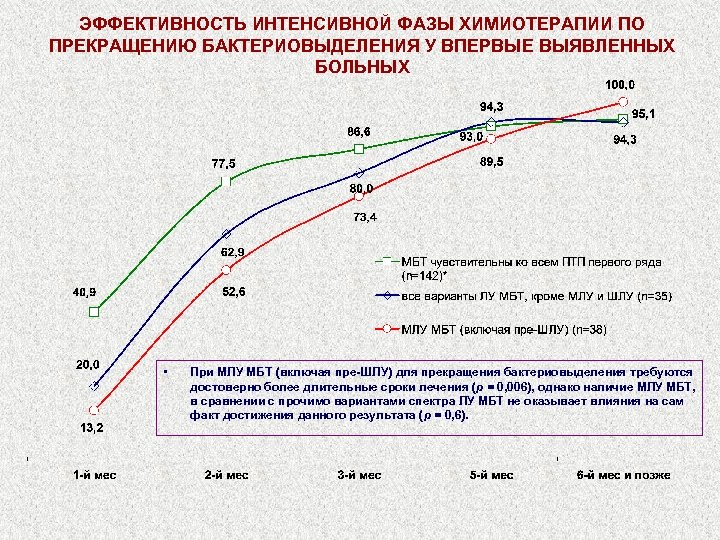
ЭФФЕКТИВНОСТЬ ИНТЕНСИВНОЙ ФАЗЫ ХИМИОТЕРАПИИ ПО ПРЕКРАЩЕНИЮ БАКТЕРИОВЫДЕЛЕНИЯ У ВПЕРВЫЕ ВЫЯВЛЕННЫХ БОЛЬНЫХ • При МЛУ МБТ (включая пре-ШЛУ) для прекращения бактериовыделения требуются достоверно более длительные сроки лечения (р = 0, 006), однако наличие МЛУ МБТ, в сравнении с прочимо вариантами спектра ЛУ МБТ не оказывает влияния на сам факт достижения данного результата (р = 0, 6).
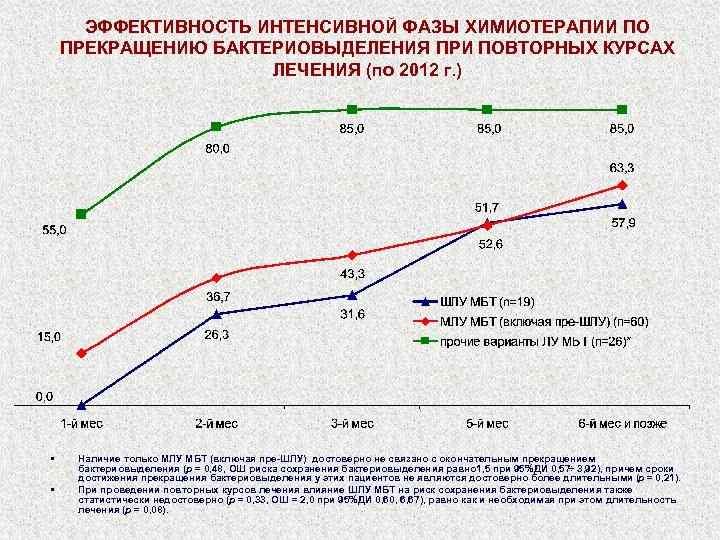
ЭФФЕКТИВНОСТЬ ИНТЕНСИВНОЙ ФАЗЫ ХИМИОТЕРАПИИ ПО ПРЕКРАЩЕНИЮ БАКТЕРИОВЫДЕЛЕНИЯ ПРИ ПОВТОРНЫХ КУРСАХ ЛЕЧЕНИЯ (по 2012 г. ) • • Наличие только МЛУ МБТ (включая пре-ШЛУ) достоверно не связано с окончательным прекращением бактериовыделения (р = 0, 48, ОШ риска сохранения бактериовыделения равно 1, 5 при 95%ДИ 0, 57÷ 3, 92), причем сроки достижения прекращения бактериовыделения у этих пациентов не являются достоверно более длительными (р = 0, 21). При проведении повторных курсов лечения влияние ШЛУ МБТ на риск сохранения бактериовыделения также статистически недостоверно (р = 0, 33, ОШ = 2, 0 при 95%ДИ 0, 6, 67), равно как и необходимая при этом длительность лечения (р = 0, 08).

ПОСЛЕДСТВИЯ ПОБОЧНЫХ РЕАКЦИЙ НА ПРОТИВОТУБЕРКУЛЕЗНЫЕ ПРЕПАРАТЫ Отмечены (в той или иной степени) у 84, 6% больных, из получавших химиотерапию по I/III режиму в МНПЦБТ в 2010 г. Ø Ø Ø отмена, как минимум, одного ПТП - 48, 1%, полное прерывание химиотерапии у 7, 7% больных снижение мотивации к лечению нарушение фармакокинетики - снижение эффективных концентраций ПТП замедление репаративных процессов

ХИМИО…. терапия


Сочетание антимикобактериальной терапии с иными видами лечения ü Воздействие на воспалительный процесс ü Восстановление функции пораженного органа ü Предотвращение и купирование побочных эффектов химиотерапии ü Модулирование иммунологического ответа ü Обеспечение полноценных репаративных процессов ü Восстановление физиологически адекватного уровня активности клеточных и гуморальных эффекторов иммунной системы
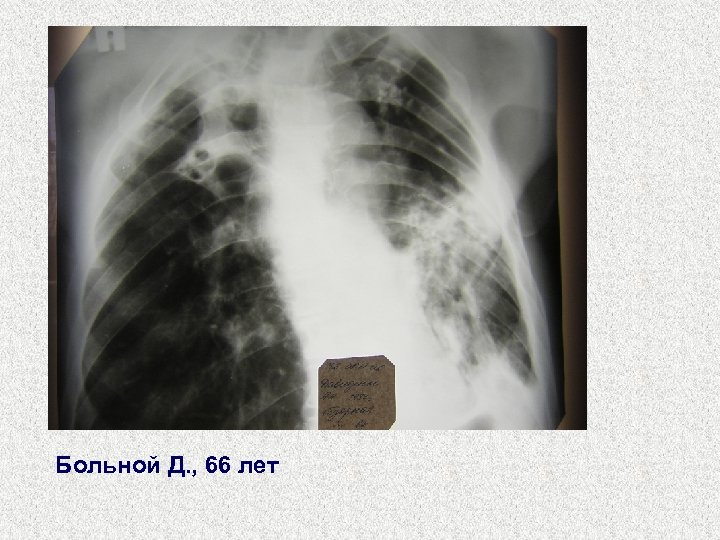
Больной Д. , 66 лет
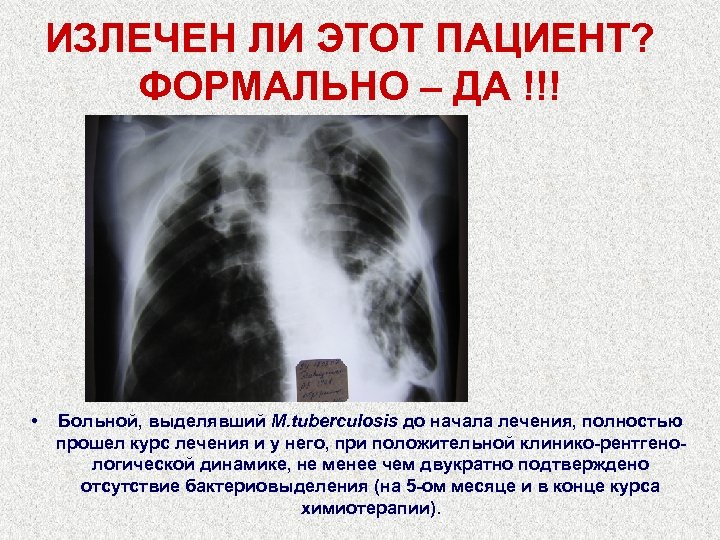
ИЗЛЕЧЕН ЛИ ЭТОТ ПАЦИЕНТ? ФОРМАЛЬНО – ДА !!! • Больной, выделявший M. tuberculosis до начала лечения, полностью прошел курс лечения и у него, при положительной клинико-рентгенологической динамике, не менее чем двукратно подтверждено отсутствие бактериовыделения (на 5 -ом месяце и в конце курса химиотерапии).

• Неполноценность фагоцитарной реакции благоприятствует хроническому течению специфического воспаления с развитием грубых морфологических изменений. Изменения тканевого метаболизма и реактивности организма существенно влияют на динамику и исход туберкулезного воспаления в процессе лечения.

• Средства обеспечения эффективной этиотропной терапии должны, с одной стороны, нарушать закономерности жизненного цикла возбудителя, с другой восстанавливать физиологически адекватный уровень активности клеточных и гуморальных эффекторов иммунной системы

МОДУЛИРОВАНИЕ ИММУНОЛОГИЧЕСКОГО ОТВЕТА • Иммунная система человека - очень сложнпя, нелинейная сетевая структура, обладающая громадным потенциалом в отношении незначительных модификаций путей передачи сигналов, что в последующем приводит к выработке цитокинов с далеко идущими последствиями для дальнейших изменений в организме • Последние могут быть и благоприятными, однако не являются в полной мере предсказуемыми, желательными или контролируемыми

Новая фармакологическая группа – innate defense regulators (IDR): ü ü Усиление элиминации возбудителя Уменьшение повреждения тканей Опосредованное противоинфекционное действие Модулирование иммунного ответа Регуляторы внутренних защитных систем организма - синтезированные пептиды защитной системы, обладающие неспецифическим противовирусным и антибактериальным эффектом без непосредственного противоинфекционного действия

Новая фармакологическая группа – innate defense regulators (IDR): • Обеспечение физиологически необходимого уровня взаимодействия иммунной системы с нервной и эндокринной системами • Обеспечение реализации терапевтического эффекта других лекарственных средств Первым и единственным на настоящий момент лекарственным препаратом, разрешенным к медицинскому применению и отвечающим требованиям к IDR, признан Глутоксим®.

На сегодняшний день в США, Канаде, Европе, Китае реализуются подходы лечения хронических инфекционных и пролиферативновоспалительных заболеваний, в которых используется противомикробный, антивирусный, противоопухолевый, иммуномодулирующий эффект дефенсинов ü Дефенсины – это катионные амфипатические пептиды с длиной ≈ 30 аминокислот и трехнитевой β-пластинчатой структурой, содержащей три дисульфидные связи ü На основании способа дисульфидного связывания дефенсины разделяют на семейства – α-, β- и реже встречающиеся Θ-дефенсины ü У человека α-дефенсины образуются в гранулах нейтрофилов (как часть их противомикробного арсенала) и в клетках крипт кишечника, а также в других лейкоцитах и эпителиоцитах ü β-дефенсины производятся в эпителии слизистых, коже и в некоторых лейкоцитах ü Θ-дефензины – циклические пептиды с высокой анти-ВИЧ активностью, которые не образуются у человека и пока были выявлены только у обезьян Старого Света

Единственным зарегистрированным препаратом, фармакологическая активность которого опосредована способностью восстанавливать ситуационно обусловленный уровень образования дефенсинов, является Глутоксим

Глутоксим • • • обладает иммуномодулирующей, токсикомодифицирующей, гемостимулирующей, гепатопртекторной активностями стимулирует процесс экзоцитоза содержимого внутриклеточных везикул, включая выброс макрофагами микобактерий туберкулеза подавляет мембранозависимые механизмы лекарственной устойчивости некоторых микроорганизмов Широта фармакологических эффектов препарата обусловлена его способностью инициировать механизмы, восстанавливающие функционально активную конформацию рецепторов цитокинов и, соответственно, чувствительность к ним клеток Многогранность фармакологических эффектов российского препарата Глутоксим® определила целесообразность его лечебного применения при хронических заболеваниях, ведущим патогенетическим фактором которых являются иммунный и метаболический дисбаланcы, нарушение детоксикационной и выделительной функций печени, лекарственная устойчивость к химиотерапевтическим агентам
ГЛУТОКСИМ - метаболический иммунокорректор, содержащий аминокислоты (бис-γ-L-глутамил-Lцистенил-бис-глицин), которые транспортируются в пораженные клетки. Этот вариант иммунокоррекции осуществляет не «исправление» , а поддержку адаптивных перестроек внутриклеточного обмена лимфоцитов. Синтезирован в России Прошел все необходимые доклинические исследования Включен в перечень ЖНВЛС, рекомендован к применению при туберкулезe

• Глутоксим оказывает комплексное воздействие на клеточный метаболизм, активирует функцию нормальных клеток и инициирует процесс элиминации из организма генетически дефектных клеток. Под его воздействием повышается эффективность макрофагально-фагоцитарной реакции и устойчивость клеток к различным токсическим факторам.

Прогнозируемые эффекты Глутоксима I группа эффектов Увеличение эффективности химиотерапии у больных туберкулёзом при различных спектрах ЛУ МБТ и уменьшение риска развития ЛУ МБТ II группа эффектов Улучшение переносимости этиотропного лечения туберкулеза III группа эффектов Повышение эффективности хирургического лечения у больных туберкулёзом

ОБЕСПЕЧЕНИЕ ПОЛНОЦЕННОГО ЭТИОТРОПНОГО ЛЕЧЕНИЯ БОЛЬНЫХ ТУБЕРКУЛЕЗОМ Ø ОСНОВНАЯ ЗАДАЧА: Добиться включения всех компонентов интенсивного лечения туберкулеза в клинические протоколы и стандарты оказания медицинской помощи больным туберкулезом
52abb27fc0df4fda245f1d740471d3b2.ppt