Объемный анализ (титриметрия). Методы нейтрализации и


Объемный анализ (титриметрия). Методы нейтрализации и иодометрии.

n Аналитическая химия – наука о методах качественного и количественного определения химического состава вещества или их смесей. n Качественный анализ устанавливает, из каких элементов, ионов или молекул, состоит вещество. n Количественный анализ определяет количественные соотношения составных частей в анализируемом объекте. Применяется для определения химического состава крови, желудочного сока, мочи при анализе отдельных органов, тканей, воздуха, питьевых и стоячих вод, почвы, пищевых продуктов.

Методы количественного анализа n Физико-химические – основаны на изучении физико-химических свойств анализируемого вещества и позволяют определить концентрации растворов по изменению электропроводности, силы тока, интенсивности окраски раствора и другие. n Химические 1. Гравиметрический (весовой) – основан на точном измерении веса осадка – продукта реакции. 2. Титриметрический (объемный) – основан на точном измерении объема раствора реактива, израсходованного на реакцию с определяемым веществом.

Требования к реакциям в объемном анализе n Реакция должна протекать быстро и до конца n Не должно быть побочных реакций. n Конец реакции должен хорошо фиксироваться.

Требования к объемному анализу n Точное измерение объемов реагирующих веществ n Концентрация одного из растворов должна быть точно известна n Точное определение конца реакции

Раствор с точно известной концентрацией – титрант.

Процесс прибавления титранта к раствору определяемого вещества, называется титрованием. Титрование всегда ведется до точки эквивалентности.

Точка эквивалентности – это конец реакции, когда количество прибавленного раствора титранта эквивалентно количеству определяемого вещества. Точка эквивалентности определяется: n По изменению окраски самого определяемого вещества в растворе n По выпадению осадка n По изменению правильно выбранного индикатора

Расчеты в объемном анализе: Закону эквивалентов: вещества реагируют между собой в количествах, пропорциональных их эквивалентам. n(X) = n(T) или c(1/z X) · V(X)=c(1/z T) · V(T) c(1/z X) – молярная концентрация эквивалента – число моль эквивалентов вещества (Х) в 1 литре раствора.

Эквивалент M(1/z·X) вещества– реальная или условная частица. В данной кислотно основной (КО) реакции она эквивалентна одному протону (Н+)или в данной окислительно восстановительной реакции (ОВР) – одному электрону (ē). M(1/z. X) = 1/z · M(X), г/моль

Для обменных реакций z число замещенных ионов Н+ в кислоте, число ОН в основании, суммарный заряд обменивающихся ионов в солях. M(1/z. НСI)=1/1 М (HCI)=36, 6 г/моль M(1/z H 2 SO 4)=1/2 М (H 2 SO 4)=98/2=49 г/моль для реакции H 2 SO 4+Na. OH=Na 2 SO 4 M(1/z H 2 SO 4)=1/1 М (H 2 SO 4)=98 г/моль для реакции M(1/z. Ca(ОH)2)=1/2 Ca(ОН)2=74/2=37 г/моль M(1/z. AI 2(SO 4)3)=1/3 · 2 M AI 2(SO 4)3

Для ОВР M(1/z окислителя или восстановителя) = 1/z·M(окислителя или восстановителя) Z – число электронов, принятых окислителем или отданных восстановителем. KMn. O 4+Fe. SO 4+H 2 SO 4 K 2 SO 4+Mn. SO 4+ +Fe. SO 4 +H 2 O Mn+7 +5ē Mn+2 M(1/z KMn. O 4)=1/5 M (KMn. O 4) Fe+2 -1ē Fe+3 M(1/z Fe. SO 4 )=1/1 M (Fe. SO 4)

Основная задача объемного анализа - нахождение титра вещества (Т(Х) ) Т(Х) – это масса вещества (Х) в 1 мл раствора. Т(Х) = m(X)г , г/мл V(раствор)мл Из формулы 2 m(X) = c(1/z·X) ·M(1/z·X), г в 1000 мл раствора, отсюда Т(Х) = c(1/z·X) · M(1/z·X) , г/мл 1000 Точную концентрацию титрантов определяют с помощью стандартных веществ.

Требования для стандартных веществ n Вещество должно быть химически чистым (х. ч. ) n Состав должен строго соответствовать химической формуле n Вещество должно иметь кристаллическую структуру, хорошо растворяться в воде n Вещество должно иметь большую молярную массу

Концентрации титрантов определяют по растворам стандартных веществ, а затем концентрации растворов анализируемых веществ определяют по растворам титрантов Формулы для расчета С(1/z·Т)=V (станд. р ра) · С(1/z станд. р ра) V(титранта) С(1/z·X)=V (станд. р ра) · С(1/z станд. р ра) V(титранта)

Кислотно-основное титрование (метод нейтрализации) Используя для количественного определения содержания кислот, щелочей, гидролизующихся солей, кислотности желудочного сока, мочи, молока, буферной емкости крови, лекарств, воды, пищевых продуктов. В основе метода лежит реакция нейтрализации: Н+ + ОН– → Н 2 О

Титрант в ацидиметрии – растворы сильных кислот (H 2 SO 4, HCl) используются для определения концентраций растворов щелочей и солей, имеющих щелочную реакцию при гидролизе (Na 2 CO 3, Na. B 4 O 7∙ 10 H 2 O, Na. HCO 3, жесткая вода Са(HCO 3)2, Mg(HCO 3)2) Титранты в алкалиметрии – растворы сильных оснований (Na. OH, KOH) используются для определения концентраций растворов кислот и солей, имеющих кислую реакцию при гидролизе (NH 4 CI)

Стандартные вещества для определения концентрации титрантов кислот Na 2 CO 3∙ 10 H 2 O – сода Na. B 4 O 7∙ 10 H 2 O – тетраборат натрия (бура) Стандартные вещества для определения концентрации титрантов щелочей H 2 C 2 O 4∙ 2 H 2 O – щавелевая кислота (CH 2)2(COOH)2 – янтарная кислота
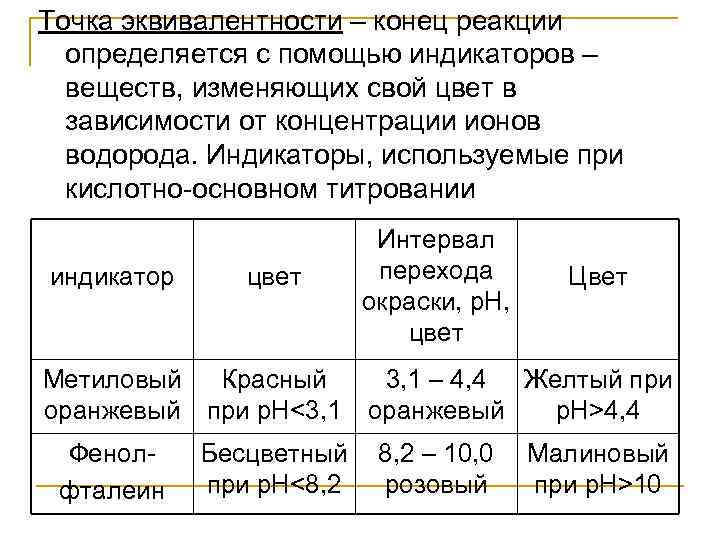
Точка эквивалентности – конец реакции определяется с помощью индикаторов – веществ, изменяющих свой цвет в зависимости от концентрации ионов водорода. Индикаторы, используемые при кислотно основном титровании Интервал индикатор цвет перехода Цвет окраски, р. Н, цвет Метиловый Красный 3, 1 – 4, 4 Желтый при оранжевый при р. Н<3, 1 оранжевый р. Н>4, 4 Фенол Бесцветный 8, 2 – 10, 0 Малиновый фталеин при р. Н<8, 2 розовый при р. Н>10

Окраска метиловым оранжевым растворов с различной р. Н< 3, 1; р. Н 3, 1 – 4, 4; р. Н>4, 4

Окраска растворов с различной р. Н фенолфталеином р. Н< 8, 2 р. Н> 10, 0

Титрование сильной кислоты сильным основанием. Кривая титрования показывает зависимость р. Н раствора от объема добавленного титранта. HCl + Na. OH → Na. Cl + Н 2 O V(HCl, Na. OH)=10 мл; C(HCI, Na. OH) = 0, 1 моль/л Точка эквивалентности при р. Н=7 Скачок титрования р. Н 4 – 10. Индикаторы метиловый оранжевый, фенолфталеин. Скачок титрования – резкое изменение р. Н около точки эквивалентности от одной капли прибавленного титранта.

Иодометрия – это метод объемного анализа, позволяющий определять содержание как окислителей, так и восстановителей. Это связано с тем, что значение φ I 2 / 2 I– = 0, 54 В находится в середине таблицы стандартных окислительно восстановительных потенциалов.

Основные реакции метода I 2 + 2ē 2 I– используется для определения восстановителей 2 I– 2ē I 2 используется для определения окислителей Титранты: растворы иода I 2 (Ох) и тиосульфата натрия Na 2 S 2 O 3 · 5 H 2 O (Red).

Основная реакция при титровании I 2 + 2 Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 (тетратионат натрия) φ S 4 O 62–/ S 2 O 32– =0, 09 По этой реакции можно рассчитать молярные массы эквивалентов титрантов I 2 + 2ē = 2 I– М(1/z I 2)=1/2 М = 127 (г/моль) 2 S 2 O 32– 2ē = S 4 O 62– М(1/z Na 2 S 2 O 3 · 5 H 2 O)=2 М/2 = 248 (г/моль)

Растворы готовят заранее, выдерживают 10 дней и определяют концентрацию по стандартным веществам: K 2 Cr 2 O 7, КВr. O 3. Растворы иода I 2 готовят растворением навески в присутствии иодида калия KI, т. к. сам иод плохо растворяется в воде. Концентрацию раствора иода определяют по раствору тиосульфата натрия точной концентрации.

Индикатор в иодометрии – крахмал. Свежеприготовленный раствор крахмала дает с иодом синее окрашивание. Крахмал добавляют перед самым концом реакции, когда большая часть иода оттитрована и раствор имеет бледно желтую окраску. Конец реакции определяют по исчезновению синей окраски.

Определение окислителя в иодометрии Окислители – вещества, имеющие φ Ox/Red > φ I 2 / 2 I–. К ним относят KMn. O 4, K 2 Cr 2 O 7 Cl 2 в хлорной извести Ca(OCl)2, , CI 2 в водопроводной воде, Br 2 в природных водах, KCIO 3, KIO 3, H 2 O 2, Fe+3 и др.

Косвенное титрование В этом методе используют вспомогательный раствор KI. Две стадии косвенного титрования: 1. Окислитель выделяет из иодида калия KI эквивалентное количество иода I 2 Ox + KI + H+ Red + I 2+K+ 2. Выделившийся иод оттитровывается эквивалентным количеством тиосульфата натрия I 2 + 2 Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 n(1/z Ox)=n(1/z I 2)=n(1/z Na 2 S 2 O 3) C(1/z Ox)= V(Na 2 S 2 O 3) · C(1/z Na 2 S 2 O 3) V(Ox)

Прямое титрование Определяют сильные восстановители, которые легко окисляются иодом и имеют φ Ox/Red < φ I 2 / 2 I–. К ним относят сульфиды Na 2 S, сульфиты Na 2 SO 3, тиосульфат Na 2 S 2 O 3, аскорбиновую кислоту, As 2 O 3. Титрант: иод I 2 Red+ I 2=2 I–+Ox n(1/z Red)=n(1/z I 2) C(1/z. Red)=V(I 2) · C(1/z I 2) V(Red)

Обратное титрование Для определения растворов слабых восстановителей, у которых φOx/Red≈φI 2/2 I– и скорость реакции мала, или летучих восстановителей формальдегид, глюкоза, фенол, сахар в крови, фермент пероксидаза, H 2 S. Титранты: растворы I 2 и Na 2 S 2 O 3 · 5 H 2 O

Принцип обратного титрования: к раствору определяемого вещества (восстановителя) добавляют точный избыток одного титранта (I 2), а затем остаток его, не вступивший в реакцию с определяемым веществом, оттитровывают другим титрантом (Na 2 S 2 O 3 · 5 H 2 O) Red+ I 2 2 I–+Ox 1. H 2 S+ I 2 = 2 НI +S 2. I 2 + 2 Na 2 S 2 O 3 = 2 Na. I + Na 2 S 4 O 6

n (1/z Red)= n(1/z I 2 )=n(1/z Na 2 S 2 O 3) n(1/z Red)=n(1/z I 2 )= n(1/z Na 2 S 2 O 3) C (1/z Red)= = C(1/z I 2) · V(I 2) C(1/z. Na 2 S 2 O 3) · V(Na 2 S 2 O 3) V(Red)
Объемный анализ (титриметрия).ppt
- Количество слайдов: 33

