Объемный анализ 2015.pptx
- Количество слайдов: 17

Объемный анализ Методическая разработка, часть II, глава IV

Аналитическая химия – наука об определении химического состава веществ и их химического строения.

Виды химического анализа Качественный: Количественный: • дает сведения о том, какие компоненты включает в себя анализируемый объект • дает сведения о количественном содержании всех или отдельных компонентов

Требования, предъявляемые к методам аналитической химии: • правильность и хорошая воспроизводимость результатов • низкий предел обнаружения компонентов • избирательность, экспрессность и простота анализа • возможность автоматизации анализа • экономичность определений

Методы аналитической химии Классические методы (точность 0, 1 -0, 2%) • гравиметрия (выделение вещества в чистом виде и его взвешивание) • титриметрия (измерение объема титранта (раствора с точно известной концентрацией), затраченного на реакцию с заранее известным точным объемом анализируемого вещества) Инструментальные методы (точность 25%) • спектрофотометрия • масс-спектрометрия • атомноабсорбционный анализ и др.

Титриметрические методы Определяемое вещество (X) – состав известен, концентрация неизвестна Титрант (T) – состав известен, концентрация известна Раствор титранта постепенно, небольшими порциями, добавляют к раствору определяемого вещества до тех пор, пока реакция между X и T не пройдет до конца. Этот процесс называют титрованием. Момент, когда реакция между X и T проходит до конца, называется точкой эквивалентности.

Закон эквивалентов вещества реагируют между собой в эквивалентных количествах X- определяемое вещество Т - титрант

Реакция титрования должна отвечать следующим требованиям: • • быть строго стехиометричной протекать быстро протекать количественно должен существовать способ фиксирования точки эквивалентности (точку эквивалентности устанавливают по изменению цвета индикатора или какоголибо физико-химического свойства раствора)
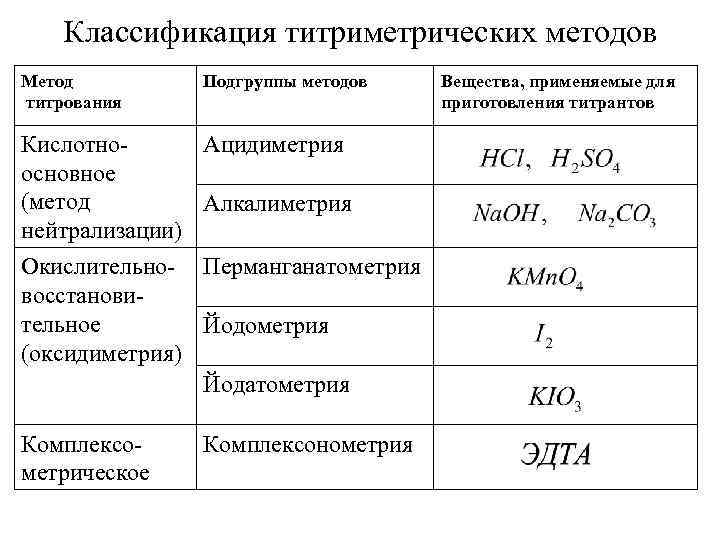
Классификация титриметрических методов Метод титрования Подгруппы методов Кислотно. Ацидиметрия основное (метод Алкалиметрия нейтрализации) Окислительно- Перманганатометрия восстановительное Йодометрия (оксидиметрия) Йодатометрия Комплексометрическое Комплексонометрия Вещества, применяемые для приготовления титрантов
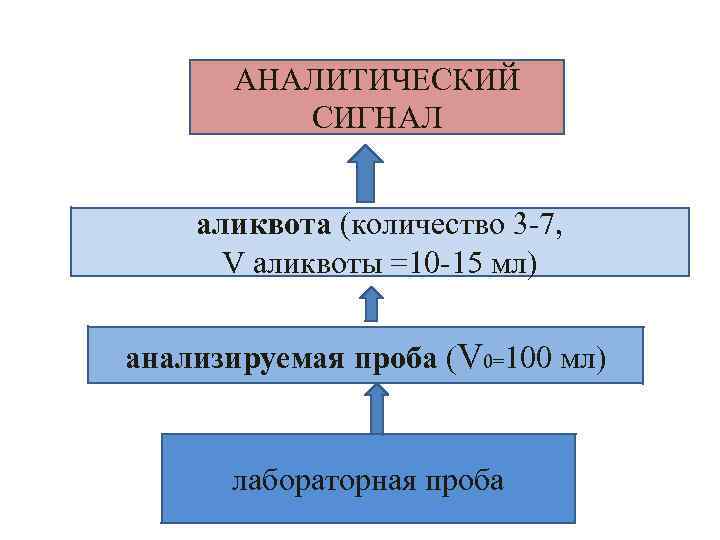
АНАЛИТИЧЕСКИЙ СИГНАЛ аликвота (количество 3 -7, V аликвоты =10 -15 мл) анализируемая проба (V 0=100 мл) лабораторная проба

Аналитический сигнал – среднее из измерений физической величины, функционально связанной с содержанием определяемого компонента. В объемном анализе аналитическим сигналом является среднее значение объема титранта.

Обработка аналитического сигнала По закону эквивалентов:

Кислотно-основные индикаторы Индикатор Область перехода окраски Изменение окраски Метиловый оранжевый 3, 1 -4, 4 Метиловый красный 4, 4 -6, 2 3, 36 5, 00 Красная- желтая Красная-желтая Бромтимоловый синий Тимоловый синий Фенолфталеин 7, 30 9, 20 9, 53 Желтая-синяя Бесцв. -малиновая 6, 0 -7, 6 8, 0 -9, 6 8, 2 -9, 8 Интервал перехода окраски индикатора

Выбор индикатора • Тимоловый синий • Бромтимоловый синий • Метиловый оранжевый
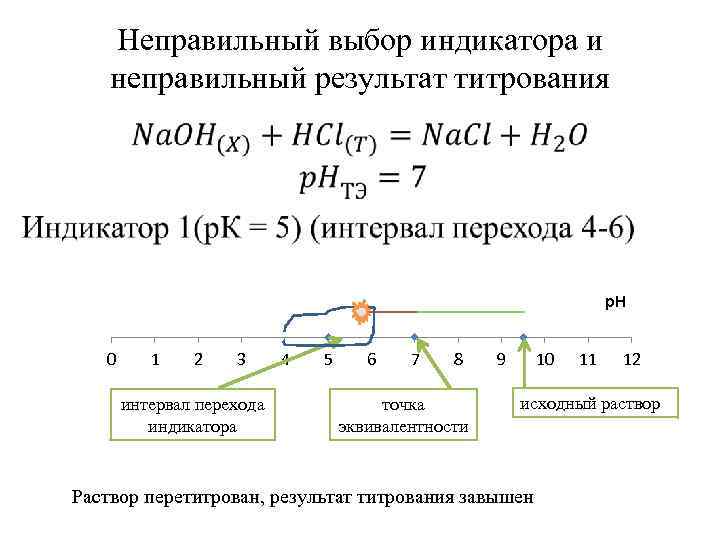
Неправильный выбор индикатора и неправильный результат титрования • p. H 0 1 2 3 интервал перехода индикатора 4 5 6 7 8 точка эквивалентности 9 10 11 12 исходный раствор Раствор перетитрован, результат титрования завышен

Расчет коэффициентов z в методе нейтрализации •

Формулы Х –определяемое вещество Т - титрант - объем анализируемой пробы - объем аликвоты (1) (2) (3) (4)
Объемный анализ 2015.pptx