729bfe3c2defe0d59a112675d9d850a1.ppt
- Количество слайдов: 23

О способах формирования интереса к процессу познания на уроках химии (из опыта работы учителя МОУ ”Староалейская средняя общеобразовательная школа № 2”Челноковой Е. Н. )

Обучение химии начинается в 8 классе и поначалу учащиеся демонстрируют интерес к данному предмету. Но с течением времени, когда они сталкиваются с той бездной знаний, которую таит в себе данная наука, энтузиазм стихает. Одним становится неинтересно. Другим предмет даётся с трудом, третьи просто зарабатывают отметки. Одним из условий успешного обучения является умение учителя вызвать интерес к предмету. В настоящее время по прежнему актуальными являются методы, основанные на использовании игровых технологий при обучении химии

Игра ребёнка не есть пустая забава. Она имеет высокий смысл и глубокое значение, в ней развивается и проявляется весь человек в своих самых тончайших задатках Ф. Фребель

9 класс Соли угольной кислоты. Загадка: В чёрном поле заяц белый Прыгал, бегал, петли делал след за ним был тоже бел. Кто же этот заяц? (мел) Задание: найдите среди веществ формулу мела Na. Cl Na. HCO 3 K 2 CO 3 Na. NO 3 Ca. CO 3 Ba. SO 4 Определите тему урока

8 класс – Галогены (угадайте элемент) 1. 2. 3. 4. 5. Был открыт в 1811 г. французским химиком Б. Куртуа. Название ему дал Ж. Л. Гей Люссак. Образованное им простое вещество получают из морских водорослей (ламинарии), попутных нефтяных вод и солёной воды некоторых озер. Недостаток его вызывает нарушение обмена веществ, заболевание щитовидной железы. Кристаллы простого вещества при нагревании возгоняются, минуя жидкое состояние, образуя фиолетовый пар. (Йод)
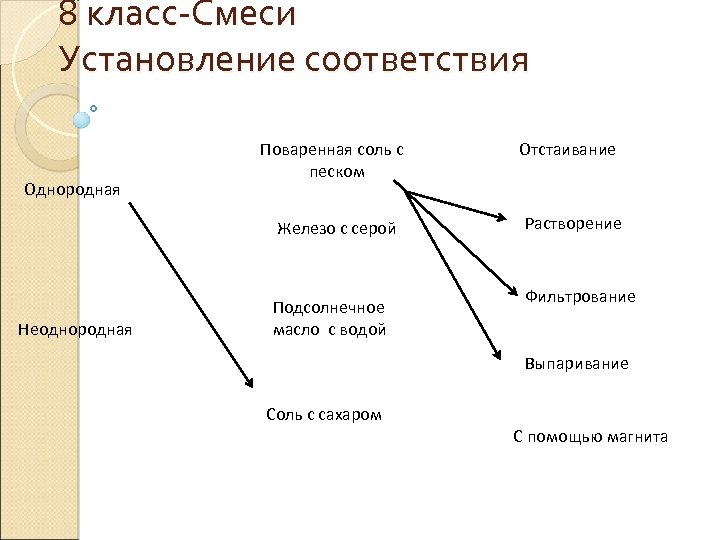
8 класс Смеси Установление соответствия Однородная Поваренная соль с песком Железо с серой Неоднородная Подсолнечное масло с водой Отстаивание Растворение Фильтрование Выпаривание Соль с сахаром С помощью магнита
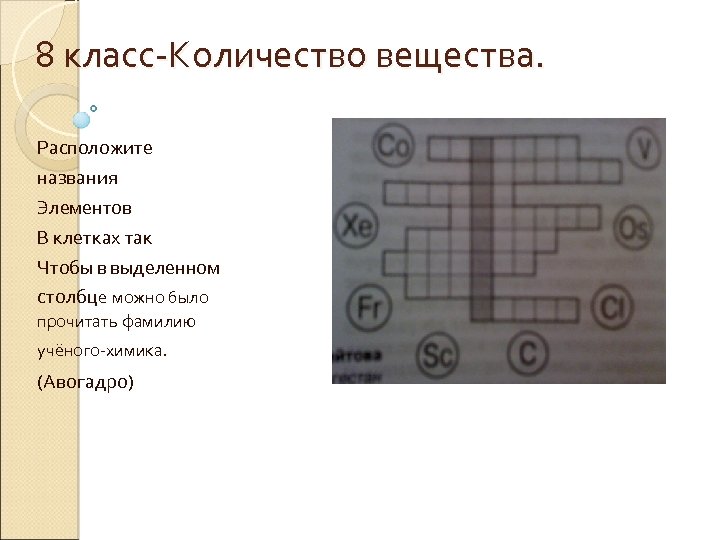
8 класс Количество вещества. Расположите названия Элементов В клетках так Чтобы в выделенном столбце можно было прочитать фамилию учёного химика. (Авогадро)
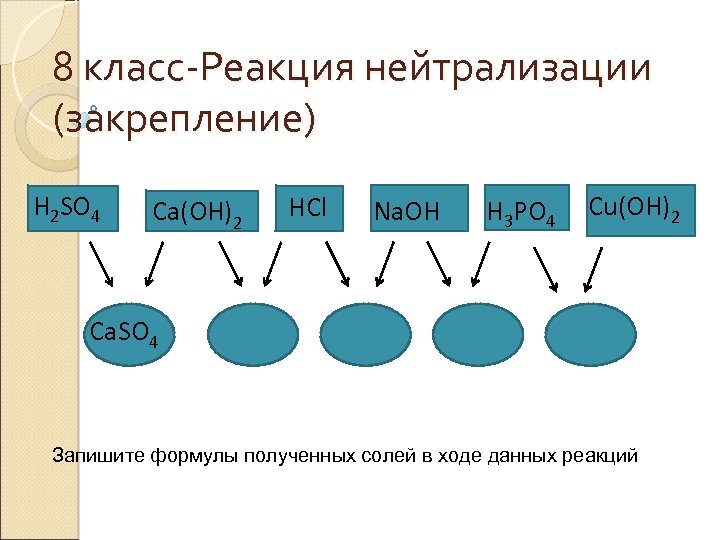
8 класс Реакция нейтрализации (закрепление) H 2 SO 4 Ca(OH)2 HCl Na. OH H 3 PO 4 Cu(OH)2 Ca. SO 4 Запишите формулы полученных солей в ходе данных реакций

Учебник это основной источник знаний по предмету, средство формирования учебных умений и овладения приёмами познавательной деятельности. Однако некоторые учащиеся считают, что понять текст учебника можно лишь после объяснения учителя. Это означает, что у них не сформирована привычка размышлять над материалом учебника. Самостоятельно находить ответы на поставленные вопросы. Поэтому я предлагаю следующие варианты работы с текстом учебника:

Укажите в таблице состав сплавов. Из букв соответствующих основному компоненту сплава, вы составите название самого твёрдого метала: , а из букв, соответствующих тем металлам, которых в сплаве меньше, название драгоценного металла: Название сплава Бронза Латунь Мельхиор Дюральалюминний Металл, входящий в состав сплава Al Sn Mg Zn Mn Cu Ni С П Е У Ш Х Б А Ф Н Л В Р Ц Г В Ш Ю Н О А М Я Т Б И Н А

Укажите в таблице легирующие элементы, придающие стали указанные свойства. Из букв, соответствующих правильным ответам, вы составите название сплава ртути с другим металлом. Свойства стали Легирующие элементы Cr Ni Mn Ti W А Б М Р А Корриозная стойкость Л Ь О Г Н З А М А У Твёрдость Механическая прочность

Чем одарить одаренного ребенка Во время контрольной работы, дети успешно освоившие материал темы имеют возможность проверить свои знания выполняя творческие задания (индивидуально или работая в паре) Задача: В лаборатории на столе стоят пять колб с водными растворами различных веществ. На каждой колбе имеется этикетка с названием. На первой колбе написано ”иодид бария”, на второй –”карбонат натрия”, на третьей ”серная кислота”, на четвертой –’’хлорид меди” и на пятой – ”гидроксид натрия. ” К сожалению , этикетки перепутаны, так что ни один из растворов не подписан правильно. При сливании раствора из первой колбы с раствором из второй колбы выделяется газ. А при смешивании раствора из первой колбы с содержимым третьей колбы образуется белый осадок. 1) Как поменять этикетки местами, чтобы все колбы были подписаны правильно? 2) Напишите уравнения реакций. Упомянутых в условии задачи? 3) Какие ещё реакции можно провести между указанными веществами? (Турнир им. М. В. Ломоносова, 2001)

Химия без опытов не химия! Один из стимулов обучения химии в школе демонстрация красочных интересных опытов. В связи с этим предлагаю ребятам самим осуществить опыты которые бы дали основу для изучения материала или его закрепления


Использование WEB квестов в процессе обучения WEB квесты представляют собой мини проекты, основанные на поиске информации в Интернете или в других информационных ресурсах. Нами(мной и ребятами 9 классов) организованы проекты по следующим темам ’’Металлы’’ и “Неметаллы”. Вот один из них:

СИЛИЦИУМ Выполнил: Бережнов Кирилл и Постников Алексей Проверил: Челнокова Елена Николаевна. 2009 год
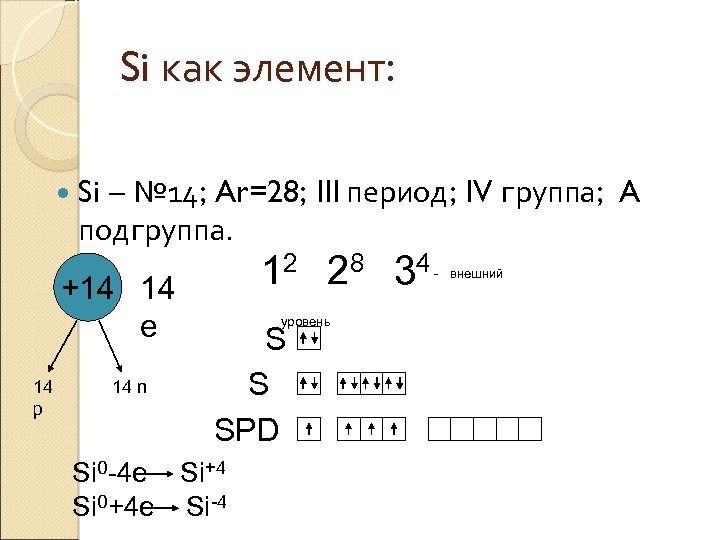
Si как элемент: Si – № 14; Ar=28; III период; IV группа; A подгруппа. +14 14 e 14 p 14 n 12 28 34 уровень S S SPD Si 0 -4 e Si+4 Si 0+4 e Si-4 - внешний

Si как простое вещество: Химические свойства: Кремний горит в кислороде, образуя известный уже вам диоксид кремния, или оксид кремния(ГУ): Si + О 2 = Si. O 2 Будучи неметаллом, при нагревании он соединяется с металлами с образованием силицидов, например: Si + 2 Mg = Mg 2 Si Кремний взаимодействует с концентрированными водными растворами щелочей, образуя силикаты и водород: Si + 2 Na. OH + H 2 O = Na 2 Si 03 + 2 H 2

Соединения Si: Оксид кремния(1 У), или диоксид кремния, или кремнезем Si. O 2, является кислотным оксидом. Он имеет атомную а не молекулярную кристаллическую решетку. Поэтому Si. O 2 твердое и тугоплавкое вещество. Он не растворяется в воде и кислотах, кроме, как в плавиковой, но взаимодействует при высоких температурах со щелочами с образованием солей кремниевой кислоты силикатов: Si. O 2 + 2 Na. OH = Na 2 Si 03 + H 2 O

Получение Si: Кремний получают, восстанавливая его из диоксида магнием или углеродом: Si. O 2 + 2 Mg = 2 Mg. O + Si; Si. O 2 + 2 C = Si + 2 C 0.

Применение Si: Кремний применяют для получения полупроводниковых материалов, а также кислотоупорных сплавов. При сплавлении кварцевого песка с углем при высоких температурах образуется карбид кремния Si. C, который по твердости уступает только алмазу. Поэтому его используют для затачивания резцов металлорежущих станков и шлифовки драгоценных камней. Из расплавленного кварца изготавливают различную кварцевую химическую посуду, которая может выдерживать высокую температуру и не трескается при резком охлаждении. Соединения кремния служат основой для производства стекла и цемента. Обычное оконное стекло имеет состав, который можно выразить формулой: Na 2 O • Са. О • 6 Si. O 2 Его получают в специальных стекловаренных печах сплавлением смеси соды, известняка и песка. Отличительная особенность стекла — способность размягчаться и в расплавленном состоянии принимать любую форму, которая сохраняется при застывании стекла. На этом основано производство посуды и других изделий из стекла. Другой важный материал, получаемый на основе соедине ния кремния, —цемент. Его получают спеканием глины и из вестняка в специальных вращающихся печах. Если порошок цемента смешать с водой, то образуется цементное тесто, или, как его называют строители, «раствор» , который постепенно затвердевает. При добавлении к цементу песка или щебня в качестве наполнителя получают бетон. Прочность бетона воз растает, если в него вводится железный каркас, — получается железобетон, из которого готовят стеновые панели, блоки пе рекрытий, фермы мостов и т. д.

Открытие Si Хотя уже в глубокой древности люди широко использовали в своем быту соединения кремния, сам кремний в элементарном состоянии был впервые получен в 1825 г. шведским химиком Й. Я. Берцелиусом. Однако за 12 лет до него кремний получили Ж. Гей Люссак и Л. Тенар, но он был очень загрязнен примесями. Латинское название силициум берет свое начало от лат. силекс — кремень. Русское название «кремний» происходит от греч. кремнос — утес, скала.

Цветное стекло в витражах церкви Сент-Ша-пель, Париж
729bfe3c2defe0d59a112675d9d850a1.ppt