790f50badece3f1b8d3defc6a658a058.ppt
- Количество слайдов: 39
 NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI Dr. Aşkın GÖRGÜLÜ Süleyman Demirel Üniversitesi Tıp Fakültesi
NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI Dr. Aşkın GÖRGÜLÜ Süleyman Demirel Üniversitesi Tıp Fakültesi
 n n n Glial tümörler SSS’nin primer nöroektodermal tümörleridir. Beyin tümörlerinin % 50’sini oluşturur. Düşük Grade’li Glial (DGG) Tümörler WHO sınıflamasına göre grade I – II tümörler olup heterojen bir gruptur. (Kleihues, et al. 2000)
n n n Glial tümörler SSS’nin primer nöroektodermal tümörleridir. Beyin tümörlerinin % 50’sini oluşturur. Düşük Grade’li Glial (DGG) Tümörler WHO sınıflamasına göre grade I – II tümörler olup heterojen bir gruptur. (Kleihues, et al. 2000)
 n En sık görülen DGG tümörler astrositom, oligodendrogliom ve mikst gliomlardır (WHO Grade II). n Klinik tabloları benzerdir. Diffüz, infiltratif lezyonlardır. İnsidanları giderek artmaktadır. n n (Gilbert et al 2007, Shaw et al. 2008)
n En sık görülen DGG tümörler astrositom, oligodendrogliom ve mikst gliomlardır (WHO Grade II). n Klinik tabloları benzerdir. Diffüz, infiltratif lezyonlardır. İnsidanları giderek artmaktadır. n n (Gilbert et al 2007, Shaw et al. 2008)
 n n n Radyolojik tanı + İzlem Biopsi + RT Cerrahi Rezeksiyon ± RT ± Kemoterapi
n n n Radyolojik tanı + İzlem Biopsi + RT Cerrahi Rezeksiyon ± RT ± Kemoterapi
 n Doku tanısı gereklidir. 20 DGG şüpheli olgu (MR +) Stereotaktik biyopsi DGG tümör Anaplastik astrositoma (50%) (45%) Ensefalit (5%) (Kondziolka D, et al: J Neurosurg. 79(4): 533 -6, 1993)
n Doku tanısı gereklidir. 20 DGG şüpheli olgu (MR +) Stereotaktik biyopsi DGG tümör Anaplastik astrositoma (50%) (45%) Ensefalit (5%) (Kondziolka D, et al: J Neurosurg. 79(4): 533 -6, 1993)
 Yazar δ Yıl (Hasta Sayısı) _______________________________ ≤ 1985 1986– 1990 1991– 1995 1996– 2000 Daha geniş rezeksiyonu öneren çalışmalar Laws Jr, et al, 1984 (461) Soffietti, et al. , 1989 (85) North, et al. , 1990 (77) Philippon, et al. , 1993 Rajan, et al. , 1994 (82) Ito, et al. , 1994 Janny, et al. , 1994 Shaw, et al. , 1994 (71) Nicolato, etal, 1995 (74) Bahary, et al, 1996 (63) Karim, et al, 1996 (343) Piepmeier, et al, 1996 (55) Scerrati, et al, 1996 (131) Leighton, et al. , 1997 (167) Lote, et al. , 1997 (97) Jeremic, et al, 1998 (37 Peraud, et al, 1998 (75) Daha geniş rezeksiyonu yararlı bulmayan çalışmalar Piepmeier, 1987 (60) Medberry, et al, 1988 (50) Shaw, et al. , 1989 (126) Shaw, et al. , 1989 Whitton&Bloom, 1990 (88) Eyre, et al. , 1993 (54) Miralbell, et al, 1993 (49) Shibamoto, et al, 1993 (101) Singer, 1995 (43) Lote, et al. , 1997 (379) Rudoler, et al. , 1998 (30) Bauman, et al. , 1993 (401) (Keles et al. 2001)
Yazar δ Yıl (Hasta Sayısı) _______________________________ ≤ 1985 1986– 1990 1991– 1995 1996– 2000 Daha geniş rezeksiyonu öneren çalışmalar Laws Jr, et al, 1984 (461) Soffietti, et al. , 1989 (85) North, et al. , 1990 (77) Philippon, et al. , 1993 Rajan, et al. , 1994 (82) Ito, et al. , 1994 Janny, et al. , 1994 Shaw, et al. , 1994 (71) Nicolato, etal, 1995 (74) Bahary, et al, 1996 (63) Karim, et al, 1996 (343) Piepmeier, et al, 1996 (55) Scerrati, et al, 1996 (131) Leighton, et al. , 1997 (167) Lote, et al. , 1997 (97) Jeremic, et al, 1998 (37 Peraud, et al, 1998 (75) Daha geniş rezeksiyonu yararlı bulmayan çalışmalar Piepmeier, 1987 (60) Medberry, et al, 1988 (50) Shaw, et al. , 1989 (126) Shaw, et al. , 1989 Whitton&Bloom, 1990 (88) Eyre, et al. , 1993 (54) Miralbell, et al, 1993 (49) Shibamoto, et al, 1993 (101) Singer, 1995 (43) Lote, et al. , 1997 (379) Rudoler, et al. , 1998 (30) Bauman, et al. , 1993 (401) (Keles et al. 2001)
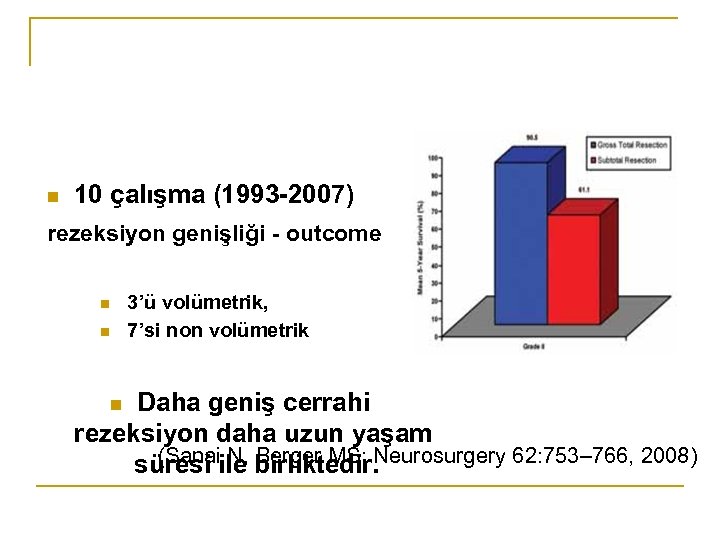 n 10 çalışma (1993 -2007) rezeksiyon genişliği - outcome 3’ü volümetrik, 7’si non volümetrik n n Daha geniş cerrahi rezeksiyon daha uzun yaşam (Sanai N, Berger MS: Neurosurgery 62: 753– 766, 2008) süresi ile birliktedir. n
n 10 çalışma (1993 -2007) rezeksiyon genişliği - outcome 3’ü volümetrik, 7’si non volümetrik n n Daha geniş cerrahi rezeksiyon daha uzun yaşam (Sanai N, Berger MS: Neurosurgery 62: 753– 766, 2008) süresi ile birliktedir. n
 n Postop tümör volümü (rezidü) 0 cm 3 (% 100 rezeksiyon) % 0 rekürrens <10 cm 3 % 14. 8 rekürrens >10 cm 3 % 46. 2 rekürrens ~ 54 ay ~ 50 ay ~ 46. 2 ay p= 0. 0023 (Berger et al: Cancer 74: 1774 -91, 1994)
n Postop tümör volümü (rezidü) 0 cm 3 (% 100 rezeksiyon) % 0 rekürrens <10 cm 3 % 14. 8 rekürrens >10 cm 3 % 46. 2 rekürrens ~ 54 ay ~ 50 ay ~ 46. 2 ay p= 0. 0023 (Berger et al: Cancer 74: 1774 -91, 1994)
 n Rezidü volümü > 10 cm 3 < 10 cm 3 % 46. 2 malign transformasyon % 3. 7 malign transformasyon p= 0. 0009 5 yıl izlem (Berger et al: Cancer 74: 1774 -91, 1994)
n Rezidü volümü > 10 cm 3 < 10 cm 3 % 46. 2 malign transformasyon % 3. 7 malign transformasyon p= 0. 0009 5 yıl izlem (Berger et al: Cancer 74: 1774 -91, 1994)
 n Tümör progresyonu ve malign transformasyon total-subtotal rezeksiyonlarda daha azdır. Malign transformasyon total %0 subtotal % 66. 6 parsiyal % 100 biyopsi % 100 4 yıl izlem n (Kılıc T, et al: J Clin Neurosci. 2002 ; 9(5): 549 -52)
n Tümör progresyonu ve malign transformasyon total-subtotal rezeksiyonlarda daha azdır. Malign transformasyon total %0 subtotal % 66. 6 parsiyal % 100 biyopsi % 100 4 yıl izlem n (Kılıc T, et al: J Clin Neurosci. 2002 ; 9(5): 549 -52)
 n DGG’li olgularda uzun süreli tümör kontrolü için agresif cerrahi tedavinin en iyi seçenek olduğuna yönelik artan bir fikir birliği vardır. Ancak olguların çoğunluğunda radyolojik total rezeksiyon mümkün değildir. (Claus EB, et al. : Cancer 103(6): 1227– 1233, 2005) (Piepmeier JM: J Neurooncol 92: 253– 259, 2009)
n DGG’li olgularda uzun süreli tümör kontrolü için agresif cerrahi tedavinin en iyi seçenek olduğuna yönelik artan bir fikir birliği vardır. Ancak olguların çoğunluğunda radyolojik total rezeksiyon mümkün değildir. (Claus EB, et al. : Cancer 103(6): 1227– 1233, 2005) (Piepmeier JM: J Neurooncol 92: 253– 259, 2009)
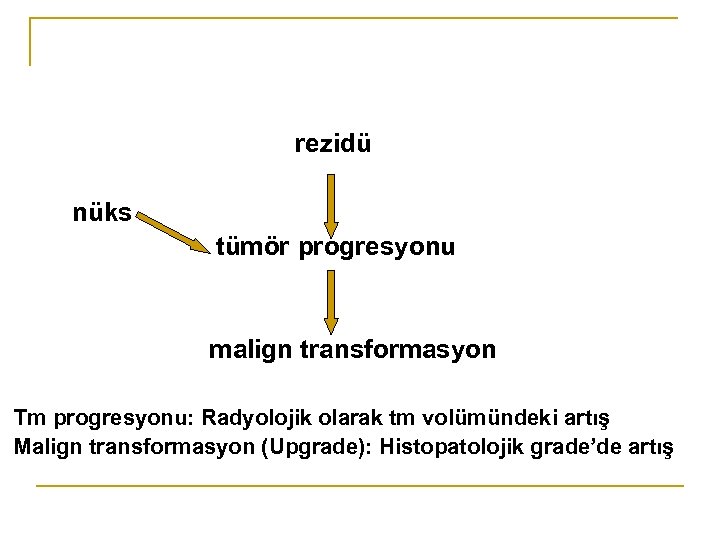 rezidü nüks tümör progresyonu malign transformasyon Tm progresyonu: Radyolojik olarak tm volümündeki artış Malign transformasyon (Upgrade): Histopatolojik grade’de artış
rezidü nüks tümör progresyonu malign transformasyon Tm progresyonu: Radyolojik olarak tm volümündeki artış Malign transformasyon (Upgrade): Histopatolojik grade’de artış
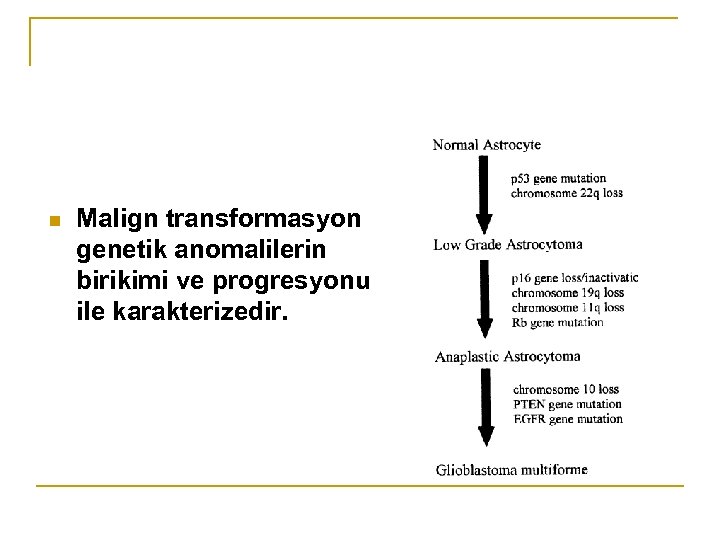 n Malign transformasyon genetik anomalilerin birikimi ve progresyonu ile karakterizedir.
n Malign transformasyon genetik anomalilerin birikimi ve progresyonu ile karakterizedir.
 Malign transformasyon çeşitli serilerde % 13 – 86 arasında bildirilmiştir. n DGG tümörlerde olgu kaybının en büyük nedeni malign transformasyondur. n (Afra D 1978, Laws ER 1984, Muller w 1977, Phillon JH 1993, Piepmeier 2009, Schmidt 2003)
Malign transformasyon çeşitli serilerde % 13 – 86 arasında bildirilmiştir. n DGG tümörlerde olgu kaybının en büyük nedeni malign transformasyondur. n (Afra D 1978, Laws ER 1984, Muller w 1977, Phillon JH 1993, Piepmeier 2009, Schmidt 2003)
 NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI ? ? ? CERRAHİ radyoterapi kemoterapi
NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI ? ? ? CERRAHİ radyoterapi kemoterapi
 n 130 yetişkin DGG tümör n Relapsda (~ takip 94 ay) Cerrahi (n=96) 2. total rezeksiyon Total rezeksiyon (ilk kez) Parsiyel r / Biyopsi % 33. 1 (% 26. 1) (% 27. 1) (% 46. 8) n Malign dejenerasyon ~ 71. 3 ay n 2 defa total rezeksiyon yapılan olgularda mt gelişmedi.
n 130 yetişkin DGG tümör n Relapsda (~ takip 94 ay) Cerrahi (n=96) 2. total rezeksiyon Total rezeksiyon (ilk kez) Parsiyel r / Biyopsi % 33. 1 (% 26. 1) (% 27. 1) (% 46. 8) n Malign dejenerasyon ~ 71. 3 ay n 2 defa total rezeksiyon yapılan olgularda mt gelişmedi.
 Relapsda malign transformasyon gelişmeyen olgularda total rezeksiyon yaşam süresini uzatır (p<0. 05). n (Rezvan A, et al. : Acta Neurochir 151: 1359– 1365, 2009)
Relapsda malign transformasyon gelişmeyen olgularda total rezeksiyon yaşam süresini uzatır (p<0. 05). n (Rezvan A, et al. : Acta Neurochir 151: 1359– 1365, 2009)
 fonksiyonal alanları tutan grade II gliomlarda çok aşamalı cerrahi yaklaşım n 2 olgu sunumu n f. MRI – intraoperatif mapping 2 kez subtotal rezeksiyon Malign transformasyon yok n n n
fonksiyonal alanları tutan grade II gliomlarda çok aşamalı cerrahi yaklaşım n 2 olgu sunumu n f. MRI – intraoperatif mapping 2 kez subtotal rezeksiyon Malign transformasyon yok n n n
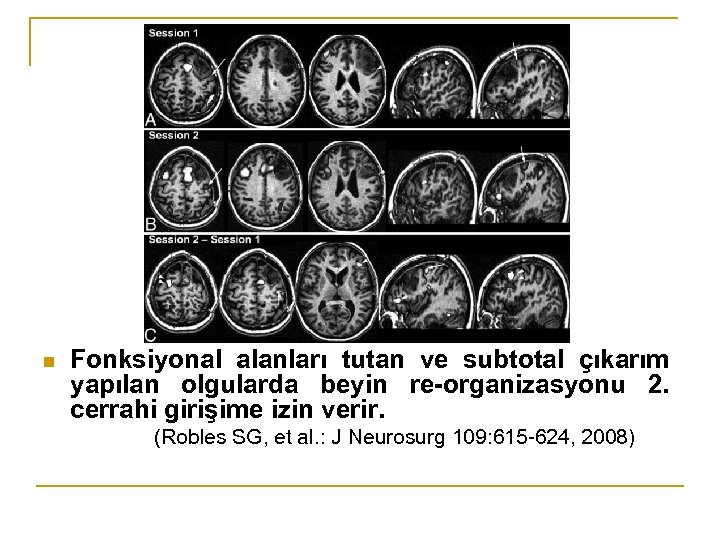 n Fonksiyonal alanları tutan ve subtotal çıkarım yapılan olgularda beyin re-organizasyonu 2. cerrahi girişime izin verir. (Robles SG, et al. : J Neurosurg 109: 615 -624, 2008)
n Fonksiyonal alanları tutan ve subtotal çıkarım yapılan olgularda beyin re-organizasyonu 2. cerrahi girişime izin verir. (Robles SG, et al. : J Neurosurg 109: 615 -624, 2008)
 n rekurren 19 DGG tümör (fonksiyonal alanları tutan) 1. cerrahi ~ 4. 1 yıl 2. cerrahi total r subtotal r biyopsi (f MRI + intraoperatif mapping) 1 olgu 13 5
n rekurren 19 DGG tümör (fonksiyonal alanları tutan) 1. cerrahi ~ 4. 1 yıl 2. cerrahi total r subtotal r biyopsi (f MRI + intraoperatif mapping) 1 olgu 13 5
 Olguların % 84’ü normal yaşamına döndü takip 6. 6 yıl – olgu kaybı yok (Martino J, et al. Acta Neurochir 151: 427– 436, 2009)
Olguların % 84’ü normal yaşamına döndü takip 6. 6 yıl – olgu kaybı yok (Martino J, et al. Acta Neurochir 151: 427– 436, 2009)
 “multistage surgical approach” (Duffau H: Curr Opin Oncol; 21(6): 543 -9, 2009) (Martino J, et al. Acta Neurochir 151: 427– 436, 2009) (Robles SG et al. J Neurosurg 109: 615– 624, 2008)
“multistage surgical approach” (Duffau H: Curr Opin Oncol; 21(6): 543 -9, 2009) (Martino J, et al. Acta Neurochir 151: 427– 436, 2009) (Robles SG et al. J Neurosurg 109: 615– 624, 2008)
 n İkinci operasyonun zamanlaması ? ? ? ? The authors suggested to ‘over indicate’ an early re-intervention in order to anticipate the second surgery before the anaplastic transformation (Duffau H 2009, Martino J 2009, Robles SG 2008)
n İkinci operasyonun zamanlaması ? ? ? ? The authors suggested to ‘over indicate’ an early re-intervention in order to anticipate the second surgery before the anaplastic transformation (Duffau H 2009, Martino J 2009, Robles SG 2008)
 İkinci cerrahinin zamanlamasına karar vermek için malign transformasyonun güvenilir göstergelerine ihtiyaç vardır.
İkinci cerrahinin zamanlamasına karar vermek için malign transformasyonun güvenilir göstergelerine ihtiyaç vardır.
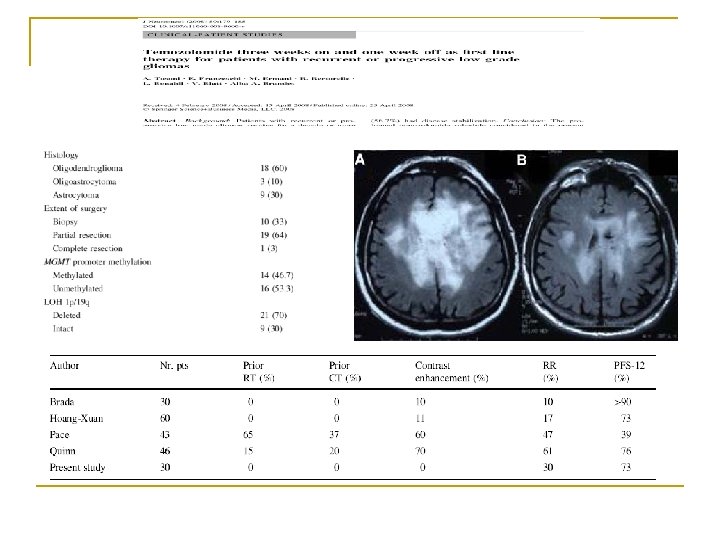
 n Gliomas: Predicting time to progression or survival with cerebral blood volume measurement at dynamic susceptibility-weighted contrast-enhanced perfusion MR imaging Law M, et al. : Radiology 247: 490 -498, 2008 n Prognostic value of choline and creatine in WHO grade II gliomas. Hattingen E, et al. : Neuroradiology 50: 759– 767, 2008 n n n Predictive value of multimodality MRI using conventional, perfusion, and spectroscopy MR in anaplastic transformation of low grade oligodendrogliomas. Hlaihel C, et al: J Neurooncol. 97(1): 2010 Low-grade gliomas: six-month tumor growth predicts patient outcome better than admission tumor volume, relative cerebral blood volume, and apparent diffusion coefficient. Caseiras BG et al: Radiology; 253(2): 505 -12, 2009 Volumes and growth rates of untreated adult low grade gliomas indicate risk of early malignant transformation. Res J, et al. : Eur J Radiol 72: 54 -64, 2009
n Gliomas: Predicting time to progression or survival with cerebral blood volume measurement at dynamic susceptibility-weighted contrast-enhanced perfusion MR imaging Law M, et al. : Radiology 247: 490 -498, 2008 n Prognostic value of choline and creatine in WHO grade II gliomas. Hattingen E, et al. : Neuroradiology 50: 759– 767, 2008 n n n Predictive value of multimodality MRI using conventional, perfusion, and spectroscopy MR in anaplastic transformation of low grade oligodendrogliomas. Hlaihel C, et al: J Neurooncol. 97(1): 2010 Low-grade gliomas: six-month tumor growth predicts patient outcome better than admission tumor volume, relative cerebral blood volume, and apparent diffusion coefficient. Caseiras BG et al: Radiology; 253(2): 505 -12, 2009 Volumes and growth rates of untreated adult low grade gliomas indicate risk of early malignant transformation. Res J, et al. : Eur J Radiol 72: 54 -64, 2009
 n Kolin / kreatin ~ 15. 4 ay > 2. 4 < 2. 4 n % 83 mt (+) % 100 mt (-) Tümör volüm ve büyüme oranı / yıl tm büyümesi / yıl n mt (-) > 6 ay % 56 mt (+) % 16 % 26 < 6 ay mt (+) > 3 (4)mm mt (+) Serebral kan volüm ölçümü r. CBV > 1. 75 ~ 365 gün mt (+) < 1. 75 ~ 889 gün mt (+)
n Kolin / kreatin ~ 15. 4 ay > 2. 4 < 2. 4 n % 83 mt (+) % 100 mt (-) Tümör volüm ve büyüme oranı / yıl tm büyümesi / yıl n mt (-) > 6 ay % 56 mt (+) % 16 % 26 < 6 ay mt (+) > 3 (4)mm mt (+) Serebral kan volüm ölçümü r. CBV > 1. 75 ~ 365 gün mt (+) < 1. 75 ~ 889 gün mt (+)
 NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI ? ? ? cerrahi RADYOTERAPİ kemoterapi
NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI ? ? ? cerrahi RADYOTERAPİ kemoterapi
 n n EORTC 22845 311 olgu q - gözlem (RT tm progresyonuna kadar ertelendi) q - RT (54 Gy) RT + RT (-) ~ yaşam süresi 7. 4 yıl 7. 2 yıl p= 0. 87 ~ PFS 5. 3 yıl 3. 4 yıl p< 0. 0001
n n EORTC 22845 311 olgu q - gözlem (RT tm progresyonuna kadar ertelendi) q - RT (54 Gy) RT + RT (-) ~ yaşam süresi 7. 4 yıl 7. 2 yıl p= 0. 87 ~ PFS 5. 3 yıl 3. 4 yıl p< 0. 0001
 EORTC 22844 – 22845 ANALİZİ Düşük-yüksek risk gruplu olguların belirlenmesi n n n > 40 yaş Astrositoma histolojisi Tümör çapı ≥ 6 cm Orta hattı geçen tm Cerrahi öncesi ND <3 düşük risk grubu ≥ 3 yüksek risk grubu o. yaşam s 7. 7 yıl o. yaşam s 3. 2 yıl
EORTC 22844 – 22845 ANALİZİ Düşük-yüksek risk gruplu olguların belirlenmesi n n n > 40 yaş Astrositoma histolojisi Tümör çapı ≥ 6 cm Orta hattı geçen tm Cerrahi öncesi ND <3 düşük risk grubu ≥ 3 yüksek risk grubu o. yaşam s 7. 7 yıl o. yaşam s 3. 2 yıl
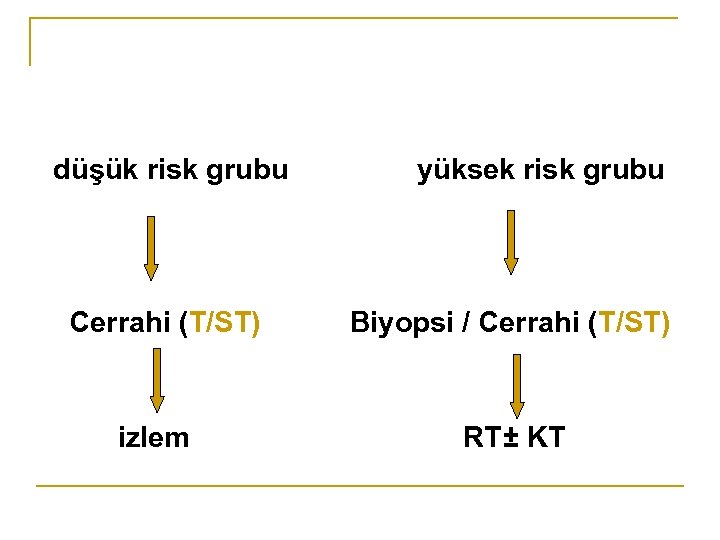 düşük risk grubu Cerrahi (T/ST) izlem yüksek risk grubu Biyopsi / Cerrahi (T/ST) RT± KT
düşük risk grubu Cerrahi (T/ST) izlem yüksek risk grubu Biyopsi / Cerrahi (T/ST) RT± KT
 n Sadece nöbet yakınması olan ve önemli oranda tümör rezeksiyonu sağlanan genç olgularda RT rekürrens veya progresyon zamanına kadar ertelenebilir. (Khan MK 2010, Kortmann RD 2004, Bent VD 2005) n Yaşlı, KPS düşük, rezidü tümörlü olgularda cerrahiyi takiben RT yapılmalıdır. ( yüksek proliferatif index – önemli derece boyanma ) (Cavaliere R 2005, Garcia DM 1985, Philippon JH 1993, Shaw EG 1993)
n Sadece nöbet yakınması olan ve önemli oranda tümör rezeksiyonu sağlanan genç olgularda RT rekürrens veya progresyon zamanına kadar ertelenebilir. (Khan MK 2010, Kortmann RD 2004, Bent VD 2005) n Yaşlı, KPS düşük, rezidü tümörlü olgularda cerrahiyi takiben RT yapılmalıdır. ( yüksek proliferatif index – önemli derece boyanma ) (Cavaliere R 2005, Garcia DM 1985, Philippon JH 1993, Shaw EG 1993)
 n 65 DGG tümör olgusu q % 49 postop RT q takip 12 yıl RT (-) % 27 RT (+) % 53 kognitif defisit p=0. 003 ‘Kognitif fonksiyonlarda güvenli dozlar olarak kabul edilen fraksiyone dozlarda bile (≤ 2 Gy) azalma saptandı. ’ MR’da kognitif defisitli tüm olgularda belirgin beyaz madde hiperintensiteleri ve kortikal atrofi mevcuttu. (Douw L, et al. : Lancet Neurol 2009, 8: 810– 818)
n 65 DGG tümör olgusu q % 49 postop RT q takip 12 yıl RT (-) % 27 RT (+) % 53 kognitif defisit p=0. 003 ‘Kognitif fonksiyonlarda güvenli dozlar olarak kabul edilen fraksiyone dozlarda bile (≤ 2 Gy) azalma saptandı. ’ MR’da kognitif defisitli tüm olgularda belirgin beyaz madde hiperintensiteleri ve kortikal atrofi mevcuttu. (Douw L, et al. : Lancet Neurol 2009, 8: 810– 818)
 NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI ? ? ? cerrahi radyoterapi KEMOTERAPİ
NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI ? ? ? cerrahi radyoterapi KEMOTERAPİ
 n n PCV TMZ (oral, daha az toksisite, KBB iyi geçer, gbm’e karşı PCV’den daha iyi cevap)
n n PCV TMZ (oral, daha az toksisite, KBB iyi geçer, gbm’e karşı PCV’den daha iyi cevap)
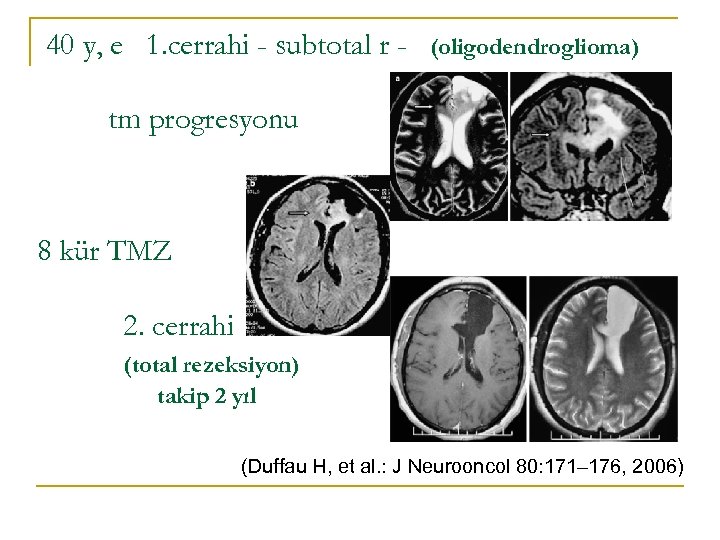 40 y, e 1. cerrahi - subtotal r - (oligodendroglioma) tm progresyonu 8 kür TMZ 2. cerrahi (total rezeksiyon) takip 2 yıl (Duffau H, et al. : J Neurooncol 80: 171– 176, 2006)
40 y, e 1. cerrahi - subtotal r - (oligodendroglioma) tm progresyonu 8 kür TMZ 2. cerrahi (total rezeksiyon) takip 2 yıl (Duffau H, et al. : J Neurooncol 80: 171– 176, 2006)
 RTOG 0424 Yüksek riskli DGG tümör TMZ / RT ECOG E 3 F 05 Progressif / semptomatik DGG tümör RT / RT + TMZ n n EORTC 22033 / 26033 DGG tümör n (>40 yaş, radyolojik progressif, yeni veya artmış ND) n n 1 p 19 q MGMT TMZ / RT
RTOG 0424 Yüksek riskli DGG tümör TMZ / RT ECOG E 3 F 05 Progressif / semptomatik DGG tümör RT / RT + TMZ n n EORTC 22033 / 26033 DGG tümör n (>40 yaş, radyolojik progressif, yeni veya artmış ND) n n 1 p 19 q MGMT TMZ / RT
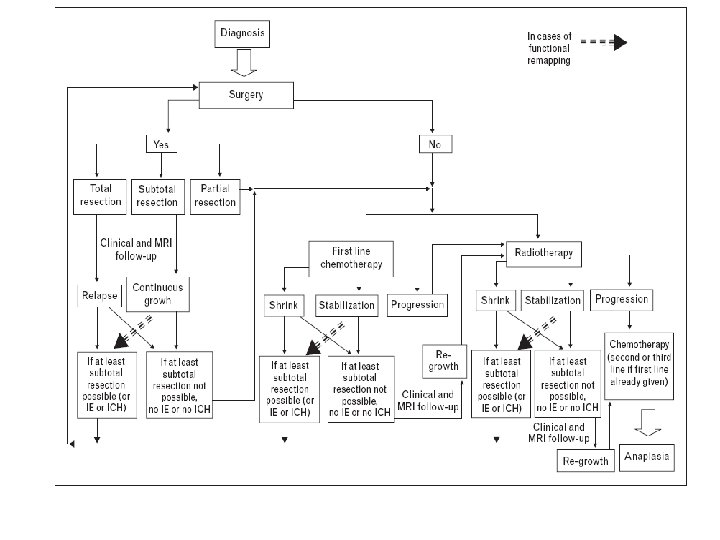 (Duffau H: Curr Opin Oncol. 2009 Nov; 21(6): 543 -9)
(Duffau H: Curr Opin Oncol. 2009 Nov; 21(6): 543 -9)
 NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI ikinci, gerekirse üçüncü rezeksiyonu içeren CERRAHİ tedavi ile kemoterapi ve radyoterapinin birlikte olduğu dinamik bir yaklaşım olmalıdır.
NÜKS ve REZİDÜ DÜŞÜK DERECELİ GLİAL TÜMÖRLERDE TEDAVİ ALGORİTMASI ikinci, gerekirse üçüncü rezeksiyonu içeren CERRAHİ tedavi ile kemoterapi ve radyoterapinin birlikte olduğu dinamik bir yaklaşım olmalıdır.


