lekcija_9_fiz-khim_svoistva.ppt.pptx
- Количество слайдов: 21
 Нуклеозиды и нуклеотиды. Первичная пространственная структура. Физико-химические свойства.
Нуклеозиды и нуклеотиды. Первичная пространственная структура. Физико-химические свойства.
 Конформация рибозной части в нуклеозидах и нуклеотидах.
Конформация рибозной части в нуклеозидах и нуклеотидах.
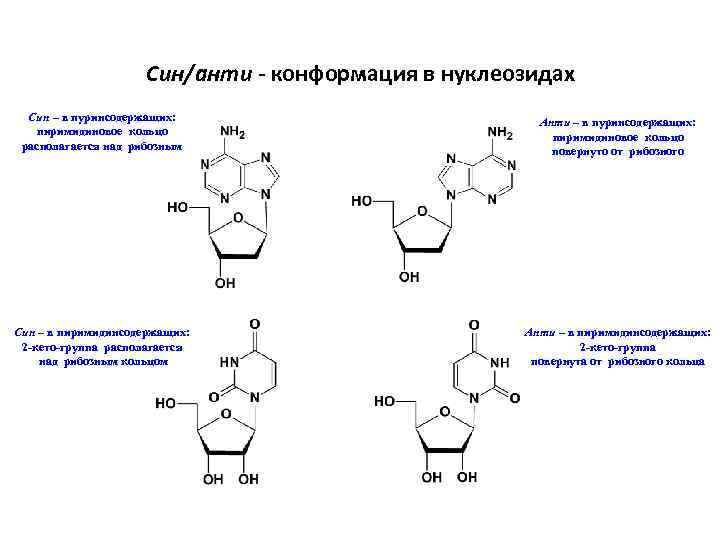 Син/анти - конформация в нуклеозидах Син – в пуринсодержащих: пиримидиновое кольцо располагается над рибозным Анти – в пуринсодержащих: пиримидиновое кольцо повернуто от рибозного Син – в пиримидинсодержащих: 2 -кето-группа располагается над рибозным кольцом Анти – в пиримидинсодержащих: 2 -кето-группа повернута от рибозного кольца
Син/анти - конформация в нуклеозидах Син – в пуринсодержащих: пиримидиновое кольцо располагается над рибозным Анти – в пуринсодержащих: пиримидиновое кольцо повернуто от рибозного Син – в пиримидинсодержащих: 2 -кето-группа располагается над рибозным кольцом Анти – в пиримидинсодержащих: 2 -кето-группа повернута от рибозного кольца
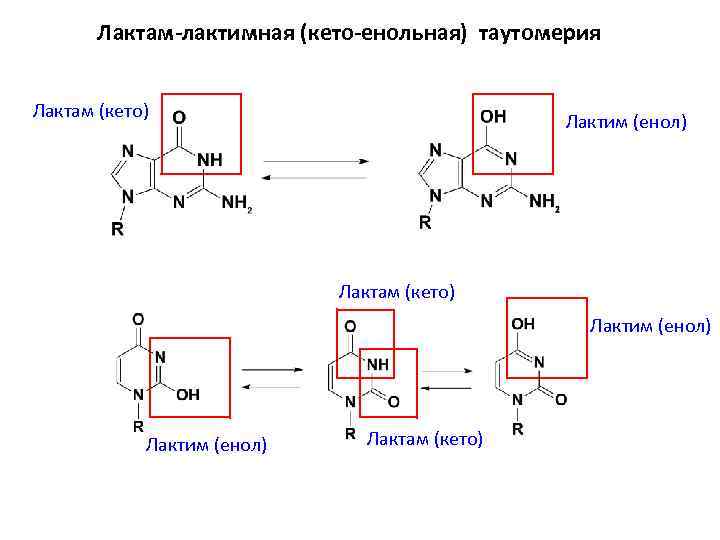 Лактам-лактимная (кето-енольная) таутомерия Лактам (кето) Лактим (енол) Лактам (кето)
Лактам-лактимная (кето-енольная) таутомерия Лактам (кето) Лактим (енол) Лактам (кето)
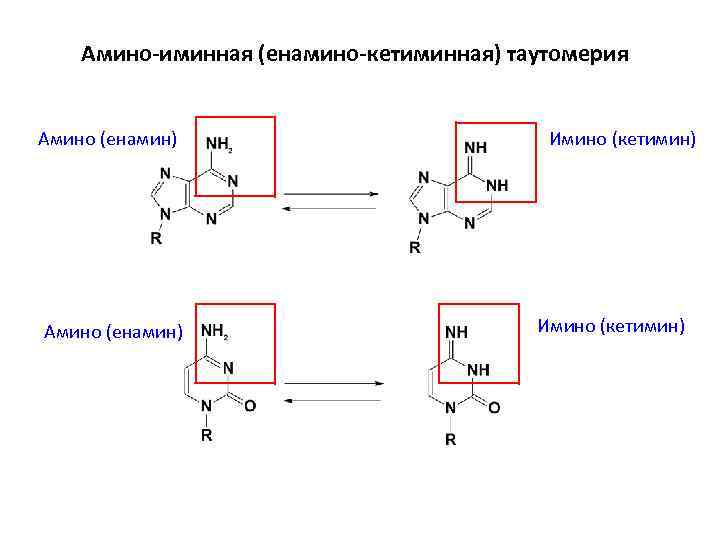 Амино-иминная (енамино-кетиминная) таутомерия Амино (енамин) Имино (кетимин)
Амино-иминная (енамино-кетиминная) таутомерия Амино (енамин) Имино (кетимин)
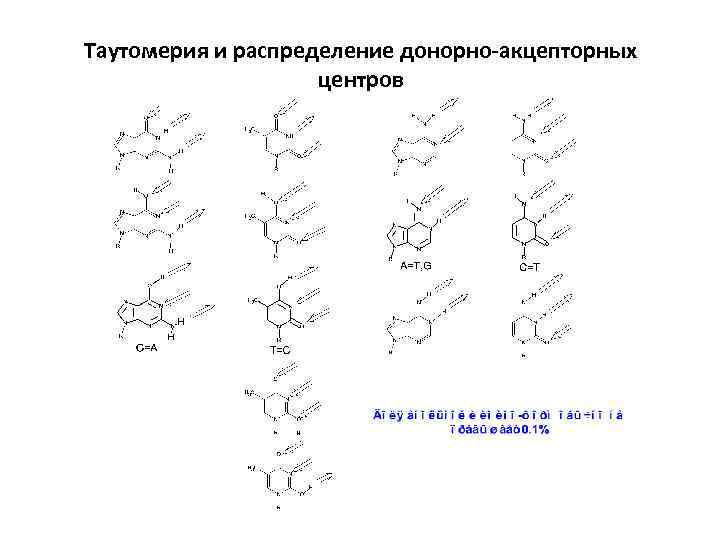 Таутомерия и распределение донорно-акцепторных центров
Таутомерия и распределение донорно-акцепторных центров
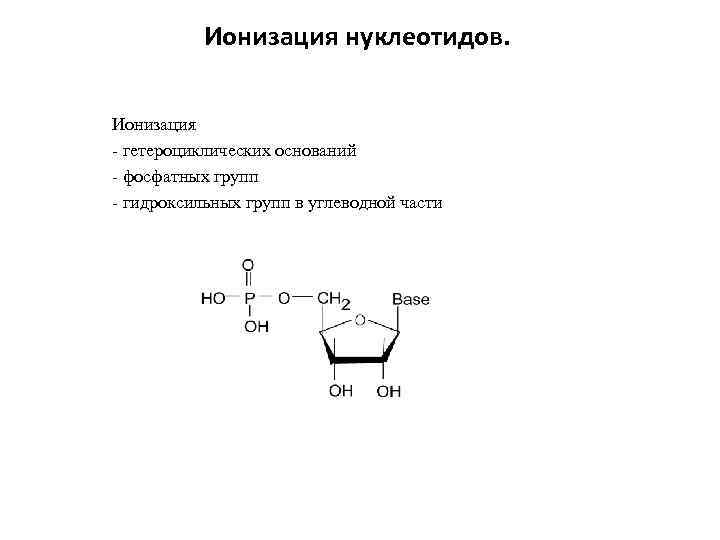 Ионизация нуклеотидов. Ионизация - гетероциклических оснований - фосфатных групп - гидроксильных групп в углеводной части
Ионизация нуклеотидов. Ионизация - гетероциклических оснований - фосфатных групп - гидроксильных групп в углеводной части
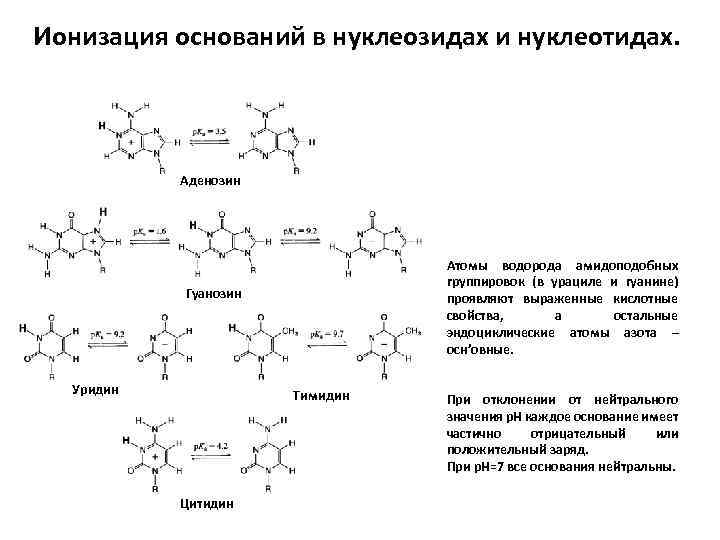 Ионизация оснований в нуклеозидах и нуклеотидах. Аденозин Атомы водорода амидоподобных группировок (в урациле и гуанине) проявляют выраженные кислотные свойства, а остальные эндоциклические атомы азота – осн’овные. Гуанозин Уридин Тимидин Цитидин При отклонении от нейтрального значения р. Н каждое основание имеет частично отрицательный или положительный заряд. При р. Н=7 все основания нейтральны.
Ионизация оснований в нуклеозидах и нуклеотидах. Аденозин Атомы водорода амидоподобных группировок (в урациле и гуанине) проявляют выраженные кислотные свойства, а остальные эндоциклические атомы азота – осн’овные. Гуанозин Уридин Тимидин Цитидин При отклонении от нейтрального значения р. Н каждое основание имеет частично отрицательный или положительный заряд. При р. Н=7 все основания нейтральны.
 Отрицательный индуктивный эффект пентозы (за счет гидроксильных групп) понижает р. Ка нуклеиновых оснований. Следствие: для дезоксирибонуклеозидов соответствующие значения р. Ка на 0. 1 -0. 3 р. Н выше. Cyt - 4. 6 Cyd – 4. 15 d. Cyd – 4. 25
Отрицательный индуктивный эффект пентозы (за счет гидроксильных групп) понижает р. Ка нуклеиновых оснований. Следствие: для дезоксирибонуклеозидов соответствующие значения р. Ка на 0. 1 -0. 3 р. Н выше. Cyt - 4. 6 Cyd – 4. 15 d. Cyd – 4. 25
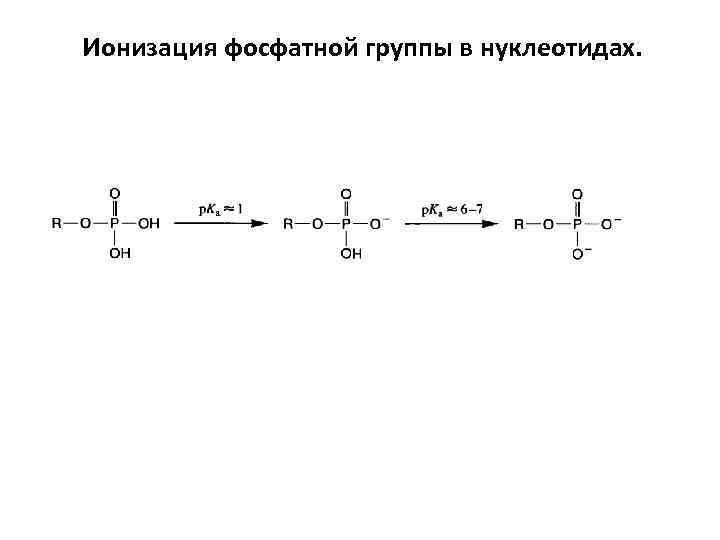 Ионизация фосфатной группы в нуклеотидах.
Ионизация фосфатной группы в нуклеотидах.
 Наличие фосфатной группы в нуклеотидах повышает соответствующие значения р. Ка (гетероцикла) на 0. 2 -0. 8 р. Н по сравнению с нуклеозидами. Gua – 3. 0; 9. 32 G – 2. 1; 9. 33 d. G - 2. 4; 9. 33 p. G - 2. 9; 9. 6
Наличие фосфатной группы в нуклеотидах повышает соответствующие значения р. Ка (гетероцикла) на 0. 2 -0. 8 р. Н по сравнению с нуклеозидами. Gua – 3. 0; 9. 32 G – 2. 1; 9. 33 d. G - 2. 4; 9. 33 p. G - 2. 9; 9. 6
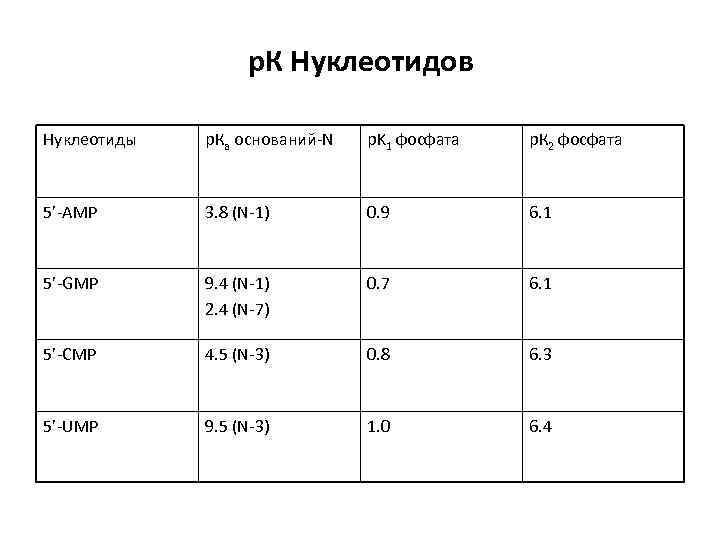 р. К Нуклеотидов Нуклеотиды р. Ка оснований-N p. K 1 фосфата р. К 2 фосфата 5’-AMP 3. 8 (N-1) 0. 9 6. 1 5’-GMP 9. 4 (N-1) 2. 4 (N-7) 0. 7 6. 1 5’-CMP 4. 5 (N-3) 0. 8 6. 3 5’-UMP 9. 5 (N-3) 1. 0 6. 4
р. К Нуклеотидов Нуклеотиды р. Ка оснований-N p. K 1 фосфата р. К 2 фосфата 5’-AMP 3. 8 (N-1) 0. 9 6. 1 5’-GMP 9. 4 (N-1) 2. 4 (N-7) 0. 7 6. 1 5’-CMP 4. 5 (N-3) 0. 8 6. 3 5’-UMP 9. 5 (N-3) 1. 0 6. 4
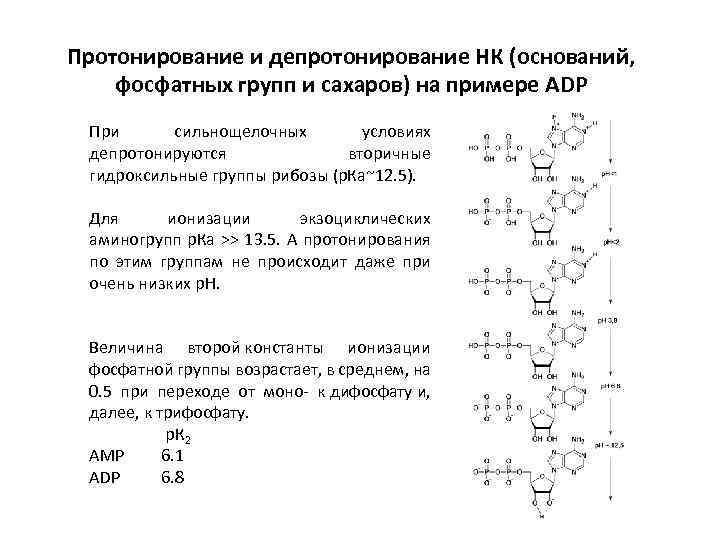 Протонирование и депротонирование НК (оснований, фосфатных групп и сахаров) на примере АDP При сильнощелочных условиях депротонируются вторичные гидроксильные группы рибозы (р. Ка~12. 5). Для ионизации экзоциклических аминогрупп р. Ка >> 13. 5. А протонирования по этим группам не происходит даже при очень низких р. Н. Величина второй константы ионизации фосфатной группы возрастает, в среднем, на 0. 5 при переходе от моно- к дифосфату и, далее, к трифосфату. р. К 2 AMP 6. 1 ADP 6. 8
Протонирование и депротонирование НК (оснований, фосфатных групп и сахаров) на примере АDP При сильнощелочных условиях депротонируются вторичные гидроксильные группы рибозы (р. Ка~12. 5). Для ионизации экзоциклических аминогрупп р. Ка >> 13. 5. А протонирования по этим группам не происходит даже при очень низких р. Н. Величина второй константы ионизации фосфатной группы возрастает, в среднем, на 0. 5 при переходе от моно- к дифосфату и, далее, к трифосфату. р. К 2 AMP 6. 1 ADP 6. 8
 Возникновение зарядов как следствие ионизации При отклонении от нейтрального значения р. Н каждое основание имеет частично отрицательный или положительный заряд. При р. Н=7 все основания нейтральны. В мономерном нуклеотиде при р. Н>7 заряд фосфатной группы -2, при р. Н<6 фосфат - однозарядный анион. При р. Н=1 и меньше - ионизации нет. Каждая фосфодиэфирная группа в олиго-(поли-)нуклеотиде содержит только один протон, с р. Ка ~1. Следовательно, при р. Н>1 каждая фосфатная группа частично заряжена. Суммарный заряд нуклеотида = заряд фосфата + заряд основания + заряд сахара
Возникновение зарядов как следствие ионизации При отклонении от нейтрального значения р. Н каждое основание имеет частично отрицательный или положительный заряд. При р. Н=7 все основания нейтральны. В мономерном нуклеотиде при р. Н>7 заряд фосфатной группы -2, при р. Н<6 фосфат - однозарядный анион. При р. Н=1 и меньше - ионизации нет. Каждая фосфодиэфирная группа в олиго-(поли-)нуклеотиде содержит только один протон, с р. Ка ~1. Следовательно, при р. Н>1 каждая фосфатная группа частично заряжена. Суммарный заряд нуклеотида = заряд фосфата + заряд основания + заряд сахара
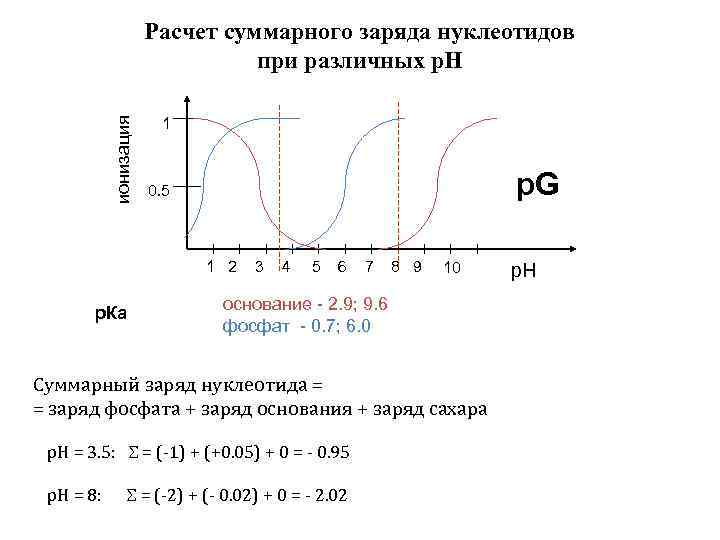 ионизация Расчет суммарного заряда нуклеотидов при различных р. Н 1 p. G 0. 5 1 2 р. Ка 3 4 5 6 7 8 9 10 основание - 2. 9; 9. 6 фосфат - 0. 7; 6. 0 Суммарный заряд нуклеотида = = заряд фосфата + заряд основания + заряд сахара р. Н = 3. 5: = (-1) + (+0. 05) + 0 = - 0. 95 р. Н = 8: = (-2) + (- 0. 02) + 0 = - 2. 02 р. Н
ионизация Расчет суммарного заряда нуклеотидов при различных р. Н 1 p. G 0. 5 1 2 р. Ка 3 4 5 6 7 8 9 10 основание - 2. 9; 9. 6 фосфат - 0. 7; 6. 0 Суммарный заряд нуклеотида = = заряд фосфата + заряд основания + заряд сахара р. Н = 3. 5: = (-1) + (+0. 05) + 0 = - 0. 95 р. Н = 8: = (-2) + (- 0. 02) + 0 = - 2. 02 р. Н
 Суммарный заряд различных нуклеотидов при одном и том же значении р. Н Заряды оснований сильнее всего различаются при р. Н=3. 5. +0. 54 – Аde; +0. 84 – Cyt; +0. 05 – Gua; 0 – Ura Заряд фосфата при р. Н=3. 5 во всех случаях -1. Следовательно, суммарный заряд нуклеотидов при р. Н=3. 5 составляет - 0. 46 – p. A; - 0. 16 – p. C; - 0. 95 – p. G; - 1. 0 – p. U
Суммарный заряд различных нуклеотидов при одном и том же значении р. Н Заряды оснований сильнее всего различаются при р. Н=3. 5. +0. 54 – Аde; +0. 84 – Cyt; +0. 05 – Gua; 0 – Ura Заряд фосфата при р. Н=3. 5 во всех случаях -1. Следовательно, суммарный заряд нуклеотидов при р. Н=3. 5 составляет - 0. 46 – p. A; - 0. 16 – p. C; - 0. 95 – p. G; - 1. 0 – p. U
 Нуклеиновые основания в кислой среде протонируются неодинаково. Это дает возможность создавать различие суммарных зарядов нуклеотидов, которое удобно использовать для разделения составляющих НК, например, путем выбора ионообменной смолы и р. Н элюента для ионообменной хроматографии.
Нуклеиновые основания в кислой среде протонируются неодинаково. Это дает возможность создавать различие суммарных зарядов нуклеотидов, которое удобно использовать для разделения составляющих НК, например, путем выбора ионообменной смолы и р. Н элюента для ионообменной хроматографии.
 УФ спектроскопия Спектральные характеристики нуклеотидов определяются нуклеозидным компонентом. УФ спектр зависит от р. Н среды.
УФ спектроскопия Спектральные характеристики нуклеотидов определяются нуклеозидным компонентом. УФ спектр зависит от р. Н среды.
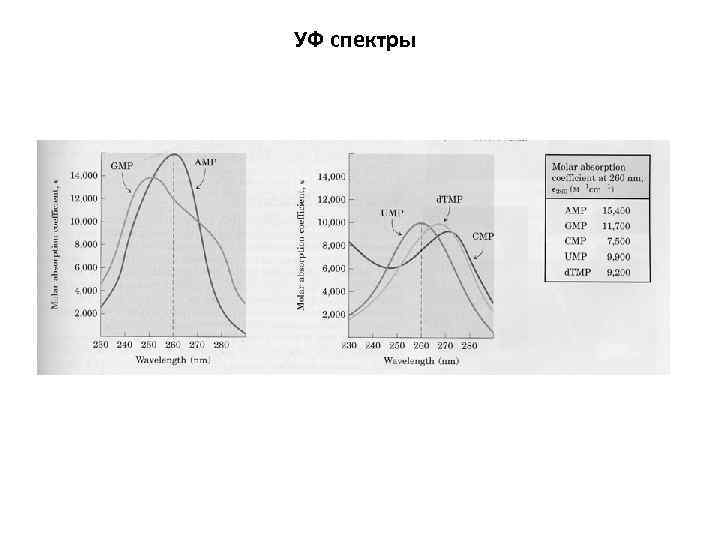 УФ спектры
УФ спектры
 УФ спектроскопия Метод УФ-спектроскопии используют для: - идентификации нуклеозидов /оснований (аденин, тимин, гуанин, цитозин) в нуклеотидном составе ДНК - количественного анализа составляющих ДНК - определения содержания (концентрации) выделенной ДНК - расчета к-ва реагентов для ПЦР - изменения пространственной структуры нуклеотидов и их полимеров (напр. , в двухцепочечной ДНК: денатурацию и ренатурацию при изменении р. Н, температуры и т. д. ) - обнаружения химических модификаций или эффектов протонирования/депротонирования оснований - и др. Программа Oligo http: //www. bio. bsu. by/molbiol/oligocalc. html
УФ спектроскопия Метод УФ-спектроскопии используют для: - идентификации нуклеозидов /оснований (аденин, тимин, гуанин, цитозин) в нуклеотидном составе ДНК - количественного анализа составляющих ДНК - определения содержания (концентрации) выделенной ДНК - расчета к-ва реагентов для ПЦР - изменения пространственной структуры нуклеотидов и их полимеров (напр. , в двухцепочечной ДНК: денатурацию и ренатурацию при изменении р. Н, температуры и т. д. ) - обнаружения химических модификаций или эффектов протонирования/депротонирования оснований - и др. Программа Oligo http: //www. bio. bsu. by/molbiol/oligocalc. html
 Физико-химические свойства нуклеозидов - кристаллические вещества, плохо растворимые в воде; - обладают слабыми основными свойствами; - склонность к протонированию убывает в ряду : C>G>A>T = U - имеют характерные р. Н-зависимые УФ спектры (см. табл. ). * В скобках приведена конц. в воде (масс. %); щел. -щелочная среда. ** В скобках приведено значение (в тысячах о. е. ).
Физико-химические свойства нуклеозидов - кристаллические вещества, плохо растворимые в воде; - обладают слабыми основными свойствами; - склонность к протонированию убывает в ряду : C>G>A>T = U - имеют характерные р. Н-зависимые УФ спектры (см. табл. ). * В скобках приведена конц. в воде (масс. %); щел. -щелочная среда. ** В скобках приведено значение (в тысячах о. е. ).


