 Нуклеофильное замещение у насыщенного атома углерода Yp + R-Xq R-Yp+1 + Xq-1 Y = H-Hal, Hal-, H-OH, OH-, ROH, RO-, CN-, RCOO-, R 3 N, R 3 P, RS-H, RS- и др. X = Hal, OH 2+, OR 2+, OCOR, OSO 2 R, NR 3+, SR 2+, N=N+ и др. Реакции, в которых нуклеофил одновременно является растворителем – реакции сольволиза
Нуклеофильное замещение у насыщенного атома углерода Yp + R-Xq R-Yp+1 + Xq-1 Y = H-Hal, Hal-, H-OH, OH-, ROH, RO-, CN-, RCOO-, R 3 N, R 3 P, RS-H, RS- и др. X = Hal, OH 2+, OR 2+, OCOR, OSO 2 R, NR 3+, SR 2+, N=N+ и др. Реакции, в которых нуклеофил одновременно является растворителем – реакции сольволиза
 Мономолекулярное нуклеофильное замещение R 3 C-X R 3 C + + Y - k 1 k-1 k 2 R 3 C + + X- R 3 CY определяет скорость определяет продукт Метод стационарных концентраций d[RX] k 1 k 2 [RX][Y] = W = dt k-1 [X] + k 2 [Y] Уменьшение константы скорости в присутствии Х- (эффект общего иона)
Мономолекулярное нуклеофильное замещение R 3 C-X R 3 C + + Y - k 1 k-1 k 2 R 3 C + + X- R 3 CY определяет скорость определяет продукт Метод стационарных концентраций d[RX] k 1 k 2 [RX][Y] = W = dt k-1 [X] + k 2 [Y] Уменьшение константы скорости в присутствии Х- (эффект общего иона)
 Схема Уинстейна Обычно ионные пары реагируют с Х(внутренний возврат), а свободный ион и разделенная ионная пара дают продукт
Схема Уинстейна Обычно ионные пары реагируют с Х(внутренний возврат), а свободный ион и разделенная ионная пара дают продукт
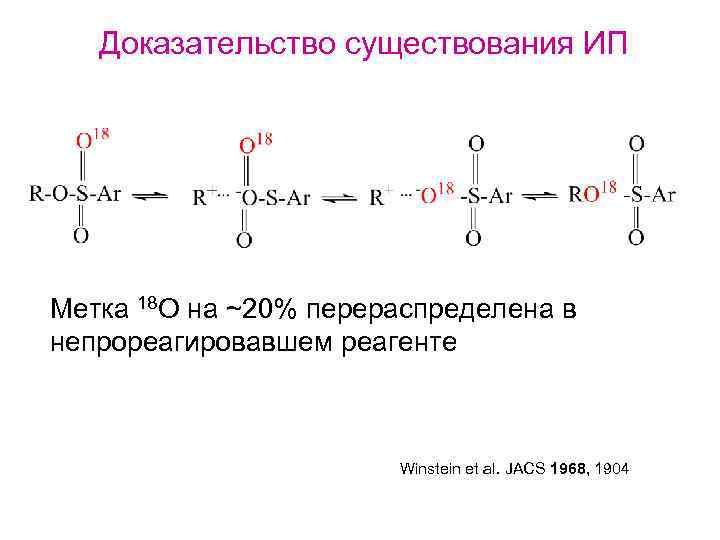 Доказательство существования ИП Meтка 18 О на ~20% перераспределена в непрореагировавшем реагенте Winstein et al. JACS 1968, 1904
Доказательство существования ИП Meтка 18 О на ~20% перераспределена в непрореагировавшем реагенте Winstein et al. JACS 1968, 1904
 Механизм SN 1 2. Проявление свойств карбокатиона (продукты замещения, отщепления, перегруппировки) а)скорость реакции увеличивается по мере роста стабильности образующегося карбокатиона б) потеря оптической активности на стадии ИП в) lg (k. X/k. H) = rs+, r (-3 -5) г) DH= велико, DS= близко к нулю
Механизм SN 1 2. Проявление свойств карбокатиона (продукты замещения, отщепления, перегруппировки) а)скорость реакции увеличивается по мере роста стабильности образующегося карбокатиона б) потеря оптической активности на стадии ИП в) lg (k. X/k. H) = rs+, r (-3 -5) г) DH= велико, DS= близко к нулю
 Кинетичекие изотопные эффекты в сольволизе SN 1 Вторичные k. H/k. D = 1. 1 1. 2 Первичные (С 14, Сl 37) k. H/k. D малы
Кинетичекие изотопные эффекты в сольволизе SN 1 Вторичные k. H/k. D = 1. 1 1. 2 Первичные (С 14, Сl 37) k. H/k. D малы
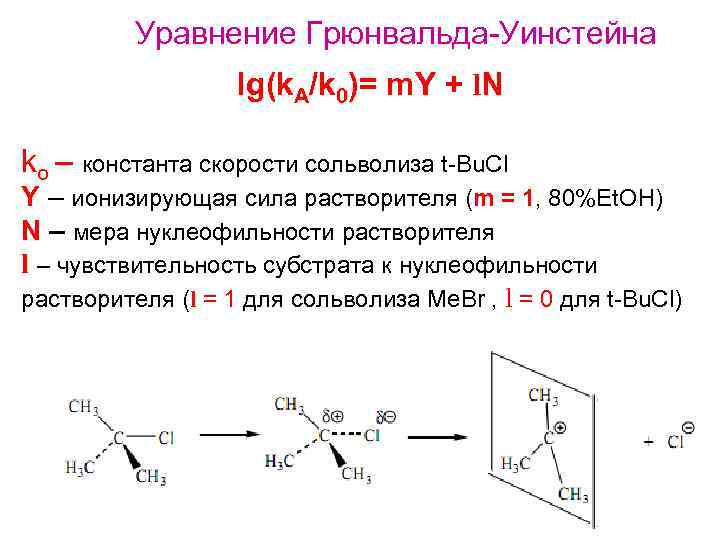 Уравнение Грюнвальда-Уинстейна lg(k. A/k 0)= m. Y + l. N ko – константа скорости сольволиза t-Bu. Cl Y – ионизирующая сила растворителя (m = 1, 80%Et. OH) N – мера нуклеофильности растворителя l – чувствительность субстрата к нуклеофильности растворителя (l = 1 для сольволиза Me. Br , l = 0 для t-Bu. Cl)
Уравнение Грюнвальда-Уинстейна lg(k. A/k 0)= m. Y + l. N ko – константа скорости сольволиза t-Bu. Cl Y – ионизирующая сила растворителя (m = 1, 80%Et. OH) N – мера нуклеофильности растворителя l – чувствительность субстрата к нуклеофильности растворителя (l = 1 для сольволиза Me. Br , l = 0 для t-Bu. Cl)
![Критерии SN 2 sp 3 sp 2 1. W = k [Y] [RX] нуклеофил Критерии SN 2 sp 3 sp 2 1. W = k [Y] [RX] нуклеофил](https://present5.com/presentation/25205551_349950153/image-8.jpg) Критерии SN 2 sp 3 sp 2 1. W = k [Y] [RX] нуклеофил участвует на lim стадии 2. Обращение конфигурации 3. DH= обычно ниже, чем для SN 1, DS= отрицательна (-15 -40 э. е) 4. Акцепторы R несколько ускоряют реакцию (r невелико, 0. 5 1. 0 )
Критерии SN 2 sp 3 sp 2 1. W = k [Y] [RX] нуклеофил участвует на lim стадии 2. Обращение конфигурации 3. DH= обычно ниже, чем для SN 1, DS= отрицательна (-15 -40 э. е) 4. Акцепторы R несколько ускоряют реакцию (r невелико, 0. 5 1. 0 )
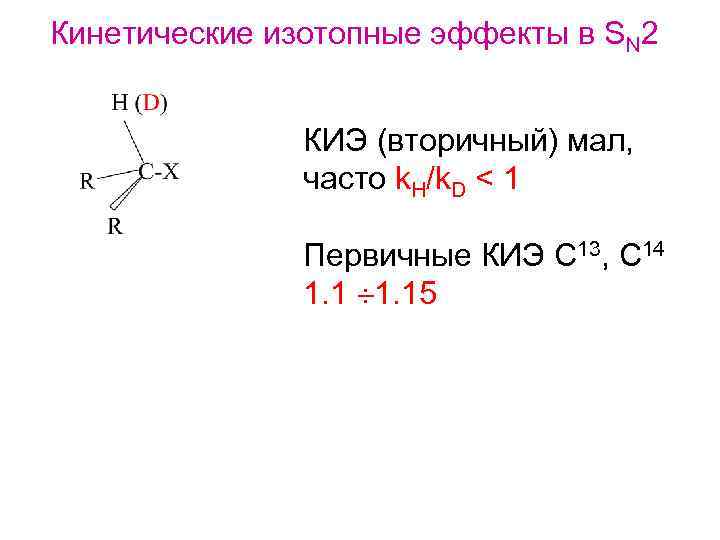 Кинетические изотопные эффекты в SN 2 КИЭ (вторичный) мал, часто k. H/k. D < 1 Первичные КИЭ С 13, С 14 1. 15
Кинетические изотопные эффекты в SN 2 КИЭ (вторичный) мал, часто k. H/k. D < 1 Первичные КИЭ С 13, С 14 1. 15
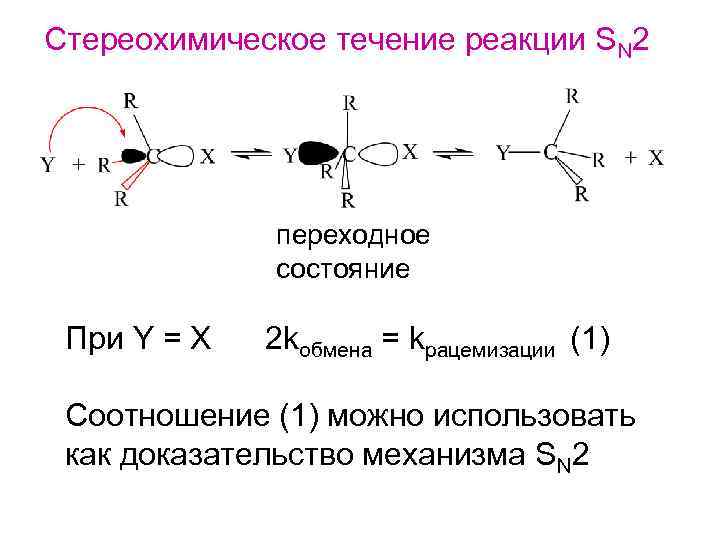 Стереохимическое течение реакции SN 2 переходное состояние При Y = X 2 kобмена = kрацемизации (1) Соотношение (1) можно использовать как доказательство механизма SN 2
Стереохимическое течение реакции SN 2 переходное состояние При Y = X 2 kобмена = kрацемизации (1) Соотношение (1) можно использовать как доказательство механизма SN 2
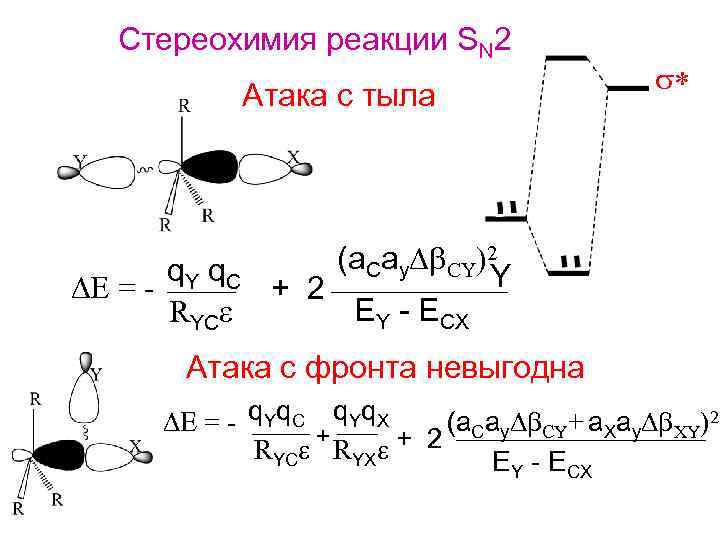 Стереохимия реакции SN 2 s* Атака с тыла q. Y q. C DE = RYCe (a. Cay. Db. CY)2 Y + 2 EY - ECX Атака с фронта невыгодна DE = - q. Yq. C + q. Yq. X (a. Cay. Db. CY+ a. Xay. Db. XY)2 RYCe RYXe + 2 E -E Y CX
Стереохимия реакции SN 2 s* Атака с тыла q. Y q. C DE = RYCe (a. Cay. Db. CY)2 Y + 2 EY - ECX Атака с фронта невыгодна DE = - q. Yq. C + q. Yq. X (a. Cay. Db. CY+ a. Xay. Db. XY)2 RYCe RYXe + 2 E -E Y CX
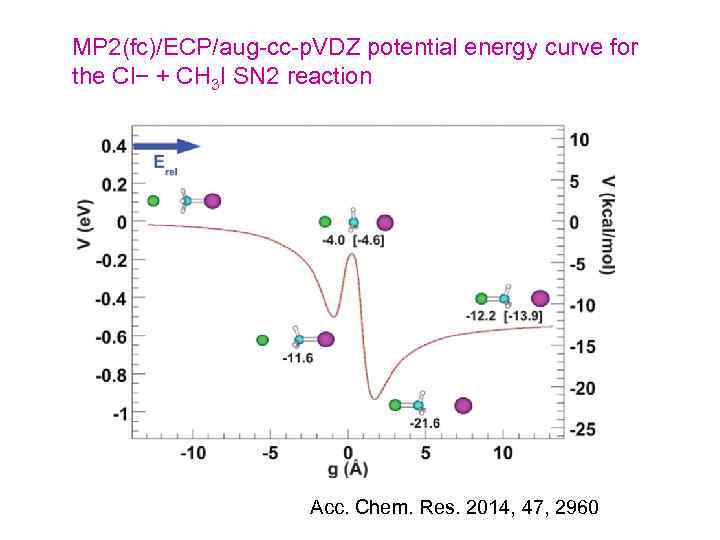 MP 2(fc)/ECP/aug-cc-p. VDZ potential energy curve for the Cl− + CH 3 I SN 2 reaction Acc. Chem. Res. 2014, 47, 2960
MP 2(fc)/ECP/aug-cc-p. VDZ potential energy curve for the Cl− + CH 3 I SN 2 reaction Acc. Chem. Res. 2014, 47, 2960
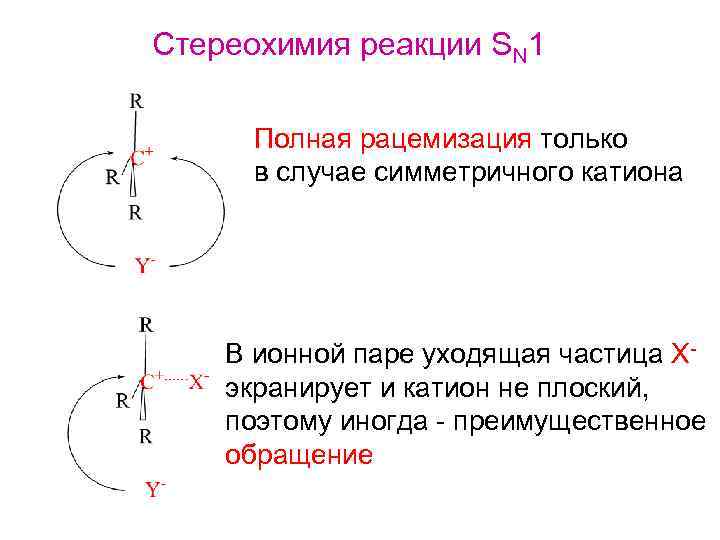 Стереохимия реакции SN 1 Полная рацемизация только в случае симметричного катиона В ионной паре уходящая частица Хэкранирует и катион не плоский, поэтому иногда - преимущественное обращение
Стереохимия реакции SN 1 Полная рацемизация только в случае симметричного катиона В ионной паре уходящая частица Хэкранирует и катион не плоский, поэтому иногда - преимущественное обращение
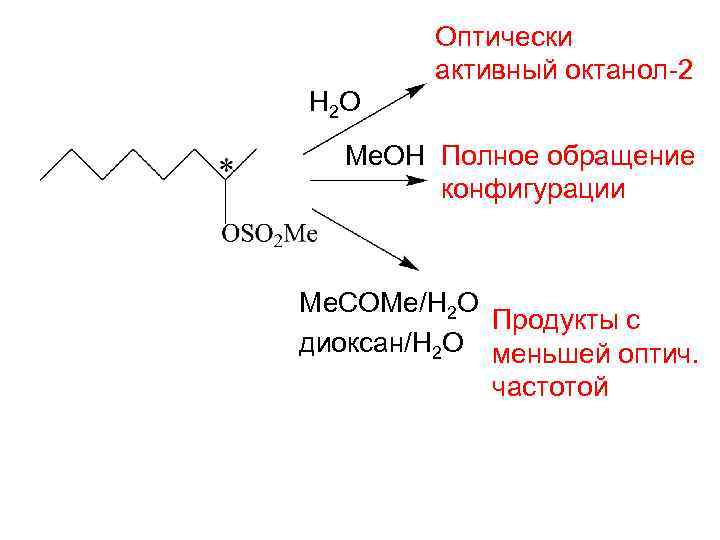 Оптически активный октанол-2 H 2 O Me. OH Полное обращение конфигурации Me. COMe/H 2 O Продукты с диоксан/H 2 O меньшей оптич. частотой
Оптически активный октанол-2 H 2 O Me. OH Полное обращение конфигурации Me. COMe/H 2 O Продукты с диоксан/H 2 O меньшей оптич. частотой
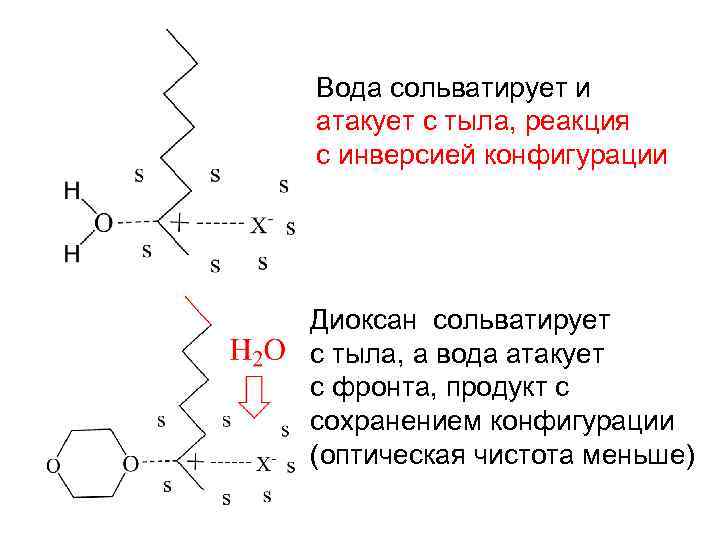 Вода сольватирует и атакует с тыла, реакция с инверсией конфигурации Диоксан сольватирует с тыла, а вода атакует с фронта, продукт с сохранением конфигурации (оптическая чистота меньше)
Вода сольватирует и атакует с тыла, реакция с инверсией конфигурации Диоксан сольватирует с тыла, а вода атакует с фронта, продукт с сохранением конфигурации (оптическая чистота меньше)