Нуклеиновые кислоты План лекции Сформировать









3874210_nukleinovuye_kislotuy_farm.ppt
- Размер: 876.5 Кб
- Количество слайдов: 50
Описание презентации Нуклеиновые кислоты План лекции Сформировать по слайдам
 Нуклеиновые кислоты
Нуклеиновые кислоты
 План лекции Сформировать представление о взаимосвязи химического строения и биологической роли нуклеиновых кислот
План лекции Сформировать представление о взаимосвязи химического строения и биологической роли нуклеиновых кислот
 План лекции 1. Структурные компоненты нуклеиновых кислот; 2. Строение нуклеиновых оснований. Лактим-лактамная таутомерия; 3. Строение и химические свойства нуклеозидов; 4. Строение и химические свойства нуклеотидов; 5. Строение и биологическая роль АТФ, АДФ, АМФ; 6. Виды структур нуклеиновых кислот; 7. Медико-биологические свойства нуклеиновых кислот.
План лекции 1. Структурные компоненты нуклеиновых кислот; 2. Строение нуклеиновых оснований. Лактим-лактамная таутомерия; 3. Строение и химические свойства нуклеозидов; 4. Строение и химические свойства нуклеотидов; 5. Строение и биологическая роль АТФ, АДФ, АМФ; 6. Виды структур нуклеиновых кислот; 7. Медико-биологические свойства нуклеиновых кислот.
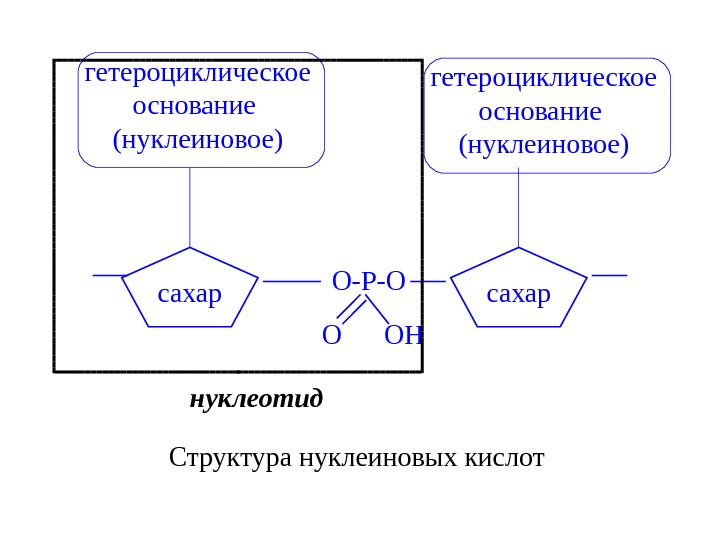
 гетероциклическое основание (нуклеиновое) сахар O-P-O O OH сахар Структура нуклеиновых кислот нуклеотид гетероциклическое основание (нуклеиновое)
гетероциклическое основание (нуклеиновое) сахар O-P-O O OH сахар Структура нуклеиновых кислот нуклеотид гетероциклическое основание (нуклеиновое)
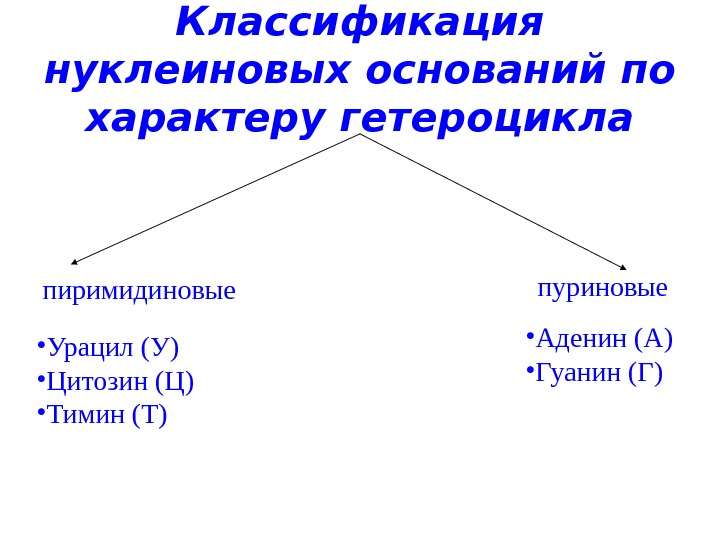
 Классификация нуклеиновых оснований по характеру гетероцикла пиримидиновые • Урацил (У) • Цитозин (Ц) • Тимин (Т) пуриновые • Аденин (А) • Гуанин (Г)
Классификация нуклеиновых оснований по характеру гетероцикла пиримидиновые • Урацил (У) • Цитозин (Ц) • Тимин (Т) пуриновые • Аденин (А) • Гуанин (Г)
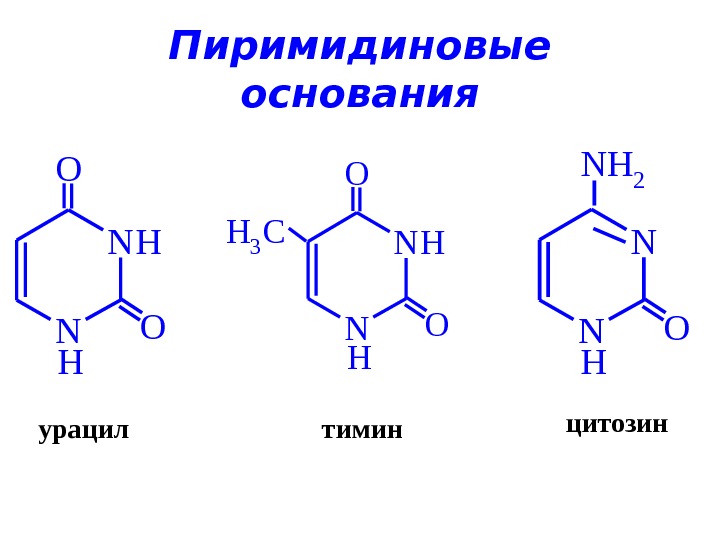
 N NH H O O H 3 C N N H O NH 2 урацил тимин цитозин. Пиримидиновые основания
N NH H O O H 3 C N N H O NH 2 урацил тимин цитозин. Пиримидиновые основания
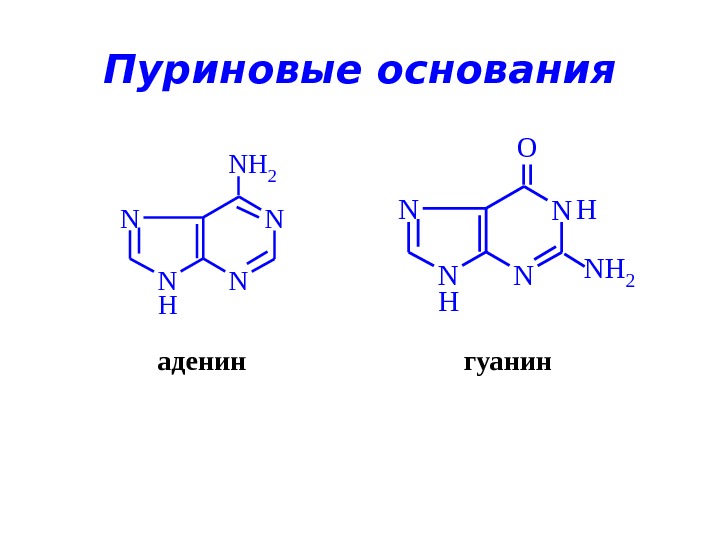
 аденин гуанин. Пуриновые основания. H N NN N NH 2 O H N NN N NH 2 H
аденин гуанин. Пуриновые основания. H N NN N NH 2 O H N NN N NH 2 H
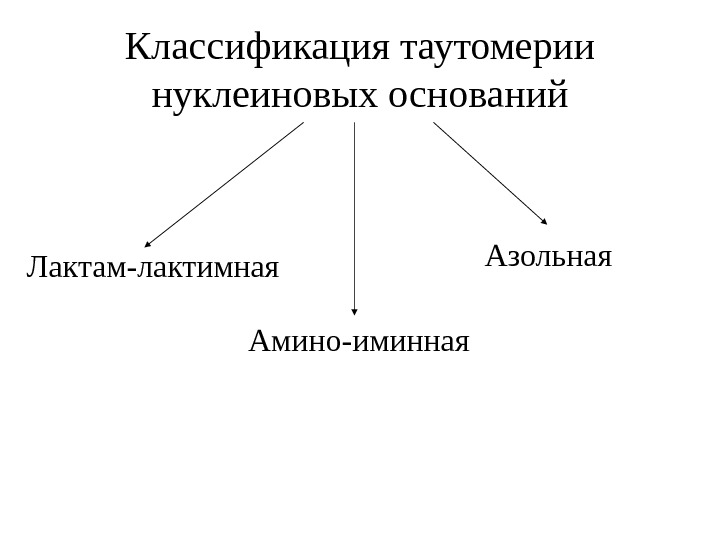
 Классификация таутомерии нуклеиновых оснований Лактам-лактимная Амино-иминная Азольная
Классификация таутомерии нуклеиновых оснований Лактам-лактимная Амино-иминная Азольная
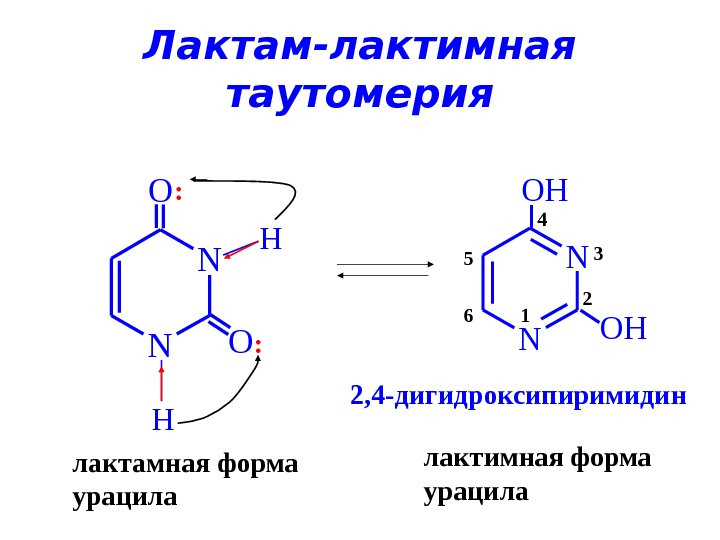
 Лактам-лактимная таутомерия N NO O H H : : N N OH OH лактамная форма урацила лактимная форма урацила 2 1 34 5 6 2, 4 -дигидроксипиримидин
Лактам-лактимная таутомерия N NO O H H : : N N OH OH лактамная форма урацила лактимная форма урацила 2 1 34 5 6 2, 4 -дигидроксипиримидин
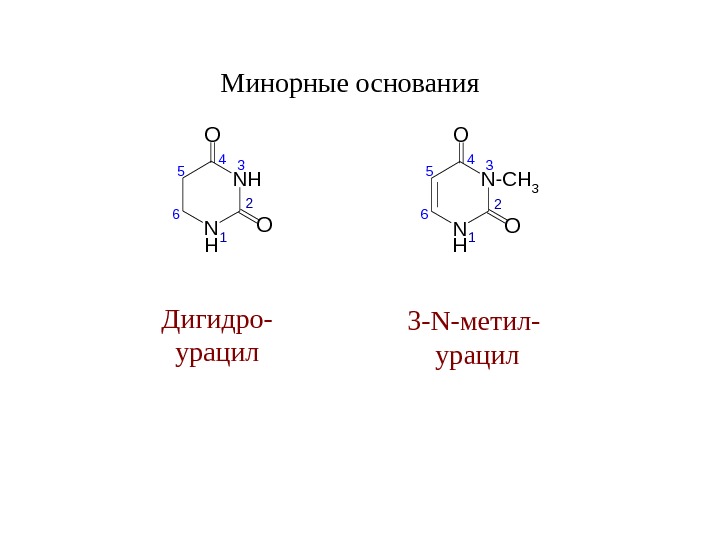
 Минорные основания N HO O 1 234 5 6 Дигидро- урацил N H N — C H 3 O O 1 234 5 6 3 — N- метил- урацил
Минорные основания N HO O 1 234 5 6 Дигидро- урацил N H N — C H 3 O O 1 234 5 6 3 — N- метил- урацил
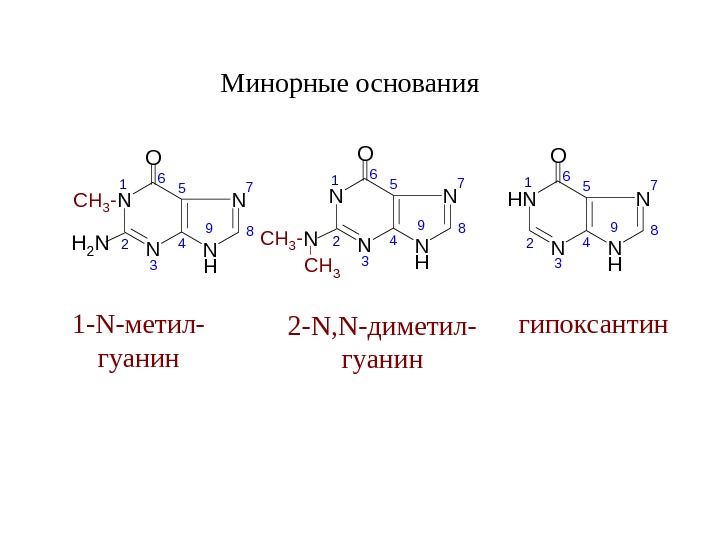
 N N H N N O H 2 N 56 4 3 2 17 89 CH 3 -Минорные основания N N HN NO N 56 4 321 7 89 CH 3 — CH 3 1 — N -метил- гуанин 2 -N, N- диметил- гуанин N N HNH NO 56 4 321 7 89 гипоксантин
N N H N N O H 2 N 56 4 3 2 17 89 CH 3 -Минорные основания N N HN NO N 56 4 321 7 89 CH 3 — CH 3 1 — N -метил- гуанин 2 -N, N- диметил- гуанин N N HNH NO 56 4 321 7 89 гипоксантин
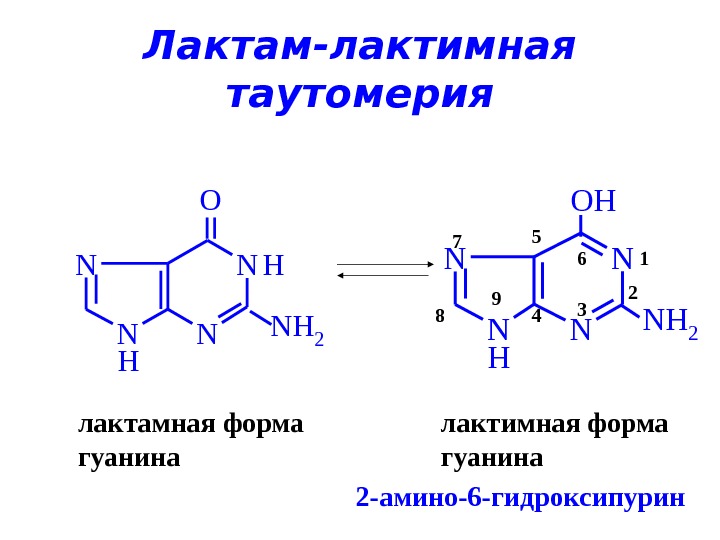
 Лактам-лактимная таутомерия. O H N NN N NH 2 H лактамная форма гуанина. N NN N H OH NH 2 лактимная форма гуанина 1 2 3 45 67 8 9 2 -амино-6 -гидроксипурин
Лактам-лактимная таутомерия. O H N NN N NH 2 H лактамная форма гуанина. N NN N H OH NH 2 лактимная форма гуанина 1 2 3 45 67 8 9 2 -амино-6 -гидроксипурин
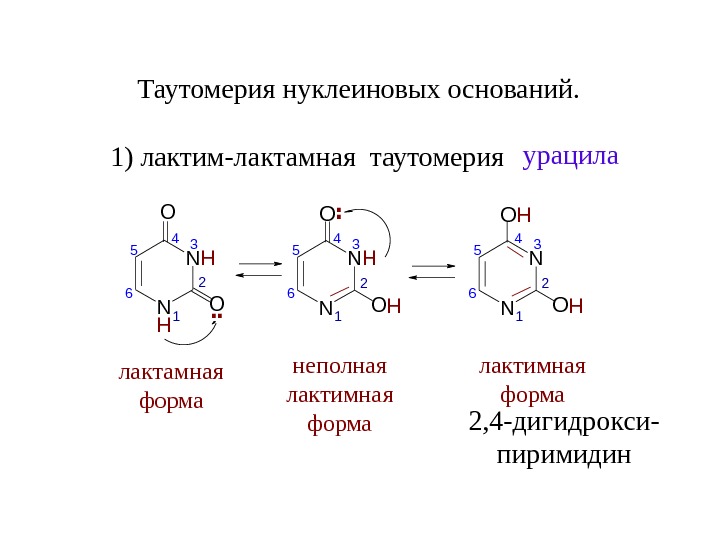
 Таутомерия нуклеиновых оснований. 1) лактим-лактамная таутомерия. N N O O 1 2 34 5 6 H H. . лактамная форма N NO O 1 234 5 6 H H. . неполная лактимная форма N NO O 1 234 5 6 H H лактимная форма 2, 4 -дигидрокси- пиримидин урацила
Таутомерия нуклеиновых оснований. 1) лактим-лактамная таутомерия. N N O O 1 2 34 5 6 H H. . лактамная форма N NO O 1 234 5 6 H H. . неполная лактимная форма N NO O 1 234 5 6 H H лактимная форма 2, 4 -дигидрокси- пиримидин урацила
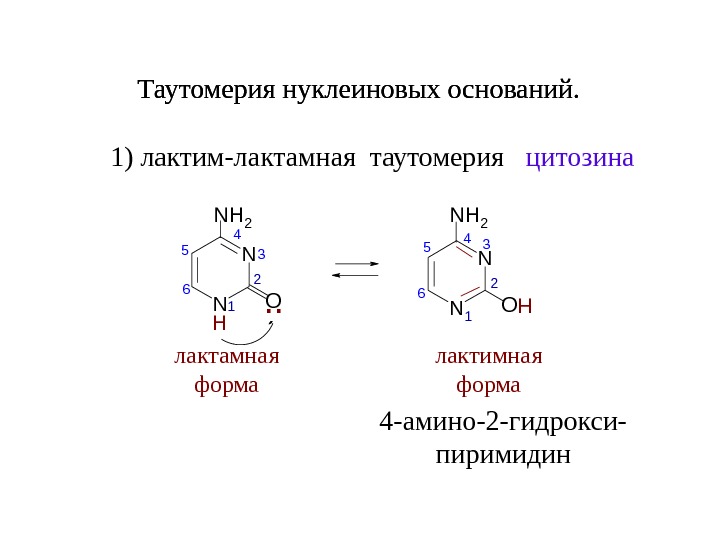
 N N ONH 2 65 4 3 2 1 H. . Таутомерия нуклеиновых оснований. цитозина N NNH 2 O 1 234 5 6 H лактамная форма лактимная форма 4 -амино-2 -гидрокси- пиримидин. Таутомерия нуклеиновых оснований. 1) лактим-лактамная таутомерия
N N ONH 2 65 4 3 2 1 H. . Таутомерия нуклеиновых оснований. цитозина N NNH 2 O 1 234 5 6 H лактамная форма лактимная форма 4 -амино-2 -гидрокси- пиримидин. Таутомерия нуклеиновых оснований. 1) лактим-лактамная таутомерия
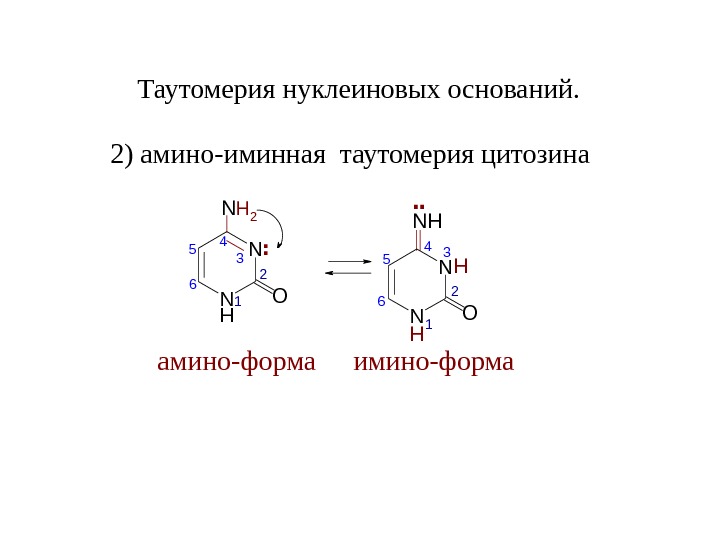
 N H N O N 6 54 3 2 1. . H 2 Таутомерия нуклеиновых оснований. 2) амино-иминная таутомерия цитозина амино-форма N N NH O 1 2 34 5 6 H H. . имино-форма
N H N O N 6 54 3 2 1. . H 2 Таутомерия нуклеиновых оснований. 2) амино-иминная таутомерия цитозина амино-форма N N NH O 1 2 34 5 6 H H. . имино-форма
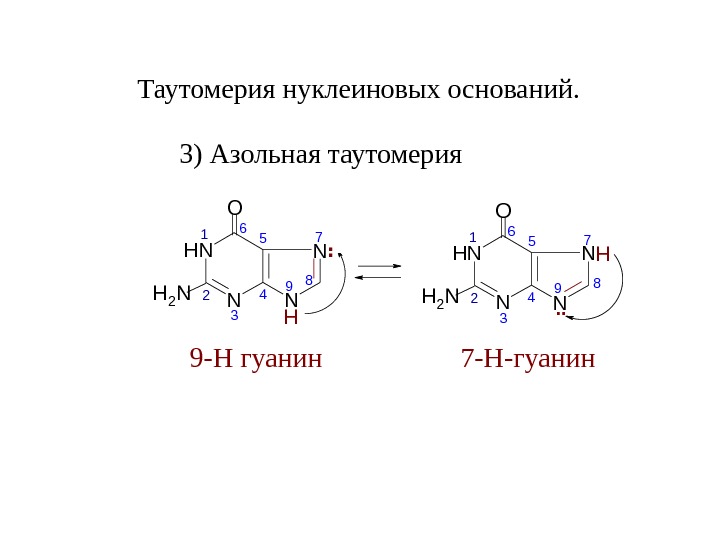
 Таутомерия нуклеиновых оснований. 3) Азольная таутомерия N N NH N O H 2 N 56 4 3 2 17 89. . H 9 -Н гуанин N NNH N O H 2 N 56 4 321 7 8 9 H. . 7 -Н-гуанин
Таутомерия нуклеиновых оснований. 3) Азольная таутомерия N N NH N O H 2 N 56 4 3 2 17 89. . H 9 -Н гуанин N NNH N O H 2 N 56 4 321 7 8 9 H. . 7 -Н-гуанин
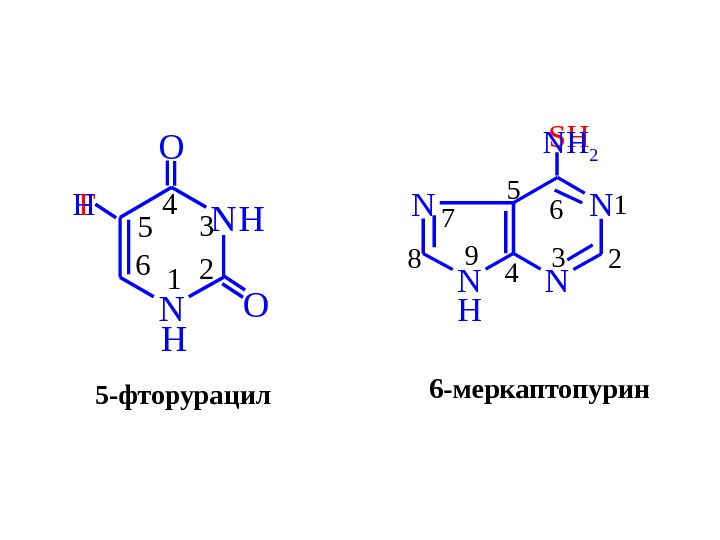
 N NH H O O 12 3 4 5 6 F 5 -фторурацил. H H N NN N 23 4 5 61 7 89 SH 6 -меркаптопурин NH
N NH H O O 12 3 4 5 6 F 5 -фторурацил. H H N NN N 23 4 5 61 7 89 SH 6 -меркаптопурин NH
 Нуклеозиды – это N- гликозиды, образованные нуклеиновыми основаниями и пентозой (рибозой или дезоксирибозой). Классификация нуклеозидов (в зависимости от природы углеводного остатка): рибонуклеозиды дезоксирибонуклеозиды (в РНК) (в ДНК)
Нуклеозиды – это N- гликозиды, образованные нуклеиновыми основаниями и пентозой (рибозой или дезоксирибозой). Классификация нуклеозидов (в зависимости от природы углеводного остатка): рибонуклеозиды дезоксирибонуклеозиды (в РНК) (в ДНК)
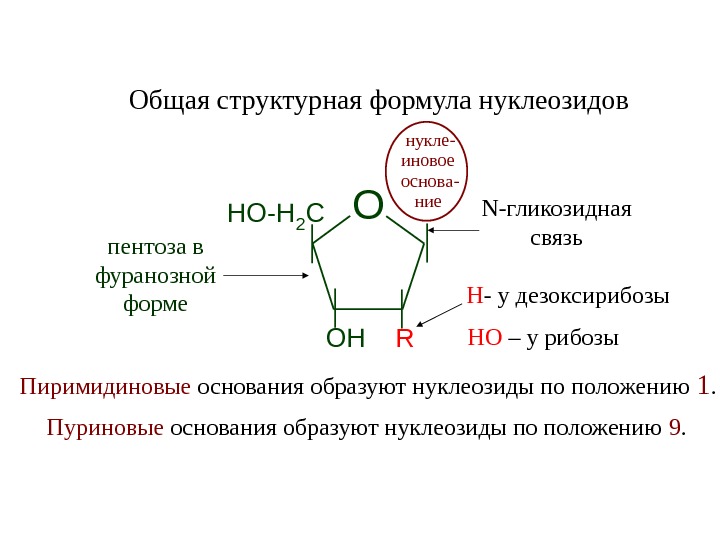
 O OHHO-H 2 C RОбщая структурная формула нуклеозидов пентоза в фуранозной форме N- гликозидная связь Н — у дезоксирибозы Пиримидиновые основания образуют нуклеозиды по положению 1. Пуриновые основания образуют нуклеозиды по положению 9. НО – у рибозы нукле- иновое основа- ние
O OHHO-H 2 C RОбщая структурная формула нуклеозидов пентоза в фуранозной форме N- гликозидная связь Н — у дезоксирибозы Пиримидиновые основания образуют нуклеозиды по положению 1. Пуриновые основания образуют нуклеозиды по положению 9. НО – у рибозы нукле- иновое основа- ние
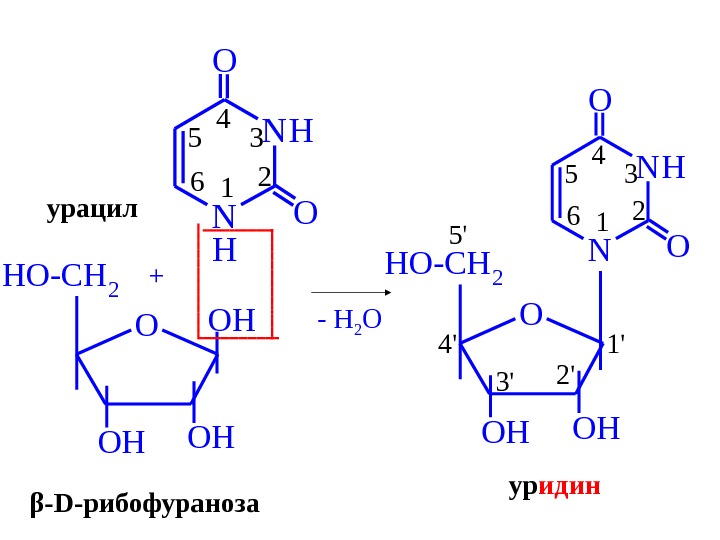
 1 2 3 4 5 6 N NH H O Oурацил O OH OH OH HO-CH 2 + β — D -рибофураноза — H 2 O 1 2 3 4 5 6 N NH O OHOH HO-CH 2 1′ 2’3′ 4′ 5′ ур идин
1 2 3 4 5 6 N NH H O Oурацил O OH OH OH HO-CH 2 + β — D -рибофураноза — H 2 O 1 2 3 4 5 6 N NH O OHOH HO-CH 2 1′ 2’3′ 4′ 5′ ур идин
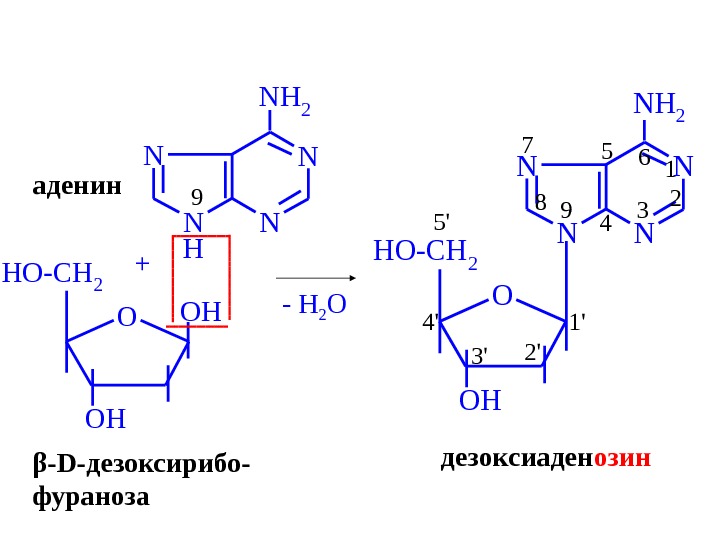
 H N NN N NH 2 9 OOH OH HO-CH 2+аденин β — D -дезоксирибо- фураноза — H 2 O N NN N NH 2 O OH HO-CH 2 1′ 2′ 3’4′ 5′ 2 3 4 5 6 17 8 9 дезоксиаден озин
H N NN N NH 2 9 OOH OH HO-CH 2+аденин β — D -дезоксирибо- фураноза — H 2 O N NN N NH 2 O OH HO-CH 2 1′ 2′ 3’4′ 5′ 2 3 4 5 6 17 8 9 дезоксиаден озин
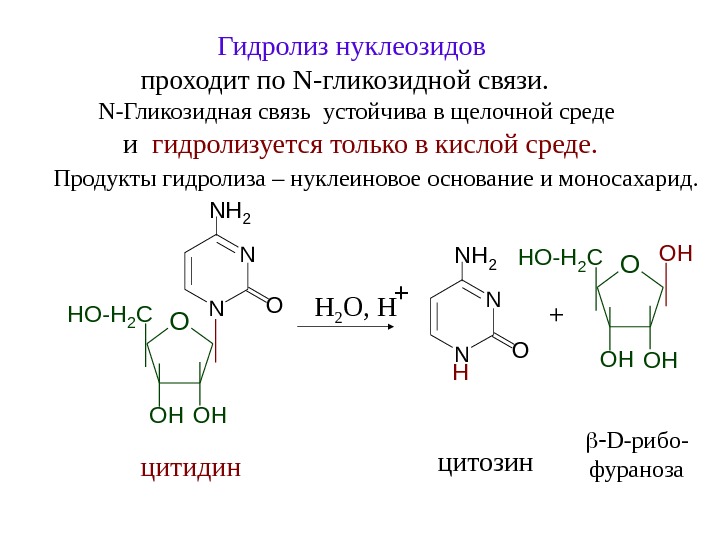
 Гидролиз нуклеозидов проходит по N- гликозидной связи. N- Гликозидная связь устойчива в щелочной среде и гидролизуется только в кислой среде. Продукты гидролиза – нуклеиновое основание и моносахарид. цитидин. N N O NH 2 O OHHO-H 2 C OH D- рибо- фураноза. N N ONH 2 H O OH HO-H 2 COH OH цитозин. H 2 O, H + +
Гидролиз нуклеозидов проходит по N- гликозидной связи. N- Гликозидная связь устойчива в щелочной среде и гидролизуется только в кислой среде. Продукты гидролиза – нуклеиновое основание и моносахарид. цитидин. N N O NH 2 O OHHO-H 2 C OH D- рибо- фураноза. N N ONH 2 H O OH HO-H 2 COH OH цитозин. H 2 O, H + +
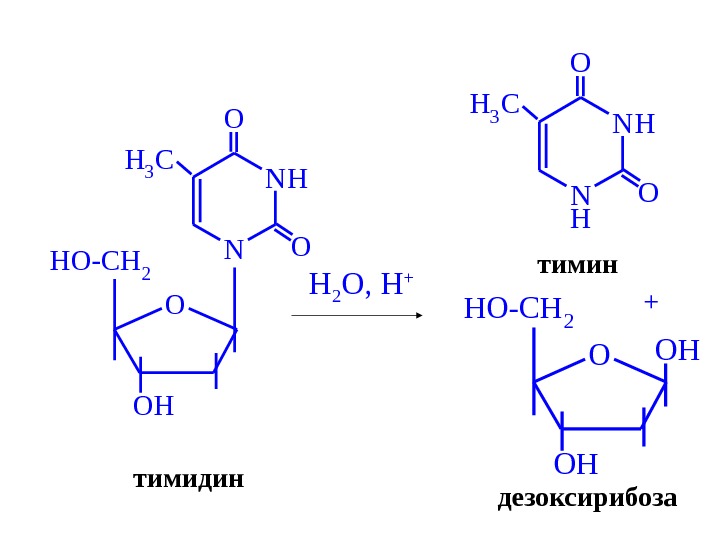
 N NH O OH HO-CH 2 H 3 Cтимидин H 2 O, H + H N N HO OH 3 C тимин OHO OH HO-CH 2 дезоксирибоза +
N NH O OH HO-CH 2 H 3 Cтимидин H 2 O, H + H N N HO OH 3 C тимин OHO OH HO-CH 2 дезоксирибоза +
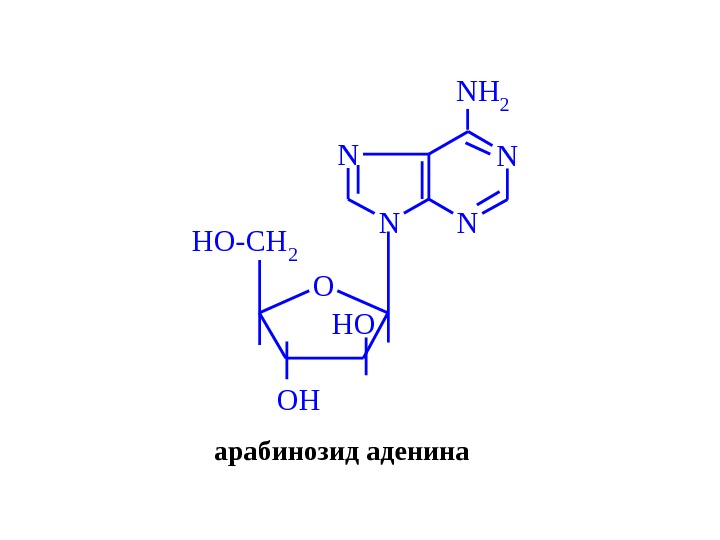
 N NN N NH 2 O OH HO-CH 2 HOарабинозид аденина
N NN N NH 2 O OH HO-CH 2 HOарабинозид аденина
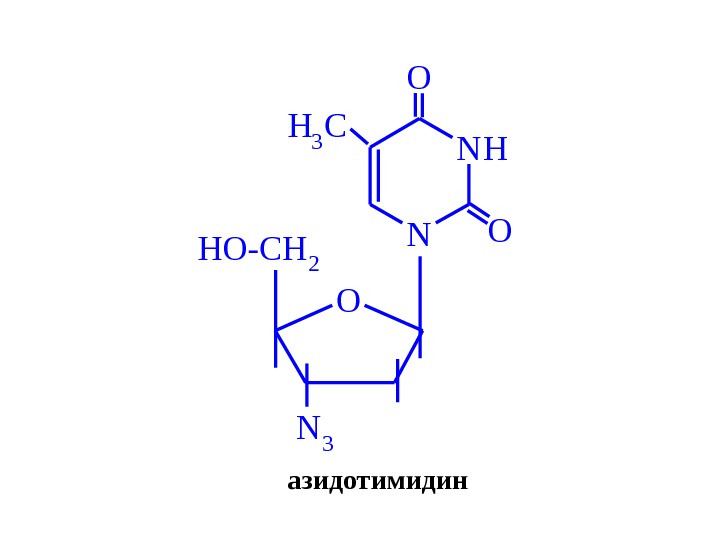
 N NH O O O HO-CH 2 H 3 C N 3 азидотимидин
N NH O O O HO-CH 2 H 3 C N 3 азидотимидин
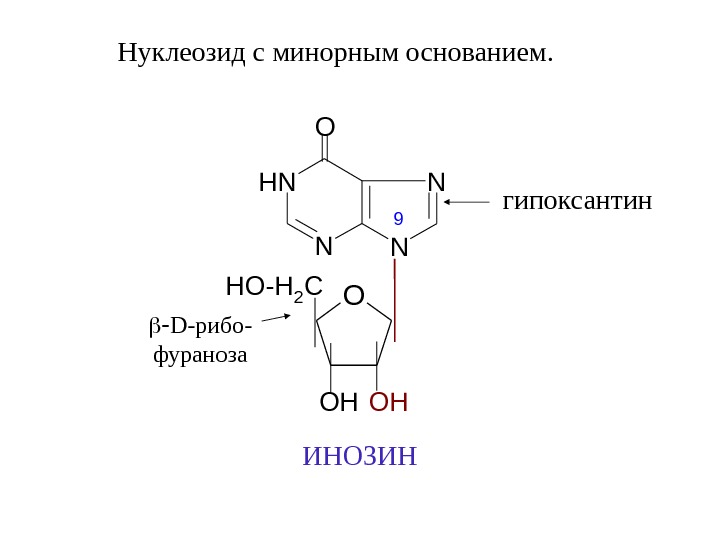
 Нуклеозид с минорным основанием. O OH HO-H 2 C OH D- рибо- фураноза N N NH N O 9 гипоксантин ИНОЗИН
Нуклеозид с минорным основанием. O OH HO-H 2 C OH D- рибо- фураноза N N NH N O 9 гипоксантин ИНОЗИН
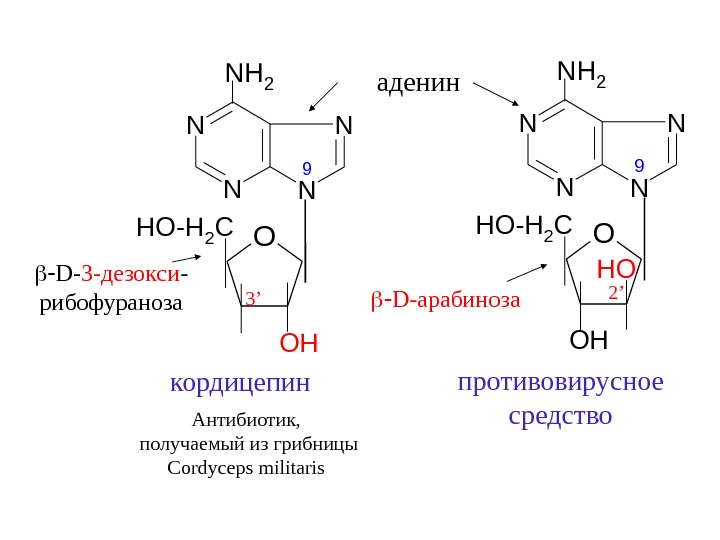
 OHO-H 2 C OH D- 3 -дезокси — рибофураноза O OH HO-H 2 C HO D- арабиноза N N N N NH 2 9 кордицепин Антибиотик, получаемый из грибницы Cordyceps militaris противовирусное средствоаденин 3 ’ 2’
OHO-H 2 C OH D- 3 -дезокси — рибофураноза O OH HO-H 2 C HO D- арабиноза N N N N NH 2 9 кордицепин Антибиотик, получаемый из грибницы Cordyceps militaris противовирусное средствоаденин 3 ’ 2’
 Нуклеотиды – сложные эфиры нуклеозидов и фосфорной кислоты (фосфаты нуклеозидов)
Нуклеотиды – сложные эфиры нуклеозидов и фосфорной кислоты (фосфаты нуклеозидов)
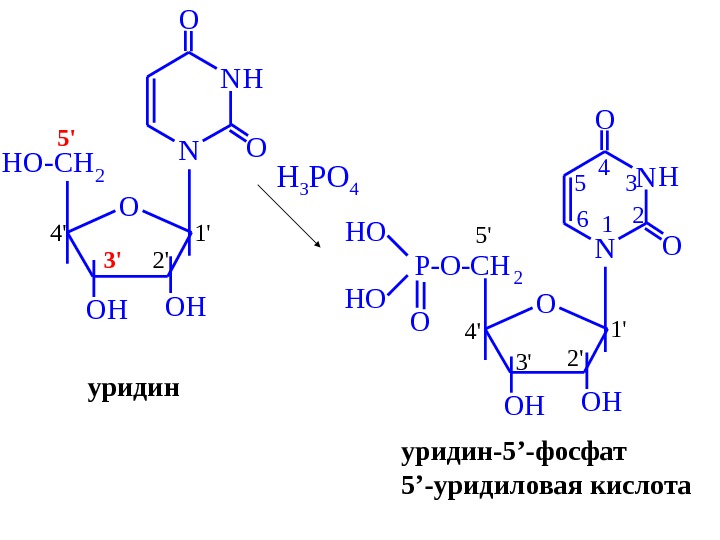
 H 3 PO 4 P-O-CH 2 HO O HO 12 3 4 5 6 N N O OHOH 1′ 2’3′ 4′ 5′ H уридин-5 ’ -фосфат 5 ’ -уридиловая кислота. N N HO O O OH OHHO-CH 2 1′ 2’3′ 4′ 5′
H 3 PO 4 P-O-CH 2 HO O HO 12 3 4 5 6 N N O OHOH 1′ 2’3′ 4′ 5′ H уридин-5 ’ -фосфат 5 ’ -уридиловая кислота. N N HO O O OH OHHO-CH 2 1′ 2’3′ 4′ 5′
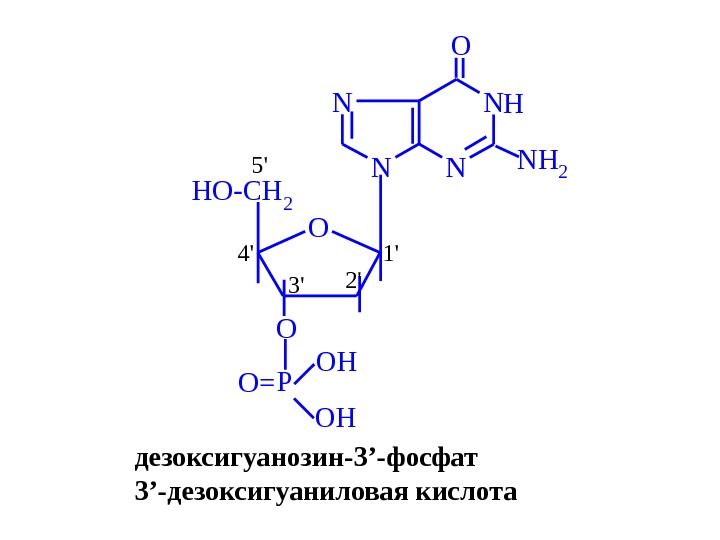
 N NN N NH 2 O O 1′ 2′ 3’4′ 5′ HO-CH 2 OH O= OH P O H дезоксигуанозин-3 ’ -фосфат 3 ’ -дезоксигуаниловая кислота
N NN N NH 2 O O 1′ 2′ 3’4′ 5′ HO-CH 2 OH O= OH P O H дезоксигуанозин-3 ’ -фосфат 3 ’ -дезоксигуаниловая кислота
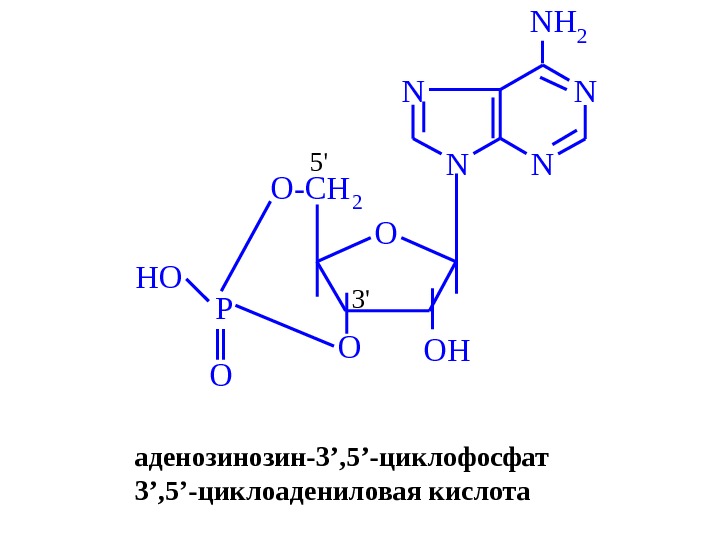
 N NN N NH 2 O OHO 3′ 5′ O-CH 2 HO O Pаденозин-3 ’ , 5 ’ -циклофосфат 3 ’ , 5 ’ -циклоадениловая кислота
N NN N NH 2 O OHO 3′ 5′ O-CH 2 HO O Pаденозин-3 ’ , 5 ’ -циклофосфат 3 ’ , 5 ’ -циклоадениловая кислота
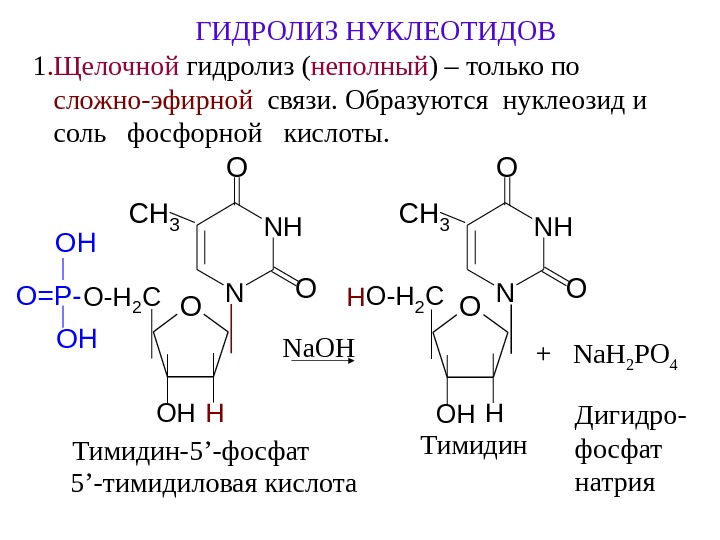
 ГИДРОЛИЗ НУКЛЕОТИДОВ 1. Щелочной гидролиз ( неполный ) – только по сложно-эфирной связи. Образуются нуклеозид и соль фосфорной кислоты. O OH O-H 2 C H Тимидин-5 ’ -фосфат N NH O O CH 3 OH OH O=P- 5 ’- тимидиловая кислота Na. OH O OH O-H 2 C H H N NH O O CH 3 Тимидин Na. H 2 PO 4 Дигидро- фосфат натрия+
ГИДРОЛИЗ НУКЛЕОТИДОВ 1. Щелочной гидролиз ( неполный ) – только по сложно-эфирной связи. Образуются нуклеозид и соль фосфорной кислоты. O OH O-H 2 C H Тимидин-5 ’ -фосфат N NH O O CH 3 OH OH O=P- 5 ’- тимидиловая кислота Na. OH O OH O-H 2 C H H N NH O O CH 3 Тимидин Na. H 2 PO 4 Дигидро- фосфат натрия+
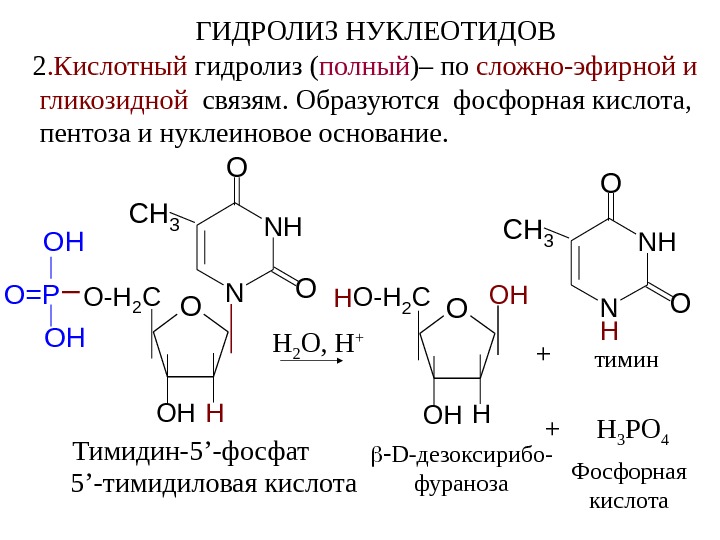
 ГИДРОЛИЗ НУКЛЕОТИДОВ 2. Кислотный гидролиз ( полный )– по сложно-эфирной и гликозидной связям. Образуются фосфорная кислота, пентоза и нуклеиновое основание. O OH O-H 2 C H Тимидин-5 ’ -фосфат N NH O O CH 3 OH OH O=P 5 ’- тимидиловая кислота O OH O-H 2 C H H OH N NH O O CH 3 H H 3 PO 4+H 2 O, H + D- дезоксирибо- фураноза Фосфорная кислота тимин +
ГИДРОЛИЗ НУКЛЕОТИДОВ 2. Кислотный гидролиз ( полный )– по сложно-эфирной и гликозидной связям. Образуются фосфорная кислота, пентоза и нуклеиновое основание. O OH O-H 2 C H Тимидин-5 ’ -фосфат N NH O O CH 3 OH OH O=P 5 ’- тимидиловая кислота O OH O-H 2 C H H OH N NH O O CH 3 H H 3 PO 4+H 2 O, H + D- дезоксирибо- фураноза Фосфорная кислота тимин +
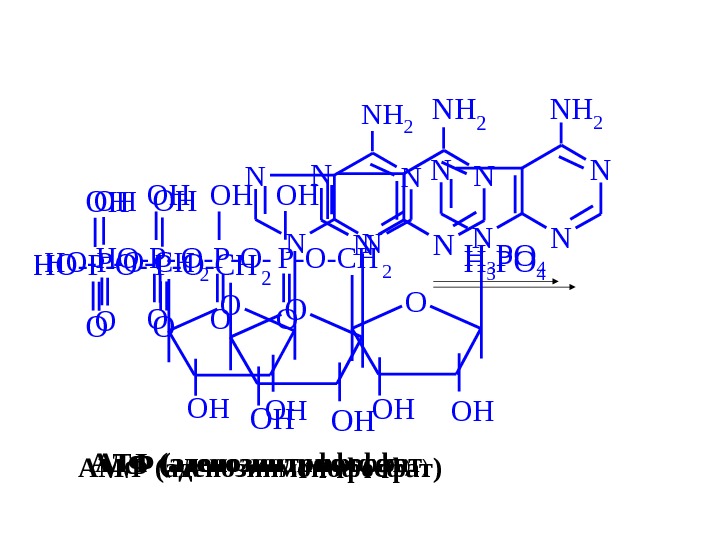
 N NN N NH 2 O OHOH HO-P-O-CH 2 O OH H 3 PO 4 АМФ (аденозинмонофосфат) N NNH 2 O OHOH P-O-CH 2 OOH HO-P-O- OH O АДФ (аденозиндифосфат ) H 3 PO 4 N NN N NH 2 O OHOH P-O-CH 2 O OH O-P-O- OH O HO-P- O OH АТФ (аденозинтрифосфат )
N NN N NH 2 O OHOH HO-P-O-CH 2 O OH H 3 PO 4 АМФ (аденозинмонофосфат) N NNH 2 O OHOH P-O-CH 2 OOH HO-P-O- OH O АДФ (аденозиндифосфат ) H 3 PO 4 N NN N NH 2 O OHOH P-O-CH 2 O OH O-P-O- OH O HO-P- O OH АТФ (аденозинтрифосфат )
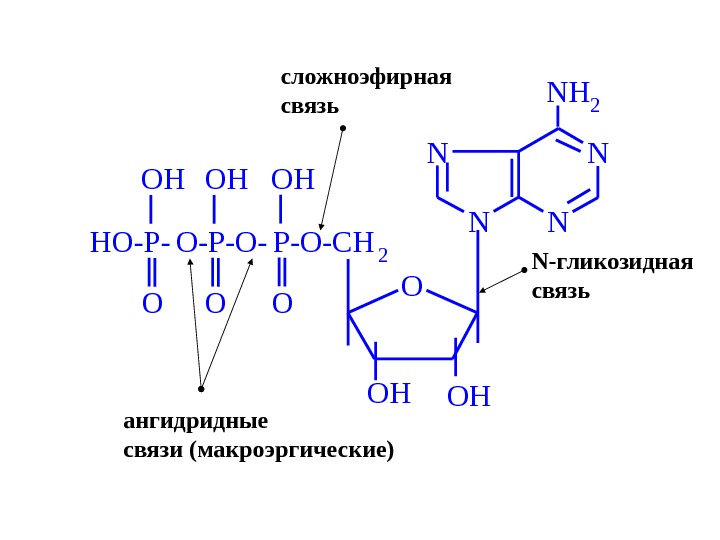
 N NN N NH 2 O OHOH P-O-CH 2 O OH O-P-O- OH O HO-P- O OH N -гликозидная связьсложноэфирная связь ангидридные связи (макроэргические)
N NN N NH 2 O OHOH P-O-CH 2 O OH O-P-O- OH O HO-P- O OH N -гликозидная связьсложноэфирная связь ангидридные связи (макроэргические)
 Биологическая роль АТФ 1. Участвует в реакциях фосфорелирования как источник фосфатных групп. 2. Источник энергии для биохимических процессов. 3. Активация аминокислот при биосинтезе белка.
Биологическая роль АТФ 1. Участвует в реакциях фосфорелирования как источник фосфатных групп. 2. Источник энергии для биохимических процессов. 3. Активация аминокислот при биосинтезе белка.
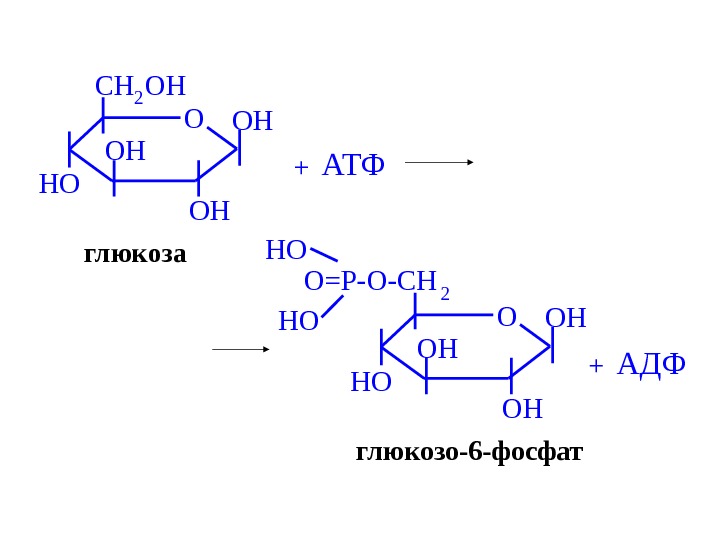
 OOH OH OH HO CH 2 OHглюкоза + АТФ OOH OH OH HO O=P-O-CH 2 HO HO глюкозо-6 -фосфат + АДФ
OOH OH OH HO CH 2 OHглюкоза + АТФ OOH OH OH HO O=P-O-CH 2 HO HO глюкозо-6 -фосфат + АДФ
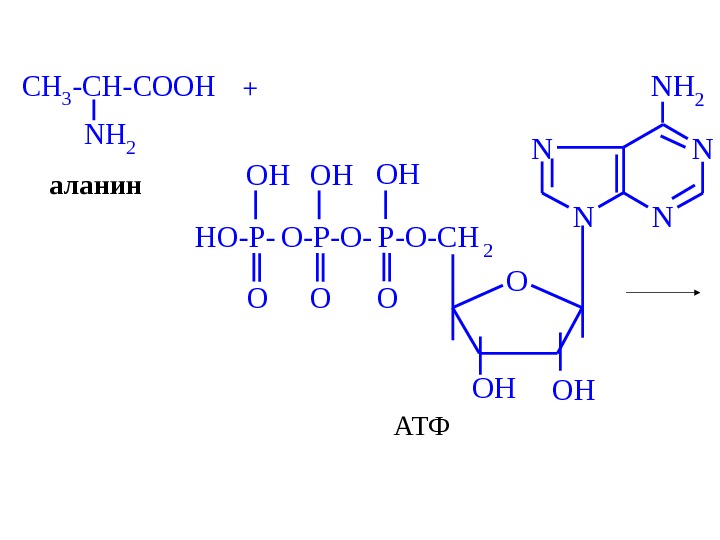
 CH 3 -CH-COOH NH 2 N NN N O OHOH P-O-CH 2 O OH O-P-O- OH O HO-P- O OH NH 2+ аланин АТФ
CH 3 -CH-COOH NH 2 N NN N O OHOH P-O-CH 2 O OH O-P-O- OH O HO-P- O OH NH 2+ аланин АТФ
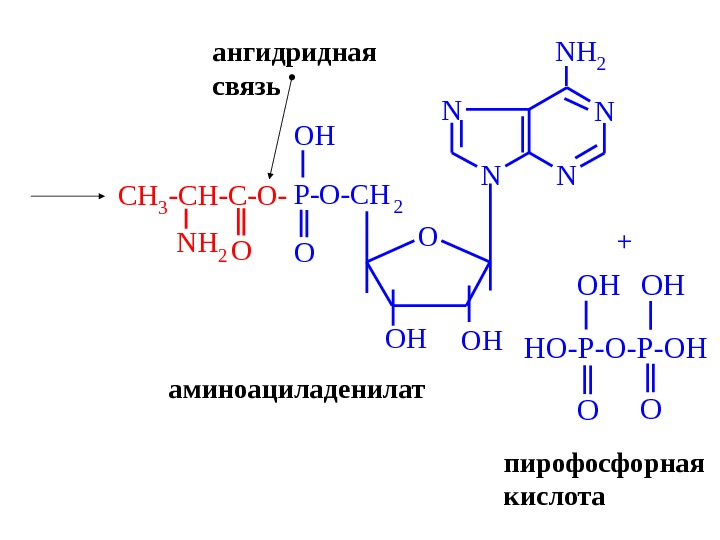
 N NN N O OHOH O OH NH 2 P-O-CH 2 CH 3 -CH-C-O- ONH 2 + HO-P-OH OO OHOH пирофосфорная кислотааминоациладенилат ангидридная связь
N NN N O OHOH O OH NH 2 P-O-CH 2 CH 3 -CH-C-O- ONH 2 + HO-P-OH OO OHOH пирофосфорная кислотааминоациладенилат ангидридная связь
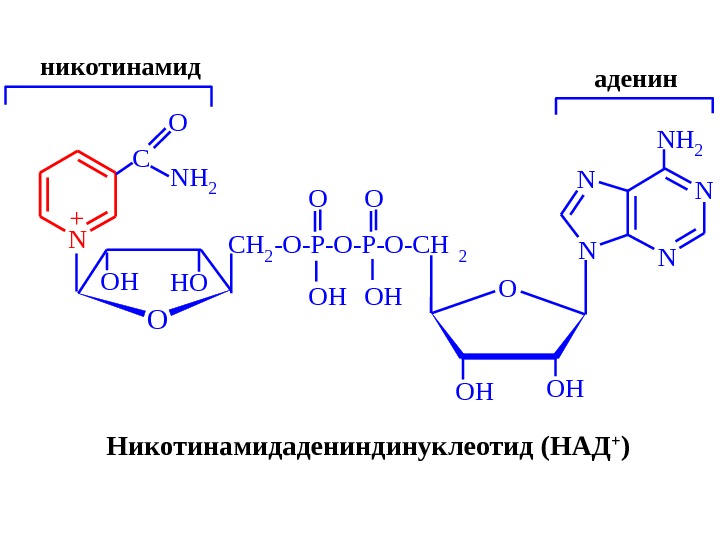
 ON C O NH 2 HOOH CH 2 -O-P-O-CH 2 OO OOHOH N N NH 2 + никотинамид аденин Никотинамидадениндинуклеотид (НАД + )
ON C O NH 2 HOOH CH 2 -O-P-O-CH 2 OO OOHOH N N NH 2 + никотинамид аденин Никотинамидадениндинуклеотид (НАД + )
 Первичная структура нуклеиновой кислоты- это последовательность нуклеотидных звеньев, связанных ковалентными связями в непрерывную цепочку полинуклеотида. Её определяют две характеристики : 1. Нуклеотидный состав — набор и соотношение нуклеотидов. 2. Нуклеотидная последовательность — порядок чередования нуклеотидных звеньев. Нуклеиновые кислоты – высокомолекулярные полимеры, мономерами которых являются нуклеотиды.
Первичная структура нуклеиновой кислоты- это последовательность нуклеотидных звеньев, связанных ковалентными связями в непрерывную цепочку полинуклеотида. Её определяют две характеристики : 1. Нуклеотидный состав — набор и соотношение нуклеотидов. 2. Нуклеотидная последовательность — порядок чередования нуклеотидных звеньев. Нуклеиновые кислоты – высокомолекулярные полимеры, мономерами которых являются нуклеотиды.
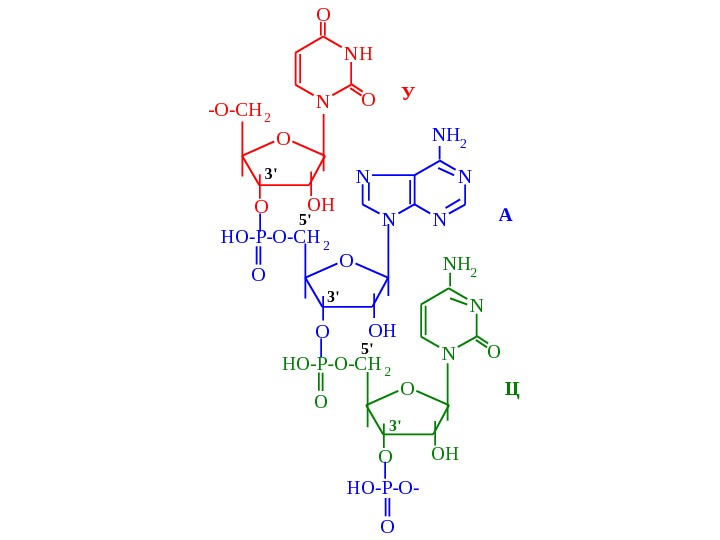
 N NH O OHO -O-CH 2 N NN N NH 2 O OH HO-P-O-CH 2 O N N O NH 2 O OHO O HO-P-O-CH 2 O HO-P-O- O У A Ц 3′ 5′ 5′ 3′ 3′
N NH O OHO -O-CH 2 N NN N NH 2 O OH HO-P-O-CH 2 O N N O NH 2 O OHO O HO-P-O-CH 2 O HO-P-O- O У A Ц 3′ 5′ 5′ 3′ 3′
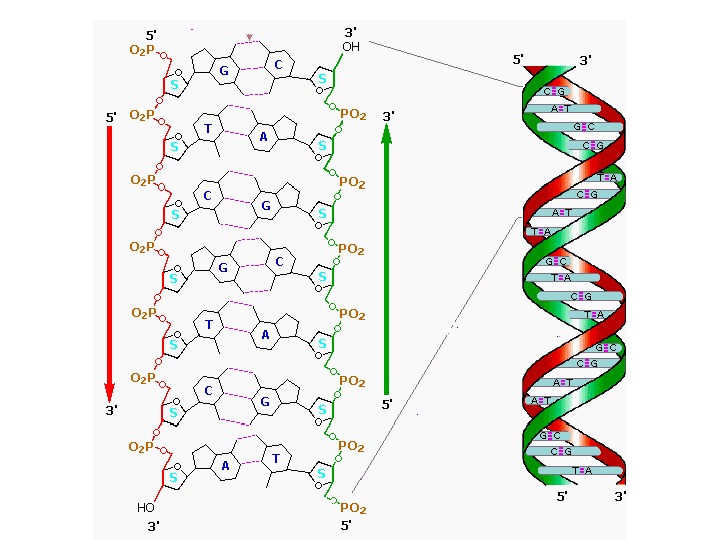
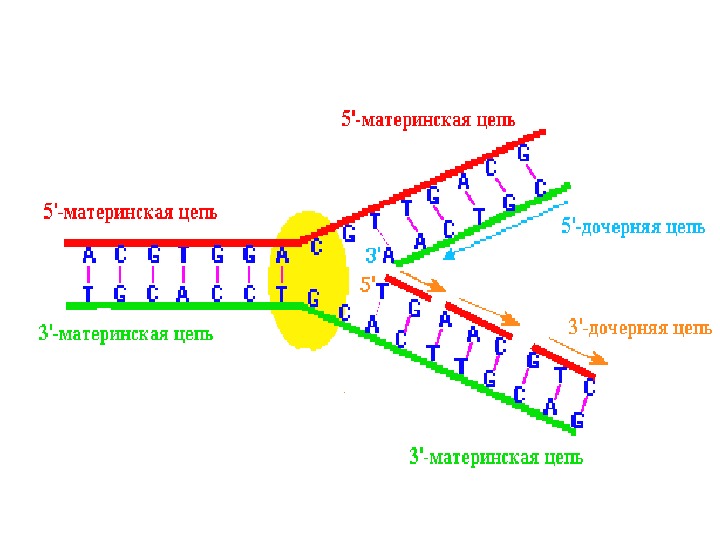
 Вторичная структура нуклеиновых кислот – пространственная организация полинуклеотидных цепей, т. е. определенное расположение полинуклеотидной цепи в пространстве
Вторичная структура нуклеиновых кислот – пространственная организация полинуклеотидных цепей, т. е. определенное расположение полинуклеотидной цепи в пространстве

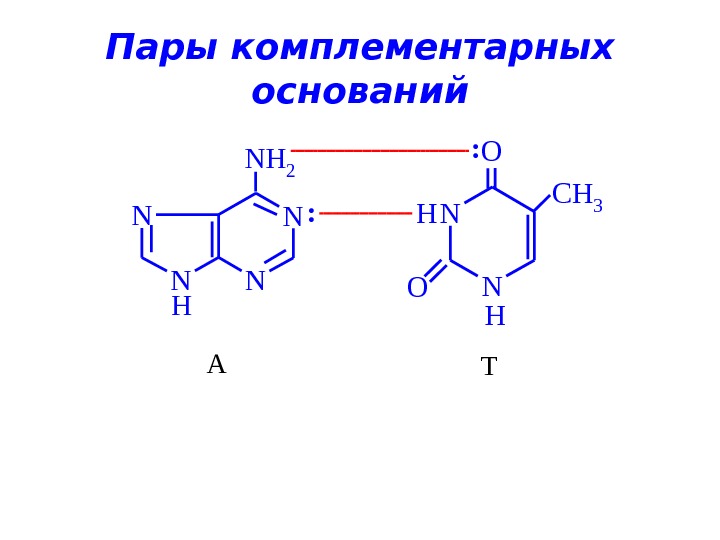
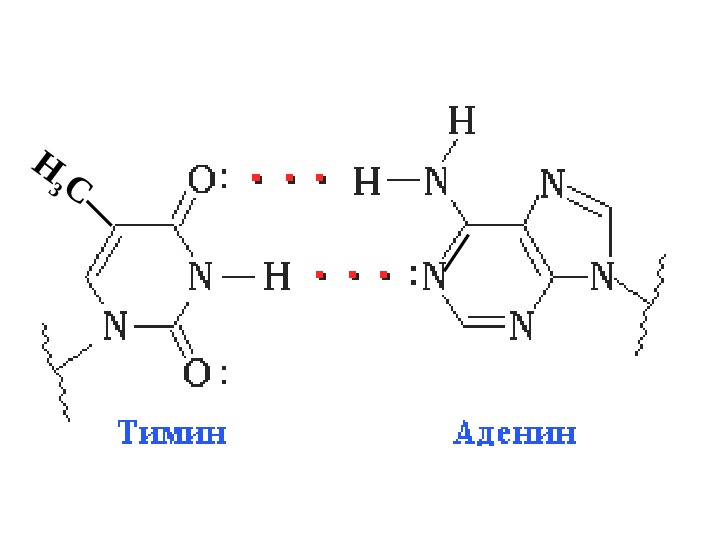
 H N NN N NH 2 : H H O O CH 3 N N : А ТПары комплементарных оснований
H N NN N NH 2 : H H O O CH 3 N N : А ТПары комплементарных оснований
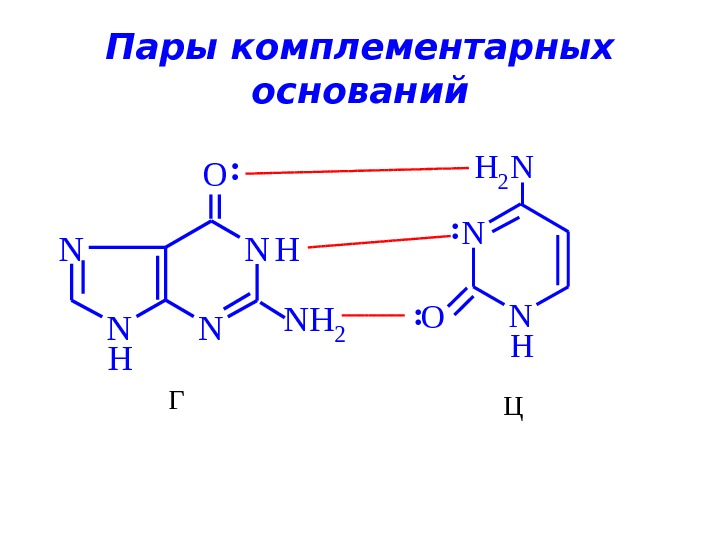
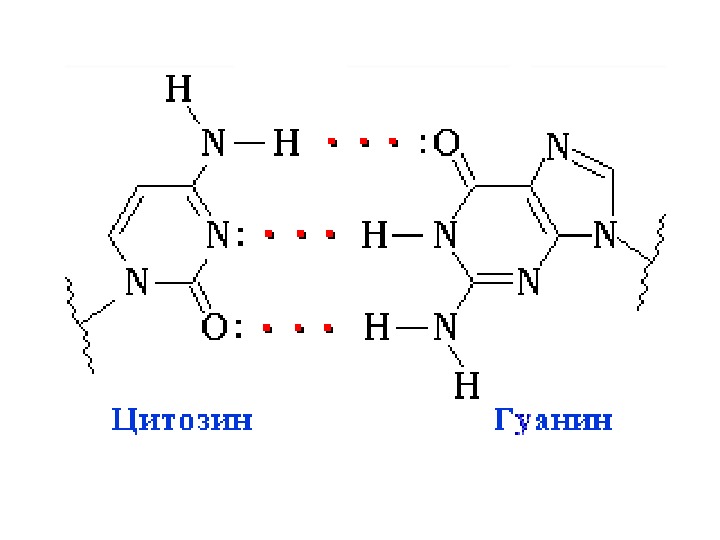
 Пары комплементарных оснований O HN N NH 2 H: H O H 2 N N N : : Г Ц
Пары комплементарных оснований O HN N NH 2 H: H O H 2 N N N : : Г Ц
 H
H

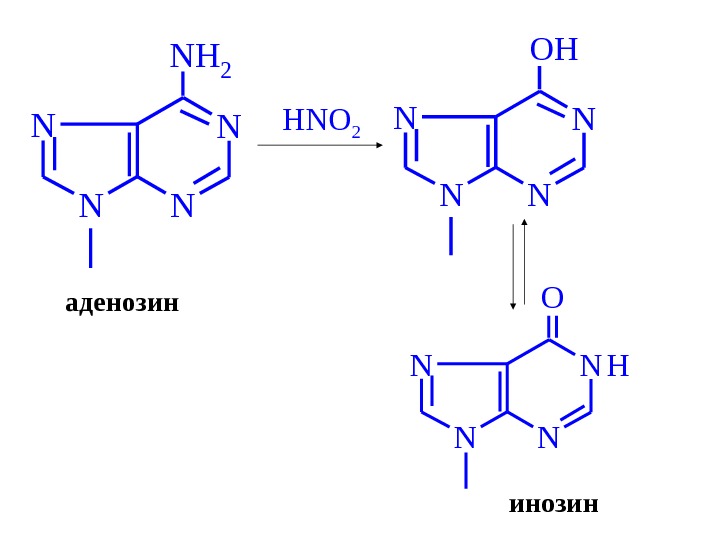
 N NN N NH 2 HNO 2 N NN N OH O N NN NH аденозин инозин
N NN N NH 2 HNO 2 N NN N OH O N NN NH аденозин инозин


