Тема_10_Нуклеиновые_кислоты.ppt
- Количество слайдов: 47
 Нуклеиновые кислоты
Нуклеиновые кислоты
 Нуклеиновые кислоты … l l l важнейшие биополимеры, осуществляющие хранение и передачу генетической информации в живой клетке 2 типа – дезоксирибонуклеиновые кислоты (ДНК) и рибонуклеиновые кислоты (РНК) ДНК – генетический материал большинства организмов В прокариотических клетках, кроме основной хромосомной ДНК, часто встречаются внехромосомные ДНК – плазмиды В эукариотических клетках основная масса ДНК – в клеточном ядре, где связана с белками в хромосомах Эукариотические клетки содержат ДНК также в различных органеллах (митохондриях, хлоропластах)
Нуклеиновые кислоты … l l l важнейшие биополимеры, осуществляющие хранение и передачу генетической информации в живой клетке 2 типа – дезоксирибонуклеиновые кислоты (ДНК) и рибонуклеиновые кислоты (РНК) ДНК – генетический материал большинства организмов В прокариотических клетках, кроме основной хромосомной ДНК, часто встречаются внехромосомные ДНК – плазмиды В эукариотических клетках основная масса ДНК – в клеточном ядре, где связана с белками в хромосомах Эукариотические клетки содержат ДНК также в различных органеллах (митохондриях, хлоропластах)
 Нуклеиновые кислоты … l l РНК В клетках имеются l l l матричные (информационные) РНК (м. РНК или и. РНК) рибосомные РНК (р. РНК) транспортные РНК (т. РНК) и ряд других РНК входят в состав многих вирусов
Нуклеиновые кислоты … l l РНК В клетках имеются l l l матричные (информационные) РНК (м. РНК или и. РНК) рибосомные РНК (р. РНК) транспортные РНК (т. РНК) и ряд других РНК входят в состав многих вирусов
 Выделение нуклеиновых кислот
Выделение нуклеиновых кислот
 l l Нуклеиновые кислоты – составная часть сложных белков – нуклеопротеидов Они обладают сильно выраженными кислыми свойствами (за счет остатков фосфорной кислоты) и при физиологических значениях р. Н имеют отрицательный заряд, поэтому взаимодействуют по типу ионной связи: l l с основными белками (гистонами) ионами металлов (Mg 2+) полиаминами (спермин, спермидин – участвуют в регуляции биосинтеза полимеров) диаминами (путресцин, образующийся из орн)
l l Нуклеиновые кислоты – составная часть сложных белков – нуклеопротеидов Они обладают сильно выраженными кислыми свойствами (за счет остатков фосфорной кислоты) и при физиологических значениях р. Н имеют отрицательный заряд, поэтому взаимодействуют по типу ионной связи: l l с основными белками (гистонами) ионами металлов (Mg 2+) полиаминами (спермин, спермидин – участвуют в регуляции биосинтеза полимеров) диаминами (путресцин, образующийся из орн)
 l l В связи с этим для выделения нуклеиновых кислот необходимо прежде всего разрушить эти сильные и многочисленные электростатические связи Для этого гомогенизированный биоматериал обрабатывают крепкими солевыми растворами (10%-ный Na. Cl) с последующим осаждением нуклеиновых кислот этиловым спиртом
l l В связи с этим для выделения нуклеиновых кислот необходимо прежде всего разрушить эти сильные и многочисленные электростатические связи Для этого гомогенизированный биоматериал обрабатывают крепкими солевыми растворами (10%-ный Na. Cl) с последующим осаждением нуклеиновых кислот этиловым спиртом
 l l l Фенольный метод (более мягкий) Гомогенат заливают водонасыщенным фенолом, встряхивают в течение 1 ч и центрифугируют В пробирке образуются 4 различных по консистенции слоя: l l верхний (водный) вязкий слой белого цвета (в этих двух слоях – основная масса нуклеиновых кислот) желеобразный прозрачный слой (желтоватый) – фенол с белками коричневый слой – остатки ткани и денатурированный белок
l l l Фенольный метод (более мягкий) Гомогенат заливают водонасыщенным фенолом, встряхивают в течение 1 ч и центрифугируют В пробирке образуются 4 различных по консистенции слоя: l l верхний (водный) вязкий слой белого цвета (в этих двух слоях – основная масса нуклеиновых кислот) желеобразный прозрачный слой (желтоватый) – фенол с белками коричневый слой – остатки ткани и денатурированный белок
 l l Можно обрабатывать солевой экстракт двойным объемом хлороформа, содержащего немного изоамилового спирта, затем перемешать до образования стойкой эмульсии и центрифугировать (верхний водный слой содержит нуклеиновые кислоты) Полученные препараты фракционируют путем l l хроматографии гель-фильтрации электрофореза и др. затем подвергают гидролизу для изучения химического состава (ферментативные, химические методы)
l l Можно обрабатывать солевой экстракт двойным объемом хлороформа, содержащего немного изоамилового спирта, затем перемешать до образования стойкой эмульсии и центрифугировать (верхний водный слой содержит нуклеиновые кислоты) Полученные препараты фракционируют путем l l хроматографии гель-фильтрации электрофореза и др. затем подвергают гидролизу для изучения химического состава (ферментативные, химические методы)
 Химический состав нуклеиновых кислот
Химический состав нуклеиновых кислот
 l При полном гидролизе нуклеиновых кислот в присутствии хлорной кислоты при нагревании образуются l l l пуриновые и пиримидиновые основания углеводы (рибоза и дезоксирибоза) фосфорная кислота
l При полном гидролизе нуклеиновых кислот в присутствии хлорной кислоты при нагревании образуются l l l пуриновые и пиримидиновые основания углеводы (рибоза и дезоксирибоза) фосфорная кислота
 Пиримидиновые основания l l l Производные пиримидина Сопряжение -электронов Бесцветное кристаллическое вещество, относящееся к классу диазинов Тпл 22 С, Ткип 124 С Хорошо растворим в воде Не дает щелочной реакции, но образует соли с сильными кислотами
Пиримидиновые основания l l l Производные пиримидина Сопряжение -электронов Бесцветное кристаллическое вещество, относящееся к классу диазинов Тпл 22 С, Ткип 124 С Хорошо растворим в воде Не дает щелочной реакции, но образует соли с сильными кислотами
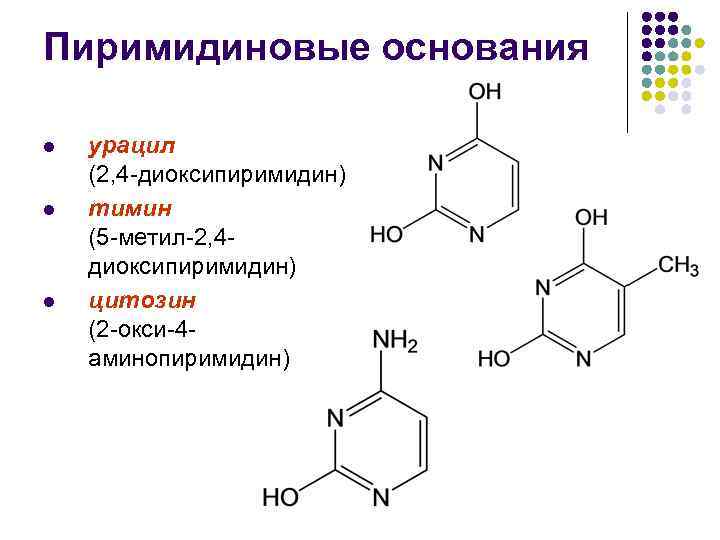 Пиримидиновые основания l l l урацил (2, 4 -диоксипиримидин) тимин (5 -метил-2, 4 диоксипиримидин) цитозин (2 -окси-4 аминопиримидин)
Пиримидиновые основания l l l урацил (2, 4 -диоксипиримидин) тимин (5 -метил-2, 4 диоксипиримидин) цитозин (2 -окси-4 аминопиримидин)
 Пиримидиновые основания l l l Урацил входит в состав только РНК Тимин – в основном в ДНК и очень редко – в некоторые РНК Тимин и урацил имеют окисленный атом углерода в положении 4 В цитозине этот атом аминирован Все производные пиримидина имеют плоское строение
Пиримидиновые основания l l l Урацил входит в состав только РНК Тимин – в основном в ДНК и очень редко – в некоторые РНК Тимин и урацил имеют окисленный атом углерода в положении 4 В цитозине этот атом аминирован Все производные пиримидина имеют плоское строение
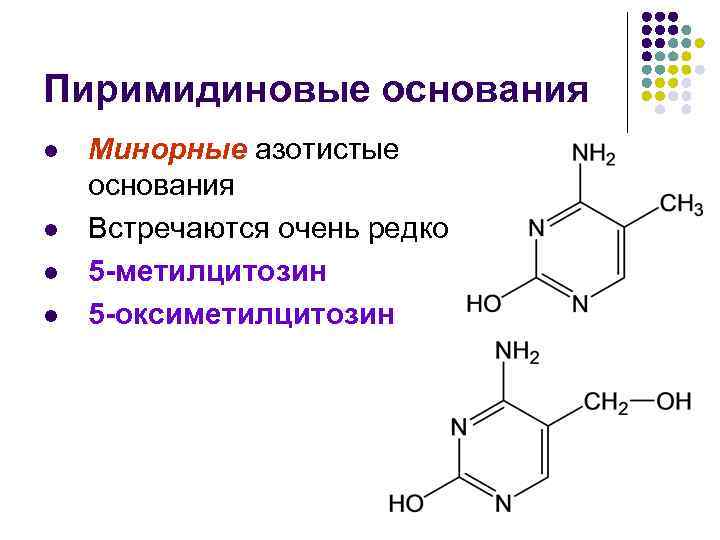 Пиримидиновые основания l l Минорные азотистые основания Встречаются очень редко 5 -метилцитозин 5 -оксиметилцитозин
Пиримидиновые основания l l Минорные азотистые основания Встречаются очень редко 5 -метилцитозин 5 -оксиметилцитозин
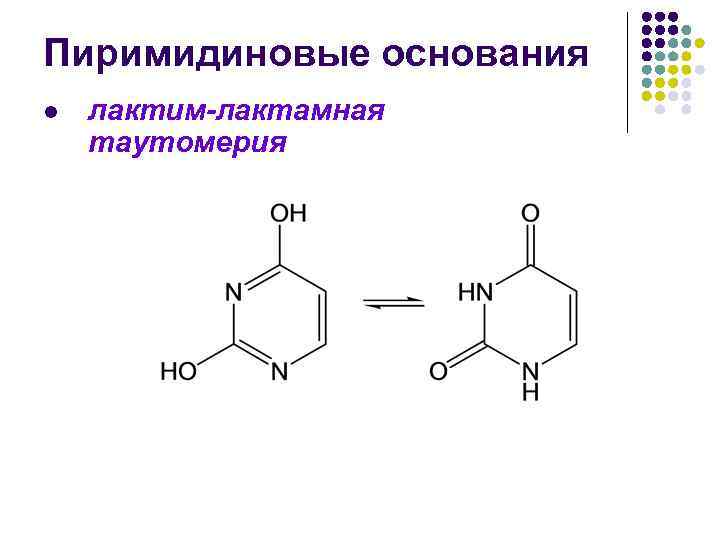 Пиримидиновые основания l лактим-лактамная таутомерия
Пиримидиновые основания l лактим-лактамная таутомерия
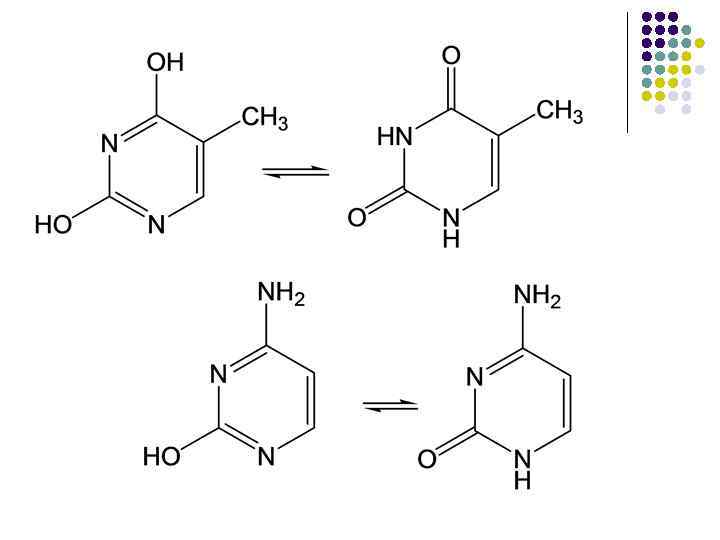
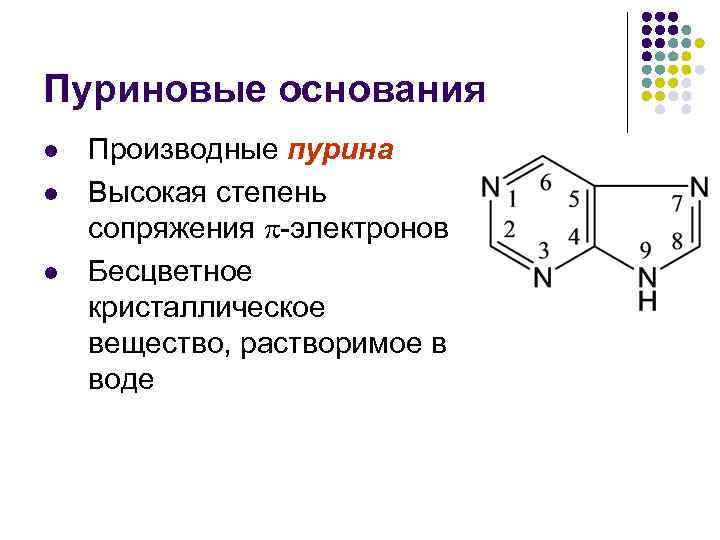 Пуриновые основания l l l Производные пурина Высокая степень сопряжения -электронов Бесцветное кристаллическое вещество, растворимое в воде
Пуриновые основания l l l Производные пурина Высокая степень сопряжения -электронов Бесцветное кристаллическое вещество, растворимое в воде
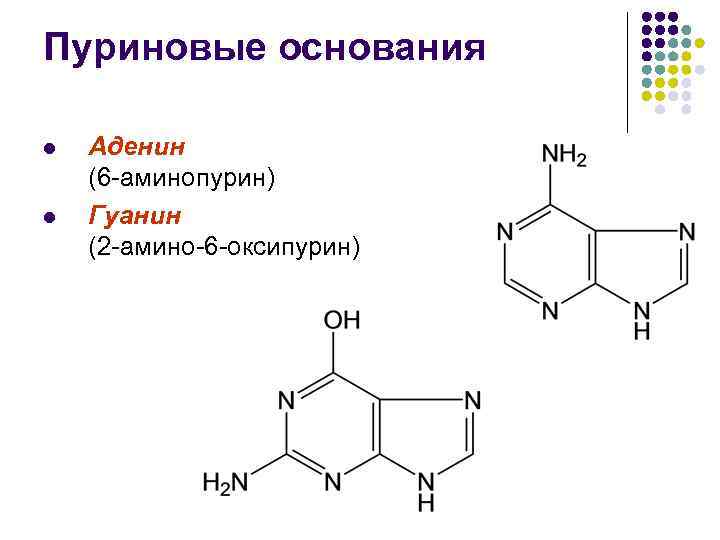 Пуриновые основания l l Аденин (6 -аминопурин) Гуанин (2 -амино-6 -оксипурин)
Пуриновые основания l l Аденин (6 -аминопурин) Гуанин (2 -амино-6 -оксипурин)
 Пуриновые основания l l Аденин и гуанин встречаются как в ДНК, так и в РНК Основным структурным их отличием является то, что атом углерода в положении 6 в гуанине окислен, а в аденине аминирован
Пуриновые основания l l Аденин и гуанин встречаются как в ДНК, так и в РНК Основным структурным их отличием является то, что атом углерода в положении 6 в гуанине окислен, а в аденине аминирован
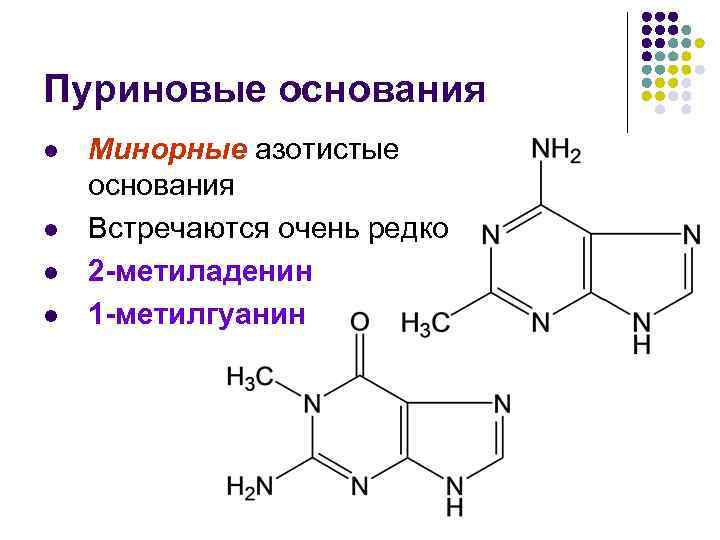 Пуриновые основания l l Минорные азотистые основания Встречаются очень редко 2 -метиладенин 1 -метилгуанин
Пуриновые основания l l Минорные азотистые основания Встречаются очень редко 2 -метиладенин 1 -метилгуанин
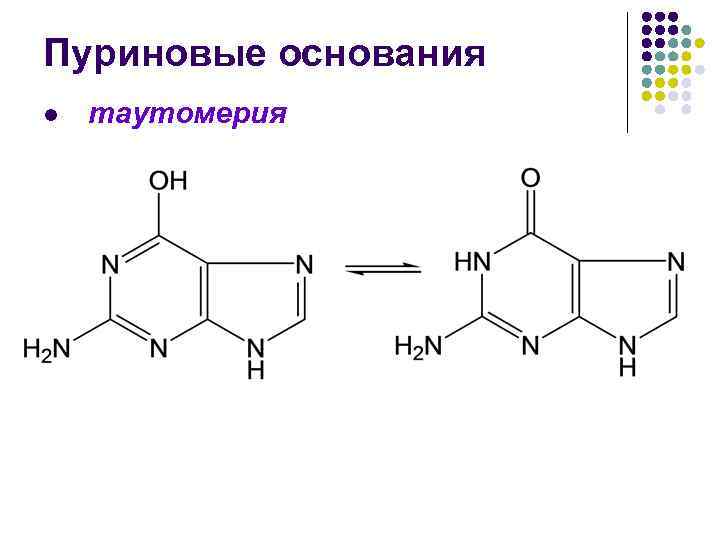 Пуриновые основания l таутомерия
Пуриновые основания l таутомерия
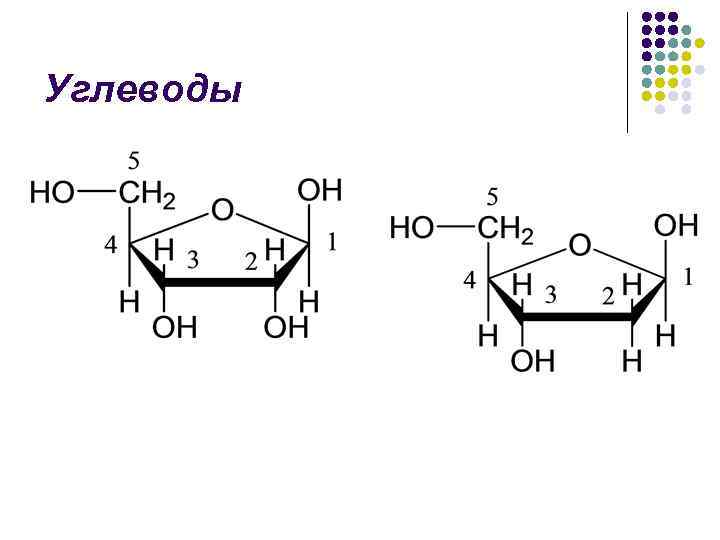 Углеводы
Углеводы
 Молекулярная масса нуклеиновых кислот
Молекулярная масса нуклеиновых кислот
 Молекулярная масса ДНК Гидродинамический метод l l В основе – линейная зависимость константы седиментации ДНК, определяемой при ультрацентрифугировании растворов ДНК, от ее Мr Электронно-микроскопический метод l l l основан на измерении длины вытянутых молекул ДНК На 0, 1 нм протяженности ее молекулы приходится масса 197
Молекулярная масса ДНК Гидродинамический метод l l В основе – линейная зависимость константы седиментации ДНК, определяемой при ультрацентрифугировании растворов ДНК, от ее Мr Электронно-микроскопический метод l l l основан на измерении длины вытянутых молекул ДНК На 0, 1 нм протяженности ее молекулы приходится масса 197
 Молекулярная масса РНК l l Те же методы Электрофорез в полиакриламидном геле – пробег РНК в геле обратно пропорционален их Мr Молекулярная масса ДНК очень большая (>> 106) Молекулярная масса РНК – от 20– 30 тыс. до 2 млн.
Молекулярная масса РНК l l Те же методы Электрофорез в полиакриламидном геле – пробег РНК в геле обратно пропорционален их Мr Молекулярная масса ДНК очень большая (>> 106) Молекулярная масса РНК – от 20– 30 тыс. до 2 млн.
 Локализация в клетке ДНК и РНК Виды ДНК и РНК
Локализация в клетке ДНК и РНК Виды ДНК и РНК
 l Количество ДНК в клетке измеряется пикограммами (1 пг = 10– 12 г) и колеблется от 0, 01 пг у кишечной палочки до нескольких пг в клетках высших организмов
l Количество ДНК в клетке измеряется пикограммами (1 пг = 10– 12 г) и колеблется от 0, 01 пг у кишечной палочки до нескольких пг в клетках высших организмов
 Виды ДНК по месту локализации Ядерная ДНК (у эукариот преобладает) Митохондриальная ДНК (у животных), хлоропластная ДНК (у растений) Центриольная ДНК Эписомальная ДНК l l l Эписомы – внехромосомные единицы наследственности микроорганизмов ДНК вирусов и фагов
Виды ДНК по месту локализации Ядерная ДНК (у эукариот преобладает) Митохондриальная ДНК (у животных), хлоропластная ДНК (у растений) Центриольная ДНК Эписомальная ДНК l l l Эписомы – внехромосомные единицы наследственности микроорганизмов ДНК вирусов и фагов
 Виды РНК по функциональному значению, Мr и локализации Транспортные РНК (т. РНК) l l Мr от 17 до 35 тыс. Содержатся в гиалоплазме, ядерном соке, матриксе хлоропластов и митохондрий Осуществляют перенос аминокислот к месту синтеза белка (к рибосомальному аппарату) Рибосомальные РНК (р. РНК) l l l l Мr от 550 до 700 тыс. у РНК 30– 40 S субчастиц рибосом 1, 1– 1, 7 106 – у РНК 50– 60 S субчастиц рибосом 40 тыс. – у 5 S РНК ~50 тыс. – у 5, 8 S РНК Локализованы в рибосомах Являются структурной основой рибосом
Виды РНК по функциональному значению, Мr и локализации Транспортные РНК (т. РНК) l l Мr от 17 до 35 тыс. Содержатся в гиалоплазме, ядерном соке, матриксе хлоропластов и митохондрий Осуществляют перенос аминокислот к месту синтеза белка (к рибосомальному аппарату) Рибосомальные РНК (р. РНК) l l l l Мr от 550 до 700 тыс. у РНК 30– 40 S субчастиц рибосом 1, 1– 1, 7 106 – у РНК 50– 60 S субчастиц рибосом 40 тыс. – у 5 S РНК ~50 тыс. – у 5, 8 S РНК Локализованы в рибосомах Являются структурной основой рибосом
 Виды РНК по функциональному значению, Мr и локализации Информационные или матричные РНК (и. РНК. м. РНК) l l l Мr от 300 тыс. до 4 106 Матричная функция в синтезе белка в составе рибосом Вирусные РНК – составные части вирусных и фаговых рибонуклеопротеидов, несут информацию, необходимую для размножения вируса в клетках хозяина Ядерные РНК – предшественники всех видов РНК эукариотической клетки
Виды РНК по функциональному значению, Мr и локализации Информационные или матричные РНК (и. РНК. м. РНК) l l l Мr от 300 тыс. до 4 106 Матричная функция в синтезе белка в составе рибосом Вирусные РНК – составные части вирусных и фаговых рибонуклеопротеидов, несут информацию, необходимую для размножения вируса в клетках хозяина Ядерные РНК – предшественники всех видов РНК эукариотической клетки
 Строение структурных элементов нуклеиновых кислот
Строение структурных элементов нуклеиновых кислот
 l l Мономерные звенья ДНК и РНК – остатки нуклеотидов, состоящих из остатков азотистого основания, рибозы или дезоксирибозы и фосфорной кислоты Они образуются при гидролизе нуклеиновых кислот водным раствором щелочи или ферментами При гидролизе РНК – рибонуклеотиды При гидролизе ДНК – дезоксирибонуклеотиды
l l Мономерные звенья ДНК и РНК – остатки нуклеотидов, состоящих из остатков азотистого основания, рибозы или дезоксирибозы и фосфорной кислоты Они образуются при гидролизе нуклеиновых кислот водным раствором щелочи или ферментами При гидролизе РНК – рибонуклеотиды При гидролизе ДНК – дезоксирибонуклеотиды
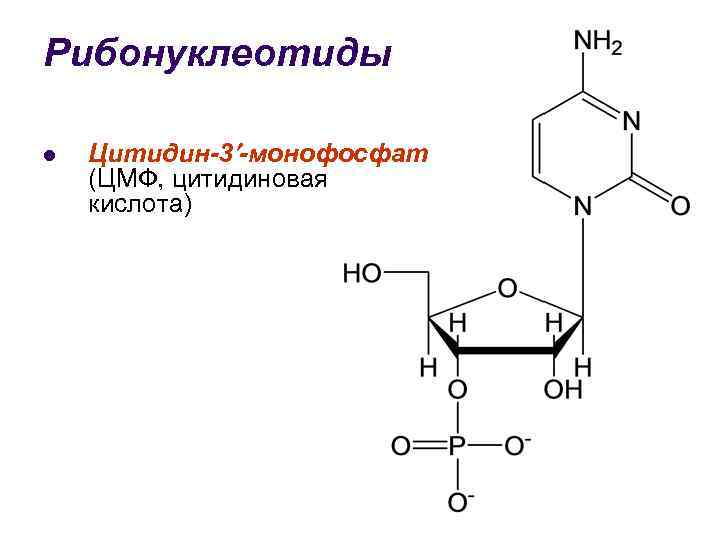 Рибонуклеотиды l Цитидин-3 -монофосфат (ЦМФ, цитидиновая кислота)
Рибонуклеотиды l Цитидин-3 -монофосфат (ЦМФ, цитидиновая кислота)
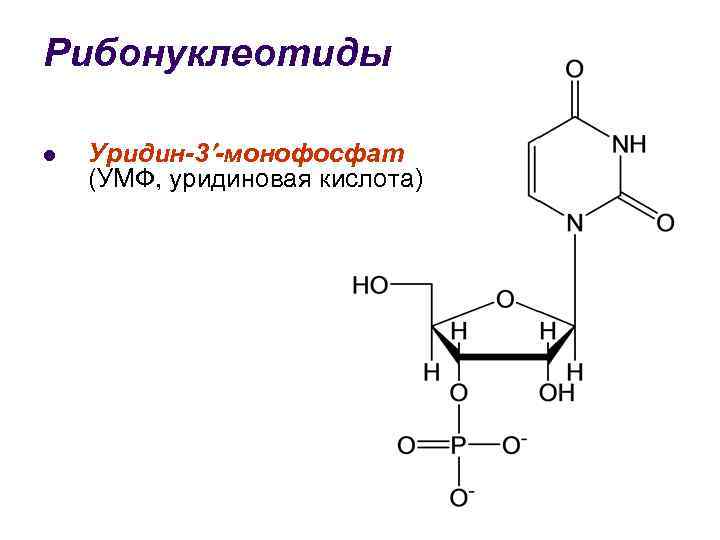 Рибонуклеотиды l Уридин-3 -монофосфат (УМФ, уридиновая кислота)
Рибонуклеотиды l Уридин-3 -монофосфат (УМФ, уридиновая кислота)
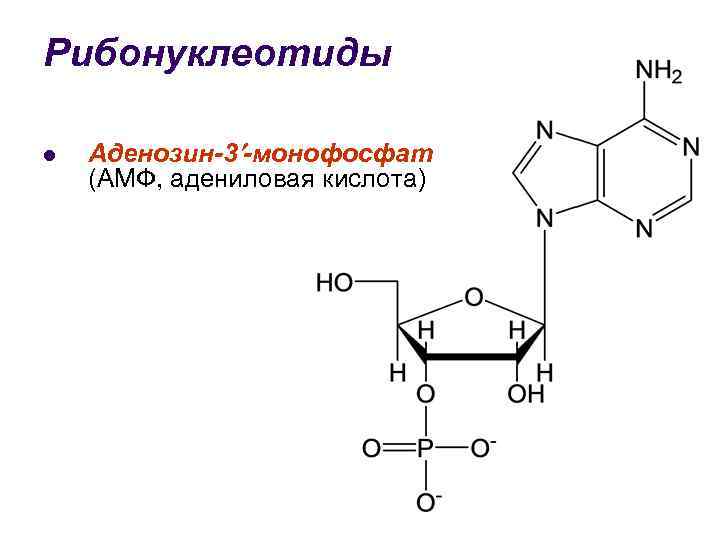 Рибонуклеотиды l Аденозин-3 -монофосфат (АМФ, адениловая кислота)
Рибонуклеотиды l Аденозин-3 -монофосфат (АМФ, адениловая кислота)
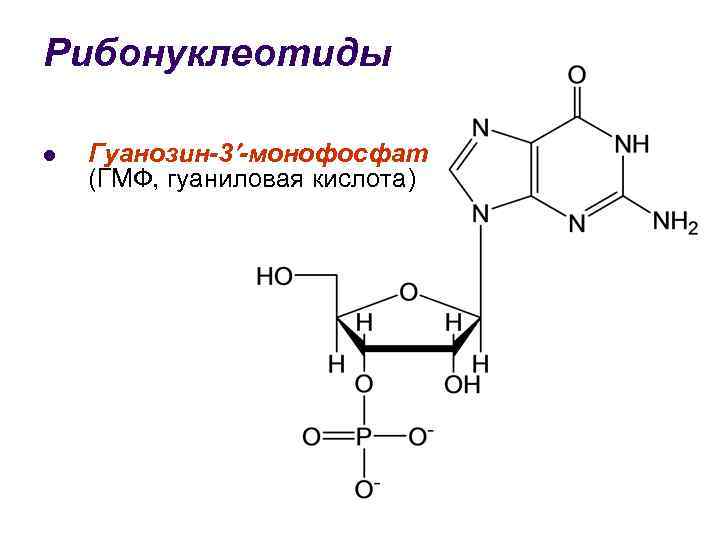 Рибонуклеотиды l Гуанозин-3 -монофосфат (ГМФ, гуаниловая кислота)
Рибонуклеотиды l Гуанозин-3 -монофосфат (ГМФ, гуаниловая кислота)
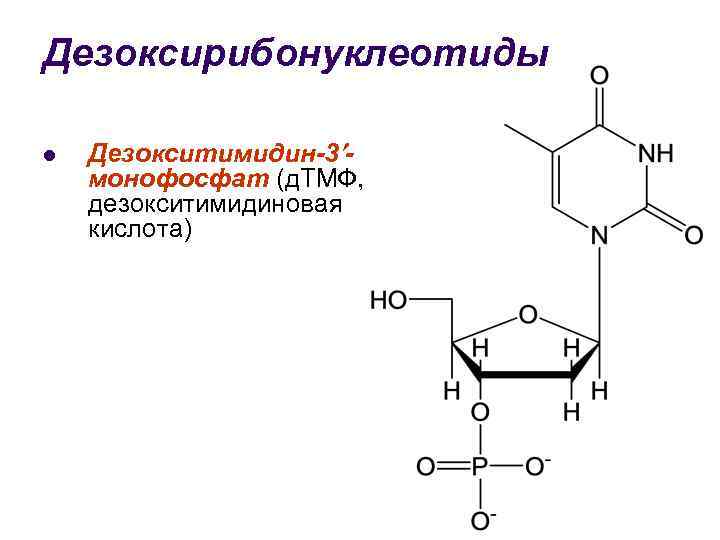 Дезоксирибонуклеотиды l Дезокситимидин-3 монофосфат (д. ТМФ, дезокситимидиновая кислота)
Дезоксирибонуклеотиды l Дезокситимидин-3 монофосфат (д. ТМФ, дезокситимидиновая кислота)
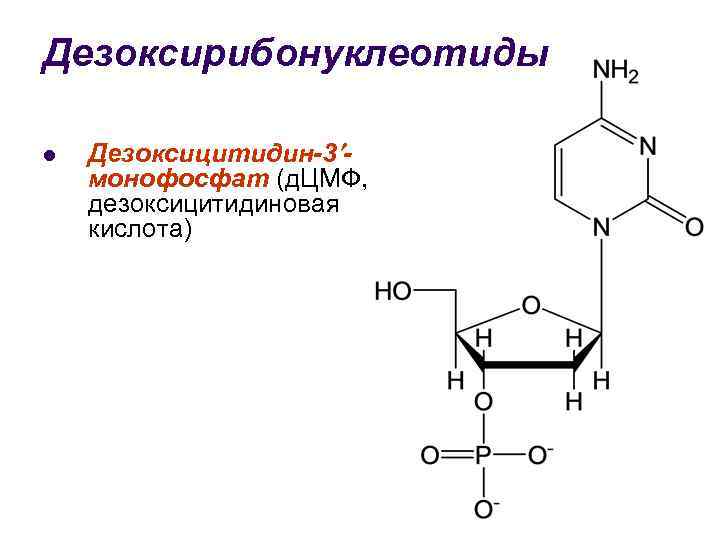 Дезоксирибонуклеотиды l Дезоксицитидин-3 монофосфат (д. ЦМФ, дезоксицитидиновая кислота)
Дезоксирибонуклеотиды l Дезоксицитидин-3 монофосфат (д. ЦМФ, дезоксицитидиновая кислота)
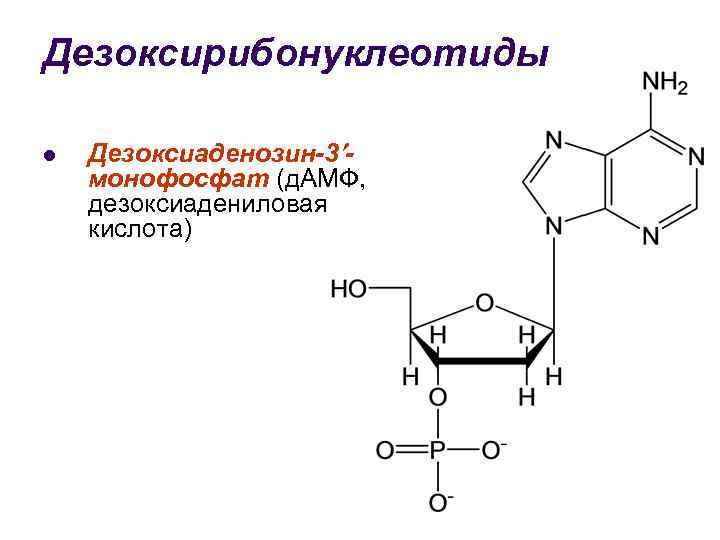 Дезоксирибонуклеотиды l Дезоксиаденозин-3 монофосфат (д. АМФ, дезоксиадениловая кислота)
Дезоксирибонуклеотиды l Дезоксиаденозин-3 монофосфат (д. АМФ, дезоксиадениловая кислота)
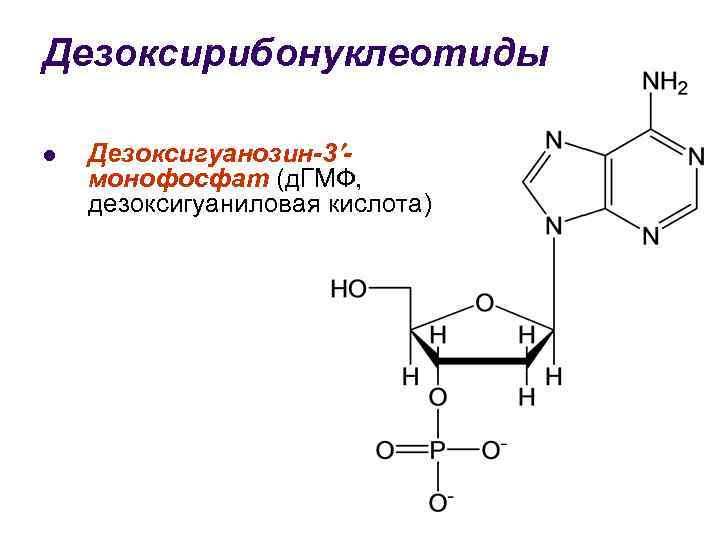 Дезоксирибонуклеотиды l Дезоксигуанозин-3 монофосфат (д. ГМФ, дезоксигуаниловая кислота)
Дезоксирибонуклеотиды l Дезоксигуанозин-3 монофосфат (д. ГМФ, дезоксигуаниловая кислота)
 l l Остаток фосфорной кислоты может быть у 5 -атома С рибозы формулы – самостоятельно
l l Остаток фосфорной кислоты может быть у 5 -атома С рибозы формулы – самостоятельно
 l l Мононуклеотиды – сильные кислоты (? ), Гидролизуются с образованием нуклеозидов: l l l l l ЦМФ цитидин + Н 3 РО 4 УМФ уридин + Н 3 РО 4 АМФ аденозин + Н 3 РО 4 ГМФ гуанозин + Н 3 РО 4 д. ЦМФ дезоксицитидин + Н 3 РО 4 д. ТМФ дезокситимидин + Н 3 РО 4 д. АМФ дезоксиаденозин + Н 3 РО 4 д. ГМФ дезоксигуанозин + Н 3 РО 4 Дают реакции по типу многоатомных спиртов и за счет азотистых оснований
l l Мононуклеотиды – сильные кислоты (? ), Гидролизуются с образованием нуклеозидов: l l l l l ЦМФ цитидин + Н 3 РО 4 УМФ уридин + Н 3 РО 4 АМФ аденозин + Н 3 РО 4 ГМФ гуанозин + Н 3 РО 4 д. ЦМФ дезоксицитидин + Н 3 РО 4 д. ТМФ дезокситимидин + Н 3 РО 4 д. АМФ дезоксиаденозин + Н 3 РО 4 д. ГМФ дезоксигуанозин + Н 3 РО 4 Дают реакции по типу многоатомных спиртов и за счет азотистых оснований
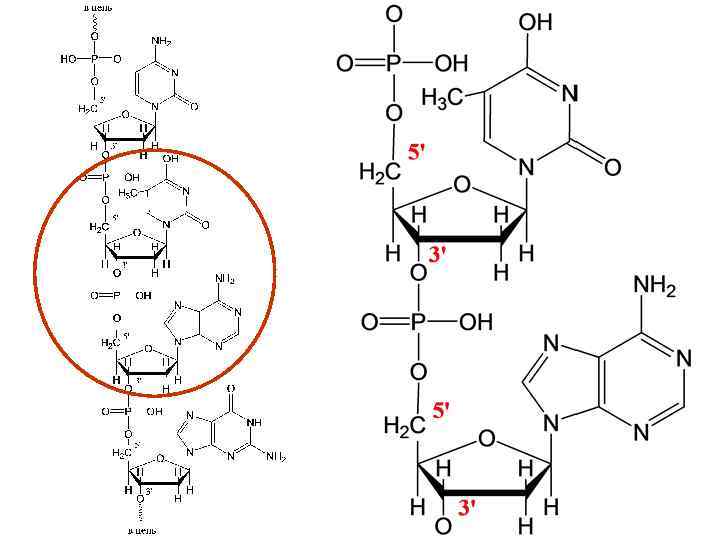
 l Мононуклеотиды, объединяясь, могут образовывать олиго- и полинуклеотиды, при этом образуются фосфодиэфирные связи между 3 атомом С углевода одного мононуклеотида и 5 -атомом С углевода другого мононуклеотида
l Мононуклеотиды, объединяясь, могут образовывать олиго- и полинуклеотиды, при этом образуются фосфодиэфирные связи между 3 атомом С углевода одного мононуклеотида и 5 -атомом С углевода другого мононуклеотида
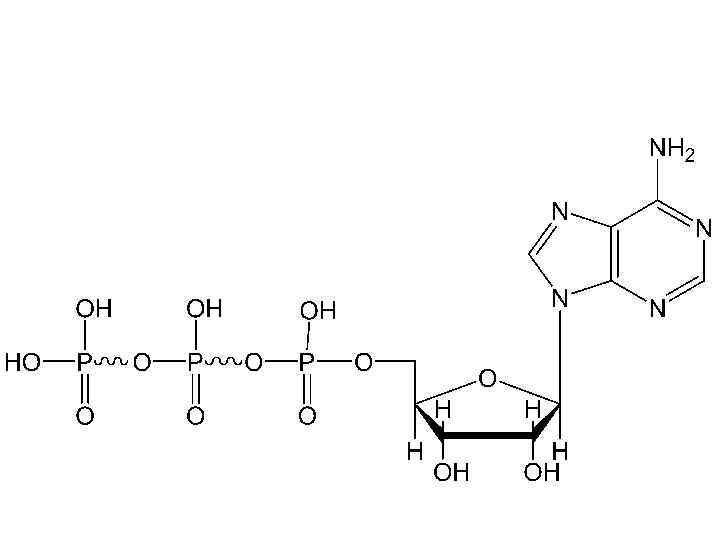
 l l Кроме монофосфатов, могут быть ди- и трифосфаты Аденозинтрифосфорная кислота (АТФ)
l l Кроме монофосфатов, могут быть ди- и трифосфаты Аденозинтрифосфорная кислота (АТФ)
 Литература l l l Березов Т. Т. , Коровкин Б. Ф. Биологическая химия. – М. : Медицина, 1983 Молекулярная биология. Структура и биосинтез нуклеиновых кислот / Под ред. А. С. Спирина. – М. : Высшая школа, 1990 Овчинников Ю. А. Биоорганическая химия. – М. : Просвещение, 1987 Филиппович Ю. Б. Основы биохимии. – М. : Высшая школа, 1993 Шерстнев М. П. , Комаров О. С. Химия и биология нуклеиновых кислот. – М. : Просвещение, 1990
Литература l l l Березов Т. Т. , Коровкин Б. Ф. Биологическая химия. – М. : Медицина, 1983 Молекулярная биология. Структура и биосинтез нуклеиновых кислот / Под ред. А. С. Спирина. – М. : Высшая школа, 1990 Овчинников Ю. А. Биоорганическая химия. – М. : Просвещение, 1987 Филиппович Ю. Б. Основы биохимии. – М. : Высшая школа, 1993 Шерстнев М. П. , Комаров О. С. Химия и биология нуклеиновых кислот. – М. : Просвещение, 1990


