DNA & RNA L.ppt
- Количество слайдов: 78

Нуклеїнові кислоти • Нуклеотиди: фундаментальні субодиниці • Нуклеїнові кислоти: структура і функція

Передача інформації в клітинах “Центральна догма” молекулярної біології Редуплікація Транскрипція ДНК м. РНК Трансляція Протеїн, лінійна послідовність амінокислот, кодується ДНК, лінійною послідовністю нуклеотидів
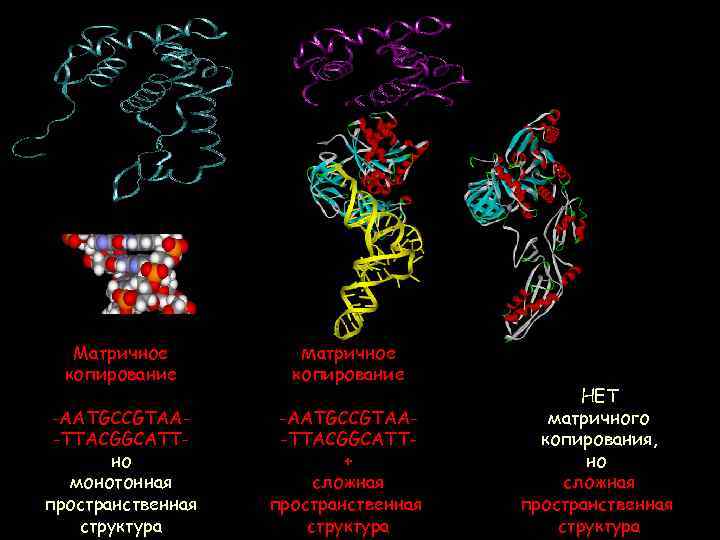
ДНК информация копирование РНК БЕЛОК информация структура копирование функция Матричное копирование -AATGCCGTAA-TTACGGCATTно монотонная пространственная структура -AATGCCGTAA-TTACGGCATT+ сложная пространственная структура функция НЕТ матричного копирования, но сложная пространственная структура
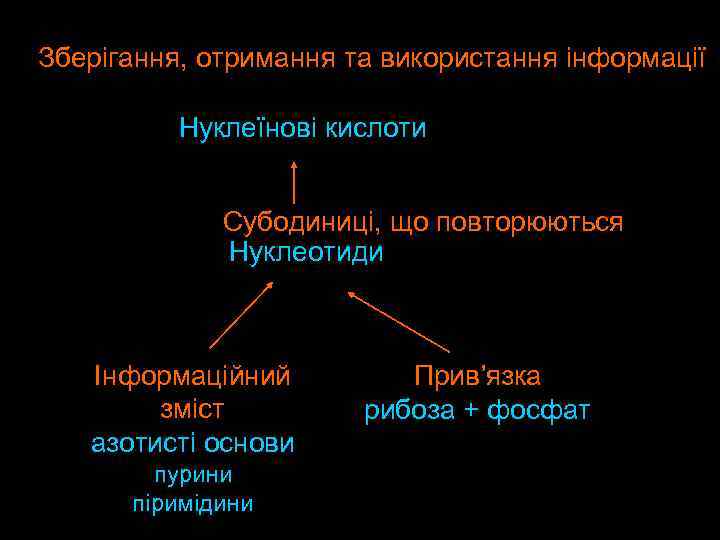
Зберігання, отримання та використання інформації Нуклеїнові кислоти Субодиниці, що повторюються Нуклеотиди Інформаційний зміст азотисті основи пурини піримідини Прив’язка рибоза + фосфат
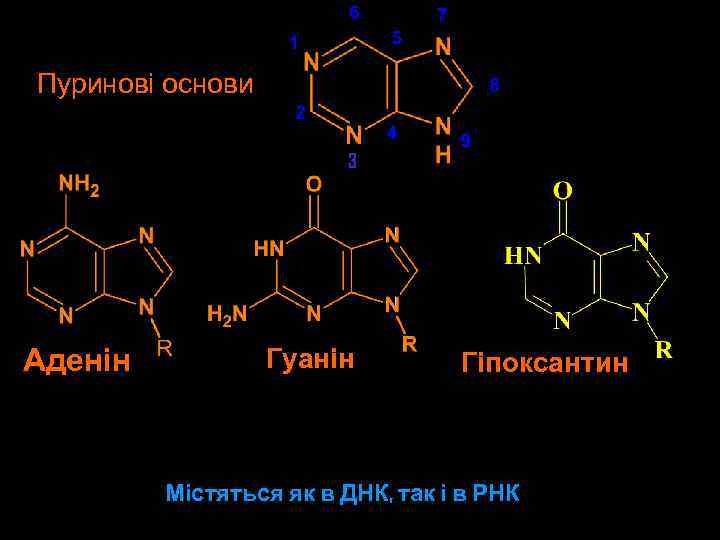
Пуринові основи 3 Аденін Гуанін Гіпоксантин Містяться як в ДНК, так і в РНК
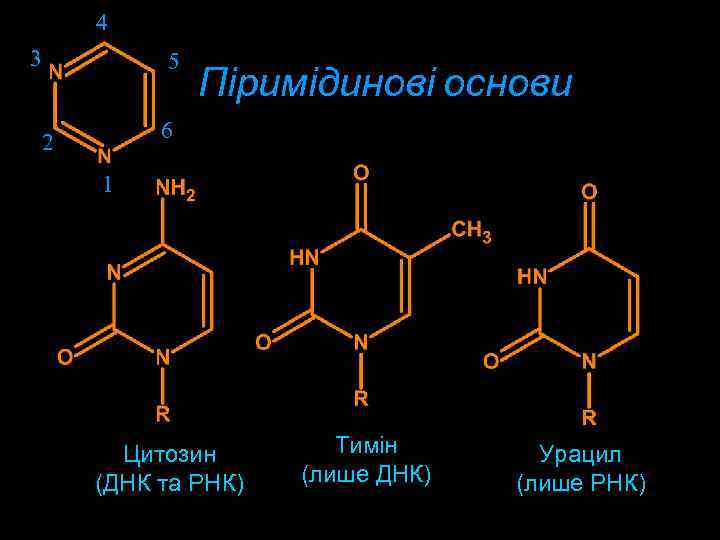
4 3 5 Піримідинові основи 6 2 1 Цитозин (ДНК та РНК) Тимін (лише ДНК) Урацил (лише РНК)
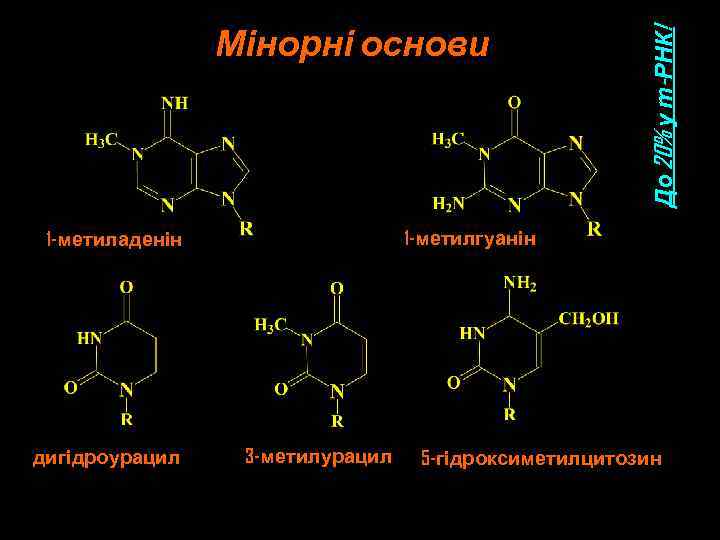
1 -метилгуанін 1 -метиладенін дигідроурацил До 20% у т-РНК! Мінорні основи 3 -метилурацил 5 -гідроксиметилцитозин
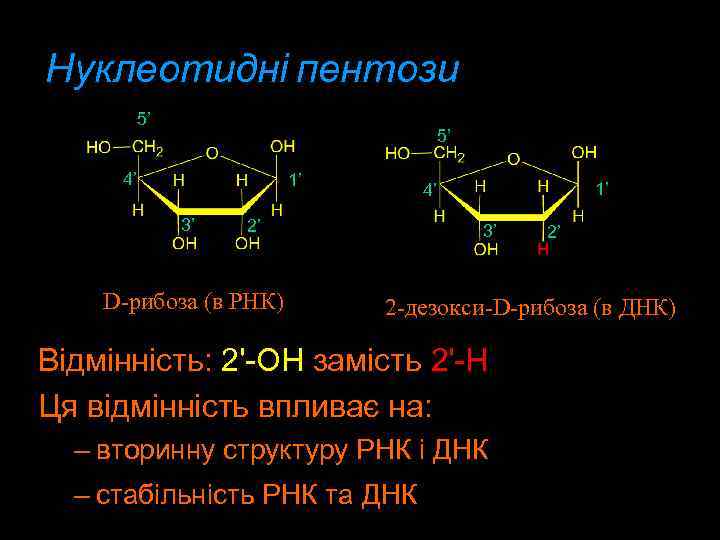
Нуклеотидні пентози 5’ 5’ 4’ 1’ 3’ 2’ D-рибоза (в РНК) 1’ 4’ 3’ 2’ 2 -дезокси-D-рибоза (в ДНК) Відмінність: 2'-OH замість 2'-H Ця відмінність впливає на: – вторинну структуру РНК і ДНК – стабільність РНК та ДНК
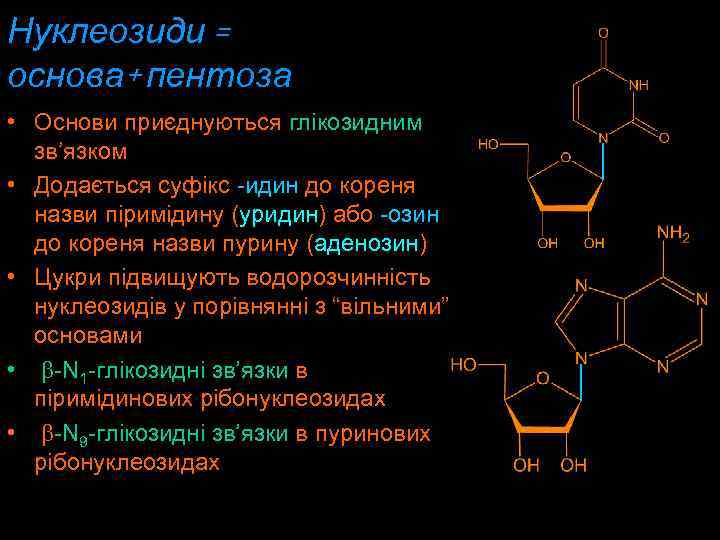
Нуклеозиди = основа+ пентоза • Основи приєднуються глікозидним зв’язком • Додається суфікс -идин дo кореня назви піримідину (уридин) або -озин до кореня назви пурину (аденозин) • Цукри підвищують водорозчинність нуклеозидів у порівнянні з “вільними” основами • b-N 1 -глікозидні зв’язки в піримідинових рібонуклеозидах • b-N 9 -глікозидні зв’язки в пуринових рібонуклеозидах
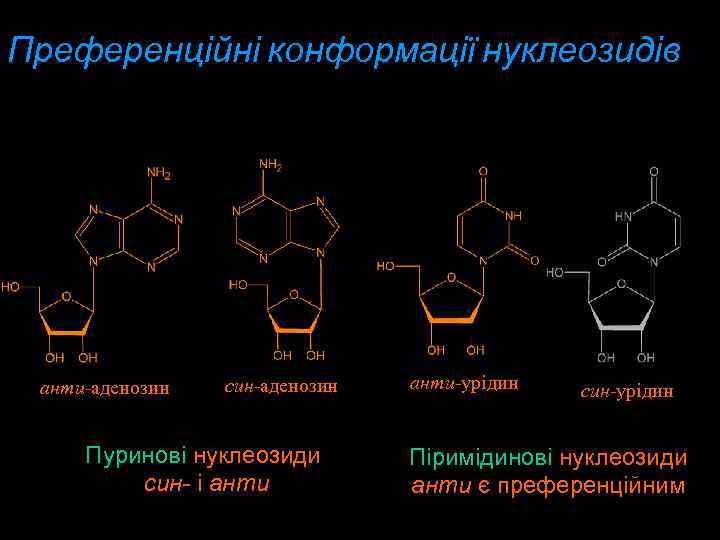
Преференційні конформації нуклеозидів aнти-аденозин син-аденозин Пуринові нуклеозиди син- і анти-урідин син-урідин Піримідинові нуклеозиди анти є преференційним
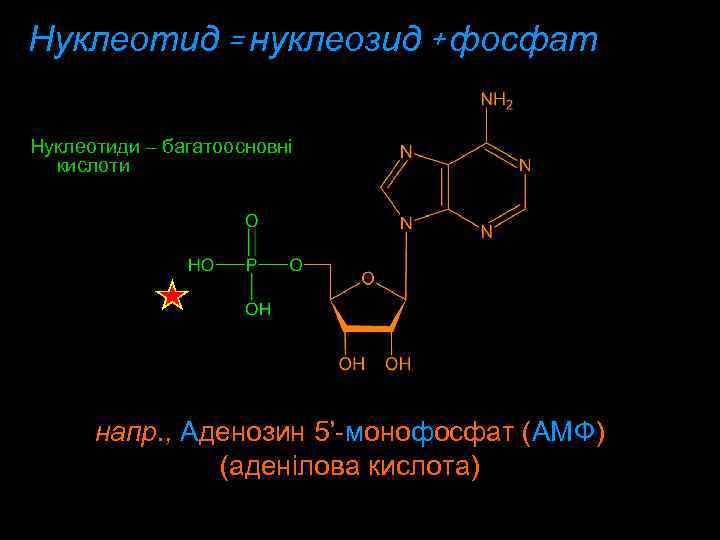
Нуклеотид = нуклеозид + фосфат Нуклеотиди – багатоосновні кислоти напр. , Aденозин 5’-мoнoфoсфат (AMФ) (аденілова кислота)

Функції нуклеотидів • Попередники полінуклеотидів ДНК і РНК • Переносники енергії через перенесення фосфорильних груп напр. , ATФ + H 2 O AДФ + Фн + eнергія – Основи служать як одиниці розпізнавання • • ATФ – енергетичний метаболізм ГTФ – синтез протеїнів ЦTФ – синтез ліпідів УTФ – синтез вуглеводів • Циклічні нуклеотиди – сигнальні молекули і регулятори клітинного метаболізму і репродукції
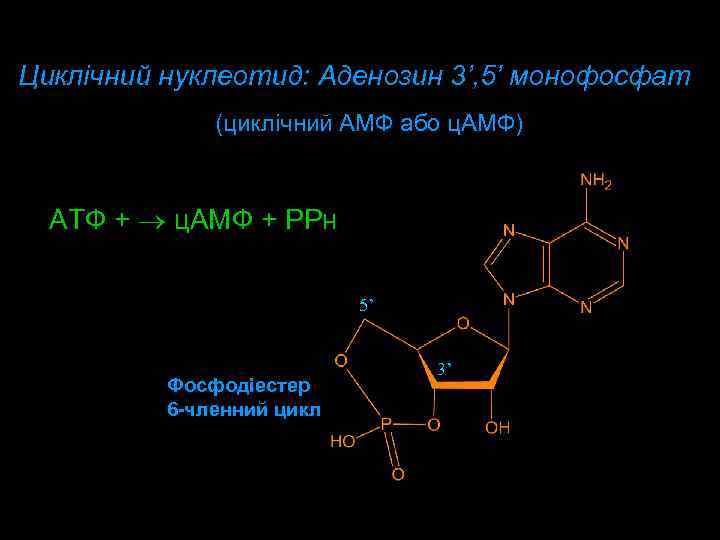
Циклічний нуклеотид: Aденозин 3’, 5’ монофосфат (циклічний AMФ або ц. AMФ) ATФ + ц. AMФ + PPн 5’ Фосфодіестер 6 -членний цикл 3’
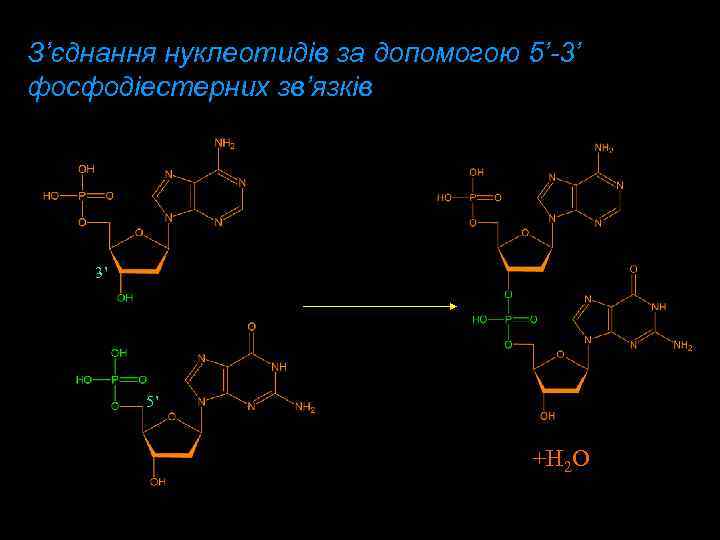
З’єднання нуклеотидів за допомогою 5’-3’ фосфодіестерних зв’язків 3’ 5’ +H 2 O
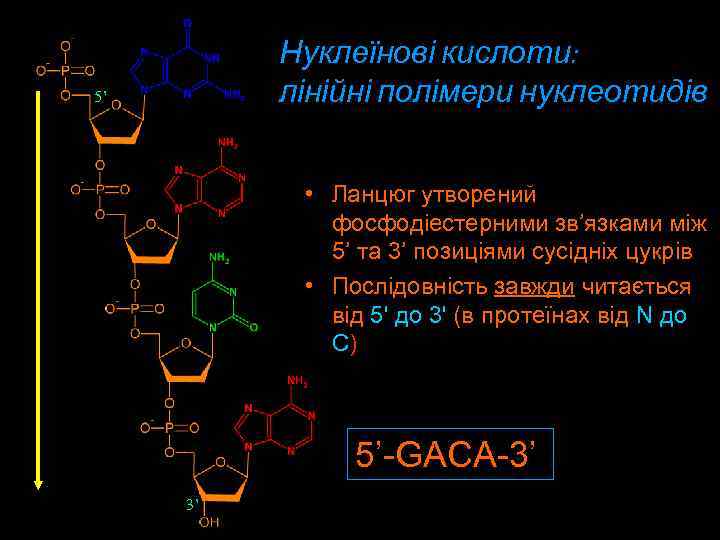
Нуклеїнові кислоти: лінійні полімери нуклеотидів 5’ • Ланцюг утворений фосфодіестерними зв’язками між 5’ та 3’ позиціями сусідніх цукрів • Послідовність завжди читається від 5' дo 3' (в протеїнах від N дo C) 5’-GACA-3’ 3’

Класи нуклеїнових кислот • ДНК – один тип, одна ціль: генетичний матеріал – характеризується первинною і вторинною структурою (спіраль), але не третинною структурою • РНК – 3 типи, 3 цілі: – первинна, вторинна і третинна структури – рибосомні РНК – основа структури та функції рибосом – матричні РНК – переносники “месседжів” – транспортні РНК – переносники амінокислот

Подвійна спіраль ДНК: коротка історія Стабілізована водневими зв’язками • “Пари основ" є наслідком Н-зв’язків: • A однієї низки утворює пару з T іншої низки • G утворює пару з C • Ервін Шаргафф знайшов явище спарювання, але не зрозумів його сенс • Розалінда Франклін РСт. А мав вирішальне значення • Френсіс Крік • Джеймс Уотсон коректна інтерпретація

ДНК как апериодический кристалл Кембридж, Англия, 1952 Д. Уотсон Ф. Крик М. Уилкинс Р. Франклин

Подвійна спіраль ДНК • Дві низки, спрямовані антипаралельно • “Пари основ“, що утворюють Hзв’язки: – A+T – G+C • Низки є комплементарними • Ван-дер-Ваальсівські взаємодії між основами, що стикуються, також стабілізують спіраль • Eлектростатичне відштовхування між фосфатними групами дестабілізує спіраль. . . • Але зв’язування протийонів (напр. , Mg 2+) мінімізує його вплив
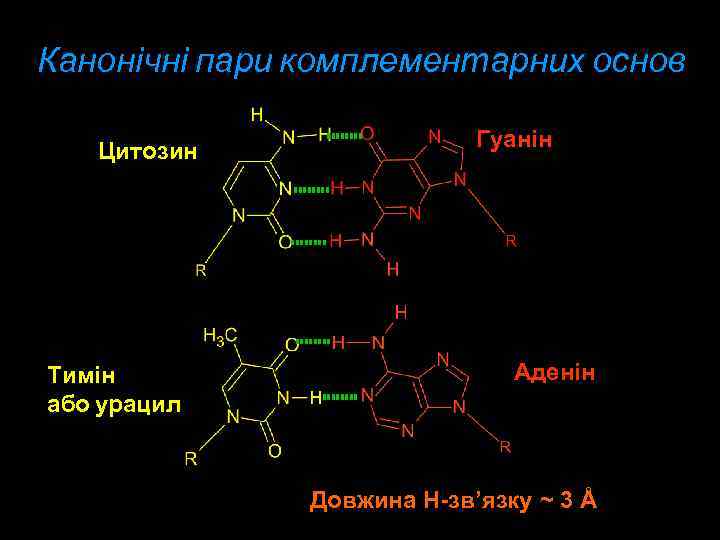
Канонічні пари комплементарних основ Цитозин Тимін або урацил Гуанін Аденін Довжина Н-зв’язку ~ 3 Å
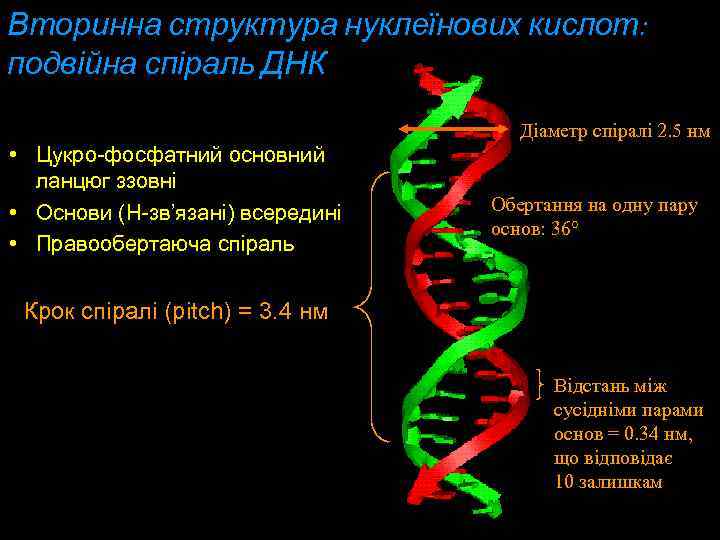
Вторинна структура нуклеїнових кислот: подвійна спіраль ДНК Діаметр спіралі 2. 5 нм • Цукро-фосфатний основний ланцюг ззовні • Основи (Н-зв’язані) всередині • Правообертаюча спіраль Обертання на одну пару основ: 36° Крок спіралі (рitch) = 3. 4 нм Відстань між сусідніми парами основ = 0. 34 нм, що відповідає 10 залишкам

Вторинна структура нуклеїнових кислот: подвійна спіраль ДНК Схема одного з ланцюгів подвійної спіралі ДНК. Основи – лише піримідини. Є вісь симетрії 10 -го порядку
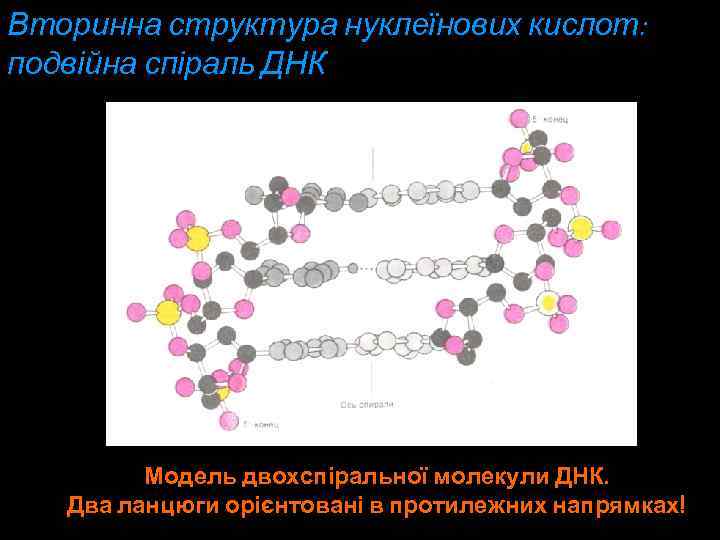
Вторинна структура нуклеїнових кислот: подвійна спіраль ДНК Модель двохспіральної молекули ДНК. Два ланцюги орієнтовані в протилежних напрямках!
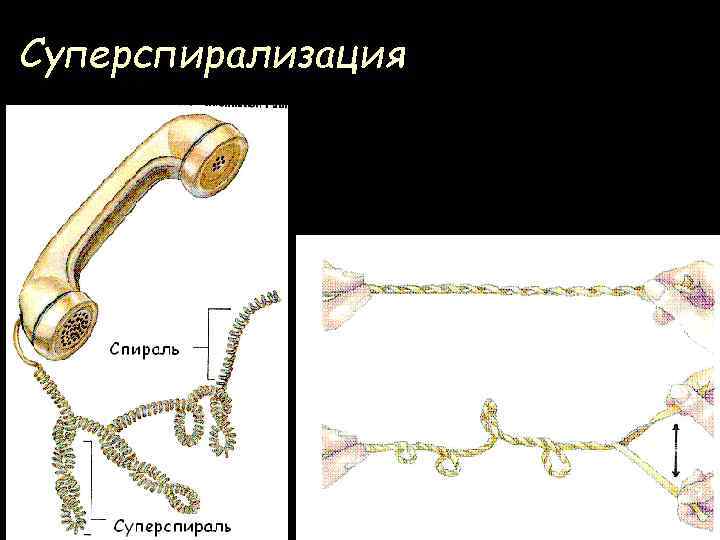
Суперспирализация
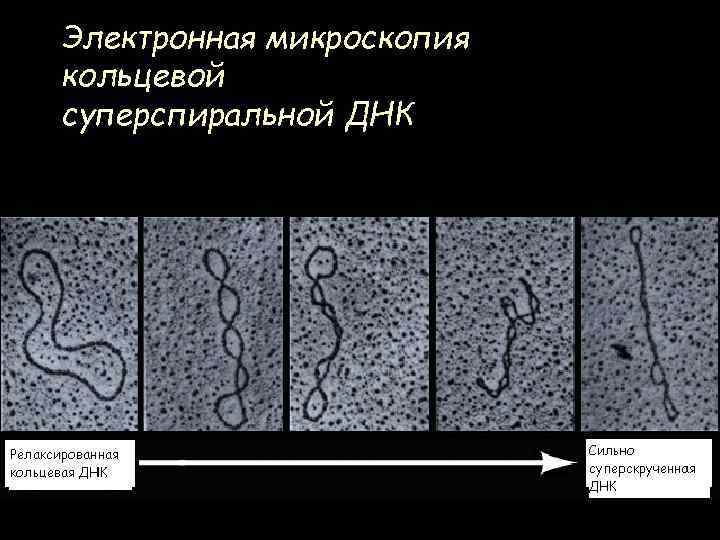
Электронная микроскопия кольцевой суперспиральной ДНК
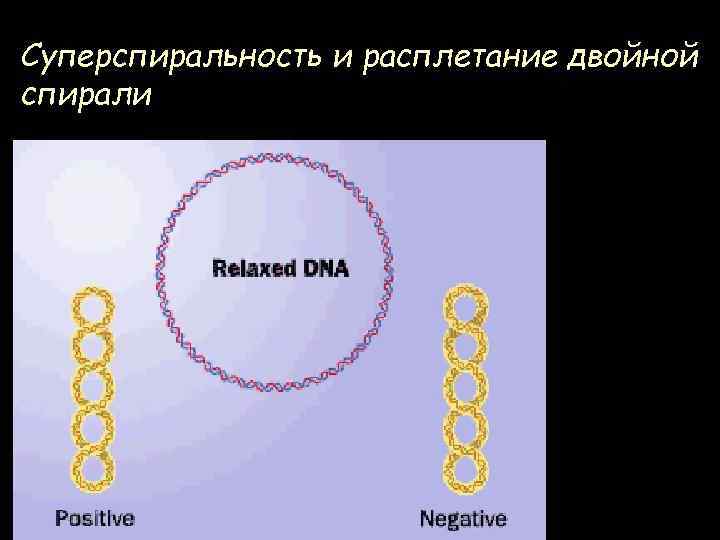
Суперспиральность и расплетание двойной спирали Lk = Tw + Wr
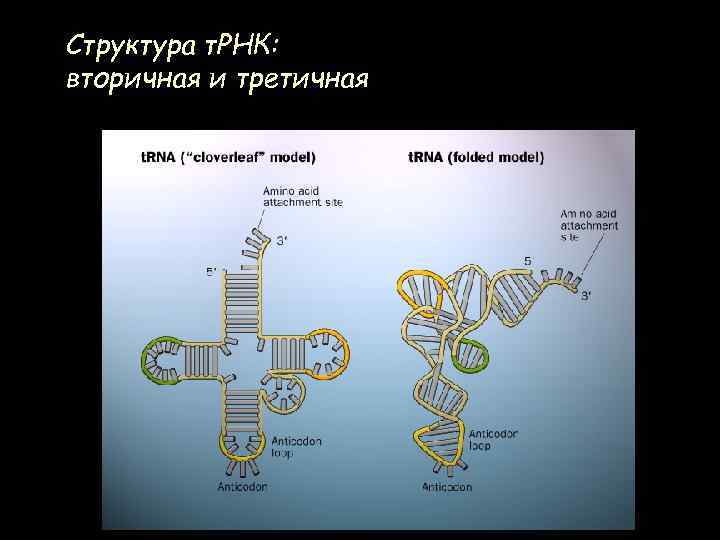
Структура т. РНК: вторичная и третичная

т. РНК белок т. РНК Мимикрия третичной структуры белок
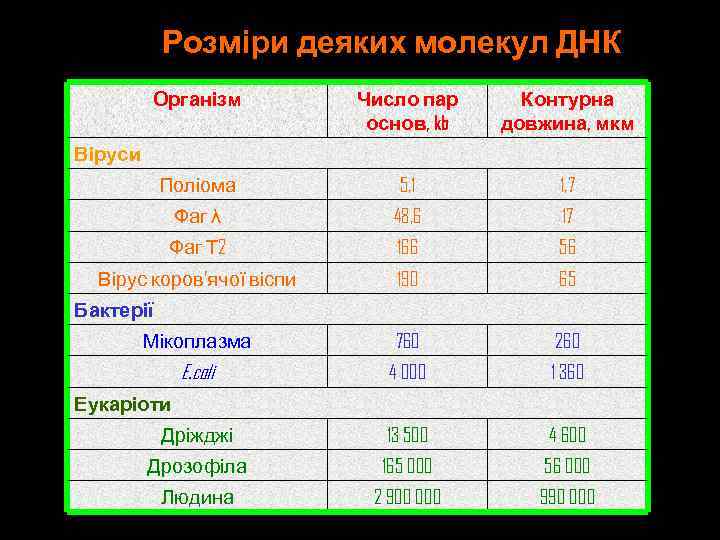
Розміри деяких молекул ДНК Організм Число пар основ, kb Контурна довжина, мкм Поліома 5, 1 1, 7 Фаг λ 48, 6 17 Фаг Т 2 166 56 Вірус коров’ячої віспи 190 65 Мікоплазма 760 260 E. coli 4 000 1 360 Дріжджі 13 500 4 600 Дрозофіла 165 000 56 000 Людина 2 900 000 990 000 Віруси Бактерії Еукаріоти

Длина ДНК человека http: //nature. web. ru/ В ядре каждой клетки человека содержится 23 пары хромосом, они содержат около 3, 2 млрд. пар нуклеотидов Суммарная длина всех 46 молекул ДНК в одной клетке равна прим. 2 м. Общая длина ДНК во всех клетках человеческого тела составляет 1011 км, что почти в тысячу раз больше расстояния от Земли до Солнца.
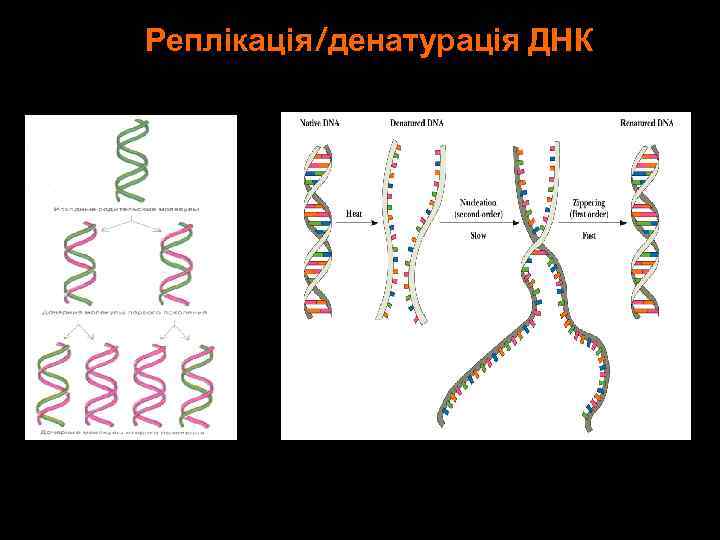
Реплікація/денатурація ДНК
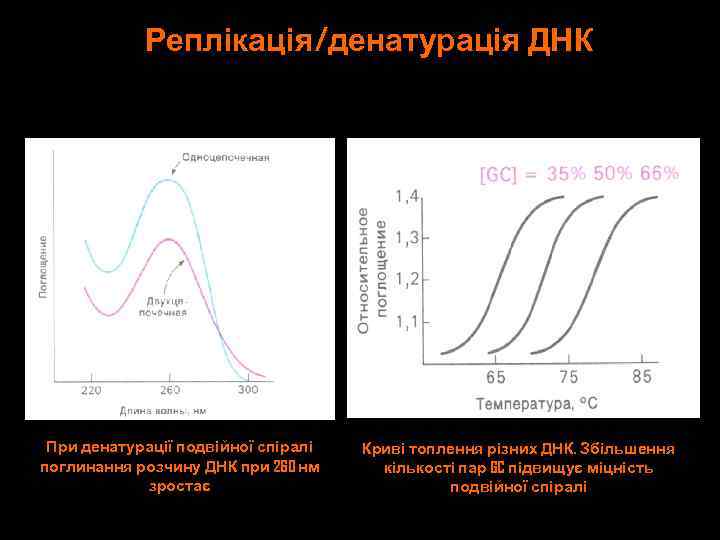
Реплікація/денатурація ДНК При денатурації подвійної спіралі поглинання розчину ДНК при 260 нм зростає Криві топлення різних ДНК. Збільшення кількості пар GC підвищує міцність подвійної спіралі
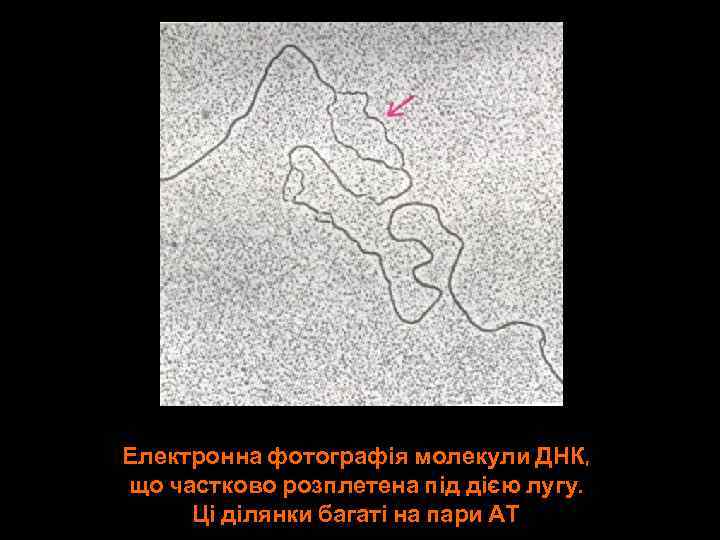
Електронна фотографія молекули ДНК, що частково розплетена під дією лугу. Ці ділянки багаті на пари АТ

Відмінності між ДНК і РНК Чому ДНК містить тімін, в той час як РНК містить урацил? ? • Цитозин спонтанно (але рідко) дезамінується з утворенням урацилу • Це може призвести до “мутації” пари основ ГЦ на AУ • Спеціальні “ремонтні” ензими розпізнають ці “мутації" та заміщують урацил на цитозин • Але якщо урацил був нормальною основою в ДНК, “ремонтні” ензими не можуть відрізнити урацил, що утворився в результаті дезамінування цитозину • Рішення: замінити урацил на тімін (5 -метил-урацил) в ДНК
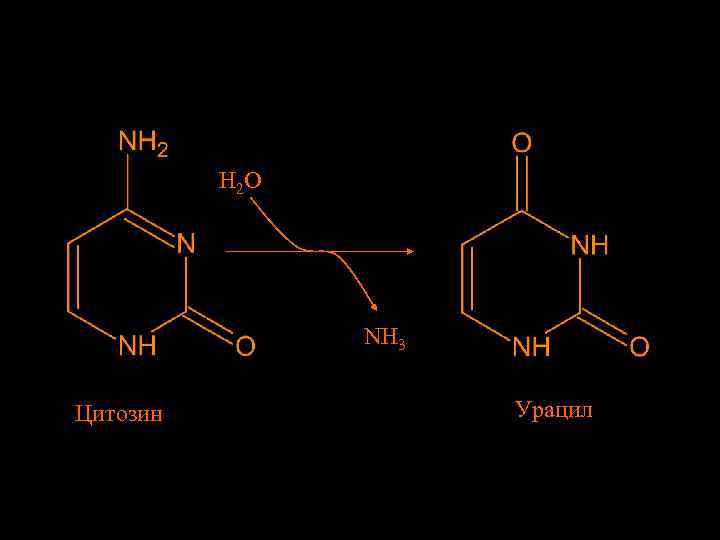
H 2 O NH 3 Цитозин Урацил
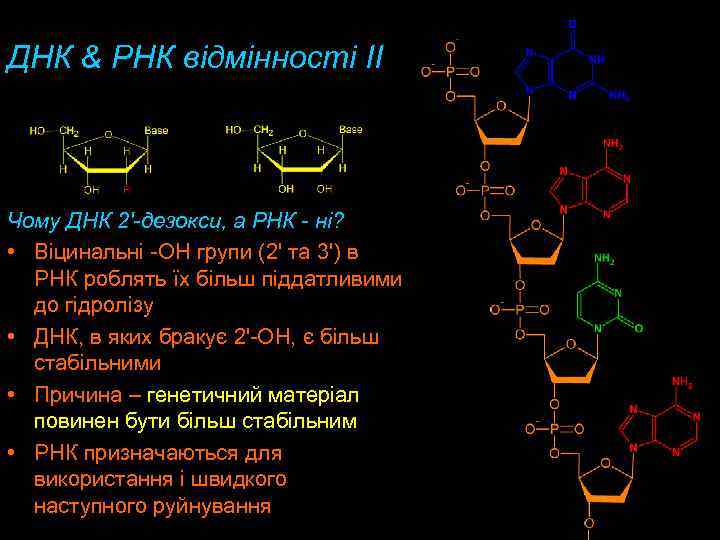
ДНК & РНК відмінності II Чому ДНК 2'-дезокси, а РНК - ні? • Віцинальні -OH групи (2' та 3') в РНК роблять їх більш піддатливими до гідролізу • ДНК, в яких бракує 2'-OH, є більш стабільними • Причина – генетичний матеріал повинен бути більш стабільним • РНК призначаються для використання і швидкого наступного руйнування

ДНК & РНК відмінності III Чому РНК можуть виявляти третинну структуру ( напр. , т. РНК, р. РНК) додатково до вторинної структури? РНК мають 2’-гідроксильні групи, потенціально здатні до утворення додаткових Н-зв’язків

Комплекси металів з основами, нуклеозидами та нуклеотидами ГОЛОВНІ ПИТАННЯ: 1. Які атоми пуринів та піримідинів є центрами приєднання ня металів у нуклеозидах та нуклеотидах? 2. Наскільки ефективно фосфат конкурує з основами за іони металів? 3. Чи можливе одночасне приєднання металів до основ і фосфатних груп?

Комплекси металів з основами, нуклеозидами та нуклеотидами фосфатні групи
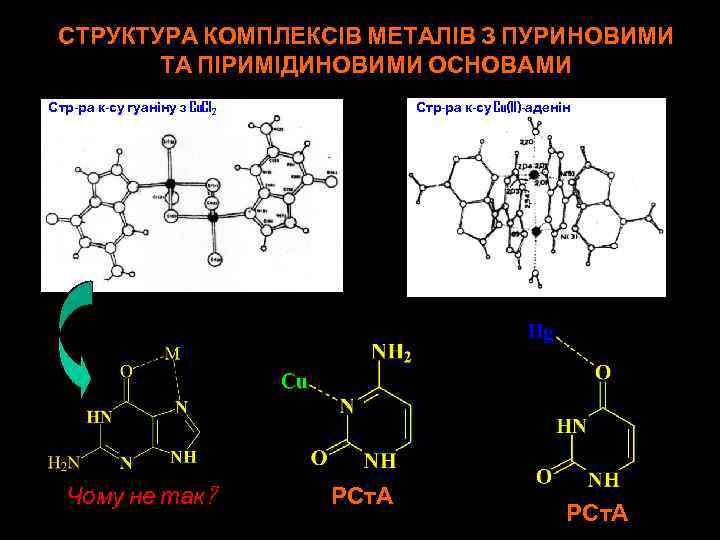
СТРУКТУРА КОМПЛЕКСІВ МЕТАЛІВ З ПУРИНОВИМИ ТА ПІРИМІДИНОВИМИ ОСНОВАМИ Стр-ра к-су гуаніну з Cu. Cl 2 Чому не так? Стр-ра к-су Cu(II)-аденін РСт. А

Зв’язування іонів металів з основами, що не приєднані до рибози не має безпосереднього біологічного інтересу, т. я. може приєднуватися до атомів N 9 пуринів та N 1 піримідинів, тоді як у нуклеозидах та нуклеотидах ці атоми не є донорами електронів
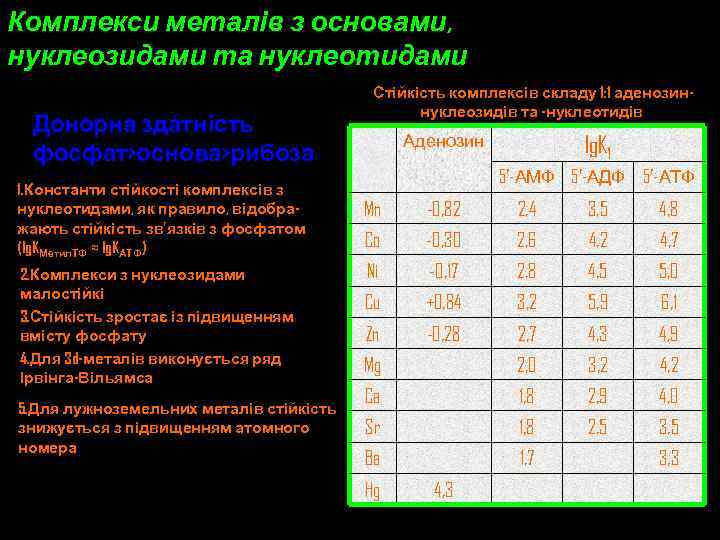
Комплекси металів з основами, нуклеозидами та нуклеотидами Донорна здатність фосфат>основа>рибоза 1. Константи стійкості комплексів з нуклеотидами, як правило, відображають стійкість зв’язків з фосфатом (lg. KМетил. ТФ ≈ lg. KАТФ) 2. Комплекси з нуклеозидами малостійкі 3. Стійкість зростає із підвищенням вмісту фосфату 4. Для 3 d-металів виконується ряд Ірвінга-Вільямса 5. Для лужноземельних металів стійкість знижується з підвищенням атомного номера Стійкість комплексів складу 1: 1 аденозиннуклеозидів та -нуклеотидів Аденозин lg. K 1 5’-АМФ 5’-АДФ 5’-АТФ Mn -0, 82 2, 4 3, 5 4, 8 Co -0, 30 2, 6 4, 2 4, 7 Ni -0, 17 2, 8 4, 5 5, 0 Cu +0, 84 3, 2 5, 9 6, 1 Zn -0, 28 2, 7 4, 3 4, 9 Mg 2, 0 3, 2 4, 2 Ca 1, 8 2, 9 4, 0 Sr 1, 8 2, 5 3, 5 Ba 1, 7 Hg 4, 3 3, 3

Комплекси металів з основами, нуклеозидами та нуклеотидами 1. Основи нуклеозидів за відносною стійкістю їх комплексів з 3 d-металами розміщуються як: G > A, C > U, T 2. Виключно висока стійкість комплексу ртуті з аденозином відображає суттєво більшу спорідненість основ до таких металів як ртуть і срібло в порівнянні з 3 d-металами. Відносна спорідненість основ до ртуті(ІІ) відповідає ряду T>C>A>G 3. Константи стійкості lg. K 1 комплексів срібла з аденозином, АМФ, АДФ, АТФ, ДНК рівні 3, 9, 4, 2, 4, 3, 4, 4, відповідно, що свідчить про відсутність звязування сріблом фосфатної групи.
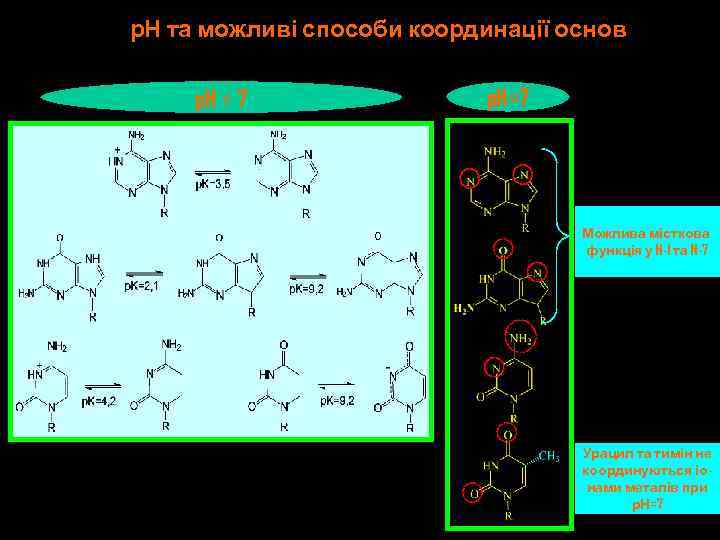
р. Н та можливі способи координації основ p. H ≠ 7 p. H=7 Можлива місткова функція у N-1 та N-7 Урацил та тимін не координуються іонами металів при р. Н=7
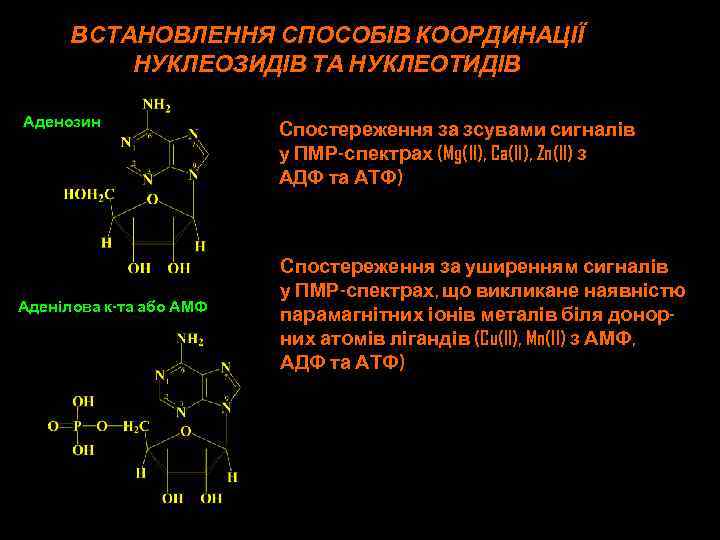
ВСТАНОВЛЕННЯ СПОСОБІВ КООРДИНАЦІЇ НУКЛЕОЗИДІВ ТА НУКЛЕОТИДІВ Аденозин Аденілова к-та або АМФ Спостереження за зсувами сигналів у ПМР-спектрах (Mg(II), Ca(II), Zn(II) з АДФ та АТФ) Спостереження за уширенням сигналів у ПМР-спектрах, що викликане наявністю парамагнітних іонів металів біля донорних атомів лігандів (Cu(II), Mn(II) з АМФ, АДФ та АТФ)
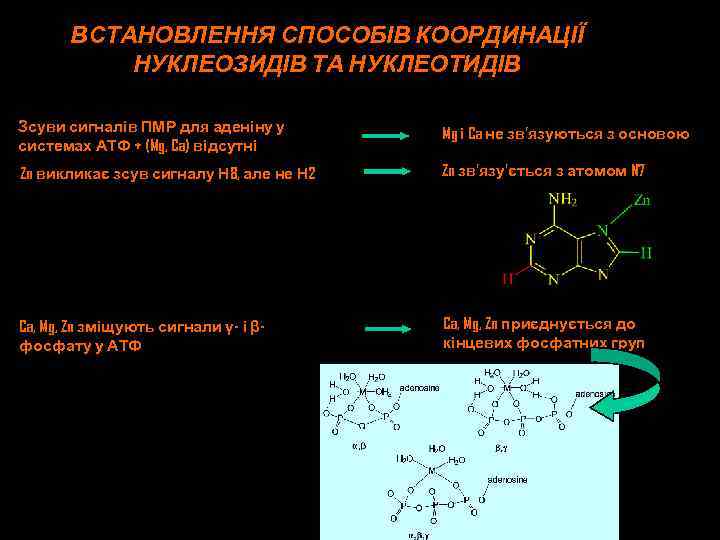
ВСТАНОВЛЕННЯ СПОСОБІВ КООРДИНАЦІЇ НУКЛЕОЗИДІВ ТА НУКЛЕОТИДІВ Зсуви сигналів ПМР для аденіну у системах АТФ + (Mg, Ca) відсутні Mg і Ca не зв’язуються з основою Zn викликає зсув сигналу Н 8, але не Н 2 Zn зв’язу’ється з атомом N 7 Ca, Mg, Zn зміщують сигнали γ- і βфосфату у АТФ Ca, Mg, Zn приєднується до кінцевих фосфатних груп
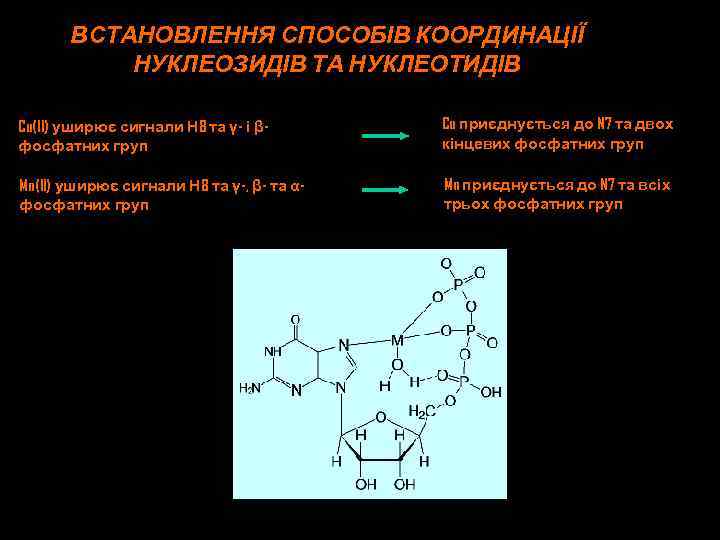
ВСТАНОВЛЕННЯ СПОСОБІВ КООРДИНАЦІЇ НУКЛЕОЗИДІВ ТА НУКЛЕОТИДІВ Cu(II) уширює сигнали Н 8 та γ- і βфосфатних груп Cu приєднується до N 7 та двох кінцевих фосфатних груп Mn(II) уширює сигнали Н 8 та γ-, β- та αфосфатних груп Mn приєднується до N 7 та всіх трьох фосфатних груп
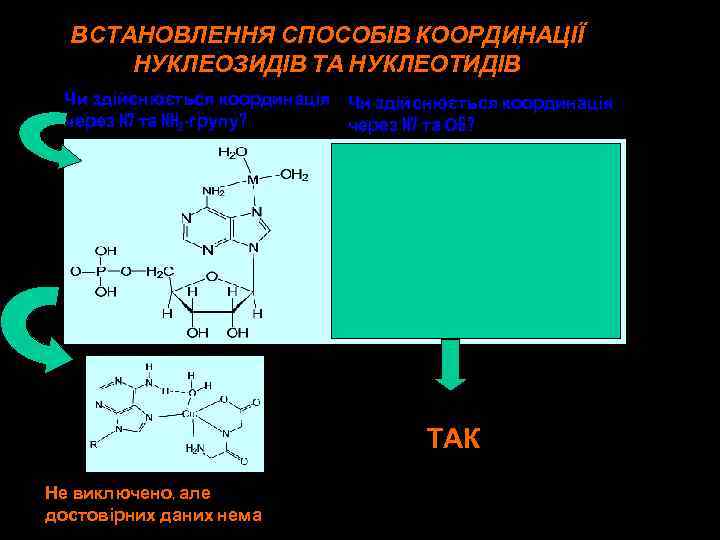
ВСТАНОВЛЕННЯ СПОСОБІВ КООРДИНАЦІЇ НУКЛЕОЗИДІВ ТА НУКЛЕОТИДІВ Чи здійснюється координація через N 7 та NH 2 -групу? через N 7 та О 6? ТАК Не виключено, але достовірних даних нема
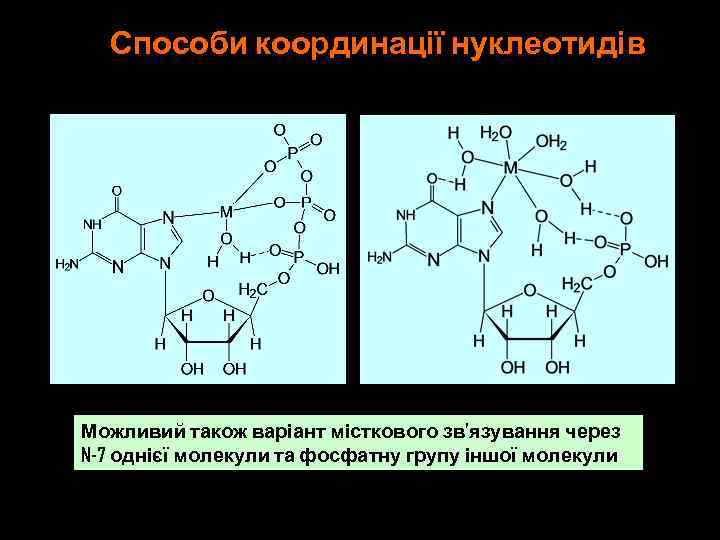
Способи координації нуклеотидів Можливий також варіант місткового зв’язування через N-7 однієї молекули та фосфатну групу іншої молекули
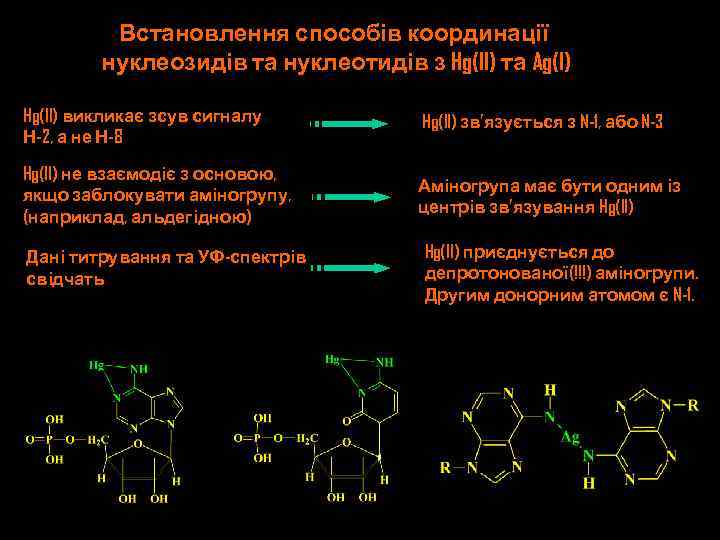
Встановлення способів координації нуклеозидів та нуклеотидів з Hg(II) та Ag(I) Hg(II) викликає зсув сигналу Н-2, а не Н-8 Hg(II) зв’язується з N-1, або N-3 Hg(II) не взаємодіє з основою, якщо заблокувати аміногрупу, (наприклад, альдегідною) Аміногрупа має бути одним із центрів зв’язування Hg(II) Дані титрування та УФ-спектрів свідчать Hg(II) приєднується до депротонованої(!!!) аміногрупи. Другим донорним атомом є N-1.
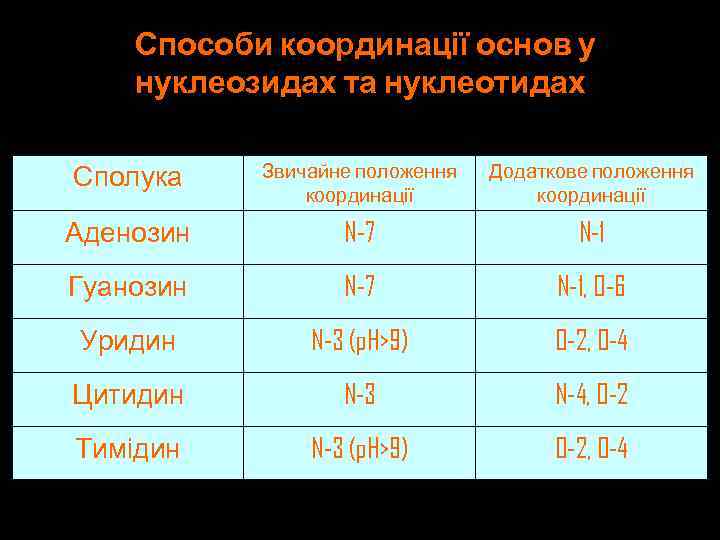
Способи координації основ у нуклеозидах та нуклеотидах Сполука Звичайне положення координації Додаткове положення координації Аденозин N-7 N-1 Гуанозин N-7 N-1, O-6 Уридин N-3 (p. H>9) O-2, O-4 Цитидин N-3 N-4, O-2 Тимідин N-3 (p. H>9) O-2, O-4
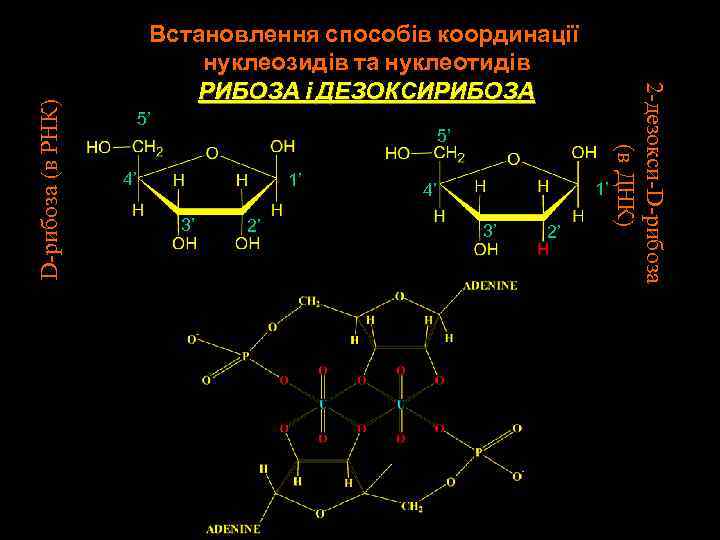
D-рибоза (в РНК) 5’ 5’ 4’ 1’ 3’ 2’ 1’ 4’ 3’ 2’ 2 -дезокси-D-рибоза (в ДНК) Встановлення способів координації нуклеозидів та нуклеотидів РИБОЗА і ДЕЗОКСИРИБОЗА
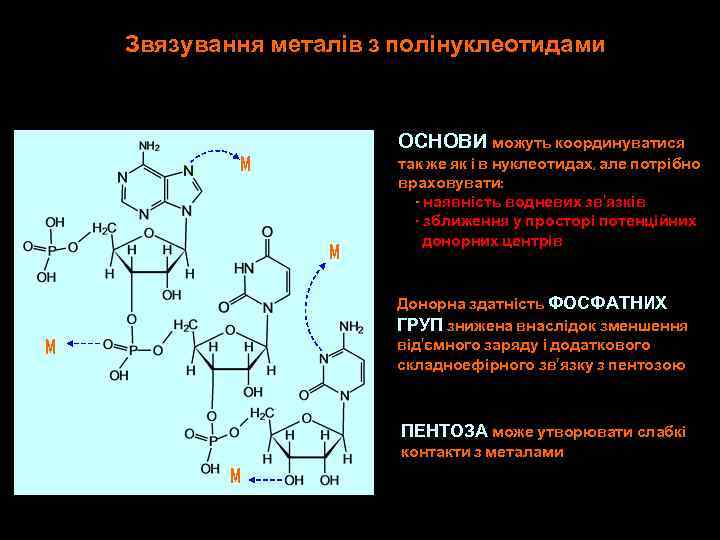
Звязування металів з полінуклеотидами ОСНОВИ можуть координуватися M M так же як і в нуклеотидах, але потрібно враховувати: - наявність водневих зв’язків - зближення у просторі потенційних донорних центрів Донорна здатність ФОСФАТНИХ ГРУП знижена внаслідок зменшення від’ємного заряду і додаткового складноефірного зв’язку з пентозою M ПЕНТОЗА може утворювати слабкі контакти з металами M

Комплексоутворення в системі Mn 2+ - поліаденілова кислота (великий надлишок) Зв’язування з основою 30% Mn 2+ зв’язані з N-7 13% Mn 2+ зв’язані з N-1 або N-3 Зв’язування з фосфатом Усі іони Mn 2+ зв’язані з фосфатними групами, причому існує три типи зв’язування 1. Mn 2+ зв’язаний з двома фосфатними групами 2. Mn 2+ зв’язаний з двома фосфатними групами та атомом азоту N-7 аденіну 3. Mn 2+ зв’язаний з двома фосфатними групами та атомом азоту N-3 або N-1 аденіну
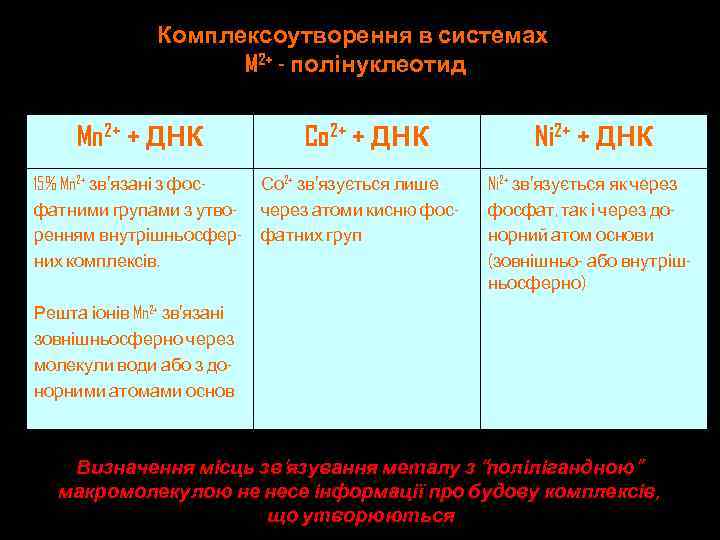
Комплексоутворення в системах M 2+ - полінуклеотид Mn 2+ + ДНК Co 2+ + ДНК 15% Mn 2+ зв’язані з фос. Со 2+ зв’язується лише фатними групами з утво- через атоми кисню фосренням внутрішньосфер- фатних груп них комплексів. Ni 2+ + ДНК Ni 2+ зв’язується як через фосфат, так і через донорний атом основи (зовнішньо- або внутрішньосферно) Решта іонів Mn 2+ зв’язані зовнішньосферно через молекули води або з донорними атомами основ Визначення місць зв’язування металу з “полілігандною” макромолекулою не несе інформації про будову комплексів, що утворюються

ВПЛИВ ІОНІВ МЕТАЛІВ НА СТРУКТУРУ ДНК 1. Стабілізація подвійної спіралі за рахунок утворення неспецифічних (електростатичні зв’язки за участю іонів лужних металів та магнію), або специфічних (утворення ковалентних зв’язків) контактів, що веде до нейтралізації негативних зарядів на подвійній спіралі. Відносна спорідненість до фосфату змінюється в ряду: Mg 2+ > Co 2+ > Ni 2+ > Mn 2+ > Zn 2+ > Cd 2+ > Cu 2+ > (Ag+ Hg 2+ Pb 2+) 2. Зв’язування з основами веде, як правило, до розриву водневих зв’вязків між комплементарними основами, що, в свою чергу, дестабілізує подвійну спіраль (зменшується Ттопл. ДНК) 3. Cu 2+ та Zn 2+ не приводять до незворотнього розкручування ДНК, утворюючи поперечні зв’язки (містки) у денатурованій ДНК. При створенні сприятливих умов (температура, концентрація електролітів) відбувається регенерація подвійної спіралі. Mg 2+ зв’язується з фосфатними групами, поперечних зв’язків не утворює і ренатурація денатурованої ДНК неможлива. 4. Hg 2+ та Ag+ зв’язуються з основами настільки міцно, що вони у стехіометричних кількостях розміщуються між ланцюгами подвійної спіралі, розривають водневі зв’язки N-H…N між основами і утворюють більш стабільний місток N-Ag(Hg)-N. 5. Висока спорідненість іонів важких металів до донорних атомів основ веде до мутагенезу, або до протипухлинних препаратів.
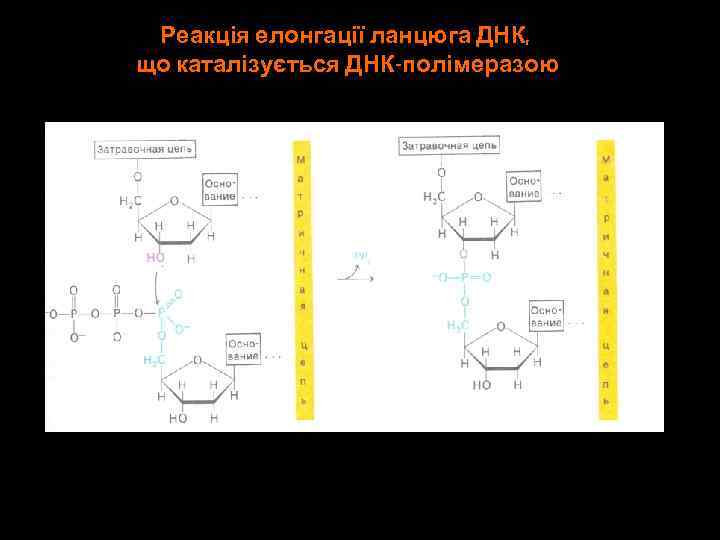
Реакція елонгації ланцюга ДНК, що каталізується ДНК-полімеразою
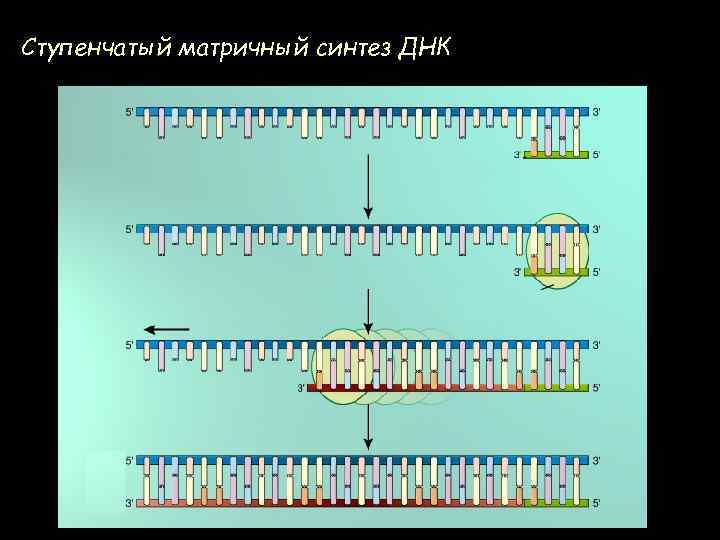
Ступенчатый матричный синтез ДНК
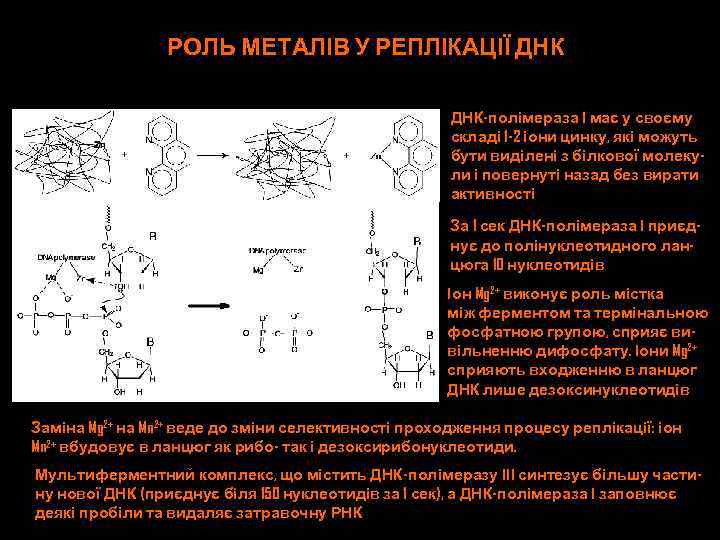
РОЛЬ МЕТАЛІВ У РЕПЛІКАЦІЇ ДНК-полімераза І має у своєму складі 1 -2 іони цинку, які можуть бути виділені з білкової молекули і повернуті назад без вирати активності За 1 сек ДНК-полімераза І приєднує до полінуклеотидного ланцюга 10 нуклеотидів Іон Mg 2+ виконує роль містка між ферментом та термінальною фосфатною групою, сприяє вивільненню дифосфату. Іони Mg 2+ сприяють входженню в ланцюг ДНК лише дезоксинуклеотидів Заміна Mg 2+ на Mn 2+ веде до зміни селективності проходження процесу реплікації: іон Mn 2+ вбудовує в ланцюг як рибо- так і дезоксирибонуклеотиди. Мультиферментний комплекс, що містить ДНК-полімеразу ІІІ синтезує більшу частину нової ДНК (приєднує біля 150 нуклеотидів за 1 сек), а ДНК-полімераза І заповнює деякі пробіли та видаляє затравочну РНК
ДНК-полимераза
ДНК-полимераза
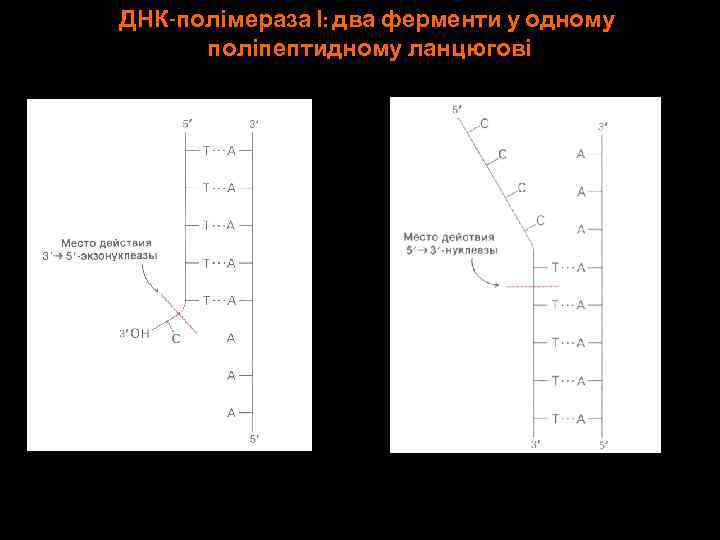
ДНК-полімераза І: два ферменти у одному поліпептидному ланцюгові
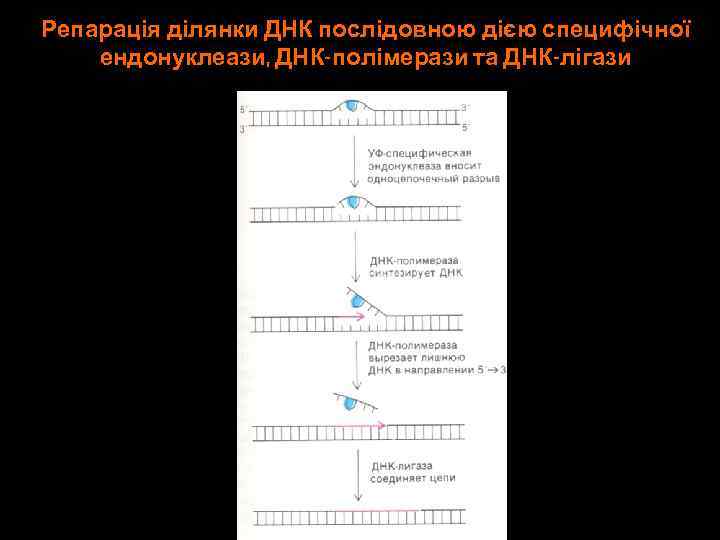
Репарація ділянки ДНК послідовною дією специфічної ендонуклеази, ДНК-полімерази та ДНК-лігази

Передача інформації в клітинах “Центральна догма” молекулярної біології Редуплікація Транскрипція ДНК м. РНК Трансляція Протеїн, лінійна послідовність амінокислот, кодується ДНК, лінійною послідовністю нуклеотидів

ТРАНСКРИПЦІЯ 1. Копіювання коду ДНК (синтез м. РНК) здійснюється за допомогою РНК-полімераз. Вони потребують ДНК як матрицю, рибонуклеозидтрифосфати та іони металів. РНК-полімераза із E. coli складається із 5 субодиниць (М = 500 000) і містить 2 іони цинку, що не виділяються при діалізі з хелатуючими лігандами Роль активатора у процесі транскрипції проявляють Mg 2+, Mn 2+, Co 2+: Mg 2+ сприяє вбудовуванню в полімерний ланцюг РНК рибонуклеотидів, а не дезоксирибонуклеотидів Mn 2+ та Co 2+ каталізують реакцію синтезу РНК набагато ефективніше, ніж Mg 2+, але вбудовують як рибонуклеотиди, так і дезоксирибонуклеотиди. Інші метали не ефективні при синтезі РНК
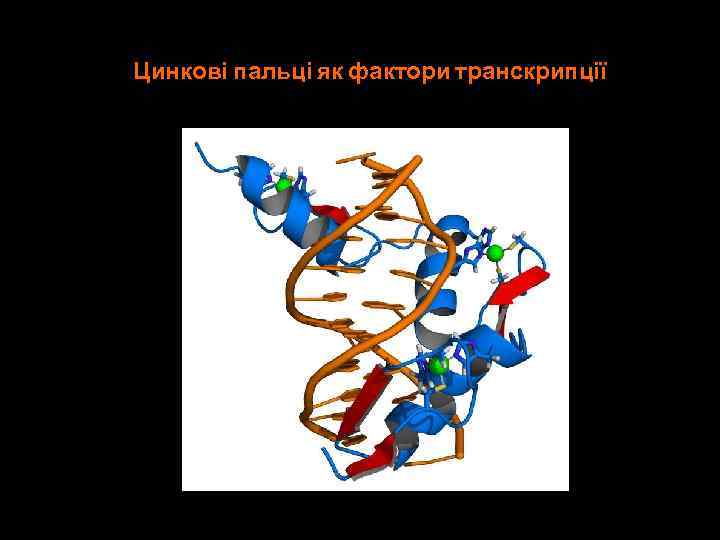
Цинкові пальці як фактори транскрипції
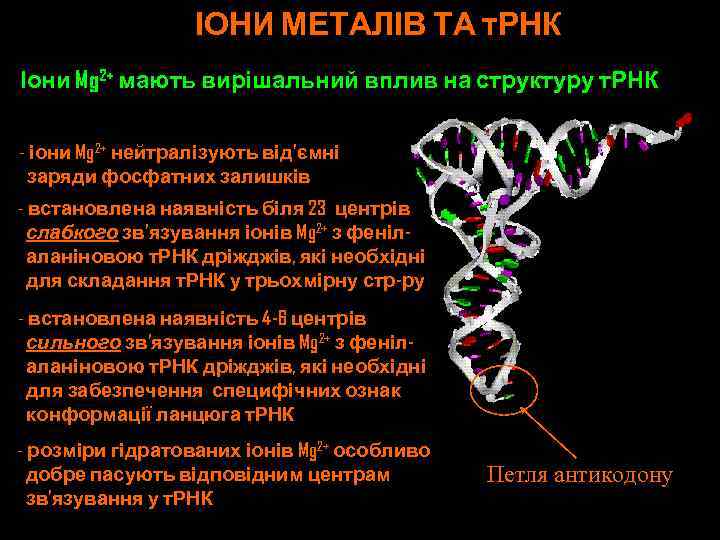
ІОНИ МЕТАЛІВ ТА т. РНК Іони Mg 2+ мають вирішальний вплив на структуру т. РНК - іони Mg 2+ нейтралізують від’ємні заряди фосфатних залишків - встановлена наявність біля 23 центрів слабкого зв’язування іонів Mg 2+ з фенілаланіновою т. РНК дріжджів, які необхідні для складання т. РНК у трьохмірну стр-ру - встановлена наявність 4 -6 центрів сильного зв’язування іонів Mg 2+ з фенілаланіновою т. РНК дріжджів, які необхідні для забезпечення специфічних ознак конформації ланцюга т. РНК - розміри гідратованих іонів Mg 2+ особливо добре пасують відповідним центрам зв’язування у т. РНК Петля антикодону
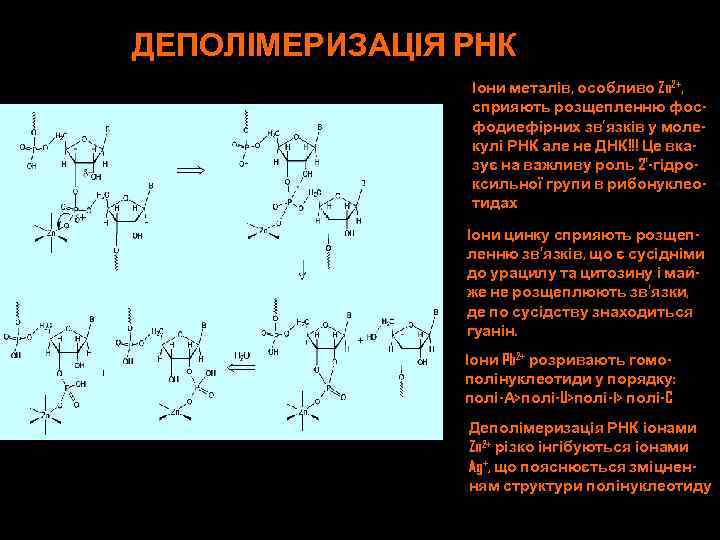
ДЕПОЛІМЕРИЗАЦІЯ РНК Іони металів, особливо Zn 2+, сприяють розщепленню фосфодиефірних зв’язків у молекулі РНК але не ДНК!!! Це вказує на важливу роль 2’-гідроксильної групи в рибонуклеотидах Іони цинку сприяють розщепленню зв’язків, що є сусідніми до урацилу та цитозину і майже не розщеплюють зв’язки, де по сусідству знаходиться гуанін. Іони Pb 2+ розривають гомополінуклеотиди у порядку: полі-А>полі-U>полі-І> полі-C Деполімеризація РНК іонами Zn 2+ різко інгібуються іонами Ag+, що пояснюється зміцненням структури полінуклеотиду
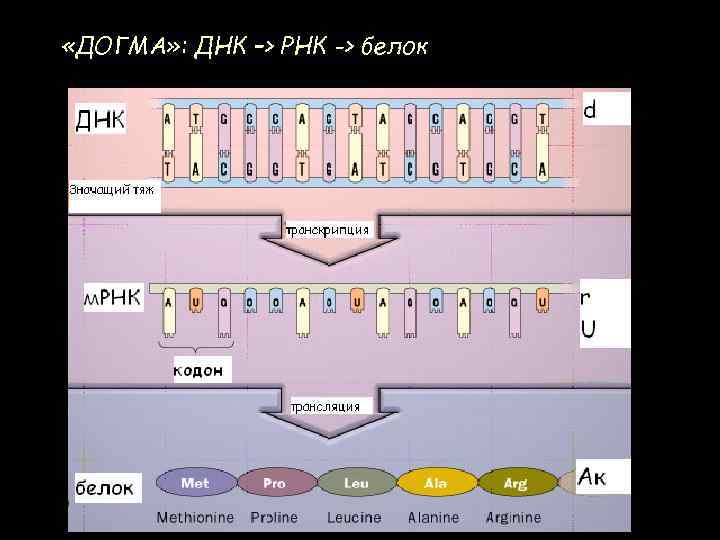
«ДОГМА» : ДНК –> РНК -> белок

ТРАНСЛЯЦИЯ – перевод генетической информации с «языка» последовательности нуклеотидов (м. РНК) на «язык» последовательности аминокислот (белок) В трансляции участвуют: - АРСаза - транспортная РНК т. РНК - матричная РНК м. РНК - рибосома (рибосомная РНК р. РНК)
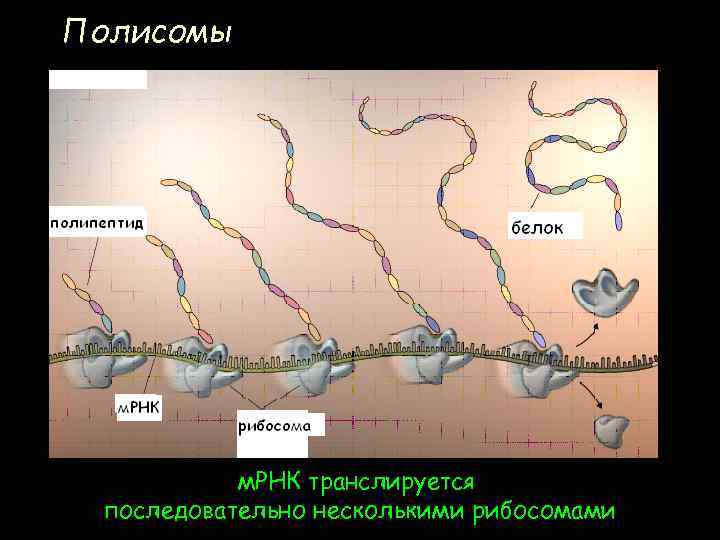
Полисомы м. РНК транслируется последовательно несколькими рибосомами
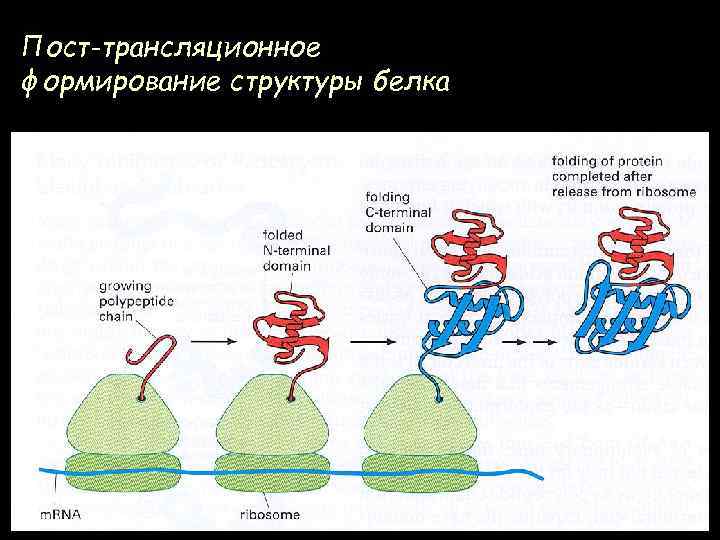
Пост-трансляционное формирование структуры белка

ТРАНСЛЯЦІЯ Синтез поліпептидних ланцюгів на рибосомах вимагає оптимальної концентрації іонів Mg 2+ (біля 10 м. М) При концентрації вищій за оптимальну у поліпептидний ланцюг можуть включатися помилкові амінокислоти
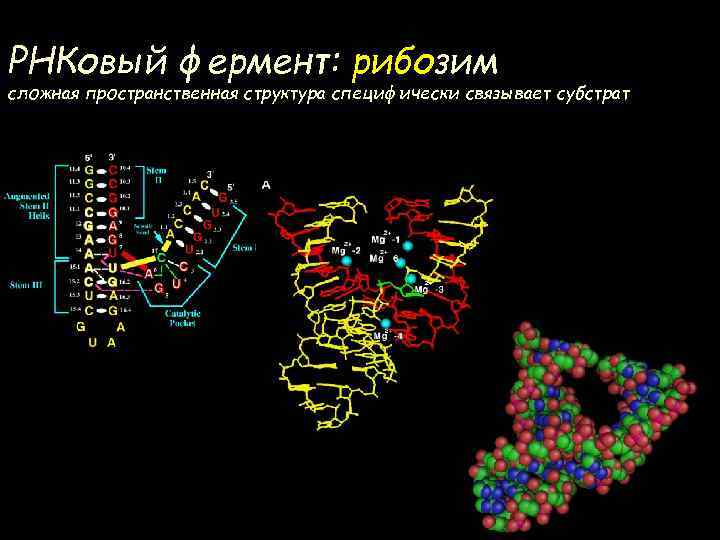
РНКовый фермент: рибозим сложная пространственная структура специфически связывает субстрат

РНК – фермент: рибозим Скорости превращения Спонтанно – 1 молекула/год Рибозим – 107 молекул/год Энзим - 1010 молекул/год

Функции нуклеиновых кислот ДНК 1. Активное хранение генетической информации. Организация вместе с белками структуры хромосом эукариот. 2. Передача генетической информации. Роль матрицы в синтезе ДНК и РНК – репликация и транскрипция. РНК 1. Передача генетической информации – транскрипция 2. Синтез полипептидных цепей белка: 3. Матрица в синтезе белка – м. РНК 4. Активация и транспорт аминокислот – т. РНК 5. Организация вместе с белками структуры рибосом – р. РНК 6. 3. Катализ - рибозимы

James Watson, reflecting on creativity “It’s necessary to be slightly underemployed if you are to do something significant”
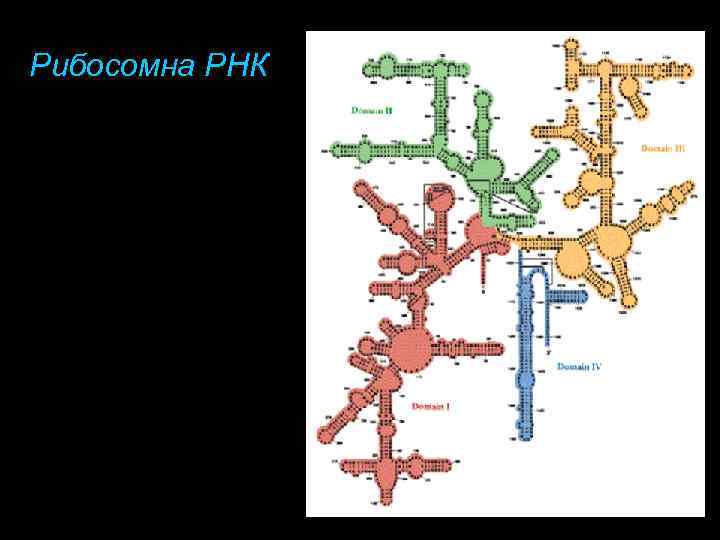
Рибосомна РНК
DNA & RNA L.ppt