Колоректальный рак - ПХТ.pptx
- Количество слайдов: 30
 Новые возможности в лечении колоректального рака таргентными препаратами докладчик: Мишина Ю. А. врач ХТО№ 2 ОБУЗ КОКОД 14. 04. 2017 Материал подготовлен при научной поддержке АО «БАЙЕР» L. RU. COM. SM. 03. 2016. 0284
Новые возможности в лечении колоректального рака таргентными препаратами докладчик: Мишина Ю. А. врач ХТО№ 2 ОБУЗ КОКОД 14. 04. 2017 Материал подготовлен при научной поддержке АО «БАЙЕР» L. RU. COM. SM. 03. 2016. 0284
 Эпидемиология колоректального рака q Колоректальный рак (КРР) - злокачественные новообразования толстого кишечника и прямой кишки q Колоректальный рак – третий по распространенности вид рака во всем мире у мужчин и второй у женщин рак легкого рак предстательной железы колоректальный рак молочной железы колоректальный рак легкого GLOBOCAN 2012 (IARC) , Section of Cancer Surveillance (10/11/2014) http: //globocan. iarc. fr/Pages/fact_sheets_cancer. aspx. L. RU. COM. SM. 03. 2016. 0284
Эпидемиология колоректального рака q Колоректальный рак (КРР) - злокачественные новообразования толстого кишечника и прямой кишки q Колоректальный рак – третий по распространенности вид рака во всем мире у мужчин и второй у женщин рак легкого рак предстательной железы колоректальный рак молочной железы колоректальный рак легкого GLOBOCAN 2012 (IARC) , Section of Cancer Surveillance (10/11/2014) http: //globocan. iarc. fr/Pages/fact_sheets_cancer. aspx. L. RU. COM. SM. 03. 2016. 0284
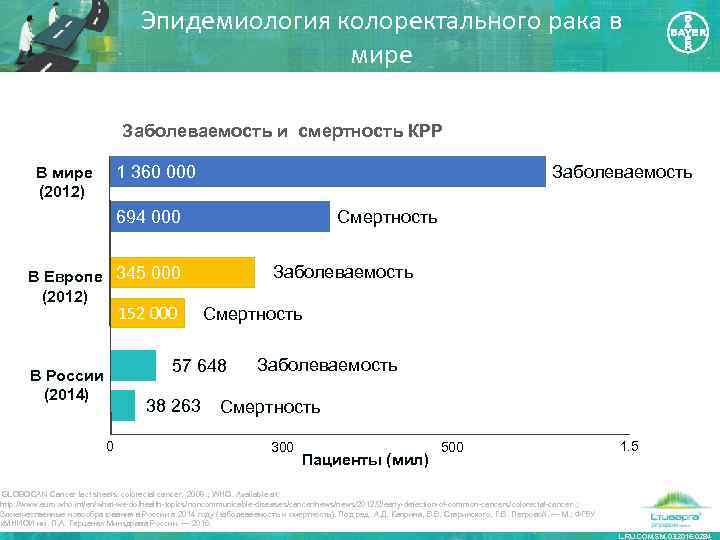 Эпидемиология колоректального рака в мире Заболеваемость и смертность КРР Заболеваемость 1 360 000 В мире (2012) 694 000 В Европе 345 000 (2012) 152 000 Смертность Заболеваемость Смертность 57 648 В России (2014) 38 263 0 Заболеваемость Смертность 300 Пациенты (мил) 500 1. 5 GLOBOCAN Cancer fact sheets: colorectal cancer. 2008. ; WHO. Available at: http: //www. euro. who. int/en/what-we-do/health-topics/noncommunicable-diseases/cancer/news/2012/2/early-detection-of-common-cancers/colorectal-cancer ; Злокачественные новообразования в России в 2014 году (заболеваемость и смертность). Под ред. А. Д. Каприна, В. В. Старинского, Г. В. Петровой. — М. : ФГБУ «МНИОИ им. П. А. Герцена» Минздрава России. — 2016. L. RU. COM. SM. 03. 2016. 0284
Эпидемиология колоректального рака в мире Заболеваемость и смертность КРР Заболеваемость 1 360 000 В мире (2012) 694 000 В Европе 345 000 (2012) 152 000 Смертность Заболеваемость Смертность 57 648 В России (2014) 38 263 0 Заболеваемость Смертность 300 Пациенты (мил) 500 1. 5 GLOBOCAN Cancer fact sheets: colorectal cancer. 2008. ; WHO. Available at: http: //www. euro. who. int/en/what-we-do/health-topics/noncommunicable-diseases/cancer/news/2012/2/early-detection-of-common-cancers/colorectal-cancer ; Злокачественные новообразования в России в 2014 году (заболеваемость и смертность). Под ред. А. Д. Каприна, В. В. Старинского, Г. В. Петровой. — М. : ФГБУ «МНИОИ им. П. А. Герцена» Минздрава России. — 2016. L. RU. COM. SM. 03. 2016. 0284
 Рекомендации по лечению колоректального рака Лекарственная терапия при неоперабельном колоректальном раке в настоящее время не вызывает сомнений Терапия КРР Гетерогенность течения заболевания: даже в случае значительного распространения процесса болезнь может протекать по-разному. Необходимы все активные препараты, при этом не имеет значения, за сколько линий терапии это будет сделано Непрерывный лечебный комплекс, в котором определение цели лечения является важной составляющей Руководство по химиотерапии опухолевых заболеваний / Под ред. Н. И. Переводчиковой, В. А. Горбуновой. 2015. – 688 с. ; Рациональная фармакотерапия в онкологии: руководство для практикующих врачей/ под ред. М. И. Давыдова, В. А. Горбуновой. 2015. – 844 с. ; Schmoll HJ, Van Cutsem E, Stein A, et al. ESMO consensus guidelines Ann Oncol. 2012; 23: 2479‐ 2516; E. Van Cutsem, A. Cervantes, B. Nordlingerб et al. Metastatic Colorectal Cancer: ESMO Clinical Practice Guidelines. Ann Oncol (2014) 25 (suppl 3): iii 1 -iii 9. L. RU. COM. SM. 03. 2016. 0284
Рекомендации по лечению колоректального рака Лекарственная терапия при неоперабельном колоректальном раке в настоящее время не вызывает сомнений Терапия КРР Гетерогенность течения заболевания: даже в случае значительного распространения процесса болезнь может протекать по-разному. Необходимы все активные препараты, при этом не имеет значения, за сколько линий терапии это будет сделано Непрерывный лечебный комплекс, в котором определение цели лечения является важной составляющей Руководство по химиотерапии опухолевых заболеваний / Под ред. Н. И. Переводчиковой, В. А. Горбуновой. 2015. – 688 с. ; Рациональная фармакотерапия в онкологии: руководство для практикующих врачей/ под ред. М. И. Давыдова, В. А. Горбуновой. 2015. – 844 с. ; Schmoll HJ, Van Cutsem E, Stein A, et al. ESMO consensus guidelines Ann Oncol. 2012; 23: 2479‐ 2516; E. Van Cutsem, A. Cervantes, B. Nordlingerб et al. Metastatic Colorectal Cancer: ESMO Clinical Practice Guidelines. Ann Oncol (2014) 25 (suppl 3): iii 1 -iii 9. L. RU. COM. SM. 03. 2016. 0284
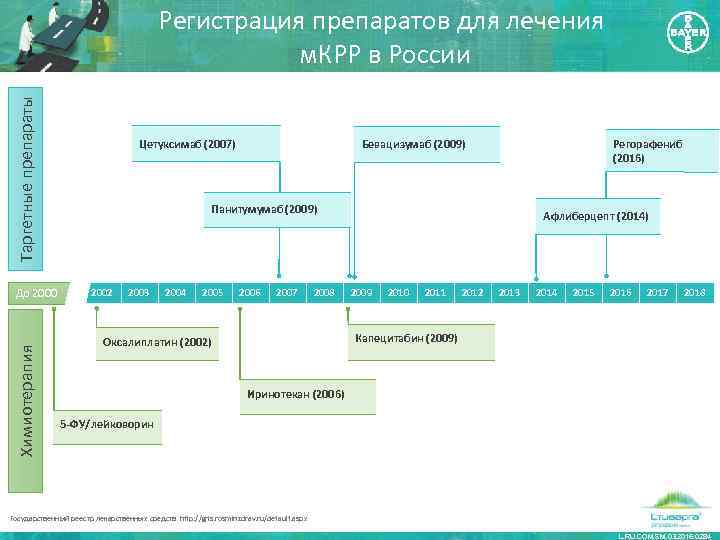 Таргетные препараты Регистрация препаратов для лечения м. КРР в России Химиотерапия До 2000 Регорафениб (2016) Бевацизумаб (2009) Цетуксимаб (2007) Панитумумаб (2009) 2002 2003 2004 2005 2006 2007 2008 Афлиберцепт (2014) 2009 2010 2011 2012 2013 2014 2015 2016 2017 2018 Капецитабин (2009) Оксалиплатин (2002) Иринотекан (2006) 5 -ФУ/лейковорин Государственный реестр лекарственных средств http: //grls. rosminzdrav. ru/default. aspx L. RU. COM. SM. 03. 2016. 0284
Таргетные препараты Регистрация препаратов для лечения м. КРР в России Химиотерапия До 2000 Регорафениб (2016) Бевацизумаб (2009) Цетуксимаб (2007) Панитумумаб (2009) 2002 2003 2004 2005 2006 2007 2008 Афлиберцепт (2014) 2009 2010 2011 2012 2013 2014 2015 2016 2017 2018 Капецитабин (2009) Оксалиплатин (2002) Иринотекан (2006) 5 -ФУ/лейковорин Государственный реестр лекарственных средств http: //grls. rosminzdrav. ru/default. aspx L. RU. COM. SM. 03. 2016. 0284
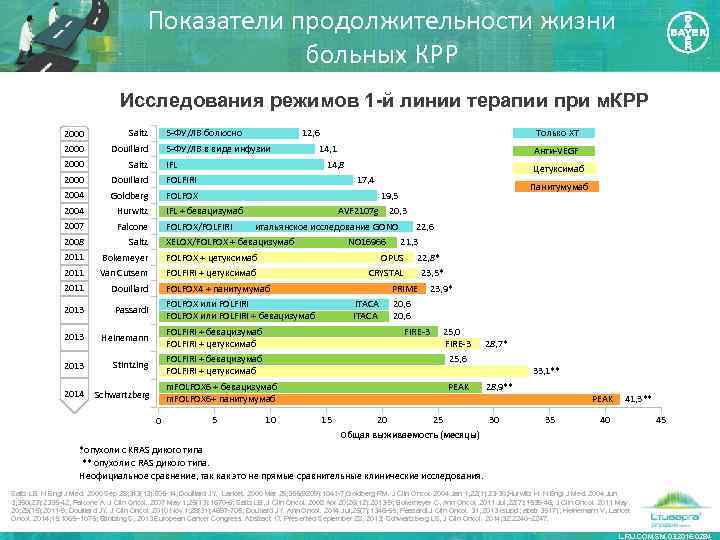 Показатели продолжительности жизни больных КРР Исследования режимов 1 -й линии терапии при м. КРР 5 -ФУ/ЛВ болюсно Только ХТ 2000 Saltz 12, 6 2000 Douillard 2000 Saltz 2000 Douillard FOLFIRI 2004 Goldberg FOLFOX 2004 Hurwitz IFL + бевацизумаб AVF 2107 g 2007 Falcone FOLFOX/FOLFIRI итальянское исследование GONO 2008 Saltz 2011 Bokemeyer FOLFOX + цетуксимаб OPUS 2011 Van Cutsem FOLFIRI + цетуксимаб CRYSTAL 2011 Douillard 2013 Passardi 2013 Heinemann 2013 Stintzing 2014 Schwartzberg 5 -ФУ/ЛВ в виде инфузии 14, 1 Анти-VEGF 14, 8 IFL Цетуксимаб 17, 4 Панитумумаб 19, 5 XELOX/FOLFOX + бевацизумаб NO 16966 20, 3 22, 6 21, 3 22, 8* FOLFOX 4 + панитумумаб PRIME FOLFOX или FOLFIRI ITACA FOLFOX или FOLFIRI + бевацизумаб ITACA 23, 5* 23, 9* 20, 6 FOLFIRI + бевацизумаб FIRE-3 25, 0 FOLFIRI + цетуксимаб FIRE-3 28, 7* 25, 6 FOLFIRI + бевацизумаб FOLFIRI + цетуксимаб 33, 1** m. FOLFOX 6 + бевацизумаб PEAK 28, 9** m. FOLFOX 6+ панитумумаб PEAK 0 5 10 15 20 25 30 35 41, 3** 40 45 Общая выживаемость (месяцы) *опухоли с KRAS дикого типа ** опухоли с RAS дикого типа. Неофициальное сравнение, так как это не прямые сравнительные клинические исследования. Saltz LB. N Engl J Med. 2000 Sep 28; 343(13): 905 -14; Douillard JY. Lancet. 2000 Mar 25; 355(9209): 1041 -7; Goldberg RM. J Clin Oncol. 2004 Jan 1; 22(1): 23 -30; Hurwitz H. N Engl J Med. 2004 Jun 3; 350(23): 2335 -42; Falcone A. J Clin Oncol. 2007 May 1; 25(13): 1670 -6; Saltz LB, J Clin Oncol. 2008 Apr 20; 26(12): 2013 -9; Bokemeyer C, Ann Oncol. 2011 Jul; 22(7): 1535 -46; J Clin Oncol. 2011 May 20; 29(15): 2011 -9; Douillard JY. J Clin Oncol. 2010 Nov 1; 28(31): 4697 -705; Douillard JY. Ann Oncol. 2014 Jul; 25(7): 1346 -55; Passardi. J Clin Oncol. 31, 2013 (suppl; abstr 3517); Heinemann V, Lancet Oncol. 2014; 15: 1065– 1075; Stintzing S, 2013 European Cancer Congress. Abstract 17. Presented September 28, 2013; Schwartzberg LS, J Clin Oncol. 2014; 32: 2240– 2247. L. RU. COM. SM. 03. 2016. 0284
Показатели продолжительности жизни больных КРР Исследования режимов 1 -й линии терапии при м. КРР 5 -ФУ/ЛВ болюсно Только ХТ 2000 Saltz 12, 6 2000 Douillard 2000 Saltz 2000 Douillard FOLFIRI 2004 Goldberg FOLFOX 2004 Hurwitz IFL + бевацизумаб AVF 2107 g 2007 Falcone FOLFOX/FOLFIRI итальянское исследование GONO 2008 Saltz 2011 Bokemeyer FOLFOX + цетуксимаб OPUS 2011 Van Cutsem FOLFIRI + цетуксимаб CRYSTAL 2011 Douillard 2013 Passardi 2013 Heinemann 2013 Stintzing 2014 Schwartzberg 5 -ФУ/ЛВ в виде инфузии 14, 1 Анти-VEGF 14, 8 IFL Цетуксимаб 17, 4 Панитумумаб 19, 5 XELOX/FOLFOX + бевацизумаб NO 16966 20, 3 22, 6 21, 3 22, 8* FOLFOX 4 + панитумумаб PRIME FOLFOX или FOLFIRI ITACA FOLFOX или FOLFIRI + бевацизумаб ITACA 23, 5* 23, 9* 20, 6 FOLFIRI + бевацизумаб FIRE-3 25, 0 FOLFIRI + цетуксимаб FIRE-3 28, 7* 25, 6 FOLFIRI + бевацизумаб FOLFIRI + цетуксимаб 33, 1** m. FOLFOX 6 + бевацизумаб PEAK 28, 9** m. FOLFOX 6+ панитумумаб PEAK 0 5 10 15 20 25 30 35 41, 3** 40 45 Общая выживаемость (месяцы) *опухоли с KRAS дикого типа ** опухоли с RAS дикого типа. Неофициальное сравнение, так как это не прямые сравнительные клинические исследования. Saltz LB. N Engl J Med. 2000 Sep 28; 343(13): 905 -14; Douillard JY. Lancet. 2000 Mar 25; 355(9209): 1041 -7; Goldberg RM. J Clin Oncol. 2004 Jan 1; 22(1): 23 -30; Hurwitz H. N Engl J Med. 2004 Jun 3; 350(23): 2335 -42; Falcone A. J Clin Oncol. 2007 May 1; 25(13): 1670 -6; Saltz LB, J Clin Oncol. 2008 Apr 20; 26(12): 2013 -9; Bokemeyer C, Ann Oncol. 2011 Jul; 22(7): 1535 -46; J Clin Oncol. 2011 May 20; 29(15): 2011 -9; Douillard JY. J Clin Oncol. 2010 Nov 1; 28(31): 4697 -705; Douillard JY. Ann Oncol. 2014 Jul; 25(7): 1346 -55; Passardi. J Clin Oncol. 31, 2013 (suppl; abstr 3517); Heinemann V, Lancet Oncol. 2014; 15: 1065– 1075; Stintzing S, 2013 European Cancer Congress. Abstract 17. Presented September 28, 2013; Schwartzberg LS, J Clin Oncol. 2014; 32: 2240– 2247. L. RU. COM. SM. 03. 2016. 0284
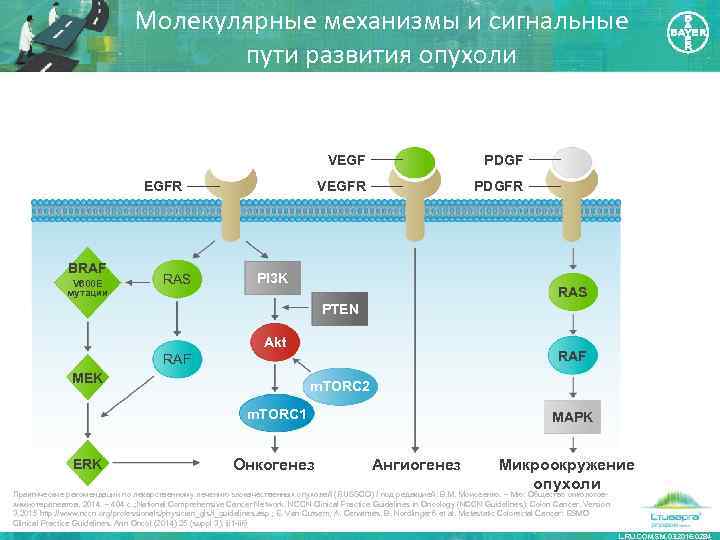 Молекулярные механизмы и сигнальные пути развития опухоли VEGFR BRAF V 600 E мутации RAS PDGFR PI 3 K RAS PTEN Akt RAF MEK m. TORC 2 m. TORC 1 ERK Онкогенез MAPK Ангиогенез Микроокружение опухоли Практические рекомендации по лекарственному лечению злокачественных опухолей (RUSSCO) / под редакцией: В. М. Моисеенко. – Мю: Общество онкологовхимиотерапевтов, 2014. – 404 с. ; National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Colon Cancer. Version 3. 2015 http: //www. nccn. org/professionals/physician_gls/f_guidelines. asp ; E. Van Cutsem, A. Cervantes, B. Nordlinger б et al. Metastatic Colorectal Cancer: ESMO Clinical Practice Guidelines. Ann Oncol (2014) 25 (suppl 3): iii 1 -iii 9 L. RU. COM. SM. 03. 2016. 0284
Молекулярные механизмы и сигнальные пути развития опухоли VEGFR BRAF V 600 E мутации RAS PDGFR PI 3 K RAS PTEN Akt RAF MEK m. TORC 2 m. TORC 1 ERK Онкогенез MAPK Ангиогенез Микроокружение опухоли Практические рекомендации по лекарственному лечению злокачественных опухолей (RUSSCO) / под редакцией: В. М. Моисеенко. – Мю: Общество онкологовхимиотерапевтов, 2014. – 404 с. ; National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Colon Cancer. Version 3. 2015 http: //www. nccn. org/professionals/physician_gls/f_guidelines. asp ; E. Van Cutsem, A. Cervantes, B. Nordlinger б et al. Metastatic Colorectal Cancer: ESMO Clinical Practice Guidelines. Ann Oncol (2014) 25 (suppl 3): iii 1 -iii 9 L. RU. COM. SM. 03. 2016. 0284
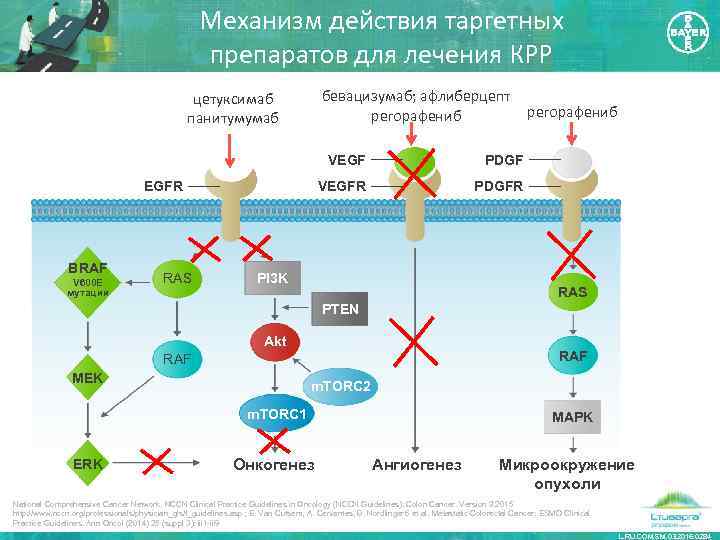 Механизм действия таргетных препаратов для лечения КРР бевацизумаб; афлиберцепт регорафениб цетуксимаб панитумумаб VEGF BRAF V 600 E мутации RAS PDGF VEGFR регорафениб PDGFR PI 3 K RAS PTEN Akt RAF MEK m. TORC 2 m. TORC 1 ERK Онкогенез MAPK Ангиогенез Микроокружение опухоли National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Colon Cancer. Version 3. 2015 http: //www. nccn. org/professionals/physician_gls/f_guidelines. asp ; E. Van Cutsem, A. Cervantes, B. Nordlinger б et al. Metastatic Colorectal Cancer: ESMO Clinical Practice Guidelines. Ann Oncol (2014) 25 (suppl 3): iii 1 -iii 9 L. RU. COM. SM. 03. 2016. 0284
Механизм действия таргетных препаратов для лечения КРР бевацизумаб; афлиберцепт регорафениб цетуксимаб панитумумаб VEGF BRAF V 600 E мутации RAS PDGF VEGFR регорафениб PDGFR PI 3 K RAS PTEN Akt RAF MEK m. TORC 2 m. TORC 1 ERK Онкогенез MAPK Ангиогенез Микроокружение опухоли National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Colon Cancer. Version 3. 2015 http: //www. nccn. org/professionals/physician_gls/f_guidelines. asp ; E. Van Cutsem, A. Cervantes, B. Nordlinger б et al. Metastatic Colorectal Cancer: ESMO Clinical Practice Guidelines. Ann Oncol (2014) 25 (suppl 3): iii 1 -iii 9 L. RU. COM. SM. 03. 2016. 0284
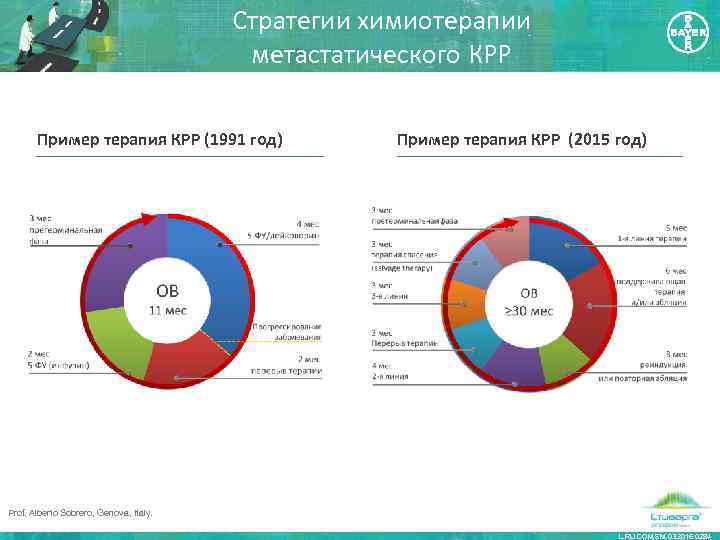 Стратегии химиотерапии метастатического КРР Пример терапия КРР (1991 год) Пример терапия КРР (2015 год) Prof. Alberto Sobrero, Genova, Italy. L. RU. COM. SM. 03. 2016. 0284
Стратегии химиотерапии метастатического КРР Пример терапия КРР (1991 год) Пример терапия КРР (2015 год) Prof. Alberto Sobrero, Genova, Italy. L. RU. COM. SM. 03. 2016. 0284
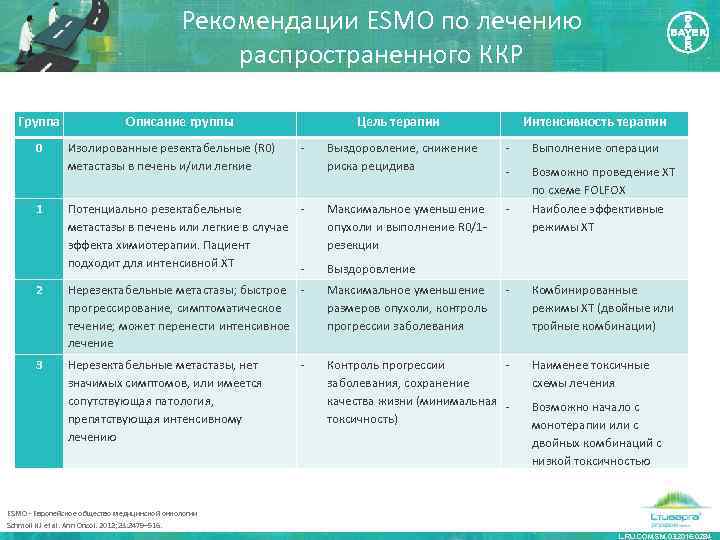 Рекомендации ESMO по лечению распространенного ККР Группа 0 Описание группы Интенсивность терапии Выздоровление, снижение риска рецидива Выполнение операции Потенциально резектабельные метастазы в печень или легкие в случае эффекта химиотерапии. Пациент подходит для интенсивной ХТ Максимальное уменьшение опухоли и выполнение R 0/1 резекции Возможно проведение ХТ по схеме FOLFOX Наиболее эффективные режимы ХТ 2 Нерезектабельные метастазы; быстрое прогрессирование, симптоматическое течение; может перенести интенсивное лечение Максимальное уменьшение размеров опухоли, контроль прогрессии заболевания 3 Нерезектабельные метастазы, нет значимых симптомов, или имеется сопутствующая патология, препятствующая интенсивному лечению Контроль прогрессии заболевания, сохранение качества жизни (минимальная токсичность) 1 Изолированные резектабельные (R 0) метастазы в печень и/или легкие Цель терапии Выздоровление Комбинированные режимы ХТ (двойные или тройные комбинации) Наименее токсичные схемы лечения Возможно начало с монотерапии или с двойных комбинаций с низкой токсичностью ESMO - Европейское общество медицинской онкологии Schmoll HJ et al. Ann Oncol. 2012; 23: 2479– 516. L. RU. COM. SM. 03. 2016. 0284
Рекомендации ESMO по лечению распространенного ККР Группа 0 Описание группы Интенсивность терапии Выздоровление, снижение риска рецидива Выполнение операции Потенциально резектабельные метастазы в печень или легкие в случае эффекта химиотерапии. Пациент подходит для интенсивной ХТ Максимальное уменьшение опухоли и выполнение R 0/1 резекции Возможно проведение ХТ по схеме FOLFOX Наиболее эффективные режимы ХТ 2 Нерезектабельные метастазы; быстрое прогрессирование, симптоматическое течение; может перенести интенсивное лечение Максимальное уменьшение размеров опухоли, контроль прогрессии заболевания 3 Нерезектабельные метастазы, нет значимых симптомов, или имеется сопутствующая патология, препятствующая интенсивному лечению Контроль прогрессии заболевания, сохранение качества жизни (минимальная токсичность) 1 Изолированные резектабельные (R 0) метастазы в печень и/или легкие Цель терапии Выздоровление Комбинированные режимы ХТ (двойные или тройные комбинации) Наименее токсичные схемы лечения Возможно начало с монотерапии или с двойных комбинаций с низкой токсичностью ESMO - Европейское общество медицинской онкологии Schmoll HJ et al. Ann Oncol. 2012; 23: 2479– 516. L. RU. COM. SM. 03. 2016. 0284
 Схема выбора терапии 1 и 2 -й линии согласно клинической группе по рекомендациям ESMO 1 -я линия терапии Группа 0 Изолированные резектабельные (R 0) метастазы в печень и/или легкие Группа 1 Потенциально резектабельные Наиболее эффективные режимы ХТ Группа 2 Симптоматическое течение Режимы ХТ средней интенсивности Группа 3 Множественные метастазы, нет значимых симптомов, нет риска быстрого ухудшения состояния Щадящие режимы ХТ 2 -я линия терапии Согласно рекомендациям – отсутствие системной ХТ или ХТ по схеме FOLFOX KRAS дикий тип • двойная комбинация ХТ ± цетуксимаб/панитумумаб • двойная комбинация ХТ ± бевацизумаб • тройная комбинация ХТ KRAS мутации • двойная комбинация ХТ ± бевацизумаб • тройная комбинация ХТ • • 5 -ФУ капецитабин± бевацизумаб • Режимы на основе иринотекана ± бевацизумаб при резистентности к оксалиплантину • Режимы на основе оксалиплатина± бевацизумаб при резистентности к иринотекану Рефрактерные к ХТ пациенты с KRAS дикого типа: • Режимы на основе иринотекана ± цетуксимаб или панитумумаб при резистентности к оксалиплантину • Режимы на основе оксалиплатина± цетуксимаб или панитумумаб при резистентности к иринотекану ХТ – химиотерапия; двойная комбинация ХТ – схемы FOLFOX, FOLFIRI, XELOX, XELIRI R 0 = in sano (полное удаление очага), R 1 = возможная микроскопическая остаточная опухоль, R 2 = макро/микроскопическая остаточная опухоль. ESMO - Европейское общество медицинской онкологии Schmoll HJ et al. Ann Oncol. 2012; 23: 2479– 516. L. RU. COM. SM. 03. 2016. 0284
Схема выбора терапии 1 и 2 -й линии согласно клинической группе по рекомендациям ESMO 1 -я линия терапии Группа 0 Изолированные резектабельные (R 0) метастазы в печень и/или легкие Группа 1 Потенциально резектабельные Наиболее эффективные режимы ХТ Группа 2 Симптоматическое течение Режимы ХТ средней интенсивности Группа 3 Множественные метастазы, нет значимых симптомов, нет риска быстрого ухудшения состояния Щадящие режимы ХТ 2 -я линия терапии Согласно рекомендациям – отсутствие системной ХТ или ХТ по схеме FOLFOX KRAS дикий тип • двойная комбинация ХТ ± цетуксимаб/панитумумаб • двойная комбинация ХТ ± бевацизумаб • тройная комбинация ХТ KRAS мутации • двойная комбинация ХТ ± бевацизумаб • тройная комбинация ХТ • • 5 -ФУ капецитабин± бевацизумаб • Режимы на основе иринотекана ± бевацизумаб при резистентности к оксалиплантину • Режимы на основе оксалиплатина± бевацизумаб при резистентности к иринотекану Рефрактерные к ХТ пациенты с KRAS дикого типа: • Режимы на основе иринотекана ± цетуксимаб или панитумумаб при резистентности к оксалиплантину • Режимы на основе оксалиплатина± цетуксимаб или панитумумаб при резистентности к иринотекану ХТ – химиотерапия; двойная комбинация ХТ – схемы FOLFOX, FOLFIRI, XELOX, XELIRI R 0 = in sano (полное удаление очага), R 1 = возможная микроскопическая остаточная опухоль, R 2 = макро/микроскопическая остаточная опухоль. ESMO - Европейское общество медицинской онкологии Schmoll HJ et al. Ann Oncol. 2012; 23: 2479– 516. L. RU. COM. SM. 03. 2016. 0284
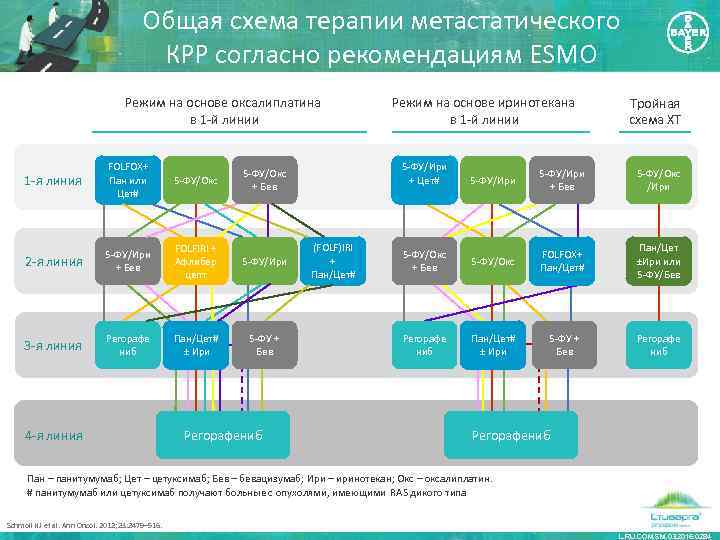 Общая схема терапии метастатического КРР согласно рекомендациям ESMO Режим на основе оксалиплатина в 1 -й линии 1 -я линия FOLFOX+ Пан или Цет# 5 -ФУ/Окс 2 -я линия 5 -ФУ/Ири + Бев FOLFIRI + Афлибер цепт 5 -ФУ/Ири 3 -я линия Регорафе ниб Пан/Цет# ± Ири 5 -ФУ + Бев 4 -я линия 5 -ФУ/Ири + Цет# 5 -ФУ/Окс + Бев Регорафениб Режим на основе иринотекана в 1 -й линии (FOLF)IRI + Пан/Цет# Тройная схема ХТ 5 -ФУ/Ири + Бев 5 -ФУ/Окс /Ири 5 -ФУ/Окс + Бев 5 -ФУ/Окс FOLFOX+ Пан/Цет# Пан/Цет ±Ири или 5 -ФУ/Бев Регорафе ниб Пан/Цет# ± Ири 5 -ФУ + Бев Регорафе ниб Регорафениб Пан – панитумумаб; Цет – цетуксимаб; Бев – бевацизумаб; Ири – иринотекан; Окс – оксалиплатин. # панитумумаб или цетуксимаб получают больные с опухолями, имеющими RAS дикого типа Schmoll HJ et al. Ann Oncol. 2012; 23: 2479– 516. L. RU. COM. SM. 03. 2016. 0284
Общая схема терапии метастатического КРР согласно рекомендациям ESMO Режим на основе оксалиплатина в 1 -й линии 1 -я линия FOLFOX+ Пан или Цет# 5 -ФУ/Окс 2 -я линия 5 -ФУ/Ири + Бев FOLFIRI + Афлибер цепт 5 -ФУ/Ири 3 -я линия Регорафе ниб Пан/Цет# ± Ири 5 -ФУ + Бев 4 -я линия 5 -ФУ/Ири + Цет# 5 -ФУ/Окс + Бев Регорафениб Режим на основе иринотекана в 1 -й линии (FOLF)IRI + Пан/Цет# Тройная схема ХТ 5 -ФУ/Ири + Бев 5 -ФУ/Окс /Ири 5 -ФУ/Окс + Бев 5 -ФУ/Окс FOLFOX+ Пан/Цет# Пан/Цет ±Ири или 5 -ФУ/Бев Регорафе ниб Пан/Цет# ± Ири 5 -ФУ + Бев Регорафе ниб Регорафениб Пан – панитумумаб; Цет – цетуксимаб; Бев – бевацизумаб; Ири – иринотекан; Окс – оксалиплатин. # панитумумаб или цетуксимаб получают больные с опухолями, имеющими RAS дикого типа Schmoll HJ et al. Ann Oncol. 2012; 23: 2479– 516. L. RU. COM. SM. 03. 2016. 0284
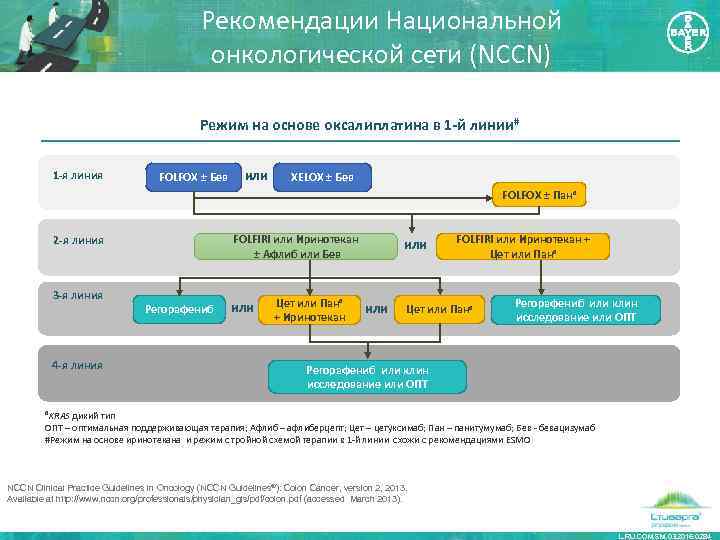 Рекомендации Национальной онкологической сети (NCCN) Режим на основе оксалиплатина в 1 -й линии# 1 -я линия FOLFOX ± Бев или XELOX ± Бев FOLFOX ± Панa FOLFIRI или Иринотекан ± Афлиб или Бев 2 -я линия 3 -я линия 4 -я линия Регорафениб или Цет или Панa + Иринотекан или FOLFIRI или Иринотекан + Цет или Панa Регорафениб или клин исследование или ОПТ a. KRAS дикий тип ОПТ – оптимальная поддерживающая терапия; Афлиб – афлиберцепт; Цет – цетуксимаб; Пан – панитумумаб; Бев - бевацизумаб #Режим на основе иринотекана и режим с тройной схемой терапии в 1 -й линии схожи с рекомендациями ESMO NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®): Colon Cancer, version 2, 2013. Available at http: //www. nccn. org/professionals/physician_gls/pdf/colon. pdf (accessed March 2013). L. RU. COM. SM. 03. 2016. 0284
Рекомендации Национальной онкологической сети (NCCN) Режим на основе оксалиплатина в 1 -й линии# 1 -я линия FOLFOX ± Бев или XELOX ± Бев FOLFOX ± Панa FOLFIRI или Иринотекан ± Афлиб или Бев 2 -я линия 3 -я линия 4 -я линия Регорафениб или Цет или Панa + Иринотекан или FOLFIRI или Иринотекан + Цет или Панa Регорафениб или клин исследование или ОПТ a. KRAS дикий тип ОПТ – оптимальная поддерживающая терапия; Афлиб – афлиберцепт; Цет – цетуксимаб; Пан – панитумумаб; Бев - бевацизумаб #Режим на основе иринотекана и режим с тройной схемой терапии в 1 -й линии схожи с рекомендациями ESMO NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®): Colon Cancer, version 2, 2013. Available at http: //www. nccn. org/professionals/physician_gls/pdf/colon. pdf (accessed March 2013). L. RU. COM. SM. 03. 2016. 0284
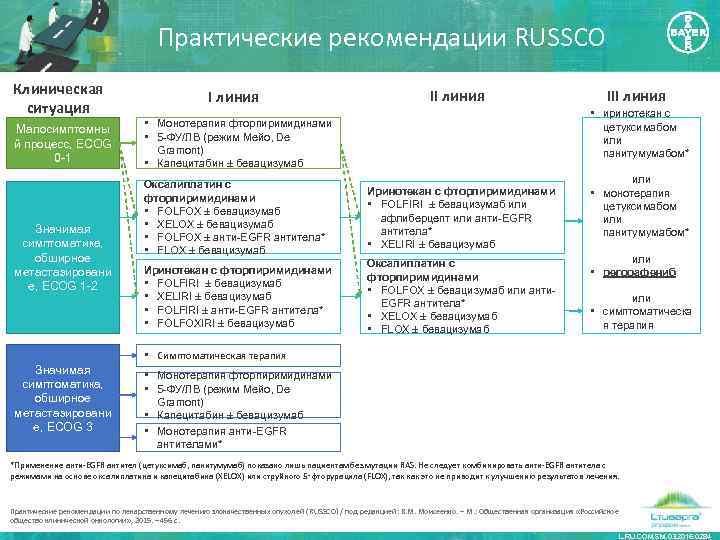 Практические рекомендации RUSSCO Клиническая ситуация Малосимптомны й процесс, ECOG 0 -1 Значимая симптоматика, обширное метастазировани е, ECOG 1 -2 I линия II линия III линия • иринотекан с цетуксимабом или панитумумабом* • Монотерапия фторпиримидинами • 5 -ФУ/ЛВ (режим Мейо, De Gramont) • Капецитабин ± бевацизумаб Оксалиплатин с фторпиримидинами • FOLFOX ± бевацизумаб • XELOX ± бевацизумаб • FOLFOX ± анти-EGFR антитела* • FLOX ± бевацизумаб Иринотекан с фторпиримидинами • FOLFIRI ± бевацизумаб или афлиберцепт или анти-EGFR антитела* • XELIRI ± бевацизумаб Иринотекан с фторпиримидинами • FOLFIRI ± бевацизумаб • XELIRI ± бевацизумаб • FOLFIRI ± анти-EGFR антитела* • FOLFOXIRI ± бевацизумаб Оксалиплатин с фторпиримидинами • FOLFOX ± бевацизумаб или анти. EGFR антитела* • XELOX ± бевацизумаб • FLOX ± бевацизумаб или • монотерапия цетуксимабом или панитумумабом* или • регорафениб или • симптоматическа я терапия • Симптоматическая терапия Значимая симптоматика, обширное метастазировани е, ECOG 3 • Монотерапия фторпиримидинами • 5 -ФУ/ЛВ (режим Мейо, De Gramont) • Капецитабин ± бевацизумаб • Монотерапия анти-EGFR антителами* *Применение анти-EGFR антител (цетуксимаб, панитумумаб) показано лишь пациентам без мутации RAS. Не следует комбинировать анти-EGFR антитела с режимами на основе оксалиплатина и капецитабина (XELOX) или струйного 5‑фторурацила (FLOX), так как это не приводит к улучшению результатов лечения. Практические рекомендации по лекарственному лечению злокачественных опухолей ( RUSSCO) / под редакцией: В. М. Моисеенко. – М. : Общественная организация «Российское общество клинической онкологии» , 2015. – 456 с. L. RU. COM. SM. 03. 2016. 0284
Практические рекомендации RUSSCO Клиническая ситуация Малосимптомны й процесс, ECOG 0 -1 Значимая симптоматика, обширное метастазировани е, ECOG 1 -2 I линия II линия III линия • иринотекан с цетуксимабом или панитумумабом* • Монотерапия фторпиримидинами • 5 -ФУ/ЛВ (режим Мейо, De Gramont) • Капецитабин ± бевацизумаб Оксалиплатин с фторпиримидинами • FOLFOX ± бевацизумаб • XELOX ± бевацизумаб • FOLFOX ± анти-EGFR антитела* • FLOX ± бевацизумаб Иринотекан с фторпиримидинами • FOLFIRI ± бевацизумаб или афлиберцепт или анти-EGFR антитела* • XELIRI ± бевацизумаб Иринотекан с фторпиримидинами • FOLFIRI ± бевацизумаб • XELIRI ± бевацизумаб • FOLFIRI ± анти-EGFR антитела* • FOLFOXIRI ± бевацизумаб Оксалиплатин с фторпиримидинами • FOLFOX ± бевацизумаб или анти. EGFR антитела* • XELOX ± бевацизумаб • FLOX ± бевацизумаб или • монотерапия цетуксимабом или панитумумабом* или • регорафениб или • симптоматическа я терапия • Симптоматическая терапия Значимая симптоматика, обширное метастазировани е, ECOG 3 • Монотерапия фторпиримидинами • 5 -ФУ/ЛВ (режим Мейо, De Gramont) • Капецитабин ± бевацизумаб • Монотерапия анти-EGFR антителами* *Применение анти-EGFR антител (цетуксимаб, панитумумаб) показано лишь пациентам без мутации RAS. Не следует комбинировать анти-EGFR антитела с режимами на основе оксалиплатина и капецитабина (XELOX) или струйного 5‑фторурацила (FLOX), так как это не приводит к улучшению результатов лечения. Практические рекомендации по лекарственному лечению злокачественных опухолей ( RUSSCO) / под редакцией: В. М. Моисеенко. – М. : Общественная организация «Российское общество клинической онкологии» , 2015. – 456 с. L. RU. COM. SM. 03. 2016. 0284
 Обоснование рекомендаций терапии препаратом регорафениб q Торговое наименование препарата: Стиварга®/Stivarga® q Международное непатентованное наименование: регорафениб/ regorafenib q Противоопухолевой препарат, ингибитор протеинкиназы q Лекарственная форма и описание: овальные таблетки, покрытые пленочной оболочкой, светло-розового цвета, на одной стороне методом выдавливания нанесено « 40» , на другой стороне – «BAYER» q Препарат Стиварга®(регорафениб) зарегистрирован для пациентов с метастатическим колоректальным раком, которым уже проводилась или не показана § химиотерапия фторпиримидиновыми препаратами, § терапия, направленная против сосудистого эндотелиального фактора роста (VEGF) § и терапия, направленная против рецепторов эпидермального фактора роста (EGFR) при диком типе KRAS Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016; L. RU. COM. SM. 03. 2016. 0284
Обоснование рекомендаций терапии препаратом регорафениб q Торговое наименование препарата: Стиварга®/Stivarga® q Международное непатентованное наименование: регорафениб/ regorafenib q Противоопухолевой препарат, ингибитор протеинкиназы q Лекарственная форма и описание: овальные таблетки, покрытые пленочной оболочкой, светло-розового цвета, на одной стороне методом выдавливания нанесено « 40» , на другой стороне – «BAYER» q Препарат Стиварга®(регорафениб) зарегистрирован для пациентов с метастатическим колоректальным раком, которым уже проводилась или не показана § химиотерапия фторпиримидиновыми препаратами, § терапия, направленная против сосудистого эндотелиального фактора роста (VEGF) § и терапия, направленная против рецепторов эпидермального фактора роста (EGFR) при диком типе KRAS Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016; L. RU. COM. SM. 03. 2016. 0284
 Обоснование рекомендаций терапии препаратом регорафениб q Эффективность препарата регорафениб при м. КРР была подтверждена в двух клинических исследованиях III фазы CORRECT и CONCUR q Применение препарата регорафениб достоверно увеличивает общую выживаемость у пациентов с метастатическим колоректальным раком и функциональным статусом по ECOG 0– 1 после прогрессирования на фоне стандартной терапии независимо от статуса KRAS • в клиническом исследовании CORRECT риск смерти в группе пациентов, получавших препарат регорафениб, снизился на 23% • в клиническом исследовании CONCUR риск смерти в группе пациентов, получавших препарат регорафениб, снизился на 45% q Препарат регорафениб имеет предсказуемый и контролируемый профиль безопасности Grothey A. , Van Cutsem E. , Sobrero A. et al; for the CORRECT Study Group. Regorafenib monotherapy for previously treated metastatic colorectal cancer (CORRECT): an international, multicentre, randomised, placebo-controlled, phase 3 trial. Lancet. 2013; 381: 303– 312. ; Li J. , Qin S. , Xu R. , Yau T. C. et al. Regorafenib plus best supportive care versus placebo plus best supportive care in Asian patients with previously treated metastatic colorectal cancer (CONCUR): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2015 Jun; 16(6): 619– 29. L. RU. COM. SM. 03. 2016. 0284
Обоснование рекомендаций терапии препаратом регорафениб q Эффективность препарата регорафениб при м. КРР была подтверждена в двух клинических исследованиях III фазы CORRECT и CONCUR q Применение препарата регорафениб достоверно увеличивает общую выживаемость у пациентов с метастатическим колоректальным раком и функциональным статусом по ECOG 0– 1 после прогрессирования на фоне стандартной терапии независимо от статуса KRAS • в клиническом исследовании CORRECT риск смерти в группе пациентов, получавших препарат регорафениб, снизился на 23% • в клиническом исследовании CONCUR риск смерти в группе пациентов, получавших препарат регорафениб, снизился на 45% q Препарат регорафениб имеет предсказуемый и контролируемый профиль безопасности Grothey A. , Van Cutsem E. , Sobrero A. et al; for the CORRECT Study Group. Regorafenib monotherapy for previously treated metastatic colorectal cancer (CORRECT): an international, multicentre, randomised, placebo-controlled, phase 3 trial. Lancet. 2013; 381: 303– 312. ; Li J. , Qin S. , Xu R. , Yau T. C. et al. Regorafenib plus best supportive care versus placebo plus best supportive care in Asian patients with previously treated metastatic colorectal cancer (CONCUR): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2015 Jun; 16(6): 619– 29. L. RU. COM. SM. 03. 2016. 0284
 Дизайн исследования CORRECT Пациенты с м. КРР (N=760), с зафиксированным прогрессированием опухоли, либо при непереносимости стандартной терапии ОС по ECOG= 0 или 1 РАНДОМИЗАЦИЯ 2: 1 Международное, рандомизированное, многоцентровое, двойное слепое, плацебо-контролируемое исследование фазы III Стиварга® 160 мг перорально 1 р/д + ОПТ 3 недели прием препарата, 1 неделя перерыв (n=505) Плацебо + ОПТ 3 недели прием препарата, 1 неделя перерыв (n=255) Продолжение лечения до прогрессирования заболевания или до появления неприемлемого токсического действия Оценка опухоли каждые 8 недель по критериям RECIST 1. 1 Первичная конечная точка: общая выживаемость (ОВ) Вторичные конечные точки: выживаемость без прогрессирования заболевания (ВБП), показатель объективного ответа опухоли, показатель контроля заболевания Критерии включения: во время или в течение 3 месяцев последнего приема зарегистрированных стандартных методов лечения, или они должны были прекратить стандартное лечение из-за развития неприемлемой токсичности. В настоящем исследовании к стандартной терапии м. КРР относились препараты: фторпиримидин, оксалиплатин, иринотекан, бевацизумаб и цетуксимаб или панитумумаб (при наличии опухоли с KRAS дикого типа). ОПТ - оптимальная поддерживающая терапия; ОС по ECOG - общее состояние по шкале Восточной объединенной группы онкологов; RECIST - критерии оценки ответа солидных опухолей Grothey A et al. Lancet. 2013; 381: 303 -312. L. RU. COM. SM. 03. 2016. 0284
Дизайн исследования CORRECT Пациенты с м. КРР (N=760), с зафиксированным прогрессированием опухоли, либо при непереносимости стандартной терапии ОС по ECOG= 0 или 1 РАНДОМИЗАЦИЯ 2: 1 Международное, рандомизированное, многоцентровое, двойное слепое, плацебо-контролируемое исследование фазы III Стиварга® 160 мг перорально 1 р/д + ОПТ 3 недели прием препарата, 1 неделя перерыв (n=505) Плацебо + ОПТ 3 недели прием препарата, 1 неделя перерыв (n=255) Продолжение лечения до прогрессирования заболевания или до появления неприемлемого токсического действия Оценка опухоли каждые 8 недель по критериям RECIST 1. 1 Первичная конечная точка: общая выживаемость (ОВ) Вторичные конечные точки: выживаемость без прогрессирования заболевания (ВБП), показатель объективного ответа опухоли, показатель контроля заболевания Критерии включения: во время или в течение 3 месяцев последнего приема зарегистрированных стандартных методов лечения, или они должны были прекратить стандартное лечение из-за развития неприемлемой токсичности. В настоящем исследовании к стандартной терапии м. КРР относились препараты: фторпиримидин, оксалиплатин, иринотекан, бевацизумаб и цетуксимаб или панитумумаб (при наличии опухоли с KRAS дикого типа). ОПТ - оптимальная поддерживающая терапия; ОС по ECOG - общее состояние по шкале Восточной объединенной группы онкологов; RECIST - критерии оценки ответа солидных опухолей Grothey A et al. Lancet. 2013; 381: 303 -312. L. RU. COM. SM. 03. 2016. 0284
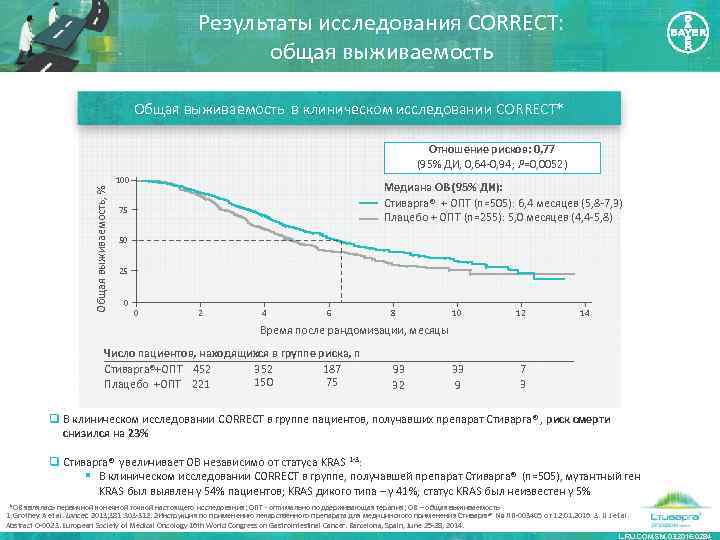 Результаты исследования CORRECT: общая выживаемость Общая выживаемость в клиническом исследовании CORRECT* Общая выживаемость, % Отношение рисков: 0, 77 (95% ДИ, 0, 64 -0, 94; P=0, 0052) 100 Медиана OВ (95% ДИ): Стиварга® + ОПТ (n=505): 6, 4 месяцев (5, 8 -7, 3) Плацебо + ОПТ (n=255): 5, 0 месяцев (4, 4 -5, 8) 75 50 25 0 0 2 4 6 8 10 12 33 9 14 7 3 Время после рандомизации, месяцы Число пациентов, находящихся в группе риска, n Стиварга®+ОПТ 452 352 187 150 75 Плацебо +ОПТ 221 93 32 q В клиническом исследовании CORRECT в группе пациентов, получавших препарат Стиварга® , риск смерти снизился на 23% q Стиварга® увеличивает ОВ независимо от статуса KRAS 1 -3: § В клиническом исследовании CORRECT в группе, получавшей препарат Стиварга® (n=505), мутантный ген KRAS был выявлен у 54% пациентов; KRAS дикого типа – у 41%; статус KRAS был неизвестен у 5% *OВ являлась первичной конечной точкой настоящего исследования; ОПТ - оптимально поддерживающая терапия; ОВ – общая выживаемость 1. Grothey A et al. Lancet. 2013; 381: 303 -312. 2 Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016 3. Li J et al. Abstract O-0023. European Society of Medical Oncology 16 th World Congress on Gastrointestinal Cancer. Barcelona, Spain, June 25 -28, 2014. L. RU. COM. SM. 03. 2016. 0284
Результаты исследования CORRECT: общая выживаемость Общая выживаемость в клиническом исследовании CORRECT* Общая выживаемость, % Отношение рисков: 0, 77 (95% ДИ, 0, 64 -0, 94; P=0, 0052) 100 Медиана OВ (95% ДИ): Стиварга® + ОПТ (n=505): 6, 4 месяцев (5, 8 -7, 3) Плацебо + ОПТ (n=255): 5, 0 месяцев (4, 4 -5, 8) 75 50 25 0 0 2 4 6 8 10 12 33 9 14 7 3 Время после рандомизации, месяцы Число пациентов, находящихся в группе риска, n Стиварга®+ОПТ 452 352 187 150 75 Плацебо +ОПТ 221 93 32 q В клиническом исследовании CORRECT в группе пациентов, получавших препарат Стиварга® , риск смерти снизился на 23% q Стиварга® увеличивает ОВ независимо от статуса KRAS 1 -3: § В клиническом исследовании CORRECT в группе, получавшей препарат Стиварга® (n=505), мутантный ген KRAS был выявлен у 54% пациентов; KRAS дикого типа – у 41%; статус KRAS был неизвестен у 5% *OВ являлась первичной конечной точкой настоящего исследования; ОПТ - оптимально поддерживающая терапия; ОВ – общая выживаемость 1. Grothey A et al. Lancet. 2013; 381: 303 -312. 2 Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016 3. Li J et al. Abstract O-0023. European Society of Medical Oncology 16 th World Congress on Gastrointestinal Cancer. Barcelona, Spain, June 25 -28, 2014. L. RU. COM. SM. 03. 2016. 0284
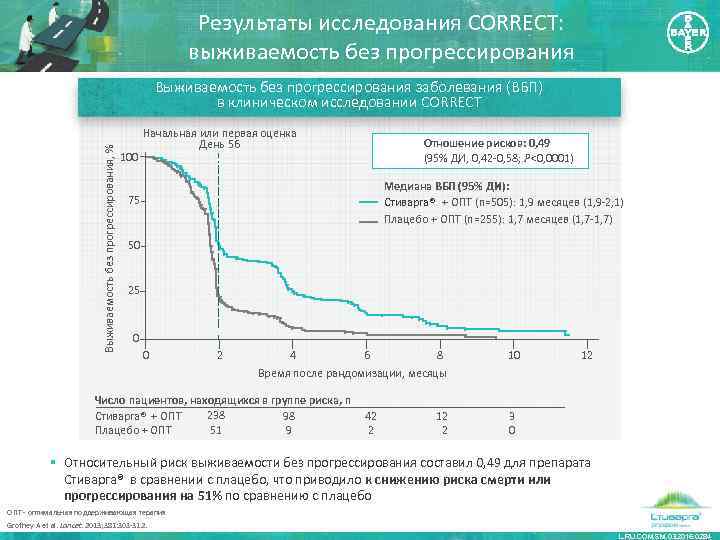 Результаты исследования CORRECT: выживаемость без прогрессирования Выживаемость без прогрессирования, % Выживаемость без прогрессирования заболевания (ВБП) в клиническом исследовании CORRECT 100 Начальная или первая оценка День 56 Отношение рисков: 0, 49 (95% ДИ, 0, 42 -0, 58; P<0, 0001) Медиана ВБП (95% ДИ): Стиварга® + ОПТ (n=505): 1, 9 месяцев (1, 9 -2, 1) Плацебо + ОПТ (n=255): 1, 7 месяцев (1, 7 -1, 7) 75 50 25 0 0 2 4 6 8 Время после рандомизации, месяцы Число пациентов, находящихся в группе риска, n 238 Стиварга® + ОПТ 98 51 Плацебо + ОПТ 9 42 2 10 12 3 0 § Относительный риск выживаемости без прогрессирования составил 0, 49 для препарата Стиварга® в сравнении с плацебо, что приводило к снижению риска смерти или прогрессирования на 51% по сравнению с плацебо ОПТ - оптимальная поддерживающая терапия Grothey A et al. Lancet. 2013; 381: 303 -312. L. RU. COM. SM. 03. 2016. 0284
Результаты исследования CORRECT: выживаемость без прогрессирования Выживаемость без прогрессирования, % Выживаемость без прогрессирования заболевания (ВБП) в клиническом исследовании CORRECT 100 Начальная или первая оценка День 56 Отношение рисков: 0, 49 (95% ДИ, 0, 42 -0, 58; P<0, 0001) Медиана ВБП (95% ДИ): Стиварга® + ОПТ (n=505): 1, 9 месяцев (1, 9 -2, 1) Плацебо + ОПТ (n=255): 1, 7 месяцев (1, 7 -1, 7) 75 50 25 0 0 2 4 6 8 Время после рандомизации, месяцы Число пациентов, находящихся в группе риска, n 238 Стиварга® + ОПТ 98 51 Плацебо + ОПТ 9 42 2 10 12 3 0 § Относительный риск выживаемости без прогрессирования составил 0, 49 для препарата Стиварга® в сравнении с плацебо, что приводило к снижению риска смерти или прогрессирования на 51% по сравнению с плацебо ОПТ - оптимальная поддерживающая терапия Grothey A et al. Lancet. 2013; 381: 303 -312. L. RU. COM. SM. 03. 2016. 0284
 Результаты исследования CORRECT: показатель контроля заболевания Показатель контроля заболевания в клиническом исследовании CORRECT 41% Стиварга® + ОПТ 15% Плацебо + ОПТ Улучшение в 2, 7 x раза § Показатель контроля заболевания (полный или частичный ответ + стабилизация заболевания в течении не менее 6 недель после рандомизации) составил 41% для пациентов, получавших препарат Стиварга® , и 15% для пациентов, получавших плацебо § В клиническом исследовании CORRECT показатель контроля заболевания в группе пациентов, получавших препарат Стиварга® почти в 3 раза выше чем в группе плацебо ОПТ - оптимальная поддерживающая терапия Grothey A et al. Lancet. 2013; 381: 303 -312. L. RU. COM. SM. 03. 2016. 0284
Результаты исследования CORRECT: показатель контроля заболевания Показатель контроля заболевания в клиническом исследовании CORRECT 41% Стиварга® + ОПТ 15% Плацебо + ОПТ Улучшение в 2, 7 x раза § Показатель контроля заболевания (полный или частичный ответ + стабилизация заболевания в течении не менее 6 недель после рандомизации) составил 41% для пациентов, получавших препарат Стиварга® , и 15% для пациентов, получавших плацебо § В клиническом исследовании CORRECT показатель контроля заболевания в группе пациентов, получавших препарат Стиварга® почти в 3 раза выше чем в группе плацебо ОПТ - оптимальная поддерживающая терапия Grothey A et al. Lancet. 2013; 381: 303 -312. L. RU. COM. SM. 03. 2016. 0284
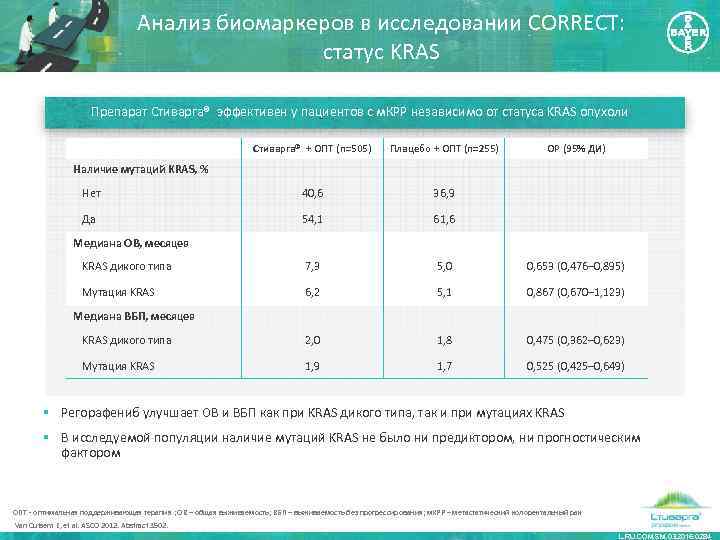 Анализ биомаркеров в исследовании CORRECT: статус KRAS Препарат Стиварга® эффективен у пациентов с м. КРР независимо от статуса KRAS опухоли Стиварга® + ОПТ (n=505) Плацебо + ОПТ (n=255) ОР (95% ДИ) Нет 40, 6 36, 9 Да 54, 1 61, 6 KRAS дикого типа 7, 3 5, 0 0, 653 (0, 476– 0, 895) Мутация KRAS 6, 2 5, 1 0, 867 (0, 670– 1, 123) KRAS дикого типа 2, 0 1, 8 0, 475 (0, 362– 0, 623) Мутация KRAS 1, 9 1, 7 0, 525 (0, 425– 0, 649) Наличие мутаций KRAS, % Медиана ОВ, месяцев Медиана ВБП, месяцев § Регорафениб улучшает ОВ и ВБП как при KRAS дикого типа, так и при мутациях KRAS § В исследуемой популяции наличие мутаций KRAS не было ни предиктором, ни прогностическим фактором ОПТ - оптимальная поддерживающая терапия ; ОВ – общая выживаемость; ВБП – выживаемость без прогрессирования; м. КРР – метастатический колоректальный рак Van Cutsem E, et al. ASCO 2012. Abstract 3502. L. RU. COM. SM. 03. 2016. 0284
Анализ биомаркеров в исследовании CORRECT: статус KRAS Препарат Стиварга® эффективен у пациентов с м. КРР независимо от статуса KRAS опухоли Стиварга® + ОПТ (n=505) Плацебо + ОПТ (n=255) ОР (95% ДИ) Нет 40, 6 36, 9 Да 54, 1 61, 6 KRAS дикого типа 7, 3 5, 0 0, 653 (0, 476– 0, 895) Мутация KRAS 6, 2 5, 1 0, 867 (0, 670– 1, 123) KRAS дикого типа 2, 0 1, 8 0, 475 (0, 362– 0, 623) Мутация KRAS 1, 9 1, 7 0, 525 (0, 425– 0, 649) Наличие мутаций KRAS, % Медиана ОВ, месяцев Медиана ВБП, месяцев § Регорафениб улучшает ОВ и ВБП как при KRAS дикого типа, так и при мутациях KRAS § В исследуемой популяции наличие мутаций KRAS не было ни предиктором, ни прогностическим фактором ОПТ - оптимальная поддерживающая терапия ; ОВ – общая выживаемость; ВБП – выживаемость без прогрессирования; м. КРР – метастатический колоректальный рак Van Cutsem E, et al. ASCO 2012. Abstract 3502. L. RU. COM. SM. 03. 2016. 0284
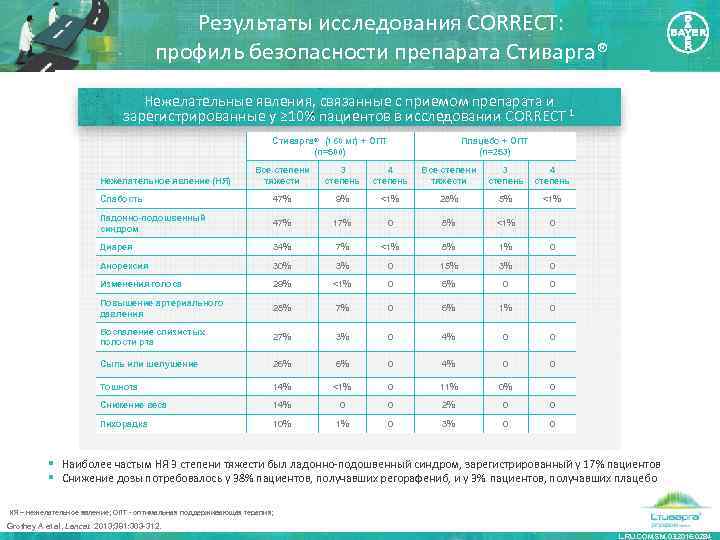 Результаты исследования CORRECT: профиль безопасности препарата Стиварга® Нежелательные явления, связанные с приемом препарата и зарегистрированные у ≥ 10% пациентов в исследовании CORRECT 1 Стиварга® (160 мг) + ОПТ (n=500) Плацебо + ОПТ (n=253) Все степени тяжести 3 степень 4 степень Слабость 47% 9% <1% 28% 5% <1% Ладонно-подошвенный синдром 47% 17% 0 8% <1% 0 Диарея 34% 7% <1% 8% 1% 0 Aнорексия 30% 3% 0 15% 3% 0 Изменения голоса 29% <1% 0 6% 0 0 Повышение артериального давления 28% 7% 0 6% 1% 0 Воспаление слизистых полости рта 27% 3% 0 4% 0 0 Сыпь или шелушение 26% 6% 0 4% 0 0 Тошнота 14% <1% 0 11% 0% 0 Снижение веса 14% 0 0 2% 0 0 Лихорадка 10% 1% 0 3% 0 0 Нежелательное явление (НЯ) § Наиболее частым НЯ 3 степени тяжести был ладонно-подошвенный синдром, зарегистрированный у 17% пациентов § Снижение дозы потребовалось у 38% пациентов, получавших регорафениб, и у 3% пациентов, получавших плацебо НЯ – нежелательное явление; ОПТ - оптимальная поддерживающая терапия; Grothey A et al. Lancet. 2013; 381: 303 -312. L. RU. COM. SM. 03. 2016. 0284
Результаты исследования CORRECT: профиль безопасности препарата Стиварга® Нежелательные явления, связанные с приемом препарата и зарегистрированные у ≥ 10% пациентов в исследовании CORRECT 1 Стиварга® (160 мг) + ОПТ (n=500) Плацебо + ОПТ (n=253) Все степени тяжести 3 степень 4 степень Слабость 47% 9% <1% 28% 5% <1% Ладонно-подошвенный синдром 47% 17% 0 8% <1% 0 Диарея 34% 7% <1% 8% 1% 0 Aнорексия 30% 3% 0 15% 3% 0 Изменения голоса 29% <1% 0 6% 0 0 Повышение артериального давления 28% 7% 0 6% 1% 0 Воспаление слизистых полости рта 27% 3% 0 4% 0 0 Сыпь или шелушение 26% 6% 0 4% 0 0 Тошнота 14% <1% 0 11% 0% 0 Снижение веса 14% 0 0 2% 0 0 Лихорадка 10% 1% 0 3% 0 0 Нежелательное явление (НЯ) § Наиболее частым НЯ 3 степени тяжести был ладонно-подошвенный синдром, зарегистрированный у 17% пациентов § Снижение дозы потребовалось у 38% пациентов, получавших регорафениб, и у 3% пациентов, получавших плацебо НЯ – нежелательное явление; ОПТ - оптимальная поддерживающая терапия; Grothey A et al. Lancet. 2013; 381: 303 -312. L. RU. COM. SM. 03. 2016. 0284
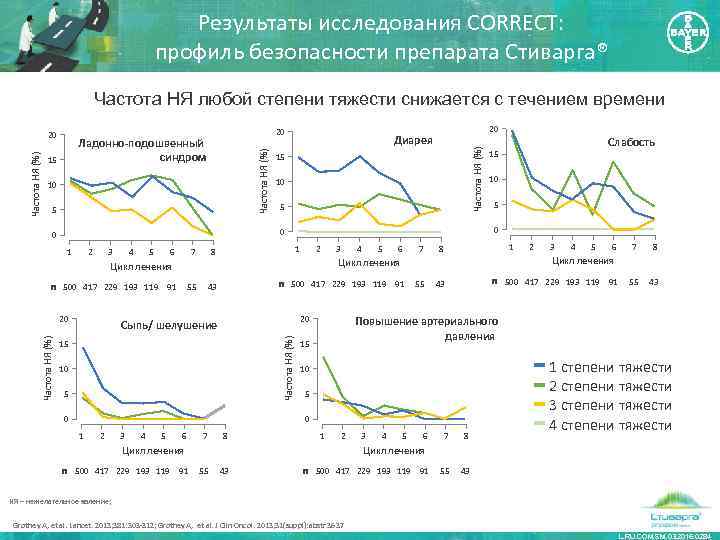 Результаты исследования CORRECT: профиль безопасности препарата Стиварга® Частота НЯ любой степени тяжести снижается с течением времени 20 15 10 5 1 2 3 4 5 6 7 55 1 8 43 2 20 3 4 5 6 20 Частота НЯ (%) 15 10 5 0 7 1 8 55 3 4 5 6 7 8 55 43 Повышение артериального давления 15 10 5 1 2 Цикл лечения n 500 417 229 193 119 91 2 n 500 417 229 193 119 91 43 0 2 5 Цикл лечения n 500 417 229 193 119 91 Сыпь/ шелушение 1 10 Цикл лечения n 500 417 229 193 119 91 Слабость 15 0 0 0 Частота НЯ (%) 20 Диарея Частота НЯ (%) Ладонно-подошвенный синдром Частота НЯ (%) 20 3 4 5 6 7 8 55 ━ 1 степени тяжести ━ 2 степени тяжести ━ 3 степени тяжести ━ 4 степени тяжести 43 Цикл лечения 55 43 n 500 417 229 193 119 91 НЯ – нежелательное явление; Grothey A, et al. Lancet. 2013; 381: 303 -312; Grothey A, et al. J Clin Oncol. 2013; 31(suppl): abstr 3637 L. RU. COM. SM. 03. 2016. 0284
Результаты исследования CORRECT: профиль безопасности препарата Стиварга® Частота НЯ любой степени тяжести снижается с течением времени 20 15 10 5 1 2 3 4 5 6 7 55 1 8 43 2 20 3 4 5 6 20 Частота НЯ (%) 15 10 5 0 7 1 8 55 3 4 5 6 7 8 55 43 Повышение артериального давления 15 10 5 1 2 Цикл лечения n 500 417 229 193 119 91 2 n 500 417 229 193 119 91 43 0 2 5 Цикл лечения n 500 417 229 193 119 91 Сыпь/ шелушение 1 10 Цикл лечения n 500 417 229 193 119 91 Слабость 15 0 0 0 Частота НЯ (%) 20 Диарея Частота НЯ (%) Ладонно-подошвенный синдром Частота НЯ (%) 20 3 4 5 6 7 8 55 ━ 1 степени тяжести ━ 2 степени тяжести ━ 3 степени тяжести ━ 4 степени тяжести 43 Цикл лечения 55 43 n 500 417 229 193 119 91 НЯ – нежелательное явление; Grothey A, et al. Lancet. 2013; 381: 303 -312; Grothey A, et al. J Clin Oncol. 2013; 31(suppl): abstr 3637 L. RU. COM. SM. 03. 2016. 0284
 Результаты исследования CORRECT: профиль безопасности препарата Стиварга® Дни, медиана q В данном анализе изучается время между началом лечения и первым развитием НЯ и максимальной степенью тяжести этих нежелательных явлений q Представляющие интерес нежелательные явления развивались в начале лечения Диарея (n=214) 31, 5 23, 5 Утомляемость (n=317 a) 20, 0 15, 0 Ладонно-подошвенный 22, 0 синдром (n=234) 15, 0 Повышение 15, 0 артериального 14, 0 давления(n=151) q Медиана времени составляла 14, 0– 23, 5 дней Сыпь/шелушение (n=145) 15, 0 Максимальная степень НЯ Первый случай НЯ НЯ – нежелательное явление; ЛПС – ладонно-подошвенный синдром a. n=316 для максимальной степени тяжести Grothey A, et al. Lancet. 2013; 381: 303 -312; Grothey A, et al. J Clin Oncol. 2013; 31(suppl): abstr 3637 L. RU. COM. SM. 03. 2016. 0284
Результаты исследования CORRECT: профиль безопасности препарата Стиварга® Дни, медиана q В данном анализе изучается время между началом лечения и первым развитием НЯ и максимальной степенью тяжести этих нежелательных явлений q Представляющие интерес нежелательные явления развивались в начале лечения Диарея (n=214) 31, 5 23, 5 Утомляемость (n=317 a) 20, 0 15, 0 Ладонно-подошвенный 22, 0 синдром (n=234) 15, 0 Повышение 15, 0 артериального 14, 0 давления(n=151) q Медиана времени составляла 14, 0– 23, 5 дней Сыпь/шелушение (n=145) 15, 0 Максимальная степень НЯ Первый случай НЯ НЯ – нежелательное явление; ЛПС – ладонно-подошвенный синдром a. n=316 для максимальной степени тяжести Grothey A, et al. Lancet. 2013; 381: 303 -312; Grothey A, et al. J Clin Oncol. 2013; 31(suppl): abstr 3637 L. RU. COM. SM. 03. 2016. 0284
 Выводы исследования CORRECT Эффективность q Первичная конечная точка исследования CORRECT была достигнута на момент второго запланированного промежуточного анализа общей выживаемости, и составила 6, 4 месяцев в группе препарата Стиварга® и 5, 0 месяцев в группе плацебо q В клиническом исследовании CORRECT в группе пациентов, получавших препарат Стиварга® , риск смерти снизился на 23% q Эффективность препарата Стиварга® не зависит от статуса KRAS опухоли Безопасность q Основными нежелательными явлениями в группе регорафениба были ладонно-подошвенный синдром, слабость, диарея, анорексия, изменения голоса, повышение артериального давления, воспаления слизистой оболочки полости рта и сыпь/шелушение q Большинство нежелательных явлений произошли в начале курса лечения и контролировались за счет снижения дозы или временного прекращения приема препарата Качество жизни q Качество жизни у пациентов в исследовании CORRECT было сопоставимым в группах регорафениба и плацебо L. RU. COM. SM. 03. 2016. 0284
Выводы исследования CORRECT Эффективность q Первичная конечная точка исследования CORRECT была достигнута на момент второго запланированного промежуточного анализа общей выживаемости, и составила 6, 4 месяцев в группе препарата Стиварга® и 5, 0 месяцев в группе плацебо q В клиническом исследовании CORRECT в группе пациентов, получавших препарат Стиварга® , риск смерти снизился на 23% q Эффективность препарата Стиварга® не зависит от статуса KRAS опухоли Безопасность q Основными нежелательными явлениями в группе регорафениба были ладонно-подошвенный синдром, слабость, диарея, анорексия, изменения голоса, повышение артериального давления, воспаления слизистой оболочки полости рта и сыпь/шелушение q Большинство нежелательных явлений произошли в начале курса лечения и контролировались за счет снижения дозы или временного прекращения приема препарата Качество жизни q Качество жизни у пациентов в исследовании CORRECT было сопоставимым в группах регорафениба и плацебо L. RU. COM. SM. 03. 2016. 0284
 Профили пациентов, которым рекомендовано лечение препаратом регорафениб L. RU. COM. SM. 03. 2016. 0284
Профили пациентов, которым рекомендовано лечение препаратом регорафениб L. RU. COM. SM. 03. 2016. 0284
 Профили пациентов, которым рекомендовано лечение препаратом регорафениб Пациент А Метастатический колоректальный рак (м. КРР) Дикий тип KRAS ECOG 0 или 1 Прогрессирование после терапии предыдущих линий §химиотерапия фторпиримидиновыми препаратами 5 -ФУ/Окс /Ири §терапия, направленная против сосудистого эндотелиального фактора роста (VEGF) бевацизумаб §терапия, направленная против рецепторов эпидермального фактора роста (EGFR) при диком типе KRAS панитумумаб или цетуксимаб Рекомендации: назначение препарата Стиварга®(регорафениб) после прогрессирования на фоне стандартной терапии м. КРР при диком типе KRAS *Изображенные на фото лица не являются реальными пациентами; ОС по ECOG - общее состояние по шкале Восточной объединенной группы онкологов Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016; Практические рекомендации по лекарственному лечению злокачественных опухолей (RUSSCO) / Под ред. В. М. Моисеенко. – М. : Общественная организация «Российское общество клинической онкологии» , 2015. – 456 с. ; National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: Colon Cancer. Version 1. 2015. www. nccn. org/professionals/physician_gls/pdf/colon. pdf. ; Van Cutsem E. , Cervantes A. , Nordlinger B. et al. Metastatic colorectal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2014; 00: iii 1–iii 9. L. RU. COM. SM. 03. 2016. 0284
Профили пациентов, которым рекомендовано лечение препаратом регорафениб Пациент А Метастатический колоректальный рак (м. КРР) Дикий тип KRAS ECOG 0 или 1 Прогрессирование после терапии предыдущих линий §химиотерапия фторпиримидиновыми препаратами 5 -ФУ/Окс /Ири §терапия, направленная против сосудистого эндотелиального фактора роста (VEGF) бевацизумаб §терапия, направленная против рецепторов эпидермального фактора роста (EGFR) при диком типе KRAS панитумумаб или цетуксимаб Рекомендации: назначение препарата Стиварга®(регорафениб) после прогрессирования на фоне стандартной терапии м. КРР при диком типе KRAS *Изображенные на фото лица не являются реальными пациентами; ОС по ECOG - общее состояние по шкале Восточной объединенной группы онкологов Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016; Практические рекомендации по лекарственному лечению злокачественных опухолей (RUSSCO) / Под ред. В. М. Моисеенко. – М. : Общественная организация «Российское общество клинической онкологии» , 2015. – 456 с. ; National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: Colon Cancer. Version 1. 2015. www. nccn. org/professionals/physician_gls/pdf/colon. pdf. ; Van Cutsem E. , Cervantes A. , Nordlinger B. et al. Metastatic colorectal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2014; 00: iii 1–iii 9. L. RU. COM. SM. 03. 2016. 0284
 Профили пациентов, которым рекомендовано лечение препаратом регорафениб Пациент Б Метастатический колоректальный рак (м. КРР) Мутации KRAS ECOG 0 или 1 Прогрессирование после терапии предыдущих линий §химиотерапия фторпиримидиновыми препаратами 5 -ФУ/Окс /Ири §терапия, направленная против сосудистого эндотелиального фактора роста (VEGF) бевацизумаб Рекомендации: назначение препарата Стиварга®(регорафениб) после прогрессирования на фоне стандартной терапии м. КРР при мутациях KRAS *Изображенные на фото лица не являются реальными пациентами; ОС по ECOG - общее состояние по шкале Восточной объединенной группы онкологов Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016; Практические рекомендации по лекарственному лечению злокачественных опухолей (RUSSCO) / Под ред. В. М. Моисеенко. – М. : Общественная организация «Российское общество клинической онкологии» , 2015. – 456 с. ; National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: Colon Cancer. Version 1. 2015. www. nccn. org/professionals/physician_gls/pdf/colon. pdf. ; Van Cutsem E. , Cervantes A. , Nordlinger B. et al. Metastatic colorectal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2014; 00: iii 1–iii 9. L. RU. COM. SM. 03. 2016. 0284
Профили пациентов, которым рекомендовано лечение препаратом регорафениб Пациент Б Метастатический колоректальный рак (м. КРР) Мутации KRAS ECOG 0 или 1 Прогрессирование после терапии предыдущих линий §химиотерапия фторпиримидиновыми препаратами 5 -ФУ/Окс /Ири §терапия, направленная против сосудистого эндотелиального фактора роста (VEGF) бевацизумаб Рекомендации: назначение препарата Стиварга®(регорафениб) после прогрессирования на фоне стандартной терапии м. КРР при мутациях KRAS *Изображенные на фото лица не являются реальными пациентами; ОС по ECOG - общее состояние по шкале Восточной объединенной группы онкологов Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016; Практические рекомендации по лекарственному лечению злокачественных опухолей (RUSSCO) / Под ред. В. М. Моисеенко. – М. : Общественная организация «Российское общество клинической онкологии» , 2015. – 456 с. ; National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: Colon Cancer. Version 1. 2015. www. nccn. org/professionals/physician_gls/pdf/colon. pdf. ; Van Cutsem E. , Cervantes A. , Nordlinger B. et al. Metastatic colorectal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2014; 00: iii 1–iii 9. L. RU. COM. SM. 03. 2016. 0284
 Рекомендации по применению препарата регорафениб для терапии м. КРР Рекомендации, которые могут помочь получить максимальное возможное преимущество от терапии препаратом регорафениб: q Подбор пациентов с хорошим общим состоянием (0 или 1 по шкале ECOG) после прогрессирования на фоне стандартной терапии q Проведение регулярного мониторинга нежелательных явлений с целью контроля пациентов во время приема препарата до первой оценки результатов лечения § мониторинг НЯ в течение первой недели, а затем каждые 2 недели, или чаще, по необходимости q При развитии нежелательных явлений своевременное изменение дозы препарата § подбор дозы индивидуально для контроля переносимости препарата § коррекция дозы на каждом этапе снижения дозы составляет 40 мг (1 таблетка) § повышение дозы препарата после купирования нежелательных явлений производят по рекомендации врача ОС по ECOG - общее состояние по шкале Восточной объединенной группы онкологов 1. Grothey A et al. Lancet. 2013; 381: 303 -312. 2. Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016 L. RU. COM. SM. 03. 2016. 0284
Рекомендации по применению препарата регорафениб для терапии м. КРР Рекомендации, которые могут помочь получить максимальное возможное преимущество от терапии препаратом регорафениб: q Подбор пациентов с хорошим общим состоянием (0 или 1 по шкале ECOG) после прогрессирования на фоне стандартной терапии q Проведение регулярного мониторинга нежелательных явлений с целью контроля пациентов во время приема препарата до первой оценки результатов лечения § мониторинг НЯ в течение первой недели, а затем каждые 2 недели, или чаще, по необходимости q При развитии нежелательных явлений своевременное изменение дозы препарата § подбор дозы индивидуально для контроля переносимости препарата § коррекция дозы на каждом этапе снижения дозы составляет 40 мг (1 таблетка) § повышение дозы препарата после купирования нежелательных явлений производят по рекомендации врача ОС по ECOG - общее состояние по шкале Восточной объединенной группы онкологов 1. Grothey A et al. Lancet. 2013; 381: 303 -312. 2. Инструкция по применению лекарственного препарата для медицинского применения Стиварга® № ЛП-003405 от 12. 01. 2016 L. RU. COM. SM. 03. 2016. 0284
 Спасибо за внимание! АО «БАЙЕР» . 107113, Москва, 3 -я Рыбинская ул. , д. 18, стр. 2. Тел. : +7 (495) 231 1200, факс: +7 (495) 231 1202. www. bayer. ru L. RU. COM. SM. 03. 2016. 0284
Спасибо за внимание! АО «БАЙЕР» . 107113, Москва, 3 -я Рыбинская ул. , д. 18, стр. 2. Тел. : +7 (495) 231 1200, факс: +7 (495) 231 1202. www. bayer. ru L. RU. COM. SM. 03. 2016. 0284


