Планы.ppt
- Количество слайдов: 33
 НОВЫЕ НАУЧНЫЕ ПРИНЦИПЫ И ТЕХНОЛОГИИ ИЗВЛЕЧЕНИЯ МЕТАЛЛОВ ИЗ КОМПЛЕКСНЫХ РУД И ТЕХНОГЕННЫХ ОТХОДОВ ЧТО ДАЛЬШЕ?
НОВЫЕ НАУЧНЫЕ ПРИНЦИПЫ И ТЕХНОЛОГИИ ИЗВЛЕЧЕНИЯ МЕТАЛЛОВ ИЗ КОМПЛЕКСНЫХ РУД И ТЕХНОГЕННЫХ ОТХОДОВ ЧТО ДАЛЬШЕ?
 Эксперимент 1. Расширение доказательной экспериментальной базы на основе экспериментов с разными рудами и нерудными (техногенными) материалами. Теория 2. Термодинамическая и кинетическая температура начала восстановления (методика и расчёт). 3. n – и p –проводимости ионных соединений (физика полупроводников, «кулеровская пара» ) Практика 4. Разработка технологических параметров переработки комплексных руд и техногенных материалов. 5. Создание пилотного предприятия ( «Центр превосходства» ) 2
Эксперимент 1. Расширение доказательной экспериментальной базы на основе экспериментов с разными рудами и нерудными (техногенными) материалами. Теория 2. Термодинамическая и кинетическая температура начала восстановления (методика и расчёт). 3. n – и p –проводимости ионных соединений (физика полупроводников, «кулеровская пара» ) Практика 4. Разработка технологических параметров переработки комплексных руд и техногенных материалов. 5. Создание пилотного предприятия ( «Центр превосходства» ) 2
 Теория 1. Fe. O·Cr 2 O 3 + C =Fe +Cr 2 O 3 +CO ΔGTº = 205426 – 162, 305 Т; Tнач = 1185 K 2. 2/3 Cr 2 O 3 + 18/7 C = 4/21 Cr 7 C 3 +2 CO (Tнач = 1403 K) 3. Cr 2 O 3 + 81/23 C = 2/23 Cr 23 C 6 +3 CO (Tнач = 1424 K) 4. Cr 2 O 3 + 13/3 C = 2/3 Cr 3 C 2 +3 CO (Tнач = 1430 K) 5. 2/3 Cr 2 O 3 + 2 C = 4/3 Cr + 2 CO (Tнач = 1513 K) Δ r. G T º = 0 Δr. GTº = Δr. Hº - Tºнв Δr. SºT = 0 Tºнв = Δr. Hº/Δr. SºТ 3
Теория 1. Fe. O·Cr 2 O 3 + C =Fe +Cr 2 O 3 +CO ΔGTº = 205426 – 162, 305 Т; Tнач = 1185 K 2. 2/3 Cr 2 O 3 + 18/7 C = 4/21 Cr 7 C 3 +2 CO (Tнач = 1403 K) 3. Cr 2 O 3 + 81/23 C = 2/23 Cr 23 C 6 +3 CO (Tнач = 1424 K) 4. Cr 2 O 3 + 13/3 C = 2/3 Cr 3 C 2 +3 CO (Tнач = 1430 K) 5. 2/3 Cr 2 O 3 + 2 C = 4/3 Cr + 2 CO (Tнач = 1513 K) Δ r. G T º = 0 Δr. GTº = Δr. Hº - Tºнв Δr. SºT = 0 Tºнв = Δr. Hº/Δr. SºТ 3
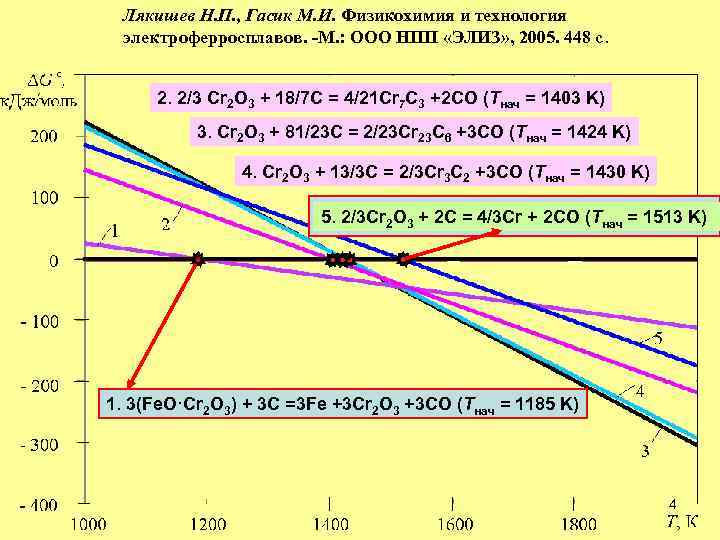 Лякишев Н. П. , Гасик М. И. Физикохимия и технология электроферросплавов. -М. : ООО НПП «ЭЛИЗ» , 2005. 448 с. 2. 2/3 Cr 2 O 3 + 18/7 C = 4/21 Cr 7 C 3 +2 CO (Tнач = 1403 K) 3. Cr 2 O 3 + 81/23 C = 2/23 Cr 23 C 6 +3 CO (Tнач = 1424 K) 4. Cr 2 O 3 + 13/3 C = 2/3 Cr 3 C 2 +3 CO (Tнач = 1430 K) 5. 2/3 Cr 2 O 3 + 2 C = 4/3 Cr + 2 CO (Tнач = 1513 K) 1. 3(Fe. O·Cr 2 O 3) + 3 C =3 Fe +3 Cr 2 O 3 +3 CO (Tнач = 1185 K) 4
Лякишев Н. П. , Гасик М. И. Физикохимия и технология электроферросплавов. -М. : ООО НПП «ЭЛИЗ» , 2005. 448 с. 2. 2/3 Cr 2 O 3 + 18/7 C = 4/21 Cr 7 C 3 +2 CO (Tнач = 1403 K) 3. Cr 2 O 3 + 81/23 C = 2/23 Cr 23 C 6 +3 CO (Tнач = 1424 K) 4. Cr 2 O 3 + 13/3 C = 2/3 Cr 3 C 2 +3 CO (Tнач = 1430 K) 5. 2/3 Cr 2 O 3 + 2 C = 4/3 Cr + 2 CO (Tнач = 1513 K) 1. 3(Fe. O·Cr 2 O 3) + 3 C =3 Fe +3 Cr 2 O 3 +3 CO (Tнач = 1185 K) 4
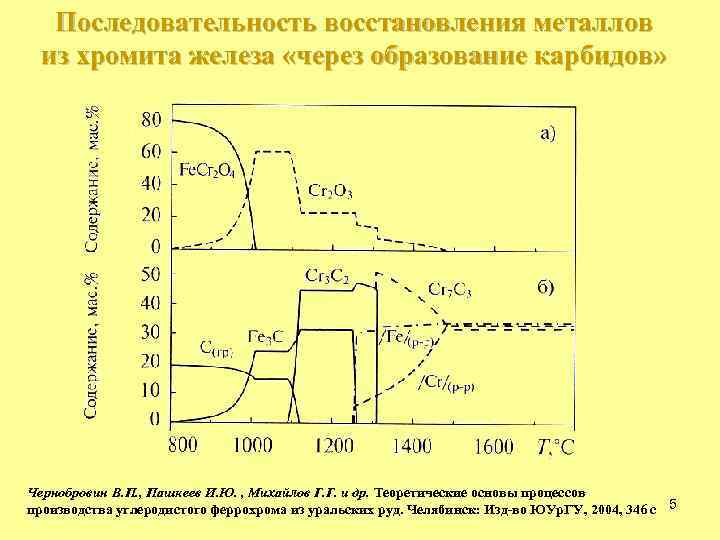 Последовательность восстановления металлов из хромита железа «через образование карбидов» Чернобровин В. П. , Пашкеев И. Ю. , Михайлов Г. Г. и др. Теоретические основы процессов производства углеродистого феррохрома из уральских руд. Челябинск: Изд-во ЮУр. ГУ, 2004, 346 с 5
Последовательность восстановления металлов из хромита железа «через образование карбидов» Чернобровин В. П. , Пашкеев И. Ю. , Михайлов Г. Г. и др. Теоретические основы процессов производства углеродистого феррохрома из уральских руд. Челябинск: Изд-во ЮУр. ГУ, 2004, 346 с 5
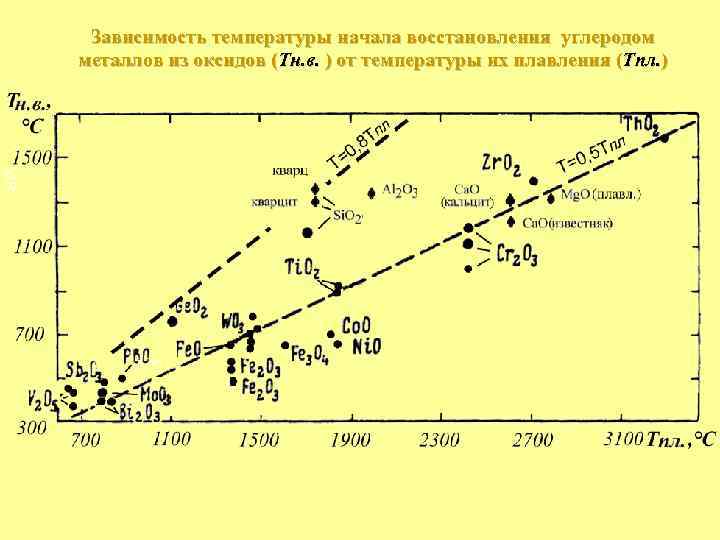 Зависимость температуры начала восстановления углеродом металлов из оксидов (Tн. в. ) от температуры их плавления (Тпл. ) Lg R T, °C
Зависимость температуры начала восстановления углеродом металлов из оксидов (Tн. в. ) от температуры их плавления (Тпл. ) Lg R T, °C
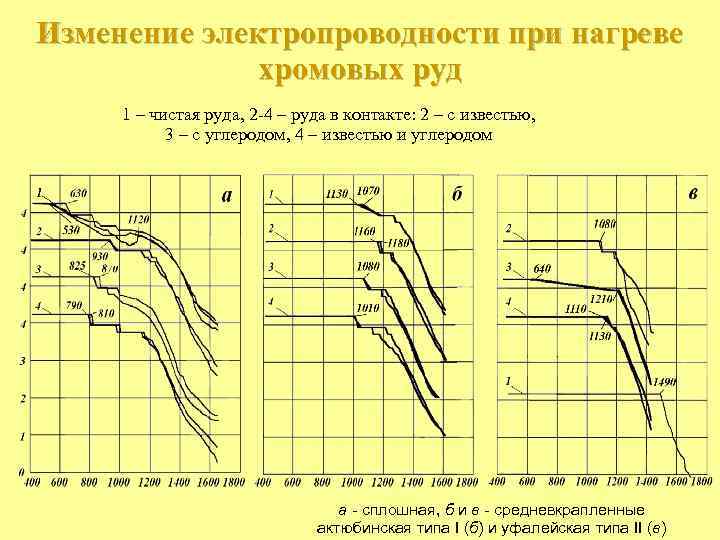 Изменение электропроводности при нагреве хромовых руд 1 – чистая руда, 2 -4 – руда в контакте: 2 – с известью, 3 – с углеродом, 4 – известью и углеродом а - сплошная, б и в - средневкрапленные актюбинская типа I (б) и уфалейская типа II (в)
Изменение электропроводности при нагреве хромовых руд 1 – чистая руда, 2 -4 – руда в контакте: 2 – с известью, 3 – с углеродом, 4 – известью и углеродом а - сплошная, б и в - средневкрапленные актюбинская типа I (б) и уфалейская типа II (в)
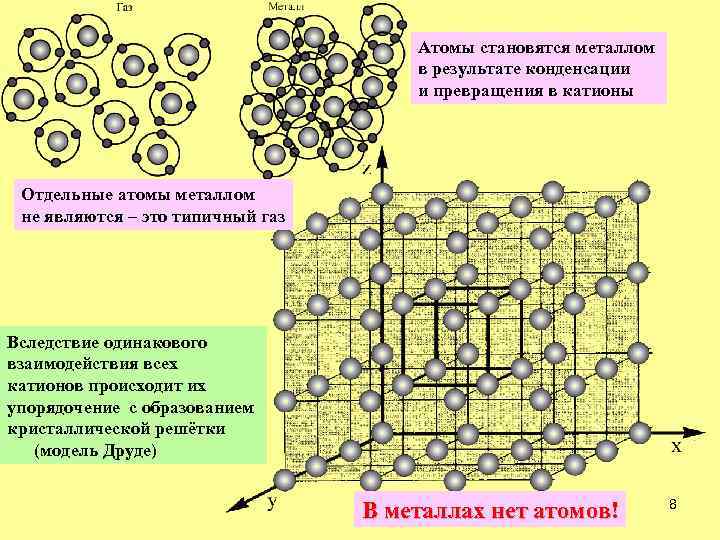 Атомы становятся металлом в результате конденсации и превращения в катионы Отдельные атомы металлом не являются – это типичный газ Вследствие одинакового взаимодействия всех катионов происходит их упорядочение с образованием кристаллической решётки (модель Друде) В металлах нет атомов! 8
Атомы становятся металлом в результате конденсации и превращения в катионы Отдельные атомы металлом не являются – это типичный газ Вследствие одинакового взаимодействия всех катионов происходит их упорядочение с образованием кристаллической решётки (модель Друде) В металлах нет атомов! 8
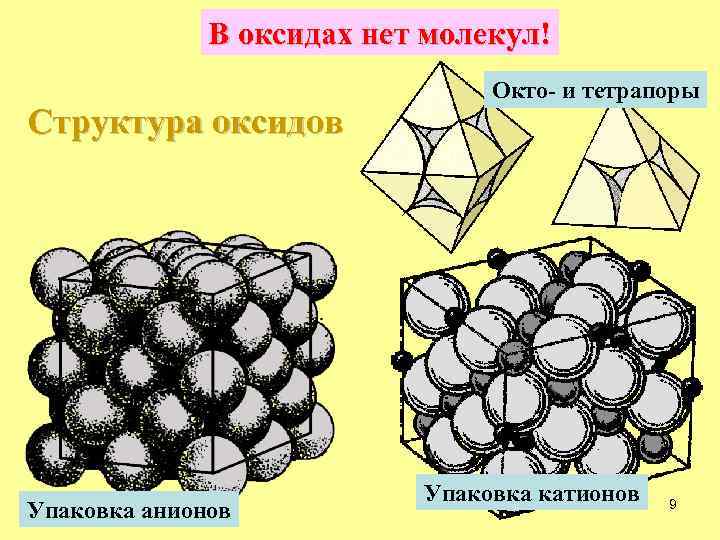 В оксидах нет молекул! Структура оксидов Упаковка анионов Окто- и тетрапоры Упаковка катионов 9
В оксидах нет молекул! Структура оксидов Упаковка анионов Окто- и тетрапоры Упаковка катионов 9
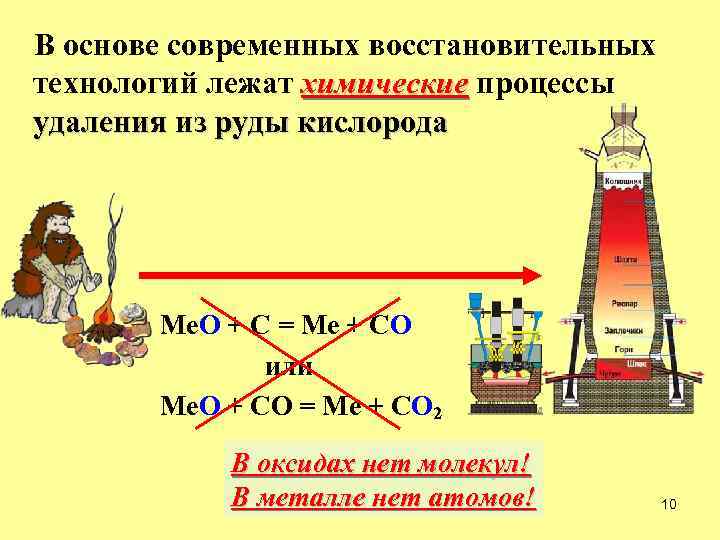 В основе современных восстановительных технологий лежат химические процессы удаления из руды кислорода Me. O + C = Me + CO или Me. O + CО = Me + CO 2 В оксидах нет молекул! В металле нет атомов! 10
В основе современных восстановительных технологий лежат химические процессы удаления из руды кислорода Me. O + C = Me + CO или Me. O + CО = Me + CO 2 В оксидах нет молекул! В металле нет атомов! 10
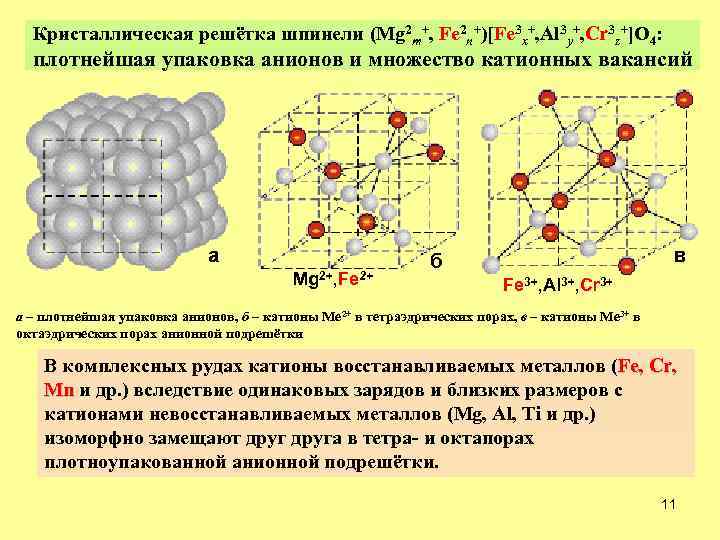 Кристаллическая решётка шпинели (Mg 2 m+, Fe 2 n+)[Fe 3 x+, Al 3 y+, Cr 3 z+]O 4: плотнейшая упаковка анионов и множество катионных вакансий а Mg 2+, Fe 2+ в б Fe 3+, Al 3+, Cr 3+ а – плотнейшая упаковка анионов, б – катионы Ме 2+ в тетраэдрических порах, в – катионы Ме 3+ в октаэдрических порах анионной подрешётки В комплексных рудах катионы восстанавливаемых металлов (Fe, Cr, Mn и др. ) вследствие одинаковых зарядов и близких размеров с катионами невосстанавливаемых металлов (Mg, Al, Ti и др. ) изоморфно замещают друга в тетра- и октапорах плотноупакованной анионной подрешётки. 11
Кристаллическая решётка шпинели (Mg 2 m+, Fe 2 n+)[Fe 3 x+, Al 3 y+, Cr 3 z+]O 4: плотнейшая упаковка анионов и множество катионных вакансий а Mg 2+, Fe 2+ в б Fe 3+, Al 3+, Cr 3+ а – плотнейшая упаковка анионов, б – катионы Ме 2+ в тетраэдрических порах, в – катионы Ме 3+ в октаэдрических порах анионной подрешётки В комплексных рудах катионы восстанавливаемых металлов (Fe, Cr, Mn и др. ) вследствие одинаковых зарядов и близких размеров с катионами невосстанавливаемых металлов (Mg, Al, Ti и др. ) изоморфно замещают друга в тетра- и октапорах плотноупакованной анионной подрешётки. 11
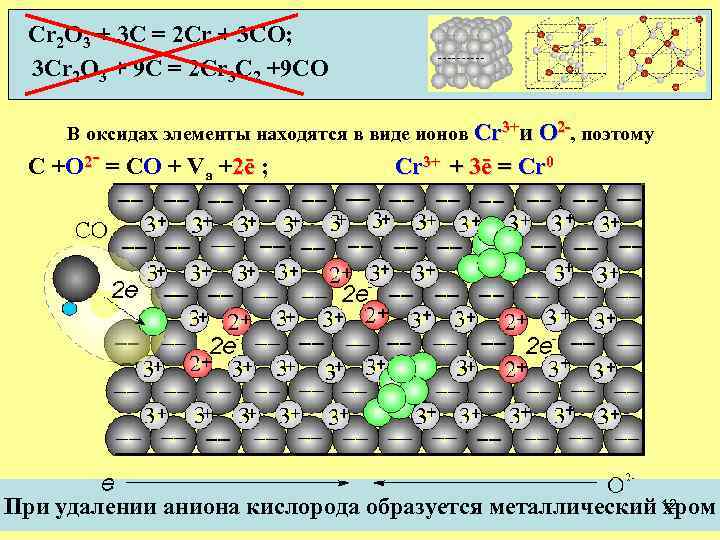 Cr 2 O 3 + 3 C = 2 Cr + 3 CO; 3 Cr 2 O 3 + 9 C = 2 Cr 3 C 2 +9 CO В оксидах элементы находятся в виде ионов Cr 3+и О 2 -, поэтому С +О 2 - = СО + Vа +2ē ; Cr 3+ + 3ē = Cr 0 При удалении аниона кислорода образуется металлический 12 хром
Cr 2 O 3 + 3 C = 2 Cr + 3 CO; 3 Cr 2 O 3 + 9 C = 2 Cr 3 C 2 +9 CO В оксидах элементы находятся в виде ионов Cr 3+и О 2 -, поэтому С +О 2 - = СО + Vа +2ē ; Cr 3+ + 3ē = Cr 0 При удалении аниона кислорода образуется металлический 12 хром
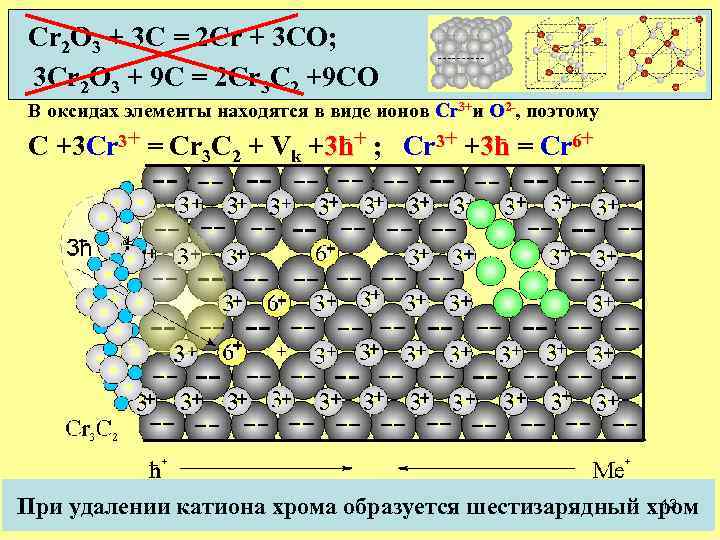 Cr 2 O 3 + 3 C = 2 Cr + 3 CO; 3 Cr 2 O 3 + 9 C = 2 Cr 3 C 2 +9 CO В оксидах элементы находятся в виде ионов Cr 3+и О 2 -, поэтому С +3 Cr 3+ = Сr 3 C 2 + Vk +3ћ+ ; Cr 3+ +3ћ = Cr 6+ 13 При удалении катиона хрома образуется шестизарядный хром
Cr 2 O 3 + 3 C = 2 Cr + 3 CO; 3 Cr 2 O 3 + 9 C = 2 Cr 3 C 2 +9 CO В оксидах элементы находятся в виде ионов Cr 3+и О 2 -, поэтому С +3 Cr 3+ = Сr 3 C 2 + Vk +3ћ+ ; Cr 3+ +3ћ = Cr 6+ 13 При удалении катиона хрома образуется шестизарядный хром
 В кристаллической решётке оксидов элементы находятся в виде ионов Me 2+ и О 2 -, поэтому С +О 2 - = СО + Vа +2ē ; Me 2+ 2+ 2ē = Me 0 Δ r. G T º = 0 Δr. GTº = Δr. Hº - Tºнв Δr. SºT = 0 Tºнв = Δr. Hº/Δr. SºТ 14
В кристаллической решётке оксидов элементы находятся в виде ионов Me 2+ и О 2 -, поэтому С +О 2 - = СО + Vа +2ē ; Me 2+ 2+ 2ē = Me 0 Δ r. G T º = 0 Δr. GTº = Δr. Hº - Tºнв Δr. SºT = 0 Tºнв = Δr. Hº/Δr. SºТ 14
 Практика 1. 2. 3. Сидериты. Титаномагнетиты. Хромиты. 4. Шлаки и шламы. 15
Практика 1. 2. 3. Сидериты. Титаномагнетиты. Хромиты. 4. Шлаки и шламы. 15
 Кусочки сидеритовой руды после восстановления железа 16
Кусочки сидеритовой руды после восстановления железа 16
 Металло-магнезиальный композит в куске сидеритовой руды 17
Металло-магнезиальный композит в куске сидеритовой руды 17
 Растворение металло-магнезиального композита в сталеплавильном шлаке АМЗ 18
Растворение металло-магнезиального композита в сталеплавильном шлаке АМЗ 18
 Состав оксидов, % масс. : 1 – 80, 08 Mg. O; 0, 59 Al 203; 0, 22 Si. O 2; 0, 29 Ca. O; 7, 84 Mn. O; 10, 98 Fe. O; 2 – 25, 74 Mg. O; 0, 80 Al 2 O 3; 37, 57 Si. O 2; 26, 74 Ca. O; 5, 79 Mn. O; 3, 35 Fe. O 19
Состав оксидов, % масс. : 1 – 80, 08 Mg. O; 0, 59 Al 203; 0, 22 Si. O 2; 0, 29 Ca. O; 7, 84 Mn. O; 10, 98 Fe. O; 2 – 25, 74 Mg. O; 0, 80 Al 2 O 3; 37, 57 Si. O 2; 26, 74 Ca. O; 5, 79 Mn. O; 3, 35 Fe. O 19
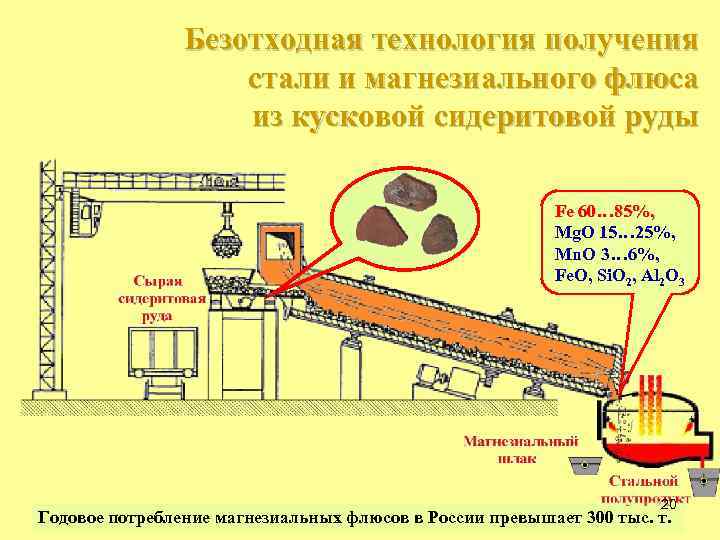 Безотходная технология получения стали и магнезиального флюса из кусковой сидеритовой руды Fe 60… 85%, Mg. O 15… 25%, Mn. O 3… 6%, Fe. O, Si. O 2, Al 2 O 3 20 Годовое потребление магнезиальных флюсов в России превышает 300 тыс. т.
Безотходная технология получения стали и магнезиального флюса из кусковой сидеритовой руды Fe 60… 85%, Mg. O 15… 25%, Mn. O 3… 6%, Fe. O, Si. O 2, Al 2 O 3 20 Годовое потребление магнезиальных флюсов в России превышает 300 тыс. т.
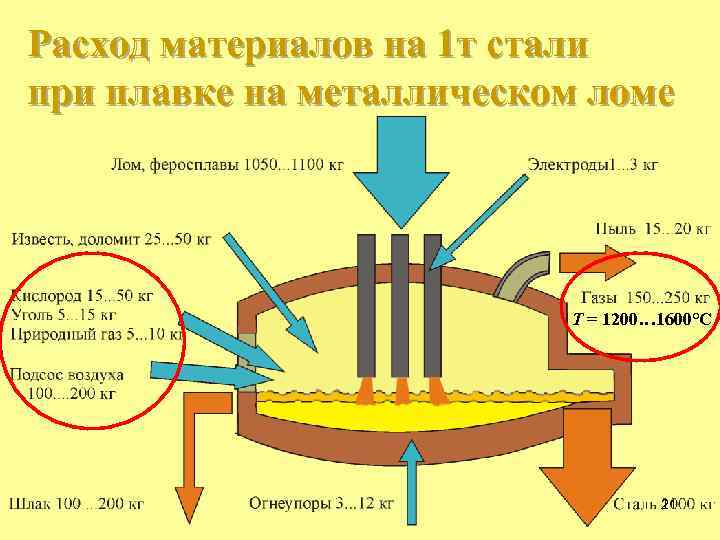 Расход материалов на 1 т стали при плавке на металлическом ломе T = 1200… 1600°C 21
Расход материалов на 1 т стали при плавке на металлическом ломе T = 1200… 1600°C 21
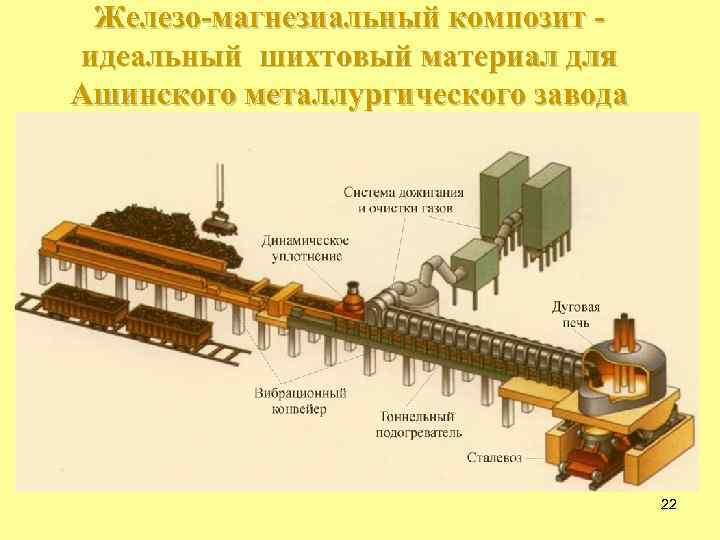 Железо-магнезиальный композит идеальный шихтовый материал для Ашинского металлургического завода 22
Железо-магнезиальный композит идеальный шихтовый материал для Ашинского металлургического завода 22
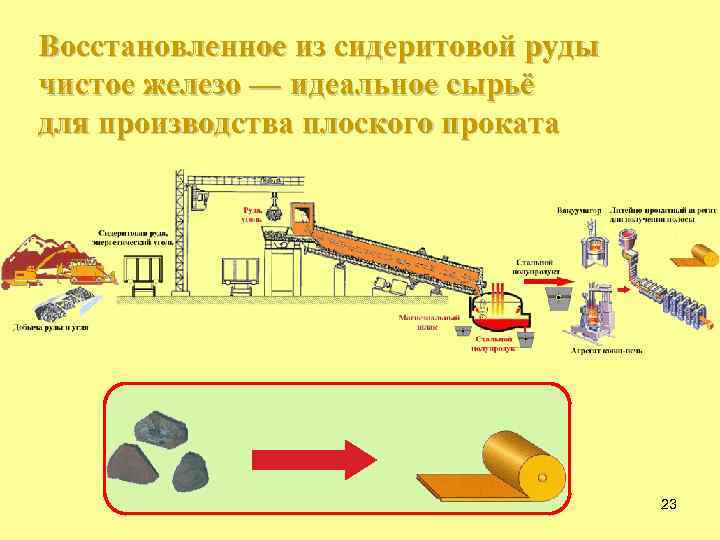 Восстановленное из сидеритовой руды чистое железо –– идеальное сырьё для производства плоского проката 23
Восстановленное из сидеритовой руды чистое железо –– идеальное сырьё для производства плоского проката 23
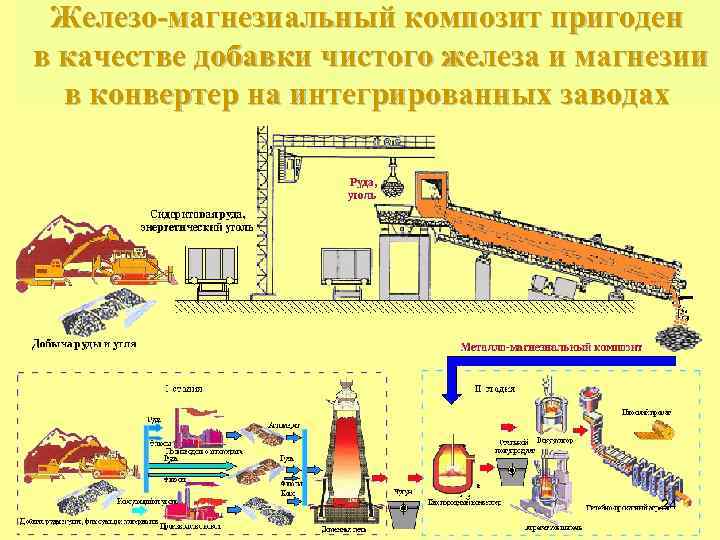 Железо-магнезиальный композит пригоден в качестве добавки чистого железа и магнезии в конвертер на интегрированных заводах 24
Железо-магнезиальный композит пригоден в качестве добавки чистого железа и магнезии в конвертер на интегрированных заводах 24
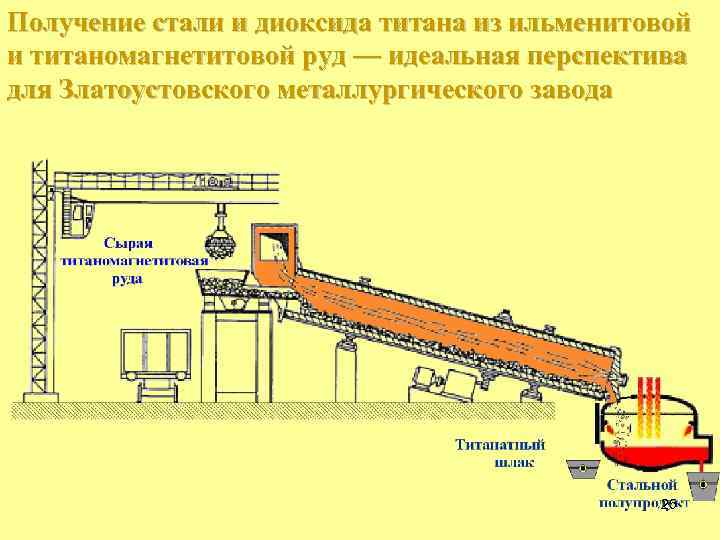 Получение стали и диоксида титана из ильменитовой и титаномагнетитовой руд –– идеальная перспектива для Златоустовского металлургического завода 25
Получение стали и диоксида титана из ильменитовой и титаномагнетитовой руд –– идеальная перспектива для Златоустовского металлургического завода 25
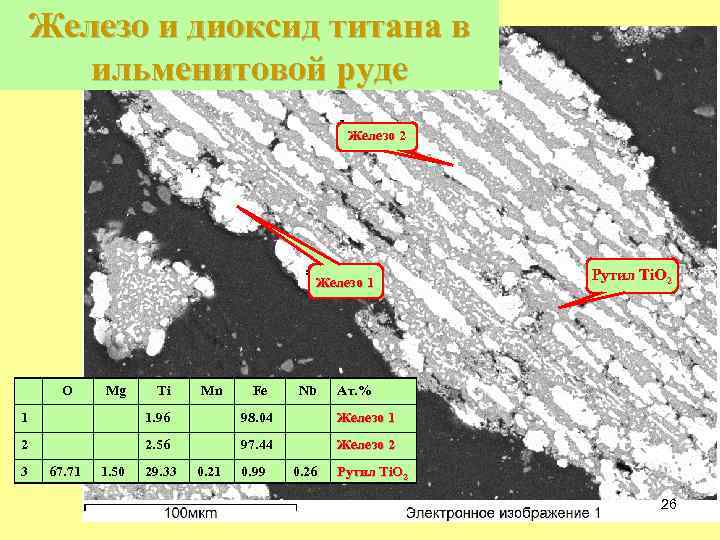 Железо и диоксид титана в ильменитовой руде Железо 2 Железо 1 O Mg Ti Mn Fe Nb Рутил Ti. O 2 Ат. % 1 1. 96 98. 04 Железо 1 2 2. 56 97. 44 Железо 2 3 67. 71 1. 50 29. 33 0. 21 0. 99 0. 26 Рутил Ti. O 2 26
Железо и диоксид титана в ильменитовой руде Железо 2 Железо 1 O Mg Ti Mn Fe Nb Рутил Ti. O 2 Ат. % 1 1. 96 98. 04 Железо 1 2 2. 56 97. 44 Железо 2 3 67. 71 1. 50 29. 33 0. 21 0. 99 0. 26 Рутил Ti. O 2 26
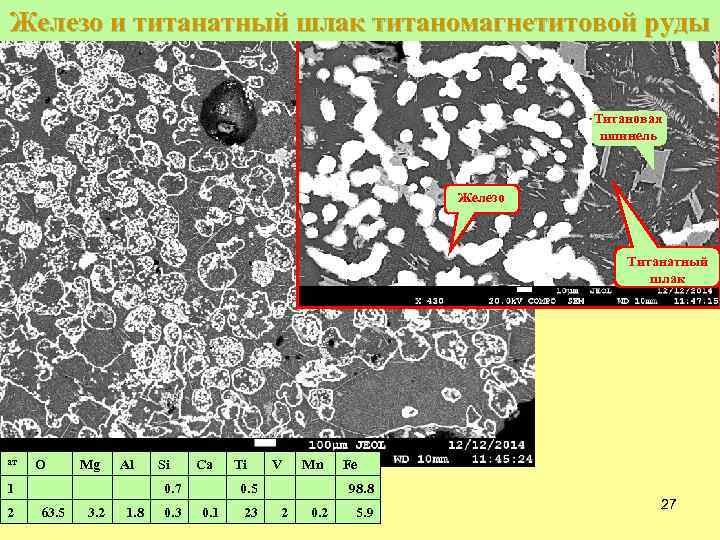 Железо и титанатный шлак титаномагнетитовой руды Титановая шпинель Железо Титанатный шлак ат O Mg Al 1 2 Si Ca 0. 7 63. 5 3. 2 1. 8 0. 3 Ti V Mn 0. 5 0. 1 23 Fe 98. 8 2 0. 2 5. 9 27
Железо и титанатный шлак титаномагнетитовой руды Титановая шпинель Железо Титанатный шлак ат O Mg Al 1 2 Si Ca 0. 7 63. 5 3. 2 1. 8 0. 3 Ti V Mn 0. 5 0. 1 23 Fe 98. 8 2 0. 2 5. 9 27
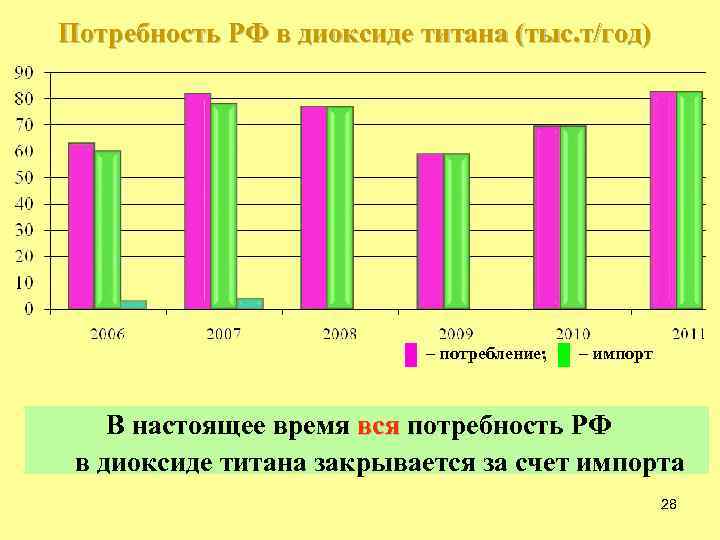 Потребность РФ в диоксиде титана (тыс. т/год) – потребление; – импорт В настоящее время вся потребность РФ п в диоксиде титана закрывается за счет импорта 28
Потребность РФ в диоксиде титана (тыс. т/год) – потребление; – импорт В настоящее время вся потребность РФ п в диоксиде титана закрывается за счет импорта 28
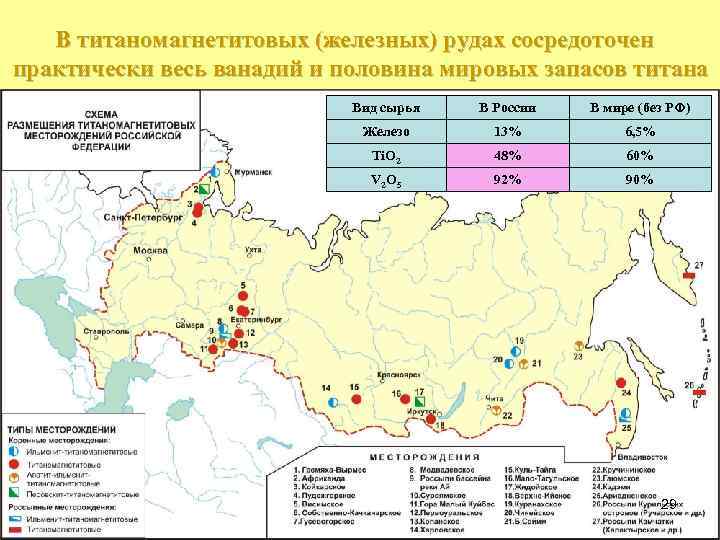 В титаномагнетитовых (железных) рудах сосредоточен практически весь ванадий и половина мировых запасов титана Вид сырья В России В мире (без РФ) Железо 13% 6, 5% Ti. O 2 48% 60% V 2 O 5 92% 90% 29
В титаномагнетитовых (железных) рудах сосредоточен практически весь ванадий и половина мировых запасов титана Вид сырья В России В мире (без РФ) Железо 13% 6, 5% Ti. O 2 48% 60% V 2 O 5 92% 90% 29
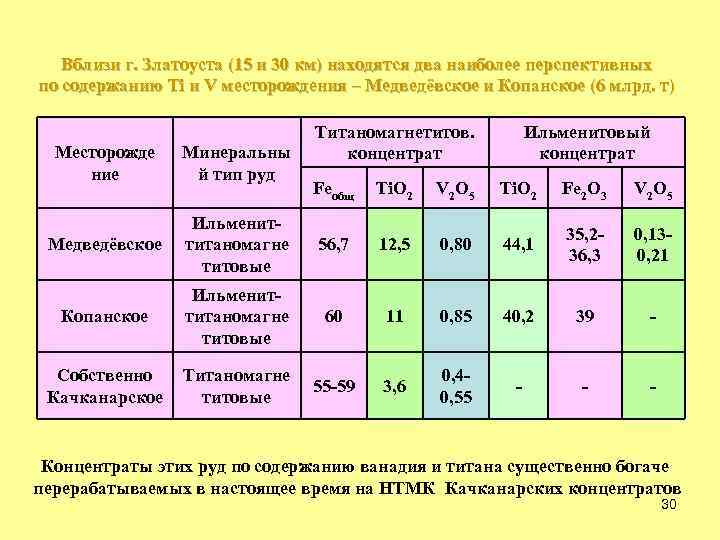 Вблизи г. Златоуста (15 и 30 км) находятся два наиболее перспективных по содержанию Ti и V месторождения – Медведёвское и Копанское (6 млрд. т) Месторожде ние Минеральны й тип руд Титаномагнетитов. концентрат Ильменитовый концентрат Feобщ Ti. O 2 V 2 O 5 Ti. O 2 Fe 2 O 3 V 2 O 5 Медведёвское Ильмениттитаномагне титовые 56, 7 12, 5 0, 80 44, 1 35, 236, 3 0, 130, 21 Копанское Ильмениттитаномагне титовые 60 11 0, 85 40, 2 39 - Собственно Качканарское Титаномагне титовые 55 -59 3, 6 0, 40, 55 - - - Концентраты этих руд по содержанию ванадия и титана существенно богаче перерабатываемых в настоящее время на НТМК Качканарских концентратов 30
Вблизи г. Златоуста (15 и 30 км) находятся два наиболее перспективных по содержанию Ti и V месторождения – Медведёвское и Копанское (6 млрд. т) Месторожде ние Минеральны й тип руд Титаномагнетитов. концентрат Ильменитовый концентрат Feобщ Ti. O 2 V 2 O 5 Ti. O 2 Fe 2 O 3 V 2 O 5 Медведёвское Ильмениттитаномагне титовые 56, 7 12, 5 0, 80 44, 1 35, 236, 3 0, 130, 21 Копанское Ильмениттитаномагне титовые 60 11 0, 85 40, 2 39 - Собственно Качканарское Титаномагне титовые 55 -59 3, 6 0, 40, 55 - - - Концентраты этих руд по содержанию ванадия и титана существенно богаче перерабатываемых в настоящее время на НТМК Качканарских концентратов 30
 Схема безотходной переработки шламов 31 31 На выходе три востребованных продукта
Схема безотходной переработки шламов 31 31 На выходе три востребованных продукта
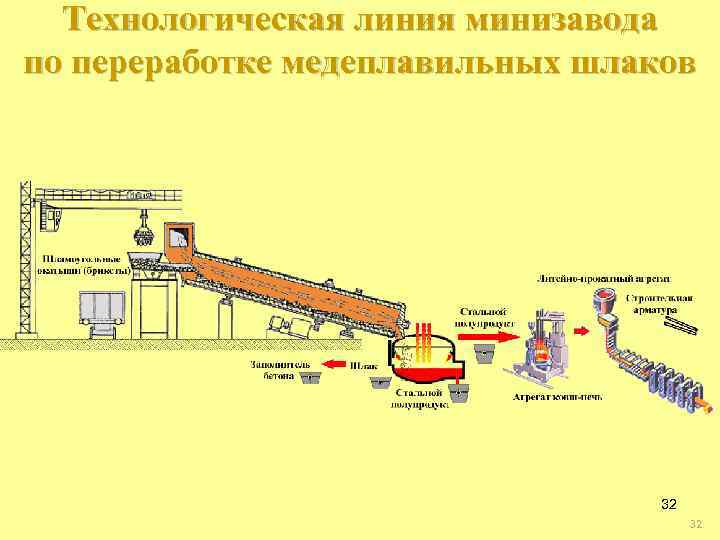 Технологическая линия минизавода по переработке медеплавильных шлаков 32 32
Технологическая линия минизавода по переработке медеплавильных шлаков 32 32
 Арматурный пруток из стали, полученной из железа медеплавильных шлаков C 0. 28 S 0. 04 P 0. 04 Cu 0. 97 Si 0. 58 Mn 1. 32 As 0. 18 Ni 0. 17 Cr 0. 08 Al 0. 14 33 33
Арматурный пруток из стали, полученной из железа медеплавильных шлаков C 0. 28 S 0. 04 P 0. 04 Cu 0. 97 Si 0. 58 Mn 1. 32 As 0. 18 Ni 0. 17 Cr 0. 08 Al 0. 14 33 33


