Е.Г. Лютвина 07.04.15.pptx
- Количество слайдов: 29
 НОВЫЕ НАПРАВЛЕНИЯ В ЛЕЧЕНИИ HCV-ИНФЕКЦИИ Лютвина Елена Геннадьевна Заведующая консультативно-диагностическим отделением БУЗ ОО «ИКБ N 1 имени Далматова Д. М. »
НОВЫЕ НАПРАВЛЕНИЯ В ЛЕЧЕНИИ HCV-ИНФЕКЦИИ Лютвина Елена Геннадьевна Заведующая консультативно-диагностическим отделением БУЗ ОО «ИКБ N 1 имени Далматова Д. М. »
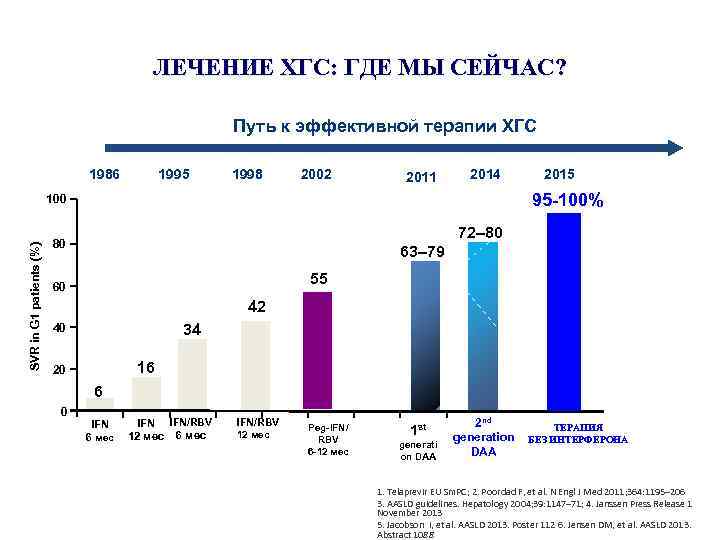 ЛЕЧЕНИЕ ХГС: ГДЕ МЫ СЕЙЧАС? Путь к эффективной терапии ХГС 1986 1995 1998 2002 2011 2014 95 -100% 100 SVR in G 1 patients (%) 2015 72– 80 80 63– 79 55 60 42 34 40 16 20 6 0 IFN 6 мес IFN/RBV 12 мес Peg-IFN/ RBV 6 -12 мес 1 st generati on DAA 2 nd generation DAA ТЕРАПИЯ БЕЗ ИНТЕРФЕРОНА 1. Telaprevir EU Sm. PC; 2. Poordad F, et al. N Engl J Med 2011; 364: 1195– 206 3. AASLD guidelines. Hepatology 2004; 39: 1147– 71; 4. Janssen Press Release 1 November 2013 5. Jacobson I, et al. AASLD 2013. Poster 112 6. Jensen DM, et al. AASLD 2013. Abstract 1088
ЛЕЧЕНИЕ ХГС: ГДЕ МЫ СЕЙЧАС? Путь к эффективной терапии ХГС 1986 1995 1998 2002 2011 2014 95 -100% 100 SVR in G 1 patients (%) 2015 72– 80 80 63– 79 55 60 42 34 40 16 20 6 0 IFN 6 мес IFN/RBV 12 мес Peg-IFN/ RBV 6 -12 мес 1 st generati on DAA 2 nd generation DAA ТЕРАПИЯ БЕЗ ИНТЕРФЕРОНА 1. Telaprevir EU Sm. PC; 2. Poordad F, et al. N Engl J Med 2011; 364: 1195– 206 3. AASLD guidelines. Hepatology 2004; 39: 1147– 71; 4. Janssen Press Release 1 November 2013 5. Jacobson I, et al. AASLD 2013. Poster 112 6. Jensen DM, et al. AASLD 2013. Abstract 1088
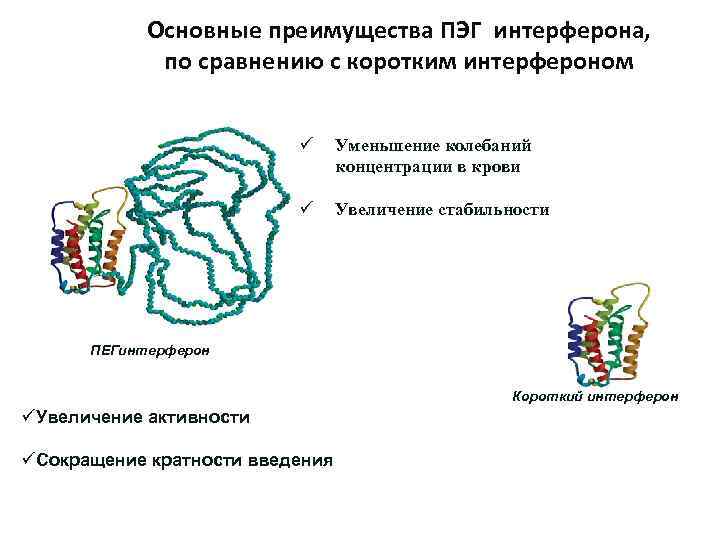 Основные преимущества ПЭГ интерферона, по сравнению с коротким интерфероном ü Уменьшение колебаний концентрации в крови ü Увеличение стабильности ПЕГинтерферон Короткий интерферон üУвеличение активности üСокращение кратности введения
Основные преимущества ПЭГ интерферона, по сравнению с коротким интерфероном ü Уменьшение колебаний концентрации в крови ü Увеличение стабильности ПЕГинтерферон Короткий интерферон üУвеличение активности üСокращение кратности введения
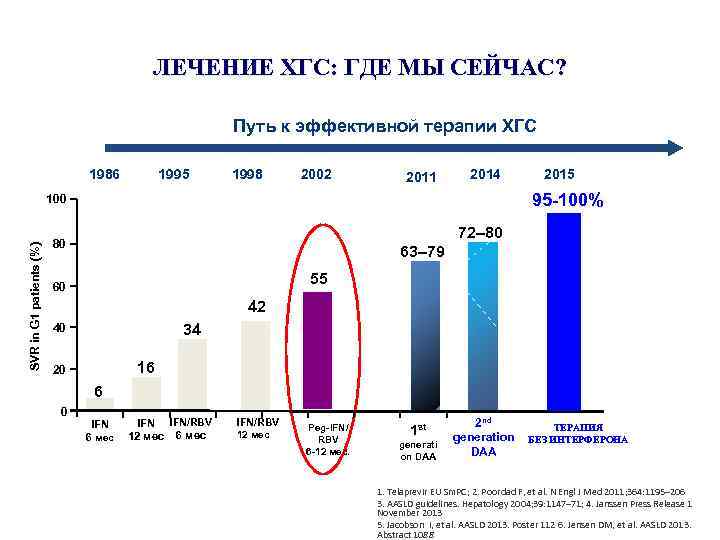 ЛЕЧЕНИЕ ХГС: ГДЕ МЫ СЕЙЧАС? Путь к эффективной терапии ХГС 1986 1995 1998 2002 2011 2014 95 -100% 100 SVR in G 1 patients (%) 2015 72– 80 80 63– 79 55 60 42 34 40 16 20 6 0 IFN 6 мес IFN/RBV 12 мес Peg-IFN/ RBV 6 -12 мес. 1 st generati on DAA 2 nd generation DAA ТЕРАПИЯ БЕЗ ИНТЕРФЕРОНА 1. Telaprevir EU Sm. PC; 2. Poordad F, et al. N Engl J Med 2011; 364: 1195– 206 3. AASLD guidelines. Hepatology 2004; 39: 1147– 71; 4. Janssen Press Release 1 November 2013 5. Jacobson I, et al. AASLD 2013. Poster 112 6. Jensen DM, et al. AASLD 2013. Abstract 1088
ЛЕЧЕНИЕ ХГС: ГДЕ МЫ СЕЙЧАС? Путь к эффективной терапии ХГС 1986 1995 1998 2002 2011 2014 95 -100% 100 SVR in G 1 patients (%) 2015 72– 80 80 63– 79 55 60 42 34 40 16 20 6 0 IFN 6 мес IFN/RBV 12 мес Peg-IFN/ RBV 6 -12 мес. 1 st generati on DAA 2 nd generation DAA ТЕРАПИЯ БЕЗ ИНТЕРФЕРОНА 1. Telaprevir EU Sm. PC; 2. Poordad F, et al. N Engl J Med 2011; 364: 1195– 206 3. AASLD guidelines. Hepatology 2004; 39: 1147– 71; 4. Janssen Press Release 1 November 2013 5. Jacobson I, et al. AASLD 2013. Poster 112 6. Jensen DM, et al. AASLD 2013. Abstract 1088
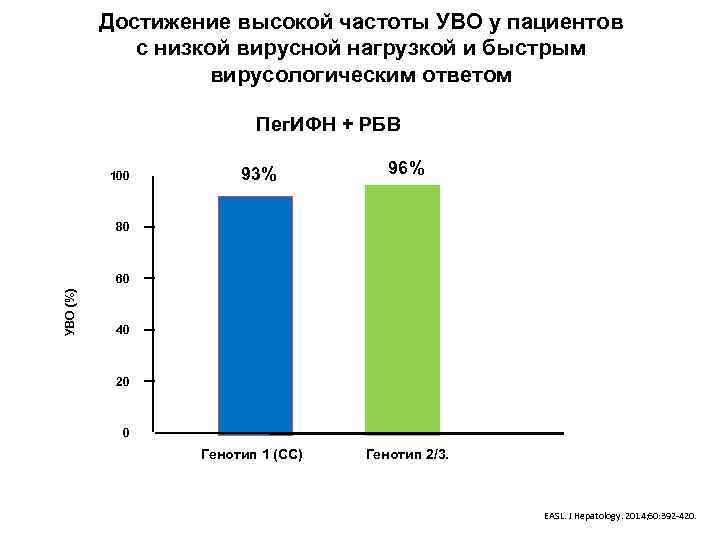 Достижение высокой частоты УВО у пациентов с низкой вирусной нагрузкой и быстрым вирусологическим ответом Пег. ИФН + РБВ 100 93% 96% 80 УВО (%) 60 40 20 0 Генотип 1 (СС) Генотип 2/3. EASL. J Hepatology. 2014; 60: 392 -420.
Достижение высокой частоты УВО у пациентов с низкой вирусной нагрузкой и быстрым вирусологическим ответом Пег. ИФН + РБВ 100 93% 96% 80 УВО (%) 60 40 20 0 Генотип 1 (СС) Генотип 2/3. EASL. J Hepatology. 2014; 60: 392 -420.
 Недостатки двойной терапии с применением ПЕГинтерферона и рибавирина • Зависимость эффективности терапии от исходных характеристик вируса (генотип, вирусная нагрузка, вариант интерлейкина В 28) и пациента (стадия заболевания, пол, возраст, рассовая принадлежность, ИМТ, инсулинорезистентность, стеатоз печени). • Четкие ограничения к применению у пациентов с циррозом. • Довольно высокая частота развития НЯ на фоне терапии (и как следствие - снижение качества жизни и приверженности пациентов к лечению)
Недостатки двойной терапии с применением ПЕГинтерферона и рибавирина • Зависимость эффективности терапии от исходных характеристик вируса (генотип, вирусная нагрузка, вариант интерлейкина В 28) и пациента (стадия заболевания, пол, возраст, рассовая принадлежность, ИМТ, инсулинорезистентность, стеатоз печени). • Четкие ограничения к применению у пациентов с циррозом. • Довольно высокая частота развития НЯ на фоне терапии (и как следствие - снижение качества жизни и приверженности пациентов к лечению)
 «Идеальная» схема лечения HCV-инфекции • Максимально высокая эффективность лечения (независимо от исходных характеристик) • Укорочение сроков ПВТ • Минимизация нежелательных явлений • Удобство применения
«Идеальная» схема лечения HCV-инфекции • Максимально высокая эффективность лечения (независимо от исходных характеристик) • Укорочение сроков ПВТ • Минимизация нежелательных явлений • Удобство применения
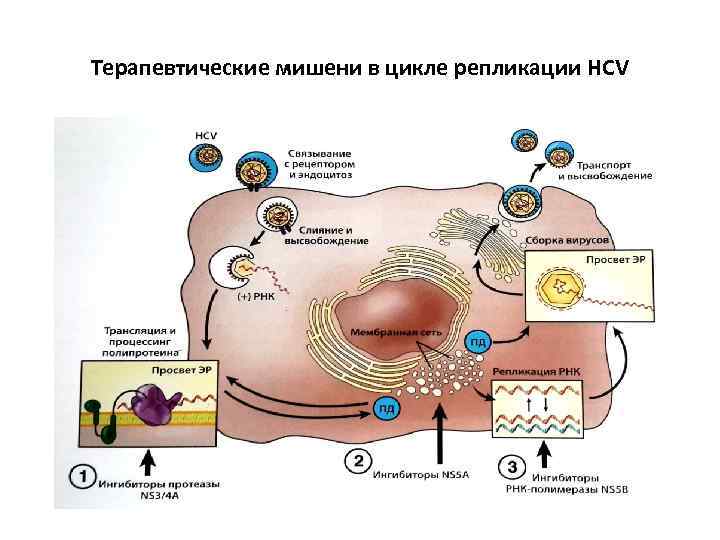 Терапевтические мишени в цикле репликации HCV
Терапевтические мишени в цикле репликации HCV
 Препараты прямого противовирусного действия (ПППД, DAA – Direct Acting Antivirals) – ингибиторы протеазы ВГС открыли новую эру в лечении ХГС 1 генотипа В Америке и странах ЕЭС телапревир и боцепревир одобрены к применению в составе «тройной» терапии в 2011 г В России одобрены к применению в декабре 2012 – телапревир (Инсиво), в мае 2013 – боцепревир (Виктрелис).
Препараты прямого противовирусного действия (ПППД, DAA – Direct Acting Antivirals) – ингибиторы протеазы ВГС открыли новую эру в лечении ХГС 1 генотипа В Америке и странах ЕЭС телапревир и боцепревир одобрены к применению в составе «тройной» терапии в 2011 г В России одобрены к применению в декабре 2012 – телапревир (Инсиво), в мае 2013 – боцепревир (Виктрелис).
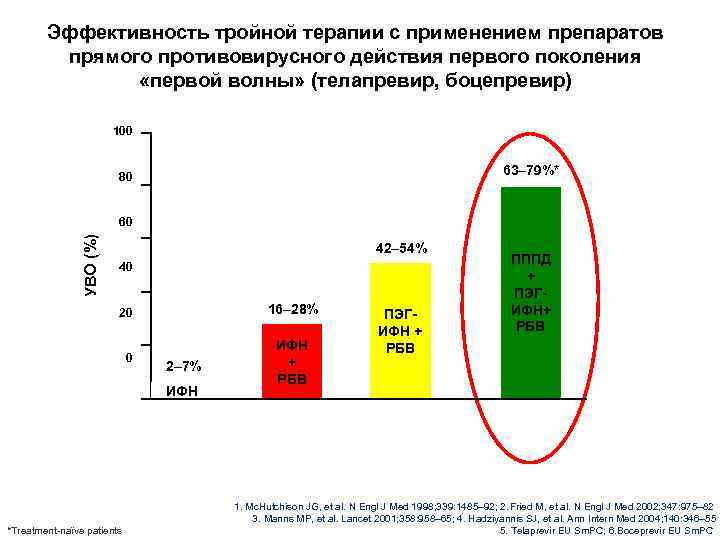 Эффективность тройной терапии с применением препаратов прямого противовирусного действия первого поколения «первой волны» (телапревир, боцепревир) 100 63– 79%* 80 УВО (%) 60 42– 54% 40 20 16– 28% 0 ИФН + РБВ 2– 7% ИФН *Treatment-naïve patients ПЭГИФН + РБВ ПППД + ПЭГИФН+ РБВ 1. Mc. Hutchison JG, et al. N Engl J Med 1998; 339: 1485– 92; 2. Fried M, et al. N Engl J Med 2002; 347: 975– 82 3. Manns MP, et al. Lancet 2001; 358: 958– 65; 4. Hadziyannis SJ, et al. Ann Intern Med 2004; 140: 346– 55 5. Telaprevir EU Sm. PC; 6. Boceprevir EU Sm. PC
Эффективность тройной терапии с применением препаратов прямого противовирусного действия первого поколения «первой волны» (телапревир, боцепревир) 100 63– 79%* 80 УВО (%) 60 42– 54% 40 20 16– 28% 0 ИФН + РБВ 2– 7% ИФН *Treatment-naïve patients ПЭГИФН + РБВ ПППД + ПЭГИФН+ РБВ 1. Mc. Hutchison JG, et al. N Engl J Med 1998; 339: 1485– 92; 2. Fried M, et al. N Engl J Med 2002; 347: 975– 82 3. Manns MP, et al. Lancet 2001; 358: 958– 65; 4. Hadziyannis SJ, et al. Ann Intern Med 2004; 140: 346– 55 5. Telaprevir EU Sm. PC; 6. Boceprevir EU Sm. PC
 Показатели УВО в зависимости от результатов предыдущего лечения Пег ИФН+Р не леченные рецидив частичный ответ нулевой ответ 33 -44% 24 -29% 7 -13% 5% Пег ИФН+Р+(Вос/Tvr) 63 -75% 75 -88% 52 -59% 33 -40% Пациенты с циррозом - 53, 9% (после рецидива) 38, 3% (с частичным ответом) 0% (с «нулевым» ответом)
Показатели УВО в зависимости от результатов предыдущего лечения Пег ИФН+Р не леченные рецидив частичный ответ нулевой ответ 33 -44% 24 -29% 7 -13% 5% Пег ИФН+Р+(Вос/Tvr) 63 -75% 75 -88% 52 -59% 33 -40% Пациенты с циррозом - 53, 9% (после рецидива) 38, 3% (с частичным ответом) 0% (с «нулевым» ответом)
 Схема тройной терапии с Боцепревиром для первичных больных с F 0 -3
Схема тройной терапии с Боцепревиром для первичных больных с F 0 -3
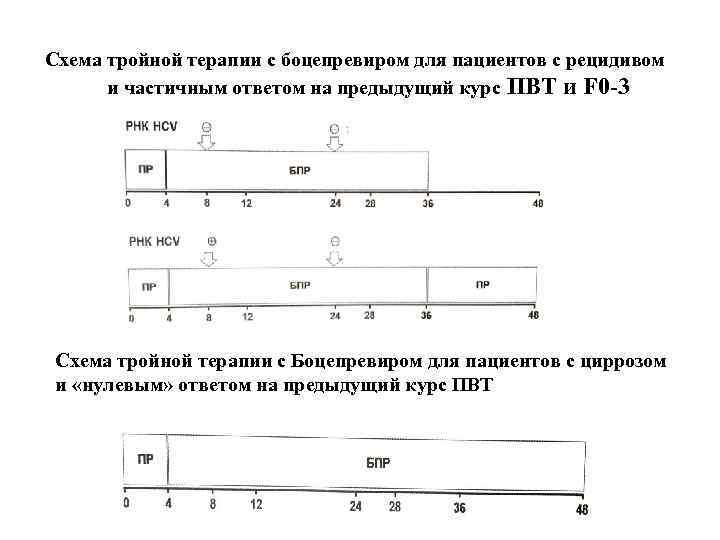 Схема тройной терапии с боцепревиром для пациентов с рецидивом и частичным ответом на предыдущий курс ПВТ и F 0 -3 Схема тройной терапии с Боцепревиром для пациентов с циррозом и «нулевым» ответом на предыдущий курс ПВТ
Схема тройной терапии с боцепревиром для пациентов с рецидивом и частичным ответом на предыдущий курс ПВТ и F 0 -3 Схема тройной терапии с Боцепревиром для пациентов с циррозом и «нулевым» ответом на предыдущий курс ПВТ
 Блоки для построения новых режимов терапии гепатита С ABT-450*/r G 1/4 + Ombitasvir* Simeprevir Interferon Free + + Protease inhibitor RBV NS 5 A G 2/3 NS 5 B inhibitor IFN-free ± ± Nuc inhibitors + 2011 Jul–Dec 2012 Telaprevir Jan–Jun Jul–Dec Sofosbuvir (G 1, 4, 5, 6) Jul–Dec ± BMS-325* Jan–Jun 2014 Simeprevir (G 1, 4) Daclatasvir* RBV Jan–Jun 2013 + ± RBV Jan–Jun Asunaprevir* Sofosbuvir+ Ledipasvir FDC* Sofosbuvir Jul–Dec IFN-based Dasabuvir* Sofosbuvir Jul–Dec 2015 Faldaprevir* (G 1) Boceprevir Daclatasvir* (G 1, 2, 3, 4) Triple therapy Nuc - nucleotide polymerase inhibitor; NS 5 A - hepatitis C virus non-structural protein 5 a protease inhibitor *Not yet approved in Europe
Блоки для построения новых режимов терапии гепатита С ABT-450*/r G 1/4 + Ombitasvir* Simeprevir Interferon Free + + Protease inhibitor RBV NS 5 A G 2/3 NS 5 B inhibitor IFN-free ± ± Nuc inhibitors + 2011 Jul–Dec 2012 Telaprevir Jan–Jun Jul–Dec Sofosbuvir (G 1, 4, 5, 6) Jul–Dec ± BMS-325* Jan–Jun 2014 Simeprevir (G 1, 4) Daclatasvir* RBV Jan–Jun 2013 + ± RBV Jan–Jun Asunaprevir* Sofosbuvir+ Ledipasvir FDC* Sofosbuvir Jul–Dec IFN-based Dasabuvir* Sofosbuvir Jul–Dec 2015 Faldaprevir* (G 1) Boceprevir Daclatasvir* (G 1, 2, 3, 4) Triple therapy Nuc - nucleotide polymerase inhibitor; NS 5 A - hepatitis C virus non-structural protein 5 a protease inhibitor *Not yet approved in Europe
 Симепревир (SMV) Производитель - компания Янссен-Силаг Интернешнл НВ, подразделение фармацевтических препаратов ООО «Джонсон & Джонсон» На Российском рынке – торговое наименование «Совриад» (зарегистрирован в России в феврале 2014 года) В других странах - Олисио (Olysio) • • • Пероральный ингибитор NS 3/4 A протеазы ВГС 2 поколения Удобный режим приема - одна таблетка, один раз в день Безопасен и хорошо переносим • Симепревир (Sovriad®) показан для лечения хронического гепатита С, обусловленного ВГС 1 -го генотипа в качестве компонента тройной терапии • Применяется как в составе схем с ПЭГ-ИНФ и рибавирином, так и в безинтерфероновых комбинациях • Обеспечивает более высокий процент получения УВО, по сравнению с двойной терапией, даже в группе «трудных» пациентов • Улучшенный профиль безопасности у пациентов с компенсированным циррозом печени, по сравнению с ингибиторами протеазы 1 поколения. 1. Reesink H, et al. Gastroenterology 2010; 138: 913– 21 ; 2. Moreno C, et al. J Hepatol 2012; 56: 1247– 53 ; 3. Fried M, et al. AASLD 2011. Oral presentation; 4. Zeuzem S. et al. EASL 2011. Poster LB-2998; 5. Fried M, et al. AASLD 2012. Poster 769; 16 6. Jacobson I, et al. EASL 2013. Poster 1425
Симепревир (SMV) Производитель - компания Янссен-Силаг Интернешнл НВ, подразделение фармацевтических препаратов ООО «Джонсон & Джонсон» На Российском рынке – торговое наименование «Совриад» (зарегистрирован в России в феврале 2014 года) В других странах - Олисио (Olysio) • • • Пероральный ингибитор NS 3/4 A протеазы ВГС 2 поколения Удобный режим приема - одна таблетка, один раз в день Безопасен и хорошо переносим • Симепревир (Sovriad®) показан для лечения хронического гепатита С, обусловленного ВГС 1 -го генотипа в качестве компонента тройной терапии • Применяется как в составе схем с ПЭГ-ИНФ и рибавирином, так и в безинтерфероновых комбинациях • Обеспечивает более высокий процент получения УВО, по сравнению с двойной терапией, даже в группе «трудных» пациентов • Улучшенный профиль безопасности у пациентов с компенсированным циррозом печени, по сравнению с ингибиторами протеазы 1 поколения. 1. Reesink H, et al. Gastroenterology 2010; 138: 913– 21 ; 2. Moreno C, et al. J Hepatol 2012; 56: 1247– 53 ; 3. Fried M, et al. AASLD 2011. Oral presentation; 4. Zeuzem S. et al. EASL 2011. Poster LB-2998; 5. Fried M, et al. AASLD 2012. Poster 769; 16 6. Jacobson I, et al. EASL 2013. Poster 1425
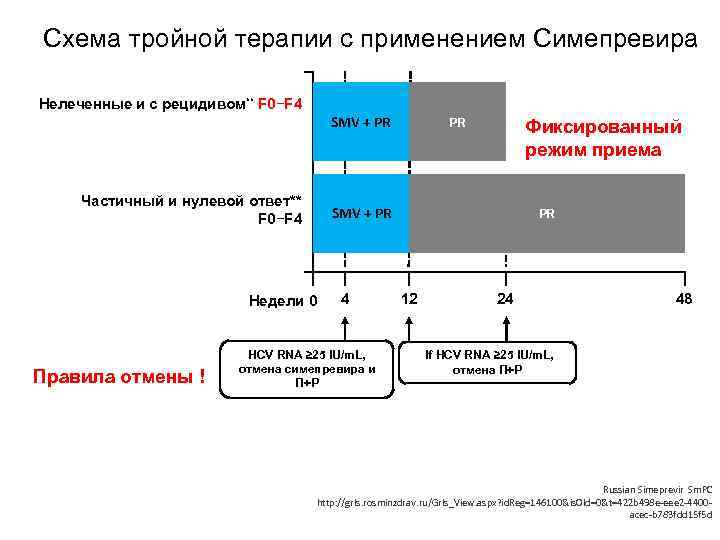 Схема тройной терапии с применением Симепревира Нелеченные и с рецидивом** F 0−F 4 SMV + PR Частичный и нулевой ответ** F 0−F 4 Фиксированный режим приема SMV + PR Недели 0 Правила отмены ! PR 4 HCV RNA ≥ 25 IU/m. L, отмена симепревира и П+Р PR 12 24 48 If HCV RNA ≥ 25 IU/m. L, отмена П+Р Russian Simeprevir Sm. PC http: //grls. rosminzdrav. ru/Grls_View. aspx? id. Reg=146100&is. Old=0&t=422 b 498 e-eee 2 -4400 acec-b 783 fdd 15 f 5 d
Схема тройной терапии с применением Симепревира Нелеченные и с рецидивом** F 0−F 4 SMV + PR Частичный и нулевой ответ** F 0−F 4 Фиксированный режим приема SMV + PR Недели 0 Правила отмены ! PR 4 HCV RNA ≥ 25 IU/m. L, отмена симепревира и П+Р PR 12 24 48 If HCV RNA ≥ 25 IU/m. L, отмена П+Р Russian Simeprevir Sm. PC http: //grls. rosminzdrav. ru/Grls_View. aspx? id. Reg=146100&is. Old=0&t=422 b 498 e-eee 2 -4400 acec-b 783 fdd 15 f 5 d
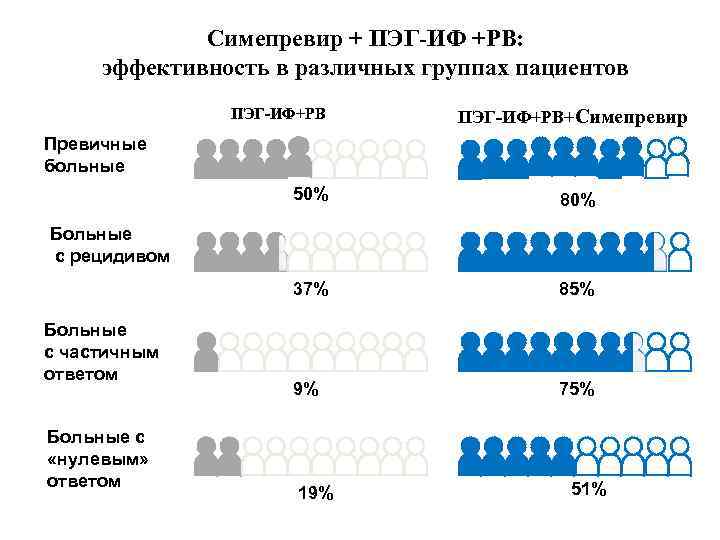 Симепревир + ПЭГ-ИФ +РВ: эффективность в различных группах пациентов ПЭГ-ИФ+РВ+Симепревир Превичные больные 50% 80% 37% 85% 9% 75% Больные с рецидивом Больные с частичным ответом Больные с «нулевым» ответом 19% 51%
Симепревир + ПЭГ-ИФ +РВ: эффективность в различных группах пациентов ПЭГ-ИФ+РВ+Симепревир Превичные больные 50% 80% 37% 85% 9% 75% Больные с рецидивом Больные с частичным ответом Больные с «нулевым» ответом 19% 51%
 Препараты прямого противовирусного действия второго поколения Ингибиторы NS 4/5 протеазы: • асунапревир • паритапревир/ритонавир • данапревир • фалдапревир Нуклеозидные ингибиторы NS 5 B-полимеразы • софосбувир Ингибиторы NS 5 A региона HCV: • даклатасвир • ледипасвир • омбитасвир
Препараты прямого противовирусного действия второго поколения Ингибиторы NS 4/5 протеазы: • асунапревир • паритапревир/ритонавир • данапревир • фалдапревир Нуклеозидные ингибиторы NS 5 B-полимеразы • софосбувир Ингибиторы NS 5 A региона HCV: • даклатасвир • ледипасвир • омбитасвир
 Софосбувир (Совальди) Таблетка 400 мг 1 раз в день (в составе комбинированной терапии) • ингибитор вирусной NS 5 B РНК-полимеразы • одобрен к медицинскому применению в США и Евросоюзе с 2014 года под торговым названием «Совальди» ( фармацевтичесая компания - Gilead, США). Преимущества Софосбувира: • высокая эффективность; • возможность проведения короткого 12 -недельного курса терапии у значительной части больных; • хорошая переносимость, в т. ч. за счет сокращения сроков лечения; • отсутствие выраженного негативного влияния на качество жизни пациентов; • возможность его применения в безинтерфероновых схемах больным не только с генотипом 1, но и с генотипами 2, 3 ВГС.
Софосбувир (Совальди) Таблетка 400 мг 1 раз в день (в составе комбинированной терапии) • ингибитор вирусной NS 5 B РНК-полимеразы • одобрен к медицинскому применению в США и Евросоюзе с 2014 года под торговым названием «Совальди» ( фармацевтичесая компания - Gilead, США). Преимущества Софосбувира: • высокая эффективность; • возможность проведения короткого 12 -недельного курса терапии у значительной части больных; • хорошая переносимость, в т. ч. за счет сокращения сроков лечения; • отсутствие выраженного негативного влияния на качество жизни пациентов; • возможность его применения в безинтерфероновых схемах больным не только с генотипом 1, но и с генотипами 2, 3 ВГС.
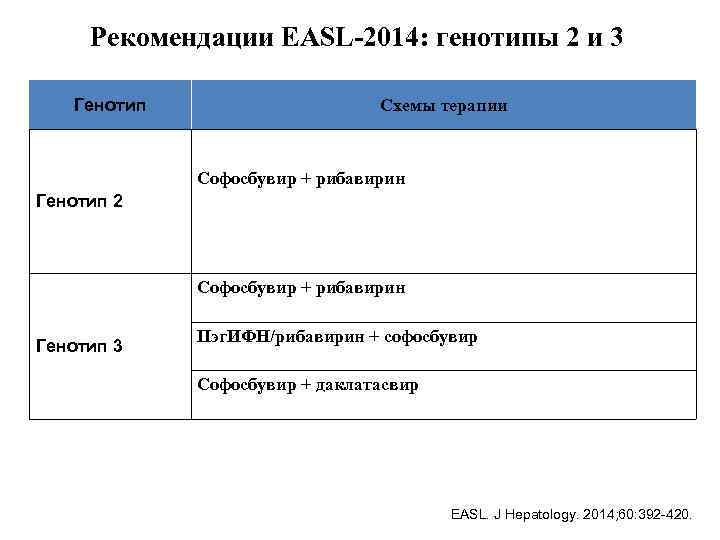 Рекомендации EASL-2014: генотипы 2 и 3 Генотип Схемы терапии Софосбувир + рибавирин Генотип 2 Софосбувир + рибавирин Генотип 3 Пэг. ИФН/рибавирин + софосбувир Софосбувир + даклатасвир EASL. J Hepatology. 2014; 60: 392 -420.
Рекомендации EASL-2014: генотипы 2 и 3 Генотип Схемы терапии Софосбувир + рибавирин Генотип 2 Софосбувир + рибавирин Генотип 3 Пэг. ИФН/рибавирин + софосбувир Софосбувир + даклатасвир EASL. J Hepatology. 2014; 60: 392 -420.
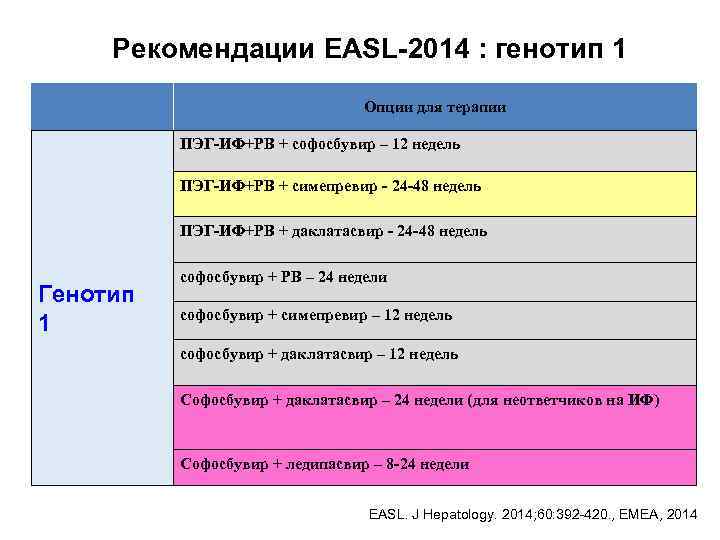 Рекомендации EASL-2014 : генотип 1 Опции для терапии ПЭГ-ИФ+РВ + софосбувир – 12 недель ПЭГ-ИФ+РВ + симепревир - 24 -48 недель ПЭГ-ИФ+РВ + даклатасвир - 24 -48 недель Генотип 1 софосбувир + РВ – 24 недели софосбувир + симепревир – 12 недель софосбувир + даклатасвир – 12 недель Софосбувир + даклатасвир – 24 недели (для неответчиков на ИФ) Софосбувир + ледипасвир – 8 -24 недели EASL. J Hepatology. 2014; 60: 392 -420. , EMEA, 2014
Рекомендации EASL-2014 : генотип 1 Опции для терапии ПЭГ-ИФ+РВ + софосбувир – 12 недель ПЭГ-ИФ+РВ + симепревир - 24 -48 недель ПЭГ-ИФ+РВ + даклатасвир - 24 -48 недель Генотип 1 софосбувир + РВ – 24 недели софосбувир + симепревир – 12 недель софосбувир + даклатасвир – 12 недель Софосбувир + даклатасвир – 24 недели (для неответчиков на ИФ) Софосбувир + ледипасвир – 8 -24 недели EASL. J Hepatology. 2014; 60: 392 -420. , EMEA, 2014
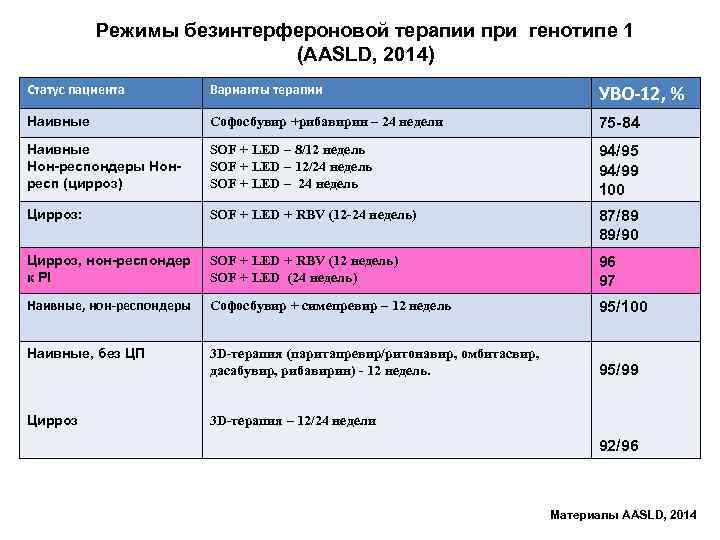 Режимы безинтерфероновой терапии при генотипе 1 (AASLD, 2014) Статус пациента Варианты терапии УВО-12, % Наивные Софосбувир +рибавирин – 24 недели 75 -84 Наивные Нон-респондеры Нонресп (цирроз) SOF + LED – 8/12 недель SOF + LED – 12/24 недель SOF + LED – 24 недель 94/95 94/99 100 Цирроз: SOF + LED + RBV (12 -24 недель) 87/89 89/90 Цирроз, нон-респондер к PI SOF + LED + RBV (12 недель) SOF + LED (24 недель) 96 97 Наивные, нон-респондеры Софосбувир + симепревир – 12 недель 95/100 Наивные, без ЦП 3 D-терапия (паритапревир/ритонавир, омбитасвир, дасабувир, рибавирин) - 12 недель. 95/99 Цирроз 3 D-терапия – 12/24 недели 92/96 Материалы AASLD, 2014
Режимы безинтерфероновой терапии при генотипе 1 (AASLD, 2014) Статус пациента Варианты терапии УВО-12, % Наивные Софосбувир +рибавирин – 24 недели 75 -84 Наивные Нон-респондеры Нонресп (цирроз) SOF + LED – 8/12 недель SOF + LED – 12/24 недель SOF + LED – 24 недель 94/95 94/99 100 Цирроз: SOF + LED + RBV (12 -24 недель) 87/89 89/90 Цирроз, нон-респондер к PI SOF + LED + RBV (12 недель) SOF + LED (24 недель) 96 97 Наивные, нон-респондеры Софосбувир + симепревир – 12 недель 95/100 Наивные, без ЦП 3 D-терапия (паритапревир/ритонавир, омбитасвир, дасабувир, рибавирин) - 12 недель. 95/99 Цирроз 3 D-терапия – 12/24 недели 92/96 Материалы AASLD, 2014
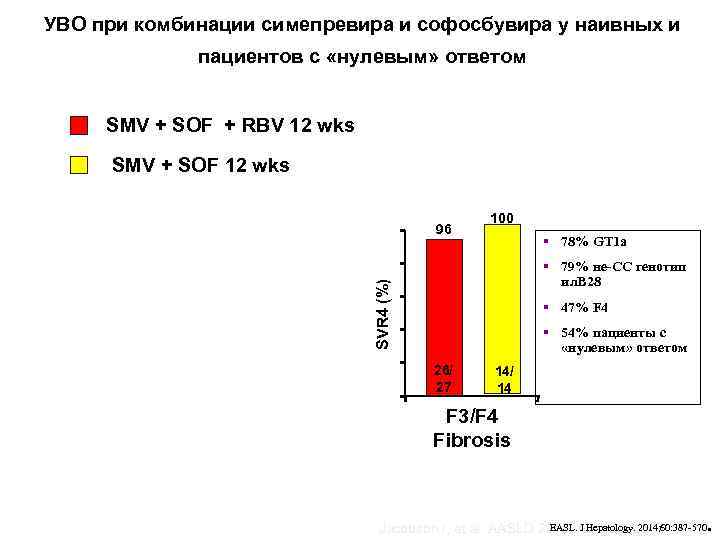 УВО при комбинации симепревира и софосбувира у наивных и пациентов с «нулевым» ответом SMV + SOF + RBV 12 wks SMV + SOF 12 wks 96 100 § 78% GT 1 a 60 40 20 0 § 79% не-CC генотип ил. В 28 SVR 4 (%) SVR 12 (%) 80 § 47% F 4 § 54% пациенты с «нулевым» ответом 26/ 27 14/ 14 F 3/F 4 Fibrosis . EASL. J Hepatology. 2014; 60: 387 -570 Jacobson I, et al. AASLD 2013. Abstract LB-3.
УВО при комбинации симепревира и софосбувира у наивных и пациентов с «нулевым» ответом SMV + SOF + RBV 12 wks SMV + SOF 12 wks 96 100 § 78% GT 1 a 60 40 20 0 § 79% не-CC генотип ил. В 28 SVR 4 (%) SVR 12 (%) 80 § 47% F 4 § 54% пациенты с «нулевым» ответом 26/ 27 14/ 14 F 3/F 4 Fibrosis . EASL. J Hepatology. 2014; 60: 387 -570 Jacobson I, et al. AASLD 2013. Abstract LB-3.
 HARVONI (Харвони) фармацевтичесая компания Gilead, США ледипасвир + софосбувир. 1 таблетка 1 раз в день. одобрен к применению в США и Евросоюзе с октября 2014 года) Возможно проведение терапии пациентов с генотипом 1 HCV без рибавирина. «наивные» пациенты, ранее леченые пациенты и пациенты с F 3 (генотип 1 HCV) : • • • HARVONI + РВ в течение 12 недель - УВО 12 – у 100% пациентов HARVONI (монотерапия) 12 недель - УВО 12 - у 97% пациентов HARVONI (монотерапия) 12 недель у пациентов с циррозом- УВО 12 - у 70% пациентов Хорошая переносимость терапии – почти у половины пациентов не наблюдалось никаких побочных эффектов.
HARVONI (Харвони) фармацевтичесая компания Gilead, США ледипасвир + софосбувир. 1 таблетка 1 раз в день. одобрен к применению в США и Евросоюзе с октября 2014 года) Возможно проведение терапии пациентов с генотипом 1 HCV без рибавирина. «наивные» пациенты, ранее леченые пациенты и пациенты с F 3 (генотип 1 HCV) : • • • HARVONI + РВ в течение 12 недель - УВО 12 – у 100% пациентов HARVONI (монотерапия) 12 недель - УВО 12 - у 97% пациентов HARVONI (монотерапия) 12 недель у пациентов с циррозом- УВО 12 - у 70% пациентов Хорошая переносимость терапии – почти у половины пациентов не наблюдалось никаких побочных эффектов.
 VIEKIRA-PAK (Виекира-Пак) – (омбитасвир+паритапревир/ритонавир + дасабувир 4 таблетки в день (3 утром, 1 вечером) Монотерапия HCV 1 генотипа в течение 8 -12 недель с эффективностью до 95, 5%! Полностью пероральная схема лечения, не требующая применения интерферонов. Данная комбинация одобрена для лечения хронического гепатита С генотипа 1 в сочетании с рибавирином или без него, в том числе у пациентов с компенсированным циррозом печени, у пациентов, ожидающих трансплантацию печени, у пациентов с сочетанной инфекцией ВГС/ВИЧ и у пациентов, которые перенесли пересадку печени.
VIEKIRA-PAK (Виекира-Пак) – (омбитасвир+паритапревир/ритонавир + дасабувир 4 таблетки в день (3 утром, 1 вечером) Монотерапия HCV 1 генотипа в течение 8 -12 недель с эффективностью до 95, 5%! Полностью пероральная схема лечения, не требующая применения интерферонов. Данная комбинация одобрена для лечения хронического гепатита С генотипа 1 в сочетании с рибавирином или без него, в том числе у пациентов с компенсированным циррозом печени, у пациентов, ожидающих трансплантацию печени, у пациентов с сочетанной инфекцией ВГС/ВИЧ и у пациентов, которые перенесли пересадку печени.
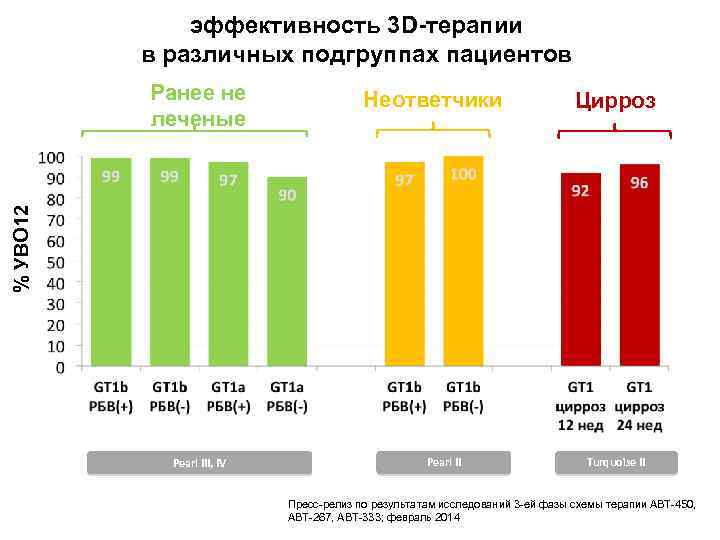 эффективность 3 D-терапии в различных подгруппах пациентов Неответчики Цирроз % УВО 12 Ранее не леченые Pearl III, IV Pearl II Turquoise II Пресс-релиз по результатам исследований 3 -ей фазы схемы терапии ABT-450, ABT-267, ABT-333; февраль 2014
эффективность 3 D-терапии в различных подгруппах пациентов Неответчики Цирроз % УВО 12 Ранее не леченые Pearl III, IV Pearl II Turquoise II Пресс-релиз по результатам исследований 3 -ей фазы схемы терапии ABT-450, ABT-267, ABT-333; февраль 2014
 Результаты новейших исследований вселяют надежду, что в скором времени высокоэффективные, хорошо переносимые и удобные в применении схемы терапии без интерферона займут первое место в лечении гепатита С и откроют перспективу полного излечения этой инфекции. «СЛЕДУЮЩЕЕ ПОКОЛЕНИЕ ЛЮДЕЙ БУДЕТ ЖИТЬ БЕЗ ВИРУСНОГО ГЕПАТИТА С. » /М. Р. MANNS/
Результаты новейших исследований вселяют надежду, что в скором времени высокоэффективные, хорошо переносимые и удобные в применении схемы терапии без интерферона займут первое место в лечении гепатита С и откроют перспективу полного излечения этой инфекции. «СЛЕДУЮЩЕЕ ПОКОЛЕНИЕ ЛЮДЕЙ БУДЕТ ЖИТЬ БЕЗ ВИРУСНОГО ГЕПАТИТА С. » /М. Р. MANNS/
 СПАСИБО ЗА ВНИМАНИЕ
СПАСИБО ЗА ВНИМАНИЕ


