Гемоглобин.ppt
- Количество слайдов: 37

НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ Кафедра медицинской химии СТРУКТУРА ГЕМОГЛОБИНА (Белки плазмы крови) профессор, д. м. н. Потеряева Ольга Николаевна 18 апреля 2012 г.

ПЛАН ЛЕКЦИИ 1. Эритроциты – специализированные клетки, переносящие кислород. 2. Структура гемоглобина. Физиологические и патологические формы. 3. Синтез гемоглобина. 4. Нарушение структуры Цель: разобрать структуру гемоглобина с позиций знания о белке, его функциональной роли в организме.
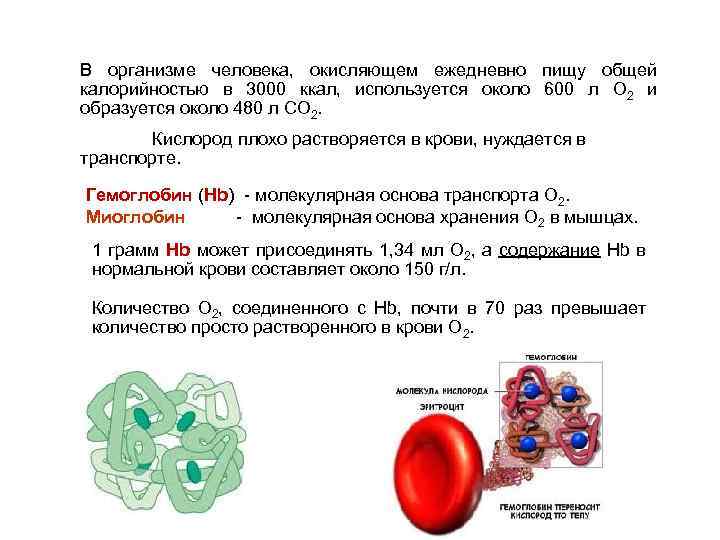
В организме человека, окисляющем ежедневно пищу общей калорийностью в 3000 ккал, используется около 600 л О 2 и образуется около 480 л СО 2. Кислород плохо растворяется в крови, нуждается в транспорте. Гемоглобин (Нb) - молекулярная основа транспорта О 2. Миоглобин - молекулярная основа хранения О 2 в мышцах. 1 грамм Нb может присоединять 1, 34 мл О 2, а содержание Hb в нормальной крови составляет около 150 г/л. Количество О 2, соединенного с Hb, почти в 70 раз превышает количество просто растворенного в крови О 2.

• Гемоглобин содержится в крови не в растворенном состоянии, а внутри специализированных клеток - эритроцитов. • У человека эритроциты (Э) – рудиментарные клетки, не способные к самовоспроизведению. Э не содержат ядра, митохондрий, лизосом, эндоплазматического ретикулума и рибосом. Живут 120 дней. • Hb располагается на периферии эритроцита в структурированном виде, образуя гемо-липостроматиновый комплекс. • Всего в эритроците может располагаться около 34 млн молекул Hb. Состав Hb в эритроцитах меняется, начиная от эмбрионального периода и до взрослого организма. •
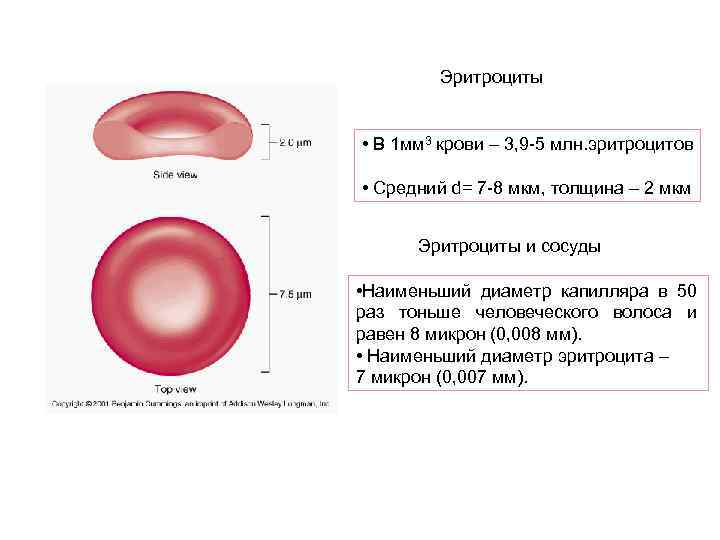
Эритроциты • В 1 мм 3 крови – 3, 9 -5 млн. эритроцитов • Средний d= 7 -8 мкм, толщина – 2 мкм Эритроциты и сосуды • Наименьший диаметр капилляра в 50 раз тоньше человеческого волоса и равен 8 микрон (0, 008 мм). • Наименьший диаметр эритроцита – 7 микрон (0, 007 мм).
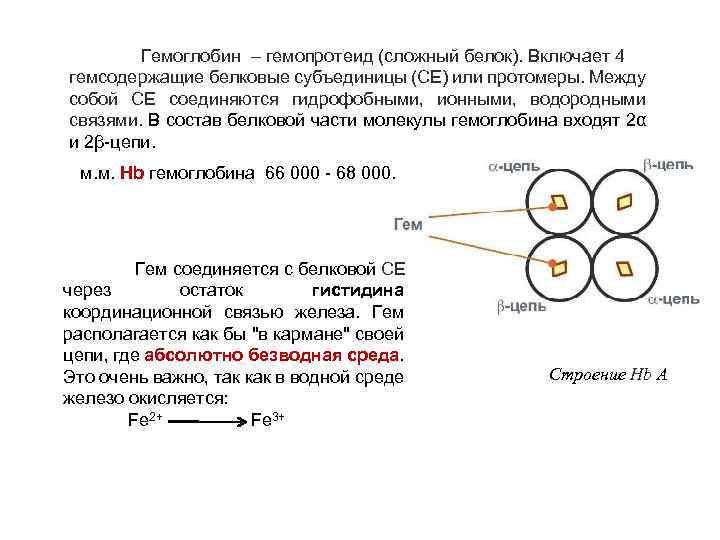
Гемоглобин – гемопротеид (сложный белок). Включает 4 гемсодержащие белковые субъединицы (СЕ) или протомеры. Между собой СЕ соединяются гидрофобными, ионными, водородными связями. В состав белковой части молекулы гемоглобина входят 2α и 2β-цепи. м. м. Нb гемоглобина 66 000 - 68 000. Гем соединяется с белковой СЕ через остаток гистидина координационной связью железа. Гем располагается как бы "в кармане" своей цепи, где абсолютно безводная среда. Это очень важно, так как в водной среде железо окисляется: Fe 2+ Fe 3+ Строение Hb А
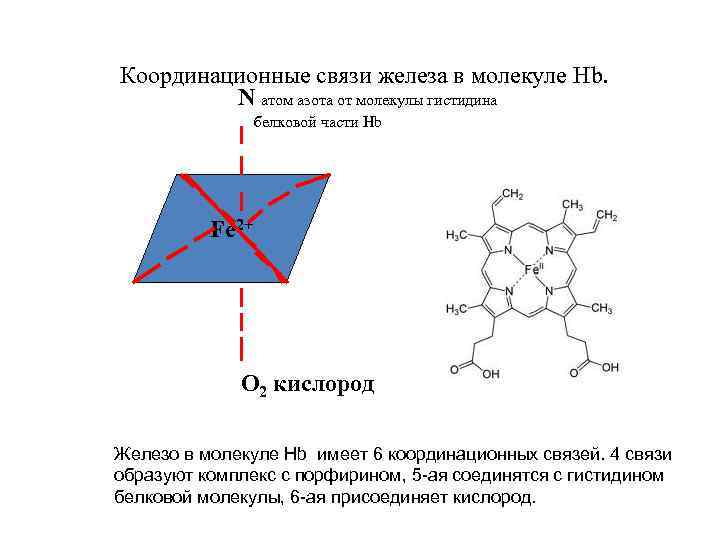
Координационные связи железа в молекуле Hb. N атом азота от молекулы гистидина белковой части Hb Fe 2+ O 2 кислород Железо в молекуле Hb имеет 6 координационных связей. 4 связи образуют комплекс с порфирином, 5 -ая соединятся с гистидином белковой молекулы, 6 -ая присоединяет кислород.

Нормальные формы гемоглобина • Hb. Р – примитивный гемоглобин, содержит 2ξ- (кси-) и 2ε-цепи (эпсилон-), встречается в эмбрионе между 7 -12 неделями жизни. • Hb. F фетальный (fetal – плод) гемоглобин, содержит 2α- и 2γ-цепи, появляется через 12 недель внутриутробного развития и является основным после 3 месяцев беременности. Обладает повышенным сродством к кислороду, менее стоек к разрушению. • Hb. A (adult - взрослый) – гемоглобин взрослых, доля составляет 98%, содержит 2α- и 2β-цепи, у плода появляется через 3 месяца жизни и к рождению составляет 80% всего гемоглобина. • Hb. A 2 – гемоглобин взрослых, доля составляет 2%, содержит 2αи 2δ-цепи (дельта-).

Функциональные формы гемоглобина • Восстановленный НHb - свободный от кислорода. • Hb. O 2 – оксигемоглобин, образуется при связывании кислорода в легких, в легочных венах его 94 -98% от всего количества гемоглобина. • Hb. CO 2 – карбгемоглобин (карбамино. Hb), образуется при связывании углекислого газа в тканях, в венозной крови составляет 15 -20% от всего количества гемоглобина. Карбгемоглобин - соединение очень нестойкое и быстро диссоциирует в легочных капиллярах с отщеплением СО 2. В виде карбаминовой формы из ткани к легким переносится от 3 до 10% (до 20%) всего углекислого газа. Основная масса СО 2 транспортируется с кровью к легким в форме бикарбоната (Na. HCO 3).

Патологические формы гемоглобина Hb. S – гемоглобин серповидно-клеточной анемии. Met. Hb – метгемоглобин, форма гемоглобина, включающая трехвалентный ион железа вместо двухвалентного. При использовании сульфаниламидов, употреблении нитратов пищевых продуктов, при недостаточности аскорбиновой кислоты ускоряется переход Fe 2+ в Fe 3+. Образующийся met. Hb не способен связывать кислород и возникает гипоксия тканей. Для восстановления ионов железа в клинике используют аскорбиновую кислоту. Hb. A 1 С – гликозилированный гемоглобин. Концентрация его нарастает при хронической гипергликемии и является хорошим скрининговым показателем уровня глюкозы крови за длительный период времени.

Hb. CO – карбоксигемоглобин, образуется при наличии СО (угарный газ) во вдыхаемом воздухе. Угарный газ является активным ингибитором гемсодержащих ферментов (цитохромоксидазы а 3 дыхательной цепи). СО - оксид С (II) – угарный газ – продукт неполного окисления С. Не имеет запаха. Попадая в легкие быстро проходит ч/з альвеолярнокапиллирную мембрану, растворяется в плазме крови, диффундирует в эритроциты и вступает в химическое взаимодействие с Hb: Hb. О 2 + СО = Hb. СО + О 2 карбокси. Hb Карбоксигемоглобин, прочный комплекс, который неспособен осуществлять перенос кислорода. Сродство гемоглобина к угарному газу выше его сродства к кислороду, поэтому даже небольшое количество угарного газа в воздухе (более 0, 1% CO в воздухе) является опасным для жизни.
Расщепление карбокси. Hb на Hb и CO происходит в 10 000 раз медленнее, чем расщепление оксигемоглобина на Hb и O 2. Поэтому уровень карбокси. Hb у курящих в 15 раз выше, чем у некурящих.

Миоглобин

Миоглобин – мономер, состоит из 153 аминокислот с мм 17 000 Dа и по структуре сходен с β-цепью гемоглобина. Белок локализован в мышечной ткани. Миоглобин обладает более высоким сродством к кислороду по сравнению с гемоглобином. Это свойство обусловливает функцию миоглобина – депонирование кислорода в мышечной клетке и использование его только при значительном уменьшении парциального давления О 2 в мышце (ниже 10 мм рт. ст).

Гемоглобин – тетрамер (4 СЕ), которые содержат 4 гема, 4 иона Fe 2+ - обратимо связывает четыре молекулы кислорода. Рис. Кривые насыщения кислородом миоглобина и гемоглобина При парциальном Р кислорода 1 -2 мм рт. ст. миоглобин на 50% насыщен кислородом. Кривая насыщения имеет вид гиперболы. При парциальном Р 20 мм рт. ст. – насыщение 95%. 2
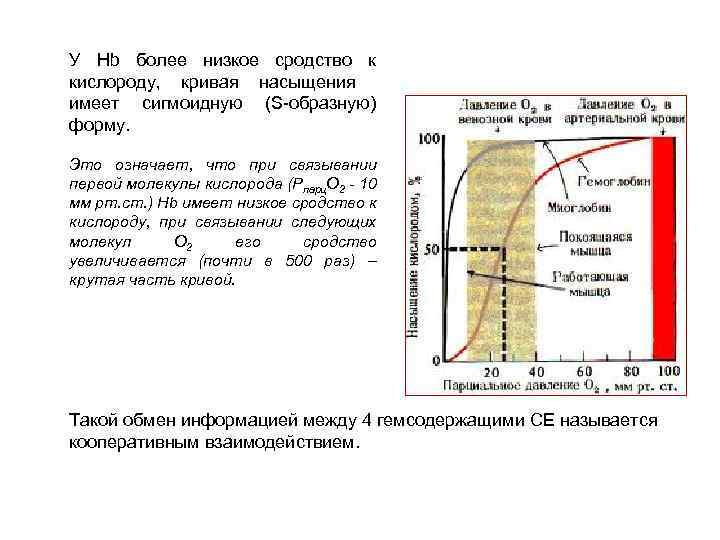
У Hb более низкое сродство к кислороду, кривая насыщения имеет сигмоидную (S-образную) форму. Это означает, что при связывании первой молекулы кислорода (Рпарц. О 2 - 10 мм рт. ст. ) Hb имеет низкое сродство к кислороду, при связывании следующих молекул О 2 его сродство увеличивается (почти в 500 раз) – крутая часть кривой. Такой обмен информацией между 4 гемсодержащими СЕ называется кооперативным взаимодействием.
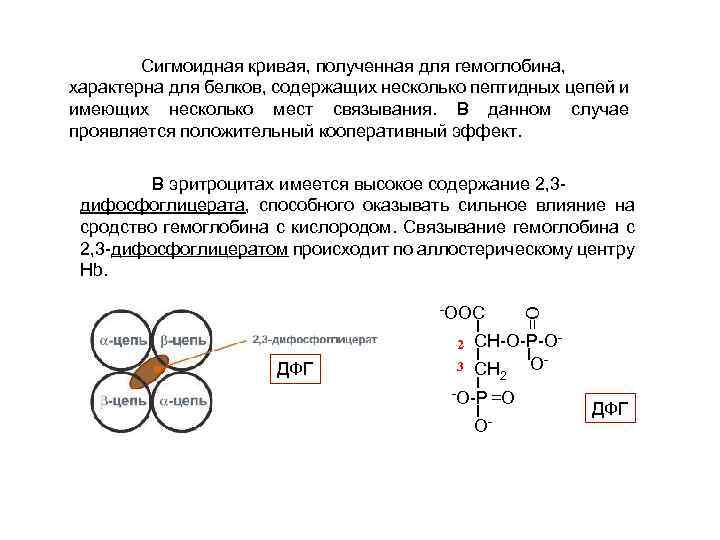
Сигмоидная кривая, полученная для гемоглобина, характерна для белков, содержащих несколько пептидных цепей и имеющих несколько мест связывания. В данном случае проявляется положительный кооперативный эффект. В эритроцитах имеется высокое содержание 2, 3 дифосфоглицерата, способного оказывать сильное влияние на сродство гемоглобина с кислородом. Связывание гемоглобина с 2, 3 -дифосфоглицератом происходит по аллостерическому центру Hb. 2 ДФГ 3 =О -ООС СН-О-Р-ООСН 2 -О-Р =О О- ДФГ

2, 3 -Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с βцепями, образуя связь между атомами кислорода 2, 3 -ДФГ и аминогруппами концевого валина обеих β-цепей. Функция 2, 3 -дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду. Это имеет особенное значение при подъеме на высоту, при нехватке кислорода во вдыхаемом воздухе. В тканях за счет увеличения содержания 2, 3 -дифосфоглицерата отдача кислорода возрастает в 2 раза. Такое повышение наблюдается у людей при гипоксии, вызванной заболеваниями легких.

Изменение р. Н среды 7, 4 Влияние р. Н на сродство гемоглобина к кислороду носит название эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается. При повышении концентрации Н+ (снижение р. Н) в тканях возрастает освобождение кислорода из оксигемоглобина. Кроме кислорода Hb осуществляет перенос двух конечных продуктов тканевого дыхания Н+ и СО 2. Перенос протонов (1 молекула Hb может переносить 4 Н+ ) делает гемоглобин участником буферной системы.
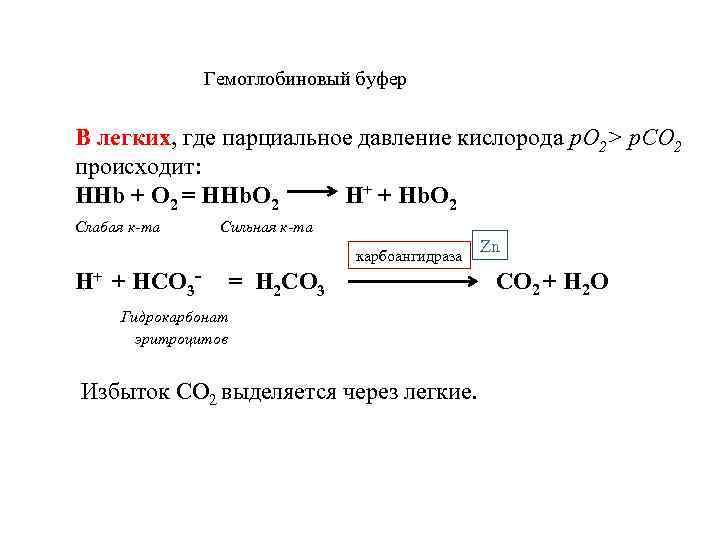
Гемоглобиновый буфер В легких, где парциальное давление кислорода р. О 2> р. СО 2 происходит: HHb + О 2 = HHb. О 2 H+ + Hb. О 2 Слабая к-та Сильная к-та H+ + НСО 3 - карбоангидраза = Н 2 СО 3 Гидрокарбонат эритроцитов Избыток СО 2 выделяется через легкие. Zn СО 2 + H 2 О
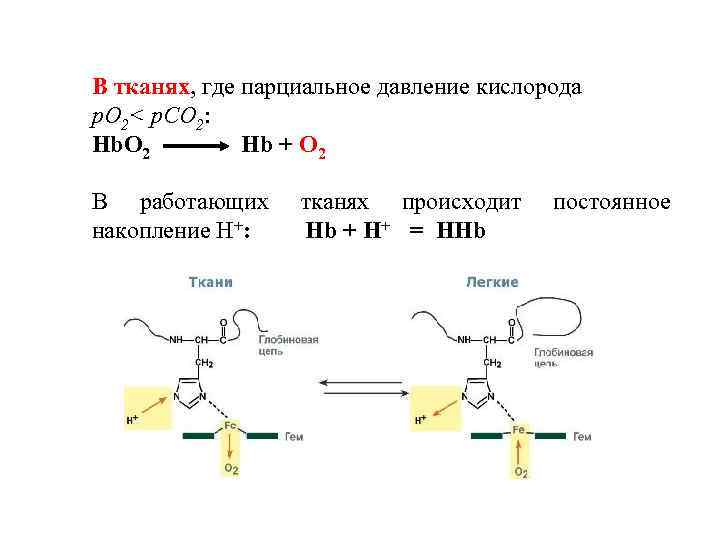
В тканях, где парциальное давление кислорода р. О 2< р. СО 2: Hb. О 2 Hb + О 2 В работающих накопление Н+: тканях происходит Hb + Н+ = НHb постоянное
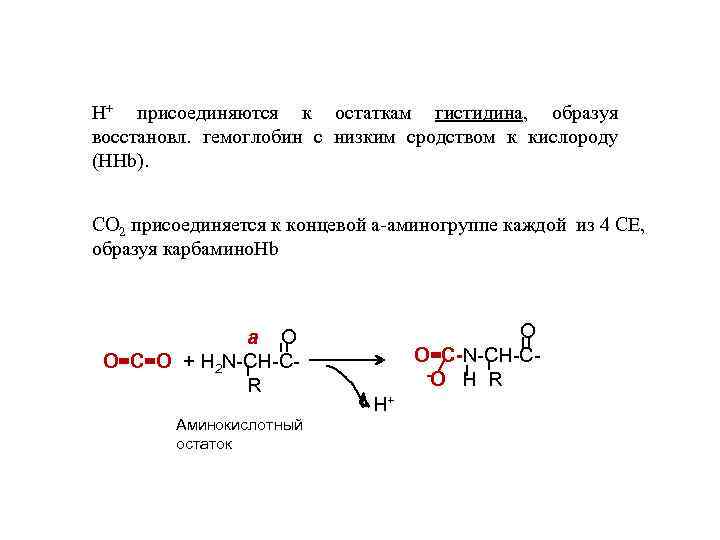
Н+ присоединяются к остаткам гистидина, образуя восстановл. гемоглобин с низким сродством к кислороду (НHb). СО 2 присоединяется к концевой а-аминогруппе каждой из 4 СЕ, образуя карбамино. Hb a О О=С=О + H 2 N-CH-CR Аминокислотный остаток О О=С-N-CH-C-О Н R Н+
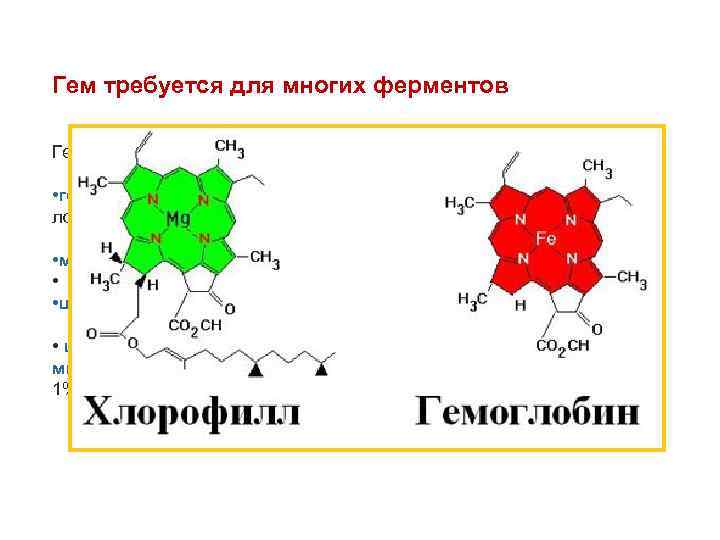
Гем требуется для многих ферментов Гем является небелковой частью многих гемопротеинов: • гемоглобин (до 85% общего количества гема организма) локализован в эритроцитах и клетках костного мозга • миоглобин скелетных мышц и миокарда (17%) • • цитохромы дыхательной цепи и P 450 • цитохромоксидаза, гомогентизатоксидаза, пероксидаза, миелопероксидаза, каталаза, тиреопероксидаза и т. д. – менее 1%.
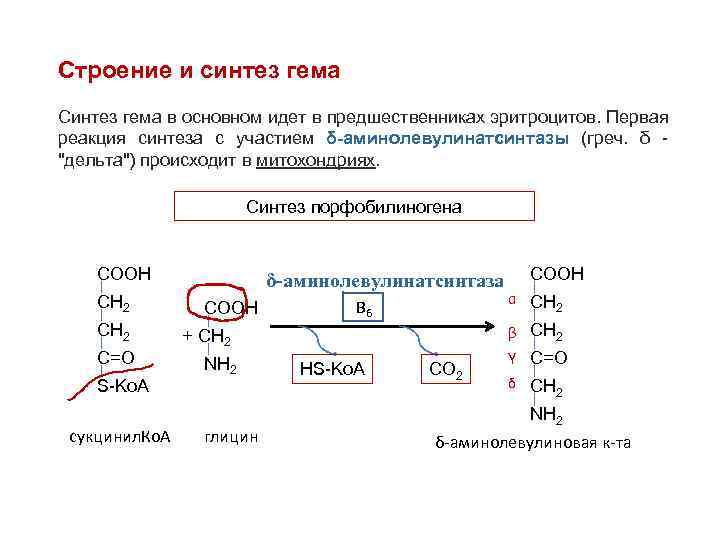
Строение и синтез гема Синтез гема в основном идет в предшественниках эритроцитов. Первая реакция синтеза с участием δ-аминолевулинатсинтазы (греч. δ "дельта") происходит в митохондриях. Синтез порфобилиногена СООН СН 2 С=О S-Ko. A сукцинил. Ко. А δ-аминолевулинатсинтазa СООН глицин HS-Ko. A СО 2 α СН 2 β В 6 + СН 2 NН 2 СООН СН 2 γ С=О δ СН 2 NН 2 δ-аминолевулиновая к-та
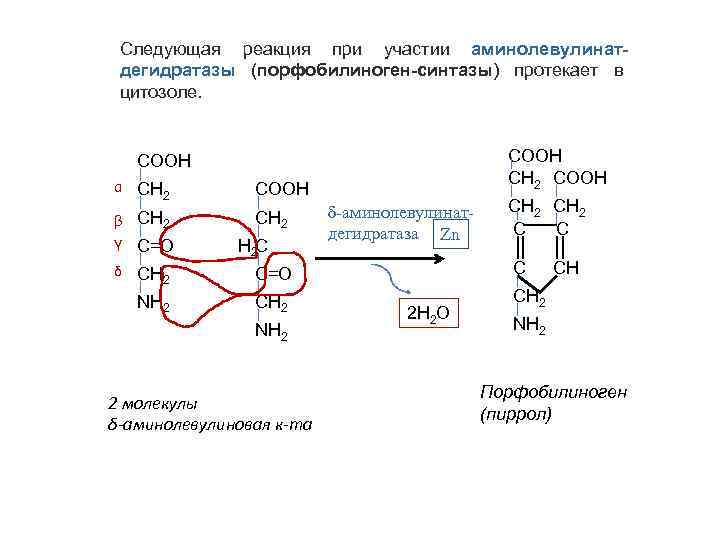
Следующая реакция при участии аминолевулинатдегидратазы (порфобилиноген-синтазы) протекает в цитозоле. СООН СН 2 СООН α СН 2 СООН β СН 2 γ С=О δ СН 2 С=О С NН 2 СН 2 Н 2 С NН 2 2 молекулы δ-аминолевулиновая к-та δ-аминолевулинатдегидратаза Zn 2 Н 2 О СН 2 С С СН NН 2 Порфобилиноген (пиррол)
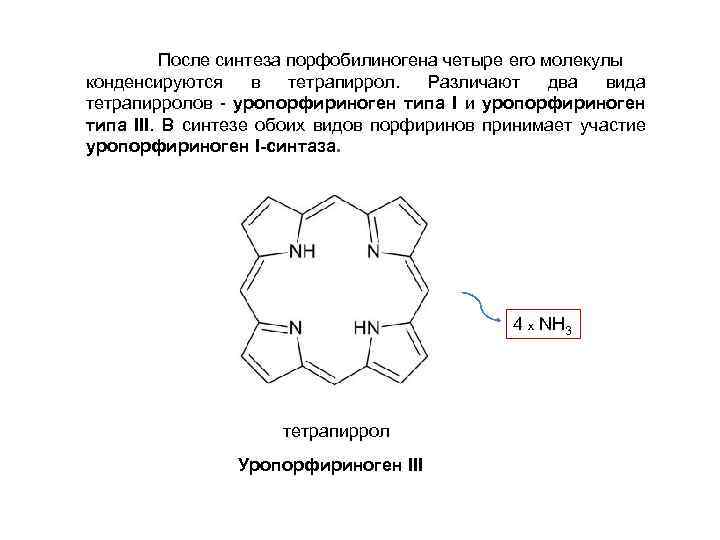
После синтеза порфобилиногена четыре его молекулы конденсируются в тетрапиррол. Различают два вида тетрапирролов - уропорфириноген типа I и уропорфириноген типа III. В синтезе обоих видов порфиринов принимает участие уропорфириноген I-синтаза. 4 х NН 3 тетрапиррол Уропорфириноген III
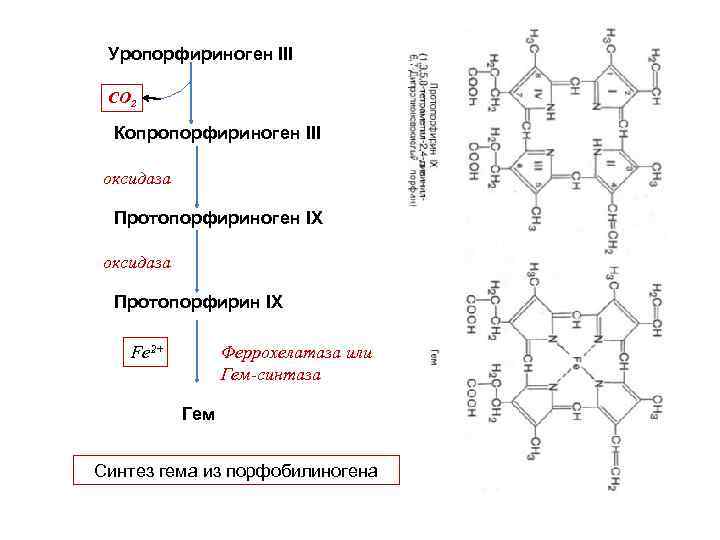
Уропорфириноген III СО 2 Копропорфириноген III оксидаза Протопорфириноген IX оксидаза Протопорфирин IX Fe 2+ Феррохелатаза или Гем-синтаза Гем Синтез гема из порфобилиногена

Регуляция синтеза гема 1. Основным регуляторным ферментом синтеза гема является аллостерический фермент аминолевулинатсинтаза • гем после взаимодействия с молекулой белка-репрессора формирует активный репрессорный комплекс, связывается с ДНК и подавляет транскрипцию м. РНК для фермента, синтез фермента прекращается. • гем оказывает отрицательный аллостерический эффект на фермент. 2. Положительные модуляторы аминолевулинатсинтазы: • гипоксия тканей, которая в эритропоэтических тканях индуцирует синтез фермента. • достаточное количество ионов железа • стероидные гормоны

У гемоглобина есть молекулярные болезни Серповидно-клеточная анемия Hb. S – гемоглобин серповидно-клеточной анемии. В ДНК в результате точковой мутации происходит включение в 6 -м положении β-цепи аминокислоты валин вместо глутаминовой к-ты. Замена гидрофильной а. к. на гидрофобную влечет изменение свойств всей молекулы и формирование на поверхности гемоглобина "липкого" участка. При дезоксигенации гемоглобина (отдача О 2) участок "раскрывается" и связывает одну молекулу гемоглобина S с другими подобными. Результатом является полимеризация гемоглобиновых молекул и образование крупных белковых тяжей, вызывающих деформацию эритроцита и гемолиз.
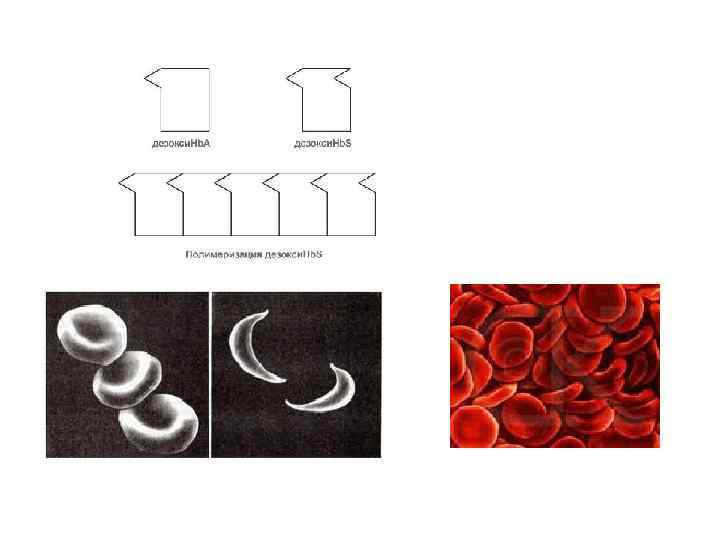
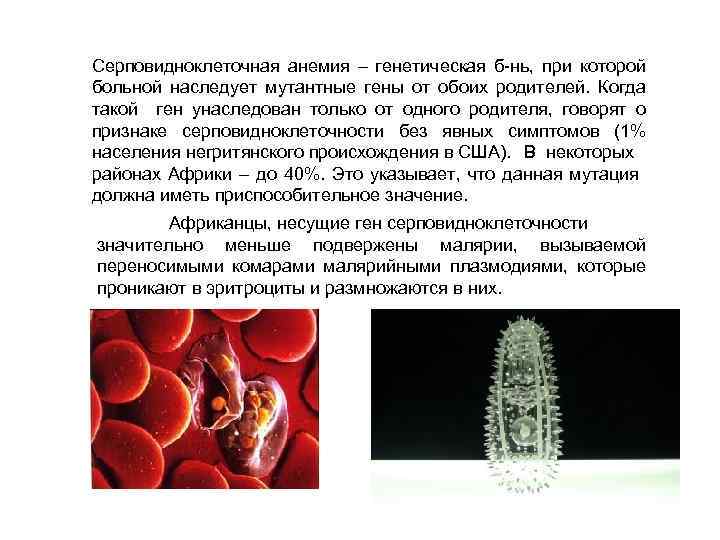
Серповидноклеточная анемия – генетическая б-нь, при которой больной наследует мутантные гены от обоих родителей. Когда такой ген унаследован только от одного родителя, говорят о признаке серповидноклеточности без явных симптомов (1% населения негритянского происхождения в США). В некоторых районах Африки – до 40%. Это указывает, что данная мутация должна иметь приспособительное значение. Африканцы, несущие ген серповидноклеточности значительно меньше подвержены малярии, вызываемой переносимыми комарами малярийными плазмодиями, которые проникают в эритроциты и размножаются в них.

Из журнала Science (11. 2011): “Когда в клетку проникает малярийный паразит, он начинает использовать цитоскелет эритроцитов в своих целях. Из актиновых филаментов, протянутых под мембраной, плазмодий конструирует транспортную систему, с помощью которой отправляет наружу собственный белок адгезин. Этот адгезин (от лат. adhaesio прилипание), переброшенный на наружную сторону мембраны эритроцитов, делает клетки крови липкими. Эритроциты слипаются и оседают на стенках сосудов: это происходит, когда паразиту на очередном этапе жизненного цикла нужно выйти из кровотока”. Оказалось, что в клетках с серповидноклеточной мутацией плазмодию трудно заставить цитоскелет работать на себя.
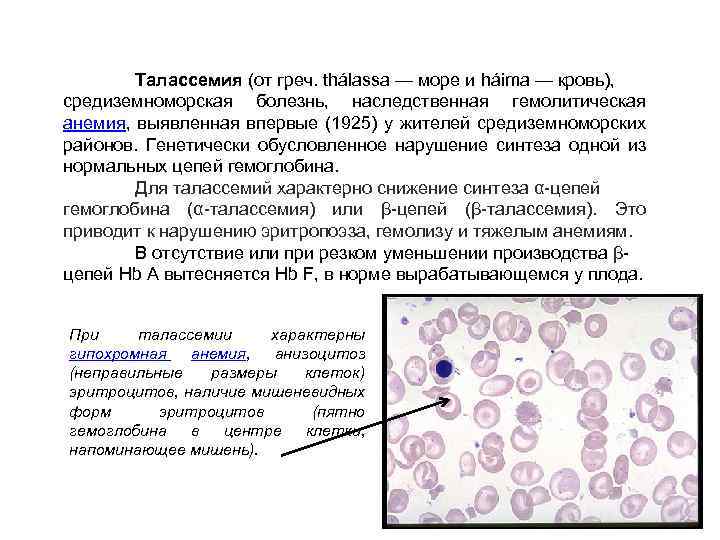
Талассемия (от греч. thálassa — море и háima — кровь), средиземноморская болезнь, наследственная гемолитическая анемия, выявленная впервые (1925) у жителей средиземноморских районов. Генетически обусловленное нарушение синтеза одной из нормальных цепей гемоглобина. Для талассемий характерно снижение синтеза α-цепей гемоглобина (α-талассемия) или β-цепей (β-талассемия). Это приводит к нарушению эритропоэза, гемолизу и тяжелым анемиям. В отсутствие или при резком уменьшении производства βцепей Hb А вытесняется Hb F, в норме вырабатывающемся у плода. При талассемии характерны гипохромная анемия, анизоцитоз (неправильные размеры клеток) эритроцитов, наличие мишеневидных форм эритроцитов (пятно гемоглобина в центре клетки, напоминающее мишень).
Нарушение синтеза гемоглобина Порфирии – это группа гетерогенных наследственных заболеваний, возникающих в результате нарушения синтеза гема и повышения содержания порфиринов и их предшественников в организме. Выделяют наследственные и приобретенные формы порфирии. Приобретенные формы порфирий носят токсический характер и вызываются действием гексахлорбензола, солей свинца и других тяжелых металлов (ингибирование порфобилиногенсинтазы, феррохелатазы и др. ), лекарственными препаратами (антигрибковый антибиотик гризеофульфин). гексахлорбензол
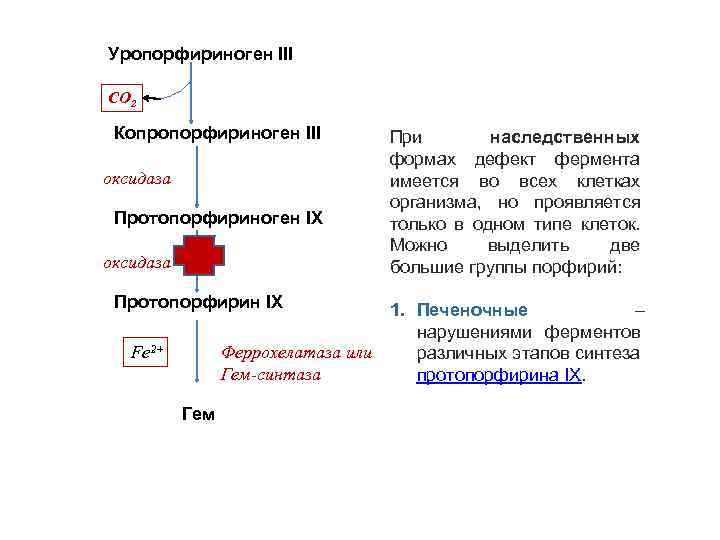
Уропорфириноген III СО 2 Копропорфириноген III оксидаза Протопорфириноген IX оксидаза Протопорфирин IX При наследственных формах дефект фермента имеется во всех клетках организма, но проявляется только в одном типе клеток. Можно выделить две большие группы порфирий: 1. Печеночные – нарушениями ферментов Феррохелатаза или различных этапов синтеза Гем-синтаза протопорфирина IX. Fe 2+ Гем

Заболевание проявляется после достижения половой зрелости из-за повышенной потребности гепатоцитов в цитохроме Р 450 для обезвреживания половых стероидов. Обострение состояния также часто бывает после приема лекарственных препаратов, метаболизм которых требует участия цитохрома Р 450. Потребление и снижение концентрации гема, необходимого для синтеза цитохрома Р 450, активирует аминолевулинатсинтазу. В результате больные экскретируют с мочой большие количества порфобилиногена и аминолевулиновой кислоты. На свету порфобилиноген окисляется в окрашенные порфобилин и порфирин, и это является причиной потемнения мочи при ее стоянии на свету при доступе воздуха.

2. Эритропоэтические – аутосомно-рецессивные нарушения некоторых ферментов синтеза протопорфирина IX в эритроидных клетках. При этом смещается баланс реакций образования уропорфириногенов в сторону синтеза уропорфириногена I. Симптомы заболевания схожи с предыдущим, но дополнительно наблюдаются гемолитические явления и светочувствительность кожи, обусловленная наличием уропорфириногенов.
Гемоглобин.ppt