Минеральный обмен.ppt
- Количество слайдов: 54

НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ Кафедра медицинской химии МИНЕРАЛЬНЫЙ ОБМЕН профессор, доктор медицинских наук Потеряева Ольга Николаевна 29 февраля 2012 г.

Цель – выявить биологическую активность химических элементов, составляющих минеральную основу организма. План лекции 1. Что такое минеральный обмен. 2. Макроэлементы: Ca, P, Mg Микроэлементы: Fe, Cu, F, I, Se, Zn 3. Суточная потребность, содержание в продуктах, биологическая роль. Минеральный обмен – совокупность процессов всасывания, усвоения, распределения, превращения и выделения из организма тех веществ, которые находятся в нём преимущественно в виде неорганических соединений.

Крупнейший русский ученый Владимир Иванович Вернадский (1863 -1945) положил начало исследованиям биологической роли химических элементов (основатель биогеохимии). В организме было обнаружено свыше 70 элементов таблицы Менделеева, 47 из них присутствуют постоянно и называются биогенными. Большинство химических элементов в ПСЭ представлены металлами, но природа использует в качестве материалов для строительства живых организмов, главным образом неметаллы. Пять Э составляют органическую основу живых организмов: О - 62, 4%, С - 21, 2%, Н – 9, 7%, N -3, 1% и S ˂ 1%, т. е. более 96% веса. Н 2 N-C-NН 2 O Мочевина (продукт обезвреживания аммиака) Н 2 N-СН-СООН СН 2 S- СН 3 аминокислота – метионин

5 основных макроэлементов входят в состав воды (60%), белков (18%), жиров (15%) и углеводов (3%). Остальные элементы (чуть более 3%), не входящие в органическую основу, принято считать минеральными. Из минеральных компонентов 75% приходится на долю кальция, фосфора и магния. По количественному содержанию в организме минеральные компоненты делятся на макроэлементы, если их больше чем 0, 01 % от массы тела (К, Na, P, Cl, Са, Мg) и микроэлементы (Cu, Zn, Cr, Mn, Fe, Co, Se, F, I). Главным критерием, по которому обычно отличают макро- и микроэлементы является ежедневная суточная потребность организма в элементе. Макроэлемент - потребность 100 мг в сутки, микроэлемент – не превышает 10 мг в сутки (и даже мкг).

Основное значение минеральных компонентов заключается: 1. Поддержание гомеостаза внутренней среды организма кислотно-щелочного резерва (КЩР) крови, осмотического давления, буферной емкости (калий, натрий, хлор, фосфор). 2. Формирование и сохранение структур плотных тканей, например скелета (кальций, фосфор, магний, фтор). 3. Специфическая регуляция ферментативных реакций, где макроили микроэлементы участвуют в качестве кофактора; 4. Детоксикация (железо в составе цитохрома Р-450). 5. Основа биоэлектрических явлений: проведение нервного импульса, мышечное сокращение (натрий, кальций). 6. Участие в системе свертывания крови (кальций). 7. Гормональной регуляция (йод, цинк входят в состав гормонов). 8. Входят в состав комплексных соединений (гемоглобин, миоглобин, цитохромы, вит. В 12).
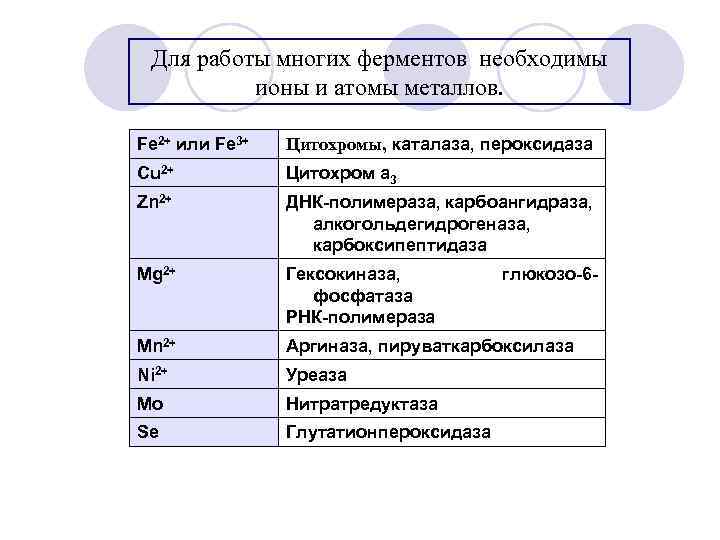
Для работы многих ферментов необходимы ионы и атомы металлов. Fe 2+ или Fe 3+ Цитохромы, каталаза, пероксидаза Cu 2+ Цитохром а 3 Zn 2+ ДНК-полимераза, карбоангидраза, алкогольдегидрогеназа, карбоксипептидаза Mg 2+ Гексокиназа, фосфатаза РНК-полимераза Mn 2+ Аргиназа, пируваткарбоксилаза Ni 2+ Уреаза Mo Нитратредуктаза Se Глутатионпероксидаза глюкозо-6 -

Макро-и микроэлементы неравномерно распределяются между клеткой и средой. У человека в плазме крови, межклеточной и спинномозговой жидкостях из катионов преобладает Na+, из анионов — Cl- и HCO 3 -. Внутри большинства клеток из катионов преобладает К+; содержание Mg 2+ в клетках выше, чем в плазме крови. Минеральный состав жидкостей, выделяемых поджелудочной, молочной и др. железами, значительно отличается от плазмы крови и обусловлен специфической секреторной активностью клеток железистого эпителия. (см. табл. ).
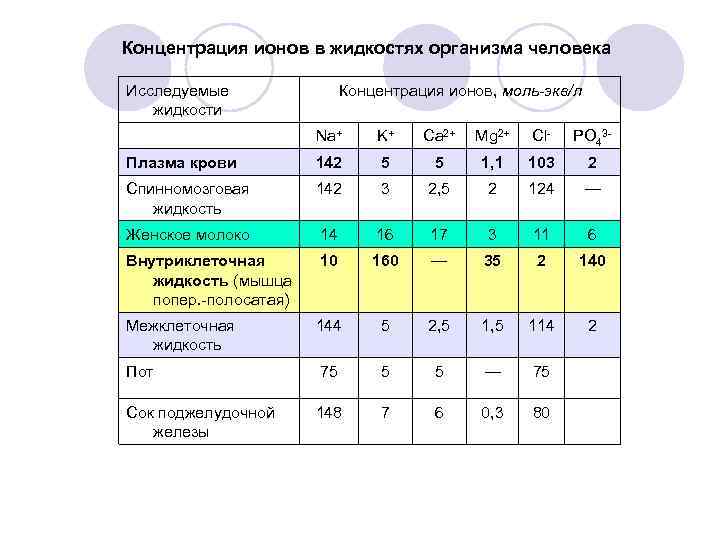
Концентрация ионов в жидкостях организма человека Исследуемые жидкости Концентрация ионов, моль-экв/л Na+ K+ Ca 2+ Mg 2+ Сl- PO 43 - Плазма крови 142 5 5 1, 1 103 2 Спинномозговая жидкость 142 3 2, 5 2 124 — Женское молоко 14 16 17 3 11 6 Внутриклеточная жидкость (мышца попер. -полосатая) 10 160 — 35 2 140 Межклеточная жидкость 144 5 2, 5 114 2 Пот 75 5 5 — 75 Сок поджелудочной железы 148 7 6 0, 3 80

К альций Суточная потребность у взрослых людей до 800 мг. Беременным, кормящим женщинам и подросткам – до 1500 мг. Основные источники – молоко, твердые сыры, творог и др. молочные продукты. (Кальцием богаты люцерна и ботва сахарной свеклы). Из всего алиментарного Са 2+ (поступившего с пищей) в кишечнике усваивается только 30 -50%.

В организме взрослого человека содержится более 1 кг кальция (~1, 4% от всего веса организма). Са 2+ почти целиком находится в костях и зубах (97%) и лишь 3% в биологических жидкостях и мягких тканях. Са и Р формируют основное неорганическое вещество костной и зубной ткани в виде гидроксиапатитов: 75% гидроксиапатита 3 Са 3(РО 4)2 Са(ОН)2 20% карбоапатита 3 Са 3(РО 4)2 Са. СО 3 0, 7% фторапатита 3 Са 3(РО 4)2 Са(ОН)F

В плазме крови человека - 2, 2 -2, 75 ммоль/л. 2 формы Са 2+: половина связана с органическими фосфатами и белками и свободные ионы Са 2+ - 1, 2 ммоль/л. Внутри клетки, в ее цитоплазме – концентрация ионов Са 2+ в 10 000 раз меньше (100 нмолей) - «кальциевый вакуум» . Для его поддержания в мембранах клетки функционируют сложно организованные белки, обеспечивающие вход ионов Са 2+ в цитоплазму по градиенту концентрации (Са 2+ - каналы), а также системы активного транспорта против градиента концентрации с использованием энергии АТФ (Са 2+ - насосы).

Согласованное функционирование систем пассивного и активного транспорта ионов Са 2+ через цитоплазматическую мембрану позволяет поддерживать его содержание в клетке на низком (базальном) уровне. Кратковременное (транзиторное) повышение концентрации Са 2+ (от 10 -7 до 10 -5 сек) клетка воспринимает как регуляторный сигнал. Повышение ионов Са 2+ в цитоплазме на продолжительное время (в течение десятков минут) приводит к гибели клеток.

Основная функция Са 2+ в клетке заключается в передаче регуляторных сигналов. q Ионы Са 2+ являются вторичными посредниками действия гормонов и медиаторов (А, НА, АХ, серотонин, вазопрессин, факторы роста). Увеличение кальция в невозбудимых клетках (клетки крови, гепатоциты, эндотелий сосудов) приводит к изменению метаболизма, морфологии, пролиферации, секреции клетки. q В возбудимых клетках (нейроны, мышечные волокна) при входе ионов Са 2+ в клетку происходит деполяризация мембраны, в рез-те мышцы сокращаются или происходит передача нервного импульса.

В плазме крови ионы Са 2+, несвязанные с фосфатами и белками, участвуют в свертывании крови. Са является IV фактором (из 13) свёртывания. Удаление Са 2+ из крови (декальцинирование) приводит к тому, что кровь не свёртывается! Са 2+ - в 104 -105 раз повышает скорость образования тромба.
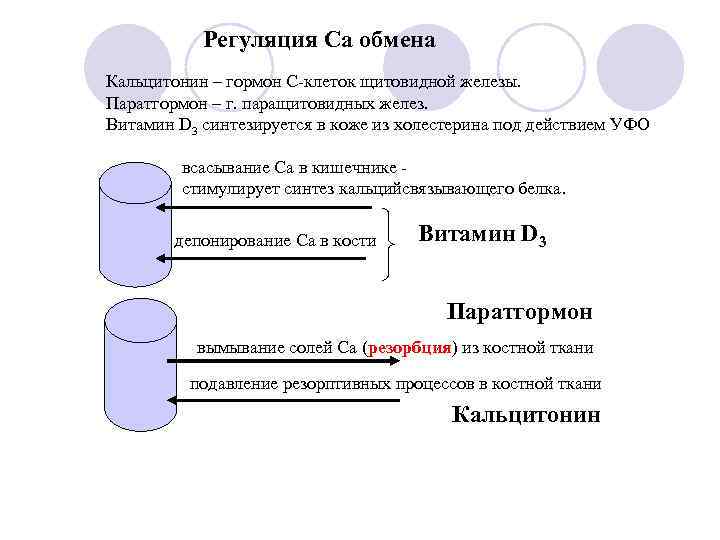
Регуляция Са обмена Кальцитонин – гормон С-клеток щитовидной железы. Паратгормон – г. паращитовидных желез. Витамин D 3 синтезируется в коже из холестерина под действием УФО всасывание Са в кишечнике стимулирует синтез кальцийсвязывающего белка. депонирование Са в кости Витамин D 3 Паратгормон вымывание солей Са (резорбция) из костной ткани подавление резорптивных процессов в костной ткани Кальцитонин
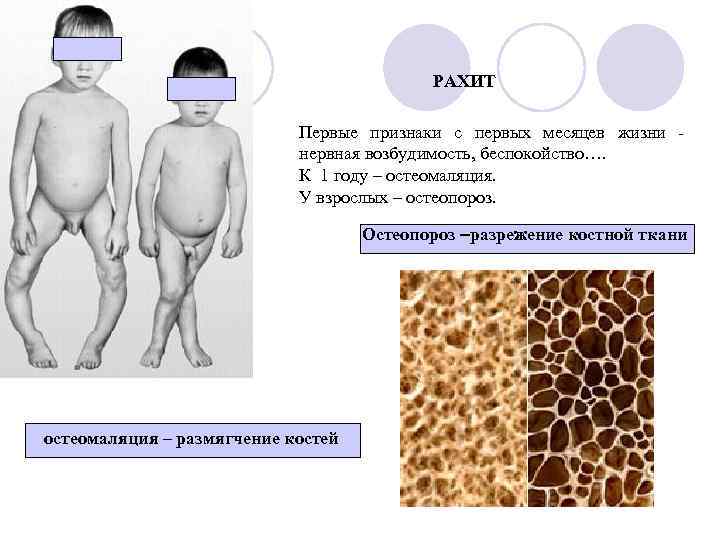
РАХИТ Первые признаки с первых месяцев жизни нервная возбудимость, беспокойство…. К 1 году – остеомаляция. У взрослых – остеопороз. Остеопороз –разрежение костной ткани остеомаляция – размягчение костей

ФОСФОР Суточная потребность 1200 -2000 мг/сут. Распространен в мясе, рыбе, молочных продуктах (молоко, сыр). Много - в фасоли, горохе, крупах (овсяной, перловой, ячневой), орехах, капусте, моркови, чесноке, шпинате. Пищевая недостаточность фосфатов практически не встречается.

Содержание Р в организме 1% от массы тела. 1. 85 -87% находится в костной ткани и зубной эмали. Са 2+ образует с фосфором плохо растворимые солифосфаты: Са 3(РО 4)2 Са. НРО 4 Са(Н 2 РО 4)2 в порядке увеличения растворимости. Соотношение Са: Р = 2: 1
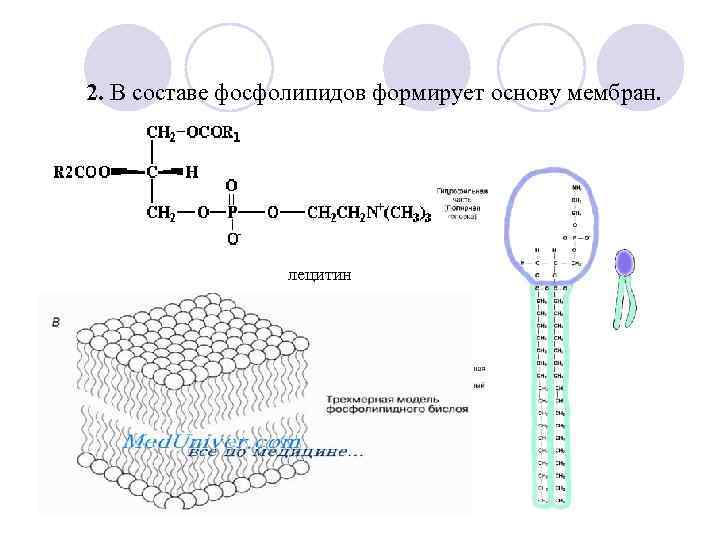
2. В составе фосфолипидов формирует основу мембран. лецитин
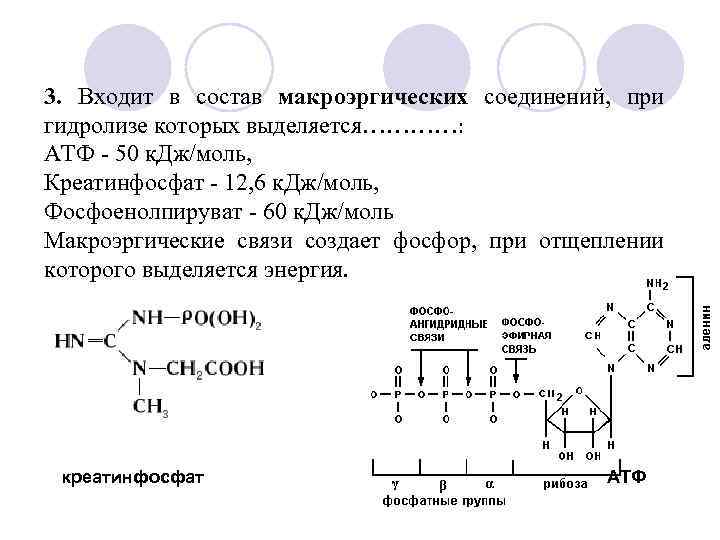
3. Входит в состав макроэргических соединений, при гидролизе которых выделяется…………: АТФ - 50 к. Дж/моль, Креатинфосфат - 12, 6 к. Дж/моль, Фосфоенолпируват - 60 к. Дж/моль Макроэргические связи создает фосфор, при отщеплении которого выделяется энергия. креатинфосфат АТФ
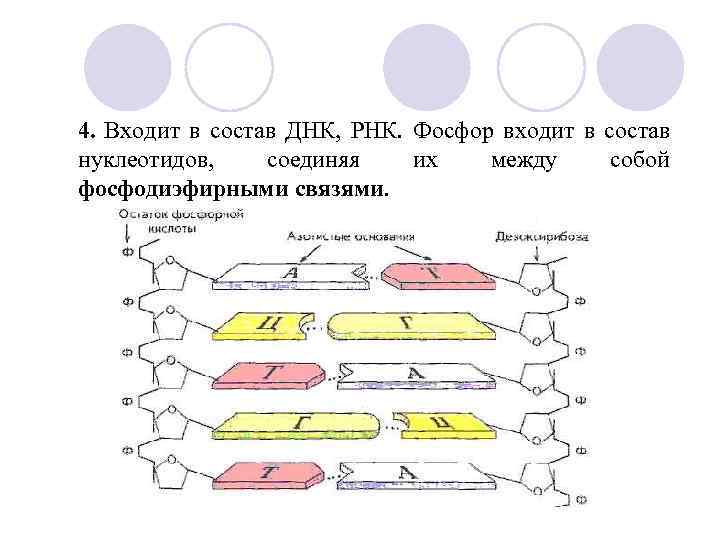
4. Входит в состав ДНК, РНК. Фосфор входит в состав нуклеотидов, соединяя их между собой фосфодиэфирными связями.

5. Входят в состав фосфатной буферной системы. Na. Н 2 РО 4 Дигидрофосфат Выполняет роль слабой к-ты Na 2 НРО 4 гидрофосфат натрия соль данной к-ты и сильного основания Играет важную роль в поддержании р. Н внутриклеточной жидкости и слюны.

МАГНИЙ Суточная потребность 500— 600 мг/сут. Хлорофилл зеленых овощей. Цельные орехи, бобы, зерновая завязь, необработанные злаки (удаление оболочки из зародышевых слоев до 80% снижает содержание), гречка. Мед. Какао (шоколад).
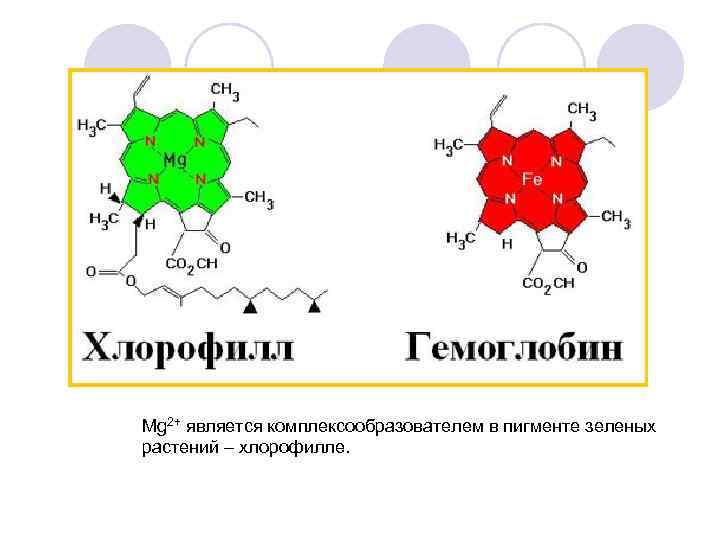
Mg 2+ является комплексообразователем в пигменте зеленых растений – хлорофилле.

Всего в организме 40 г Mg 2+ (~ 0, 06%). Половина находится в костной ткани. Mg 2+ находится внутри клеток – второй по содержанию внутриклеточный катион (после калия). Содержание его в клетке в 10 – 30 раз выше, чем в плазме. 1. Играет важную роль в поддержании К, Nа-гомеостаза. ¶ участвует в передачи нервного импульса ¶ поддерживает осмотического давления внутри клетки Магний необходим для работы транспортного белка Na+/К+-АТФазы, которая регулирует выброс Na из клетки (против градиента концентрации.
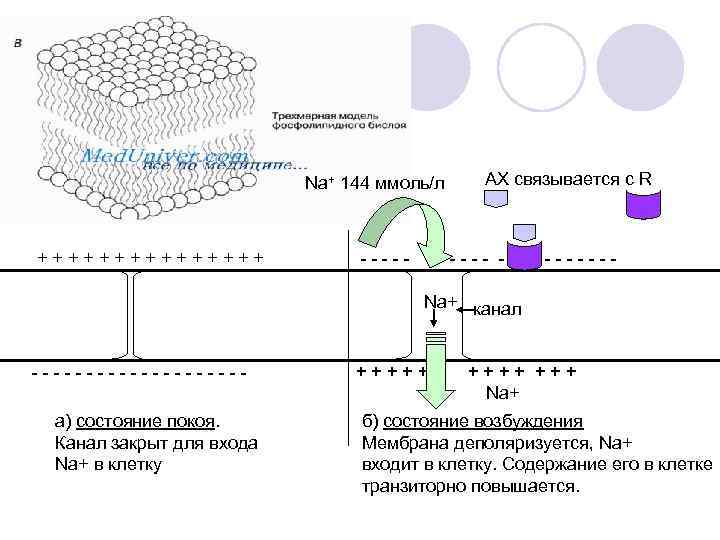
Na+ 144 ммоль/л + + + + - - - АХ связывается с R ---- - - - - Na+ канал ----------а) состояние покоя. Канал закрыт для входа Na+ в клетку +++++ +++ Na+ б) состояние возбуждения Мембрана деполяризуется, Na+ входит в клетку. Содержание его в клетке транзиторно повышается.

2. Придает прочность зубам. 3. Активатор АТФ - зависимых реакций: а) трансляция белка (синтез белка) б) синтез РНК, ДНК из нуклеотидов Во внутриклеточной жидкости АТФ присутствуют в виде активных комплексов: Mg 2+ + АТФ 4 - = Mg. АТФ 2 Mg 2+ + АДФ 3 - = Mg. АТФ- и АДФ
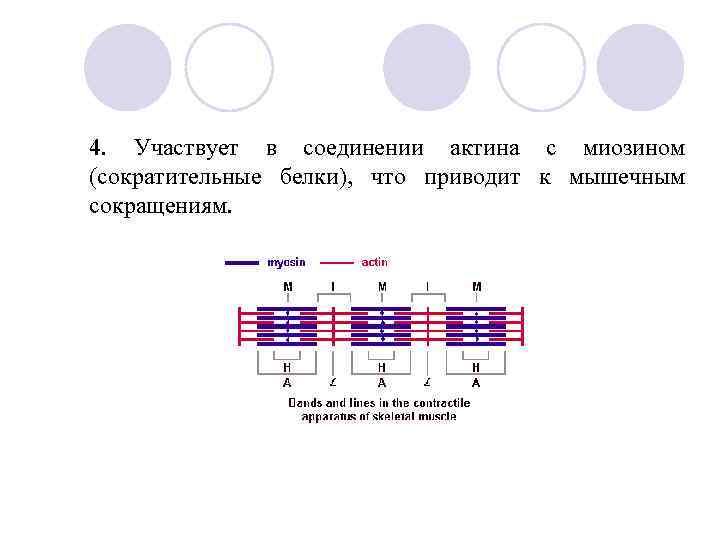
4. Участвует в соединении актина с миозином (сократительные белки), что приводит к мышечным сокращениям.

Магний выводится из организма при употреблении спиртных напитков, крепкого кофе и чая. Дефицит магния встречается часто и проявляется нарушением психики: повышенная раздражительность, утомляемость, плохой сон. При недостатке магния могут появляться мышечные подергивания, замедление роста, нарушение нервно-мышечной деятельности. Ионы Mg 2+ (Mg. SO 4), введенные в/в, вызывают угнетение ЦНС, снижают кровяное давление, расслабляют тонус желчевыводящих путей. Mg. SO 4× 7 H 2 O (горькая соль) – слабительное средство.

железо Суточная потребность 12 -15 мг, в некоторых случаях до 30 мг. Содержится в животных продуктах: печени, мясе, кровяной колбасе, желтках. Несколько меньше железа содержат растительные продукты: брусника, черника, гранаты. Такое же содержание в цельном зерне, фасоли, шпинате, семенах тыквы и подсолнечника. Молоко содержит очень мало железа (поэтому детей нельзя больше года держать только на молочной диете).

В организме человека содержится около 3, 5 г железа (~ 0, 005% от всего веса человека). В кишечнике Fe 2+, соединяясь с апоферритином ферритин В крови транспортируется специальным белком – трансферрином. Основная масса сконцентрирована в дыхательном пигменте эритроцитов – гемоглобине, в миоглобине и цитохромах – ферментах тканевого дыхания.
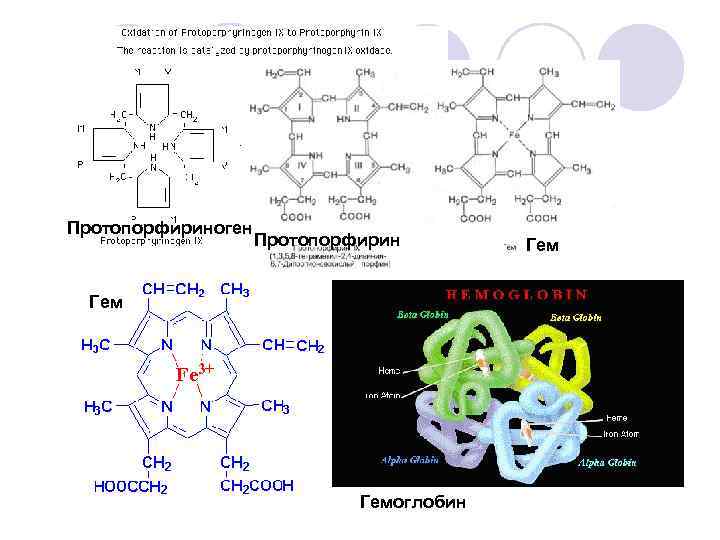
Протопорфириноген Протопорфирин Гемоглобин Гем
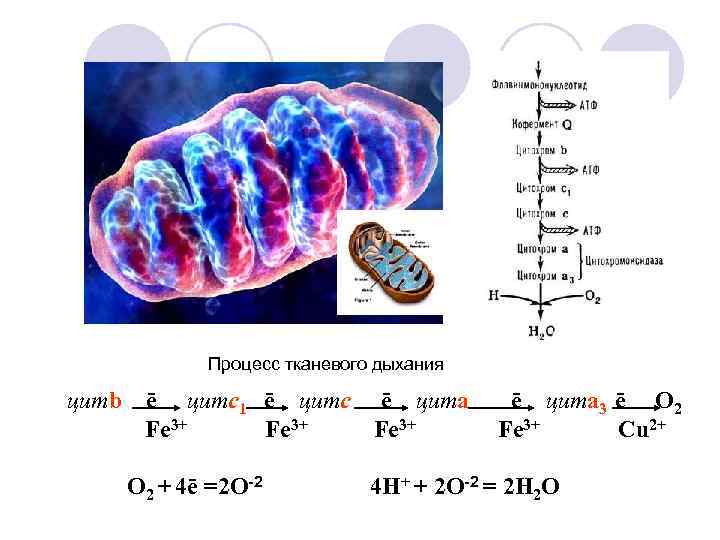
Процесс тканевого дыхания цитb ē цитс1 ē цитс ē цита Fe 3+ О 2 + 4ē =2 О-2 ē цита 3 ē О 2 Fe 3+ Cu 2+ 4 Н+ + 2 О-2 = 2 Н 2 О
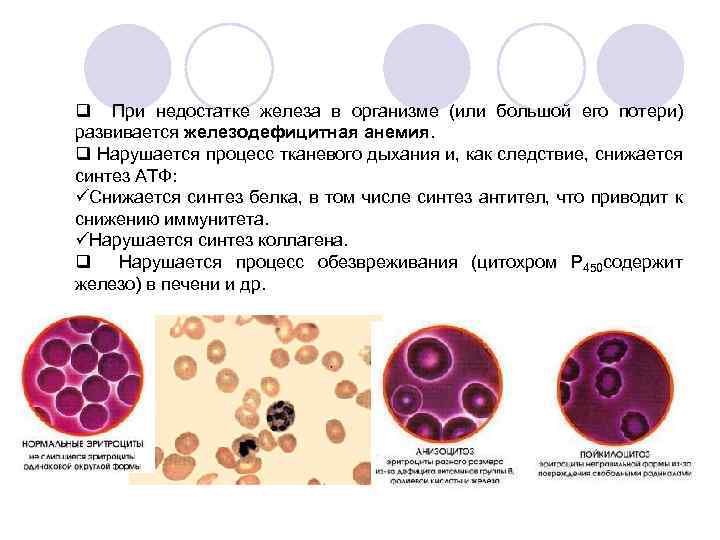
q При недостатке железа в организме (или большой его потери) развивается железодефицитная анемия. q Нарушается процесс тканевого дыхания и, как следствие, снижается синтез АТФ: üСнижается синтез белка, в том числе синтез антител, что приводит к снижению иммунитета. üНарушается синтез коллагена. q Нарушается процесс обезвреживания (цитохром Р 450 содержит железо) в печени и др.

ФТОР Большинство продуктов питания содержит в среднем 0, 2 -0, 3 мг фтора на кг веса. В рыбе его – 5 до 15 мг (макрель, лосось, сардины), а в криле - неправдоподобно высокое и опасное для здоровья его количество (1 кг сырой массы – 2 г этого элемента, а в вареной массе – приблизительно 750 мг). Богат фтором чай. Количество фтора в готовом напитке зависит от его крепости, длительности настоя. Наилучшим вкусом и ароматом обладает чай, настаивающийся 5 мин, в 1 стакане этого чая содержится 0, 2 мг фтора.

Суточная потребность во фторе 1 -2 мг/сутки Входит в состав костной системы и зубов (фторапатит). Недостаток фтора кариес зубов. Избыток – флюороз. Содержание фтора менее 0, 5 мг/л в воде – слишком мало, 1 -1, 5 мг/л – достаточное количество, а больше – уже слишком много! Разница между полезной и вредными дозами очень мала. Поэтому воду не фторируют, но добавляют его в зубные пасты.
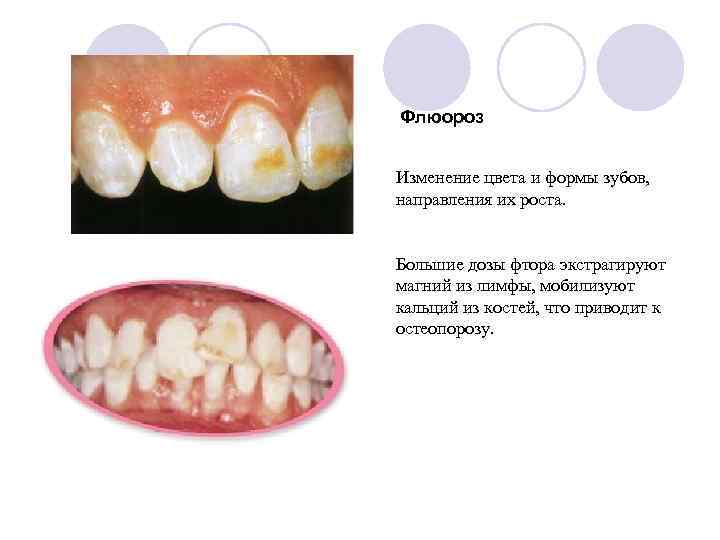
Флюороз Изменение цвета и формы зубов, направления их роста. Большие дозы фтора экстрагируют магний из лимфы, мобилизуют кальций из костей, что приводит к остеопорозу.

Йод Суточная потребность – 100 - 150 мкг в сутки Источниками йода могут быть йодированная соль, морские продукты, особенно морская капуста, некоторые салаты. В организме 25 мг I 2, больше половины сосредоточено в щитовидной железе.
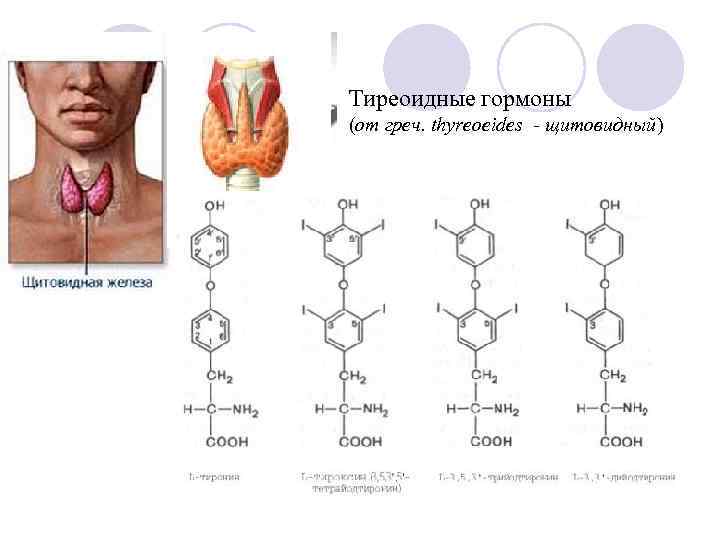
Тиреоидные гормоны (от греч. thyreoeides - щитовидный)
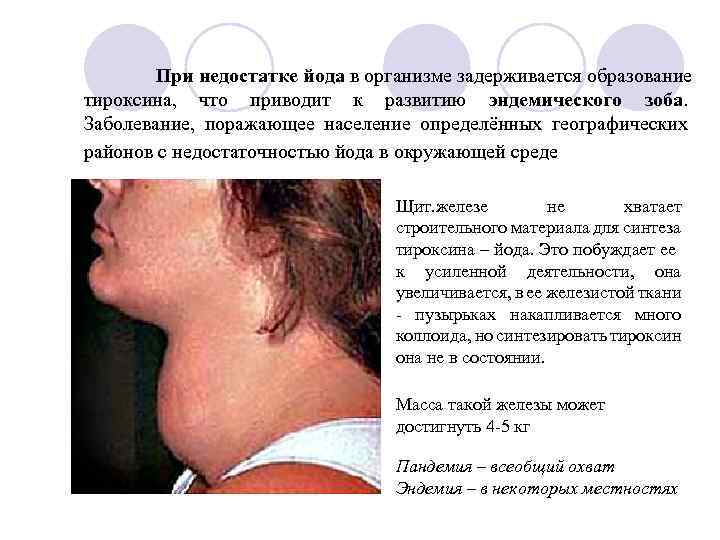
При недостатке йода в организме задерживается образование тироксина, что приводит к развитию эндемического зоба. Заболевание, поражающее население определённых географических районов с недостаточностью йода в окружающей среде Щит. железе не хватает строительного материала для синтеза тироксина – йода. Это побуждает ее к усиленной деятельности, она увеличивается, в ее железистой ткани - пузырьках накапливается много коллоида, но синтезировать тироксин она не в состоянии. Масса такой железы может достигнуть 4 -5 кг Пандемия – всеобщий охват Эндемия – в некоторых местностях

Селен Потребность – 100 -200 мкг в сутки. Высокое содержание Se обнаружено в зерне (особенно пшеница), а также чесноке, грибах свиных и говяжьих почках. Селен с греч. selen - луна.

Антиоксидантное свойство 1. Se является коферментом глутатионпероксидазы (ГПО) и пероксидазы (ПО). Ферменты антиоксидантной защиты. Ферменты разрушают перекись водорода и органические перекиси: Se-ПО 2 Н 2 О 2 R-OOH 2 Н 2 О + О 2 Se-ГПО + 2 Г-SH Органические восстан. глутатион перекиси ROH + H 2 O+ ГS-SГ окисленный глутатион Г-SH - глутатион, трипептид в состав которого входят Sсодержащая аминокислота ЦИС, ГЛУ и ГЛИ.

2. Способствует выведению из организма тяжелых Ме. В плазме крови селен циркулирует в составе белка селенпротеина (открыт 1977 и изучен 1987 г. г. ). В его состав входит до 10 -11 атомов Se. Содержание в плазме - 51± 4 мкг/мл. Белок связывает ионы Cd, Pb Hg. 3. Селен снижает риск мутаций в молекуле ДНК. Эпидемиологические исследования установили взаимосвязь между недостатком селена и канцерогенезом (развитием рака). Se на 40% снижает заболеваемость раком и на 50% уменьшает смертность.

При глубоком недостатке Se развивается селенодефицитные состояния: 1. Б-нь Кешан (название провинции на северо-востоке Китая) выражается кардиомиопатией: аритмия, увеличение размеров сердца, точечные некрозы миокарды – в рез-те сердечная недостаточность. В настоящее время доказано, что причина заболевания - энтеровирусная инфекция (Coxsackivirus ВЗ) на фоне глубокого селенодефицита. Недостаток селена и витамина Е позволяет Коксакивирусу мутировать (перерождаться) в вирулентный штамм, вызывающий поражение сердца. 2. Возрастает вероятность развития опухолей.
Спектральный анализ волос и ногтей Для диагностики микро- и макроэлементов волосы и ногти являются наиболее благодатным материалом. В период роста они подпитываются циркулирующей кровью, лимфой, внеклеточной жидкостью. К моменту выхода из ростковой зоны волосы и ногти затвердевают и жестко фиксируют состав и соотношение накопленных за фазу роста веществ. q Волос хранит интегральную информацию о минеральном обмене организма – от нескольких недель до нескольких месяцев или лет (в среднем волос вырастает на 0, 1 мм в день). q Некоторые токсичные вещества можно обнаружить только этим способом.

Физиологическая роль Cu Продукт Дрожжи для выпечки Кунжутное семя Тыквенные семечки Куриные сердца (вареные) Говядина (отварная) Арахис Какао-порошок Семечки подсолнечника Язык говяжий (отварной) Кедровые орехи Индюшиные ножки (жаренные в гриле) Попкорн Яичный желток Пшеничная мука грубого помола Грецкие орехи Арахисовое масло Кокосовый орех Сардины Цинк 9, 97 7, 75 7, 44 7, 30 7, 06 6, 68 6, 37 5, 29 4, 80 4, 28 4, 13 3, 44 3, 11 2, 93 2, 73 2, 51 2, 01 1, 40 В организме взрослого содержится до 100 мг Cu. Суточная потребность 2, 5 -5 мг. Встречается в составе многих продуктов: яйца, печень, рыба, молоко, хлебопродукты, капуста, картофель, фрукты, крапива, печень, орехи, грибы, бобы сои, кофе.

Около 50% сод-ся в мышцах и костной ткани, меньше печени (депо) и мозге. Соединения меди обладают высокой биологической активностью. В растениях медь участвует в процессах синтеза хлорофилла, у млекопитающих - гема. Биологическая роль связана с участием Cu в построении ряда ферментов и белков: аскорбатоксидаза 8 ионов Cu 2+ Аскорбиновая к-та дезоксиаскорбиновая к-та цитохромоксидаза Cu 2+ в составе цитохром а 3 О 2 + 4ē 2 О-2 Последняя р-ция тканевого дыхания, в которой Cu передает 4ē на молекулярный кислород, превращая его в атомарный. При взаимодействии с 4 Н+ образует эндогенную воду: 4 Н+ + 2 О-2 = 2 Н 2 О

Медь присутствует в системе антиоксидантной защиты организма, являясь кофактором фермента супероксиддисмутазы (СОД), участвующей в нейтрализации свободных радикалов кислорода (АФК). СОД Cu 2+ О 2 - +2 Н+ Н 2 О 2 +О 2 Каталаза Fe 2+ 2 Н 2 О 2 2 Н 2 О+О 2 Se-ПО 2 Н 2 О 2 2 Н 2 О + О 2 Se-ГПО R-OOH + 2 Г-SH ROH + H 2 O+ ГS-SГ Органические восстан. глутатион окисленный перекиси глутатион Г-SH - глутатион, трипептид в состав которого входят S-содержащая аминокислота цистеин.
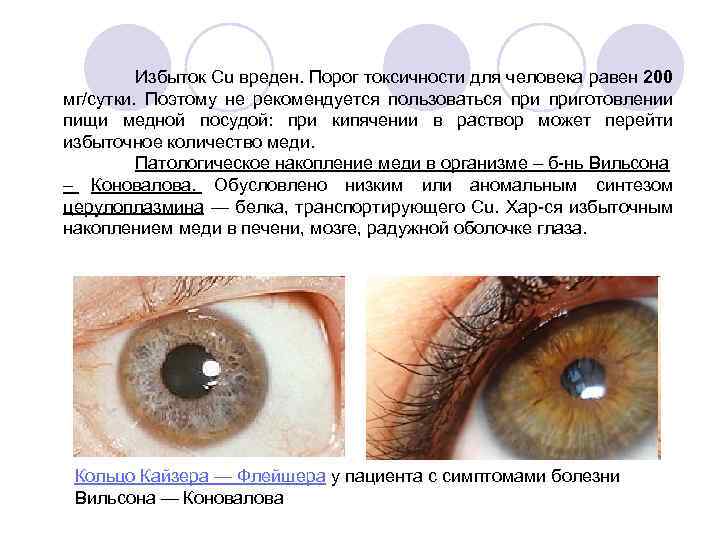
Избыток Cu вреден. Порог токсичности для человека равен 200 мг/сутки. Поэтому не рекомендуется пользоваться приготовлении пищи медной посудой: при кипячении в раствор может перейти избыточное количество меди. Патологическое накопление меди в организме – б-нь Вильсона – Коновалова. Обусловлено низким или аномальным синтезом церулоплазмина — белка, транспортирующего Cu. Хар-ся избыточным накоплением меди в печени, мозге, радужной оболочке глаза. Кольцо Кайзера — Флейшера у пациента с симптомами болезни Вильсона — Коновалова

В медицине. Со времен Парацельса до наших дней в фармакопее значатся глазные цинковые капли (0, 25%-ный раствор Zn. SO 4). Как присыпка издавна применяется цинковая соль стеариновой кислоты. Zn – хороший антисептик. Суспензия, в которую входят инсулин и хлорид цинка – эффективное средство против диабета, действующее лучше, чем чистый инсулин. недостаточном поступлении этого элемента в организм (менее 1 мг/день), а порог токсичности составляет 600 мг/день. Zn содержится в говядине, печени, морских продуктах (устрицы, моллюски, сельдь), тыквенные семечки, пшеничных зародышах, рисовых отрубях, овсяной муке. В организме взрослого человека содержится 1, 5 -3 г цинка.

В крови Zn сосредоточен в значительной степени в эритроцитах. В плазме 80 - 85% цинка связано с альбуминами, 1 -2% цинка свободны. В организме цинк кумулируется (накапливается) в печени, простате, сетчатке, поперечно-полосатых мышцах, костях. Цинк активирует более 200 металлоэнзимов: Цинк способствует синтезу белка. q Содержится в РНК- и ДНК-полимеразах, ферментах осуществляющих синтез нуклеиновых кислот. Входит в состав фермента ключевой реакции биосинтеза гема. Способствует делению, росту, размножению клеток. Поэтому называется анаболическим эл-том. q Zn помогает поджелудочной железе вырабатывать инсулин и связываться ему с клеточными рецепторами. q Zn особенно много в сетчатке глаза, он является важным веществом для поддержания и улучшения зрения. Дефицит цинка нарушает усвоение глюкозы клетками хрусталика глаза и способствует образованию катаракты. Способствует усвоению витамина А, необходимого для поддержания зрения.
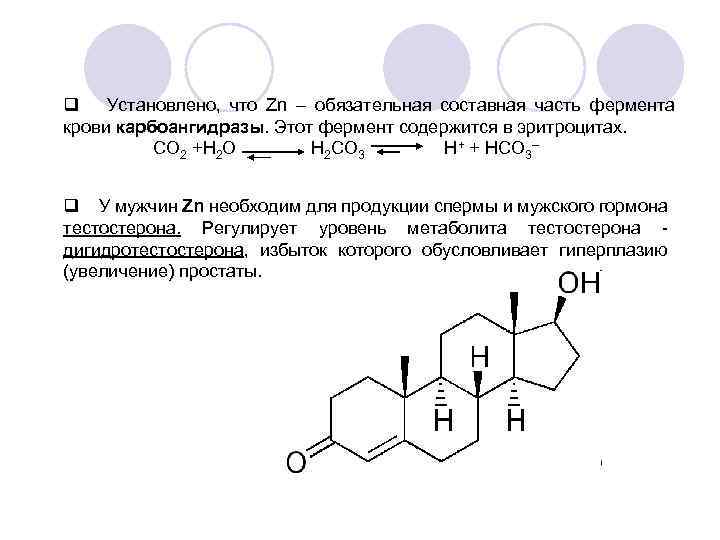
q Установлено, что Zn – обязательная составная часть фермента крови карбоангидразы. Этот фермент содержится в эритроцитах. CO 2 +H 2 O Н 2 CO 3 Н+ + НCO 3– q У мужчин Zn необходим для продукции спермы и мужского гормона тестостерона. Регулирует уровень метаболита тестостерона - дигидротестостерона, избыток которого обусловливает гиперплазию (увеличение) простаты.
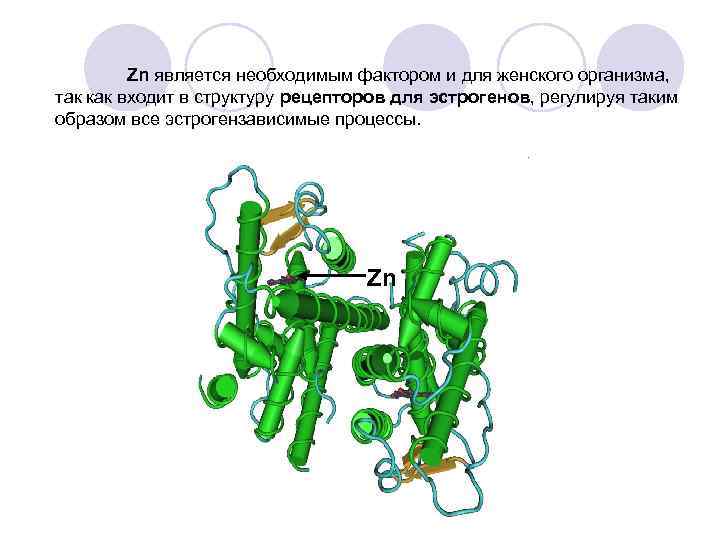
Zn является необходимым фактором и для женского организма, так как входит в структуру рецепторов для эстрогенов, регулируя таким образом все эстрогензависимые процессы. Zn
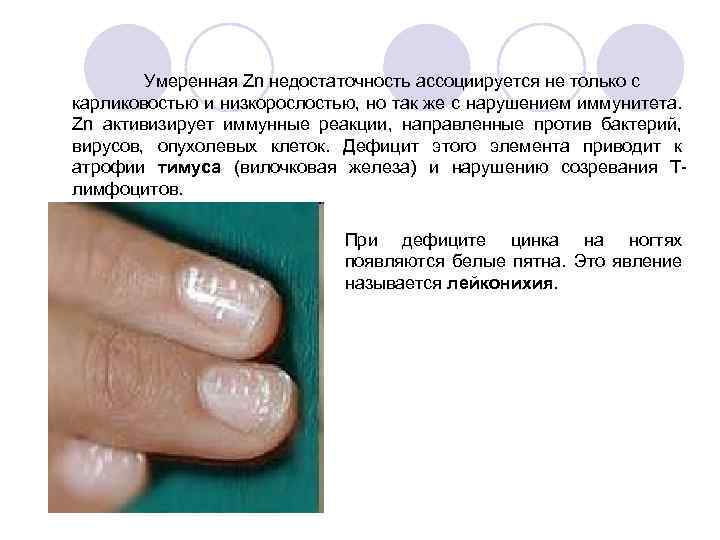
Умеренная Zn недостаточность ассоциируется не только с карликовостью и низкорослостью, но так же с нарушением иммунитета. Zn активизирует иммунные реакции, направленные против бактерий, вирусов, опухолевых клеток. Дефицит этого элемента приводит к атрофии тимуса (вилочковая железа) и нарушению созревания Tлимфоцитов. При дефиците цинка на ногтях появляются белые пятна. Это явление называется лейконихия.
Минеральный обмен.ppt