Artykbaeva_Asem.pptx
- Количество слайдов: 77

Ноцицептивная система ЦНС. Болевой синдром в неврологии Выполнила: Артыкбаева Асем Факултет: ОМ Группа: 10 -34 -1

План: 1. Введение 2. Определение боли 3. Соотношение понятий "боль" и "ноцицепция « 4. Ноцицептивная система 5. Рецепторный аппарат ноцицептивной системы 6. Общие механизмы болевой чувствительности. 7. Система "контроля ворот « 8. Антиноцицептивная система 9. Структура боли 10. Разновидности физической боли 11. Оценка боли План

Боль, как реакция на повреждающие (ноцицептивные) воздействия представляет собой важнейший биологический феномен, непосредственно обеспечивающий выживание организма в экстремальных условиях. Боль рассматривают как ключевой фактор эволюционного развития животного мира (Houdart, 1993). Это представление о боли нашло отражение в большинстве ее существующих определений.

П. К. Анохин определял боль как "реакцию, мобилизующую разнообразные функциональные системы для защиты организма от воздействия вредящего фактора и включающую сознание, память, мотивации и эмоции". Определение, рекомендуемое Международной Ассоциацией Исследования Боли, трактующее ее как "неприятное сенсорное и эмоциональное ощущение, связанное действительным или потенциальным повреждением ткани, или описываемое в терминах такого повреждения". При этом подчеркивается, что боль всегда субъективна, зависит от предшествующего жизненного опыта и множества индивидуальных особенностей.

Болевые ощущения присущи уже простейшим животным и даже по некоторым данным растениям. В настоящее время установлено, что человек способен ощущать боль уже во время внутриутробного этапа развития. Так в Амстердаме были представлены новые сведения, указывающие на то, что к 30 й неделе плод способен реагировать сокращениями мимической мускулатуры в ответ на болевые раздражители. То, что новорожденные испытывают боль, уже практически не подлежит оспариванию.
Боль для пациентов один из важнейших клинических признаков любого патологического процесса и одно из самых отрицательных проявлений болезни. В то же время своевременная и правильная оценка болевого синдрома помогает врачу составить представление о характере заболевания.
Реакция на боль чрезвычайно индивидуальна, так как зависит от влияния факторов, из которых основное значение имеют локализация, степень повреждения тканей, конституциональные особенности нервной системы, воспитание, эмоциональное состояние пациента в момент нанесения болевого раздражения

Из всех видов чувствительности боль занимает особое место. В то время как другие виды чувствительности в качестве адекватного раздражителя имеют определенный физический фактор (тепловой, тактильный, электрический и пр. ), боль сигнализирует о таких состояниях органов, которые требуют специальных сложных приспособительных реакций. Для боли нет единого универсального раздражителя. Как общее выражение в сознании человека боль вызывается разнообразными факторами в различных органах.
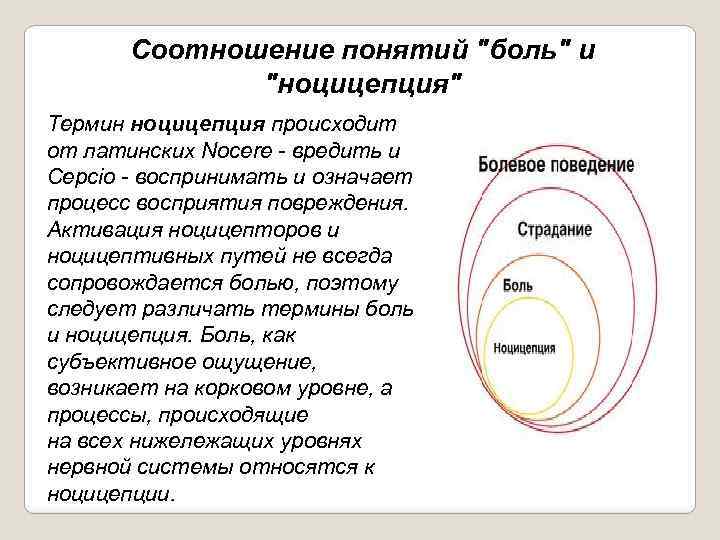
Соотношение понятий "боль" и "ноцицепция" Термин ноцицепция происходит от латинских Nocere вредить и Cepcio воспринимать и означает процесс восприятия повреждения. Активация ноцицепторов и ноцицептивных путей не всегда сопровождается болью, поэтому следует различать термины боль и ноцицепция. Боль, как субъективное ощущение, возникает на корковом уровне, а процессы, происходящие на всех нижележащих уровнях нервной системы относятся к ноцицепции.
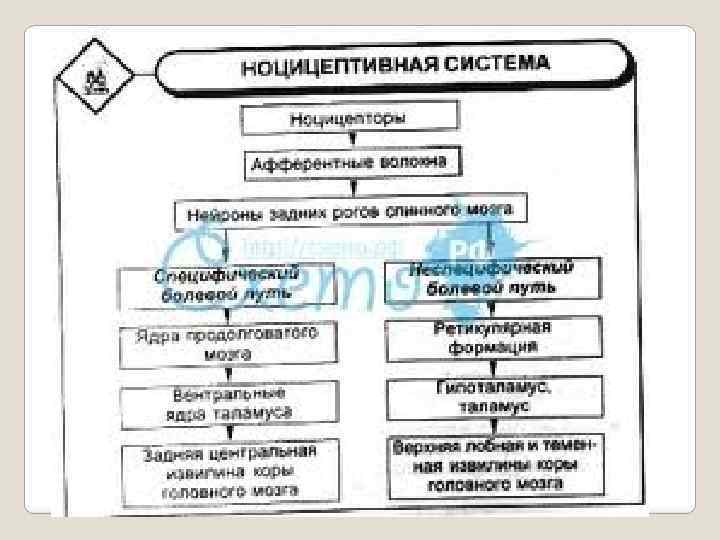

Ноцицептивная система представлена нервными структурами, их элементами и биохимическими механизмами восприятия повреждающих воздействий и подробно описана. В отличие от ноцицепции боль представляет собой более сложное ощущение, в котором ноцицепция соединяется с субъективным опытом, включающим сильный эмоциональный (аффективный) компонент.

Ноцицептивная система (от лат. посеге — повреждать, recipio, receptum — брать, принимать) представляет сложно организованную многоуровневую сенсорную систему, ответственную за восприятие и оценку повреждающего воздействия и формирование специфического субъективно отрицательного ощущения боли. Ноцицептивная система (НЦС) по данным современной медицины, как и различные анализаторы, представлена: 1 рецепторным, 2 проводниковым и 3 центральным звеньями (отделами, аппаратами).
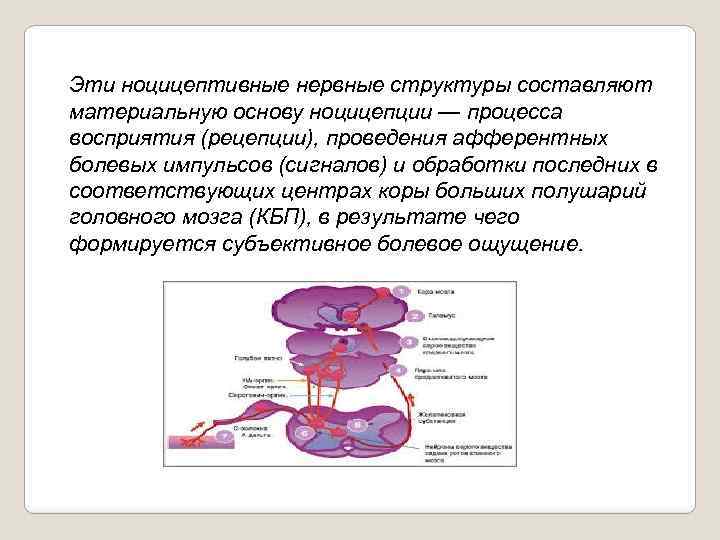
Эти ноцицептивные нервные структуры составляют материальную основу ноцицепции — процесса восприятия (рецепции), проведения афферентных болевых импульсов (сигналов) и обработки последних в соответствующих центрах коры больших полушарий головного мозга (КБП), в результате чего формируется субъективное болевое ощущение.

Рецепторный аппарат ноцицептивной системы представлен различными по механизму активации болевыми рецепторами: мономодальными (механическими); бимодальными (механическими и термическими); полимодальными (механическими, давления, термическими, химическими и др. )
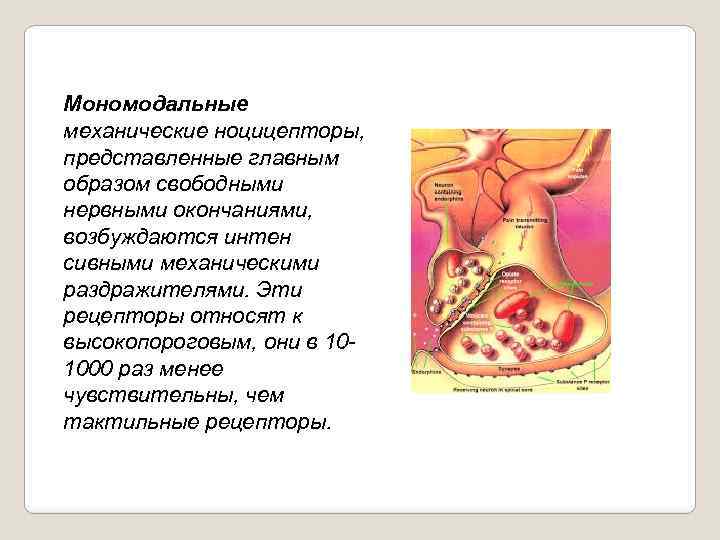
Мономодальные механические ноцицепторы, представленные главным образом свободными нервными окончаниями, возбуждаются интен сивными механическими раздражителями. Эти рецепторы относят к высокопороговым, они в 10 1000 раз менее чувствительны, чем тактильные рецепторы.
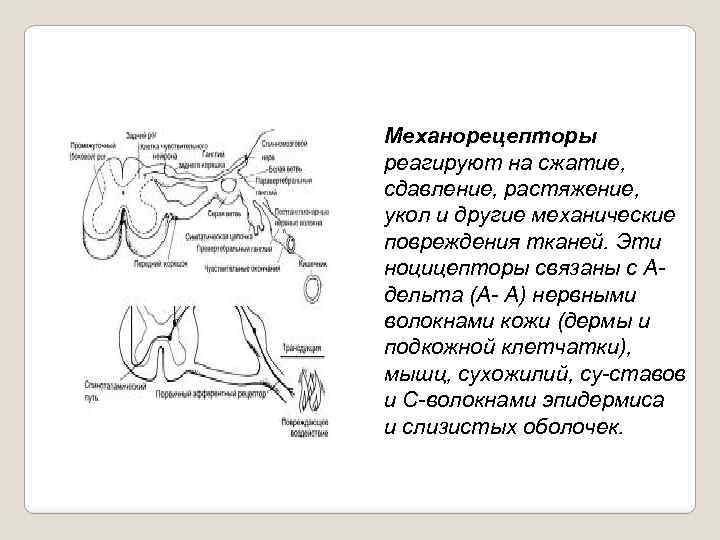
Механорецепторы реагируют на сжатие, сдавление, растяжение, укол и другие механические повреждения тканей. Эти ноцицепторы связаны с А дельта (А А) нервными волокнами кожи (дермы и подкожной клетчатки), мышц, сухожилий, су ставов и С волокнами эпидермиса и слизистых оболочек.

Бимодальные механические и термические ноцицепторы. Первые (их большинство) возбуждаются в ответ на действие механических раздражителей в виде укола, повреждения, сдавления тканей. Вторые (их меньшее количество) — температурными факторами, которые либо превышают +40 °С, либо меньше +10 °С. Под влиянием механо и теплораздражителей возбуждаются соответствующие рецепторы, связан ные с А А волокнами. В то же время часть механических и холодовых рецепторов активизируют ноцицепторы, связанные с С волокнами.

Полимодальные ноцицепторы возбуждаются разнообразными по природе (меха ническими, термическими, химическими и др. ) раздражителями, связанными пре имущественно с С волокнами. Хемоноцицепторы представлены во всех (особенно глубоких) слоях кожи, в мышцах, суставах, связках, внутренних органах (сердце, желудке, кишках, печени, селезёнке и др. ), спинном и головном мозге. Хемоноцицепторы связаны с тонкими афферентами как немиелинизированных (С ), так и миелинизированных (А А) нерв ных волокон.

Передача болевых импульсов, реализуемая от ноцицепторов через А А волокна осуществляется по филогенетически более молодому, экстероцептивному отделу ноцицептивной системы и формирует эпикритическую боль, а реализуемая через С волокна — по эволюционно более древнему, интерцептивному отделу ноцицептив ной системы и формирует протопатическую боль.

Хемоноцицепторы по данным патологической физиологии человека возбуждаются (деполяризуются) под влиянием увеличенного количества различных химических веществ — алгогенов, имеющих разное происхождение: тканевые — гистамин, ряд простагландинов, ионы натрия, кальция, во дорода и др. ; нейронные — выделяемые нервными окончаниями нейрокинины, субстанция Р, соматостатин и др. ; плазменные — плазмакинины, брадикинин, каллидин, контактный фактор Хагемана — XII фактор свёртывания крови и др.

Одни хемоноцицепторы (их большинство) реагируют только на химические раздражители, другие — на химические и термические, третьи — на химические, термические и механические стимулы. Показано, что механо , терморецепторы и рецепторы давления в коже и слизи стых оболочках распределены неравномерно. В частности, болевых точек в 9 раз больше, чем точек давления. Последних больше, чем холодовых и тепловых точек. Холодовых в 9 раз больше, чем тепловых точек.
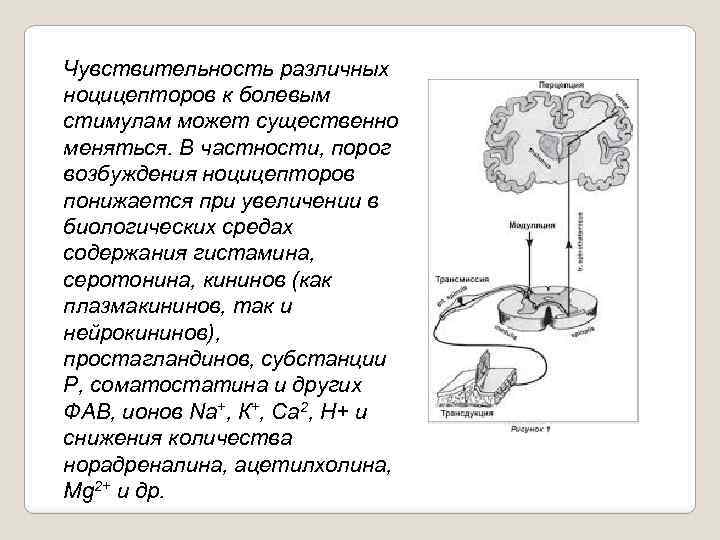
Чувствительность различных ноцицепторов к болевым стимулам может существенно меняться. В частности, порог возбуждения ноцицепторов понижается при увеличении в биологических средах содержания гистамина, серотонина, кининов (как плазмакининов, так и нейрокининов), простагландинов, субстанции Р, соматостатина и других ФАВ, ионов Na+, К+, Са 2, Н+ и снижения количества норадреналина, ацетилхолина, Mg 2+ и др.

Общие механизмы болевой (ноцицептивной) чувствительности. Афферентные (приносящие) ноцицептивные периферические нервы содержат первичные волокна малого диаметра, имеющие рецепторы в различных органах и тканях. Ощущение боли сопряжено с появлением электрической активности деполяризацией чувствительных нервных окончаний. Для чувствительных окончаний возбуждающими могут явиться разнообразные механические, термические, химические стимулы.

Согласно одной гипотезе, боль не является специфическим чувством, и не существует специальных рецепторов, воспринимающих только болевое раздражение. Любое раздражение тех или иных рецепторов может вызвать чувство боли, если сила раздражения достаточно велика.

Согласно другой, более распространенной точке зрения, существуют специальные болевые рецепторы, характеризующиеся высоким порогом восприятия возбуждающиеся стимулами "повреждающей" интенсивности.
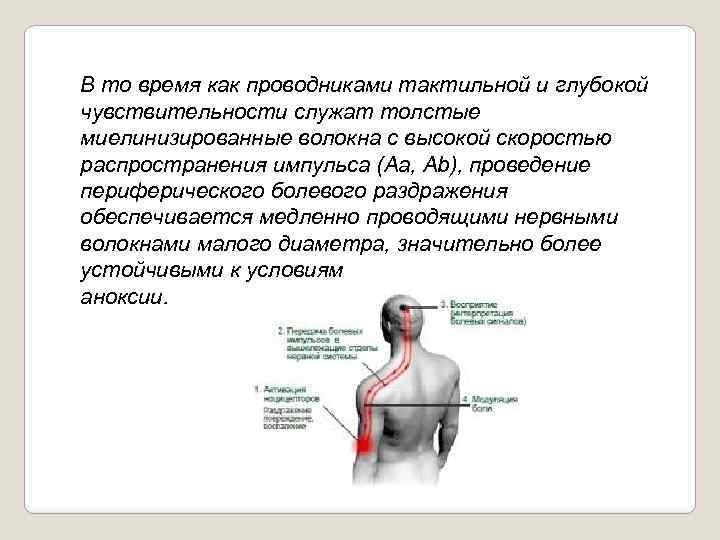
В то время как проводниками тактильной и глубокой чувствительности служат толстые миелинизированные волокна с высокой скоростью распространения импульса (Аa, Аb), проведение периферического болевого раздражения обеспечивается медленно проводящими нервными волокнами малого диаметра, значительно более устойчивыми к условиям аноксии.

Существуют афферентные ноцицептивные волокна двух типов: · С полимодальные ноцицепторы (PMN) немиелинизированные С волокна с низкой скоростью проведения импульса (< 1 м/с); при их раздражении ощущается отсроченная тупая диффузная жгучая длительная боль (протопатическая); · Аd миелинизированные волокна с более высокой скоростью проведения импульса; при их раздражении ощущается немедленная острая, четко локализованная, быстро стихающая (эпикритическая) боль.
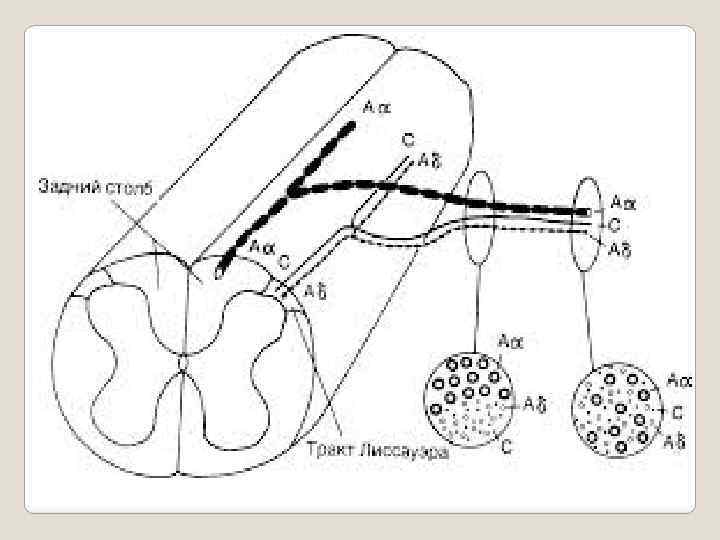

Аксоны афферентных ноцицептивных волокон заканчиваются в столбах заднего рога спинного мозга Локализация окончаний чувствительных волокон в столбах заднего рога спинного мозга.

Аксоны афферентных чувствительных нервных волокон заканчиваются в соответствующих сегментах заднего рога спинного мозга. Здесь они контактируют с передаточными нейронами спиноталамического пути. Аb волокна, ответственные за тактильную чувствительность, проецируются в III VI сегментах. Аd волокна, ответственные за тактильную чувствительность и ноцицепцию, проецируются в I III и V сегментах. С волокна, проводящие болевые, температурные и тактильные стимулы, проецируются в I и II сегментах
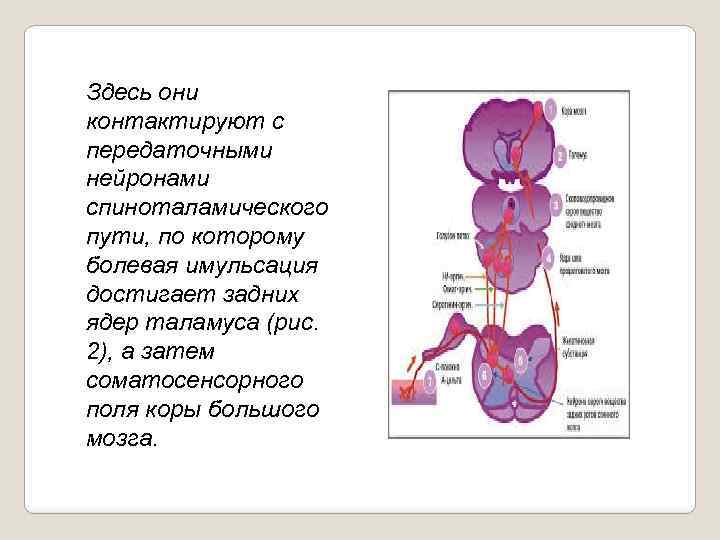
Здесь они контактируют с передаточными нейронами спиноталамического пути, по которому болевая имульсация достигает задних ядер таламуса (рис. 2), а затем соматосенсорного поля коры большого мозга.
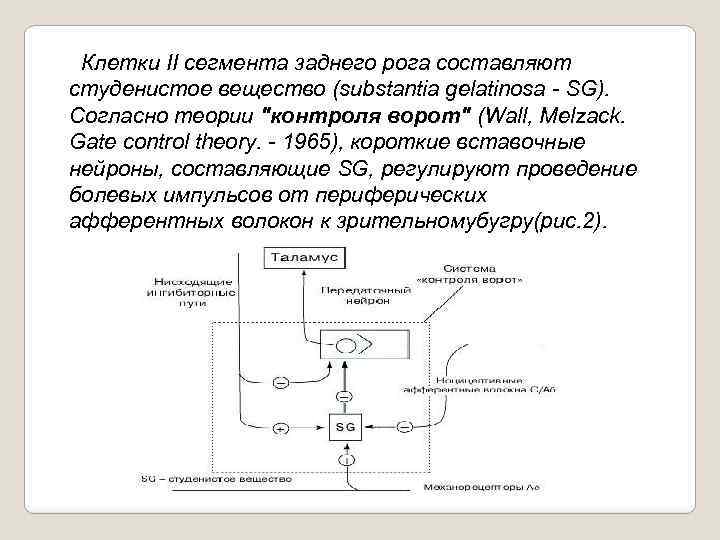
Клетки II сегмента заднего рога составляют студенистое вещество (substantia gelatinosa SG). Согласно теории "контроля ворот" (Wall, Melzack. Gate control theory. 1965), короткие вставочные нейроны, составляющие SG, регулируют проведение болевых импульсов от периферических афферентных волокон к зрительномубугру(рис. 2).
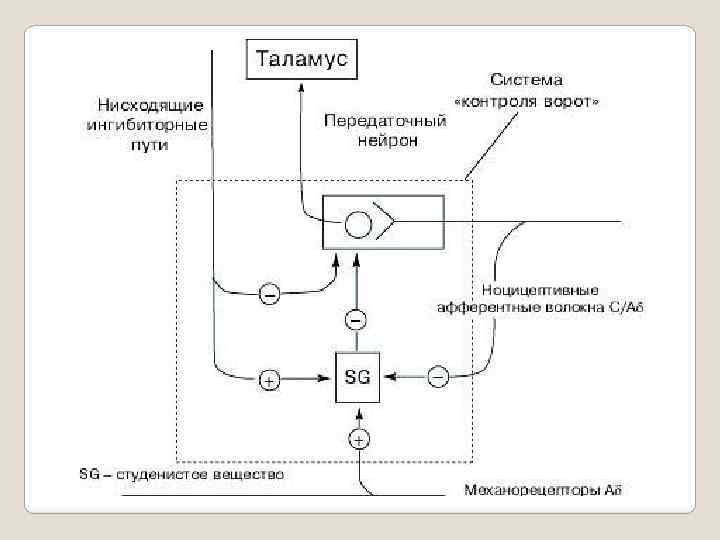

Система "контроля ворот" Аксоны афферентных ноцицептивных волокон контактируют с передаточными нейронами спиноталамического пути, по которому болевая имульсация достигает задних ядер таламуса, а затем соматосенсорного поля коры большого мозга. Нервные клетки SG подавляют передачу нервного импульса от афферентных ноцицептивных волокон и нейронами спиноталамического тракта. SG интернейроны активируются нисходящими ингибиторными нейронами и волокнами неноцицептивной чувствительности; тормозятся афферентными ноцицептивными С волокнами
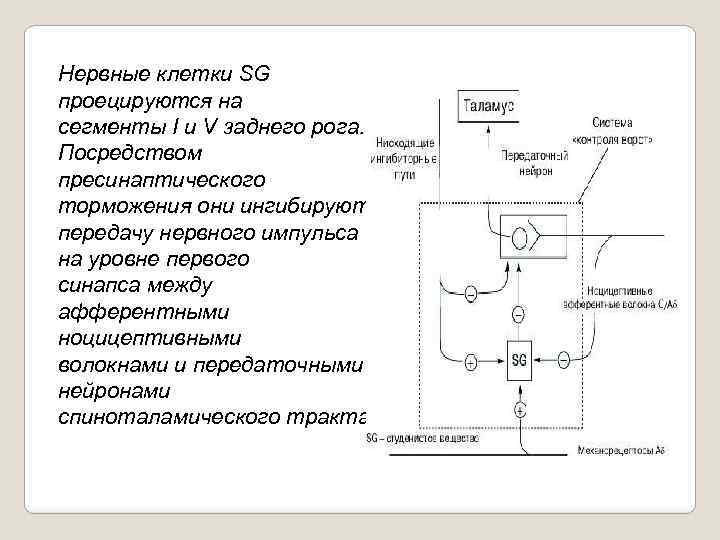
Нервные клетки SG проецируются на сегменты I и V заднего рога. Посредством пресинаптического торможения они ингибируют передачу нервного импульса на уровне первого синапса между афферентными ноцицептивными волокнами и передаточными нейронами спиноталамического тракта.

Активность самих SG интернейронов подвержена модулирующим влияниям. Они активируются нисходящими ингибиторными нейронами или неноцицептивными афферентными импульсами (например, импульсами тактильной чувствительности, проводящимся по Аb волокнам). Таким образом, нервные импульсы, приходящие по толстым волокнам, "закрывают ворота" для потока болевой импульсации. "Отвлекающие процедуры", усиливающие импульсацию в толстых миелиновых волокнах, способствуют уменьшению чувства боли. При повреждении толстых волокон (например, в условиях гипоксии, при механическом повреждении) болевая чувствительность усиливается
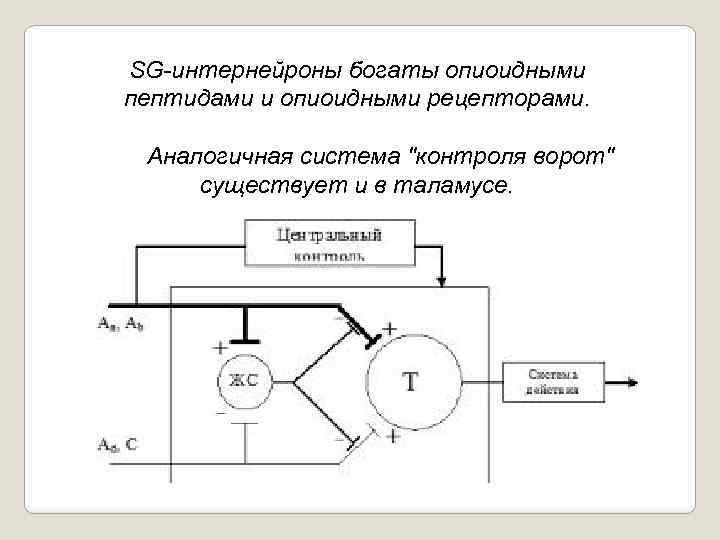
SG интернейроны богаты опиоидными пептидами и опиоидными рецепторами. Аналогичная система "контроля ворот" существует и в таламусе.
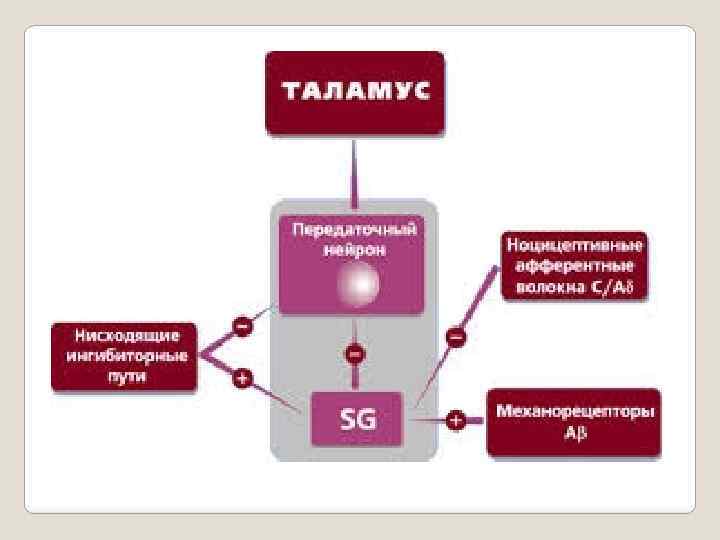

Антиноцицептивная система Результаты многочисленных наблюдений и исследований позволили сформировать представление о существовании в организме антиноцицептивной системы, подавляющей восприятие боли. Структуры, относящиеся к этой системе, включают некоторые зоны центрального серого вещества, покрышки моста, миндалевидного тела, гиппокампа, ядер мозжечка, сетчатой формации. Они оказывают нисходящий, цереброспинальный, контроль афферентного "притока", вызывая торможение нейронов спинного мозга.

Гуморальные механизмы регуляции ноцицептивной чувствительности Можно заключить, что ноцицептивные нервные окончания являются хемочувствительными, поскольку воздействие всех раздражителей, вызывающих ощущение боли (механические, термические, воспалительные, ишемические, химические), связано с изменением химического окружения болевых рецепторов.
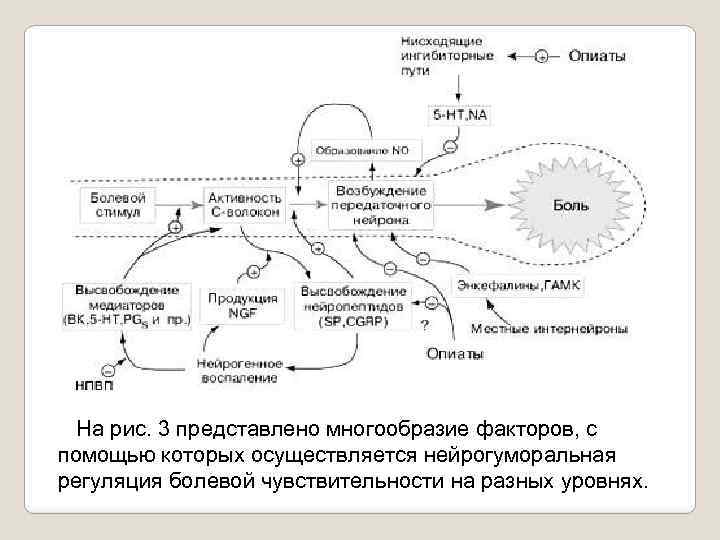
На рис. 3 представлено многообразие факторов, с помощью которых осуществляется нейрогуморальная регуляция болевой чувствительности на разных уровнях.
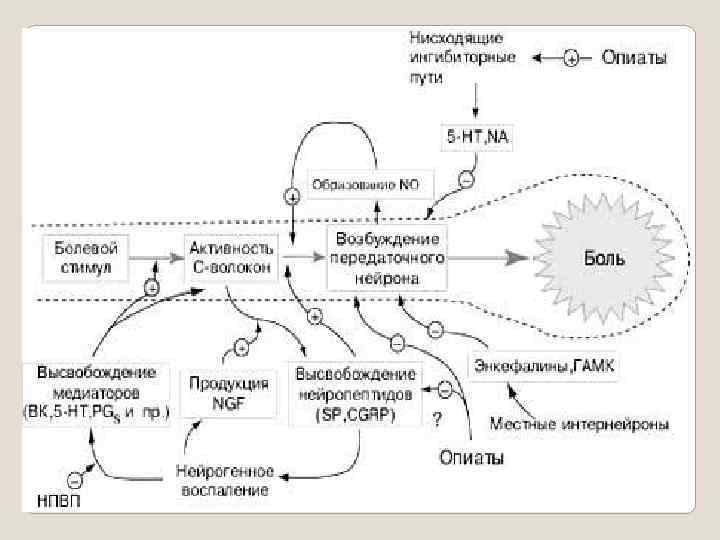

Рис. 3. Механизмы регуляции ноцицептивного пути. Болевой стимул воспринимается ноцицептивными афферентными волокнами, передающими возбуждение передаточным нейронам спиноталамического тракта. Далее по таламокортикальным волокнам импульс достигает коры головного мозга, где формируется восприятие боли. Передача болевого импульса с периферии на передаточные нейроны спиноталамического тракта облегчается посредством NO, SP и CGRP. Медиаторами нисходящих цереброспинальных антиноцицептивных импульсов служат 5 HT, NA. Медиаторами антиноцицептивных импульсов от SG нейронов энкефалины, ГАМК.

При нейрогенном воспалении наблюдается избыточное и длительное высвобождение нейропептидов SP, CGRP из С волокон, поддерживаемое такими воспалительными веществами, как BK, 5 HT, PGs и NGF. Применение НПВП позволяет уменьшить продукцию воспалительных медиаторов. Опиаты снижают болевую чувствительность посредством активации нисходящих антиноцицептивных сигналов и угнетения передаточных нейронов спиноталамического тракта. NGF фактор роста нервов, BK брадикинин, 5 НТ 5 гидрокситриптамин (серотонин), PGs простагландины, NA норадреналин, SP субстанция Р, CGRP пептид, относящийся к гену кальцитонина

Химические медиаторы, участвующие в ноцицептивной передаче и регуляции потока болевых импульсов. 1. Нейротрансмиттеры: o 5 гидрокситриптамин (5 НТ) представляет собой наиболее активный медиатор; o гистамин (наиболее вероятно, что он вызывает скорее зуд, нежели боль). 2. Кинины: o брадикинин мощный продуцент боли, способствующий высвобождению простагландинов, усиливающих болевой эффект; является агонистом специфических рецепторов, сопряженных с G белком; o каллидин вызывает аналогичные эффекты.

3. Низкий р. Н способствует открытию протонактивируемых катионных каналов ноцицептивных афферентных нейронов. 4. АТФ стимулирует открытие АТФ активируемых катионных каналов чувствительных нейронов. 5. Молочная кислота стимулирует открытие протонактивируемых катионных каналов ноцицептивных афферентных нейронов, является потенциальным медиатором ишемической боли. 6. Ионы К+ стимулируют катионные обменники (К+/Н+; К+/Na+); потенциальные медиаторы ишемической боли.
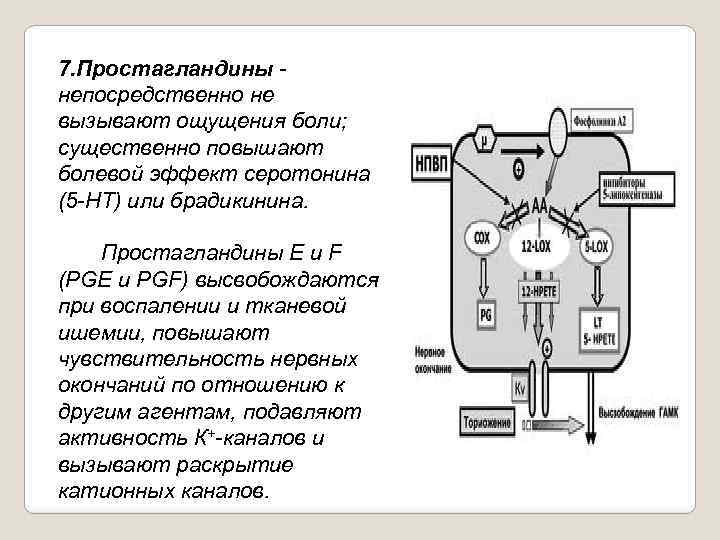
7. Простагландины непосредственно не вызывают ощущения боли; существенно повышают болевой эффект серотонина (5 НТ) или брадикинина. Простагландины Е и F (PGE и PGF) высвобождаются при воспалении и тканевой ишемии, повышают чувствительность нервных окончаний по отношению к другим агентам, подавляют активность К+ каналов и вызывают раскрытие катионных каналов.
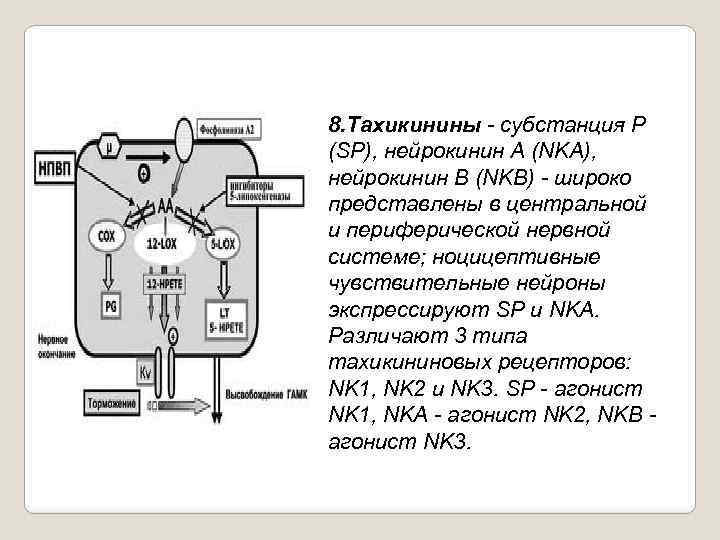
8. Тахикинины субстанция Р (SP), нейрокинин А (NKA), нейрокинин В (NKB) широко представлены в центральной и периферической нервной системе; ноцицептивные чувствительные нейроны экспрессируют SP и NKA. Различают 3 типа тахикининовых рецепторов: NK 1, NK 2 и NK 3. SР агонист NK 1, NKА агонист NK 2, NKВ агонист NK 3.
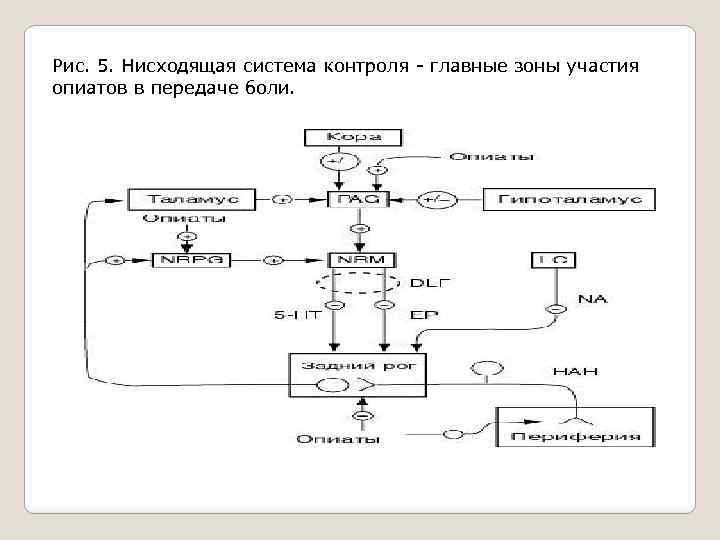
Рис. 5. Нисходящая система контроля - главные зоны участия опиатов в передаче боли.

Опиоиды снижают чувствительность болевых рецепторов, угнетают синаптическую передачу болевого импульса на уровне заднего рога спинного мозга. Под их воздействием активируется антиноцицептивный цереброспинальный контроль: возрастает поток активирующих импульсов из парагигантоклеточного ретикулярного ядра и периакведуктального серого вещества к большому ядру шва, нейроны которого тормозят передачу ноцицептивного сигнала на уровне задних рогов спинного мозга. PAG периакведуктальное серое вещество, NRPG парагигантоклеточное ретикулярное ядро, NRM большое ядро шва, LC locus ceruleus, DLF дорсолатеральный канатик, 5 HT 5 гидрокситриптамин (серотонин), EP энкефалин, NA норадреналин, HAH ноцицептивный афферентный нейрон (по Fields, Basbaum, 1994)
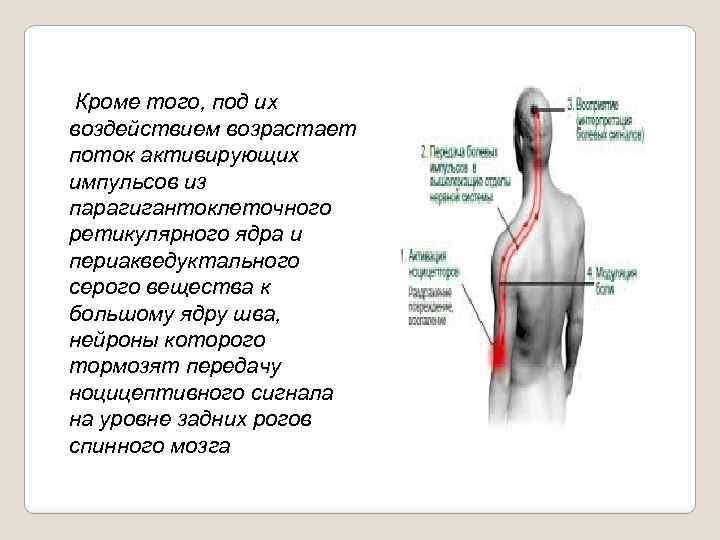
Кроме того, под их воздействием возрастает поток активирующих импульсов из парагигантоклеточного ретикулярного ядра и периакведуктального серого вещества к большому ядру шва, нейроны которого тормозят передачу ноцицептивного сигнала на уровне задних рогов спинного мозга

Современная нейропатологическая концепция (Крыжановский, 1997) в качестве обязательного компонента развития болевых синдромов рассматривает ослабление тормозного контроля со стороны антиноцицептивной системы. Элементы антиноцицептивной системы распределены на всех уровнях проведения болевой информации, она включает определенные структуры и механизмы, деятельность которых направлена на подавление боли. Постоянное взаимодействие ноцицептивной и антиноцицептивной систем осуществляют функцию контроля боли.

Активация ноцицептивной системы в норме вызывает и повышение активности антиноцицептивных механизмов. Взаимодействие механизмов ноцицепции и антиноцицепции происходит уже на уровне периферических афферентных ноцицептивных волокон. Психоэмоциональные компоненты боли, традиционно рассматривавшиеся как результат взаимодействия нейрохимических механизмов коркового и подкоркового уровней организации системы контроля боли, в значительной мере предопределяются от периферическими механизмами.

Ослабление тормозного контроля со стороны антиноцицептивной системы провоцирует образование ансамблей взаимодействующих гиперактивных ноцицептивных нейронов, по определению Г. Н. Крыжановского генераторов патологически усиленного возбуждения (ГПУВ). Первичные ГПУВ в соответствии с характером повреждающего воздействия и собственными морфо функциональными особенностями индуцируют появление вторичных генераторов, существенно изменяющих нормальную структуру системы болевой чувствительности. Новая патодинамическая структура системы контроля боли составляет патологическую алгическую систему. Патологическая алгическияя система в зависимости от своих конкретных характеристик определяет клиническую картину болевого синдрома. В отличие от адаптогенного характера физиологической, патологическая боль оказывает дезадаптирующее влияние на организм.

Определение боли В отличие от других сенсорных модальностей боль дает мало сведений об окружающем нас мире, а скорее сообщает о внешних или внутренних опасностях, грозящих нашему телу. Тем самым она защищает нас от долговременного вреда и поэтому необходима для нормальной жизни. Если бы боль нас не предостерегала, уже при самых обыденных действиях мы часто наносили бы себе повреждения и вскоре стали бы калеками.

Следовательно, боль повышает наши шансы на выживание и в этом отношении сходна с другими чувствами. По многим своим физиологическим свойствам она также полностью сравнима с ними, хотя и отличается широким спектром особенностей. Чтобы наилучшим образом помочь человеку, испытывающему боль, надо понимать эти ее специфические черты
Известно много попыток точно и кратко охарактеризовать боль; Я выбрали формулировку, опубликованную несколько лет назад одним международным комитетом экспертов журнал «Раш» . «Боль неприятное сенсорное и эмоциональное переживание, связанное с истинным или потенциальным повреждением ткани или описываемое в терминах такого повреждения» .
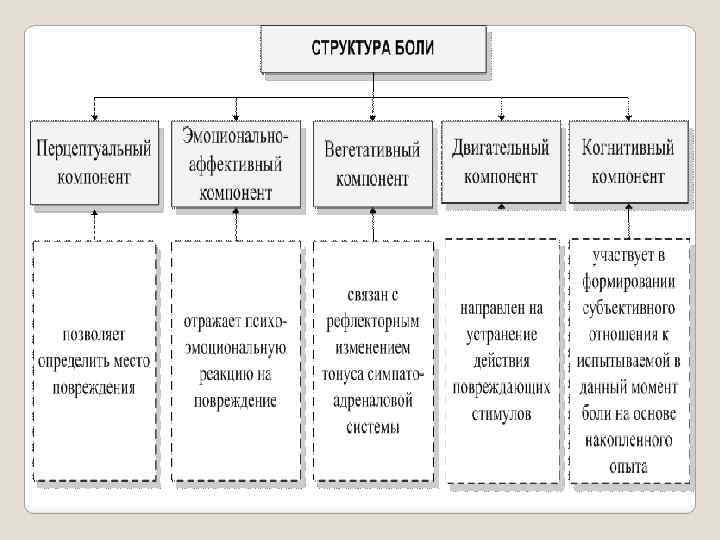

Согласно современным представлениям различают: 1 физиологическую и 2 патологическую боль выделяют три основных типа боли: 1 соматогенную, 2 нейрогенную и 3 психогенную. Нет четких границ между собственно соматогенной и висцеральной болью, психогенной и идиопатической болью. Существующая классификация боли далека от совершенства и границы между отдельными типами и классами болевых синдромов весьма условны.
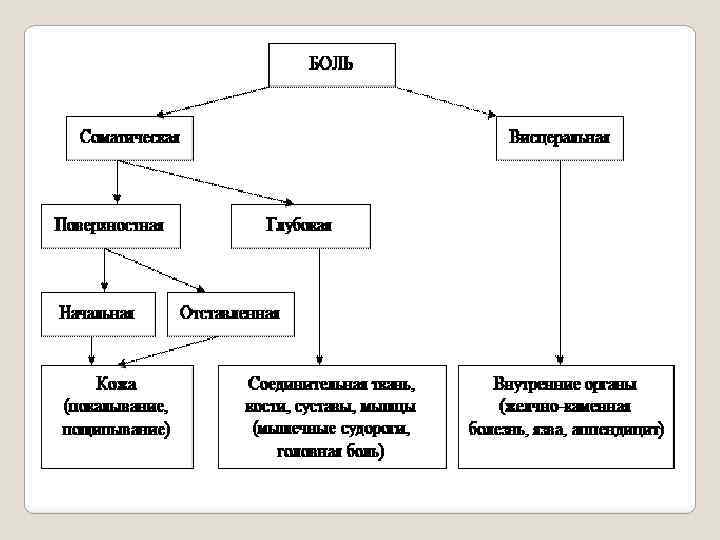

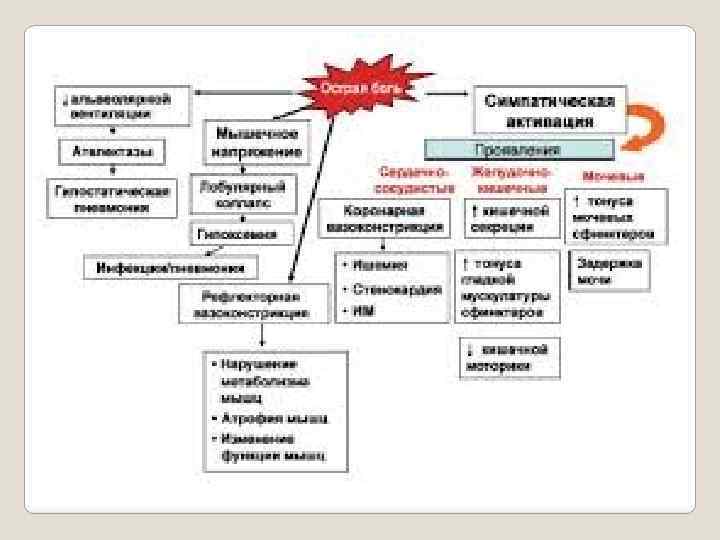
Разновидности физической боли Острая боль определяется как краткая по времени проявления боль с легко идентифицируемой причиной. Острая боль — это предупреждение организму о существующей в данный момент опасности органического повреждения или заболевания. Часто стойкая и острая боль сопровождается также ноющей болью. Острая боль обычно концентрируется в определённом участке перед тем, как она каким то образом распространится шире. Этот тип боли обычно хорошо поддаётся излечению.
Хроническая боль первоначально определялась как боль, которая продолжается около 6 месяцев и более. Сейчас она определяется как боль, которая упорно сохраняется дольше того соответствующего отрезка времени, в течение которого она обычно должна завершаться. Часто она более трудная для излечения, чем острая боль.

Особое внимание требуется при обращении к любым болям, которые стали хроническими. В исключительных случаях нейрохирурги могут провести сложную операцию по удалению отдельных частей головного мозга пациента, чтобы справиться с хроническими болями. Подобное вмешательство может избавить пациента от субъективного ощущения боли, но так как сигналы от болевого очага всё равно будут передаваться по нейронам, тело продолжит реагировать на них

Кожная боль возникает при повреждении кожи или подкожных тканей. Кожные ноцицепторы оканчиваются чуть ниже кожи, и благодаря высокой концентрации нервных окончаний предоставляют высокоточное, локализованное ощущение боли малой продолжительности.

Соматическая боль возникает в связках, сухожилиях, суставах, костях, кровяных сосудах и даже в самих нервах. Она определяется соматическими ноцицепторами. По причине нехватки болевых рецепторов в этих участках они производят тупую, плохо локализуемую, более продолжительную боль, чем у кожных болей. Сюда входят, например, растяжения суставов и сломанные кости.

Внутренняя боль возникает от внутренних органов тела. Внутренние ноцицепторы расположены в органах и во внутренних полостях. Ещё большая нехватка болевых рецепторов в этих участках тела приводит к появлению более нудящей и продолжительной, по сравнению с соматической, боли. Внутреннюю боль особенно тяжело локализовать, и некоторые внутренние органические повреждения представляют собой «приписываемые» боли, когда ощущение боли приписывается участку тела, которое никак не связано с участком самого повреждения.

Сердечная ишемия (недостаточное содержание крови в сердечной мышце) — это, возможно, самый известный пример приписываемой боли; ощущение может располагаться как отдельное чувство боли чуть выше грудной клетки, в левом плече, руке или даже в ладони. Приписываемая боль может объясняться открытием того, что болевые рецепторы во внутренних органах также возбуждают и спинномозговые нейроны, которые возбуждаются при кожных повреждениях. После того, как мозг начинает ассоциировать возбуждение этих спинномозговых нейронов со стимуляцией соматических тканей в коже или мускулатуре, болевые сигналы, идущие от внутренних органов, начинают интерпретироваться мозгом как происходящие от кожи.

Фантомная боль в конечностях — ощущение боли, возникающее в утраченной конечности или в конечности, которая не чувствуется с помощью обычных ощущений. Данное явление практически всегда связано со случаями ампутаций и паралича. Кроме фантомных болей, регистрируют фантомы — не связанное с болью ощущение человеком утраченной конечности.

Невропатическая боль ( «невралгия» ) может появиться как результат повреждения или заболевания самих нервных тканей (например, зубная боль). Это может нарушить возможность чувствительных нервов передавать правильную информацию таламусу (отделу промежуточного мозга), и отсюда мозг неправильно интерпретирует болевые стимулы, даже если отсутствуют очевидные физиологические причины боли.

Психогенная боль Психогенную боль диагностируют в отсутствие органического заболевания или в том случае, когда последнее не может объяснить характер и выраженность болевого синдрома. Психогенная боль всегда имеет хронический характер и возникает на фоне психических расстройств: депрессии, тревоги, ипохондрии, истерии, фобии. У значительной части больных важную роль играют психосоциальные факторы (неудовлетворенность работой, стремление получить моральную или материальную выгоду). Особенно тесные связи существуют между хронической болью и депрессией.

Патологическая боль — измененное восприятие болевых импульсов в результате нарушений в корковых и подкорковых отделах центральной нервной системы. Нарушения могут возникать на любом уровне ноцицептивной системы, а также при нарушении связи между ноцицептивными восходящими структурами и антиноцицептивной системой

Душевная боль — это специфическое психическое переживание, не связанное с органическими или функциональными расстройствами. Зачастую сопутствует депрессии, душевному расстройству. Чаще продолжительна и связана с потерей близкого человека.

Оценка боли Объективная оценка боли является главной методологической проблемой алгологии, ибо трудно, если вообще возможно, измерить субъективное ощущение, каковым по определению является боль. В связи с этим предпринимались многочисленные попытки оценивать боль по различным ее коррелятам в виде спонтанной и вызванной биоэлектрической активности мозга и мышц, гемодинамическим, термографическим биохимическим и иным показателям. Однако ни один из них не является достаточно специфичным, коэффициенты корреляции между ними и субъективными болевыми ощущениями как правило оказываются не достоверными.

В клинической практике для оценки боли используют различные варианты интервью, наиболее известным из которых является Мак Гилловский болевой опросник. Выбранные пациентом сенсорные, интенсивностные и аффективные характеристики актуальной боли определенным образом ранжируются и представляются в цифровом выражении. Методы оценки собственно боли дополняются тестами качества жизни, позволяющими определить выраженность дезадаптации пациента. Простейшим и самым распросраненным алгометрическим методом является визуально аналоговая шкала, на которой пациент фиксирует положение, соответствующее интенсивности его актуального болевого ощущения в диапазоне от полного отсутствия боли до максимального воображаемого уровня ее выраженности.

На основании самооценок различных компонентов боли, факторов провоцирующих ее возникновение и влияния на качество жизни с использованием принципа визуально аналоговой шкалы строится индивидуальный "профиль боли" (рис. 1). По длине радиальных отрезков профиля проводят дифференциальную оценку различных компонентов боли, а по площади всего профиля ее интегральную оценку. В зависимости от конкретной ситуации можно менять количество и вид шкал профиля, например вводить шкалы характеризующие выраженность вегетативных, психических или иных индивидуальных проявлений боли. Метод удобен для мониторинга боли служит целям вспомогательной дифференциальной диагностики, оценки эффективности использования тех или иных методов обезболивания. Построение пациентами собственных болевых профилей способствует обучению их самостоятельному контролю боли, обычно оказывает психотерапевтический эффект

Список литературы: Медицинские сайты: 1. http: //www. ty-doctor. ru/1_abst_reanim. html 2. http: //chitalky. ru/? p=5221 3. http: //www. all-pages. com/news/1/16/44/10558. html 4. http: //humbio. ru/humbio/har/003 fa 790. htm 5. http: //pathologi. com/index. php? option=com_content&view=arti cle&id=1263: 2010 -09 -19 -12 -24 -41&catid=61: 2010 -09 -19 -12 -0921&Itemid=82 6. http: //megaznanie. ru/index. php/encyclopedia/medicine/47192010 -08 -05 -13 -31 -42. html 7. http: //honestmed. ru/index. php? page=syndrome 8. « Нервные болезни» Е. И. Гусев, В. Е. Гречко, Г. С. Бурд. 1998 г 9. « Неврология» Смағұл Қайшыбаев, Алматы 2009 г 10. www. google. kz, https: //ru. wikipedia. org
Artykbaeva_Asem.pptx