ПЛР(Креницька Дарина).ppt
- Количество слайдов: 26

ННЦ «Інститут біології» кафедра: біохімії Полімеразна ланцюгова реакція (ПЛР) Виконала: студентка 2 курсу, 6 групи Креницька Дарина Ігорівна 1

Полімеразна ланцюгова реакція (ПЛР) q Метод створено К. Мюллісом у 1983 р. q Полімеразна ланцюгова реакція (ПЛР) – це метод ампліфікації певної ділянки ДНК чи РНК in vitro Кері Мюлліс Нобелівський лауреат з хімії, 1993 р. q. Під час ПЛР багатократно повторюють синтез певної ділянки ДНК. Метод дає змогу розмножити певні молекули ДНК до мільйонів копій (мікрограмових кількостей) навіть тоді, коли у вихідному зразку є лише одна копія цієї молекули q Використовують ДНК-полімеразу та олігонуклеотидні праймери, що комплементарні до 3’-кінців фрагмента матриці, який хочуть ампліфікувати 2

q У ПЛР використовують термостабільні полімерази, як наприклад, Taq-полімеразу з термофільної бактерії Thermus aquaticus q Оптимальна температура для реакції полімеризації, яку каталізує цей фермент, – від 75 до 80°С. При нагріванні інкубаційної суміші фермент не денатурує. Тому після кожного циклу немає потреби знов вносити полімеразу у реакційну суміш. Це дало змогу автоматизувати ПЛР та досягти надзвичайно високого ступеня продуктивності та чутливості методу q При високій температурі спарювання праймерів та матриці більш специфічне, ніж при температурі 37°С, й не відбувається ампліфікації небажаних ділянок ДНК. Це суттєво підвищує специфічність і чутливість методу q Процес здійснюється в автоматичній ПЛРмашині, яка нагріває та охолоджує пробірки із реакційною сумішшю за дуже короткий проміжок часу 3
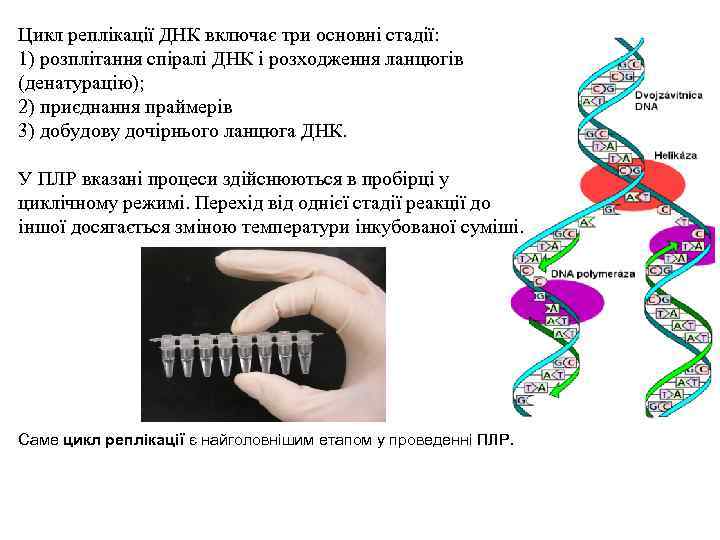
Цикл реплікації ДНК включає три основні стадії: 1) розплітання спіралі ДНК і розходження ланцюгів (денатурацію); 2) приєднання праймерів 3) добудову дочірнього ланцюга ДНК. У ПЛР вказані процеси здійснюються в пробірці у циклічному режимі. Перехід від однієї стадії реакції до іншої досягається зміною температури інкубованої суміші. Саме цикл реплікації є найголовнішим етапом у проведенні ПЛР.
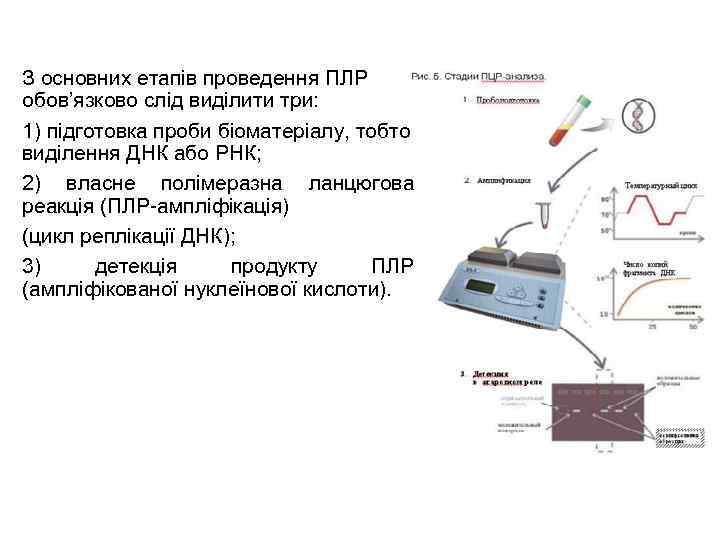
З основних етапів проведення ПЛР обов’язково слід виділити три: 1) підготовка проби біоматеріалу, тобто виділення ДНК або РНК; 2) власне полімеразна ланцюгова реакція (ПЛР-ампліфікація) (цикл реплікації ДНК); 3) детекція продукту ПЛР (ампліфікованої нуклеїнової кислоти).
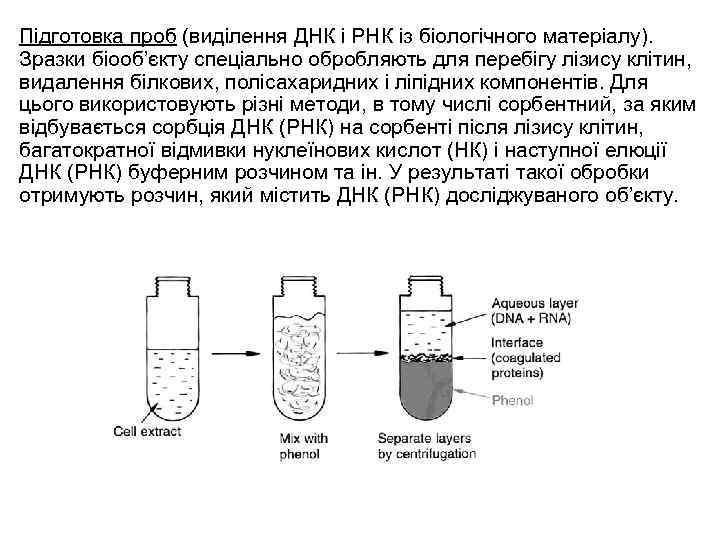
Підготовка проб (виділення ДНК і РНК із біологічного матеріалу). Зразки біооб’єкту спеціально обробляють для перебігу лізису клітин, видалення білкових, полісахаридних і ліпідних компонентів. Для цього використовують різні методи, в тому числі сорбентний, за яким відбувається сорбція ДНК (РНК) на сорбенті після лізису клітин, багатократної відмивки нуклеїнових кислот (НК) і наступної елюції ДНК (РНК) буферним розчином та ін. У результаті такої обробки отримують розчин, який містить ДНК (РНК) досліджуваного об’єкту.

Отриманий розчин ДНК можна зберігати протягом тижня за температури 2 – 8 °С та до року (за температури – 60 °С). Не підлягає зберіганню розчин очищеної РНК. Його необхідно відразу ж використовувати у дослідженнях. Проби можна зберігати тільки у вигляді отриманих з допомогою зворотної транскрипції розчинів комплементарної ДНК (к. ДНК).
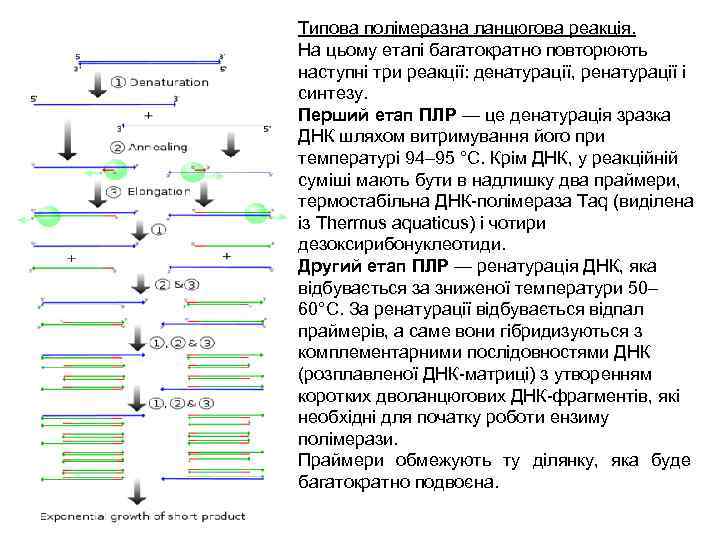
Типова полімеразна ланцюгова реакція. На цьому етапі багатократно повторюють наступні три реакції: денатурації, ренатурації і синтезу. Перший етап ПЛР — це денатурація зразка ДНК шляхом витримування його при температурі 94– 95 °С. Крім ДНК, у реакційній суміші мають бути в надлишку два праймери, термостабільна ДНК-полімераза Taq (виділена із Thermus aquaticus) і чотири дезоксирибонуклеотиди. Другий етап ПЛР — ренатурація ДНК, яка відбувається за зниженої температури 50– 60°С. За ренатурації відбувається відпал праймерів, а саме вони гібридизуються з комплементарними послідовностями ДНК (розплавленої ДНК-матриці) з утворенням коротких дволанцюгових ДНК-фрагментів, які необхідні для початку роботи ензиму полімерази. Праймери обмежують ту ділянку, яка буде багатократно подвоєна.
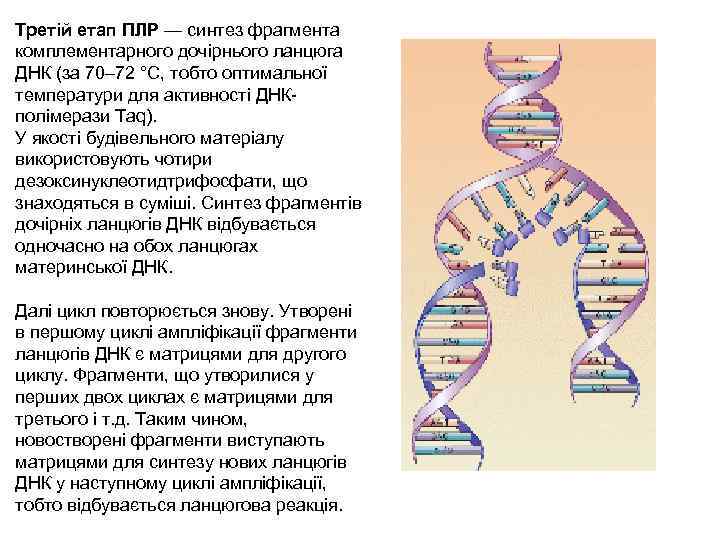
Третій етап ПЛР — синтез фрагмента комплементарного дочірнього ланцюга ДНК (за 70– 72 °С, тобто оптимальної температури для активності ДНКполімерази Taq). У якості будівельного матеріалу використовують чотири дезоксинуклеотидтрифосфати, що знаходяться в суміші. Синтез фрагментів дочірніх ланцюгів ДНК відбувається одночасно на обох ланцюгах материнської ДНК. Далі цикл повторюється знову. Утворені в першому циклі ампліфікації фрагменти ланцюгів ДНК є матрицями для другого циклу. Фрагменти, що утворилися у перших двох циклах є матрицями для третього і т. д. Таким чином, новостворені фрагменти виступають матрицями для синтезу нових ланцюгів ДНК у наступному циклі ампліфікації, тобто відбувається ланцюгова реакція.
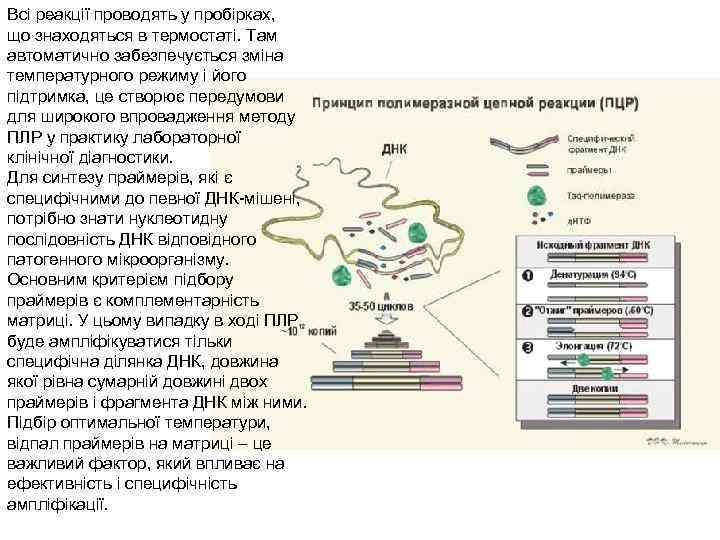
Всі реакції проводять у пробірках, що знаходяться в термостаті. Там автоматично забезпечується зміна температурного режиму і його підтримка, це створює передумови для широкого впровадження методу ПЛР у практику лабораторної клінічної діагностики. Для синтезу праймерів, які є специфічними до певної ДНК-мішені, потрібно знати нуклеотидну послідовність ДНК відповідного патогенного мікроорганізму. Основним критерієм підбору праймерів є комплементарність матриці. У цьому випадку в ході ПЛР буде ампліфікуватися тільки специфічна ділянка ДНК, довжина якої рівна сумарній довжині двох праймерів і фрагмента ДНК між ними. Підбір оптимальної температури, відпал праймерів на матриці – це важливий фактор, який впливає на ефективність і специфічність ампліфікації.
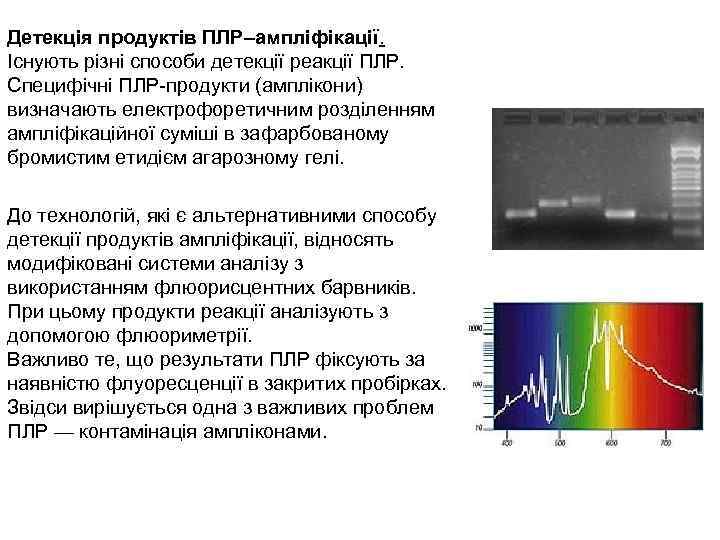
Детекція продуктів ПЛР–ампліфікації. Існують різні способи детекції реакції ПЛР. Специфічні ПЛР-продукти (амплікони) визначають електрофоретичним розділенням ампліфікаційної суміші в зафарбованому бромистим етидієм агарозному гелі. До технологій, які є альтернативними способу детекції продуктів ампліфікації, відносять модифіковані системи аналізу з використанням флюорисцентних барвників. При цьому продукти реакції аналізують з допомогою флюориметрії. Важливо те, що результати ПЛР фіксують за наявністю флуоресценції в закритих пробірках. Звідси вирішується одна з важливих проблем ПЛР — контамінація ампліконами.
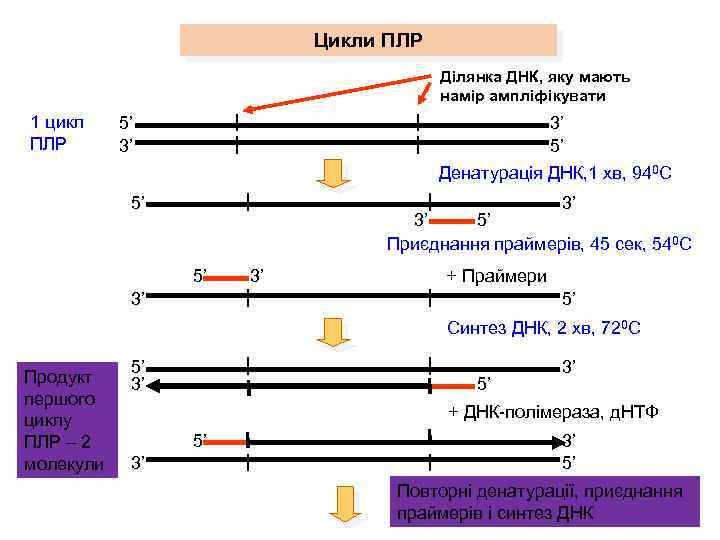
Цикли ПЛР Ділянка ДНК, яку мають намір ампліфікувати 1 цикл ПЛР 5’ 3’ 3’ 5’ Денатурація ДНК, 1 хв, 940 С 5’ 3’ 3’ 5’ Приєднання праймерів, 45 сек, 540 С 5’ 3’ + Праймери 3’ 5’ Синтез ДНК, 2 хв, 720 С Продукт першого циклу ПЛР – 2 молекули 5’ 3’ + ДНК-полімераза, д. НТФ 5’ 3’ 3’ 5’ Повторні денатурації, приєднання 12 праймерів і синтез ДНК
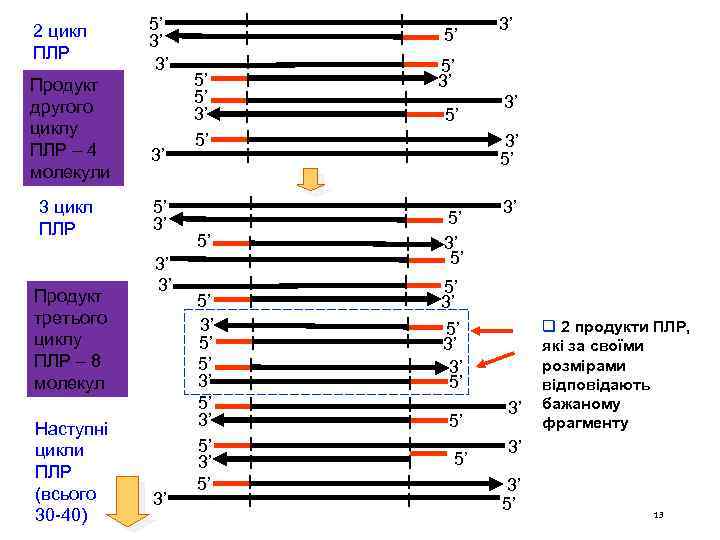
2 цикл ПЛР Продукт другого циклу ПЛР – 4 молекули 3 цикл ПЛР Продукт третього циклу ПЛР – 8 молекул Наступні цикли ПЛР (всього 30 -40) 5’ 3’ 3’ 5’ 5’ 5’ 3’ 5’ 3’ 5’ 3’ 3’ 5’ 5’ 5’ 3’ q 2 продукти ПЛР, які за своїми розмірами відповідають бажаному фрагменту 3’ 3’ 5’ 13

q Кількість сегментів ДНК, що оточені з обох кінців праймерами, з кожним циклом ПЛР збільшується експоненціально (наближається до залежності 2 n, де n — кількість циклів) q Продукти ПЛР аналізують за допомогою гель-електрофорезу Цикл К-сть копій потрібного сегменту 1 0 2 0 3 2 4 4 8 64 10 256 20 262144 30 268435456 Маркерні фрагменти ПЛРпродукти ПЛР-продукт – це окрема смуга (фракція) ДНК, яку виявляють після електрофорезу та 14 оброблення гелю бромідом етидію

Методи ПЛР: • ПЛР зі зворотною транскрипцією- використовується для ампліфікації, виділення або ідентифікації відомої послідовності з бібліотекии РНК. Перед звичайною ПЛР проводять транскрипцію молекули РНК за допомогою зворотної транскриптазиі отримують комплементарну ДНК (к. ДНК). Цим методом часто визначають, де і коли експресуються певні гени. • Асиметрична ПЛР ( Assymetric PCR) — проводиться тоді, коли потрібно ампліфікувати переважно один з ланцюжків початкової ДНК. Використовується в деяких методиках секвенування і гібридизаційного аналізу. ПЛР проводиться за класичним сценарієм, за винятком того, що один з праймерів береться у великому надлишку. 15

Методи ПЛР: • Мультиплексна ПЛР ( Multiplex PCR) — використання великого числа унікальних праймерів в одній реакції ПЛР для отримання кількох продуктів ПЛР різної довжини. Така реакція заміняє кілька окремих реакцій ПЛР, які вимагали би більшої кількості реагентів та часу. Температури відпалу кожного з наборів праймерів повинні бути оптимізовані, щоб вони могли правильно працювати в межах однієї реакції. Крім того, розміри ділянок ДНК, які ампліфікуються, повинні достатньо відрізнятися, щоб їх можна було розрізнити за допомогою гелевого електрофорезу. • Віртуальна ПЛР (in silico PCR) - математичний метод комп'ютерного аналізу теоретичної полімеразної ланцюгової реакції c використанням списку послідовностей праймерів (або ДНК-зондів) для передбачення потенційної ампліфікації ДНК досліджуваного геному, хромосоми, кільцевої ДНК або будьякого іншого ділянки ДНК. 16

Методи ПЛР: • Метод молекулярних колоній (або «ПЛР в гелі» , PCR Colony) — поліакріламідний гель полімеризують зі всіма компонентами ПЛР на поверхні і проводять термоциклування. У точках, які містять ДНК, до якої підібрані праймери, відбувається ампліфікація з утворенням молекулярних колоній. • Вкладена ПЛР (Nested PCR) — застосовується для зменшення частки побічних продуктів реакції. Використовують дві пари праймерів і проводять дві послідовні реакції. Друга пара праймерів ампліфікує ділянку ДНК усередині продукту першої реакції. 17

Методи ПЛР: • Інвертована ПЛР (Inverse PCR) — використовується в тому випадку, якщо відома лише невелика ділянка усередині потрібної послідовності. Цей метод особливо корисний, коли потрібно визначити фланкуючі(сусідні) послідовності після вставки ДНК в геном. Для здійснення інвертованої ПЛР проводять ряд розрізів ДНКрестриктазами з подальшим лігуванням. В результаті відомі фрагменти утворюються на обох кінцях невідомої ділянки, після чого можна проводити звичайну ПЛР. • Touchdown ПЛР (Touchdown PCR) — за допомогою цього методу зменшують вплив неспецифічної гібридизації праймерів на утворення продукту. Перші цикли проводять при температурі, вищій за температуру відпалу, потім кожні декілька циклів температуру знижують. За певної температури система пройде через смугу оптимальної специфічності праймерів до ДНК. 18

Методи ПЛР: • ПЛР довгих фрагментів ( Long-range PCR) — модифікація ПЛР для ампліфікації протяжних ділянок ДНК (10 kbp і більше). Використовують дві полімерази, одна з яких — Taq-полімераза з високою процесивністю (тобто полімераза здатна за один прохід синтезувати довгий ланцюг ДНК), а друга — ДНК полімераза з 3'5' ендонуклеазною активністю. Друга полімераза необхідна для того, щоб коригувати помилки, внесені першою. • ПЛР в реальному часі (або кількісна ПЛР)- метод включає в себе одночасно детекцію і кількісне визначення (вимірювання безпосередньо кількості копій, або вимір копій щодо внесеної ДНК або додаткових калібрувальних генів) специфічної послідовності ДНК у зразку. Метод використовує загальні принципи ПЛР. Основна відмінність полягає в тому, що вимірюється кількість ампліфікованої ДНК в реальному часі після кожного циклу ампліфікаці 19

Методи ПЛР: • ПЛР з аналізом у «кінцевій точці» (End-point PCR)модифікація методу ПЛР, яка дозволяє враховувати результаті реакції за флуоресценцією після ампліфікації без відкриття пробірки. Таким чином, вирішується одна із проблем ПЛР- проблема контамінації ампліконами. Один із варіантів Метод «FLASH» : специфічна гібридизація в процесі ампліфікації з ДНК-зондами, міченими флуорофорами. • ПЛР з «гарячим» стартом(hot-start PCR)-модифікація ПЛР з використанням ДНК-полімерази, в якій полімеразна активність блокується при кімнатній температурі антитілами або імітують антитіла невеликими молекулами типу Affibody, тобто в момент постановки реакції до першої денатурації в ПЛР. Зазвичай, перша денатурація проводиться при 95 ° C протягом 10 хвилин. 20

Методи ПЛР: • Імунна-ПЛР • ПЛР зі швидкою ампліфікацією кінців к. ДНК(RACEPCR) • Груп-специфічна ПЛР- ПЛР для родинних послідовностей всередині одного або між різними видами, використовуючи консервативні праймери до цих послідовностей. Протилежний цьому методу є - унікальна ПЛР -підбір праймерів для ампліфікації тільки конкретної послідовності серед споріднених послідовностей. 21

Недоліки ПЛР q Треба мати інформацію про нуклеотидну послідовність ДНК- мішені, щоб синтезувати праймери q Висока чутливість ПЛР примушує враховувати можливе забруднення зразків сторонньою ДНК, наприклад ДНК мікроорганізмів, або ДНК дослідника q Неточність реплікації ДНК під час ПЛР. Наприклад Taqполімеразі не властива 3’-5’екзонуклеазна активність, тому помилки під час синтезу ДНК виникають з підвищеною частотою. До 40% нових ланцюгів, що утворені Taq-полімеразою можуть містити неправильні нуклеотиди q Існує ймовірність, що частина праймерів будуть гібридизуватися з неспецифічними (небажаними) послідовностями і вони будуть ампліфіковані q У ході ПЛР синтезуються відносно короткі ланцюги (до 5 т. п. н. ). Зі зростанням довжини сегменту, який мають намір ампліфікувати, зростають труднощі у проведенні ПЛР 22

Переваги ПЛР q Висока чутливість методу. Він дає змогу виявити 1 певну послідовність ДНК на 100 тис – 1 млн клітин. Можна надійно виявити однокопійні гени у таких великих і складних геномах, як геном людини q Невелика кількість матеріалу, необхідного для ПЛР. Достатньо однієї клітини, щоб за допомогою ПЛР ампліфікувати її ДНК q Для ПЛР не завжди потрібна високоочищена ДНК може бути частково деградованою і виділятися з незвичайних джерел (наприклад, тканин, фіксованих у 10% формаліні і залитих у парафінові блоки, слини, волосяних сумок, нігтів, кісток, клаптиків шкіри, спинномозкової рідини, крові, що висохла тощо) q Швидкість. 25 – 50 циклів ПЛР проходять за 2 - 4 год q Велика кількість продуктів ПЛР (мкг). Розмножений in vitro фрагмент отримують у кількостях, достатніх для його прямого секвенування та інших процедур. Оскільки при цьому не потрібно проміжного етапу клонування фрагмента ДНК у векторних молекулах, то ПЛР називають безклітинним молекулярним клонуванням (cell-free molecular cloning) 23

Праймери для ПЛР q Вибір праймерів – найважливіший етап у проведенні ПЛР. Послідовність нуклеотидів праймера залежить від послідовності ДНК -мішені q Розмір праймерів – 18 – 25 нуклеотидів. Їх синтезують на автоматичних синтезаторах ДНК q Найважливіше значення має: довжина праймерів, їхній нуклеотидний склад, те, які нуклеотиди є на 3’-кінці праймера. Усі ці чинники визначають наскільки специфічно приєднується праймер до ДНК-мішені і чи пройде ПЛР Оптимізація ПЛР оптимізують за такими параментами як: q Кількість циклів q Час і температура проходження окремих етапів q Концентрація праймера і його послідовність q Концентрація у реакційній суміші полімерази, д. НТФ, Mg 2+ 24

Застосування ПЛР q Клонування певних ділянок з геному, за умови, що можна підібрати відповідні праймери (як альтернатива short gun – клонуванню) q Пошук певних послідовностей у геномі (як альтернатива методу гібридизації нуклеїнових кислот). Це використовують для: q Виявлення мутацій та генетичного поліморфізму популяцій q Виявлення філогенетичних зв’язків між особинами, сортами, породами, штамами, популяціями, видами (ДНК-типування) q Діагностики спадкових захворювань (виявлення мутацій, які їх зумовлюють) q Виявлення патогенів (виявлення специфічних генів, а м. РНК патогенних мікроорганізмів) q Пренатальної діагностики статі q Рятування генів вимерлих організмів q Аналізу функціонування генів тощо q. Встановлення батьківства 25
Дякую за увагу! 26
ПЛР(Креницька Дарина).ppt