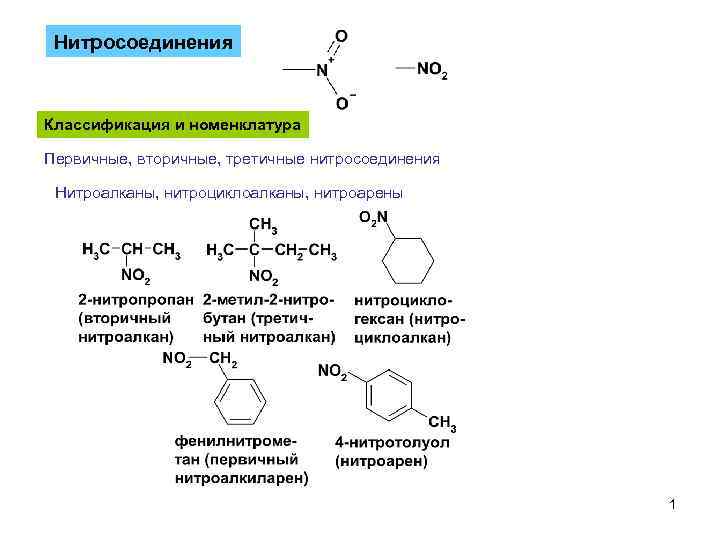
 Нитросоединения Классификация и номенклатура Первичные, вторичные, третичные нитросоединения Нитроалканы, нитроциклоалканы, нитроарены 1
Нитросоединения Классификация и номенклатура Первичные, вторичные, третичные нитросоединения Нитроалканы, нитроциклоалканы, нитроарены 1
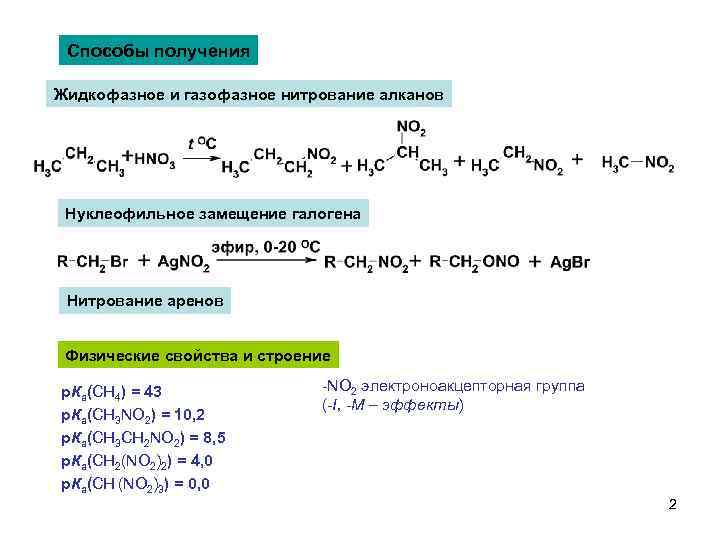 Способы получения Жидкофазное и газофазное нитрование алканов Нуклеофильное замещение галогена Нитрование аренов Физические свойства и строение р. Ка(CH 4) = 43 р. Ка(CH 3 NO 2) = 10, 2 р. Ка(CH 3 CH 2 NO 2) = 8, 5 р. Ка(CH 2(NO 2)2) = 4, 0 р. Ка(CH (NO 2)3) = 0, 0 -NO 2 электроноакцепторная группа (-I, -M – эффекты) 2
Способы получения Жидкофазное и газофазное нитрование алканов Нуклеофильное замещение галогена Нитрование аренов Физические свойства и строение р. Ка(CH 4) = 43 р. Ка(CH 3 NO 2) = 10, 2 р. Ка(CH 3 CH 2 NO 2) = 8, 5 р. Ка(CH 2(NO 2)2) = 4, 0 р. Ка(CH (NO 2)3) = 0, 0 -NO 2 электроноакцепторная группа (-I, -M – эффекты) 2
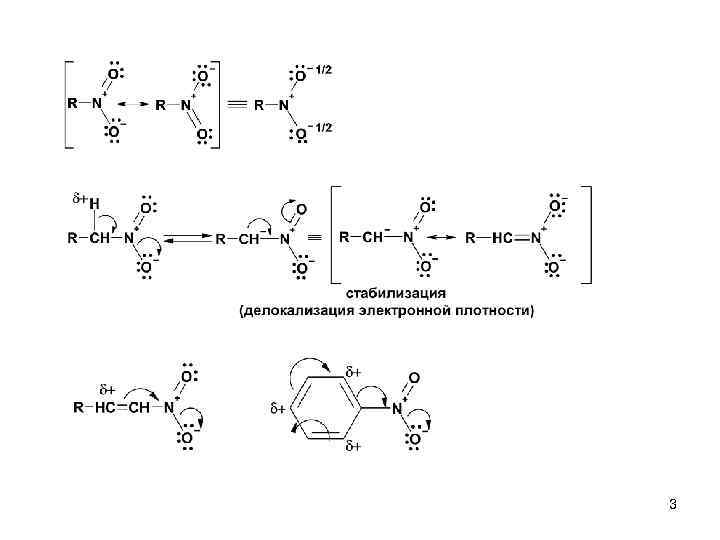 3
3
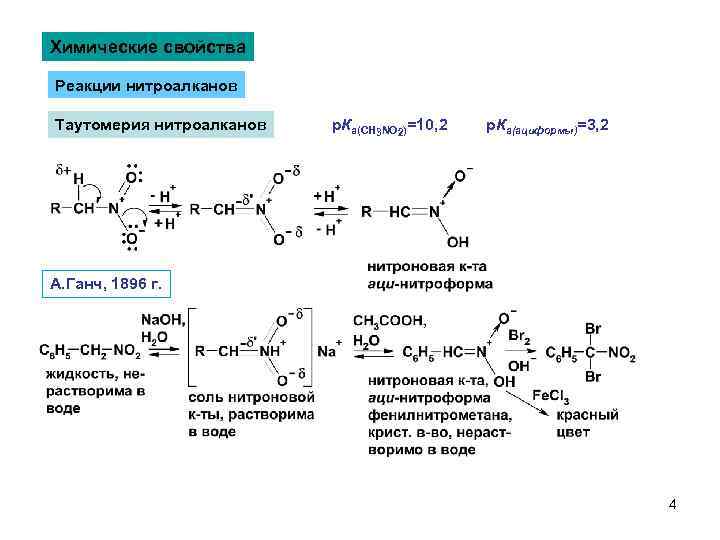 Химические свойства Реакции нитроалканов Таутомерия нитроалканов р. Ка(CH 3 NO 2)=10, 2 р. Ка(ациформы)=3, 2 А. Ганч, 1896 г. 4
Химические свойства Реакции нитроалканов Таутомерия нитроалканов р. Ка(CH 3 NO 2)=10, 2 р. Ка(ациформы)=3, 2 А. Ганч, 1896 г. 4
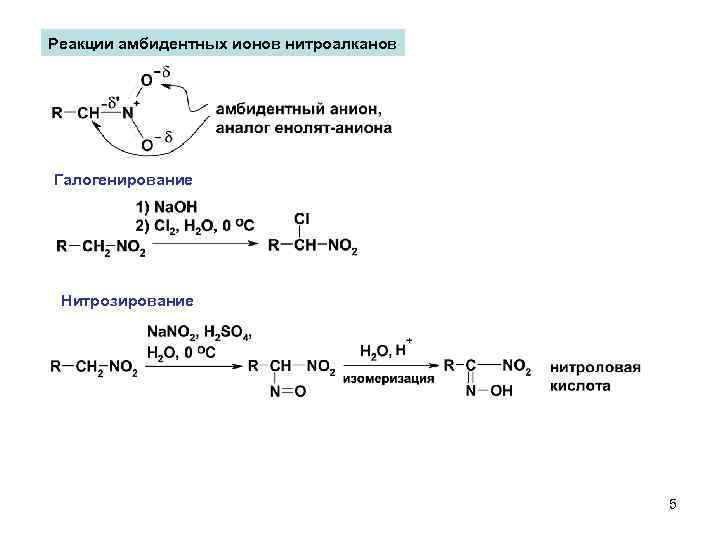 Реакции амбидентных ионов нитроалканов Галогенирование Нитрозирование 5
Реакции амбидентных ионов нитроалканов Галогенирование Нитрозирование 5
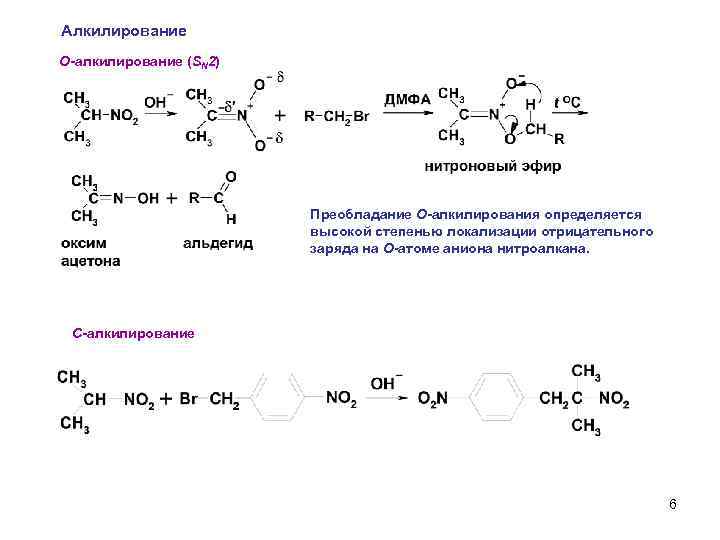 Алкилирование О-алкилирование (SN 2) Преобладание О-алкилирования определяется высокой степенью локализации отрицательного заряда на О-атоме аниона нитроалкана. C-алкилирование 6
Алкилирование О-алкилирование (SN 2) Преобладание О-алкилирования определяется высокой степенью локализации отрицательного заряда на О-атоме аниона нитроалкана. C-алкилирование 6
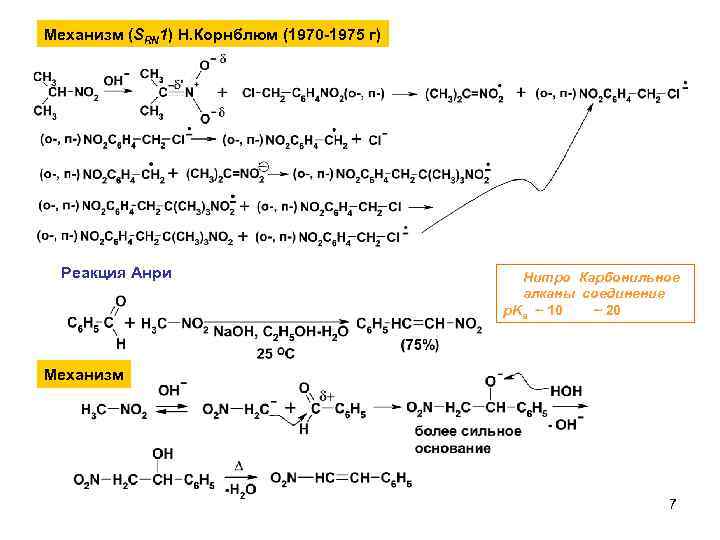 Механизм (SRN 1) Н. Корнблюм (1970 -1975 г) Реакция Анри Нитро Карбонильное алканы соединение p. Ka ~ 10 ~ 20 Механизм 7
Механизм (SRN 1) Н. Корнблюм (1970 -1975 г) Реакция Анри Нитро Карбонильное алканы соединение p. Ka ~ 10 ~ 20 Механизм 7
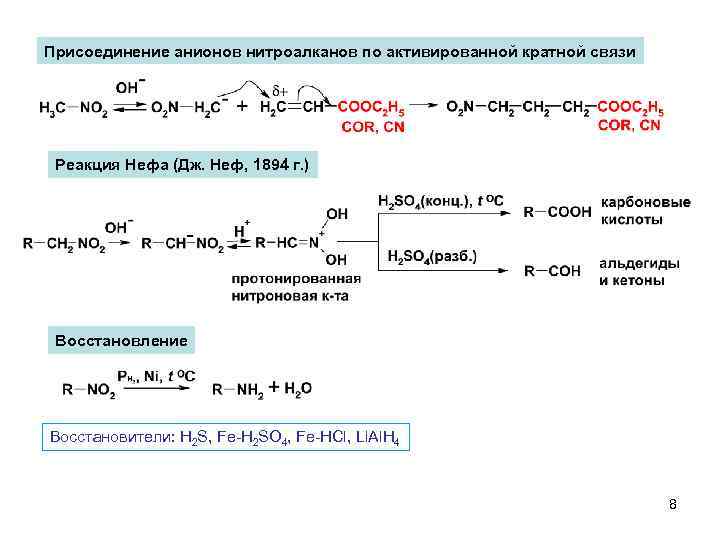 Присоединение анионов нитроалканов по активированной кратной связи Реакция Нефа (Дж. Неф, 1894 г. ) Восстановление Восстановители: H 2 S, Fe-H 2 SO 4, Fe-HCl, Li. Al. H 4 8
Присоединение анионов нитроалканов по активированной кратной связи Реакция Нефа (Дж. Неф, 1894 г. ) Восстановление Восстановители: H 2 S, Fe-H 2 SO 4, Fe-HCl, Li. Al. H 4 8
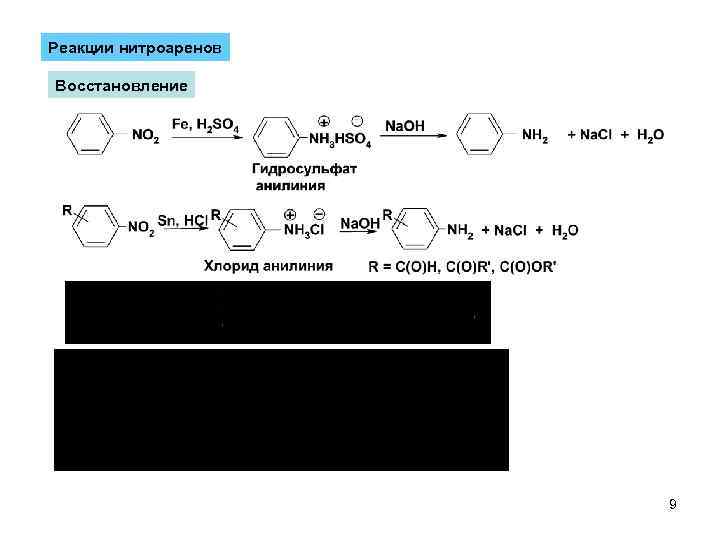 Реакции нитроаренов Восстановление 9
Реакции нитроаренов Восстановление 9
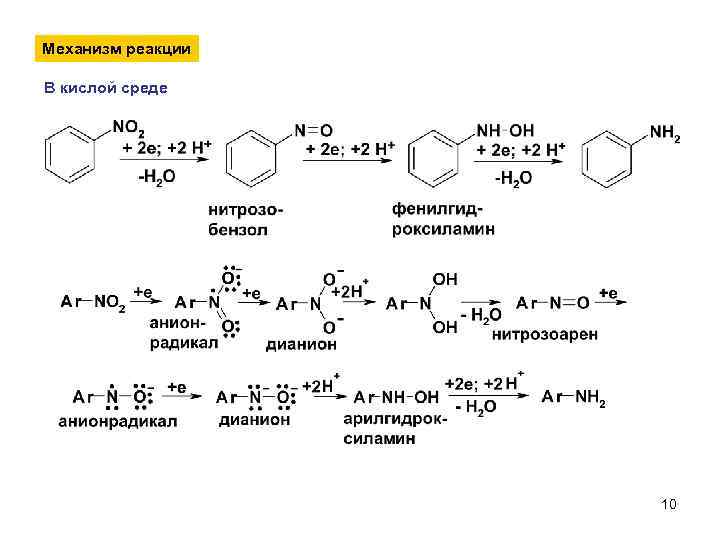 Механизм реакции В кислой среде 10
Механизм реакции В кислой среде 10
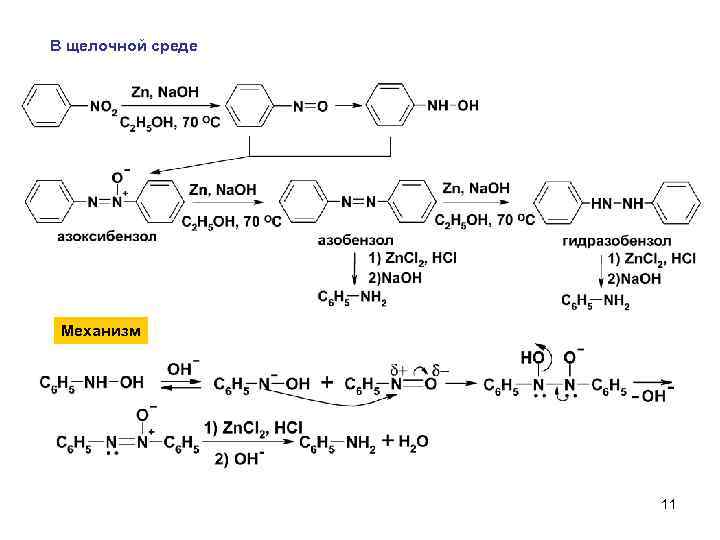 В щелочной среде Механизм 11
В щелочной среде Механизм 11
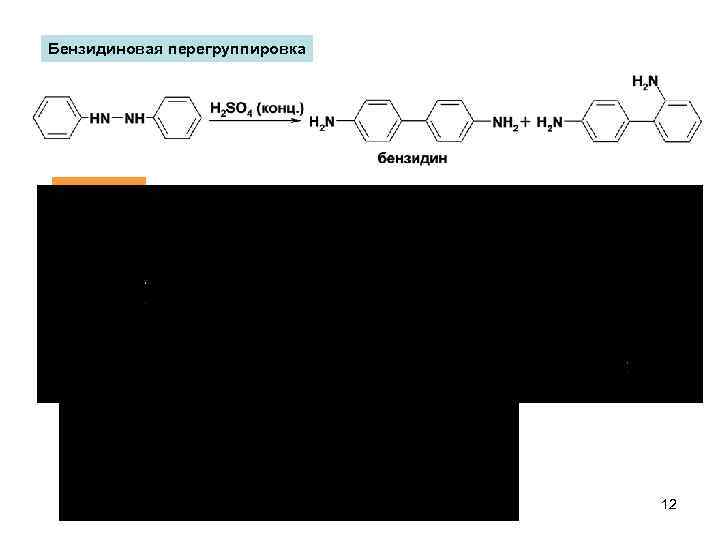 Бензидиновая перегруппировка Механизм 12
Бензидиновая перегруппировка Механизм 12
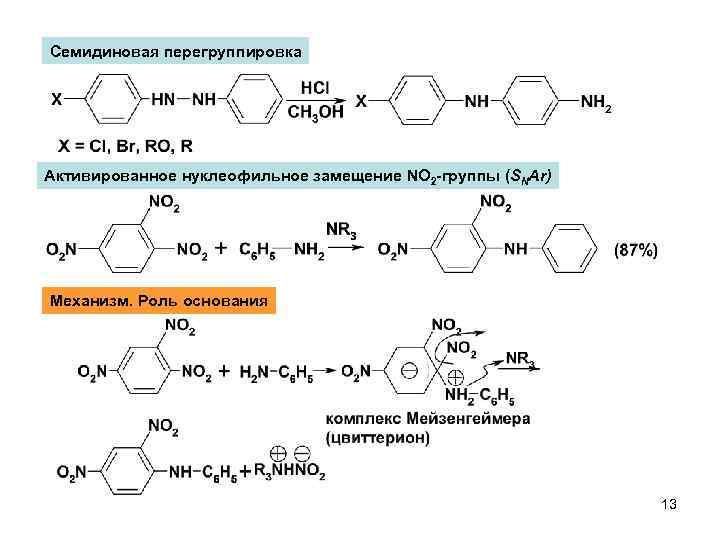 Семидиновая перегруппировка Активированное нуклеофильное замещение NO 2 -группы (SNAr) Механизм. Роль основания 13
Семидиновая перегруппировка Активированное нуклеофильное замещение NO 2 -группы (SNAr) Механизм. Роль основания 13
 14
14