 NH 3
NH 3
 История открытия аммиака NH 3 Аммиак был получен в чистом виде в 1774 г. английским химиком Джозефом Луи Пристли. Он нагревал аммониак (хлорид аммония) с гашеной известью (гидроксид кальция). Пристли назвал газ «щелочным воздухом или летучей щелочью» , поскольку водный раствор 1711 -1794 г. аммиака имел все признаки щелочи.
История открытия аммиака NH 3 Аммиак был получен в чистом виде в 1774 г. английским химиком Джозефом Луи Пристли. Он нагревал аммониак (хлорид аммония) с гашеной известью (гидроксид кальция). Пристли назвал газ «щелочным воздухом или летучей щелочью» , поскольку водный раствор 1711 -1794 г. аммиака имел все признаки щелочи.
 История открытия аммиака NH 3 В 1784 французский химик Бертолле разложением аммиака доказал его элементный состав, который в 1787 получил официальное название «нашатырь» – от латинского названия нашатырной щелочи – sal ammoniac. 1723 -1802 г. Это название сохраняется и до сих пор в большинстве западноевропейских языков (нем. Ammonium chloride, англ. Ammonia, фр. ammoniaque).
История открытия аммиака NH 3 В 1784 французский химик Бертолле разложением аммиака доказал его элементный состав, который в 1787 получил официальное название «нашатырь» – от латинского названия нашатырной щелочи – sal ammoniac. 1723 -1802 г. Это название сохраняется и до сих пор в большинстве западноевропейских языков (нем. Ammonium chloride, англ. Ammonia, фр. ammoniaque).
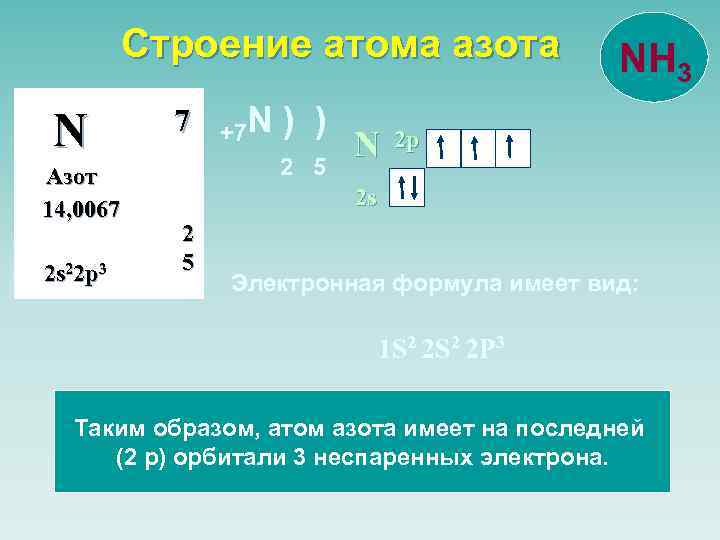 Строение атома азота N Азот 14, 0067 2 s 22 p 3 7 +7 N ) ) 2 5 N NH 3 2 p 2 s 2 5 Электронная формула имеет вид: 1 S 2 2 P 3 Таким образом, атом азота имеет на последней (2 р) орбитали 3 неспаренных электрона.
Строение атома азота N Азот 14, 0067 2 s 22 p 3 7 +7 N ) ) 2 5 N NH 3 2 p 2 s 2 5 Электронная формула имеет вид: 1 S 2 2 P 3 Таким образом, атом азота имеет на последней (2 р) орбитали 3 неспаренных электрона.
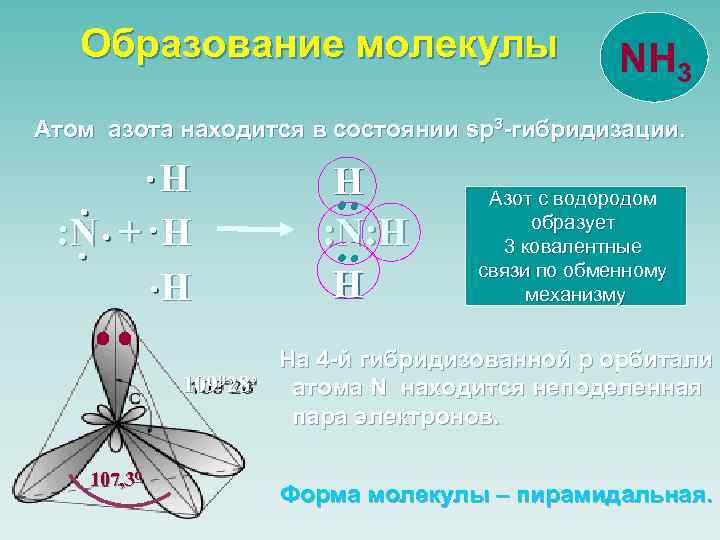 Образование молекулы NH 3 Атом азота находится в состоянии sp 3 -гибридизации. : : : : Н Н : N + H : N: Н Н Н 107, 30 Азот с водородом образует 3 ковалентные связи по обменному механизму На 4 -й гибридизованной p орбитали 109028’ атома N находится неподеленная пара электронов. Форма молекулы – пирамидальная.
Образование молекулы NH 3 Атом азота находится в состоянии sp 3 -гибридизации. : : : : Н Н : N + H : N: Н Н Н 107, 30 Азот с водородом образует 3 ковалентные связи по обменному механизму На 4 -й гибридизованной p орбитали 109028’ атома N находится неподеленная пара электронов. Форма молекулы – пирамидальная.
 Связи N-H полярные, общие электронные пары смещены в сторону атома азота как атома с большей ЭО. ЭО (Н)=2, 1 ЭО (N)=3, 5. Молекула полярная. NH 3 Азот с водородом образует 3 ковалентные связи по обменному механизму
Связи N-H полярные, общие электронные пары смещены в сторону атома азота как атома с большей ЭО. ЭО (Н)=2, 1 ЭО (N)=3, 5. Молекула полярная. NH 3 Азот с водородом образует 3 ковалентные связи по обменному механизму
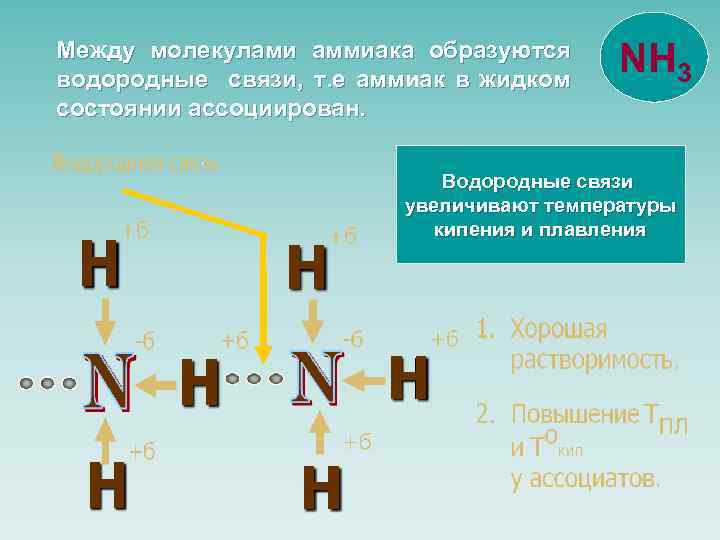 Между молекулами аммиака образуются водородные связи, т. е аммиак в жидком состоянии ассоциирован. NH 3 Водородные связи увеличивают температуры кипения и плавления
Между молекулами аммиака образуются водородные связи, т. е аммиак в жидком состоянии ассоциирован. NH 3 Водородные связи увеличивают температуры кипения и плавления
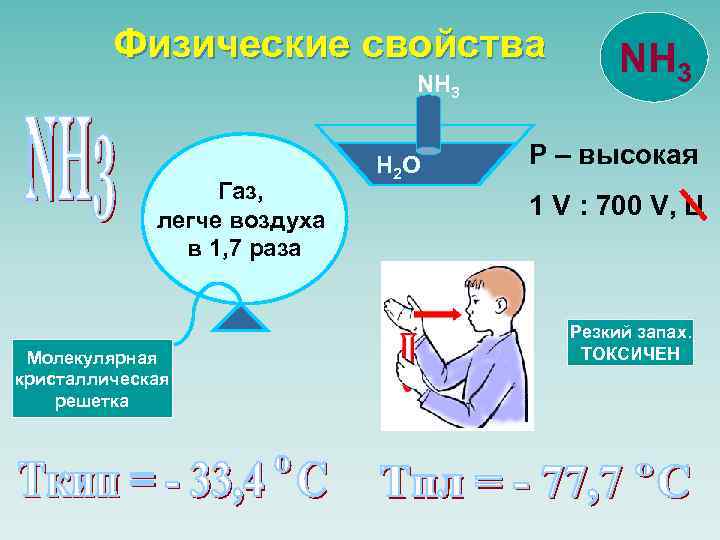 Физические свойства NH 3 Газ, легче воздуха в 1, 7 раза Молекулярная кристаллическая решетка H 2 O NH 3 Р – высокая 1 V : 700 V, Ц Резкий запах. ТОКСИЧЕН
Физические свойства NH 3 Газ, легче воздуха в 1, 7 раза Молекулярная кристаллическая решетка H 2 O NH 3 Р – высокая 1 V : 700 V, Ц Резкий запах. ТОКСИЧЕН
 В лаборатории: 1. Действием щелочей на соли аммония: t 2 NH 4 Cl + Ca(OH)2 = Ca. Cl 2 + 2 NH 3↑+2 H 2 O Нашатырь + гашеная известь 2. Гидролиз нитридов: Mg 3 N 2 + 6 H 2 O=3 Mg(OH)2+2 NH 3↑ NH 3
В лаборатории: 1. Действием щелочей на соли аммония: t 2 NH 4 Cl + Ca(OH)2 = Ca. Cl 2 + 2 NH 3↑+2 H 2 O Нашатырь + гашеная известь 2. Гидролиз нитридов: Mg 3 N 2 + 6 H 2 O=3 Mg(OH)2+2 NH 3↑ NH 3
 Химические свойства NH 3 -3 NH 3 – низшая степень окисления азота. 1. Аммиак – восстановитель 2. Основные свойства (неподеленная пара электронов) 3. Специфические свойства
Химические свойства NH 3 -3 NH 3 – низшая степень окисления азота. 1. Аммиак – восстановитель 2. Основные свойства (неподеленная пара электронов) 3. Специфические свойства
 Аммиак-восстановитель v Реакция горения аммиака (до N 2): 4 NH 3 + 3 O 2 = 2 N 2+ 6 H 2 O = NH 3
Аммиак-восстановитель v Реакция горения аммиака (до N 2): 4 NH 3 + 3 O 2 = 2 N 2+ 6 H 2 O = NH 3
 Аммиак-восстановитель NH 3 v Каталитическое окисление аммиака (до NO): 4 NH 3 + 5 O 2 = 4 NO + 6 H 2 O
Аммиак-восстановитель NH 3 v Каталитическое окисление аммиака (до NO): 4 NH 3 + 5 O 2 = 4 NO + 6 H 2 O
 v Аммиаком можно восстановить некоторые неактивные металлы: 3 Cu. O + 2 NH 3 = 3 Cu + N 2 + 3 H 2 O KMn. O 4 v Аммиак обесцвечивает перманганат калия: 2 KMn. O 4+2 NH 3= 2 KOH+N 2+ 2 H 2 O +2 Mn. O 2 NH 3 Br 2 v Аммиак обесцвечивает бромную воду: 3 Br 2 + 8 NH 3 = N 2 + 6 NH 4 Br I цвет
v Аммиаком можно восстановить некоторые неактивные металлы: 3 Cu. O + 2 NH 3 = 3 Cu + N 2 + 3 H 2 O KMn. O 4 v Аммиак обесцвечивает перманганат калия: 2 KMn. O 4+2 NH 3= 2 KOH+N 2+ 2 H 2 O +2 Mn. O 2 NH 3 Br 2 v Аммиак обесцвечивает бромную воду: 3 Br 2 + 8 NH 3 = N 2 + 6 NH 4 Br I цвет
 Основные свойства Взаимодействие с водой v Аммиак реагирует с водой, образуя гидрат аммиака (аммиачная вода): NH 3 + H 2 O =NH 4 OH Изменяет окраску индикаторов: Фенолфталеин – б/цв малиновый Лакмус становится синим Гидроксид аммония проявляет все свойства щелочей !!! NH 3
Основные свойства Взаимодействие с водой v Аммиак реагирует с водой, образуя гидрат аммиака (аммиачная вода): NH 3 + H 2 O =NH 4 OH Изменяет окраску индикаторов: Фенолфталеин – б/цв малиновый Лакмус становится синим Гидроксид аммония проявляет все свойства щелочей !!! NH 3
 Основные свойства NH 3 Взаимодействие с кислотами NH 3 + HCl → NH 4 Cl хлорид аммония (нашатырь) 2 NH 3 Дым без огня ? ! (Образуется за счет образования хлорида аммония) + H 2 SO 4 → (NH 4)2 SO 4 сульфат аммония
Основные свойства NH 3 Взаимодействие с кислотами NH 3 + HCl → NH 4 Cl хлорид аммония (нашатырь) 2 NH 3 Дым без огня ? ! (Образуется за счет образования хлорида аммония) + H 2 SO 4 → (NH 4)2 SO 4 сульфат аммония
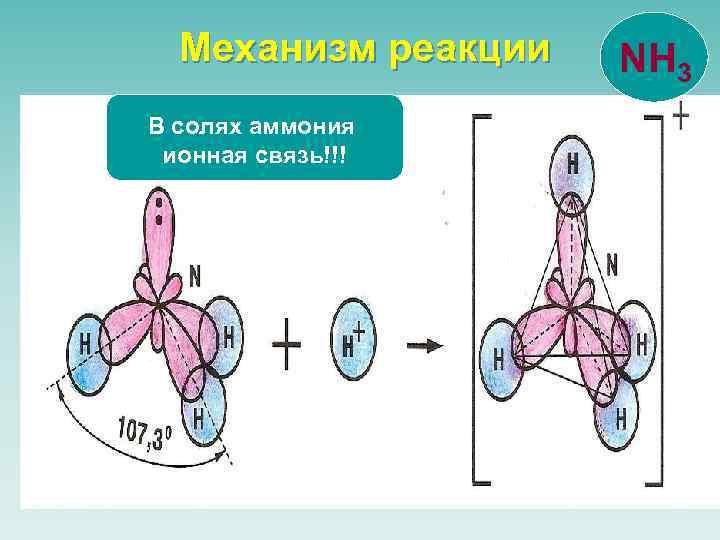 Механизм реакции В солях аммония ионная связь!!! NH 3
Механизм реакции В солях аммония ионная связь!!! NH 3
 Образование иона аммония NH 3 Три связи образованы по обменному механизму четвертая – по донорно-акцепторному. Донор - молекула или ион, имеющие свободную пару электронов. Акцептор - молекула или ион, имеющие свободную орбиталь. • • H+ + H N H АКЦЕПТОР H ДОНОР H H • • N H H +
Образование иона аммония NH 3 Три связи образованы по обменному механизму четвертая – по донорно-акцепторному. Донор - молекула или ион, имеющие свободную пару электронов. Акцептор - молекула или ион, имеющие свободную орбиталь. • • H+ + H N H АКЦЕПТОР H ДОНОР H H • • N H H +
 Специфические свойства NH 3 1. Взаимодействие с гипохлоритом натрия (образование гидразина): 2 NH 3 + Na. Cl. O = N 2 H 4 + Na. Cl+H 2 O Гидразин используют для получения ракетного топлива
Специфические свойства NH 3 1. Взаимодействие с гипохлоритом натрия (образование гидразина): 2 NH 3 + Na. Cl. O = N 2 H 4 + Na. Cl+H 2 O Гидразин используют для получения ракетного топлива
 Специфические свойства NH 3 2. Взаимодействие с активными металлами (образование амидов): 2 NH 3 + 2 К = 2 KNH 2 + Н 2
Специфические свойства NH 3 2. Взаимодействие с активными металлами (образование амидов): 2 NH 3 + 2 К = 2 KNH 2 + Н 2
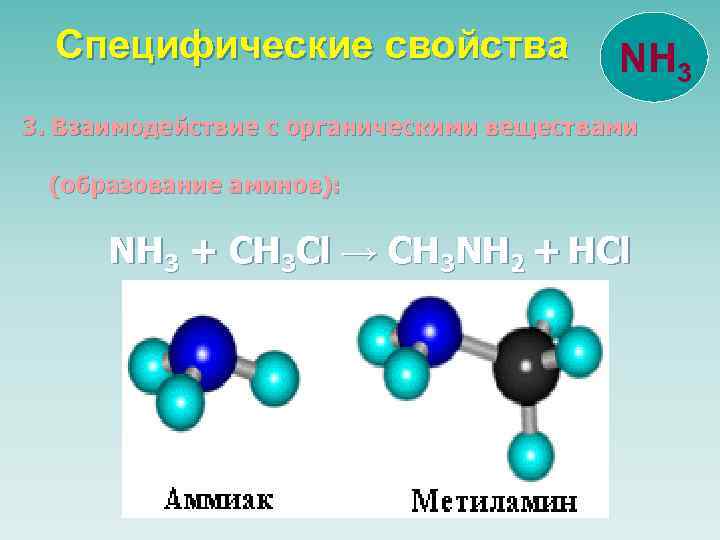 Специфические свойства NH 3 3. Взаимодействие с органическими веществами (образование аминов): NH 3 + CH 3 Cl → CH 3 NH 2 + HCl
Специфические свойства NH 3 3. Взаимодействие с органическими веществами (образование аминов): NH 3 + CH 3 Cl → CH 3 NH 2 + HCl
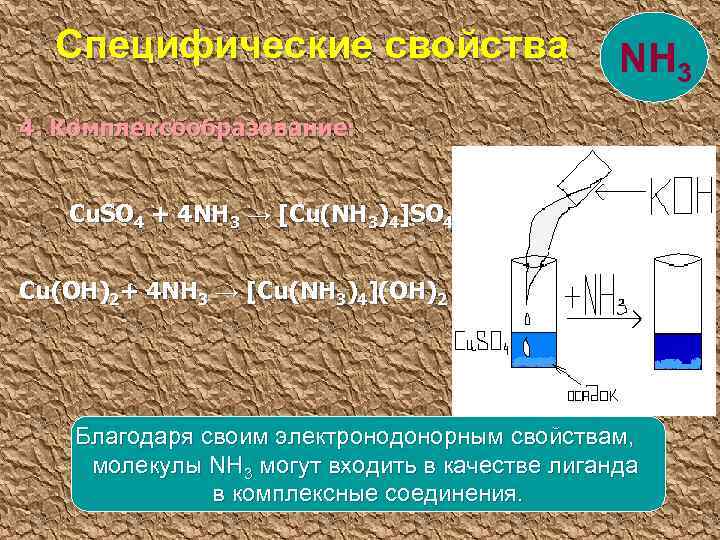 Специфические свойства NH 3 4. Комплексообразование: Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 Cu(OH)2+ 4 NH 3 → [Cu(NH 3)4](OH)2 Благодаря своим электронодонорным свойствам, молекулы NH 3 могут входить в качестве лиганда в комплексные соединения.
Специфические свойства NH 3 4. Комплексообразование: Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 Cu(OH)2+ 4 NH 3 → [Cu(NH 3)4](OH)2 Благодаря своим электронодонорным свойствам, молекулы NH 3 могут входить в качестве лиганда в комплексные соединения.
 Обобщение
Обобщение
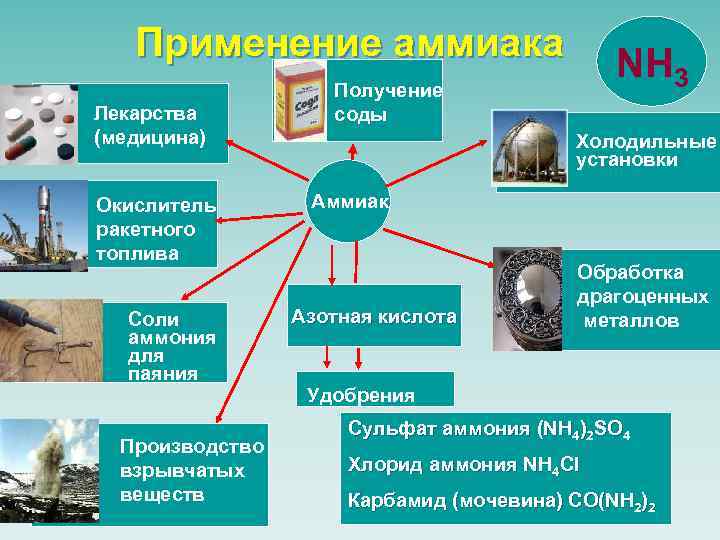 Применение аммиака Лекарства (медицина) Окислитель ракетного топлива Соли аммония для паяния Производство взрывчатых веществ NH 3 Получение соды Холодильные установки Аммиак Азотная кислота Обработка драгоценных металлов Удобрения Сульфат аммония (NH 4)2 SO 4 Хлорид аммония NH 4 Cl Карбамид (мочевина) CO(NH 2)2
Применение аммиака Лекарства (медицина) Окислитель ракетного топлива Соли аммония для паяния Производство взрывчатых веществ NH 3 Получение соды Холодильные установки Аммиак Азотная кислота Обработка драгоценных металлов Удобрения Сульфат аммония (NH 4)2 SO 4 Хлорид аммония NH 4 Cl Карбамид (мочевина) CO(NH 2)2
 Техногенные катастрофы NH 3
Техногенные катастрофы NH 3
 Отравление аммиаком NH 3 ПДК аммиака составляет 0, 001 мг/л. 1. Нельзя прикасаться к разлитому веществу, это может вызвать болезненный ожог кожных покровов. 2. При отравлении аммиаком нельзя пить, а нужно закапать в глаза альбуцид или промыть глаза раствором борной кислоты. 3. В нос закапать теплое подсолнечное, оливковое или персиковое масло, а лицо, руки и вообще пораженные участки тела промыть 2 -процентным раствором борной кислоты.
Отравление аммиаком NH 3 ПДК аммиака составляет 0, 001 мг/л. 1. Нельзя прикасаться к разлитому веществу, это может вызвать болезненный ожог кожных покровов. 2. При отравлении аммиаком нельзя пить, а нужно закапать в глаза альбуцид или промыть глаза раствором борной кислоты. 3. В нос закапать теплое подсолнечное, оливковое или персиковое масло, а лицо, руки и вообще пораженные участки тела промыть 2 -процентным раствором борной кислоты.
 Проверь себя ? Для аммиака характерны свойства: 1 NH 3 Аммиак взаимодействует с: 2 Ошибка кислот Ошибка солей щелочами Ошибка Правильно! кислотами Правильно! оснований оксидов Ошибка неметаллами Ошибка Цвет лакмуса в растворе аммиака: 3 фиолетовый Ошибка бесцветный Ошибка Аммиак – 4 восстановитель в реакции красный Ошибка С кислотами Ошибка с неметаллами Ошибка Правильно! синий С оксидами Правильно! металлов С металлами Ошибка
Проверь себя ? Для аммиака характерны свойства: 1 NH 3 Аммиак взаимодействует с: 2 Ошибка кислот Ошибка солей щелочами Ошибка Правильно! кислотами Правильно! оснований оксидов Ошибка неметаллами Ошибка Цвет лакмуса в растворе аммиака: 3 фиолетовый Ошибка бесцветный Ошибка Аммиак – 4 восстановитель в реакции красный Ошибка С кислотами Ошибка с неметаллами Ошибка Правильно! синий С оксидами Правильно! металлов С металлами Ошибка
 Готовимся к экзамену • Осуществите цепочку превращений: NH 3 N 2 NH 3 (NH 4)2 SO 4 NH 4 Cl NH 3 N 2 Li 3 N NH 3 Запишите уравнения реакций. Где возможно, рассмотрите с точки зрения ТЭД и ОВР. Приведите электронный баланс, полные и сокращенные ионные уравнения.
Готовимся к экзамену • Осуществите цепочку превращений: NH 3 N 2 NH 3 (NH 4)2 SO 4 NH 4 Cl NH 3 N 2 Li 3 N NH 3 Запишите уравнения реакций. Где возможно, рассмотрите с точки зрения ТЭД и ОВР. Приведите электронный баланс, полные и сокращенные ионные уравнения.
 Готовимся к экзамену • Решите задачи: NH 3 Уровень А: Какой объем аммиака можно получить при нагревании 7, 4 г. гидроксида кальция с хлоридом аммония ? . Уровень В: Аммиак объемом 4, 48 л (н. у) сожгли в равном объеме кислорода. Определите массу полученного азота. Уровень С: Аммиак объемом 2, 24 л (н. у) пропустили в раствор фосфорной кислоты массой 100 г с массовой долей кислоты 19, 8%. Определите состав соли и ее массовую долю в полученном растворе.
Готовимся к экзамену • Решите задачи: NH 3 Уровень А: Какой объем аммиака можно получить при нагревании 7, 4 г. гидроксида кальция с хлоридом аммония ? . Уровень В: Аммиак объемом 4, 48 л (н. у) сожгли в равном объеме кислорода. Определите массу полученного азота. Уровень С: Аммиак объемом 2, 24 л (н. у) пропустили в раствор фосфорной кислоты массой 100 г с массовой долей кислоты 19, 8%. Определите состав соли и ее массовую долю в полученном растворе.
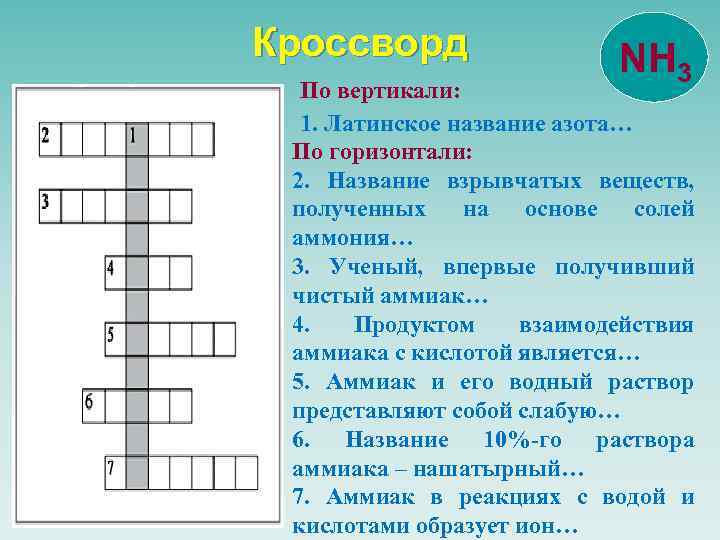 Кроссворд NH 3 По вертикали: 1. Латинское название азота… По горизонтали: 2. Название взрывчатых веществ, полученных на основе солей аммония… 3. Ученый, впервые получивший чистый аммиак… 4. Продуктом взаимодействия аммиака с кислотой является… 5. Аммиак и его водный раствор представляют собой слабую… 6. Название 10%-го раствора аммиака – нашатырный… 7. Аммиак в реакциях с водой и кислотами образует ион…
Кроссворд NH 3 По вертикали: 1. Латинское название азота… По горизонтали: 2. Название взрывчатых веществ, полученных на основе солей аммония… 3. Ученый, впервые получивший чистый аммиак… 4. Продуктом взаимодействия аммиака с кислотой является… 5. Аммиак и его водный раствор представляют собой слабую… 6. Название 10%-го раствора аммиака – нашатырный… 7. Аммиак в реакциях с водой и кислотами образует ион…


