NeuroAid_Ru_2013.pptx
- Количество слайдов: 66

Neuro. Ai. D™ - Введение 1

Био-фармацевтическая компания, специализирующаяся в области неврологии Moleac – это био-фармацевтическая компания, специализирующаяся в области неврологии, разрабатывающая и продвигающая инновационные лекарственные средства для пост-инсультной реабилитации § § § Идентификация продуктов Традиционной Китайской Медицины с целью заполнения пробела в Западном способе лечения Концентрация на финальной стадии клинических разработок, регистрации, продаже и маркетинге Широкая активность в терапевтической области, открытость на неохваченные потребности медицины Успешная разработка первого продукта – Neuro. Ai. D – для пост-инсультной реабилитации План по расширению до лечения нескольких недугов Ускоренна и безопасная модель разработки препаратов § § § Основа – комбинация натуральных продуктов с доказанной клинической эффективностью Разработка, производство и продажа в оптимизированной форме Проведение клинических исследований для доказательства безопасности и эффективности Установление молекулярных основ эффективности Идентификация и разработка наиболее простой формулы / активная молекула(ы) и новые генерированные IP Neuro. Ai. D и международное присутствие сегодня § 2 Зарегистрирован и реализовывается ~35 странах к середине 2013 года: Юго-Восточная Азия (8 стран), Ближний Восток и Африка (8 стран), Европа / СНГ (15 стран) 2
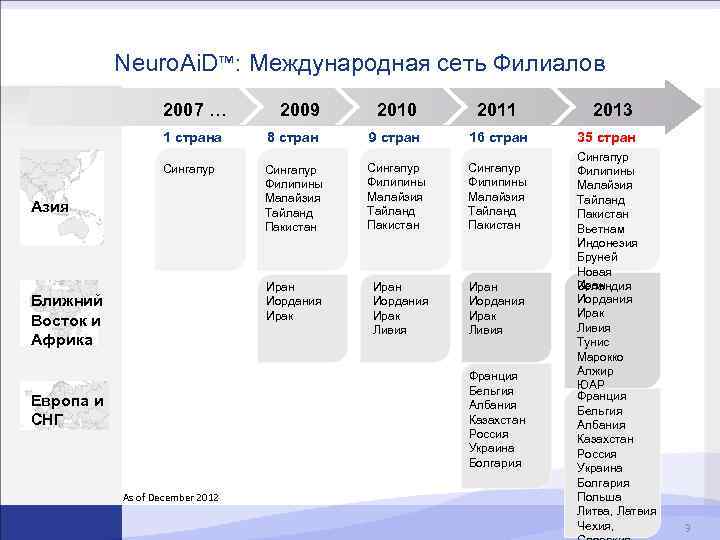
Neuro. Ai. D™: Международная сеть Филиалов 2007 … 2009 2010 2011 1 страна 8 стран 9 стран 16 стран Сингапур Филипины Малайзия Тайланд Пакистан Иран Иордания Ирак Ливия Азия Ближний Восток и Африка Франция Бельгия Албания Казахстан Россия Украина Болгария Европа и СНГ As of December 2012 2013 35 стран Сингапур Филипины Малайзия Тайланд Пакистан Вьетнам Индонезия Бруней Новая Иран Зеландия Иордания Ирак Ливия Тунис Марокко Алжир ЮАР Франция Бельгия Албания Казахстан Россия Украина Болгария Польша Литва, Латвия Чехия, 3

Ключевые лица DAVID PICARD CEO and Director DR ROBERT GAN Head of Medical Affairs Соучредитель Moleac, имеет 10 -летний опыт работы в The Boston Consulting Group ("BCG") в Европе и Азии, где занимал пост члена Worldwide Health Care Practice. Окончил два ведущих инженерных ВУЗ-а во Франции, Ecole Polytechnique и Ecole Nationale Supérieure des Mines de Paris, имеет диплом BA в области Права. Как профессор неврологии, действенный исследователь и клиницист, преподаватель в Азии и США, Др. Gan занимался лечением пациентов, перенесших инсульт, и проведением клинических исследований в течение первых 20 леи своей карьеры. До того, как присоединиться к компании Moleac, он был Regional Medical Manager по масштабному исследованию инсульта в Lunbeck. В Moleac Др. Gan с 2012 года. PROF MICHEL LAZDUNSKI DELPHINE ISAUTIER Vice President Research CFO Специалист с мировым именем в области фармакологии ионных туннелей, сделал значительный международный вклад в фундаментальные прикладные исследования в области фармакологии и патологии. Проф. Michel Lazdunski был удостоен CNRS Gold Medal, самой высокой французской награды в области науки и многих других престижных премий. Foong-Mei HUI Head of Regulatory Affairs Foong Mei Hui – специалист-фармацевт в области регистрации. Прежде чем попасть в компанию Moleac, Foong Mei приобрела 10 -летний опыт работы в частном фармацевтическом секторе и еще 10 лет в Singapore Drug Regulatory (HSA), где она занималась ключевыми вопросами, включая Deputy Head (Licensing) of Drug Registration Branch , Senior GMP auditor и Deputy Director (секция GDP). Delphine окончила ICN Nancy, а также имеет диплом DESCF в CNAM. Delphine 10 лет работала аудитором во Франции и Сингапуре в качестве менеджера компании Ernst and Young. Прежде чем попасть в Moleac в 2011 году, она занимала должность Senior Manager Finance and Human Capital в консалтинговой компании в Сингапуре. KASIA KAMINSKA EEC and CIS – International Sales Kasia окончила HEC, London School Economics, University of Silesia, University of Rome la Sapienza. После начала своей профессиональной карьеры в финансах, Kasia присоединилась к Moleac Singapore в 2009 году в качестве Product Manager and a Business Developer, вскоре заняла должность Head of Global Marketing. В 2012 г. она переехала в Польшу с целью открыть первый Moleac’s overseas Rep office, охватывающий деятельность в Восточной Европе и СНГ. CLAIRE YIM SIGOLENE COLAS DES FRANCS International sales Moleac Europe Sigolene окончила EDHEC и начала свою карьеру в Moleac Singapore в 2008, где создала ecommerce business сектор. В 2011 Sigolene присоединилась к Moleac Europe в Париже и занимается заграничными операциями с конца 2012 года. 4 Claire окончила EM Lyon и начала свою карьеру в Moleac в 2008 г. d качестве Business Development Executives. На сегодняшний день она занимается международными продажами компании Moleac на рынках Юго-Восточной Азии, Ближнего Востока и Северной Африки. 4

Основатели GERARD TARDY Non Executive Director Директор Merieux Development. Ранее занимал пост Investment Manager в Elf Technology. Основал и стал Членом Правления Citicorp Venture Capital, с того времени был ответственен за основания многих компаний. Gérard окончил HEC Paris, а также принимал участие в программе по бизнес менеджменту в Stanford University (США). BOUNMY RATTANAVAN Non Executive Director Соучредитель Tang Frères, ведущей азиатской компании по импорту/экспорту продуктов питания во Франции. Посредством работы в Tang Frères, он создал влиятельную сеть отношений в Европе и Китае, что позиционирует его в качестве желанного партнера для международных корпораций, стремящихся построить и расширить бизнес в Китае. NATACHA BEAUMONT PHILIPPE GUY Non-Executive Director Старший партнер в Boston Consulting Group, где курировал (1997 -2006) worldwide healthcare practice. Philippe несет с собой богатый опыт и перспективу в глобальной фармацевтической индустрии. Philippe является выпускником HEC. CHRISTOPHE POLINI Non-Executive Director Christophe Polinii – Company’s General Secretary of Tang Frères, где он работал больше декады. Christophe принес в Moleac обширный опыт структурных и менеджерских отношений партнерских отношений в Китае. Natacha представляет Hunza venture в Правлении Moleac. До начала работы в Hunza в 2004 г. , где она занимается курированием инвестиций головного офиса, Natacha занимала должность Senior Manager в Arthur Andersen и Ernst and Young в департаментах финансов. MARC VASSEUR Co-Founder († 1949 -2013) Соучредитель и бывший Генеральный Директор Genset. Управлял аквизицией Genset через Serono посредством тендерных процедур. Занимал должности Ген. Директора и Председателя Serono France, стал соучредителем и Ген. Директором Sobios, а также Президентом Theralpha во Франции. DAVID PICARD CEO and Director 5 Прежде чем стать соучредителем Moleac, 10 лет работал в The Boston Consulting Group ("BCG") в Европе и Азии, где был членом Worldwide Health Care Practice. Выпускник двух ведущих инженерных школ во Франции, Ecole Polytechnique и Ecole Nationale Supérieure des Mines de Paris, имеет диплом BA в области права. 5

Команда Медицинских Консультантов & Meдицинские Эксперты и Исследователи Ведущие научные эксперты-консультанты v. Prof Michel Lazdunski – Директор по Фармокологии, CNRS v. Dr Catherine Heurteux, Ведущий Исследователь в IPMC v. Dr Marc Cluzel, Основатель C&F Consulting и Старший Советник v. Dr Shreeram Agharkar, Вице-Президент Sanofi-Aventis Pharmaceuticals, Старший Советник Ведущие Медицинские Эксперты & Исследователи из академической среды v. Prof Christopher Chen – Национальный Университет в Сингапуре, Председатель Координационного Совета по Клиническим Исследованиям v. Prof Geoffrey Donnan - Национальный Институт Инсульта, Университет Мельбурна, Австралия v. Prof. Marie Germaine Bousser – Ведущий Эксперт по Неврологии в Lariboisiere Hospital, Париж, Франция, Консультант по Инсульту и Мигреням v. Professor Lawrence Wong, Глава Департамента Медицины и Терапии, Гонконг v. Dr Valery Feigin, Директор Национального Института Инсульта и Прикладных Нейронаук (NISAN), Новая Зеландия У нас имеется: Впечатляющая сеть сотрудничества Интересные темы исследований è Высокие стандарты исследований 6
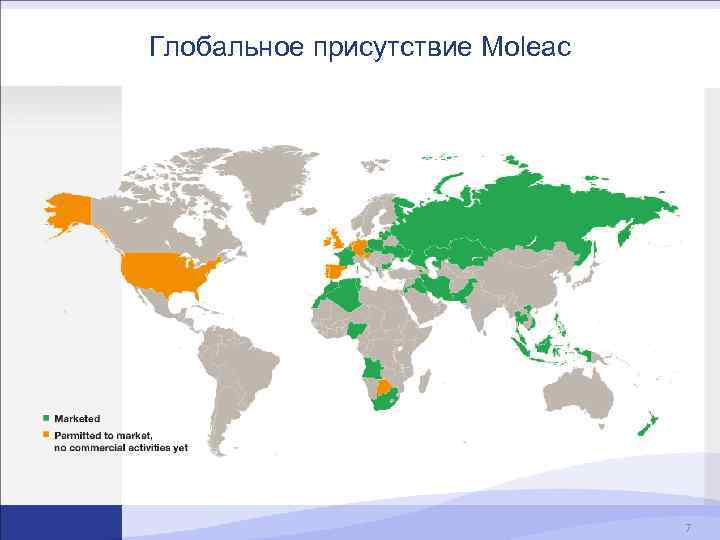
Глобальное присутствие Moleac 7

Награды / Призы “Moleac ввел на рынок продукт Neuro. Ai. D™, первый препарат, позволяющий более полно и быстро восстановиться пациентам после инсульта. . . ” “Компания Moleac удостоена the Frost & Sullivan Asia Pacific Excel-lence in Healthcare Award за успех в работе над препаратом для реабилитации после инсульта – Neuro. Ai. D™. . . ” 8

Лечение Neuro. Ai. D™ 9

Инсульт несет разрушительную мощь Ø Постоянно растущий рынок… § Ежегодно во всем мире: 20 миллионов инсультов, 15 миллионов выживших, 10 миллионов людей становятся инвалидами. § Несмотря на улучшающийся контроль факторов риска, заболеваемость инсультом растет из-за старения населения. Ø Который адресован… § Инсульт является одной из основных причин инвалидности: No. 1 причиной физической инвалидности, No. 2 причиной психических недугов, основной причиной депрессии. § Некоторые эффективные, приемлемые, специфические способы лечения ишемического инсульта: rt-PA - тромболизис (жесткий отбор пациентов), Гемикраниэктомия (отбор тяжелых пациентов), Антитромбоцитарные, Отделения инсульта, Реабилитация § Пациенты ищут альтернативную терапию для инсульта в Азии из-за неудовлетворенности результатами восстановления после него. Pandian et al; Int J Stroke 2011 (1) Источник: Американская Ассоциация по борьбе с Инсультом 10

Пробел в лечении после инсульта • Многие нейропротекторы не смогли продемонстрировать свой потенциал в ходе клинических испытаний. • Нейровосстанавливающие свойства также довольно ограничены. • Большинство историй болезни и баз данных описывают физическую реабилитацию после инсульта, лечение определенных симптомов или синдромов после инсульта, или же снижение риска его повторного появления – около 1/3 пациентов с острым инсультом оставались в средней или тяжелой степени не- функциональности на момент выписки 11

Пробел в лечении инсульта “… В случае с таким недугом, как церебральный инфаркт, последствия которого остаются настолько часто и настолько серьезны, несмотря на последние достижения в области профилактики и лечения на острой стадии болезни, позвольте рассмотреть препараты из натуральных ингредиентов с разумной долей открытости и научного скептицизма!” Bousser M-G; Cerebrovascular Diseases 2013 12

Neuro. Ai. D II • Форма капсул • Натуральные экстракты • 9 растительных компонентов: Radix astragali, Radix salviae miltiorrhizae, Radix paeoniae rubra, Rhizoma chuanxiong, Radix angelicae sinensis, Carthamus tinctorius, Prunus persica, Radix polygalae, and Rhizoma acori tatarinowii 13
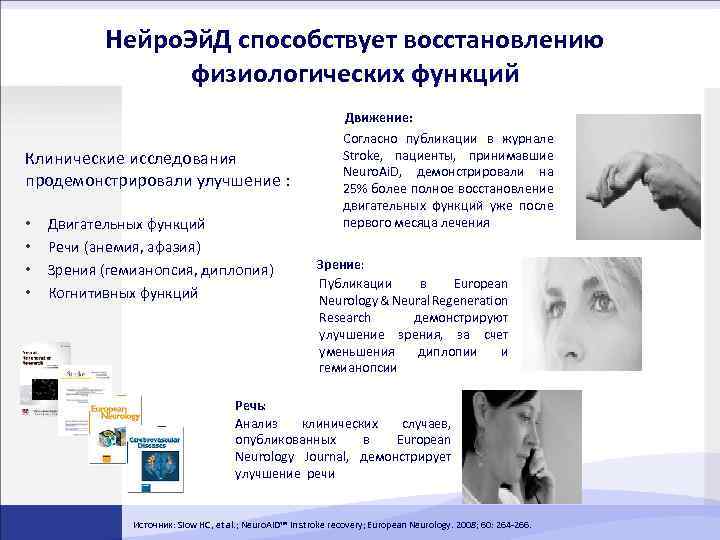
Нейро. Эй. Д способствует восстановлению физиологических функций Клинические исследования продемонстрировали улучшение : • • Двигательных функций Речи (анемия, афазия) Зрения (гемианопсия, диплопия) Когнитивных функций Движение: Согласно публикации в журнале Stroke, пациенты, принимавшие Neuro. Ai. D, демонстрировали на 25% более полное восстановление двигательных функций уже после первого месяца лечения Зрение: Публикации в European Neurology & Neural Regeneration Research демонстрируют улучшение зрения, за счет уменьшения диплопии и гемианопсии Речь: Анализ клинических случаев, опубликованных в European Neurology Journal, демонстрирует улучшение речи Источник: Siow HC, et al. ; Neuro. Ai. D™ in stroke recovery; European Neurology. 2008; 60: 264 -266.

Клинические и Научные Публикации 2009 -2013 Neuro. Ai. D хорошо исследован в хронической стадии инсульта • • British Journal of Medicine and Medical Research in 2013 - Efficacy and Tolerability of Neuroaid in patient with mild to moderate Alzheimer Disease • Neuropharmacology in 2012 – Neuroaid as a Ionic channel opener properties • Stroke research and treatment in 2011 –Efficacy and Safety data • Neuropharmacology in 2011 – Pharmacology data on global ischemia and cognition • European Journal of Internal Medicine in 2011 – Efficacy and Safety data • Neuronal Regeneration Research in 2011 – Efficacy on recovery of visual function • Neuropharmacology in 2010 - Pharmacology data on neuroprotective and neurorestorative properties in stroke • Cerebrovascular Diseases in 2010 - Safety data in acute stage • Cerebrovascular Diseases in 2009 - TIERS Pilot study • Stroke Journal in 2009 - Efficacy trial • European Neurology in 2008 - Case report • Cerebrovascular Diseases in 2008 - Safety trial • 15 Cerebrovascular Diseases in 2013 – Review of Neuroaid properties at chronic stage of Stroke (supplement issue with 6 papers) The International Journal of Stroke in 2009 - The CHIMES protocol 15

Фармакологические данные Neuro. Ai. D™ 16

Фармакологические Данные Ø Научное лидерство Prof. Michel Lazdunski, основатель Института Молекулярной и Клеточной Фармакологии в CNRS (национальный институт научных исследований) во Франции, специалист с мировым именем в области фармакологии. Ø Данные § § § Продемонстрировал доказательства механизма действия. Мощная поддержка для нашего маркетинга. Предоставил достоверные научные доказательства эффектов, полученных в ходе клинических исследований. Циклы экспериментов in vivo и in vitro с целью открыть свойства и механизм действия Neuro. Ai. D • Грызуны • Культуры нейронных связей • Человеческие стволовые клетки 17

Нейропротекция и Нейропролиферация 18
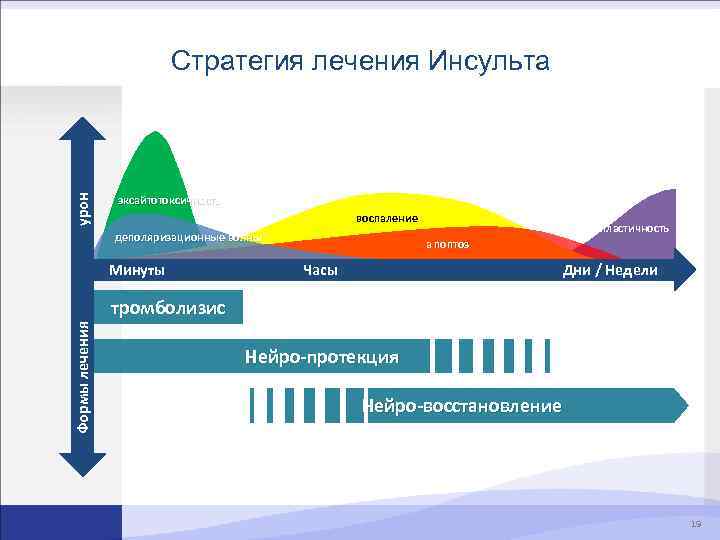
урон Стратегия лечения Инсульта эксайтотоксичность воспаление деполяризационные волны Минуты пластичность a поптоз Часы Дни / Недели Формы лечения тромболизис Нейро-протекция Нейро-восстановление 19

Neuro. Ai. D™ побуждает экспрессию вещества BDNF Уровень BDNF увеличился более чем в два раза после 6 недель лечения После 6 недель уровень BDNF был в 2. 5 раза выше в случае с лечением Neuro. Ai. D™ по сравнению с контрольной группой (p<0. 01). §BDNF регулирует выживаемость нейронов и оберегает их от глутамат-индуцированного повреждения. §BDNF вызывает пролиферацию и деление новых нейронов. BDNF (Brain Derived Neurotrophic Factor) together with other growth factors have been shown to support neuronal proliferation, differentiation and connectivity in rodent model (p<0. 01). §BDNF является посредником в выживаемости нейронов, нейропролиферации, пластичности мозга и нейрогенезисе. Нервные клетки нуждаются в BDNF для регенерации. Побуждая секрецию BDNF, Neuro. Ai. D™ воспроизводит новые нейронные связи, а также цепочки аксонов и дендртов. Results published in Neuropharmacology, 2010 20

Neuro. Ai. D™ побуждает пролиферацию нейронов / клеток Ø Эксперименты на человеческих стволовых клетках. § x 3 раза увеличивает концентрацию стволовых клеток (пролиферация). После 2 дней лечения, слабо сконцентрированные культуры под воздействием Neuro. Ai. D™ показали 3 кратное увеличение радиального скопления Нестинпозитивных клеток-предшественников (p<0. 01). Нестин – это промежуточное протеиновое волокно, участвующее в процессе роста аксонов. Ø Эксперименты на животных § в 2. 1 раза увеличилось кол-во зрелых (функциональных) нейронов. Results published in Neuropharmacology, 2010 21
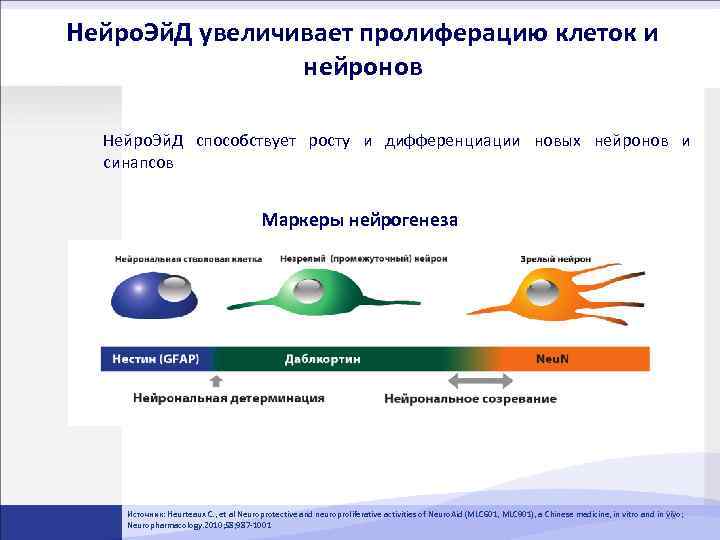
Нейро. Эй. Д увеличивает пролиферацию клеток и нейронов Нейро. Эй. Д способствует росту и дифференциации новых нейронов и синапсов Маркеры нейрогенеза Источник: Heurteaux C. , et al Neuroprotective and neuroproliferative activities of Neuro. Aid (MLC 601, MLC 901), a Chinese medicine, in vitro and in 22 vivo; Neuropharmacology. 2010; 58; 987 -1001

Нейро. Эйд стимулирует нейрогенез и синаптическую пластичность Культура клеток-нейронов под воздействием Нейро. Эй. Д изучалась методом эпифлуоресценции. Результаты показали значительное увеличение экспрессии DCX, GAP 43 и синаптотагмина. • DCX ассоциированный с микротрубочками белок, выделение которого специфично для клетокпредшественниц нейронов в зонах продолжающегося нейрогенеза головного мозга взрослого человека • GAP 43 белок роста, определяющий рост аксонов, направление конуса роста и синаптическую пластичность • Синаптотагмин – белок синаптических пузырьков, участвующий в синаптогенезе и функции синапсов Источник: Heurteaux C. , et al Neuroprotective and neuroproliferative activities of Neuro. Aid (MLC 601, MLC 901), a Chinese medicine, in vitro and in 23 vivo; Neuropharmacology. 2010; 58; 987 -1001
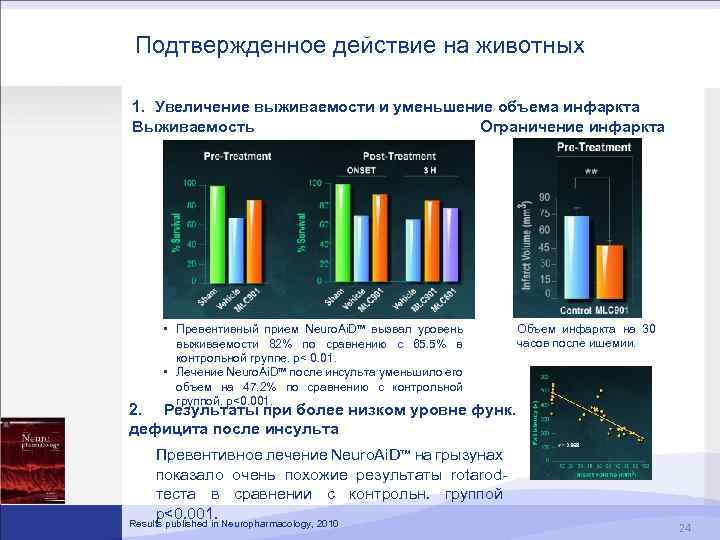
Подтвержденное действие на животных 1. Увеличение выживаемости и уменьшение объема инфаркта Выживаемость Ограничение инфаркта • Превентивный прием Neuro. Ai. D™ вызвал уровень выживаемости 82% по сравнению с 65. 5% в контрольной группе. p< 0. 01. • Лечение Neuro. Ai. D™ после инсульта уменьшило его объем на 47. 2% по сравнению с контрольной группой. p<0. 001. Объем инфаркта на 30 часов после ишемии. 2. Результаты при более низком уровне функ. дефицита после инсульта Превентивное лечение Neuro. Ai. D™ на грызунах показало очень похожие результаты rotarodтеста в сравнении с контрольн. группой p<0. 001. Results published in Neuropharmacology, 2010 24

Результаты тестов на животных 1. Защита и Нейрогенез клеток гиппокампа после Глобальной Ишемии Bax-окрашивание Уменьшение инфаркта 2. Увеличение когнитивной и двигательной активности после глобальной ишемии Results published in Neuropharmacology, 2011 25

Урон Общие Фармакологические Эффекты при Инсульте эксайтотоксичность воспаление Деполяризационные волны апоптоз Минуты Тромболизис Часы пластичность Дни / Недели Формы лечения Нейро-протекция • Снижает объем инфаркта NEURO-REPAIR • Увеличивает выделение BDNF • Повышает жизнеспособность клеток • Вызывает нейрогенез • Защищает от Глутамат-индуцированной травмы • Увеличивает рост аксонов • Снижает оксидатив- • Увеличивает синаптогенез ный стресс • Активирует каналы Katp 26 26

Клинические Данные 27

Neuro. Ai. D при неострой стадии Инсульта 28

Результат Эффективности – Функциональное Восстановление Достигнутое повышение функциональной независимости x 2. 4 § 2. 4 раза повышаются шансы достижения функциональной независимости после 1 месяца приема препарата. Пациенты, которые обрели функциональную независимость благодаря Neuro. Ai. D (из общего кол -ва 1000 человек) • • Лечение группы из 605 пациентов от 2 недель до 6 месяцев после ишемического инсульта. Независимость определяется как способность позаботиться о себе, а также внятно разговаривать. Результаты опубликованы в журнале Stroke, март 2009 29
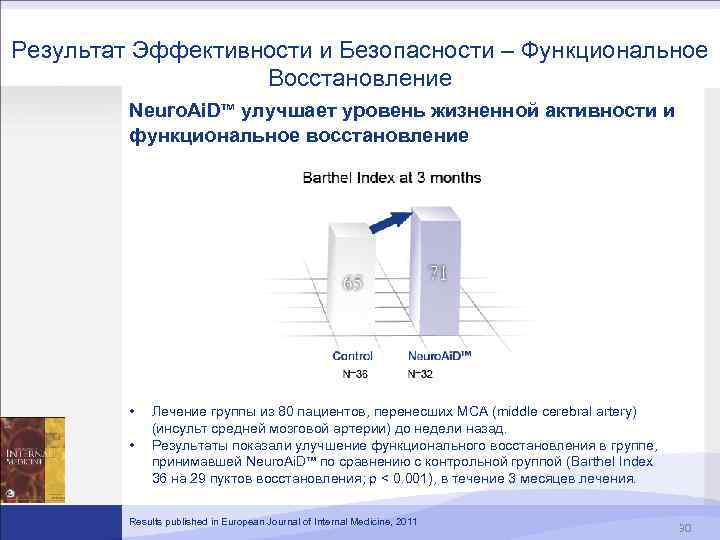
Результат Эффективности и Безопасности – Функциональное Восстановление Neuro. Ai. D™ улучшает уровень жизненной активности и функциональное восстановление • • Лечение группы из 80 пациентов, перенесших MCA (middle cerebral artery) (инсульт средней мозговой артерии) до недели назад. Результаты показали улучшение функционального восстановления в группе, принимавшей Neuro. Ai. D™ по сравнению с контрольной группой (Barthel Index 36 на 29 пуктов восстановления; p < 0. 001), в течение 3 месяцев лечения. Results published in European Journal of Internal Medicine, 2011 30

Результат Эффективности – Восстановление Моторики Восстановление дефицита моторики + 25% § На 25% более обширное восстановление моторики после 1 месяца приема препарата. Upper Proximal Limb (p = 0. 006) • • Lower Distal Limb (p = 0. 02) Лечение группы из 605 пациентов от 2 недель до 6 месяцев после ишемического инсульта. Восстановление аспектов моторных функций измерялось в шкале 0 -5 до и после лечения. Результаты опубликованы в журнале Stroke, март 2009 31
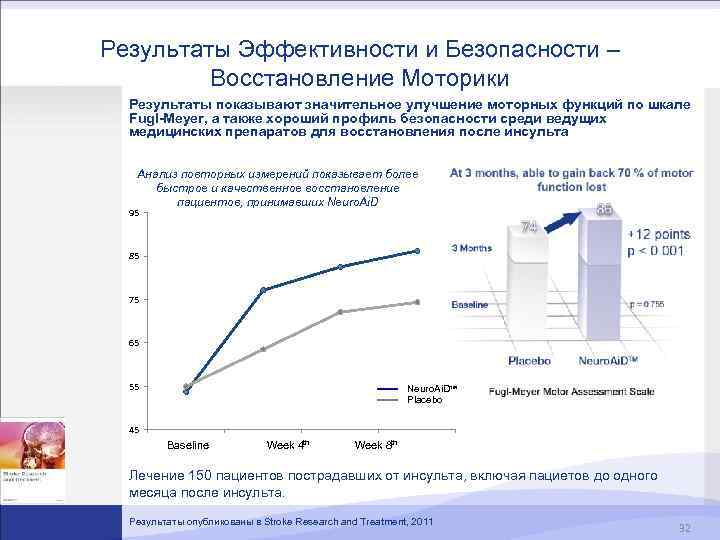
Результаты Эффективности и Безопасности – Восстановление Моторики Результаты показывают значительное улучшение моторных функций по шкале Fugl-Meyer, а также хороший профиль безопасности среди ведущих медицинских препаратов для восстановления после инсульта Анализ повторных измерений показывает более быстрое и качественное восстановление пациентов, принимавших Neuro. Ai. D 95 85 75 65 55 Neuro. Ai. D™ Placebo 45 Baseline Semaine 4 Semaine 8 Semaine Baseline Week 4 th Week 8 th 12 Лечение 150 пациентов пострадавших от инсульта, включая пациетов до одного месяца после инсульта. Результаты опубликованы в Stroke Research and Treatment, 2011 32

33

Систематические Отчеты показывают, что Neuro. Ai. D более чем в два раза улучшает результаты восстановления после инсульта Siddiqui FJ et al, Cerebrovascular Diseases 2013 34

Neuro. Ai. D в острой стадии Инсульта 35

Stroke 2013 Aug; 44(8): 2093 -2100 36

Двойное слепое, плацебо-контролируемое рандомизированное исследование: CHIMES 37
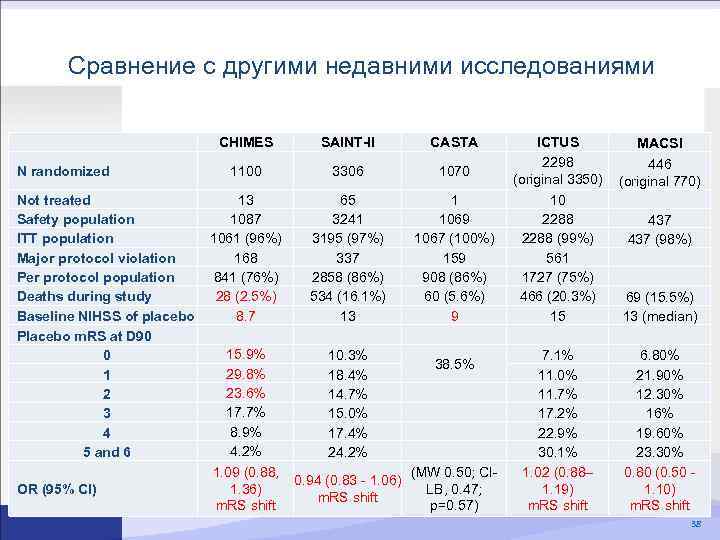
Сравнение с другими недавними исследованиями CHIMES N randomized Not treated Safety population ITT population Major protocol violation Per protocol population Deaths during study Baseline NIHSS of placebo Placebo m. RS at D 90 0 1 2 3 4 5 and 6 OR (95% CI) SAINT-II CASTA 1100 3306 1070 13 65 1 1087 3241 1069 1061 (96%) 3195 (97%) 1067 (100%) 168 337 159 841 (76%) 2858 (86%) 908 (86%) 28 (2. 5%) 534 (16. 1%) 60 (5. 6%) 8. 7 13 9 15. 9% 10. 3% 38. 5% 29. 8% 18. 4% 23. 6% 14. 7% 17. 7% 15. 0% 8. 9% 17. 4% 4. 2% 24. 2% 1. 09 (0. 88, (MW 0. 50; CI 0. 94 (0. 83 - 1. 06) 1. 36) LB, 0. 47; m. RS shift p=0. 57) ICTUS 2298 (original 3350) 10 2288 (99%) 561 1727 (75%) 466 (20. 3%) 15 7. 1% 11. 0% 11. 7% 17. 2% 22. 9% 30. 1% 1. 02 (0. 88– 1. 19) m. RS shift MACSI 446 (original 770) 437 (98%) 69 (15. 5%) 13 (median) 6. 80% 21. 90% 12. 30% 16% 19. 60% 23. 30% 0. 80 (0. 50 - 1. 10) m. RS shift 38
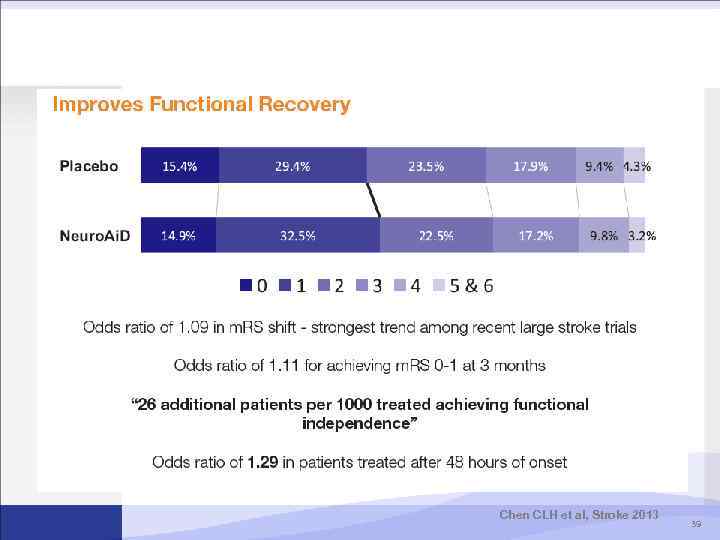
Chen CLH et al, Stroke 2013 39
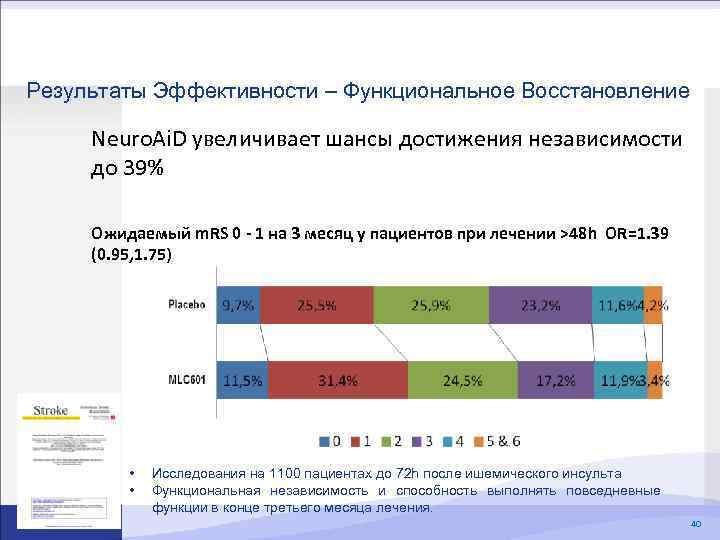
Результаты Эффективности – Функциональное Восстановление Neuro. Ai. D увеличивает шансы достижения независимости до 39% Ожидаемый m. RS 0 - 1 на 3 месяц у пациентов при лечении >48 h OR=1. 39 (0. 95, 1. 75) • • Исследования на 1100 пациентах до 72 h после ишемического инсульта Функциональная независимость и способность выполнять повседневные функции в конце третьего месяца лечения. 40
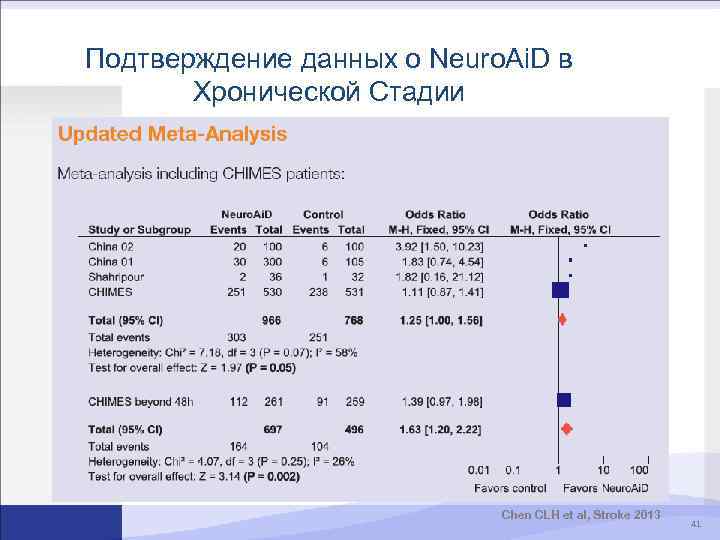
Подтверждение данных о Neuro. Ai. D в Хронической Стадии Chen CLH et al, Stroke 2013 41
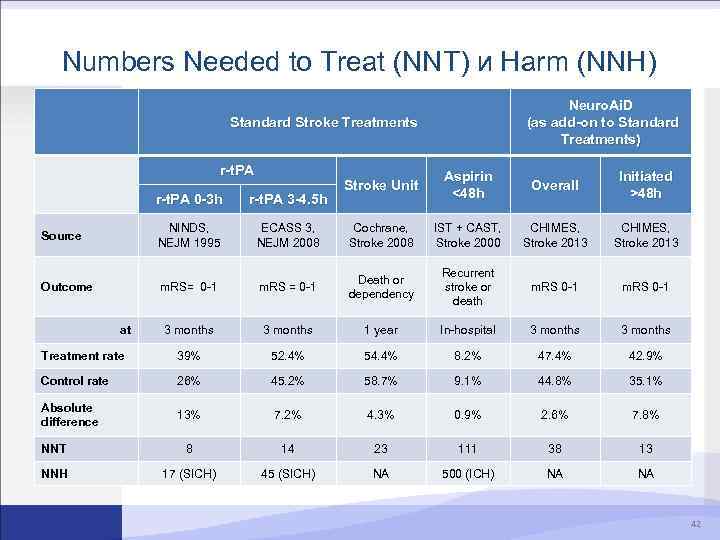
Numbers Needed to Treat (NNT) и Harm (NNH) Neuro. Ai. D (as add-on to Standard Treatments) Standard Stroke Treatments r-t. PA Stroke Unit Aspirin <48 h Overall Initiated >48 h r-t. PA 0 -3 h r-t. PA 3 -4. 5 h Source NINDS, NEJM 1995 ECASS 3, NEJM 2008 Cochrane, Stroke 2008 IST + CAST, Stroke 2000 CHIMES, Stroke 2013 Outcome m. RS= 0 -1 m. RS = 0 -1 Death or dependency Recurrent stroke or death m. RS 0 -1 3 months 1 year In-hospital 3 months Treatment rate 39% 52. 4% 54. 4% 8. 2% 47. 4% 42. 9% Control rate 26% 45. 2% 58. 7% 9. 1% 44. 8% 35. 1% Absolute difference 13% 7. 2% 4. 3% 0. 9% 2. 6% 7. 8% NNT 8 14 23 111 38 13 NNH 17 (SICH) 45 (SICH) NA 500 (ICH) NA NA at 42

Другие показатели 43

44
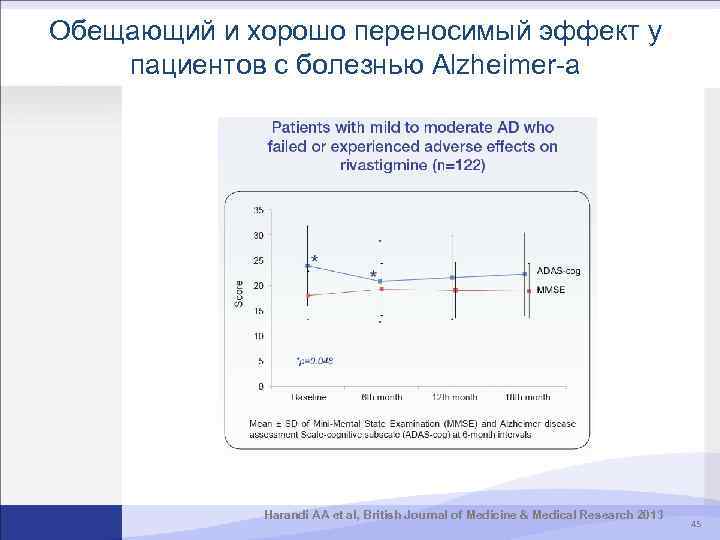
Обещающий и хорошо переносимый эффект у пациентов с болезнью Alzheimer-а Harandi AA et al, British Journal of Medicine & Medical Research 2013 45

Neuro. Ai. D™ – другие факты Ø Фармакологические исследования доказали положительный нейропластический и нейропротекторный эффект Neuro. Ai. D™. Следовательно, нейрохирургические патологии и дегенеративные болезни появляются как расширение показаний к Neuro. Ai. D™. Ø Множество исследований показало возможную связь между веществом BDNF и такими заболеваниями, как долезнь Alzheimer-а, долезнь Huntington-а, синдром Rett-а, деменция, травмы спинного мозга. Ø Геморрагические инсульты: большое кол-во отчетов отмечает положительное влияние препарата Neuro. Ai. D™ на пациентов после геморрагического инсульта. Ø Черепно-мозговые травмы (ЧМТ): отчеты показывают, что Neuro. Ai. D™ помагает пациентам с ЧМТ. Ø Дегенеративные заболевания: более поздние исследования подтверждают положительную роль Neuro. Ai. D™ в профилактике инсульта, а также в нейрогенеративных заболеваниях, что еще будет исследовано шире. Ø Сосудистые когнитивные нарушения: исследования планируются и будут проведены в ближайшем будущем. 46

Прекрасный Профиль Безопасности 47

Neuro. Ai. D™ - хорошо исследованный профиль безопасности Ø Пациенты в острой стадии (до 48 часов после инсульта) § Используя биохемические, гематологические и электрокардиологические тесты, сингапурские исследователи CHIMES доказали, что Neuro. Ai. D™ также безопасен, как плацебо для пациентов, перенесших инсульт, в течение 3 месячного лечения. § Анализ ряда физических параметров показывает и доказывает, что Neuro. Ai. D™ безопасен в острой фазе инсульта. Stroke (2013)&Cerebrovascular Diseases (2010) Ø Здоровые объекты и Пациенты до 7 дней после инсульта § Neuro. Ai. D™ не модифицировал гемостазу, гемоталогию и биохимические показатели у здоровых объектов и пациентов после инсульта (до 7 дней после инсульта). § Neuro. Ai. D™ доказал свою безопасность в качестве лекарства для постоянного приема пациентами, перенесшими инсульт. Не взаимодействует с аспирином. Cerebrovascular Diseases (2008) Ø Пациенты в хронической стадии (от 6 месяцев после инсульта и выше) § Кровь церкулирует правильно, нормальные функции почек (анализы крови и мочи), функции печени также были измерены и никаких отклонений не было выявлено в клиническом исследовании на 605 пациентах, переживших Stroke (2009) инсульт от 2 недель до 6 месяцев назад. 48
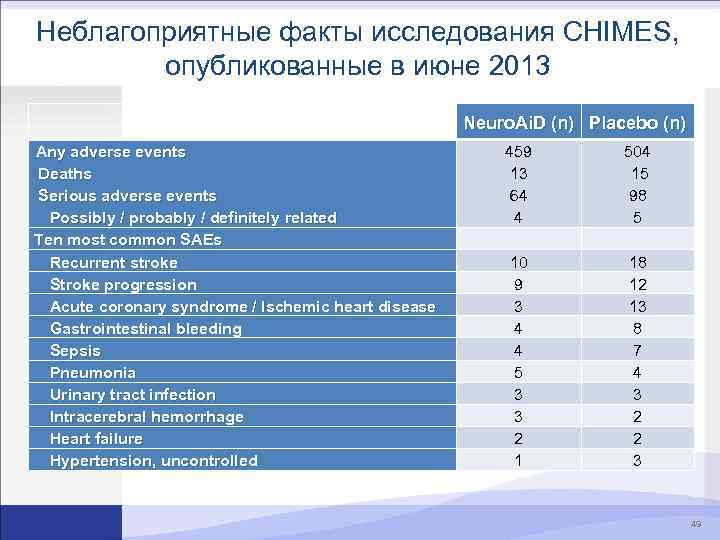
Неблагоприятные факты исследования CHIMES, опубликованные в июне 2013 Any adverse events Deaths Serious adverse events Possibly / probably / definitely related Ten most common SAEs Recurrent stroke Stroke progression Acute coronary syndrome / Ischemic heart disease Gastrointestinal bleeding Sepsis Pneumonia Urinary tract infection Intracerebral hemorrhage Heart failure Hypertension, uncontrolled Neuro. Ai. D (n) Placebo (n) 459 13 64 4 10 9 3 4 4 5 3 3 2 1 504 15 98 5 18 12 13 8 7 4 3 2 2 3 49

Итоги • Neuro. Ai. D обладает нейро-побуждающими и нейрозащитными свойствами • Neuro. Ai. D имеет огромную клиническую базу восстановления после ишемического инсульта • Лабораторные и клинические данные подходят для когнитивных нарушений/деменции • Neuro. Ai. D обладает превосходным профилем безопасности • Длительные исследования над ишемическим инсультом с далеко идущими результатами (CHIMES-E), подгруппа (CHIMES-I), сосудистые когнитивные нарушения (NEURITES) и черепно-мозговые травмы (BRAINS) 50

База данных Исследований 51
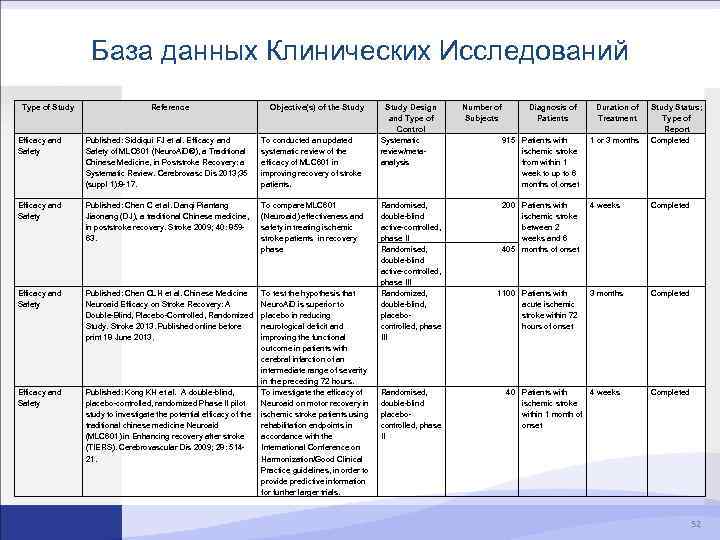
База данных Клинических Исследований Type of Study Reference Objective(s) of the Study Efficacy and Safety Published: Siddiqui FJ et al. Efficacy and Safety of MLC 601 (Neuro. Ai. D®), a Traditional Chinese Medicine, in Poststroke Recovery: a Systematic Review. Cerebrovasc Dis 2013; 35 (suppl 1): 8 -17. To conducted an updated systematic review of the efficacy of MLC 601 in improving recovery of stroke patients. Efficacy and Safety Published: Chen C et al. Danqi Piantang Jiaonang (DJ), a traditional Chinese medicine, in poststroke recovery. Stroke 2009; 40: 85963. To compare MLC 601 (Neuroaid) effectiveness and safety in treating ischemic stroke patients in recovery phase Efficacy and Safety Published: Chen CLH et al. Chinese Medicine Neuroaid Efficacy on Stroke Recovery: A Double-Blind, Placebo-Controlled, Randomized Study. Stroke 2013. Published online before print 18 June 2013. To test the hypothesis that Neuro. Ai. D is superior to placebo in reducing neurological deficit and improving the functional outcome in patients with cerebral infarction of an intermediate range of severity in the preceding 72 hours. Published: Kong KH et al. A double-blind, To investigate the efficacy of placebo-controlled, randomized Phase II pilot Neuroaid on motor recovery in study to investigate the potential efficacy of the ischemic stroke patients using traditional chinese medicine Neuroaid rehabilitation endpoints in (MLC 601) in Enhancing recovery after stroke accordance with the (TIERS). Cerebrovascular Dis 2009; 28: 514 International Conference on 21. Harmonization/Good Clinical Practice guidelines, in order to provide predictive information for further larger trials. Study Design and Type of Control Systematic review/metaanalysis Randomised, double-blind active-controlled, phase III Randomized, double-blind, placebocontrolled, phase III Randomised, double-blind placebocontrolled, phase II Number of Subjects Diagnosis of Patients Duration of Treatment 915 Patients with ischemic stroke from within 1 week to up to 6 months of onset 1 or 3 months Study Status; Type of Report Completed 200 Patients with ischemic stroke between 2 weeks and 6 405 months of onset 4 weeks Completed 1100 Patients with acute ischemic stroke within 72 hours of onset 3 months Completed 40 Patients with 4 weeks ischemic stroke within 1 month of onset Completed 52
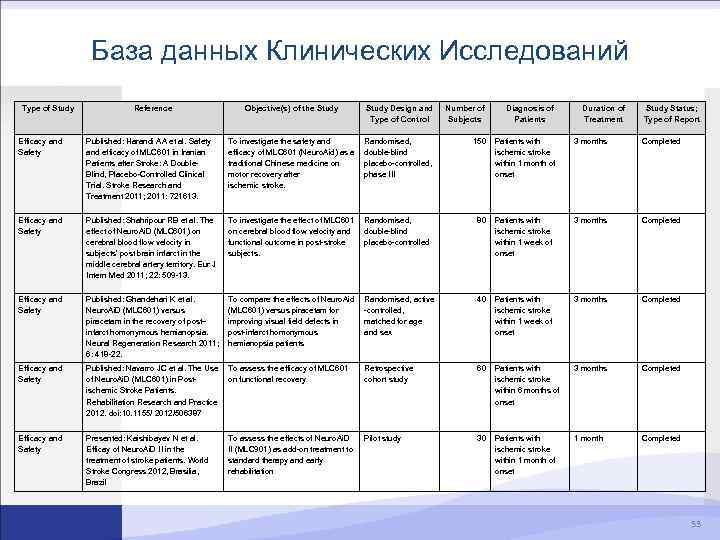
База данных Клинических Исследований Type of Study Reference Objective(s) of the Study Design and Type of Control Number of Subjects Diagnosis of Patients Duration of Treatment Study Status; Type of Report Randomised, double-blind placebo-controlled, phase III 150 Patients with ischemic stroke within 1 month of onset 3 months Completed Efficacy and Safety Published: Harandi AA et al. Safety and efficacy of MLC 601 in Iranian Patients after Stroke: A Double- Blind, Placebo-Controlled Clinical Trial. Stroke Research and Treatment 2011; 2011: 721613. To investigate the safety and efficacy of MLC 601 (Neuro. Aid) as a traditional Chinese medicine on motor recovery after ischemic stroke. Efficacy and Safety Published: Shahripour RB et al. The effect of Neuro. Ai. D (MLC 601) on cerebral blood flow velocity in subjects’ post brain infarct in the middle cerebral artery territory. Eur J Intern Med 2011; 22: 509 -13. To investigate the effect of MLC 601 Randomised, on cerebral blood flow velocity and double-blind functional outcome in post-stroke placebo-controlled subjects. 80 Patients with ischemic stroke within 1 week of onset 3 months Completed Efficacy and Safety Published: Ghandehari K et al. Neuro. Ai. D (MLC 601) versus piracetam in the recovery of post– infarct homonymous hemianopsia. Neural Regeneration Research 2011; 6: 418 -22. To compare the effects of Neuro. Aid (MLC 601) versus piracetam for improving visual field defects in post-infarct homonymous hemianopsia patients Randomised, active -controlled, matched for age and sex 40 Patients with ischemic stroke within 1 week of onset 3 months Completed Efficacy and Safety Published: Navarro JC et al. The Use To assess the efficacy of MLC 601 of Neuro. Ai. D (MLC 601) in Poston functional recovery ischemic Stroke Patients. Rehabilitation Research and Practice 2012. doi: 10. 1155/ 2012/506387 Retrospective cohort study 60 Patients with ischemic stroke within 6 months of onset 3 months Completed Efficacy and Safety Presented: Kaishibayev N et al. Efficay of Neuro. Ai. D II in the treatment of stroke patients. World Stroke Congress 2012, Brasilia, Brazil Pilot study 30 Patients with ischemic stroke within 1 month of onset 1 month Completed To assess the effects of Neuro. Ai. D II (MLC 901) as add-on treatment to standard therapy and early rehabilitation 53
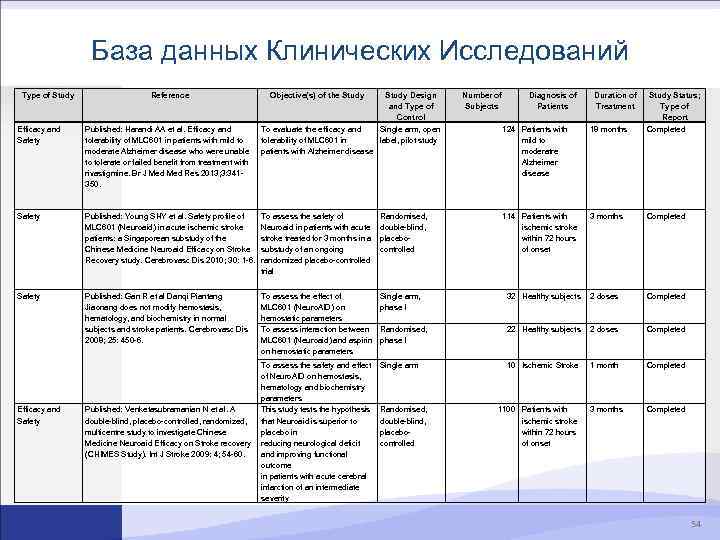
База данных Клинических Исследований Type of Study Reference Objective(s) of the Study Efficacy and Safety Published: Harandi AA et al. Efficacy and tolerability of MLC 601 in patients with mild to moderate Alzheimer disease who were unable to tolerate or failed benefit from treatment with rivastigmine. Br J Med Res 2013; 3: 341350. To evaluate the efficacy and tolerability of MLC 601 in patients with Alzheimer disease Safety Published: Young SHY et al. Safety profile of MLC 601 (Neuroaid) in acute ischemic stroke patients: a Singaporean substudy of the Chinese Medicine Neuroaid Efficacy on Stroke Recovery study. Cerebrovasc Dis 2010; 30: 1 -6. To assess the safety of Neuroaid in patients with acute stroke treated for 3 months in a substudy of an ongoing randomized placebo-controlled trial Randomised, double-blind, placebocontrolled Safety Published: Gan R et al Danqi Piantang Jiaonang does not modify hemostasis, hematology, and biochemistry in normal subjects and stroke patients. Cerebrovasc Dis 2008; 25: 450 -6. To assess the effect of MLC 601 (Neuro. AID) on hemostatic parameters To assess interaction between MLC 601 (Neuroaid) and aspirin on hemostatic parameters Single arm, phase I Efficacy and Safety To assess the safety and effect of Neuro. AID on hemostasis, hematology and biochemistry parameters Published: Venketasubramanian N et al. A This study tests the hypothesis double-blind, placebo-controlled, randomized, that Neuroaid is superior to multicentre study to investigate Chinese placebo in Medicine Neuroaid Efficacy on Stroke recovery reducing neurological deficit (CHIMES Study). Int J Stroke 2009: 4; 54 -60. and improving functional outcome in patients with acute cerebral infarction of an intermediate severity Study Design and Type of Control Single arm, open label, pilot study 124 Patients with mild to moderatre Alzheimer disease 18 months Study Status; Type of Report Completed 114 Patients with ischemic stroke within 72 hours of onset 3 months Completed 32 Healthy subjects 2 doses Completed Randomised, phase I 22 Healthy subjects 2 doses Completed Single arm 10 Ischemic Stroke 1 month Completed 3 months Completed Randomised, double-blind, placebocontrolled Number of Subjects Diagnosis of Patients 1100 Patients with ischemic stroke within 72 hours of onset Duration of Treatment 54
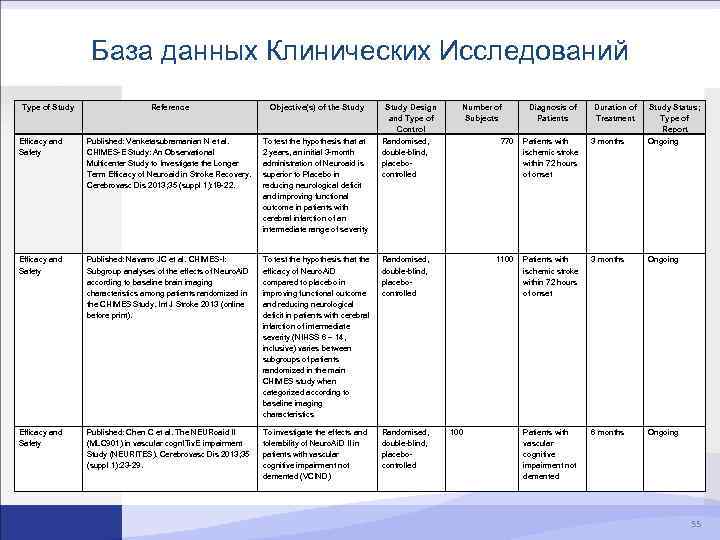
База данных Клинических Исследований Type of Study Reference Objective(s) of the Study Design and Type of Control Randomised, double-blind, placebocontrolled Efficacy and Safety Published: Venketasubramanian N et al. CHIMES-E Study: An Observational Multicenter Study to Investigate the Longer Term Efficacy of Neuroaid in Stroke Recovery. Cerebrovasc Dis 2013; 35 (suppl 1): 18 -22. To test the hypothesis that at 2 years, an initial 3 -month administration of Neuroaid is superior to Placebo in reducing neurological deficit and improving functional outcome in patients with cerebral infarction of an intermediate range of severity Efficacy and Safety Published: Navarro JC et al. CHIMES-I: Subgroup analyses of the effects of Neuro. Ai. D according to baseline brain imaging characteristics among patients randomized in the CHIMES Study. Int J Stroke 2013 (online before print). To test the hypothesis that the efficacy of Neuro. Ai. D compared to placebo in improving functional outcome and reducing neurological deficit in patients with cerebral infarction of intermediate severity (NIHSS 6 – 14, inclusive) varies between subgroups of patients randomized in the main CHIMES study when categorized according to baseline imaging characteristics Randomised, double-blind, placebocontrolled Efficacy and Safety Published: Chen C et al. The NEURoaid II (MLC 901) in vascular cogn. ITiv. E impairment Study (NEURITES). Cerebrovasc Dis 2013; 35 (suppl 1): 23 -29. To investigate the effects and tolerability of Neuro. Ai. D II in patients with vascular cognitive impairment not demented (VCIND) Randomised, double-blind, placebocontrolled Number of Subjects 770 Patients with ischemic stroke within 72 hours of onset 3 months Study Status; Type of Report Ongoing 1100 Diagnosis of Patients Duration of Treatment Patients with ischemic stroke within 72 hours of onset 3 months Ongoing Patients with vascular cognitive impairment not demented 6 months Ongoing 55
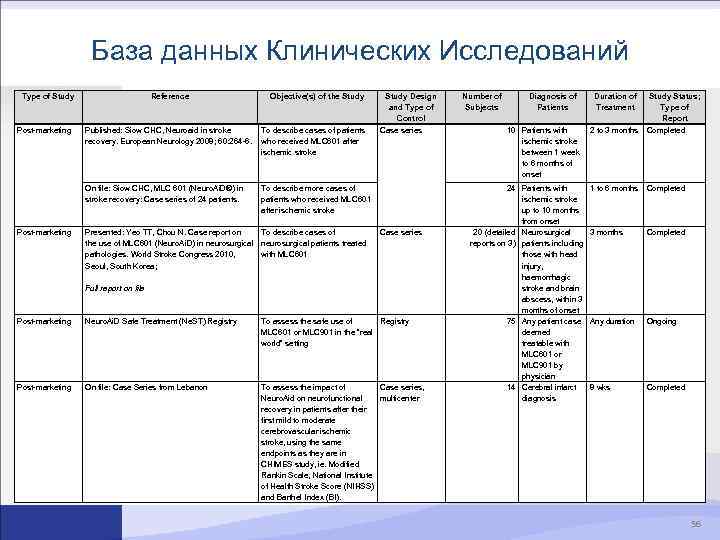
База данных Клинических Исследований Type of Study Post-marketing Reference Objective(s) of the Study Published: Siow CHC, Neuroaid in stroke recovery. European Neurology 2008; 60: 264 -6. To describe cases of patients who received MLC 601 after ischemic stroke On file: Siow CHC, MLC 601 (Neuro. Ai. D®) in stroke recovery: Case series of 24 patients. Study Design and Type of Control Case series To describe more cases of patients who received MLC 601 after ischemic stroke Post-marketing Presented: Yeo TT, Chou N. Case report on To describe cases of the use of MLC 601 (Neuro. Ai. D) in neurosurgical patients treated pathologies. World Stroke Congress 2010, with MLC 601 Seoul, South Korea; Full report on file Case series Post-marketing Neuro. Ai. D Safe Treatment (Ne. ST) Registry To assess the safe use of Registry MLC 601 or MLC 901 in the “real world” setting Post-marketing On file: Case Series from Lebanon To assess the impact of Case series, Neuro. Aid on neurofunctional multicenter recovery in patients after their first mild to moderate cerebrovascular ischemic stroke, using the same endpoints as they are in CHIMES study, ie. Modified Rankin Scale, National Institute of Health Stroke Score (NIHSS) and Barthel Index (BI). Number of Subjects Diagnosis of Patients 10 Patients with ischemic stroke between 1 week to 6 months of onset 24 Patients with ischemic stroke up to 10 months from onset 20 (detailed Neurosurgical reports on 3) patients including those with head injury, haemorrhagic stroke and brain abscess, within 3 months of onset 75 Any patient case deemed treatable with MLC 601 or MLC 901 by physician 14 Cerebral infarct diagnosis Duration of Treatment 2 to 3 months Study Status; Type of Report Completed 1 to 6 months Completed 3 months Completed Any duration Ongoing 8 wks Completed 56
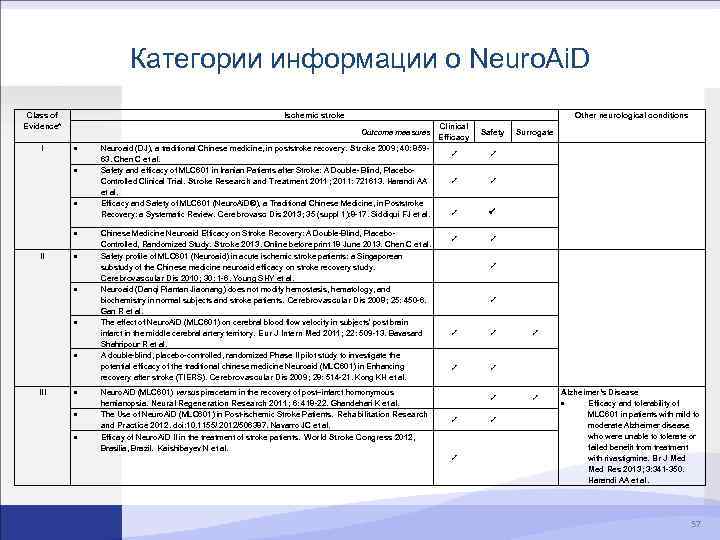
Категории информации о Neuro. Ai. D Class of Evidence* I Ischemic stroke Outcome measures III Other neurological conditions Neuroaid (DJ), a traditional Chinese medicine, in poststroke recovery. Stroke 2009; 40: 85963. Chen C et al. Safety and efficacy of MLC 601 in Iranian Patients after Stroke: A Double- Blind, Placebo. Controlled Clinical Trial. Stroke Research and Treatment 2011 ; 2011: 721613. Harandi AA et al. Efficacy and Safety of MLC 601 (Neuro. Ai. D®), a Traditional Chinese Medicine, in Poststroke Recovery: a Systematic Review. Cerebrovasc Dis 2013; 35 (suppl 1): 8 -17. Siddiqui FJ et al. Chinese Medicine Neuroaid Efficacy on Stroke Recovery: A Double-Blind, Placebo. Controlled, Randomized Study. Stroke 2013. Online before print 18 June 2013. Chen C et al. Safety profile of MLC 601 (Neuroaid) in acute ischemic stroke patients: a Singaporean substudy of the Chinese medicine neuroaid efficacy on stroke recovery study. Cerebrovascular Dis 2010; 30: 1 -6. Young SHY et al. Neuroaid (Danqi Piantan Jiaonang) does not modify hemostasis, hematology, and biochemistry in normal subjects and stroke patients. Cerebrovascular Dis 2008; 25: 450 -6. Gan R et al. The effect of Neuro. Ai. D (MLC 601) on cerebral blood flow velocity in subjects’ post brain infarct in the middle cerebral artery territory. Eur J Intern Med 2011; 22: 509 -13. Bavasard Shahripour R et al. A double-blind, placebo-controlled, randomized Phase II pilot study to investigate the potential efficacy of the traditional chinese medicine Neuroaid (MLC 601) in Enhancing recovery after stroke (TIERS). Cerebrovascular Dis 2009; 28: 514 -21. Kong KH et al. Neuro. Ai. D (MLC 601) versus piracetam in the recovery of post–infarct homonymous hemianopsia. Neural Regeneration Research 2011 ; 6: 418 -22. Ghandehari K et al. The Use of Neuro. Ai. D (MLC 601) in Post-ischemic Stroke Patients. Rehabilitation Research and Practice 2012. doi: 10. 1155/ 2012/506387. Navarro JC et al. Efficay of Neuro. Ai. D II in the treatment of stroke patients. World Stroke Congress 2012, Brasilia, Brazil. Kaishibayev N et al. Clinical Efficacy Safety Surrogate Alzheimer’s Disease Efficacy and tolerability of MLC 601 in patients with mild to moderate Alzheimer disease who were unable to tolerate or failed benefit from treatment with rivastigmine. Br J Med Res 2013; 3: 341 -350. Harandi AA et al. 57
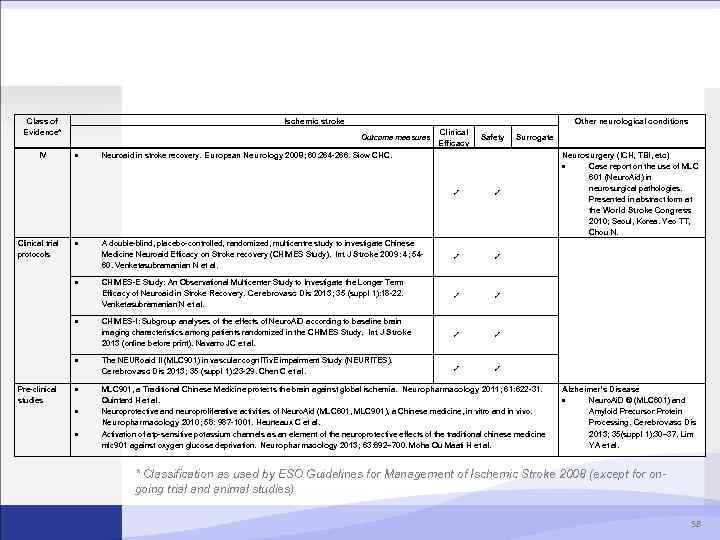
Class of Evidence* IV Ischemic stroke Other neurological conditions Outcome measures Clinical Efficacy Safety Surrogate Neuroaid in stroke recovery. European Neurology 2008; 60: 264 -266. Siow CHC. Clinical trial protocols Pre-clinical studies A double-blind, placebo-controlled, randomized, multicentre study to investigate Chinese Medicine Neuroaid Efficacy on Stroke recovery (CHIMES Study). Int J Stroke 2009: 4; 5460. Venketasubramanian N et al. CHIMES-E Study: An Observational Multicenter Study to Investigate the Longer Term Efficacy of Neuroaid in Stroke Recovery. Cerebrovasc Dis 2013; 35 (suppl 1): 18 -22. Venketasubramanian N et al. CHIMES-I: Subgroup analyses of the effects of Neuro. Ai. D according to baseline brain imaging characteristics among patients randomized in the CHIMES Study. Int J Stroke 2013 (online before print). Navarro JC et al. The NEURoaid II (MLC 901) in vascular cogn. ITiv. E impairment Study (NEURITES). Cerebrovasc Dis 2013; 35 (suppl 1): 23 -29. Chen C et al. Neurosurgery (ICH, TBI, etc) Case report on the use of MLC 601 (Neuro. Aid) in neurosurgical pathologies. Presented in abstract form at the World Stroke Congress 2010; Seoul, Korea. Yeo TT, Chou N. MLC 901, a Traditional Chinese Medicine protects the brain against global ischemia. Neuropharmacology 2011; 61: 622 -31. Quintard H et al. Neuroprotective and neuroproliferative activities of Neuro. Aid (MLC 601, MLC 901), a Chinese medicine, in vitro and in vivo. Neuropharmacology 2010; 58: 987 -1001. Heurteaux C et al. Activation of atp-sensitive potassium channels as an element of the neuroprotective effects of the traditional chinese medicine mlc 901 against oxygen glucose deprivation. Neuropharmacology 2013; 63: 692– 700. Moha Ou Maati H et al. Alzheimer’s Disease Neuro. Ai. D ® (MLC 601) and Amyloid Precursor Protein Processing. Cerebrovasc Dis 2013; 35(suppl 1): 30– 37. Lim YA et al. * Classification as used by ESO Guidelines for Management of Ischemic Stroke 2008 (except for ongoing trial and animal studies) 58

Информационные Резурсы 59
Интернет-страница для партнеров Moleac Все материалы и инструменты Neuro. Ai. D находятся в одном месте 60

Newsletters (новостные материалы) – ежемесячно Newsletter для Врачей Newsletter для Партнеров Международный Newsletter Moleac Next: develop shareholder newsletter 61

Stroke Recovery Coach (Тренинг Восстановления после Инсульта) Доступен для всех пациентов, врачей, ассоциаций для мониторинга прогресса 62
63
Реестр Nest про-активная и добровольная инициатива для мониторинга безопасности и эффективности приема Neuro. Ai. D пациентами 64

Международное Присутствие & Локальные Мероприятия 2010 2011 2012 2013 УЧАСТИЕ ØПрисутствие на международных конференциях: § JNLF во Франции, § ESC в Барселоне, § Neuromediterranee Congress в Ливии, § WSC в Сеуле, § ACNS в Малайзии… ØПрисутствие на международных конференциях: § ISC в Лос. Анджелес § JNLF в Париже § ESC в Гамбурге § WCN в Маракеше ØПрисутствие на международных конференциях: § ISC в Новом Орлеане § ESC в Лиссабоне § WSC в Бразилиа ØПрисутствие на международных конференциях: § ESC в Лондоне § WCN в Вене § APSC ØВстреча исследователей CHIMES в Сингапуре: более 50 участников, среди которых были Prof M. G. Bousser, Франция, Prof C. Chen, Сингапур… ØProf M. G. Bousser в Юго. Восточной Азии: интервью в Сингапуре и Филиппинах ØProf M. G. Bousser в Европе: интервью в Лиссабоне во время ESC ØСоздание операционного офиса в Кракове на Восточную Европу, СНГ и Балтию ØProf M. G. Bousser iв Европе: доклад на ESC в Лонлоне результатах исследования CHIMES ØProf Lazdunski в Юго. Восточной Азии: интервью в Филиппинах, Малайзия. 65

Спасибо за внимание! 66
NeuroAid_Ru_2013.pptx