НЕПРЕРЫВНОЕ КУЛЬТИВИРОВАНИЕ.ppt
- Количество слайдов: 38
 НЕПРЕРЫВНОЕ КУЛЬТИВИРОВАНИЕ МИКРООРГАНИЗМОВ • Непрерывное культивирование позволяет получить высокую производительность процесса и стабильные характеристики продукта. • Существуют два вида непрерывных процессов ферментации – тубулярные и хемостатные. • ТУБУЛЯРНЫЕ процессы реализуются в аппаратах полного вытеснения, а ХЕМОСТАТНЫЕ – в аппаратах полного смешения.
НЕПРЕРЫВНОЕ КУЛЬТИВИРОВАНИЕ МИКРООРГАНИЗМОВ • Непрерывное культивирование позволяет получить высокую производительность процесса и стабильные характеристики продукта. • Существуют два вида непрерывных процессов ферментации – тубулярные и хемостатные. • ТУБУЛЯРНЫЕ процессы реализуются в аппаратах полного вытеснения, а ХЕМОСТАТНЫЕ – в аппаратах полного смешения.
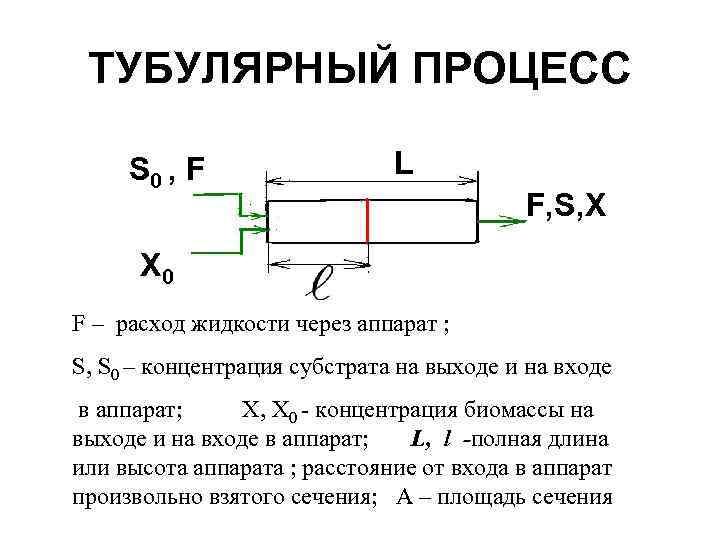 ТУБУЛЯРНЫЙ ПРОЦЕСС S 0 , F L F, S, X X 0 F – расход жидкости через аппарат ; S, S 0 – концентрация субстрата на выходе и на входе в аппарат; X, X 0 - концентрация биомассы на выходе и на входе в аппарат; L, l -полная длина или высота аппарата ; расстояние от входа в аппарат произвольно взятого сечения; А – площадь сечения
ТУБУЛЯРНЫЙ ПРОЦЕСС S 0 , F L F, S, X X 0 F – расход жидкости через аппарат ; S, S 0 – концентрация субстрата на выходе и на входе в аппарат; X, X 0 - концентрация биомассы на выходе и на входе в аппарат; L, l -полная длина или высота аппарата ; расстояние от входа в аппарат произвольно взятого сечения; А – площадь сечения
 ТУБУЛЯРНЫЙ ПРОЦЕСС • Питательная среда и посевной материал непрерывно поступают в аппарат, в котором нет обратного смешения. На входе в аппарат жидкость смешивается с посевным материалом. По мере продвижения в аппарате одновременно осуществляются рост биомассы и биосинтез продукта. • Время пребывания жидкости в апарате t. L = LA / F. • Время пребывания жидкости от входа в аппарат до произвольно взятого сечения tl =l. A /F/ • С учётом связи времени пребывания и длины аппарата кривые изменения всех концентраций такие же, как в периодическом процессе.
ТУБУЛЯРНЫЙ ПРОЦЕСС • Питательная среда и посевной материал непрерывно поступают в аппарат, в котором нет обратного смешения. На входе в аппарат жидкость смешивается с посевным материалом. По мере продвижения в аппарате одновременно осуществляются рост биомассы и биосинтез продукта. • Время пребывания жидкости в апарате t. L = LA / F. • Время пребывания жидкости от входа в аппарат до произвольно взятого сечения tl =l. A /F/ • С учётом связи времени пребывания и длины аппарата кривые изменения всех концентраций такие же, как в периодическом процессе.
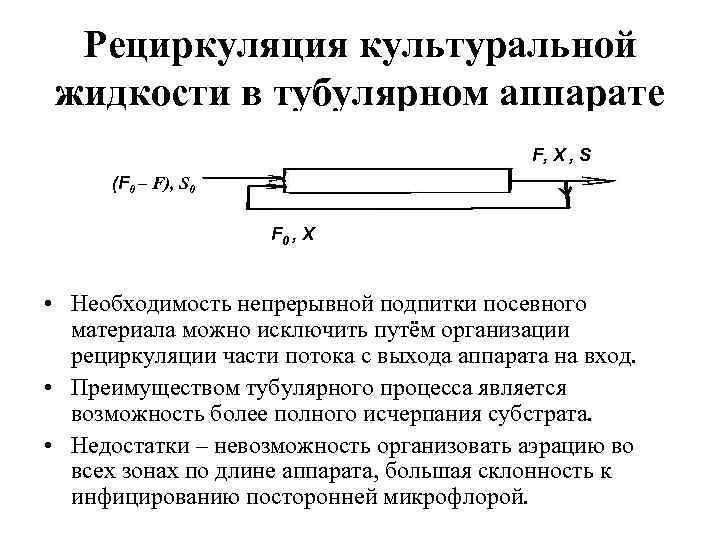 Рециркуляция культуральной жидкости в тубулярном аппарате F, X , S (F 0 – F), S 0 F 0 , X • Необходимость непрерывной подпитки посевного материала можно исключить путём организации рециркуляции части потока с выхода аппарата на вход. • Преимуществом тубулярного процесса является возможность более полного исчерпания субстрата. • Недостатки – невозможность организовать аэрацию во всех зонах по длине аппарата, большая склонность к инфицированию посторонней микрофлорой.
Рециркуляция культуральной жидкости в тубулярном аппарате F, X , S (F 0 – F), S 0 F 0 , X • Необходимость непрерывной подпитки посевного материала можно исключить путём организации рециркуляции части потока с выхода аппарата на вход. • Преимуществом тубулярного процесса является возможность более полного исчерпания субстрата. • Недостатки – невозможность организовать аэрацию во всех зонах по длине аппарата, большая склонность к инфицированию посторонней микрофлорой.
 Хемостатный процесс непрерывного культивирования • Процесс ферментации протекает в аппарате с перемешиванием. В аппарат с постоянной скоростью F подводится свежая питательная среда. • Из аппарата с той же скоростью отводится ферментационная среда, содержащая биомассу X, продукт метаболизма P, и остаточный субстрат S. • Посевной материал в аппарат подаётся только в момент запуска. Объём жидкости в аппарате V сохраняется постоянным. F, S 0 V P, S, X F, S, X, P
Хемостатный процесс непрерывного культивирования • Процесс ферментации протекает в аппарате с перемешиванием. В аппарат с постоянной скоростью F подводится свежая питательная среда. • Из аппарата с той же скоростью отводится ферментационная среда, содержащая биомассу X, продукт метаболизма P, и остаточный субстрат S. • Посевной материал в аппарат подаётся только в момент запуска. Объём жидкости в аппарате V сохраняется постоянным. F, S 0 V P, S, X F, S, X, P
 Простейшая модель процесса • Принимаем, что процесс направлен только на рост биомассы, поэтому нет специального уравнения для биосинтеза целевого продукта d. P/dt. • Принимаем субстрат-зависимую модель роста (Моно), так что ингибирующего продукта нет и уравнения для него не нужно. • Принимаем, что в процессе роста отсутствует диссимиляция биомассы ( ) • Принимаем, что для лимитирующего субстрата нет затрат на поддержание жизнедеятельности культуры (m. S = 0)
Простейшая модель процесса • Принимаем, что процесс направлен только на рост биомассы, поэтому нет специального уравнения для биосинтеза целевого продукта d. P/dt. • Принимаем субстрат-зависимую модель роста (Моно), так что ингибирующего продукта нет и уравнения для него не нужно. • Принимаем, что в процессе роста отсутствует диссимиляция биомассы ( ) • Принимаем, что для лимитирующего субстрата нет затрат на поддержание жизнедеятельности культуры (m. S = 0)
![Система уравнений • • Материальный баланс процесса: V(d. X/dt) =[μm. S/(KS + S)]XV - Система уравнений • • Материальный баланс процесса: V(d. X/dt) =[μm. S/(KS + S)]XV -](https://present5.com/presentation/-35435037_132496662/image-7.jpg) Система уравнений • • Материальный баланс процесса: V(d. X/dt) =[μm. S/(KS + S)]XV - FX V(d. S/dt)= FS 0–FS –(1/YXS) [μm. S/(KS+S)]XV Принимаем обозначение D = F/V, где D – скорость разбавления, [1/час] • Упрощённая запись системы уравнений: • d. X/dt = μX –DX • d. S/dt =D(S 0 –S) – (1/YXS) μX
Система уравнений • • Материальный баланс процесса: V(d. X/dt) =[μm. S/(KS + S)]XV - FX V(d. S/dt)= FS 0–FS –(1/YXS) [μm. S/(KS+S)]XV Принимаем обозначение D = F/V, где D – скорость разбавления, [1/час] • Упрощённая запись системы уравнений: • d. X/dt = μX –DX • d. S/dt =D(S 0 –S) – (1/YXS) μX
 Условия стационарности • В отличие от периодического процесса в непрерывном хемостатном процессе довольно быстро устанавливается стационарное состояние, при котором скорость роста биомассы будет равна скорости её вымывания из аппарата, а скорость притока субстрата за вычетом оттока остаточного субстрата равна скорости его расходования на рост биомассы микроорганизмов. • При этом (d. X/dt) = 0 и (d. S/dt) = 0
Условия стационарности • В отличие от периодического процесса в непрерывном хемостатном процессе довольно быстро устанавливается стационарное состояние, при котором скорость роста биомассы будет равна скорости её вымывания из аппарата, а скорость притока субстрата за вычетом оттока остаточного субстрата равна скорости его расходования на рост биомассы микроорганизмов. • При этом (d. X/dt) = 0 и (d. S/dt) = 0
 Параметры стационарного процесса: скорость роста • Из условий стационарности получаем: • μX – DX = 0 , откуда μ = D • Таким образом, в установившемся состоянии удельная скорость роста биомассы становится равной скорости разбавления D. Это очень удобно, поскольку скорость разбавления – это управляемый параметр, его задаёт оператор. • Если в какой-то момент времени это равенство нарушится (μ ≠ D), то скорость роста биомассы. • d. X/dt =(μ – D)X будет либо положительной (и тогда биомасса увеличивается), либо отрицательной (соответственно, концентрация биомассы уменьшается). При этом устанавливается равновесие при той же скорости разбавления, но другой концентрации биомассы.
Параметры стационарного процесса: скорость роста • Из условий стационарности получаем: • μX – DX = 0 , откуда μ = D • Таким образом, в установившемся состоянии удельная скорость роста биомассы становится равной скорости разбавления D. Это очень удобно, поскольку скорость разбавления – это управляемый параметр, его задаёт оператор. • Если в какой-то момент времени это равенство нарушится (μ ≠ D), то скорость роста биомассы. • d. X/dt =(μ – D)X будет либо положительной (и тогда биомасса увеличивается), либо отрицательной (соответственно, концентрация биомассы уменьшается). При этом устанавливается равновесие при той же скорости разбавления, но другой концентрации биомассы.
 Стационарные концентрации субстрата и биомассы • • • μ = D, или, с учётом выражения для μ : μm. S/(KS + S) = D, откуда получаем : S = KSD/ (μm – D) D(S 0 –S) – (1/YXS) μX = 0, откуда : X = YXS {S 0 - KSD/ (μm – D)} Графически выраженные зависимости X(D) S(D) называют «хемостатными кривыми»
Стационарные концентрации субстрата и биомассы • • • μ = D, или, с учётом выражения для μ : μm. S/(KS + S) = D, откуда получаем : S = KSD/ (μm – D) D(S 0 –S) – (1/YXS) μX = 0, откуда : X = YXS {S 0 - KSD/ (μm – D)} Графически выраженные зависимости X(D) S(D) называют «хемостатными кривыми»
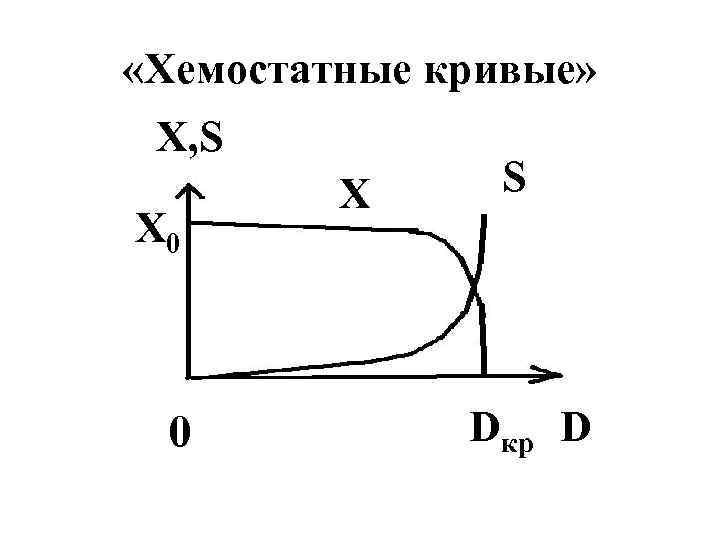 «Хемостатные кривые» X, S X 0 0 X S Dкр D
«Хемостатные кривые» X, S X 0 0 X S Dкр D
 «Вымывание» культуры • Хемостатная кривая X(D) показывает, что при повышении скорости разбавления концентрация биомассы снижается до нуля при некоторой критической скорости разбавления Dкр и при более высоких скоростях разбавления остаётся равной нулю. • Физически это означает, что культура «вымывается» : выходит больше биомассы, чем может вырасти. Ясно, что при этом концентрация субстрата в выходящем потоке такая же, как на входе в аппарат – S 0.
«Вымывание» культуры • Хемостатная кривая X(D) показывает, что при повышении скорости разбавления концентрация биомассы снижается до нуля при некоторой критической скорости разбавления Dкр и при более высоких скоростях разбавления остаётся равной нулю. • Физически это означает, что культура «вымывается» : выходит больше биомассы, чем может вырасти. Ясно, что при этом концентрация субстрата в выходящем потоке такая же, как на входе в аппарат – S 0.
 Критическая скорость разбавления • Приравнивая уравнение для концентрации биомассы нулю, получаем величину D= Dкр • X = YXS {S 0 - KSD/ (μm – D)} = 0 , откуда • Dкр = μm S 0/(KS + S 0) • Физически это означает, что критическая скорость разбавления равна удельной скорости роста биомассы при концентрации субстрата, равной его концентрации в подаваемом потоке среды.
Критическая скорость разбавления • Приравнивая уравнение для концентрации биомассы нулю, получаем величину D= Dкр • X = YXS {S 0 - KSD/ (μm – D)} = 0 , откуда • Dкр = μm S 0/(KS + S 0) • Физически это означает, что критическая скорость разбавления равна удельной скорости роста биомассы при концентрации субстрата, равной его концентрации в подаваемом потоке среды.
 Реперные точки кривой X(D) • Зависимость X(D) имеет 2 реперные точки: • X = X 0 при D = 0 и D= Dкр при X = 0 • Обе эти точки (X 0 и Dкр ) зависят от S 0 • Вид зависимостей представлен на графике (линейная для X 0 и с насыщением для Dкр ) Dкр X 0 0 S 0
Реперные точки кривой X(D) • Зависимость X(D) имеет 2 реперные точки: • X = X 0 при D = 0 и D= Dкр при X = 0 • Обе эти точки (X 0 и Dкр ) зависят от S 0 • Вид зависимостей представлен на графике (линейная для X 0 и с насыщением для Dкр ) Dкр X 0 0 S 0
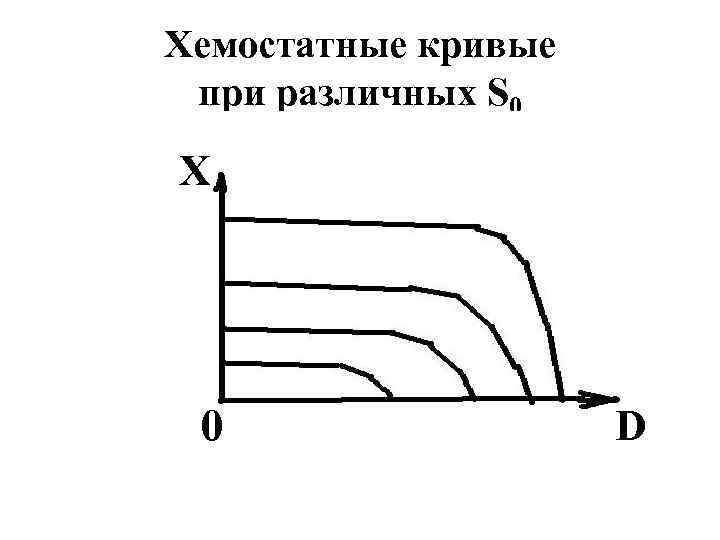 Хемостатные кривые при различных S 0 X 0 D
Хемостатные кривые при различных S 0 X 0 D
 Концентрация субстрата в свежей среде • Таким образом, и начальное положение хемостатной кривой, и точка вымывания зависят от концентрации субстрата в свежей среде (подпитке) S 0 • Эта величина наряду со скоростью разбавления является параметром, с помощью которого оператор может управлять процессом. Чем больше S 0 , тем выше концентрация биомассы в выходном потоке, причём в довольно широком диапазоне скоростей разбавления.
Концентрация субстрата в свежей среде • Таким образом, и начальное положение хемостатной кривой, и точка вымывания зависят от концентрации субстрата в свежей среде (подпитке) S 0 • Эта величина наряду со скоростью разбавления является параметром, с помощью которого оператор может управлять процессом. Чем больше S 0 , тем выше концентрация биомассы в выходном потоке, причём в довольно широком диапазоне скоростей разбавления.
 Остаточная концентрация субстрата • Интересную особенность имеет зависимость стационарной (остаточной) концентрации субстрата от начальной (входной) его концентрации. В полученной формуле нет ничего, кроме скорости разбавления и кинетических констант. • Из этого следует парадоксальный вывод: при любом изменении концентрации субстрата во входящем потоке S 0 в стационарном состоянии при заданной скорости разбавления устанавливается одна и та же остаточная концентрация субстрата S. Именно это свойство хемостата дало ему название: концентрация субстрата (химического соединения) стабилизируется сама по себе независимо от колебаний на входе.
Остаточная концентрация субстрата • Интересную особенность имеет зависимость стационарной (остаточной) концентрации субстрата от начальной (входной) его концентрации. В полученной формуле нет ничего, кроме скорости разбавления и кинетических констант. • Из этого следует парадоксальный вывод: при любом изменении концентрации субстрата во входящем потоке S 0 в стационарном состоянии при заданной скорости разбавления устанавливается одна и та же остаточная концентрация субстрата S. Именно это свойство хемостата дало ему название: концентрация субстрата (химического соединения) стабилизируется сама по себе независимо от колебаний на входе.
 Производительность хемостата • Производительность QX – количество биомассы, образующееся в единицу времени в единице объёма среды аппарата • QX =DX Подставляем выражение для X: • QX =D YXS {S 0 - KSD/ (μm – D)} • Для определения Dопт приравниваем нулю частную производную QX по D, откуда: • Dопт = μm { 1 }
Производительность хемостата • Производительность QX – количество биомассы, образующееся в единицу времени в единице объёма среды аппарата • QX =DX Подставляем выражение для X: • QX =D YXS {S 0 - KSD/ (μm – D)} • Для определения Dопт приравниваем нулю частную производную QX по D, откуда: • Dопт = μm { 1 }
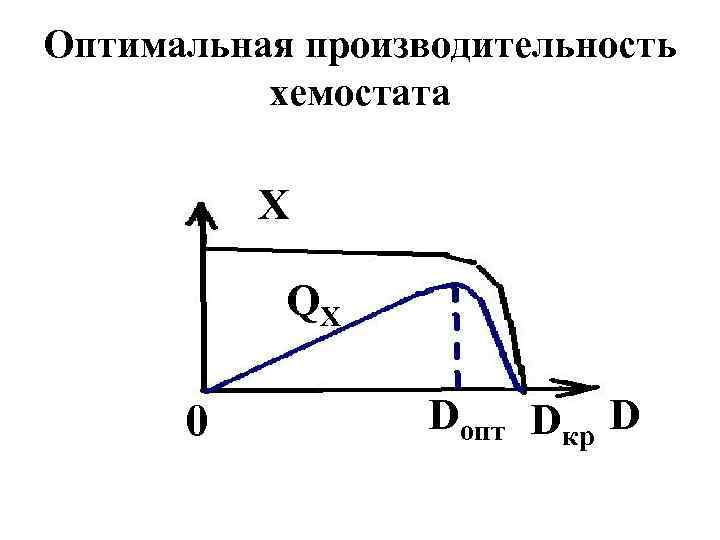 Оптимальная производительность хемостата X QX 0 Dопт Dкр D
Оптимальная производительность хемостата X QX 0 Dопт Dкр D
 Сравнение непрерывного и периодического процессов • Представляет интерес сравнить между собой в сопоставимых условиях два способа ферментации – периодический и непрерывный. • При сравнении возьмём процесс с одинаковыми кинетическими константами – максимальной удельной скоростью роста μm и характеристикой аппарата – максимально достижимой концентрацией биомассы Xm • Расчёты проведём в общем виде.
Сравнение непрерывного и периодического процессов • Представляет интерес сравнить между собой в сопоставимых условиях два способа ферментации – периодический и непрерывный. • При сравнении возьмём процесс с одинаковыми кинетическими константами – максимальной удельной скоростью роста μm и характеристикой аппарата – максимально достижимой концентрацией биомассы Xm • Расчёты проведём в общем виде.
 Периодический процесс • Преедполагается, что между двумя последовательными процессами роста микроорганизмов имеет место «пустой» , непродуктивный период, связанный с подготовкой аппарата, загрузкой среды и посевного материала и с лаг-фазой процесса – общее время t 0. • После этого от исходной концентрации X 0 до максимально достижимой в данном аппарате Xm рост идёт до самого конца ферментации (время tm) с максимальной удельной скоростью роста μm. .
Периодический процесс • Преедполагается, что между двумя последовательными процессами роста микроорганизмов имеет место «пустой» , непродуктивный период, связанный с подготовкой аппарата, загрузкой среды и посевного материала и с лаг-фазой процесса – общее время t 0. • После этого от исходной концентрации X 0 до максимально достижимой в данном аппарате Xm рост идёт до самого конца ферментации (время tm) с максимальной удельной скоростью роста μm. .
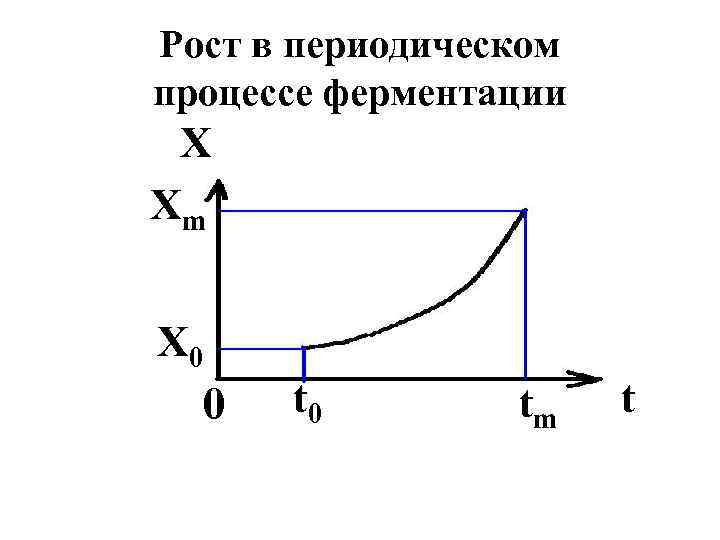 Рост в периодическом процессе ферментации X Xm X 0 0 tm t
Рост в периодическом процессе ферментации X Xm X 0 0 tm t
 Производительность периодического процесса • • d. X/dt = μm. X (при t > t 0) Решение уравнения X = X 0 e(t- t 0)μ или ln X = ln. X 0 + μm ( t - t 0) Концентрация X = Xm достигается в момент времени t = tm , для которого • ln Xm = ln X 0 + μm ( tm - t 0) , откуда • tm = t 0 + (1/ μm ) ln (Xm/X 0) • QXпериод = Xm /tm =Xm μm/[ ln (Xm/X 0) + μmt 0 ] m
Производительность периодического процесса • • d. X/dt = μm. X (при t > t 0) Решение уравнения X = X 0 e(t- t 0)μ или ln X = ln. X 0 + μm ( t - t 0) Концентрация X = Xm достигается в момент времени t = tm , для которого • ln Xm = ln X 0 + μm ( tm - t 0) , откуда • tm = t 0 + (1/ μm ) ln (Xm/X 0) • QXпериод = Xm /tm =Xm μm/[ ln (Xm/X 0) + μmt 0 ] m
 Производительность непрерывного процесса • Анализируем формулу для Dопт. Поскольку KS обычно значительно меньше S 0 , величина Dопт ≈ μm и производительность непрерывного процесса QXнепр ≈ Xm μm • Соотношение производительностей RQ: • RQ = QXнепр / QXпериод ≈ • ≈Xm μm/ {Xm μm/[ ln (Xm/X 0) + μmt 0 ]} или • RQ = ln (Xm/X 0) + μmt 0
Производительность непрерывного процесса • Анализируем формулу для Dопт. Поскольку KS обычно значительно меньше S 0 , величина Dопт ≈ μm и производительность непрерывного процесса QXнепр ≈ Xm μm • Соотношение производительностей RQ: • RQ = QXнепр / QXпериод ≈ • ≈Xm μm/ {Xm μm/[ ln (Xm/X 0) + μmt 0 ]} или • RQ = ln (Xm/X 0) + μmt 0
 Исходные данные для сравнительной оценки • В начале процесса инокулят обычно составляет по объёму около 5% от объёма среды, а концентрация биомассы в нём примерно такая же, как в конце ферментации. • Обычное время подготовки аппарата (t 0) – около 10 часов. • Величина μm для быстро растущих культур (бактерии, дрожжи) составляет 0, 5 ч-1, а для медленно растущих (грибы, актиномицеты) – 0, 05
Исходные данные для сравнительной оценки • В начале процесса инокулят обычно составляет по объёму около 5% от объёма среды, а концентрация биомассы в нём примерно такая же, как в конце ферментации. • Обычное время подготовки аппарата (t 0) – около 10 часов. • Величина μm для быстро растущих культур (бактерии, дрожжи) составляет 0, 5 ч-1, а для медленно растущих (грибы, актиномицеты) – 0, 05
 Цифровая оценка величины RQ • • • (Xm/X 0) = (100%)/(5%) = 20 Ln (Xm/X 0) ≈ 3 Упрощённая зависимость: RQ = 3 + 10 μm Таким образом, для быстро растущих культур соотношение RQ составляет ≈ 8, а для медленных ≈ 3, 5 • Итак, непрерывный процесс для процессов роста эффективнее периодического.
Цифровая оценка величины RQ • • • (Xm/X 0) = (100%)/(5%) = 20 Ln (Xm/X 0) ≈ 3 Упрощённая зависимость: RQ = 3 + 10 μm Таким образом, для быстро растущих культур соотношение RQ составляет ≈ 8, а для медленных ≈ 3, 5 • Итак, непрерывный процесс для процессов роста эффективнее периодического.
 АВТОСЕЛЕКЦИЯ • В ходе процесса непрерывного культивирования в культуре происходят изменения, в результате которых может появиться штамм, имеющий более высокую удельную скорость роста, чем исходный. • С этого момента оба штамма начинают конкурировать за субстрат. • Проведём анализ этого процесса
АВТОСЕЛЕКЦИЯ • В ходе процесса непрерывного культивирования в культуре происходят изменения, в результате которых может появиться штамм, имеющий более высокую удельную скорость роста, чем исходный. • С этого момента оба штамма начинают конкурировать за субстрат. • Проведём анализ этого процесса
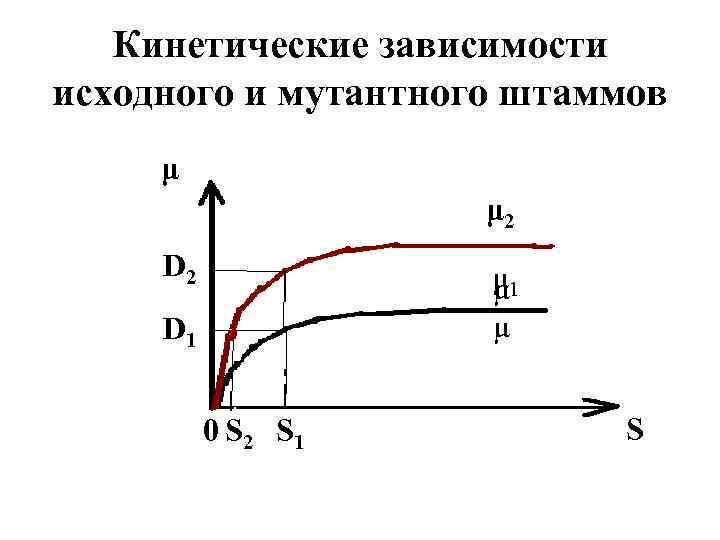 Кинетические зависимости исходного и мутантного штаммов μ μ 2 D 2 μ 1 μ μ D 1 0 S 2 S 1 S
Кинетические зависимости исходного и мутантного штаммов μ μ 2 D 2 μ 1 μ μ D 1 0 S 2 S 1 S
 Технологические параметры в процессе автоселекции • На графике изображены кинетические зависимости μ 1(S) для исходного и μ 2(S) для вновь образовавшегося мутантного штамма. • Если процесс протекает при скорости разбавления D 1 , то исходный штамм обеспечивает саморегулирование процесса при концентрации субстрата в среде S 1.
Технологические параметры в процессе автоселекции • На графике изображены кинетические зависимости μ 1(S) для исходного и μ 2(S) для вновь образовавшегося мутантного штамма. • Если процесс протекает при скорости разбавления D 1 , то исходный штамм обеспечивает саморегулирование процесса при концентрации субстрата в среде S 1.
 Как себя чувствует штамм-мутант? • Для штамма-мутанта концентрация субстрата S 1 обеспечивает удельную скорость роста μ 2(S 1) =D 2, которая значительно больше скорости разбавления D 1 • Следовательно, концентрация биомассы мутантного штамма растёт: • d. X 2/dt = {μ 2(S 1) - D 1}X > 0 • Рост продолжается до тех пор, пока концентрация субстрата не снизится до S 2.
Как себя чувствует штамм-мутант? • Для штамма-мутанта концентрация субстрата S 1 обеспечивает удельную скорость роста μ 2(S 1) =D 2, которая значительно больше скорости разбавления D 1 • Следовательно, концентрация биомассы мутантного штамма растёт: • d. X 2/dt = {μ 2(S 1) - D 1}X > 0 • Рост продолжается до тех пор, пока концентрация субстрата не снизится до S 2.
 Как себя чувствует исходный штамм? • При уменьшении концентрации субстрата концентрация биомассы исходного штамма начинает уменьшаться : • d. X 1/dt = {μ 1(S 2) - D 1}X < 0 • Следствием этого становится вымывание исходного штамма и замена его мутантным. • Концентрация биомассы при этом возрастает по сравнению с той, которая была при исходном штамме
Как себя чувствует исходный штамм? • При уменьшении концентрации субстрата концентрация биомассы исходного штамма начинает уменьшаться : • d. X 1/dt = {μ 1(S 2) - D 1}X < 0 • Следствием этого становится вымывание исходного штамма и замена его мутантным. • Концентрация биомассы при этом возрастает по сравнению с той, которая была при исходном штамме
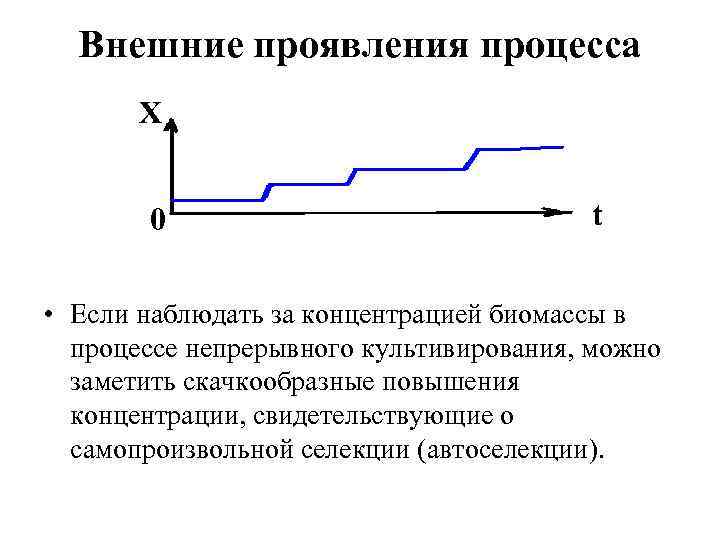 Внешние проявления процесса автоселекции X 0 t • Если наблюдать за концентрацией биомассы в процессе непрерывного культивирования, можно заметить скачкообразные повышения концентрации, свидетельствующие о самопроизвольной селекции (автоселекции).
Внешние проявления процесса автоселекции X 0 t • Если наблюдать за концентрацией биомассы в процессе непрерывного культивирования, можно заметить скачкообразные повышения концентрации, свидетельствующие о самопроизвольной селекции (автоселекции).
 Значение автоселекции • Итак, длительный непрерывный процесс может быть использован для отбора штаммов, обеспечивающих более высокую скорость роста биомассы микроорганизмов. • Улучшение штаммов по удельной скорости роста не всегда полезно. При этом иногда происходит ухудшение качества белка и других компонентов клетки и снижение её способности к биосинтезу полезных метаболитов.
Значение автоселекции • Итак, длительный непрерывный процесс может быть использован для отбора штаммов, обеспечивающих более высокую скорость роста биомассы микроорганизмов. • Улучшение штаммов по удельной скорости роста не всегда полезно. При этом иногда происходит ухудшение качества белка и других компонентов клетки и снижение её способности к биосинтезу полезных метаболитов.
 Определение кинетических констант в хемостате • В хемостате удобно определять кинетические константы. Задавая скорость разбавления, мы сразу имеем удельную скорость роста, которую в периодическом процессе можно получить лишь на основании двух-трёх измерений X на интервале времени Δt. • Концентрация субстрата S в хемостате требует только одного измерения, а в периодическом процессе – минимум двух для определения среднего значения за интервал времени. • Все эти измерения требуется проводить при 4 – 5 парах значений μ и S, так что преимущество непрерывного процесса очевидно.
Определение кинетических констант в хемостате • В хемостате удобно определять кинетические константы. Задавая скорость разбавления, мы сразу имеем удельную скорость роста, которую в периодическом процессе можно получить лишь на основании двух-трёх измерений X на интервале времени Δt. • Концентрация субстрата S в хемостате требует только одного измерения, а в периодическом процессе – минимум двух для определения среднего значения за интервал времени. • Все эти измерения требуется проводить при 4 – 5 парах значений μ и S, так что преимущество непрерывного процесса очевидно.
 Преимущества непрерывного способа культивирования 1 • Рост биомассы можно поддерживать неопределённо долго. • Можно поддерживать постоянную концентрацию биомассы. • Можно длительно поддерживать рост, лимитированный одним заданным субстратом. • Удобно определять кинетические константы. • Более высокая производительность по сравнению с периодическим.
Преимущества непрерывного способа культивирования 1 • Рост биомассы можно поддерживать неопределённо долго. • Можно поддерживать постоянную концентрацию биомассы. • Можно длительно поддерживать рост, лимитированный одним заданным субстратом. • Удобно определять кинетические константы. • Более высокая производительность по сравнению с периодическим.
 Преимущества непрерывного способа культивирования 2 • Результаты, полученные в непрерывном процессе, более надёжны и воспроизводимы, чем в периодических. • Облегчены механизация и автоматизация. • Постоянное качество готового продукта. • Меньше контакт персонала с микроорганизмами. • Возможна автоселекция микроорганизмов. • Меньше износ измерительных приборов.
Преимущества непрерывного способа культивирования 2 • Результаты, полученные в непрерывном процессе, более надёжны и воспроизводимы, чем в периодических. • Облегчены механизация и автоматизация. • Постоянное качество готового продукта. • Меньше контакт персонала с микроорганизмами. • Возможна автоселекция микроорганизмов. • Меньше износ измерительных приборов.
 Недостатки непрерывного культивирования 1 • Меньшая гибкость, регулировать можно только некоторые параметры. • Более высокие требования к постоянству качества сырья. • Больше капитальные вложения. • Трудно непрерывно дозировать нерастворимые твёрдые субстраты. • Больше опасность инфицирования из-за большей длительности культивирования.
Недостатки непрерывного культивирования 1 • Меньшая гибкость, регулировать можно только некоторые параметры. • Более высокие требования к постоянству качества сырья. • Больше капитальные вложения. • Трудно непрерывно дозировать нерастворимые твёрдые субстраты. • Больше опасность инфицирования из-за большей длительности культивирования.
 Недостатки непрерывного культивирования 2 • Возможность «вырождения» культуры за счёт автоселекции. • Не всегда достигаются хорошие результаты для биосинтеза продуктов метаболизма. • Трудно культивировать мицелиальные культуры из-за вязкости, гетерогенности и пристеночного роста. • Повышенные требования к надёжности оборудования
Недостатки непрерывного культивирования 2 • Возможность «вырождения» культуры за счёт автоселекции. • Не всегда достигаются хорошие результаты для биосинтеза продуктов метаболизма. • Трудно культивировать мицелиальные культуры из-за вязкости, гетерогенности и пристеночного роста. • Повышенные требования к надёжности оборудования


