Непредельные углеводороды.ppt
- Количество слайдов: 20
 Непредельные углеводороды АЛКЕНЫ (Олефины) Cn. H 2 n
Непредельные углеводороды АЛКЕНЫ (Олефины) Cn. H 2 n
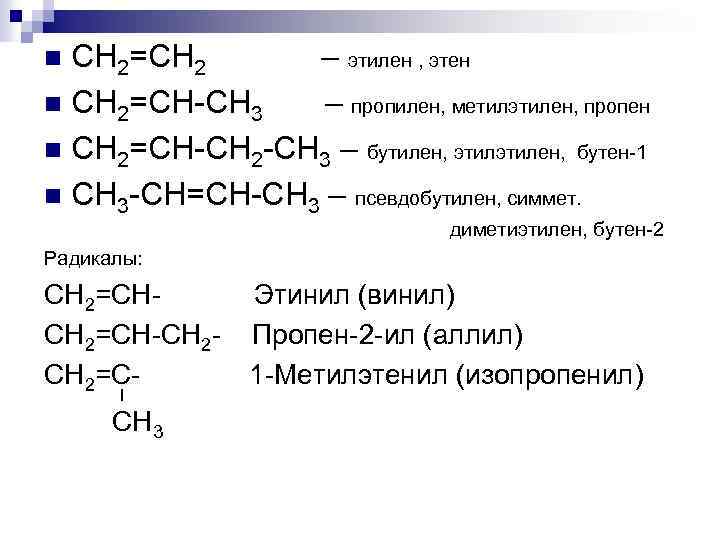 CH 2=CH 2 – этилен , этен n CH 2=CH-СН 3 – пропилен, метилэтилен, пропен n CH 2=CH-CH 2 -СН 3 – бутилен, этилен, бутен-1 n CH 3 -CH=CH-СН 3 – псевдобутилен, симмет. n диметиэтилен, бутен-2 Радикалы: CH 2=CH-CH 2=CСН 3 Этинил (винил) Пропен-2 -ил (аллил) 1 -Метилэтенил (изопропенил)
CH 2=CH 2 – этилен , этен n CH 2=CH-СН 3 – пропилен, метилэтилен, пропен n CH 2=CH-CH 2 -СН 3 – бутилен, этилен, бутен-1 n CH 3 -CH=CH-СН 3 – псевдобутилен, симмет. n диметиэтилен, бутен-2 Радикалы: CH 2=CH-CH 2=CСН 3 Этинил (винил) Пропен-2 -ил (аллил) 1 -Метилэтенил (изопропенил)
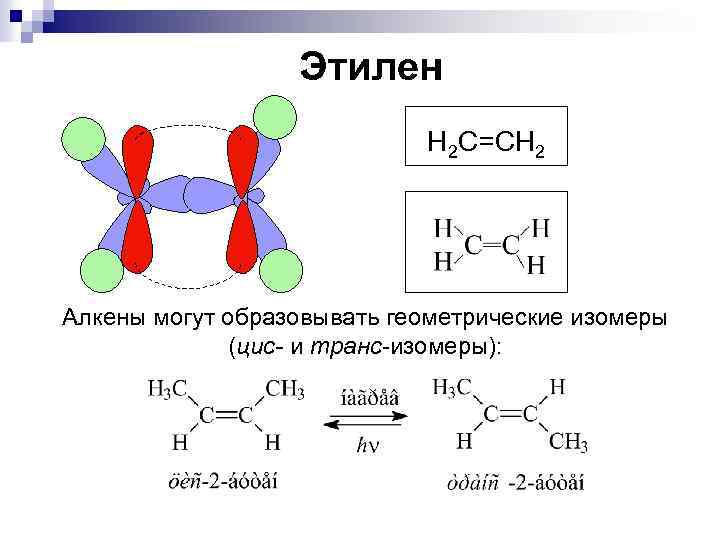 Этилен Н 2 С=СН 2 Алкены могут образовывать геометрические изомеры (цис- и транс-изомеры):
Этилен Н 2 С=СН 2 Алкены могут образовывать геометрические изомеры (цис- и транс-изомеры):
 Физические свойства Не растворимы в воде, растворимы в неполярных растворителях: бензоле, эфирах, хлороформе. n Температуры кипения близки к температурам кипения алканов. n
Физические свойства Не растворимы в воде, растворимы в неполярных растворителях: бензоле, эфирах, хлороформе. n Температуры кипения близки к температурам кипения алканов. n
 ПОЛУЧЕНИЕ Крекинг алканов: n Каталитическая дегидрогенизация (дегидрирование) алканов: n n Дегидрогалогенирование галогеналканов:
ПОЛУЧЕНИЕ Крекинг алканов: n Каталитическая дегидрогенизация (дегидрирование) алканов: n n Дегидрогалогенирование галогеналканов:
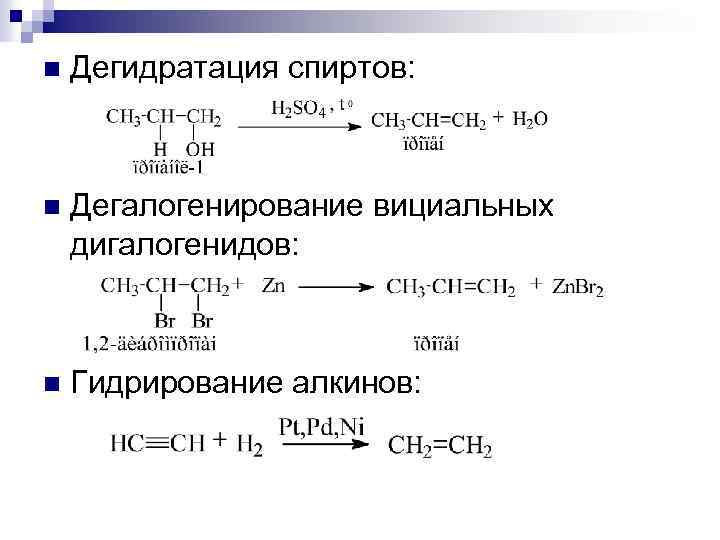 n Дегидратация спиртов: n Дегалогенирование вициальных дигалогенидов: n Гидрирование алкинов:
n Дегидратация спиртов: n Дегалогенирование вициальных дигалогенидов: n Гидрирование алкинов:
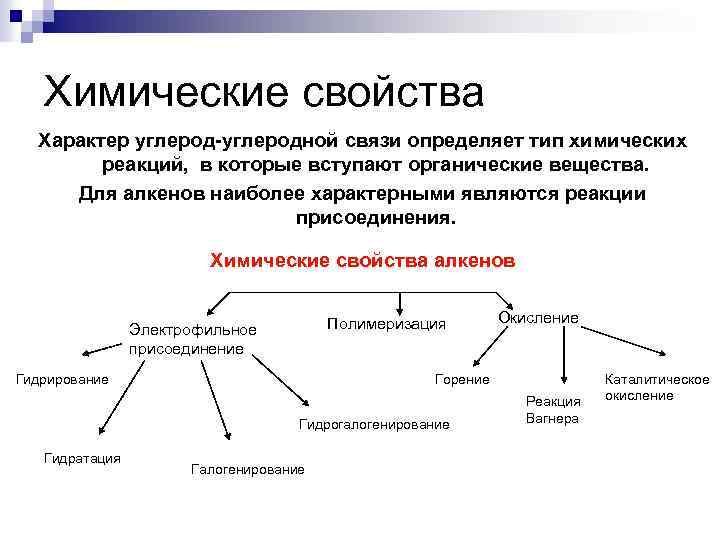 Химические свойства Характер углерод-углеродной связи определяет тип химических реакций, в которые вступают органические вещества. Для алкенов наиболее характерными являются реакции присоединения. Химические свойства алкенов Полимеризация Электрофильное присоединение Гидрирование Горение Гидрогалогенирование Гидратация Окисление Галогенирование Реакция Вагнера Каталитическое окисление
Химические свойства Характер углерод-углеродной связи определяет тип химических реакций, в которые вступают органические вещества. Для алкенов наиболее характерными являются реакции присоединения. Химические свойства алкенов Полимеризация Электрофильное присоединение Гидрирование Горение Гидрогалогенирование Гидратация Окисление Галогенирование Реакция Вагнера Каталитическое окисление
 Химические свойства n n Реакции присоединения: Присоединение галогенов (АЕ, AR) Присоединение протонных кислот и воды (АЕ) Присоединение водорода n Реакции полимеризации (Полимеризация – это процесс образования высокомолекулярного вещества путем соединения низкомолекулярных веществ, протекающих без изменения химического состава и не сопровождающийся образованием побочных продуктов) n. A An Мономер n n Полимер Цепная линейная полимеризация Ступенчатая полимеризация Радикальная полимеризация Сополимеризация (использование двух и более мономеров)
Химические свойства n n Реакции присоединения: Присоединение галогенов (АЕ, AR) Присоединение протонных кислот и воды (АЕ) Присоединение водорода n Реакции полимеризации (Полимеризация – это процесс образования высокомолекулярного вещества путем соединения низкомолекулярных веществ, протекающих без изменения химического состава и не сопровождающийся образованием побочных продуктов) n. A An Мономер n n Полимер Цепная линейная полимеризация Ступенчатая полимеризация Радикальная полимеризация Сополимеризация (использование двух и более мономеров)
 Химические свойства n Реакции окисления Гидроксилирование (реакция Вагнера) Качественная реакция на двойную связь ¨ Озонирование ¨ n Реакции замещения Не характерны для алкенов, могут протекать в особых условиях (при высокой температуре) CH 2=CH-CH 3 + Cl 2 CH 2=CH-CH 2 -Cl + HCl ¨
Химические свойства n Реакции окисления Гидроксилирование (реакция Вагнера) Качественная реакция на двойную связь ¨ Озонирование ¨ n Реакции замещения Не характерны для алкенов, могут протекать в особых условиях (при высокой температуре) CH 2=CH-CH 3 + Cl 2 CH 2=CH-CH 2 -Cl + HCl ¨
 Использование этилена
Использование этилена
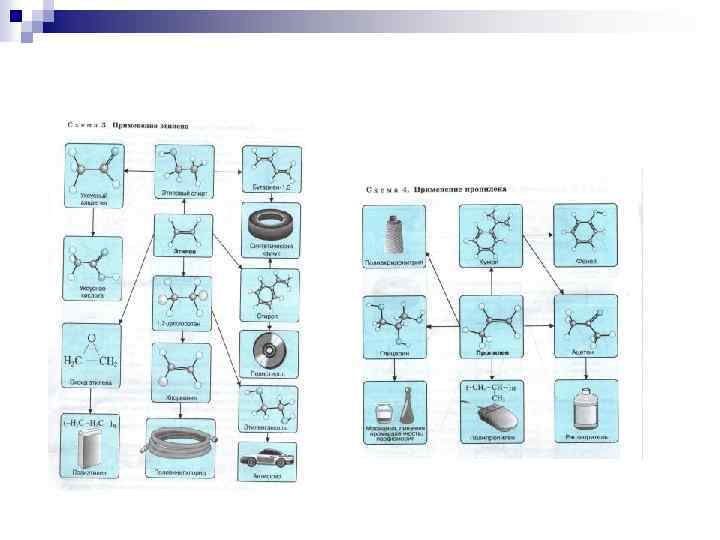
 Диеновые углеводороды Сn. Н 2 n-2
Диеновые углеводороды Сn. Н 2 n-2
 Диеновые углеводороды (алкадиены или диолефины). Непредельные соединения, содержащие в молекуле двойные связи, называются диеновыми углеводородами. Диеновые углеводороды на два атома водорода беднее, чем алкены с тем же числом углеродных атомов.
Диеновые углеводороды (алкадиены или диолефины). Непредельные соединения, содержащие в молекуле двойные связи, называются диеновыми углеводородами. Диеновые углеводороды на два атома водорода беднее, чем алкены с тем же числом углеродных атомов.
 Номенклатура и изомерия По систематической номенклатуре диеновые углеводороды называют также, как и этиленовые, но заменяют при этом суффикс –ен на –диен. Положение каждой двойной связи обозначают цифрой. Нумерацию производят таким образом, чтобы сумма цифр, обозначающая положение двойных связей, была наименьшей.
Номенклатура и изомерия По систематической номенклатуре диеновые углеводороды называют также, как и этиленовые, но заменяют при этом суффикс –ен на –диен. Положение каждой двойной связи обозначают цифрой. Нумерацию производят таким образом, чтобы сумма цифр, обозначающая положение двойных связей, была наименьшей.
 Получение диенов Основным промышленным способом получения дивинила и изопрена является дегидрирование соответствующих бутанбутиленовых или изопентанамиленовых смесей над катализатором. Впервые дивинил был получен по методу С. В. Лебедева (1874 -1934) из этилового спирта. Дивинил и изопрен в небольших количествах выделяют из продуктов пиролиза нефти.
Получение диенов Основным промышленным способом получения дивинила и изопрена является дегидрирование соответствующих бутанбутиленовых или изопентанамиленовых смесей над катализатором. Впервые дивинил был получен по методу С. В. Лебедева (1874 -1934) из этилового спирта. Дивинил и изопрен в небольших количествах выделяют из продуктов пиролиза нефти.
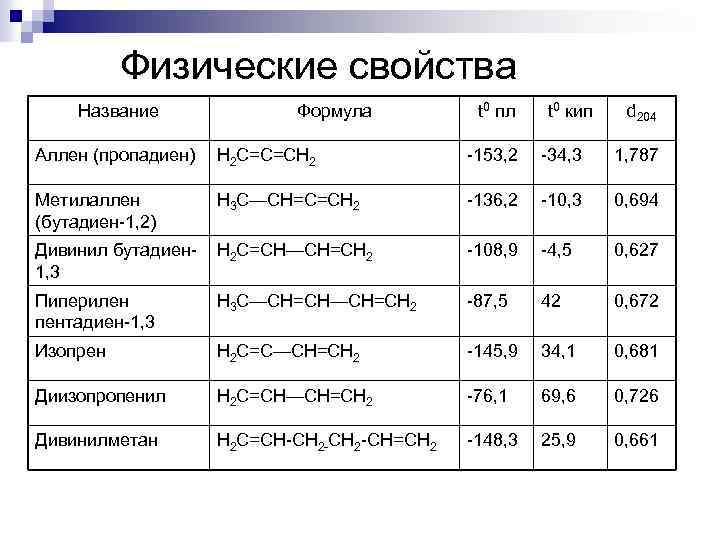 Физические свойства Название Формула t 0 пл t 0 кип d 204 Аллен (пропадиен) Н 2 С=С=СН 2 -153, 2 -34, 3 1, 787 Метилаллен (бутадиен-1, 2) Н 3 С—СН=С=СН 2 -136, 2 -10, 3 0, 694 Дивинил бутадиен 1, 3 Н 2 С=СН—СН=СН 2 -108, 9 -4, 5 0, 627 Пиперилен пентадиен-1, 3 Н 3 С—СН=СН 2 -87, 5 42 0, 672 Изопрен Н 2 С=С—СН=СН 2 -145, 9 34, 1 0, 681 Диизопропенил Н 2 С=СН—СН=СН 2 -76, 1 69, 6 0, 726 Дивинилметан Н 2 С=СН-СН 2 -СН=СН 2 -148, 3 25, 9 0, 661
Физические свойства Название Формула t 0 пл t 0 кип d 204 Аллен (пропадиен) Н 2 С=С=СН 2 -153, 2 -34, 3 1, 787 Метилаллен (бутадиен-1, 2) Н 3 С—СН=С=СН 2 -136, 2 -10, 3 0, 694 Дивинил бутадиен 1, 3 Н 2 С=СН—СН=СН 2 -108, 9 -4, 5 0, 627 Пиперилен пентадиен-1, 3 Н 3 С—СН=СН 2 -87, 5 42 0, 672 Изопрен Н 2 С=С—СН=СН 2 -145, 9 34, 1 0, 681 Диизопропенил Н 2 С=СН—СН=СН 2 -76, 1 69, 6 0, 726 Дивинилметан Н 2 С=СН-СН 2 -СН=СН 2 -148, 3 25, 9 0, 661
 Химические свойства Диены, содержащие в молекуле несопряженные (изолированные) двойные связи, ведут себя как обычные алкены. В то же время диены с сопряженными двойными связями обладают высокой реакционной способностью и отличаются рядом особенностей. Однако для тех и других характерны прежде всего реакции присоединения: - водорода (для сопряженных диенов); - галогенов (по механизмам АЕ, АR); - галогенводородов. Реакции полимеризации (Синтез Лебедева)
Химические свойства Диены, содержащие в молекуле несопряженные (изолированные) двойные связи, ведут себя как обычные алкены. В то же время диены с сопряженными двойными связями обладают высокой реакционной способностью и отличаются рядом особенностей. Однако для тех и других характерны прежде всего реакции присоединения: - водорода (для сопряженных диенов); - галогенов (по механизмам АЕ, АR); - галогенводородов. Реакции полимеризации (Синтез Лебедева)
 Каучуки и резины относятся к эластомерам. Каучуки делят на натуральный (природный) и синтетический. Натуральный каучук представляет собой высокоэластичную массу, получаемую из млечного сока (латекс – взвесь мельчайших частичек каучука в воде) некоторых тропических деревьев (гевеи бразильской и др. ) и растений (кок-сагыз, таусагыз, гваюла). Натуральный каучук – природный непредельный полимер со средней молекулярной массой от 15000 до 500000.
Каучуки и резины относятся к эластомерам. Каучуки делят на натуральный (природный) и синтетический. Натуральный каучук представляет собой высокоэластичную массу, получаемую из млечного сока (латекс – взвесь мельчайших частичек каучука в воде) некоторых тропических деревьев (гевеи бразильской и др. ) и растений (кок-сагыз, таусагыз, гваюла). Натуральный каучук – природный непредельный полимер со средней молекулярной массой от 15000 до 500000.
 Экологические аспекты n ПДК (максимально разовая) в атмосферном воздухе: Для этилена и пропена – 3 мг/м 3 n Для пентена -1 – 1, 5 мг/м 3 n Для гексенов: разовая – 0, 4 мг/м 3 и среднесуточная – 0, 085 мг/м 3 n Для бутадиена -1, 3 – 3 мг/м 3 n
Экологические аспекты n ПДК (максимально разовая) в атмосферном воздухе: Для этилена и пропена – 3 мг/м 3 n Для пентена -1 – 1, 5 мг/м 3 n Для гексенов: разовая – 0, 4 мг/м 3 и среднесуточная – 0, 085 мг/м 3 n Для бутадиена -1, 3 – 3 мг/м 3 n
 Домашнее задание n Конспект «Присоединение несимметричных соединений к несимметричным алкенам» (Правило Марковникова) Объяснить с точки зрения взаимного влияния атомов.
Домашнее задание n Конспект «Присоединение несимметричных соединений к несимметричным алкенам» (Правило Марковникова) Объяснить с точки зрения взаимного влияния атомов.


