Неорганические соединения серы.pptx
- Количество слайдов: 23
 Неорганические соединения серы ассистент кафедры химии Вят. ГГУ Селезенев Р. В.
Неорганические соединения серы ассистент кафедры химии Вят. ГГУ Селезенев Р. В.
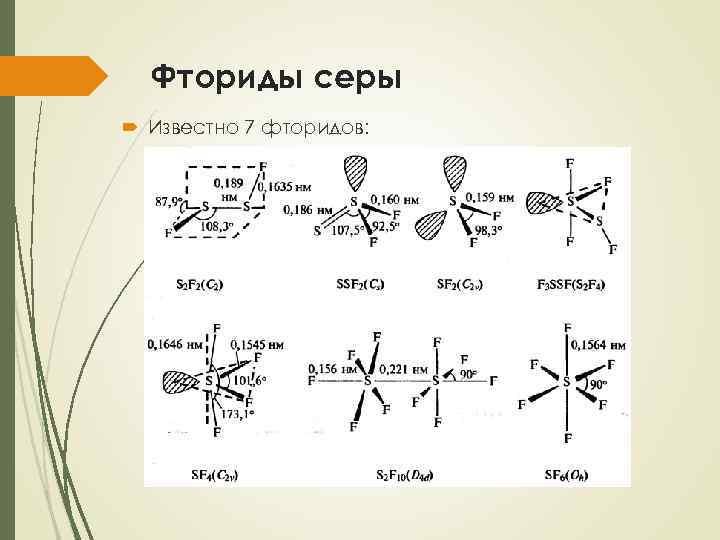 Фториды серы Известно 7 фторидов:
Фториды серы Известно 7 фторидов:
 Фториды серы. Получение Фторирование хлоридов Из дигалогенидов Фторирование серы Из простых веществ
Фториды серы. Получение Фторирование хлоридов Из дигалогенидов Фторирование серы Из простых веществ
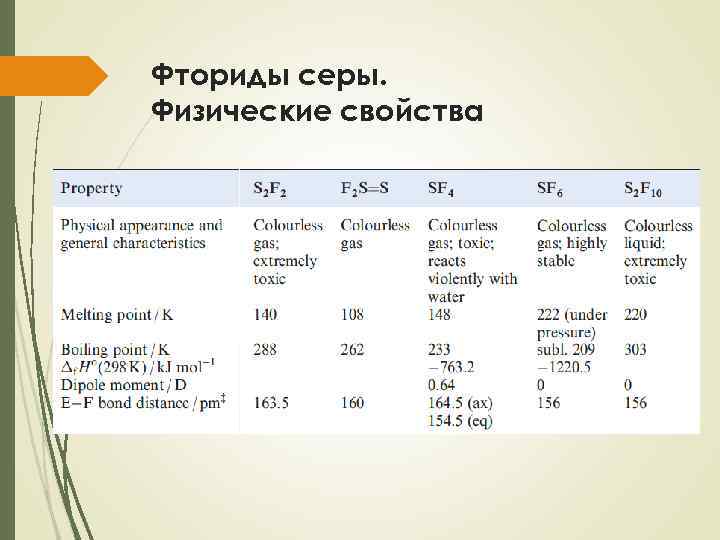 Фториды серы. Физические свойства
Фториды серы. Физические свойства
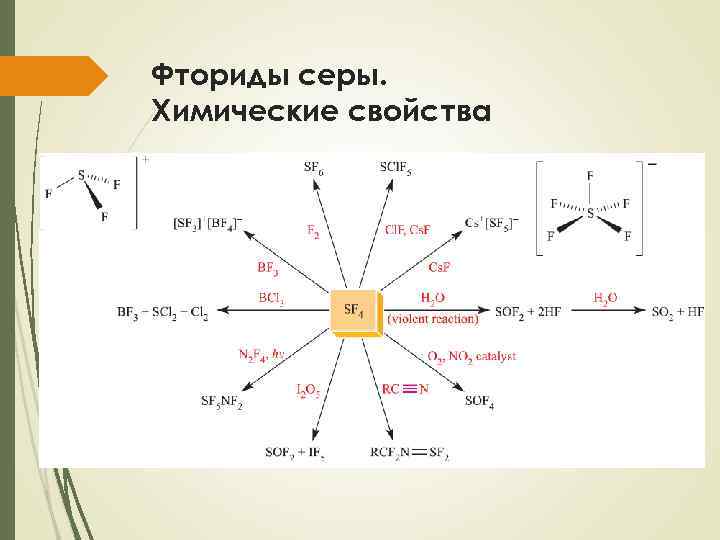 Фториды серы. Химические свойства
Фториды серы. Химические свойства
 Фториды серы. Химические свойства Гидролиз Горение в кислороде Диспропорционирование Взаимодействие с металлами Фторирующие агенты
Фториды серы. Химические свойства Гидролиз Горение в кислороде Диспропорционирование Взаимодействие с металлами Фторирующие агенты
 Хлориды серы. Физические свойства S 2 Cl 2 – золотисто-желтая ядовитая легкокипящая дурно-пахнущая жидкость, т. пл. = -76°С, т. кип. = 138°С SCl 2 – вишнево-красная ядовитая легкокипящая дурно-пахнущая жидкость, т. пл. = -122°С, т. кип. = 59°С
Хлориды серы. Физические свойства S 2 Cl 2 – золотисто-желтая ядовитая легкокипящая дурно-пахнущая жидкость, т. пл. = -76°С, т. кип. = 138°С SCl 2 – вишнево-красная ядовитая легкокипящая дурно-пахнущая жидкость, т. пл. = -122°С, т. кип. = 59°С
 Хлориды серы. Химические свойства Гидролиз с образованием H 2 S, SO 2, H 2 SO 3, H 2 SO 4, H 2 Sx. O 6 Окисляется кислородом SOCl 2 SO 2 Cl 2
Хлориды серы. Химические свойства Гидролиз с образованием H 2 S, SO 2, H 2 SO 3, H 2 SO 4, H 2 Sx. O 6 Окисляется кислородом SOCl 2 SO 2 Cl 2
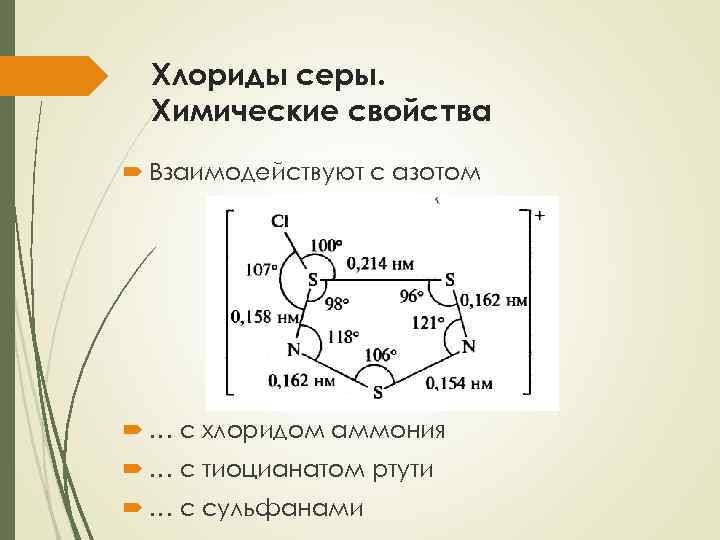 Хлориды серы. Химические свойства Взаимодействуют с азотом … с хлоридом аммония … с тиоцианатом ртути … с сульфанами
Хлориды серы. Химические свойства Взаимодействуют с азотом … с хлоридом аммония … с тиоцианатом ртути … с сульфанами
 Бромиды серы. Получение Прямой синтез SBr 2 был обнаружен как продукт, изолированный в матрице, когда через смесь S 2 Cl 2/SCl 2: Вг 2: Аг в соотношении 1: 1: 150 пропускали микроволновой разряд мощностью 80 Вт, а продукт конденсировали на окне из Csl в гелиевом криостате при 9 К Дибромсульфаны образуются при действии безводного бромоводорода на соответствующие хлориды
Бромиды серы. Получение Прямой синтез SBr 2 был обнаружен как продукт, изолированный в матрице, когда через смесь S 2 Cl 2/SCl 2: Вг 2: Аг в соотношении 1: 1: 150 пропускали микроволновой разряд мощностью 80 Вт, а продукт конденсировали на окне из Csl в гелиевом криостате при 9 К Дибромсульфаны образуются при действии безводного бромоводорода на соответствующие хлориды
 Бромиды серы. Свойства Очень нестабильны. Разлагаются при комнатной температуре S 2 Br 2 – гранатово-красная жидкость с т. пл. = -46°С, т. кип. = 54°С
Бромиды серы. Свойства Очень нестабильны. Разлагаются при комнатной температуре S 2 Br 2 – гранатово-красная жидкость с т. пл. = -46°С, т. кип. = 54°С
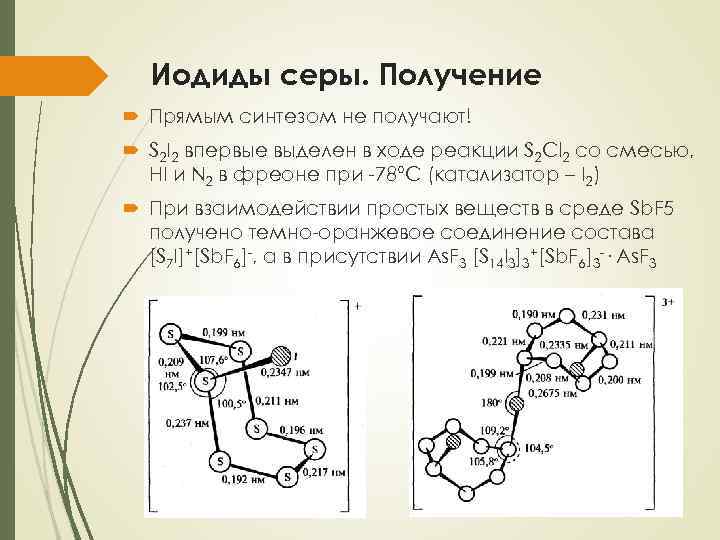 Иодиды серы. Получение Прямым синтезом не получают! S 2 I 2 впервые выделен в ходе реакции S 2 Cl 2 со смесью, HI и N 2 в фреоне при -78°С (катализатор – I 2) При взаимодействии простых веществ в среде Sb. F 5 получено темно-оранжевое соединение состава [S 7 I]+[Sb. F 6]-, а в присутствии As. F 3 [S 14 I 3]3+[Sb. F 6]3 -· As. F 3
Иодиды серы. Получение Прямым синтезом не получают! S 2 I 2 впервые выделен в ходе реакции S 2 Cl 2 со смесью, HI и N 2 в фреоне при -78°С (катализатор – I 2) При взаимодействии простых веществ в среде Sb. F 5 получено темно-оранжевое соединение состава [S 7 I]+[Sb. F 6]-, а в присутствии As. F 3 [S 14 I 3]3+[Sb. F 6]3 -· As. F 3
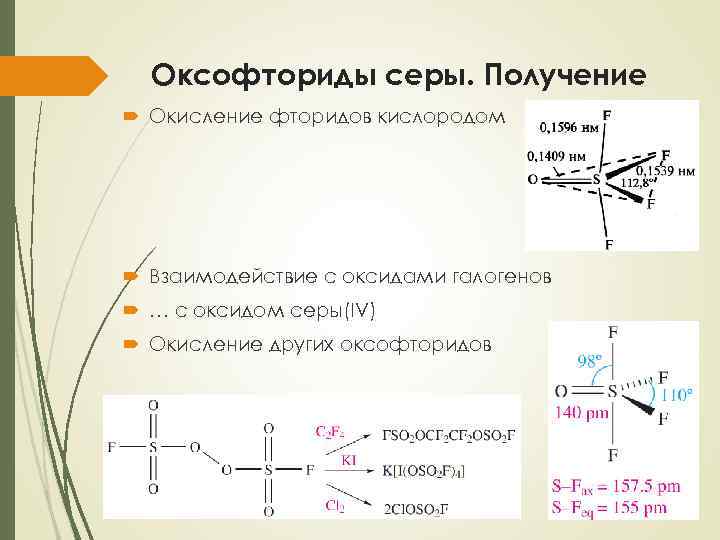 Оксофториды серы. Получение Окисление фторидов кислородом Взаимодействие с оксидами галогенов … с оксидом серы(IV) Окисление других оксофторидов
Оксофториды серы. Получение Окисление фторидов кислородом Взаимодействие с оксидами галогенов … с оксидом серы(IV) Окисление других оксофторидов
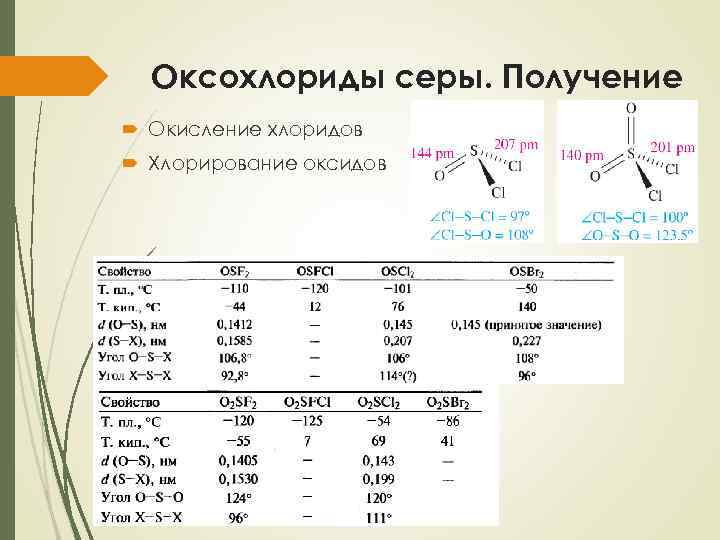 Оксохлориды серы. Получение Окисление хлоридов Хлорирование оксидов
Оксохлориды серы. Получение Окисление хлоридов Хлорирование оксидов
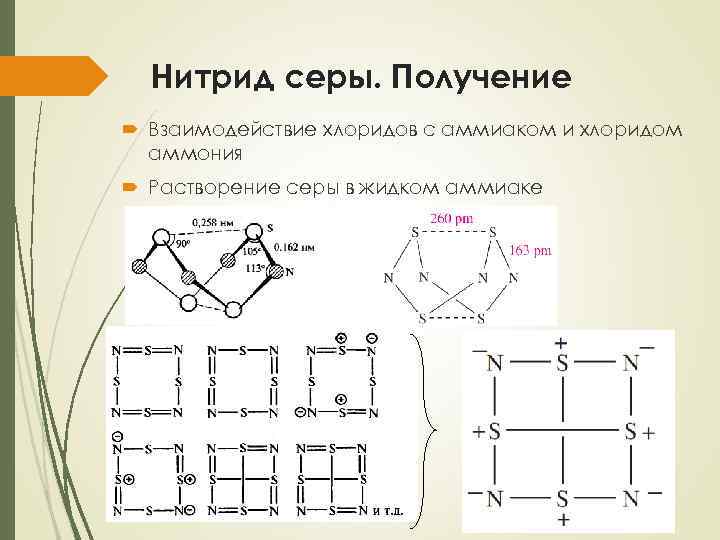 Нитрид серы. Получение Взаимодействие хлоридов с аммиаком и хлоридом аммония Растворение серы в жидком аммиаке
Нитрид серы. Получение Взаимодействие хлоридов с аммиаком и хлоридом аммония Растворение серы в жидком аммиаке
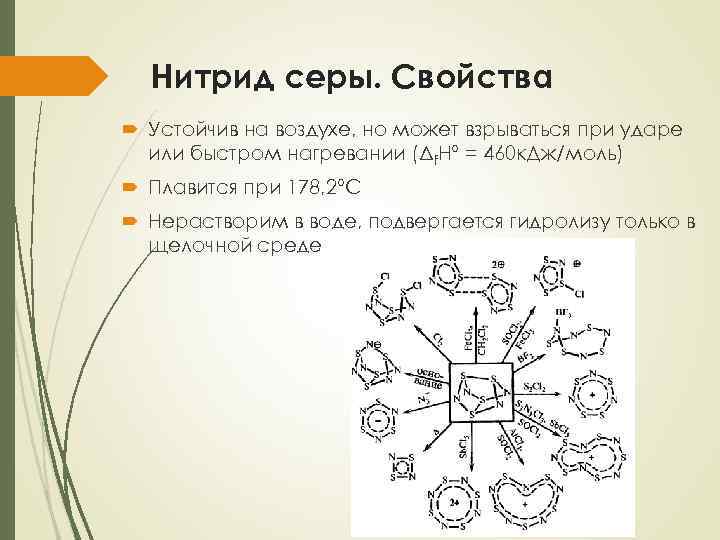 Нитрид серы. Свойства Устойчив на воздухе, но может взрываться при ударе или быстром нагревании (Δf. H° = 460 к. Дж/моль) Плавится при 178, 2°С Нерастворим в воде, подвергается гидролизу только в щелочной среде
Нитрид серы. Свойства Устойчив на воздухе, но может взрываться при ударе или быстром нагревании (Δf. H° = 460 к. Дж/моль) Плавится при 178, 2°С Нерастворим в воде, подвергается гидролизу только в щелочной среде
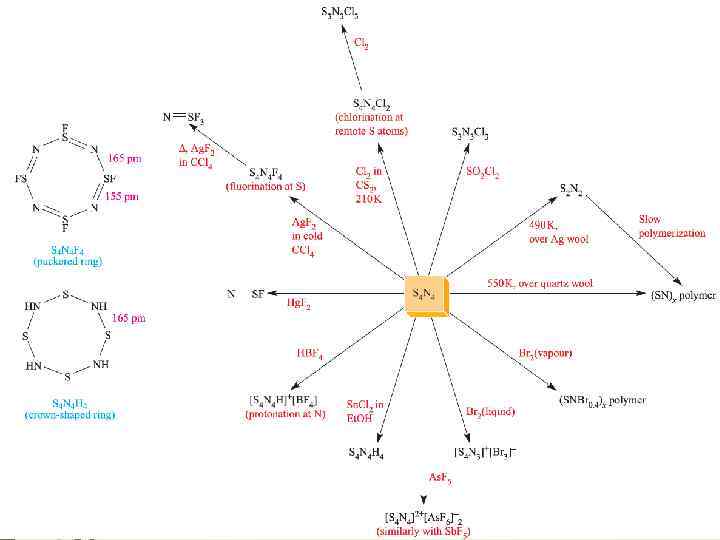
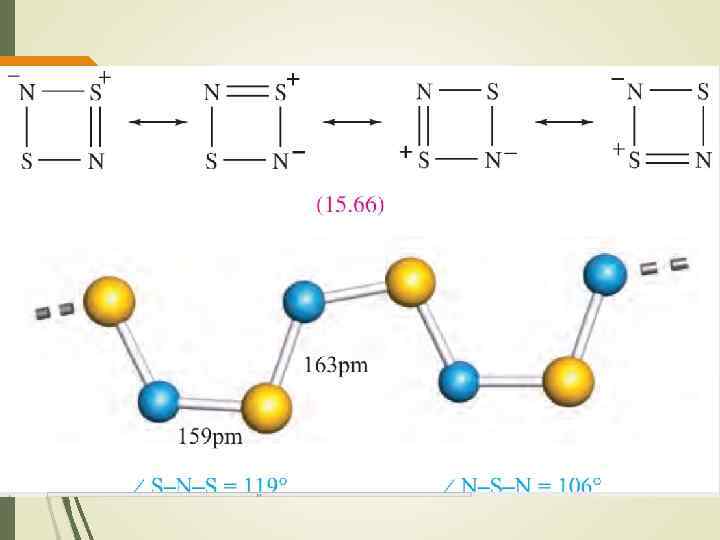
 Катионы серы
Катионы серы
 Пероксосерные кислоты Получаются при взаимодействии хлорсульфоновой кислоты с пероксидом водорода … при электролизе раствора серной кислоты (Г. Каро, 1898) Представляют собой кристаллические легкоплавкие вещества с т. пл. (H 2 SO 5) = 45°C, т. пл. (H 2 S 2 O 8) = 65°C Проявляют сильные окислительные свойства
Пероксосерные кислоты Получаются при взаимодействии хлорсульфоновой кислоты с пероксидом водорода … при электролизе раствора серной кислоты (Г. Каро, 1898) Представляют собой кристаллические легкоплавкие вещества с т. пл. (H 2 SO 5) = 45°C, т. пл. (H 2 S 2 O 8) = 65°C Проявляют сильные окислительные свойства
 Тиосерная кислота В водной среде быстро разлагается до серы, SO 2, H 2 Sn, H 2 SO 4 и т. д. Безводная кислота нестабильна и разлагается ниже 0°C Получается только в апротонных растворителях Хороший восстановитель
Тиосерная кислота В водной среде быстро разлагается до серы, SO 2, H 2 Sn, H 2 SO 4 и т. д. Безводная кислота нестабильна и разлагается ниже 0°C Получается только в апротонных растворителях Хороший восстановитель
 Ди- и политионовые кислоты Получают из дитионата бария Окисляются галогенами, перманганатом калия и др. до сульфатов Восстанавливаются (напр. , Na/Hg) до сульфитов и дитионитов В растворах разлагаются до тиосульфатов, сульфидов и т. д. Политионовые получаются в растворе Вакенродера (р-р H 2 S и SO 2) … при взаимодействии хлорсульфанов с гидросульфитами и гидротиосульфатами … при окислении тиосульфатов
Ди- и политионовые кислоты Получают из дитионата бария Окисляются галогенами, перманганатом калия и др. до сульфатов Восстанавливаются (напр. , Na/Hg) до сульфитов и дитионитов В растворах разлагаются до тиосульфатов, сульфидов и т. д. Политионовые получаются в растворе Вакенродера (р-р H 2 S и SO 2) … при взаимодействии хлорсульфанов с гидросульфитами и гидротиосульфатами … при окислении тиосульфатов


