Неорганические лекарственные средства Ca. Cl











































































 Неорганические лекарственные средства Ca. Cl 2*6 H 2 O Mg. SO 4*7 H 2 O Н 2 О 2 Hg. O Zn. SO 4*7 H 2 O Na 2 S 2 O 3*5 H 2 O
Неорганические лекарственные средства Ca. Cl 2*6 H 2 O Mg. SO 4*7 H 2 O Н 2 О 2 Hg. O Zn. SO 4*7 H 2 O Na 2 S 2 O 3*5 H 2 O
 Тема: II группа Периодической системы химических элементов им. Д. И. Менделеева. План: l Общая характеристика элементов II группы периодической системы. l Магния сульфат. l Кальция хлорид. l Цинка сульфат. l Ртути окись желтая.
Тема: II группа Периодической системы химических элементов им. Д. И. Менделеева. План: l Общая характеристика элементов II группы периодической системы. l Магния сульфат. l Кальция хлорид. l Цинка сульфат. l Ртути окись желтая.
 Общая характеристика II группы элементов периодической системы. Элементы главной подгруппы. n Входят щелочно-земельные металлы: бериллий, магний, кальций, стронций, барий, радий. n S-элементы, строение внешнего энергетического уровня – ns 2.
Общая характеристика II группы элементов периодической системы. Элементы главной подгруппы. n Входят щелочно-земельные металлы: бериллий, магний, кальций, стронций, барий, радий. n S-элементы, строение внешнего энергетического уровня – ns 2.
 Общая характеристика II группы элементов периодической системы. n Обладают ярко выраженными металлическими свойствами. n Растворимость и основной характер оснований возрастает от Ве к Ra.
Общая характеристика II группы элементов периодической системы. n Обладают ярко выраженными металлическими свойствами. n Растворимость и основной характер оснований возрастает от Ве к Ra.
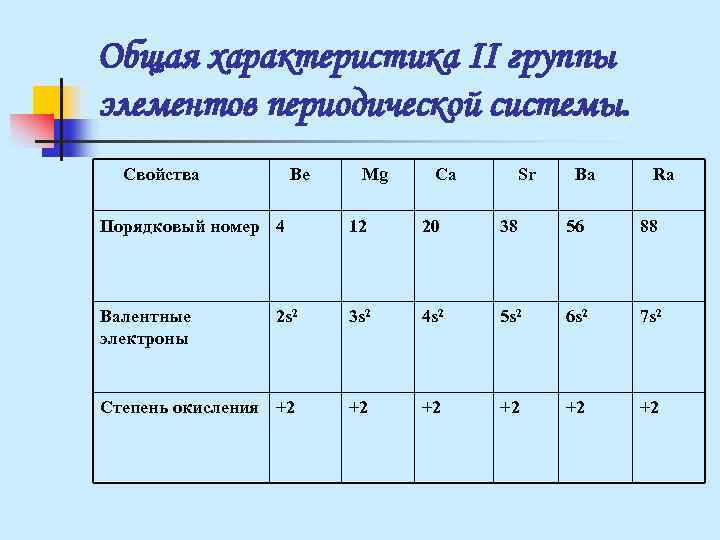
 Общая характеристика II группы элементов периодической системы. Свойства Be Mg Ca Sr Ba Ra Порядковый номер 4 12 20 38 56 88 Валентные 2 s 2 3 s 2 4 s 2 5 s 2 6 s 2 7 s 2 электроны Степень окисления +2 +2 +2
Общая характеристика II группы элементов периодической системы. Свойства Be Mg Ca Sr Ba Ra Порядковый номер 4 12 20 38 56 88 Валентные 2 s 2 3 s 2 4 s 2 5 s 2 6 s 2 7 s 2 электроны Степень окисления +2 +2 +2
 Общая характеристика II группы элементов периодической системы. Элементы побочной подгруппы. n Входят цинк, кадмий, ртуть. n d-элементы, строение внешнего энергетического уровня: d 10 s 2.
Общая характеристика II группы элементов периодической системы. Элементы побочной подгруппы. n Входят цинк, кадмий, ртуть. n d-элементы, строение внешнего энергетического уровня: d 10 s 2.
 Общая характеристика II группы элементов периодической системы n Металлические свойства ослабевают от цинка к ртути n Их гидроксиды нерастворимы воде и обладают слабоосновными свойствами.
Общая характеристика II группы элементов периодической системы n Металлические свойства ослабевают от цинка к ртути n Их гидроксиды нерастворимы воде и обладают слабоосновными свойствами.
 Общая характеристика II группы элементов периодической системы. Свойства Zn Cd Hg Порядковый номер 30 48 80 Валентные электроны 3 d 104 s 2 4 d 105 s 2 6 d 107 s 2 Степень окисления 0, +2 0, +1, +2
Общая характеристика II группы элементов периодической системы. Свойства Zn Cd Hg Порядковый номер 30 48 80 Валентные электроны 3 d 104 s 2 4 d 105 s 2 6 d 107 s 2 Степень окисления 0, +2 0, +1, +2
 Общая характеристика элементов. Магний. Нахождение в природе. n Широко распространен в природе, встречается в виде соединений: ● минерал доломит – Mg. CO 3*H 2 O ● минерал магнезит – Mg. CO 3 ● тальк – 3 Mg. O*4 Si. O 2*H 2 O
Общая характеристика элементов. Магний. Нахождение в природе. n Широко распространен в природе, встречается в виде соединений: ● минерал доломит – Mg. CO 3*H 2 O ● минерал магнезит – Mg. CO 3 ● тальк – 3 Mg. O*4 Si. O 2*H 2 O
 Общая характеристика элементов. Магний. Нахождение в природе. n Соли магния содержатся также в почве, в природных водах, особенно морской, и многих минеральных источниках.
Общая характеристика элементов. Магний. Нахождение в природе. n Соли магния содержатся также в почве, в природных водах, особенно морской, и многих минеральных источниках.
 Общая характеристика элементов. Магний. Нахождение в природе. n Пищевые источники: абрикосы, персики, цветная капуста, зерновые и бобовые культуры, орехи, отруби, свежие молочные и мясные продукты.
Общая характеристика элементов. Магний. Нахождение в природе. n Пищевые источники: абрикосы, персики, цветная капуста, зерновые и бобовые культуры, орехи, отруби, свежие молочные и мясные продукты.
 Общая характеристика элементов. Кальций. Нахождение в природе. Относится к распространенным элементам, содержание в земной коре составляет 3, 6 %. n Входит в состав зубной ткани, костей, нервной ткани, мышц, крови.
Общая характеристика элементов. Кальций. Нахождение в природе. Относится к распространенным элементам, содержание в земной коре составляет 3, 6 %. n Входит в состав зубной ткани, костей, нервной ткани, мышц, крови.
 Общая характеристика элементов. Кальций. Нахождение в природе. n Встречается в виде: ● отложений известняков, мрамора и мела – Са. СО 3 ● гидрокарбоната кальция – Са(НСО 3)2 ● гипса – Са. SO 4*2 H 2 O ●фосфорита – Са 3 РО 4
Общая характеристика элементов. Кальций. Нахождение в природе. n Встречается в виде: ● отложений известняков, мрамора и мела – Са. СО 3 ● гидрокарбоната кальция – Са(НСО 3)2 ● гипса – Са. SO 4*2 H 2 O ●фосфорита – Са 3 РО 4
 Общая характеристика элементов. Цинк. Нахождение в природе. n Встречается в виде минералов: ● галлия – Zn. CO 3 ● цинковой обманки – Zn. S.
Общая характеристика элементов. Цинк. Нахождение в природе. n Встречается в виде минералов: ● галлия – Zn. CO 3 ● цинковой обманки – Zn. S.
 Общая характеристика элементов. Цинк. Нахождение в природе. n Входит в состав мышечной, зубной и нервной ткани организма человека.
Общая характеристика элементов. Цинк. Нахождение в природе. n Входит в состав мышечной, зубной и нервной ткани организма человека.
 Общая характеристика элементов. Ртуть. Нахождение в природе n Ртуть представляет собой жидкий металл, напоминающий по блеску серебро, поэтому ее называли «серебряная вода» .
Общая характеристика элементов. Ртуть. Нахождение в природе n Ртуть представляет собой жидкий металл, напоминающий по блеску серебро, поэтому ее называли «серебряная вода» .
 Общая характеристика элементов. Ртуть. Нахождение в природе n Распространение в природе крайне невелико: ● в самородном виде, вкрапленная в горные породы.
Общая характеристика элементов. Ртуть. Нахождение в природе n Распространение в природе крайне невелико: ● в самородном виде, вкрапленная в горные породы.
 Общая характеристика элементов. Ртуть. Нахождение в природе ● в виде сульфида ртути ярко-красного цвета Hg. S – киноварь.
Общая характеристика элементов. Ртуть. Нахождение в природе ● в виде сульфида ртути ярко-красного цвета Hg. S – киноварь.
 Магния сульфат. Magnesii sulfas Mg. SO 4*7 H 2 O
Магния сульфат. Magnesii sulfas Mg. SO 4*7 H 2 O
 Магния сульфат. Впервые средство стало применяться в Англии. Первоначальное название горькая или английская соль, так как имеет солено- горький вкус.
Магния сульфат. Впервые средство стало применяться в Англии. Первоначальное название горькая или английская соль, так как имеет солено- горький вкус.
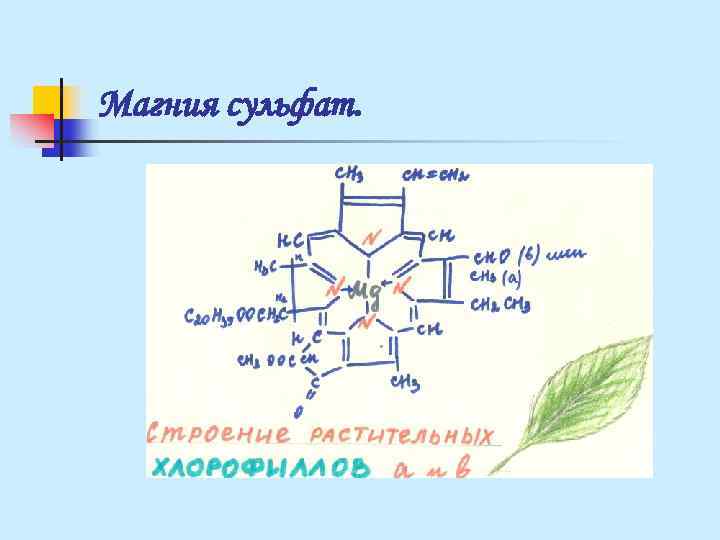
 Магния сульфат.
Магния сульфат.
 Магния сульфат. Получение. n Широко распространен в природе в виде кизерита Mg. SO 4*H 2 O 2(Mg. SO 4*7 H 2 O) - постоянный спутник каменной соли.
Магния сульфат. Получение. n Широко распространен в природе в виде кизерита Mg. SO 4*H 2 O 2(Mg. SO 4*7 H 2 O) - постоянный спутник каменной соли.
 Магния сульфат. Получение. n Получают из магнезита Mg. CO 3, обрабатывая его серной кислотой. Mg. CO 3 + H 2 SO 4 Mg. SO 4 + CO 2↑ + H 2 O Полученный раствор концентрируют упариванием до кристаллизации, при этом получается Mg. SO 4*7 H 2 O.
Магния сульфат. Получение. n Получают из магнезита Mg. CO 3, обрабатывая его серной кислотой. Mg. CO 3 + H 2 SO 4 Mg. SO 4 + CO 2↑ + H 2 O Полученный раствор концентрируют упариванием до кристаллизации, при этом получается Mg. SO 4*7 H 2 O.
 Магния сульфат. Описание. По внешнему виду сульфат магния представляет собой: n бесцветные призматические кристаллы n солено-горького вкуса
Магния сульфат. Описание. По внешнему виду сульфат магния представляет собой: n бесцветные призматические кристаллы n солено-горького вкуса
 Магния сульфат. Описание. n хорошо растворяется в воде n практически нерастворим в спирте n выветривается на воздухе.
Магния сульфат. Описание. n хорошо растворяется в воде n практически нерастворим в спирте n выветривается на воздухе.
 Магния сульфат. Подлинность. n Mg 2+: Mg. SO 4 + Na 2 HPO 4 + NH 4 OH Mg. NH 4 PO 4↓ + Na 2 SO 4 + H 2 O Выпадает белый кристаллический осадок, растворимый в уксусной кислоте. Условие: в присутствии хлорида аммония. (ГФ)
Магния сульфат. Подлинность. n Mg 2+: Mg. SO 4 + Na 2 HPO 4 + NH 4 OH Mg. NH 4 PO 4↓ + Na 2 SO 4 + H 2 O Выпадает белый кристаллический осадок, растворимый в уксусной кислоте. Условие: в присутствии хлорида аммония. (ГФ)
 Магния сульфат. Подлинность. n SO 42 -: Na 2 SO 4 + Ba. Cl 2 Ba. SO 4↓ + Na. Cl 2 Выпадает белый осадок, нерастворимый в кислотах и щелочах. (ГФ)
Магния сульфат. Подлинность. n SO 42 -: Na 2 SO 4 + Ba. Cl 2 Ba. SO 4↓ + Na. Cl 2 Выпадает белый осадок, нерастворимый в кислотах и щелочах. (ГФ)
 Магния сульфат. Количественное определение. Метод Комплексонометрия (Трилонометрия) n рабочий раствор Трилон Б n индикатор хромоген черный специальный n добавление аммиачного буферного раствора
Магния сульфат. Количественное определение. Метод Комплексонометрия (Трилонометрия) n рабочий раствор Трилон Б n индикатор хромоген черный специальный n добавление аммиачного буферного раствора
 Магния сульфат. Количественное определение. n титруют от красно-фиолетового до синего окрашивания раствора. Mg 2+ + H 2 Ind Mg. Ind + 2 H+ Mg. Ind + Na 2 H 2 Tp. Б Na 2 Mg. Tp. Б + H 2 Ind
Магния сульфат. Количественное определение. n титруют от красно-фиолетового до синего окрашивания раствора. Mg 2+ + H 2 Ind Mg. Ind + 2 H+ Mg. Ind + Na 2 H 2 Tp. Б Na 2 Mg. Tp. Б + H 2 Ind
 Магния сульфат. Применение. n Как спазмолитическое средство при гипертонической болезни в виде 25 % раствора (подкожно); n для обезболивания родов по 10– 20 мл 25 % раствора (внутримышечно);
Магния сульфат. Применение. n Как спазмолитическое средство при гипертонической болезни в виде 25 % раствора (подкожно); n для обезболивания родов по 10– 20 мл 25 % раствора (внутримышечно);
 Магния сульфат. Применение. n в качестве противосудорожного средства в тех же дозах, что и при обезболивании родов; n как желчегонное средство 20 -25 % раствор (внутрь);
Магния сульфат. Применение. n в качестве противосудорожного средства в тех же дозах, что и при обезболивании родов; n как желчегонное средство 20 -25 % раствор (внутрь);
 Магния сульфат. Применение. n в качестве слабительного средства по 15 - 30 г на прием внутрь; n оказывает успокаивающее действие на ЦНС: 9 -10 мг % - наступает снотворный эффект, при 15 -18 мг % - наркотическое состояние.
Магния сульфат. Применение. n в качестве слабительного средства по 15 - 30 г на прием внутрь; n оказывает успокаивающее действие на ЦНС: 9 -10 мг % - наступает снотворный эффект, при 15 -18 мг % - наркотическое состояние.
 Магния сульфат. Хранение. n Выпускается в порошке и ампулах, содержащих по 2, 5, 10 и 20 мл 25 % раствора. n Хранить препарат следует в небольших, хорошо закупоренных склянках с пробкой, залитых парафином, в сухом месте.
Магния сульфат. Хранение. n Выпускается в порошке и ампулах, содержащих по 2, 5, 10 и 20 мл 25 % раствора. n Хранить препарат следует в небольших, хорошо закупоренных склянках с пробкой, залитых парафином, в сухом месте.
 Кальция хлорид. Calcii chloridum Ca. Cl 2*6 H 2 O
Кальция хлорид. Calcii chloridum Ca. Cl 2*6 H 2 O
 Кальция хлорид. Пищевые источники: куриные яйца, гречневая и овсяная каша, горох, фасоль, орехи, семечки подсолнуха, апельсины, изюм, свекла, морковь, виноград, огурец, петрушка, капуста.
Кальция хлорид. Пищевые источники: куриные яйца, гречневая и овсяная каша, горох, фасоль, орехи, семечки подсолнуха, апельсины, изюм, свекла, морковь, виноград, огурец, петрушка, капуста.
 Кальция хлорид. Получение. Кальция хлорид получают обработкой карбоната кальция (мрамора) хлороводородной кислотой. Ca. CO 3 + 2 HCl Ca. Cl 2 + CO 2↑ + H 2 O
Кальция хлорид. Получение. Кальция хлорид получают обработкой карбоната кальция (мрамора) хлороводородной кислотой. Ca. CO 3 + 2 HCl Ca. Cl 2 + CO 2↑ + H 2 O
 Кальция хлорид. Получение. Образующийся диоксид углерода улетучивается, а из оставшейся воды выкристаллизовывается чистый хлорид кальция Ca. Cl 2*6 H 2 O.
Кальция хлорид. Получение. Образующийся диоксид углерода улетучивается, а из оставшейся воды выкристаллизовывается чистый хлорид кальция Ca. Cl 2*6 H 2 O.
 Кальция хлорид. Описание. Кальция хлорид представляет собой: n бесцветные призматические кристаллы n без запаха n горько-соленого вкуса
Кальция хлорид. Описание. Кальция хлорид представляет собой: n бесцветные призматические кристаллы n без запаха n горько-соленого вкуса
 Кальция хлорид. Описание. n очень легко растворим в воде, в 95 % спирте n гигроскопичный n на воздухе расплывается.
Кальция хлорид. Описание. n очень легко растворим в воде, в 95 % спирте n гигроскопичный n на воздухе расплывается.
 Кальция хлорид. Подлинность. n Са 2+: 1. Окрашивает бесцветное пламя горелки в кирпично-красный цвет. (ГФ)
Кальция хлорид. Подлинность. n Са 2+: 1. Окрашивает бесцветное пламя горелки в кирпично-красный цвет. (ГФ)
 Кальция хлорид. Подлинность. 2. С оксалатом аммония. (ГФ) Ca. Cl 2 + (NH 4)2 C 2 O 4 Ca. C 2 O 4↓ + 2 NH 4 Cl Выпадает белый мелкокристаллический осадок, легко растворимый в минеральных кислотах, нерастворимый в уксусной кислоте.
Кальция хлорид. Подлинность. 2. С оксалатом аммония. (ГФ) Ca. Cl 2 + (NH 4)2 C 2 O 4 Ca. C 2 O 4↓ + 2 NH 4 Cl Выпадает белый мелкокристаллический осадок, легко растворимый в минеральных кислотах, нерастворимый в уксусной кислоте.
 Кальция хлорид. Подлинность. Условие: 1) на холоду 2) нейтральная, слабоуксусная или слабощелочная среда.
Кальция хлорид. Подлинность. Условие: 1) на холоду 2) нейтральная, слабоуксусная или слабощелочная среда.
 Кальция хлорид. Подлинность. n Cl-: Ca. Cl 2 + 2 Ag. NO 3 2 Ag. Cl↓ + Ca(NO 3)2 Белый творожистый осадок, нерастворимый в разбавленной азотной кислоте, но растворим в растворе аммиака. Ag. Cl + 2 NH 4 OH Ag(NH 3)2 Cl + 2 H 2 O Условие: азотнокислая среда. (ГФ)
Кальция хлорид. Подлинность. n Cl-: Ca. Cl 2 + 2 Ag. NO 3 2 Ag. Cl↓ + Ca(NO 3)2 Белый творожистый осадок, нерастворимый в разбавленной азотной кислоте, но растворим в растворе аммиака. Ag. Cl + 2 NH 4 OH Ag(NH 3)2 Cl + 2 H 2 O Условие: азотнокислая среда. (ГФ)
 Кальция хлорид. Количественное определение. Метод Комплексонометрия n рабочий раствор Трилон Б n индикатор кислотный хром темно-синий
Кальция хлорид. Количественное определение. Метод Комплексонометрия n рабочий раствор Трилон Б n индикатор кислотный хром темно-синий
 Кальция хлорид. Количественное определение. n добавление аммиачного буферного раствора n титруем от красно-фиолетового до синего окрашивания раствора. Ca 2+ + H 2 Ind Ca. Ind + 2 H+ Ca. Ind + Na 2 H 2 Тр. Б Na 2 Ca. Тр. Б + H 2 Ind
Кальция хлорид. Количественное определение. n добавление аммиачного буферного раствора n титруем от красно-фиолетового до синего окрашивания раствора. Ca 2+ + H 2 Ind Ca. Ind + 2 H+ Ca. Ind + Na 2 H 2 Тр. Б Na 2 Ca. Тр. Б + H 2 Ind
 Кальция хлорид. Применение. Хранение. ● Хлорид кальция очень широко применяется в медицине: n как кровоостанавливающее средство при легочных, желудочно-кишечных, носовых и маточных кровотечениях; n в хирургической практике для повышения свертываемости крови;
Кальция хлорид. Применение. Хранение. ● Хлорид кальция очень широко применяется в медицине: n как кровоостанавливающее средство при легочных, желудочно-кишечных, носовых и маточных кровотечениях; n в хирургической практике для повышения свертываемости крови;
 Кальция хлорид. Применение. Хранение. n при аллергических заболеваниях (бронхиальная астма, крапивница) для снятия зуда; n в качестве противоядия при отравлении солями магния.
Кальция хлорид. Применение. Хранение. n при аллергических заболеваниях (бронхиальная астма, крапивница) для снятия зуда; n в качестве противоядия при отравлении солями магния.
 Кальция хлорид. Применение. Хранят кальция хлорид в небольших, хорошо закупоренных стеклянных банках с пробкой, залитых парафином, в сухом месте.
Кальция хлорид. Применение. Хранят кальция хлорид в небольших, хорошо закупоренных стеклянных банках с пробкой, залитых парафином, в сухом месте.
 Цинка сульфат. Zinci sulfas Zn. SO 4*7 H 2 O
Цинка сульфат. Zinci sulfas Zn. SO 4*7 H 2 O
 Цинка сульфат применялся в медицине с давних времен под названием белого купороса.
Цинка сульфат применялся в медицине с давних времен под названием белого купороса.
 Цинка сульфат. Пищевые источники: чеснок, лук, овсяные хлопья, субпродукты, рыба, яйца, мука грубого помола, грибы, сельдь, семена тыквы и подсолнечника.
Цинка сульфат. Пищевые источники: чеснок, лук, овсяные хлопья, субпродукты, рыба, яйца, мука грубого помола, грибы, сельдь, семена тыквы и подсолнечника.
 Цинка сульфат. Получение. n Цинка сульфат получают из природной руды – цинковой обманки, которую подвергают обжигу. 2 Zn. S + 3 O 2 2 Zn. O + 2 SO 2↑
Цинка сульфат. Получение. n Цинка сульфат получают из природной руды – цинковой обманки, которую подвергают обжигу. 2 Zn. S + 3 O 2 2 Zn. O + 2 SO 2↑
 Цинка сульфат. Получение. n Цинка оксид обрабатывают разбавленной серной кислотой, в результате образуется цинка сульфат в растворе. Zn. S + H 2 SO 4 Zn. SO 4 + H 2 O
Цинка сульфат. Получение. n Цинка оксид обрабатывают разбавленной серной кислотой, в результате образуется цинка сульфат в растворе. Zn. S + H 2 SO 4 Zn. SO 4 + H 2 O
 Цинка сульфат. Получение. n Раствор упаривают до кристаллизации соли в виде гептагидрата – Zn. SO 4*7 H 2 O
Цинка сульфат. Получение. n Раствор упаривают до кристаллизации соли в виде гептагидрата – Zn. SO 4*7 H 2 O
 Цинка сульфат. Описание. Цинка сульфат представляет собой: n бесцветные прозрачные кристаллы или мелкокристаллический порошок; n имеет вяжущий металлический вкус;
Цинка сульфат. Описание. Цинка сульфат представляет собой: n бесцветные прозрачные кристаллы или мелкокристаллический порошок; n имеет вяжущий металлический вкус;
 Цинка сульфат. Описание. n без запаха; n очень легко растворим в воде, медленно в глицерине, не растворимый в спирте; n на воздухе выветривается.
Цинка сульфат. Описание. n без запаха; n очень легко растворим в воде, медленно в глицерине, не растворимый в спирте; n на воздухе выветривается.
 Цинка сульфат. Подлинность. n Zn 2+: 1. C гексацианоферратом (II) калия. (ГФ) 3 Zn. SO 4 + 2 K 4 Fe(CN)6 K 2 Zn 3 Fe(CN)6 2↓ + 3 K 2 SO 4 Выпадает белый осадок, растворимый в щелочах и нерастворимый в кислотах.
Цинка сульфат. Подлинность. n Zn 2+: 1. C гексацианоферратом (II) калия. (ГФ) 3 Zn. SO 4 + 2 K 4 Fe(CN)6 K 2 Zn 3 Fe(CN)6 2↓ + 3 K 2 SO 4 Выпадает белый осадок, растворимый в щелочах и нерастворимый в кислотах.
 Цинка сульфат. Подлинность. 2. С сульфидом натрия. (ГФ) Zn. SO 4 + Na 2 S Zn. S↓ + Na 2 SO 4 Выпадает белый аморфный осадок, растворимый в концентрированной соляной кислоте. Условие: нейтральная среда.
Цинка сульфат. Подлинность. 2. С сульфидом натрия. (ГФ) Zn. SO 4 + Na 2 S Zn. S↓ + Na 2 SO 4 Выпадает белый аморфный осадок, растворимый в концентрированной соляной кислоте. Условие: нейтральная среда.
 Цинка сульфат. Подлинность. n SO 42 -: Zn. SO 4 + Ba. Cl 2 Ba. SO 4↓ + Zn. Cl 2 Выпадает белый осадок, нерастворимый в кислотах и щелочах. (ГФ)
Цинка сульфат. Подлинность. n SO 42 -: Zn. SO 4 + Ba. Cl 2 Ba. SO 4↓ + Zn. Cl 2 Выпадает белый осадок, нерастворимый в кислотах и щелочах. (ГФ)
 Цинка сульфат. Количественное определение. Метод Комплексонометрия n рабочий раствор Трилон Б n индикатор кислотный хром черный специальный n добавление аммиачного буферного раствора
Цинка сульфат. Количественное определение. Метод Комплексонометрия n рабочий раствор Трилон Б n индикатор кислотный хром черный специальный n добавление аммиачного буферного раствора
 Цинка сульфат. Количественное определение. n титруем то красно-фиолетового до синего окрашивания раствора. Zn 2+ + H 2 Ind Zn. Ind + 2 H+ Zn. Ind + Na 2 H 2 Тр. Б Na 2 Zn. Тр. Б + H 2 Ind
Цинка сульфат. Количественное определение. n титруем то красно-фиолетового до синего окрашивания раствора. Zn 2+ + H 2 Ind Zn. Ind + 2 H+ Zn. Ind + Na 2 H 2 Тр. Б Na 2 Zn. Тр. Б + H 2 Ind
 Цинка сульфат. Применение. Хранение. n Цинка сульфат применяется: ● наружно как антисептическое и вяжущее средство в глазной практике в виде 0, 1; 0, 25; 0, 5 % растворов;
Цинка сульфат. Применение. Хранение. n Цинка сульфат применяется: ● наружно как антисептическое и вяжущее средство в глазной практике в виде 0, 1; 0, 25; 0, 5 % растворов;
 Цинка сульфат. Применение. Хранение. ● в гинекологической практике для спринцевания в виде 0, 1 -0, 5 % раствора; ● редко назначается внутрь как рвотное средство
Цинка сульфат. Применение. Хранение. ● в гинекологической практике для спринцевания в виде 0, 1 -0, 5 % раствора; ● редко назначается внутрь как рвотное средство
 Цинка сульфат. Применение. Хранение. n Хранить следует с предосторожностью в хорошо закупоренных банках. Список Б.
Цинка сульфат. Применение. Хранение. n Хранить следует с предосторожностью в хорошо закупоренных банках. Список Б.
 Ртути окись желтая. Hydrargyri oxydum flavum Hg. O
Ртути окись желтая. Hydrargyri oxydum flavum Hg. O
 Ртути окись желтая. Латинское hydrargirum произошло от греческих слов «хюдор» - вода «аргирос» - серебро
Ртути окись желтая. Латинское hydrargirum произошло от греческих слов «хюдор» - вода «аргирос» - серебро
 Ртути окись желтая. Получение. Для получения ртути окиси желтой используют реакции осаждения ее из растворимых солей ртути.
Ртути окись желтая. Получение. Для получения ртути окиси желтой используют реакции осаждения ее из растворимых солей ртути.
 Ртути окись желтая. Получение. В разбавленный раствор щелочи медленно вливают концентрированный раствор соли ртути. Hg(NO 3)2 + 2 Na. OH 2 Na. NO 3 + Hg. O↓ + H 2 O Выпадает осадок оксида ртути ярко- желтого цвета.
Ртути окись желтая. Получение. В разбавленный раствор щелочи медленно вливают концентрированный раствор соли ртути. Hg(NO 3)2 + 2 Na. OH 2 Na. NO 3 + Hg. O↓ + H 2 O Выпадает осадок оксида ртути ярко- желтого цвета.
 Ртути окись желтая. Получение. Условие: реакция проводится в темноте, так как может образоваться закись ртути Hg 2 O черного цвета.
Ртути окись желтая. Получение. Условие: реакция проводится в темноте, так как может образоваться закись ртути Hg 2 O черного цвета.
 Ртути окись желтая. Описание. Ртути окись желтая представляет собой: n тяжелый мелкодисперсный порошок желтого или оранжево-желтого цвета; n в воде нерастворим, но легко растворим в кислотах; n на свету темнеет.
Ртути окись желтая. Описание. Ртути окись желтая представляет собой: n тяжелый мелкодисперсный порошок желтого или оранжево-желтого цвета; n в воде нерастворим, но легко растворим в кислотах; n на свету темнеет.
 Ртути окись желтая. Подлинность. n Hg 2+: Ртути окись обрабатывают разведенной хлороводородной кислотой, чтобы получить растворимую соль ртути. Hg. O + 2 HCl Hg. Cl 2 + H 2 O
Ртути окись желтая. Подлинность. n Hg 2+: Ртути окись обрабатывают разведенной хлороводородной кислотой, чтобы получить растворимую соль ртути. Hg. O + 2 HCl Hg. Cl 2 + H 2 O
 Ртути окись желтая. Подлинность. 1. C растворами щелочей. (ГФ) Hg. Cl 2 + 2 Na. OH Hg. O↓ + 2 Na. Cl + H 2 O Выпадает осадок желтого цвета, растворимый в кислотах.
Ртути окись желтая. Подлинность. 1. C растворами щелочей. (ГФ) Hg. Cl 2 + 2 Na. OH Hg. O↓ + 2 Na. Cl + H 2 O Выпадает осадок желтого цвета, растворимый в кислотах.
 Ртути окись желтая. Подлинность. 2. С раствором йодида калия. (ГФ) Hg. Cl 2 + 2 KIнедост Hg. I 2↓ + 2 KCl Выпадает осадок красного цвета, растворимый в избытке калия йодида. Hg. I 2 + 2 KI K 2 Hg. I 4
Ртути окись желтая. Подлинность. 2. С раствором йодида калия. (ГФ) Hg. Cl 2 + 2 KIнедост Hg. I 2↓ + 2 KCl Выпадает осадок красного цвета, растворимый в избытке калия йодида. Hg. I 2 + 2 KI K 2 Hg. I 4
 Ртути окись желтая. Количественное определение. Метод Нейтрализация n рабочий раствор хлороводородная кислота n индикатор м/o или м/к
Ртути окись желтая. Количественное определение. Метод Нейтрализация n рабочий раствор хлороводородная кислота n индикатор м/o или м/к
 Ртути окись желтая. Количественное определение. n титруют от желтого до красного окрашивания раствора. Hg. O + 4 KCl + H 2 O K 2 Hg. I 4 + 2 KOH + HCl KCl + H 2 O
Ртути окись желтая. Количественное определение. n титруют от желтого до красного окрашивания раствора. Hg. O + 4 KCl + H 2 O K 2 Hg. I 4 + 2 KOH + HCl KCl + H 2 O
 Ртути окись желтая. Применение. Хранение. n Желтая окись ртути применяется ● как нежное антисептическое и противовоспалител ьное средство для приготовления глазных мазей.
Ртути окись желтая. Применение. Хранение. n Желтая окись ртути применяется ● как нежное антисептическое и противовоспалител ьное средство для приготовления глазных мазей.
 Ртути окись желтая. Применение. Хранение. n Хранить следует с предосторожностью в хорошо закупоренных банках из темного стекла, так как на свету может образоваться закись ртути, что обнаруживается по потемнению препарата. Список Б.
Ртути окись желтая. Применение. Хранение. n Хранить следует с предосторожностью в хорошо закупоренных банках из темного стекла, так как на свету может образоваться закись ртути, что обнаруживается по потемнению препарата. Список Б.

