неметаллы.ppt
- Количество слайдов: 38

Неметаллы: общая характеристика.


Положение неметаллов в ПСХЭ Строение атомов Строение простых веществ: вид химической связи и тип кристаллической решетки Физические свойства: агрегатное состояние, цвет и др. Химические свойства Водородные соединения неметаллов Кислородные соединения Применение

Неметаллы – химические элементы, для атомов которых характерна способность принимать электроны до завершения внешнего слоя благодаря наличию 4 и более электронов и малому атомному радиусу по сравнению с металлами.
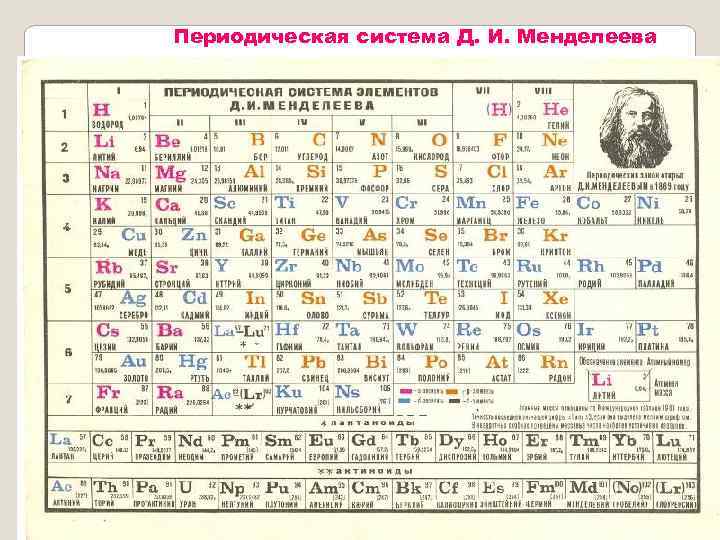
Периодическая система Д. И. Менделеева

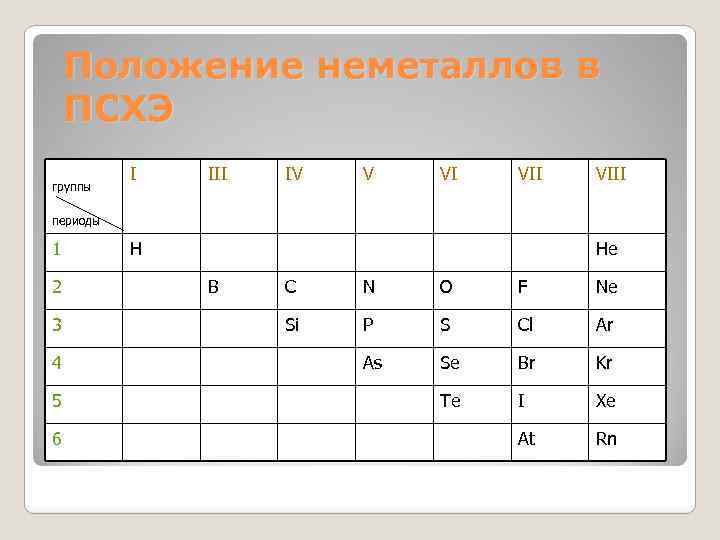
Положение неметаллов в ПСХЭ группы I III IV V VI VIII периоды 1 2 3 4 5 6 H He B C N O F Ne Si P S Cl Ar As Se Br Kr Te I Xe At Rn
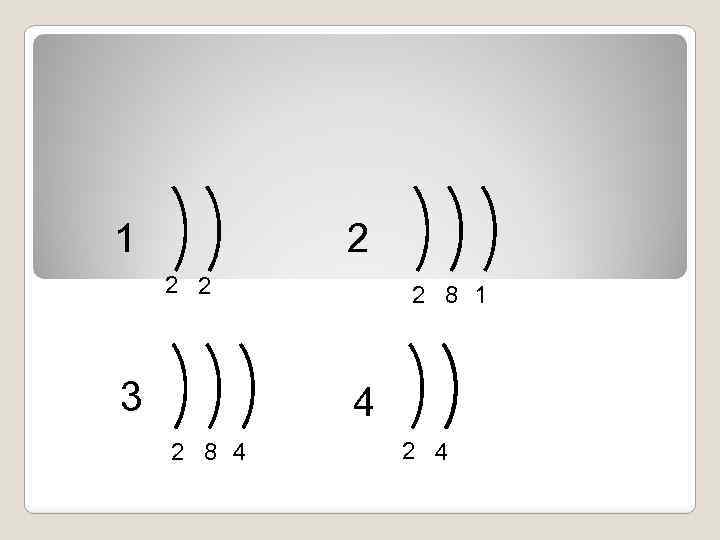
1 2 2 2 3 2 8 1 4 2 8 4 2 4

Небольшой атомный радиус На внешнем уровне 4 -8 электронов Характерно высокое значение ЭО Являются окислителями

Электронная формула атомов неметаллов
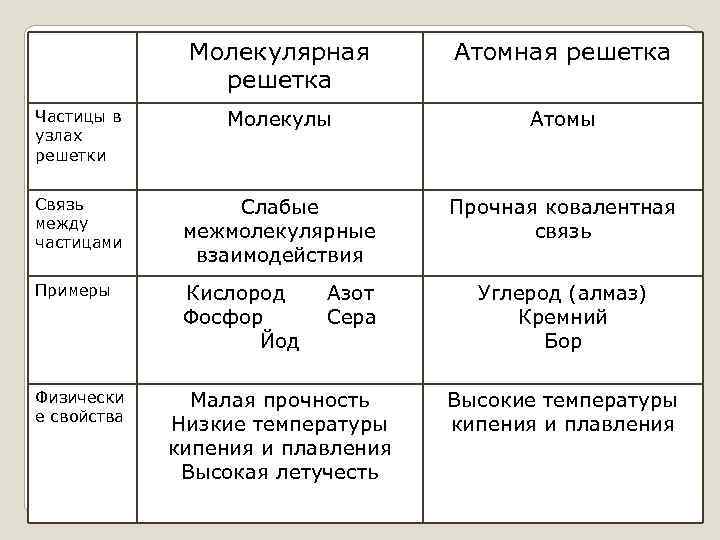
Молекулярная решетка Атомная решетка Частицы в узлах решетки Молекулы Атомы Связь между частицами Слабые межмолекулярные взаимодействия Прочная ковалентная связь Примеры Кислород Фосфор Йод Физически е свойства Азот Сера Малая прочность Низкие температуры кипения и плавления Высокая летучесть Углерод (алмаз) Кремний Бор Высокие температуры кипения и плавления Типы кристаллических решеток

ФИЗИЧЕСКИЕ СВОЙСТВА ПРОСТЫХ ВЕЩЕСТВ

Цвет простых веществ - неметаллов

КРАСНЫЙ ФОСФОР БЕСЦВЕТНЫЙ ЖЕЛТЫЙ ФИОЛЕТОВЫЙ СЕРА ЙОД УГЛЕРОД

ЧЕРНЫЙ БЕЛЫЙ ФОСФОР ГРАФИТ ФОСФОР ЖЕЛТО-ЗЕЛЕНЫЙ ХЛОР
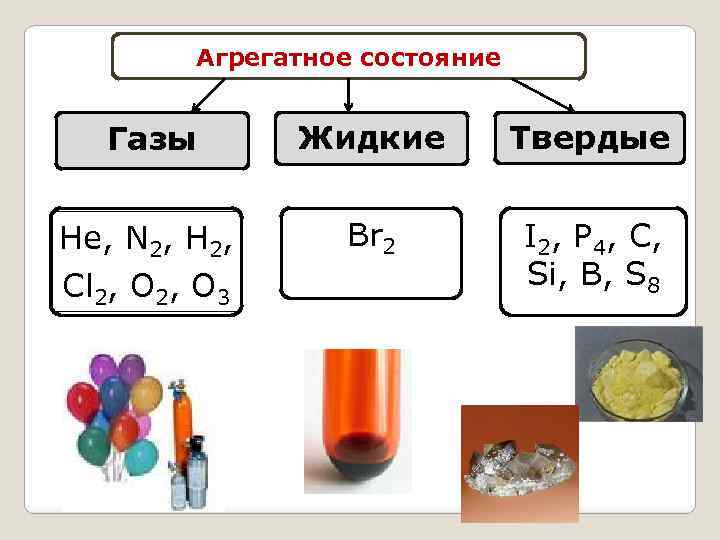
Агрегатное состояние Газы Не, N 2, Н 2, Cl 2, O 3 Жидкие Твердые Br 2 I 2, P 4, C, Si, B, S 8
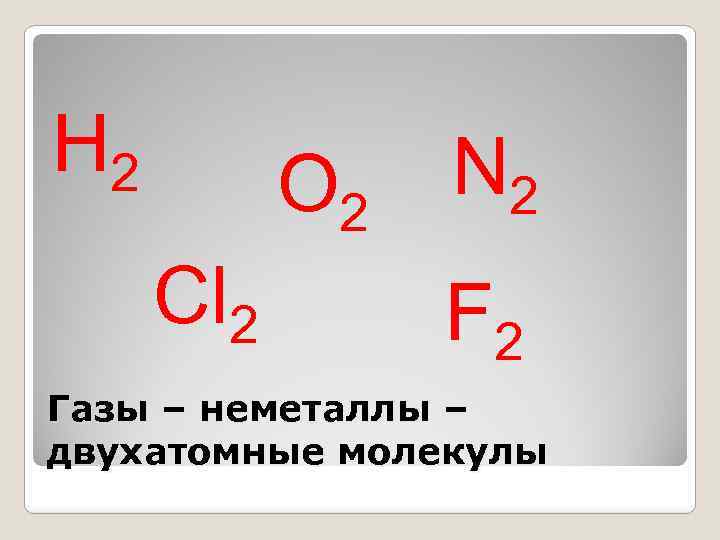
Н 2 О 2 Cl 2 N 2 F 2 Газы – неметаллы – двухатомные молекулы

3 8000 С – у графита - 2100 С - азота Температура плавления

ЧЕГО БОЛЬШЕ: ХИМИЧЕСКИХ ЭЛЕМЕНТОВ ИЛИ ПРОСТЫХ ВЕЩЕСТВ

Способность атомов одного химического элемента образовывать несколько простых веществ называют аллотропией, а эти простые вещества – аллотропными видоизменениями или модификациями

Разное типы кристаллических решеток Р - фосфор Красный фосфор - атомная Белый фосфор - молекулярная
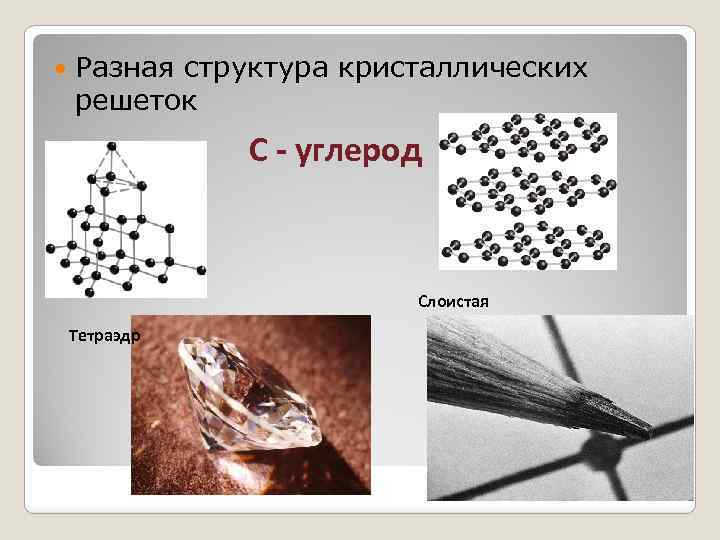
Разная структура кристаллических решеток С - углерод Слоистая Тетраэдр

Разный состав молекул О - кислород Кислород Озон

Задерживает ультрафиолетовые лучи, которые разрушительно действуют на клетки живых организмов • Озоновый слой расположен на высоте 20 – 25 км • Значение озона для Земли

Светло - синий газ с сильным запахом Имеет запах свежести Появляется после грозы Озон О 3

Содержится в воздухе сосновых лесов и морского побережья Озон в природе

Получают в специальных приборах – озонаторах при действии на кислород электрическим разрядом без искр Получение озона в лаборатории

В конце 18 века А-Л. Лавуазье установил, что воздух – не простое вещество. а смесь газов

Состав воздуха

• Азот • Кислород • Благородные газы Постоянные составные воздуха

Углекислый газ Водяные пары Озон Переменные составные воздуха

Пыль Микроорганизмы Пыльца растений Оксиды серы и азота Случайные составные воздуха
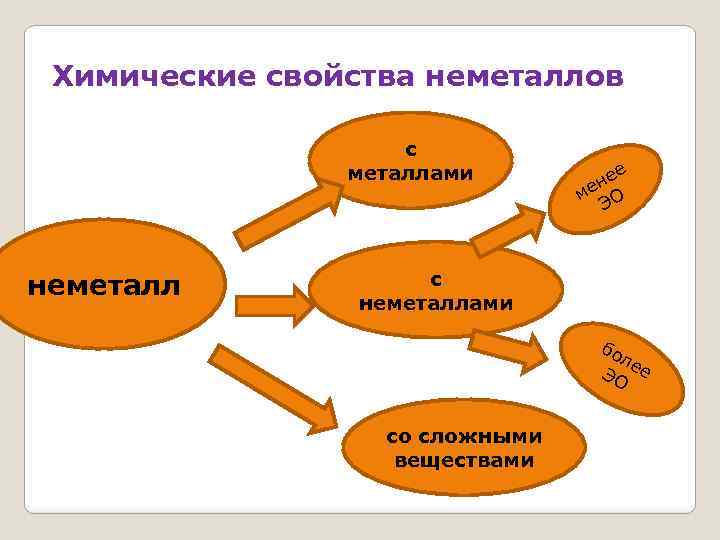
Химические свойства неметаллов с металлами неметалл е не ме О Э с неметаллами бо ле ЭО е со сложными веществами

Характерными для большинства неметаллов являются окислительные свойства. Как окислители они реагируют с металлами: Ca + Cl 2 = Ca. Cl 2 4 Li + O 2 = 2 Li 2 O 2 Na + S = Na 2 S

с неметаллами: H 2 + S = H 2 S P 4 + 5 O 2 = 2 P 2 O 5 2 P + 5 Cl 2 = 2 PCl 5 со сложными веществами: 2 Fe. Cl 2 + Cl 2 = 2 Fe. Cl 3 СН 4 + Cl 2 =СН 3 Cl+НCl

ВАРИАНТ 1 ВАРИАНТ -2 1 - А 2 - Б 3 – В 4 – Б 5 - А


ДОМАШНЕЕ ЗАДАНИЕ стр. 226 - 236, упр. 1 -4 устно, упр. 5 (1 -5) письменно презентации «Распространение неметаллов в природе» «Биологическая роль неметаллов» «Применение неметаллов»
неметаллы.ppt