ФУВ_нейропротекция.ppt
- Количество слайдов: 124

Нейропротективная терапия при церебральном инсульте И. М. Шетова Кафедра фундаментальной и клинической неврологии РГМУ Зав. кафедрой – чл. корр. РАМН, профессор В. И. Скворцова
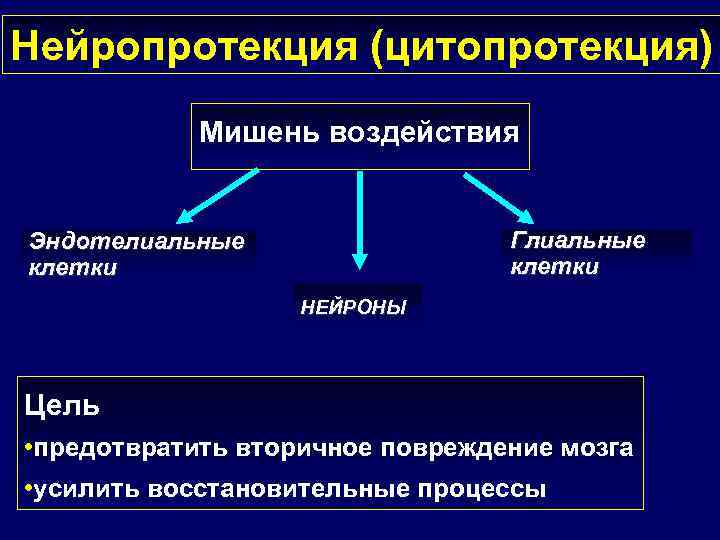
Нейропротекция (цитопротекция) Мишень воздействия Глиальные клетки Эндотелиальные клетки НЕЙРОНЫ Цель • предотвратить вторичное повреждение мозга • усилить восстановительные процессы

Система оказания помощи больному с инсультом 1. Быстрая диагностика ОНМК 2. Немедленный вызов и госпитализация при помощи СМП 3. Транспортировка с уведомлением принимающей больницы (п/о, БИТ) 4. Приоритет больным с инсультом <3 часов 5. Пациенты с инсультом должны лечиться в инсультных отделениях (уровень I). 6. Пациенты с субарахноидальным кровоизлиянием должны быть госпитализированы в центр с возможностями для нейрохирургического лечения (уровень I).

Отделения для больных с инсультом Инсультные отделения - летальности на 18%, -сокращение смертности или инвалидизации, а также сокращение смертности или потребности в стационарной помощи по сравнению с общим отделением (уровень I) -сокращение смертности от всех причин на 3№ (NNT 33), -3%-ное сокращение потребности в сестринской помощи на дому -увеличение числа неинвалидизированных выживших на 6% (NNT 16).
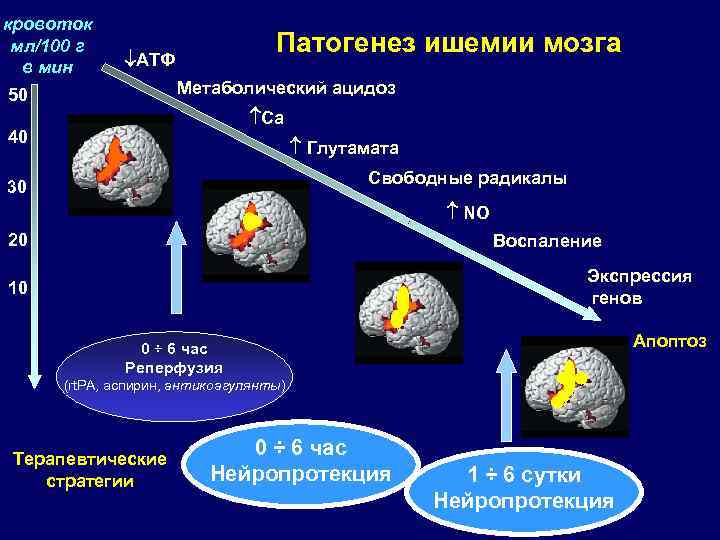
кровоток мл/100 г в мин Патогенез ишемии мозга АТФ Метаболический ацидоз 50 Ca 40 Глутамата Свободные радикалы 30 NO 20 Воспаление Экспрессия генов 10 Апоптоз 0 ÷ 6 час Реперфузия (rt. PA, аспирин, антикоагулянты) Терапевтические стратегии 0 ÷ 6 час Нейропротекция 1 ÷ 6 сутки Нейропротекция
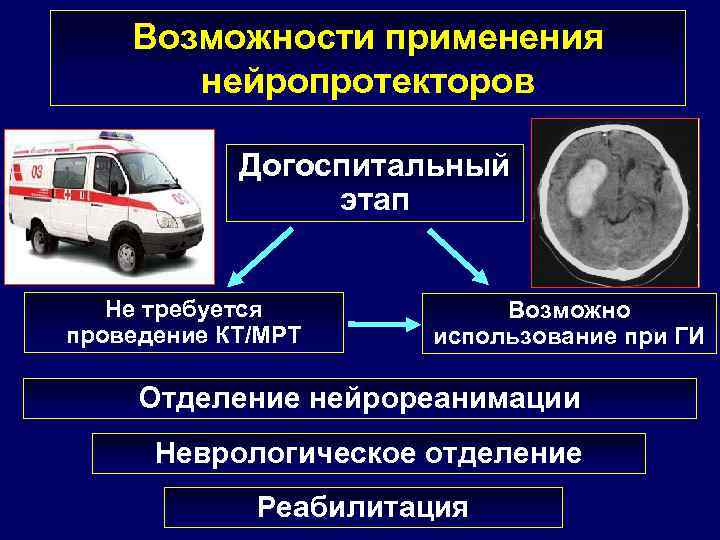
Возможности применения нейропротекторов Догоспитальный этап Не требуется проведение КТ/МРТ Возможно использование при ГИ Отделение нейрореанимации Неврологическое отделение Реабилитация

Основные принципы ведения больных в остром периоде инсульта 1. Базисная терапия (мониторинг функций дыхательной и ССС; контроль гликемии и температуры тела) 2. Реперфузия (rt-PA, аспирин, гепарин) 3. Нейропротекция: первичная (с первых минут в течение 3 дней) вторичная (с 3 -6 часа в течение 7 – 10 дней) 4. Вторичная профилактика 5. Мультидисциплинарная реабилитация
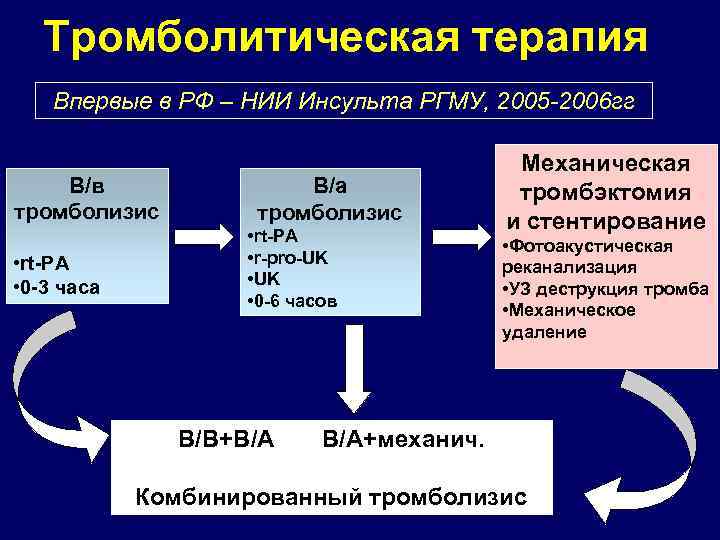
Тромболитическая терапия Впервые в РФ – НИИ Инсульта РГМУ, 2005 -2006 гг В/в тромболизис • rt-PA • 0 -3 часа В/а тромболизис • rt-PA • r-pro-UK • 0 -6 часов В/В+В/А Механическая тромбэктомия и стентирование • Фотоакустическая реканализация • УЗ деструкция тромба • Механическое удаление В/А+механич. Комбинированный тромболизис

Ожидаемые положительные эффекты нейропротективной терапии • Возможность применения на догоспитальном этапе (до КТ, МРТ) - внутри «терапевтического окна» • Увеличение удельного веса ТИА и «малых» инсультов в структуре ОНМК • Уменьшение размеров инфаркта мозга • Удлинение «терапевтического окна» с расширением возможностей для тромболизиса • Защита от реперфузионной травмы

Ограничения проведенных испытаний нейропротекторов (Joachim Rother, 2008 Stroke; 39: 523 -524) • позднее назначение (> 6 часов) • отсутствие доказательств проникновения препарата через ГЭБ • «недифференцированный» подход к выбору (критерии TOAST, локализация и объем ишемии) • отсутствие полного соответствия ответа генома экспериментальных животных и человека на ишемию • использование «грубых» клинических шкал • отсутствие изучения концентрации исследуемого препарата в плазме • современные исследования зачастую не слепые и не рандомизированные

Ограничения проведенных испытаний нейропротекторов (Joachim Rother, 2008 Stroke; 39: 523 -524) I. Позднее начало терапии • Запуск патобиохимического каскада в первые минуты-часы от индукции ишемии • Возможность применения нейропротекторов на догоспитальном этапе • Возможность (необходимость) применения при геморрагическом инсульте • Сложность контроля эффективности нейропротектора на догоспитальном этапе

Ограничения проведенных испытаний нейропротекторов (Joachim Rother, 2008 Stroke; 39: 523 -524) II. Отсутствие доказательств проникновения препарата через ГЭБ • Большинство нейротрофических факторов не проникают через ГЭБ • Нет возможности контроля проникновения нейропротектора через ГЭБ и измерения его концентрации в крови
Ограничения проведенных испытаний нейропротекторов (Joachim Rother, 2008 Stroke; 39: 523 -524) III. Несоответствие ответа генома экспериментальных животных и человека на ишемию • Геном человека на 80% соответствует геному экспериментальных животных; • ОДНАКО! Не учитываются возможные различия в ответе генома человека и животных на ишемию

Ограничения проведенных испытаний нейропротекторов (Joachim Rother, 2008 Stroke; 39: 523 -524) II. Отсутствие доказательств проникновения препарата через ГЭБ • Большинство нейротрофических факторов не проникают через ГЭБ • Нет возможности контроля проникновения нейропротектора через ГЭБ и измерения его концентрации в крови
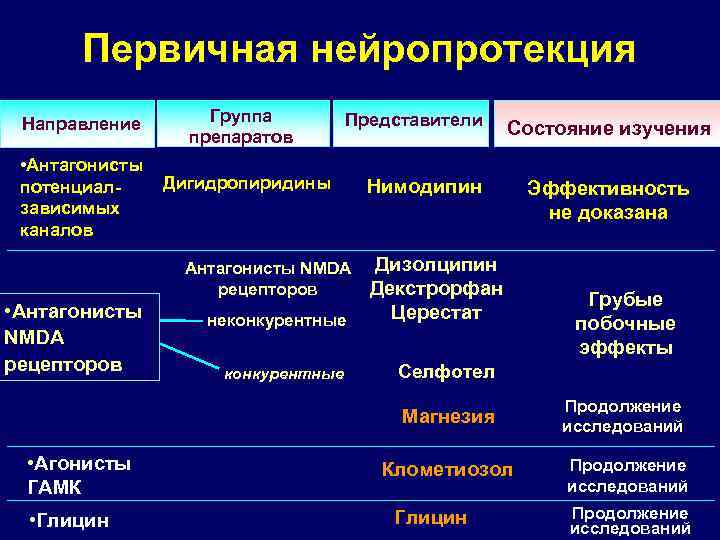
Первичная нейропротекция Направление • Антагонисты потенциалзависимых каналов Группа препаратов Представители Дигидропиридины Антагонисты NMDA рецепторов • Антагонисты NMDA рецепторов неконкурентные Состояние изучения Нимодипин Дизолципин Декстрорфан Церестат Эффективность не доказана Грубые побочные эффекты Селфотел Магнезия • Агонисты ГАМК • Глицин Продолжение исследований Клометиозол Продолжение исследований Глицин Продолжение исследований

I. Антагонисты кальциевых каналов • концепция «кальциевой гибели» клетки • воздействие на потенциал-зависимые Ca каналы • более 20 рандомизированных плацебоконтролируемых исследований • использование дигидропиридинов

I. Антагонисты кальциевых каналов • Доказана эффективность при САК НИМОДИПИН • 29 исследований при ишемическом инсульте • Побочный эффект – ГИПОТЕНЗИЯ • Эффективность при ИИ не доказана НИКАРДИПИН • Побочный эффект – ГИПОТЕНЗИЯ • Эффективность при ИИ не доказана

II. Антагонисты глутаматных рецепторов • N-methyl-d-aspartate (NMDA) рецепторы – первая мишень воздействия при ИИ • Конкурентные NMDA-антагонисты связываются напрямую с глутаматным сайтом NMDAрецептора, игнибируя действие глутамата • Неконкурентные NMDA-антагониты блокируют NMDAассоциированные ионные каналы

II. Антагонисты глутаматных рецепторов • Конкурентный антагонист NMDA рецепторов • Показана эфф. и безопасность в 2 А фазе СЕЛФОТЕЛ • Ускорение восстановления неврологических функций (95% vs. 29%) • Побочные эффекты в дозе >2 мг/кг • Галлюцинации, делирий, дизартрия, атаксия • Неконкурентный антагонист NMDA рецепторов • Уменьшение размера инфаркта на 70% в ЦЕРЕСТАТ эксперименте • Выраженные побочные эффекты при назначении адекватных доз

II. Антагонисты глутаматных рецепторов. МАГНЕЗИЯ • Исследована более чем у 3000 больных с ИИ • доступность • удобный путь введения • проникновение через ГЭБ • безопасность
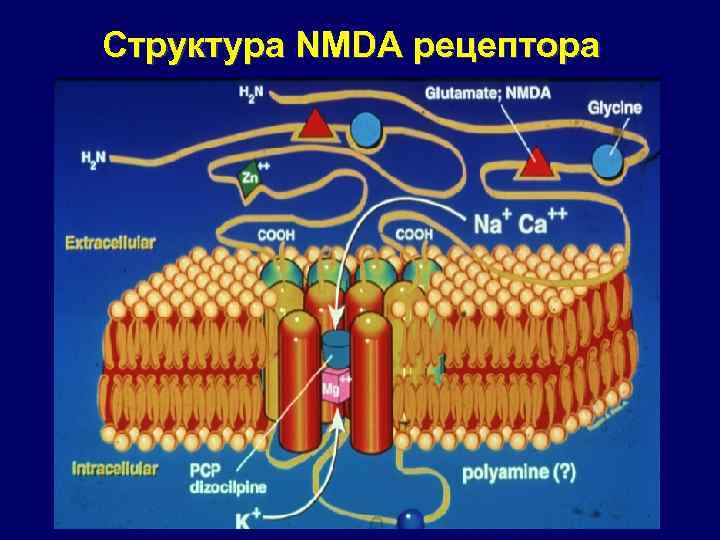
Структура NMDA рецептора

Исследование магнезии в экспериментальных условиях • дозо-зависимый эффект • уменьшение объема инфаркта • отсутствие побочных эффектов

Применение магнезии в остром периоде инсульта Мультицентровое исследование IMAGES (69 центров) 386 больных в острейшем (первые 12 часов) периоде каротидного ишемического инсульта 16 ммоль Mg. SO 4 – болюс (15 мин) 65 ммоль Mg. SO 4 - в течение суток • Безопасность • Отсутствие значимых побочных эффектов • Снижение показателей летальности и тяжелой инвалидизации при лакунарном инсульте

FAST – MAG Study Los-Angeles Prehospital Stroke Screen • 20 пациентов с симптомами инсульта • средний возраст 74 года • 4 г Mg. SO 4 на догоспитальном этапе + 16 г в течение суток 80% - ИИ 20% - ГИ Среднее время начала терапии = 100 минут 70% больных получали терапию в течение первых 2 ч Jeffrey L. , et al. FAST-MAG Pilot Trial/ Stroke, 2004
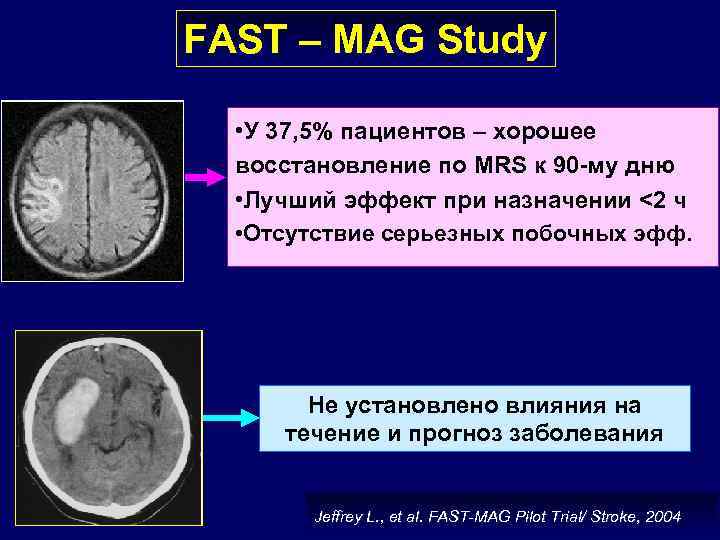
FAST – MAG Study • У 37, 5% пациентов – хорошее восстановление по MRS к 90 -му дню • Лучший эффект при назначении <2 ч • Отсутствие серьезных побочных эфф. Не установлено влияния на течение и прогноз заболевания Jeffrey L. , et al. FAST-MAG Pilot Trial/ Stroke, 2004

Средства, опосредованно воздействующие на NMDA-рецепторы ЭЛИПРОДИЛ ГАВЕСТИНЕЛ • антагонист • Антагонист глицинового полиаминового сайта NMDA • 2 крупных рандомизированных • 3 испытания у больных с исследования (1367 и 1804 инсультом больных ) • высокий риск побочных • Комбинация с rt. PA явлений • Эффект не доказан

Модуляторы нейротрансмиттерных систем АНТАГОНИСТЫ СЕРОТОНИНА • Воздействие на пре- и постсинаптические рецепторы • Гиперполяризация мембраны • Блокирование высвобождения глутамата • Угнетение апоптоза тразодон репинотан ONO-2506 6 часов Эффективность не доказана!

Эффекты Глицина Тормозное нейротрансмиттерное действие – уменьшение дисбаланса между возбуждающими и тормозными нейротрансмиттерными системами Общие метаболические эффекты – универсальный конъюгат низкомолекулярных токсичных соединений –продуктов ишемического каскада Williams R. New York 1963; 368 -404. Lavretskaya E. F. Moscow 1985; 1 -55.
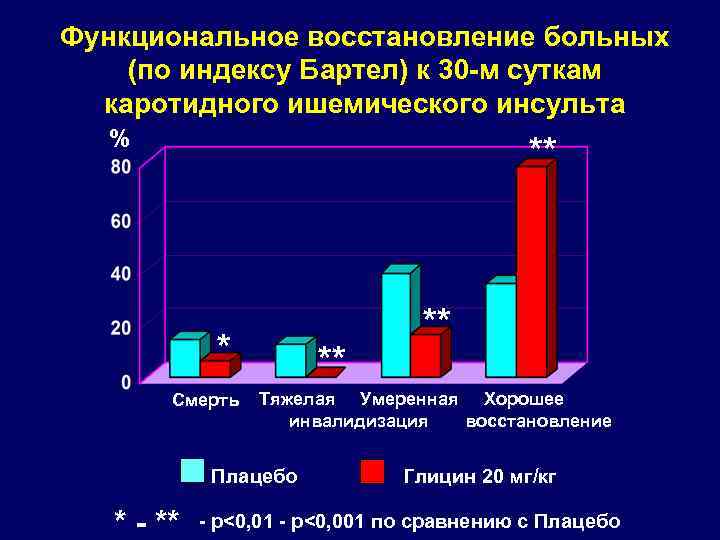
Функциональное восстановление больных (по индексу Бартел) к 30 -м суткам каротидного ишемического инсульта % ** * Смерть ** Тяжелая Умеренная Хорошее инвалидизация восстановление Плацебо * - ** ** Глицин 20 мг/кг - р<0, 01 - p<0, 001 по сравнению с Плацебо

Первичная нейропротекция. ВЫВОДЫ. • широкий спектр побочных эффектов большинства антагонистов Ca каналов и NMDA-рецепторов • неадекватные дозы • позднее начало терапии • наиболее перспективные препараты: Mg. SO 4 и глицин • целесообразна разработка комбинированных препаратов

Вторичная нейропротекция Направление • Антиоксиданты Группа препаратов Представители Состояние изучения Тирилозад Эффективность не доказана «Ловушки» свободных радикалов Блокаторы NOs Селенорганические соединения • Торможение местного воспаления • Улучшение трофического обеспечения АТ к м-лам межклеточной адгезии Нейротрофические факторы 7 -нитроиндазол Эбселен Доклинические исследования Продолжение исследований Энлимомаб Грубые побочные эффекты BDNF b. FGF IGF Доклинические исследования
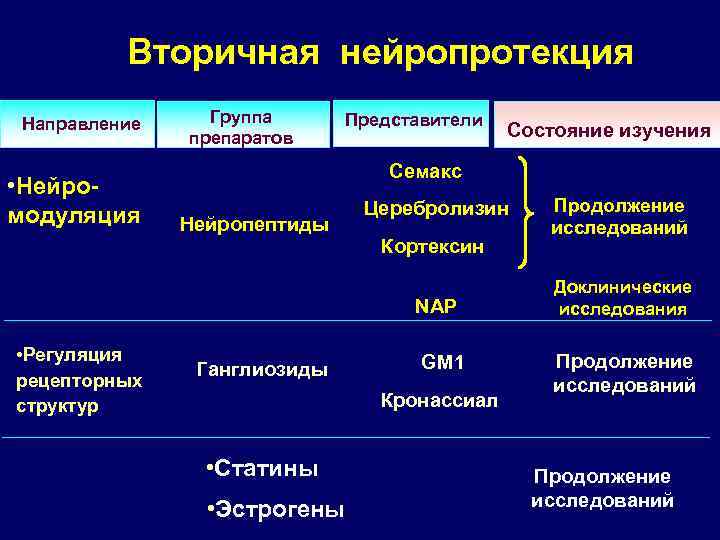
Вторичная нейропротекция Направление • Нейромодуляция Группа препаратов Представители Семакс Нейропептиды Церебролизин Кортексин NAP • Регуляция рецепторных структур Состояние изучения Ганглиозиды GM 1 Кронассиал • Статины • Эстрогены Продолжение исследований Доклинические исследования Продолжение исследований

Антиоксиданты и Антигипоксанты • Коррекция энергетического метаболизма • Нормализация функций дыхательной цепи митохондрий Физиологическая антиоксидантная система Ферментные • СОД • Каталаза Неферментные • Вит. С, Е, К • Глюкоза • Убихиноны • Коэнзим Q • каротиноиды

Антиоксиданты «Ловушки» свободных радикалов (тирилозад) Блокаторы NO-синтазы (7 -нитроиндазол) Селен-органические соединения (эбселен) Производные 3 -гидроксипиридина (эмоксипин)

Антиоксиданты 1700 пациентов с инсультом I. «Ловушки» свободных радикалов (ТИРИЛАЗАД) • 21 -аминостероид • Ингибитор ПОЛ • Выраженное ограничение инфарктной зоны в экспериментальных условиях • Исследовались дозы: 0, 6, 2 и 6 мг/кг • Малые дозы – эффективность не доказана • Большие дозы – риск побочных эффектов • Плохо проникает через ГЭБ

Антиоксиданты II. Селен-органические соединения (ЭБСЕЛЕН) • Подавляет ПОЛ • Блокирует продукцию пероксинитрит-аниона • Блокирует синтез i-NOS • Хорошо переносится • Пилотные исследования не доказали эффективности • Испытания продолжаются

Проспективное рандомизированное двойное слепое плацебоконтролируемое исследование безопасности и эффективности МЕКСИДОЛА в комплексной терапии ишемического инсульта в остром периоде Кафедра фундаментальной и клинической неврологии ГОУ ВПО РГМУ Росздрава НИИ цитохимии и молекулярной фармакологии
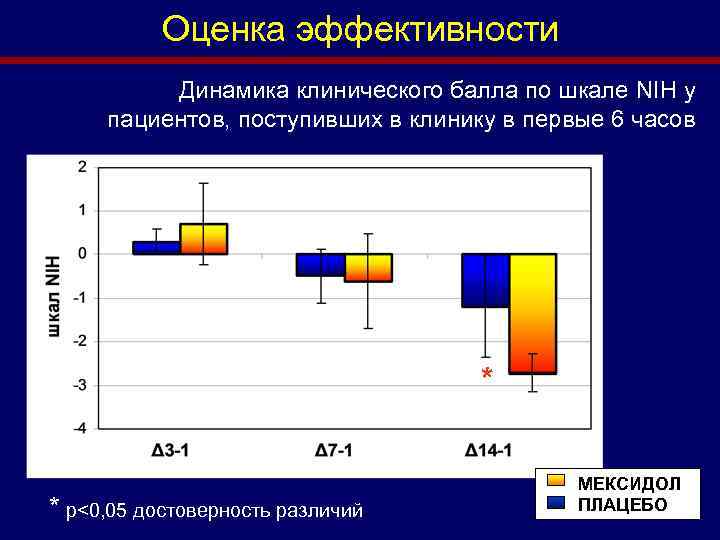
Оценка эффективности Динамика клинического балла по шкале NIH у пациентов, поступивших в клинику в первые 6 часов * * p<0, 05 достоверность различий МЕКСИДОЛ ПЛАЦЕБО
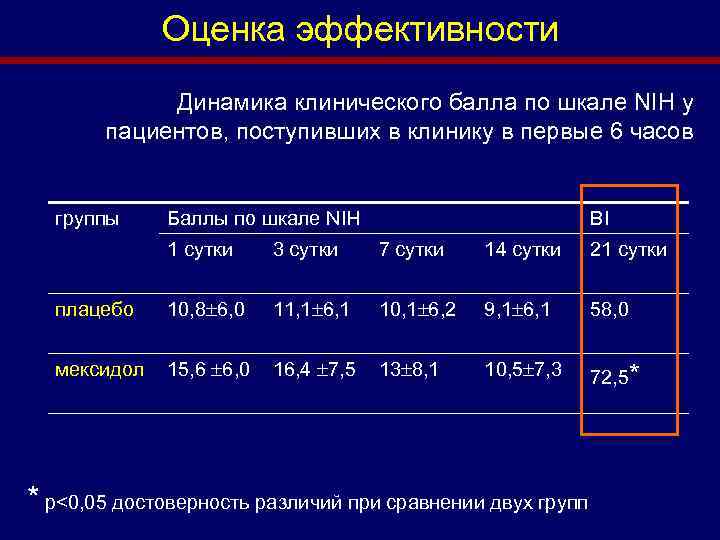
Оценка эффективности Динамика клинического балла по шкале NIH у пациентов, поступивших в клинику в первые 6 часов группы Баллы по шкале NIH BI 1 сутки 3 сутки 7 сутки 14 сутки 21 сутки плацебо 10, 8 6, 0 11, 1 6, 1 10, 1 6, 2 9, 1 6, 1 58, 0 мексидол 15, 6 6, 0 16, 4 7, 5 13 8, 1 10, 5 7, 3 72, 5* * p<0, 05 достоверность различий при сравнении двух групп

Трофические факторы NGF, b-FGF, BDNF, TGF-B 1 • Полипептиды • Репаративные и пролиферативные свойства • При быстрой экспрессии генов нейротрофинов обеспечивается расширение «терапевтического окна» • Высокий уровень нейротрофических факторов обеспечивает быстрый регресс очаговых симптомов
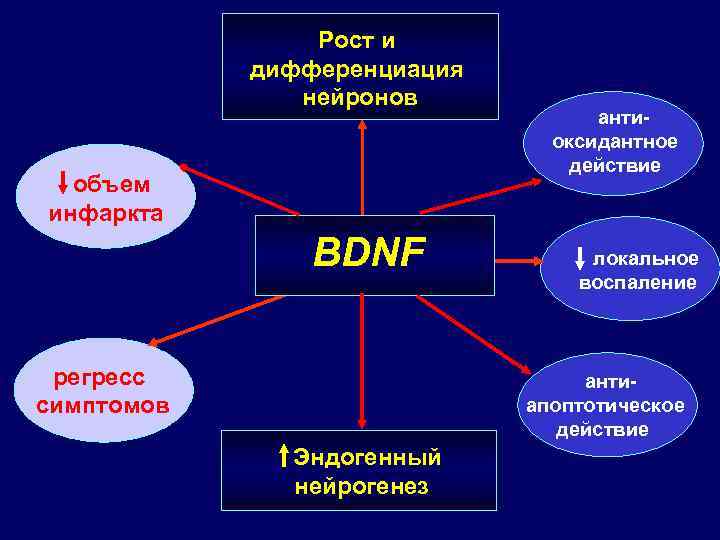
Рост и дифференциация нейронов объем инфаркта BDNF регресс симптомов антиоксидантное действие локальное воспаление антиапоптотическое действие Эндогенный нейрогенез
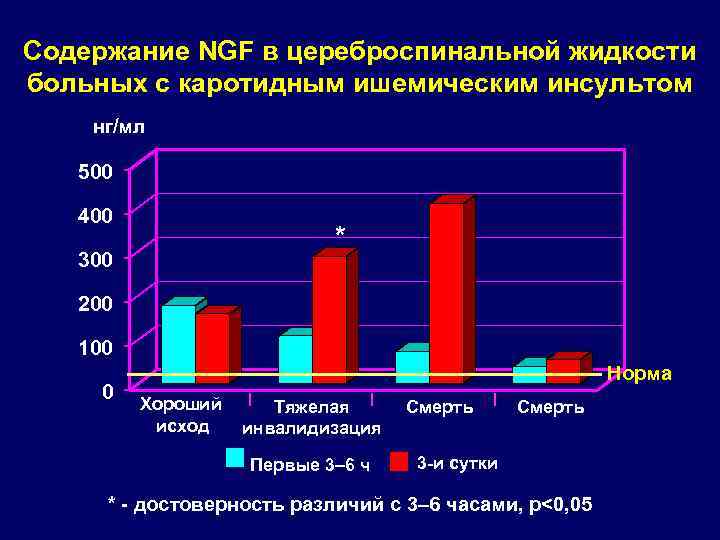
Содержание NGF в цереброспинальной жидкости больных с каротидным ишемическим инсультом нг/мл 500 400 * 300 200 100 0 Норма Хороший исход Тяжелая инвалидизация Первые 3– 6 ч Смерть 3 -и сутки * - достоверность различий с 3– 6 часами, р<0, 05
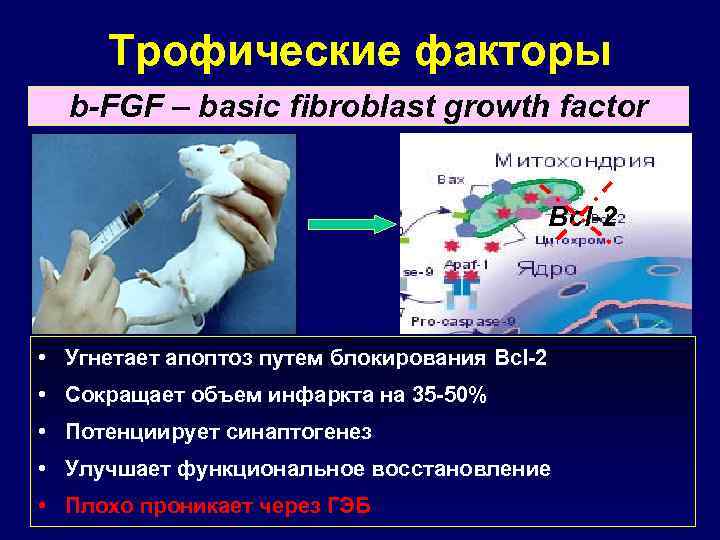
Трофические факторы b-FGF – basic fibroblast growth factor Bcl-2 • Угнетает апоптоз путем блокирования Bcl-2 • Сокращает объем инфаркта на 35 -50% • Потенциирует синаптогенез • Улучшает функциональное восстановление • Плохо проникает через ГЭБ

НЕЙРОПЕПТИДЫ • аминокислотные цепи до 10 к. Да • «нарезаются» из более крупных молекул-предшедственников (процессинг) • известно около 100 нейропептидов
НЕЙРОПЕПТИДЫ: медиаторные эффекты • Передача информации (взаимодействие с рецептором на поверхности клетки – связь с Gбелком); Влияние на: • генную экспрессию • образования синапсов • морфологию клеток глии
НЕЙРОПЕПТИДЫ: регуляторные функции • контроль за экспрессией вторичных клеточных мессенджеров и сигнальных молекул • контроль за запуском генетических программ апоптоза и антиапоптозной защиты • усиление трофического обеспечения

Нейропептиды • Эндогенные регуляторы функций ЦНС (Na-уретическая и вазомоторная регуляция) • Трофические и ростовые эффекты • Медиаторные и эффекторные свойства • Регуляция активности про- и противовоспалительных цитокинов Церебролизин • Гидролизат белковой вытяжки из ГМ свиней • Эффективная доза 10 -60 мл/сут • • • Экстракт вытяжки из коры головного мозга КРС Нормализует биоэлектрический потенциал ГМ Эффективная доза 20 мг/сут Кортексин Семакс • • Негормональный аналог фрагмента 4 -7 АКТГ Интраназальная форма введения (12 -18 мг/сут)

Преимущества пептидных препаратов при проведении нейропротективной терапии • высокая физиологическая активность • несколько лигандных групп связывания (полифункциональность) • короткое время жизни (минимум побочных эффектов) • длительное действие (развитие каскадных процессов) • малая масса (легкое проникновение через ГЭБ) трофические и ростовые, противовоспалительные, медиаторные и эффекторные свойства

СЕМАКС МЯСОЕДОВ Николай Федорович АШМАРИН Игорь Петрович Академик РАН Заместитель директора Института молекулярной генетики РАН Академик РАМН, автор создания концепции функционального континуума регуляторных пептидов

Семакс и его ближайшие аналоги Семакс (SEMAX, АКТГ 4 -10) Met-Glu-His-Phe-Pro-Glu-Pro ACTH (4 -7) Met-Glu-His-Phe ORG 2766 (O 2 )Met-Glu-His-Phe-KPhe EBIRATID (O 2 )Met-Glu-His-Phe-d. KPhe-NH-(CH 2)8 -NH 2
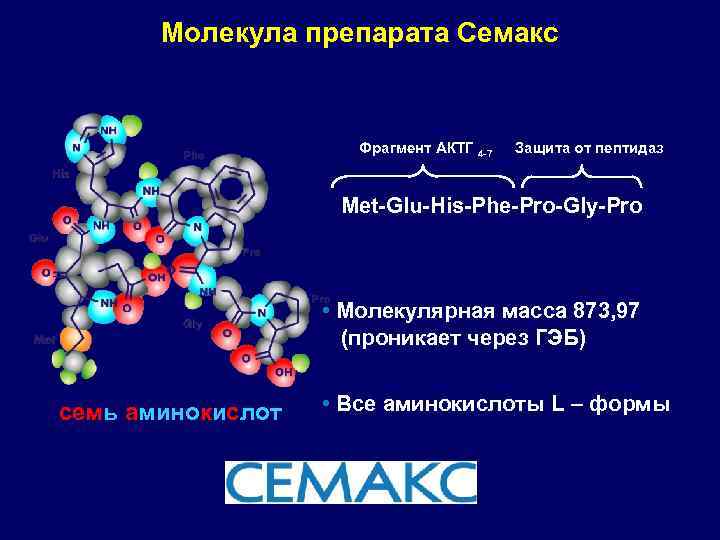
Молекула препарата Семакс Фрагмент АКТГ 4 -7 Защита от пептидаз Met-Glu-His-Phe-Pro-Gly-Pro • Молекулярная масса 873, 97 (проникает через ГЭБ) семь аминокислот • Все аминокислоты L – формы

СЕМАКС: выраженные нейропротективные и нейротрофические свойства Влияние на механизмы отсроченной смерти нейронов: - активация микроглии - нормализация цитокинового дисбаланса - уменьшение локального воспаления - снижение синтеза оксида азота - уменьшение оксидантного стресса - предотвращение индукции апоптоза Усиление холинергической нейропередачи в головном мозге (улучшение процесса обучения и памяти) Повышение уровня эндогенных нейротрофинов (факторов роста NGF, BDNF и др. )
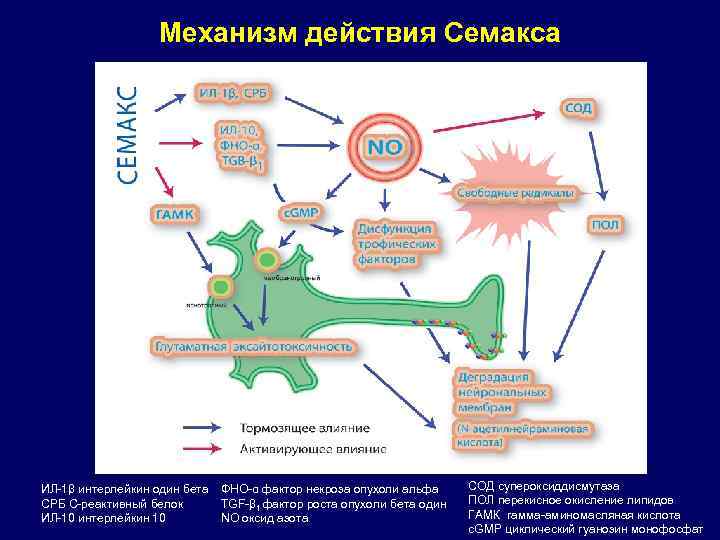
Механизм действия Семакса ИЛ-1β интерлейкин один бета СРБ С-реактивный белок ИЛ-10 интерлейкин 10 ФНО-α фактор некроза опухоли альфа TGF-β 1 фактор роста опухоли бета один NO оксид азота СОД супероксиддисмутаза ПОЛ перекисное окисление липидов ГАМК гамма-аминомасляная кислота c. GMP циклический гуанозин монофосфат
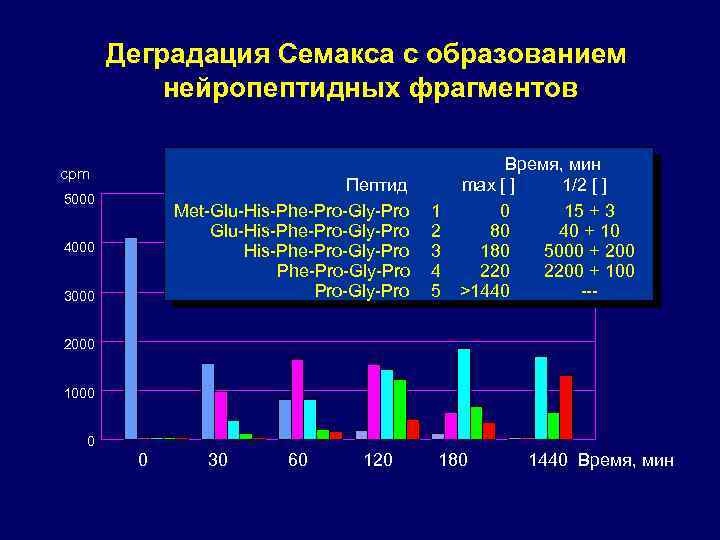
Деградация Семакса с образованием нейропептидных фрагментов cpm Пептид Met-Glu-His-Phe-Pro-Gly-Pro Pro-Gly-Pro 5000 4000 3000 1 2 3 4 5 Время, мин max [ ] 1/2 [ ] 0 15 + 3 80 40 + 10 180 5000 + 200 2200 + 100 >1440 --- 2000 1000 0 0 30 60 120 180 1440 Время, мин
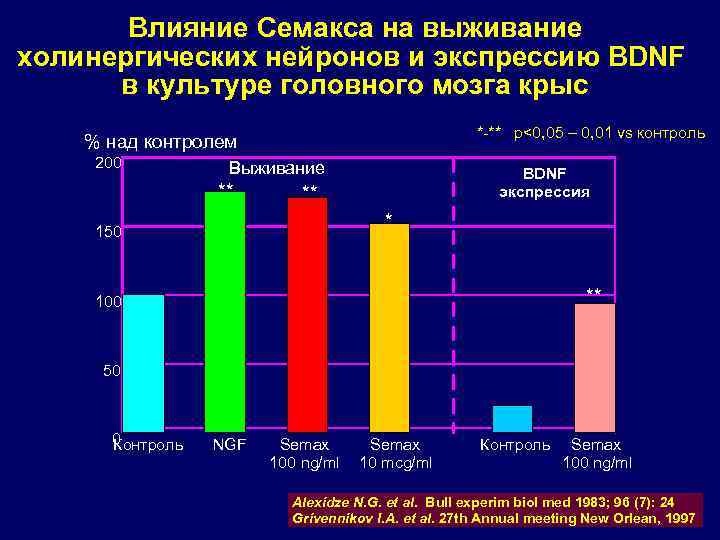
Влияние Семакса на выживание холинергических нейронов и экспрессию BDNF в культуре головного мозга крыс *-** p<0, 05 – 0, 01 vs контроль % над контролем 200 Выживание ** BDNF экспрессия ** * 150 ** 100 50 0 Контроль NGF Semax 100 ng/ml Semax 10 mcg/ml Контроль Semax 100 ng/ml Alexidze N. G. et al. Bull experim biol med 1983; 96 (7): 24 Grivennikov I. A. et al. 27 th Annual meeting New Orlean, 1997
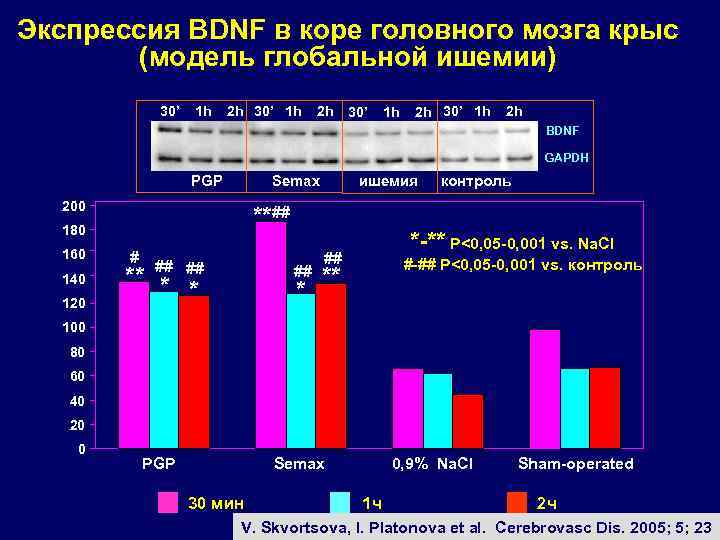
Экспрессия BDNF в коре головного мозга крыс (модель глобальной ишемии) 30’ 1 h 2 h BDNF GAPDH Semax PGP 200 ** ## 180 160 140 120 ишемия # ** ## ## * * ## * контроль *-** P<0, 05 -0, 001 vs. Na. Cl ## #-## P<0, 05 -0, 001 vs. контроль ** 100 80 60 40 20 0 PGP Semax 30 мин 0, 9% Na. Cl 1 ч Sham-operated 2 ч V. Skvortsova, I. Platonova et al. Cerebrovasc Dis. 2005; 5; 23

Применение Семакса 1% в первые часы и дни острого церебрального инсульта Рандомизированное двойное-слепое плацебо-контролируемое исследование Член-корр. РАМН, профессор В. И. Скворцова, проф. Л. В. Стаховская, к. м. н. Н. М. Ефремова, к. м. н. Н. А. Шамалов, к. м. н. И. М. Шетова Москва, РГМУ, 2007 г. Оценка эффективности Семакса 1% при церебральном инсульте Количество пациентов: 160 человек Оценка неврологического дефицита: Скандинавская, Оргогозо и оригинальная шкалы Функциональное восстановление: индекс Бартел, 30 дневная летальность

Рандомизированное двойное слепое плацебо-контролируемое исследование 160 больных с ишемическим инсультом в каротидной системе доказало высокую эффективность Семакса 1% в дозе 12 – 18 мг / сутки -ускорение регресса общемозговых и очаговых симптомов; - улучшение функционального восстановления
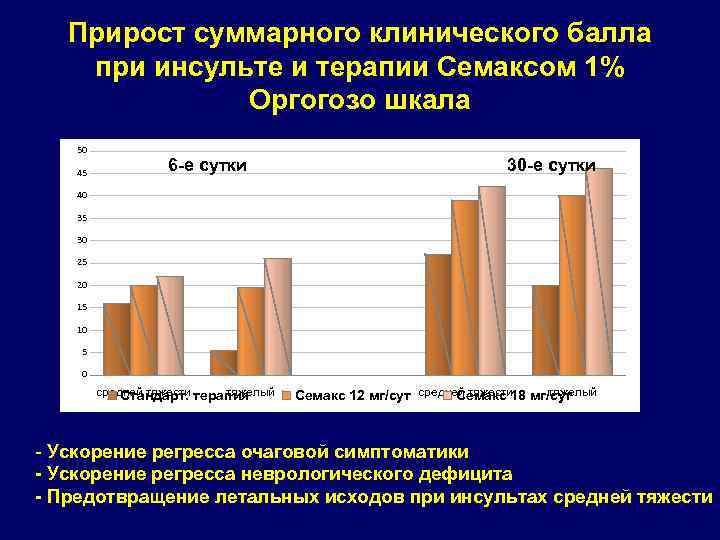
Прирост суммарного клинического балла при инсульте и терапии Семаксом 1% Оргогозо шкала 50 45 6 -е сутки 30 -е сутки 40 35 30 25 20 15 10 5 0 средней тяжести терапия тяжелый Стандарт. тяжелый Семакс 12 мг/сут средней тяжести 18 мг/сут Семакс - Ускорение регресса очаговой симптоматики - Ускорение регресса неврологического дефицита - Предотвращение летальных исходов при инсультах средней тяжести
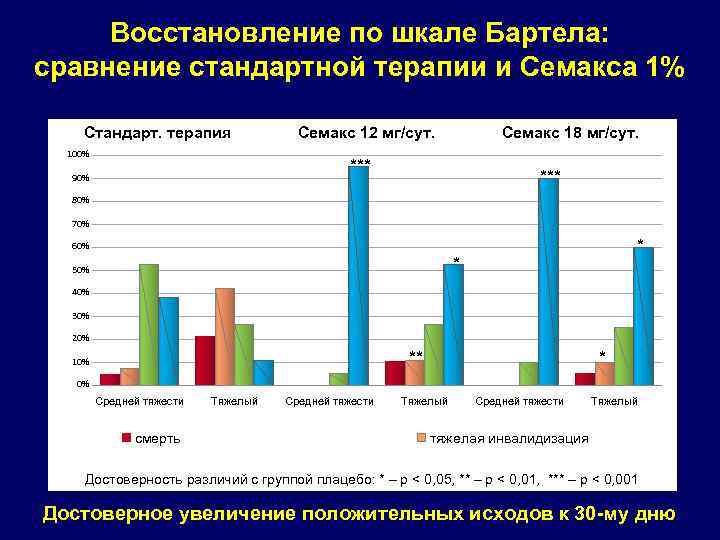
Восстановление по шкале Бартела: сравнение стандартной терапии и Семакса 1% Стандарт. терапия 100% Семакс 12 мг/сут. Семакс 18 мг/сут. *** 90% *** 80% 70% * 60% * 50% 40% 30% 20% ** 10% * 0% Средней тяжести смерть Тяжелый Средней тяжести Тяжелый тяжелая инвалидизация Достоверность различий с группой плацебо: * – p < 0, 05, ** – p < 0, 01, *** – p < 0, 001 Достоверное увеличение положительных исходов к 30 -му дню

Клинические исследования 1. Российский Государственный Медицинский Университет (Москва) 2. Московская Медицинская Академия имени И. М. Сеченова (Москва) 3. НИИ Неврологии РАМН (Москва) 4. Военно-Медицинская Академия им. С. М. Кирова (Санкт-Петербург) 5. НИИ Неврологии им. В. М. Бехтерева (Санкт-Петербург) 6. Государственный Медицинский Университет (Новосибирск) 7. НИИ Педиатрии НЦЗД РАМН (Москва)

Стандарт лечения для СМП ИНСУЛЬТ КОМА НЕУТОЧНЕННАЯ Приказ Минздравсоцразвития № 643 от 5. 09. 2006 Приказ Минздравсоцразвития № 650 от 7. 09. 2006 СЕМАКС 1%

Стандарт лечения для стационара ИНСУЛЬТ СУБАРАХНОИДАЛЬНОЕ КРОВОИЗЛИЯНИЕ ВНУТРИМОЗГОВОЕ КРОВОИЗЛИЯНИЕ ИНФАРКТ МОЗГА ТРАНЗИТОРНЫЕ ИШЕМИЧЕСКИЕ АТАКИ ПРИКАЗ МИНЗДРАВСОЦРАЗВИТИЯ № 513 ОТ 1. 08. 2007 СЕМАКС 1%

Семакс 0, 1% • Хроническая ишемическая болезнь головного мозга • Восстановительный период и последствия инсульта • Последствия черепно-мозговых травм • Восстановление после нейрохирургических вмешательств, наркоза, ионизирующего излучения • Синдром дефицита внимания с гиперактивностью • Синдром хронической усталости • Нейродегенеративные заболевания (болезнь Паркинсона, хорея Гентингтона, болезнь Альцгеймера) • Заболевания зрительного нерва (офтальмология)
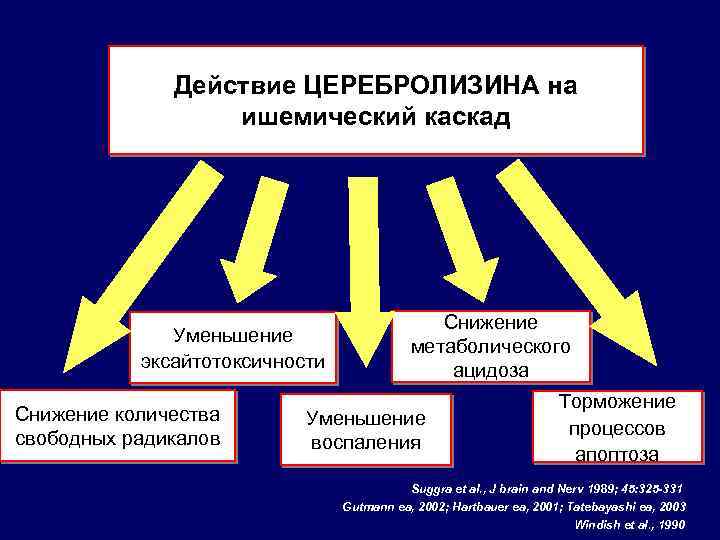
Действие ЦЕРЕБРОЛИЗИНА на ишемический каскад Уменьшение эксайтотоксичности Снижение количества свободных радикалов Снижение метаболического ацидоза Уменьшение воспаления Торможение процессов апоптоза Suggra et al. , J brain and Nerv 1989; 45: 325 -331 Gutmann ea, 2002; Hartbauer ea, 2001; Tatebayashi ea, 2003 Windish et al. , 1990

Применение ЦЕРЕБРОЛИЗИНА при остром инсульте 70 -е годы • Суточная доза – 1 -2 мл • Назначение - с 5 -го – 7 -го дней заболевания • Ноотропные эффекты
Церебролизин Энергетический метаболизм Оксидантная система Нейротрофическое обеспечение Нейромодуляция

Церебролизин 90 -е годы • Повышение экспрессии гена транспортера глутамата GLUT-1 Уменьшение глутаматной эксайтотоксичности Увеличение транспорта глюкозы к мозгу в условиях ишемии

Церебролизин 90 -е годы Ингибирование кальций-зависимых протеаз, в том числе кальпаина Увеличение экспрессии гена МАР 2 Защита цитоскелета нейронов

Церебролизин 90 -е годы аффинности связывания BDNF с рецепторами Регуляция trk-B рецепторов нейротрофинов Регуляция естественных факторов роста

Церебролизин 90 -е годы синтеза ИЛ-1ß и других провоспалительных цитокинов локальной воспалительной реакции нарушений микроциркуляции и ГЭБ

Церебролизин 10 мл в день • резистентности к гипоксии-ишемии • аэробного метаболизма, оптимизация энергозависимых функций • Антиоксидантные свойства • Специфическое нейротрофическое и модуляторное действие • функциональной интеграции нейронов и глии • экспрессии GLUT-1 транспорта глюкозы через ГЭБ • Защита структуры нейрона ( Кальпаина, MAP 2)

Церебролизин 10 - 50 мл/день • Более полный регресс неврологического дефицита • Достоверное улучшение функционального восстановления на 30 -й день • Достоверное улучшение самообслуживания в отдаленном периоде M. Windisch, 1994 G. S. Barolin, 1996 C. Stadler, 1997 G. Ladurner, 2001

Рандомизированное двойное-слепое плацебо-контролируемое исследование безопасности и эффективности Церебролизина в суточной дозе 10 мл и 50 мл у больных в остром периоде ишемического инсульта Скворцова В. И. и соавт. Инсульт 2004: 11: 51 -55
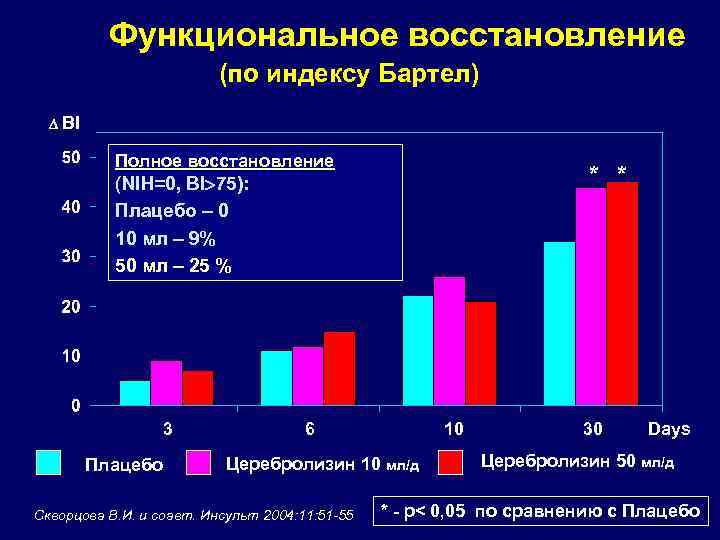
Функциональное восстановление (по индексу Бартел) BI Полное восстановление * * (NIH=0, BI 75): Плацебо – 0 10 мл – 9% 50 мл – 25 % 3 Плацебо 6 10 Церебролизин 10 мл/д Скворцова В. И. и соавт. Инсульт 2004: 11: 51 -55 30 Days Церебролизин 50 мл/д * - р< 0, 05 по сравнению с Плацебо
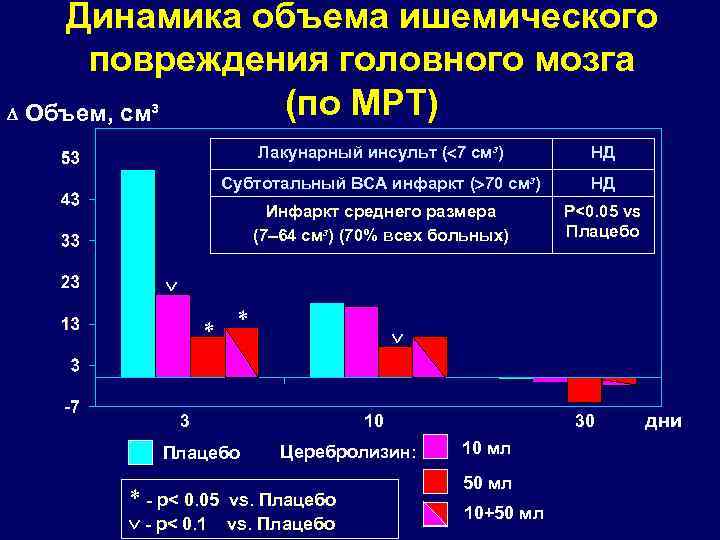
Динамика объема ишемического повреждения головного мозга (по МРТ) Объем, cм³ Лакунарный инсульт ( 7 cм³) НД Субтотальный ВСА инфаркт ( 70 cм³) НД Инфаркт среднего размера (7 64 cм³) (70% всех больных) P<0. 05 vs Плацебо * * 3 10 Плацебо * - р< 0. 05 - р< 0. 1 Церебролизин: vs. Плацебо 30 10 мл 50 мл 10+50 мл дни
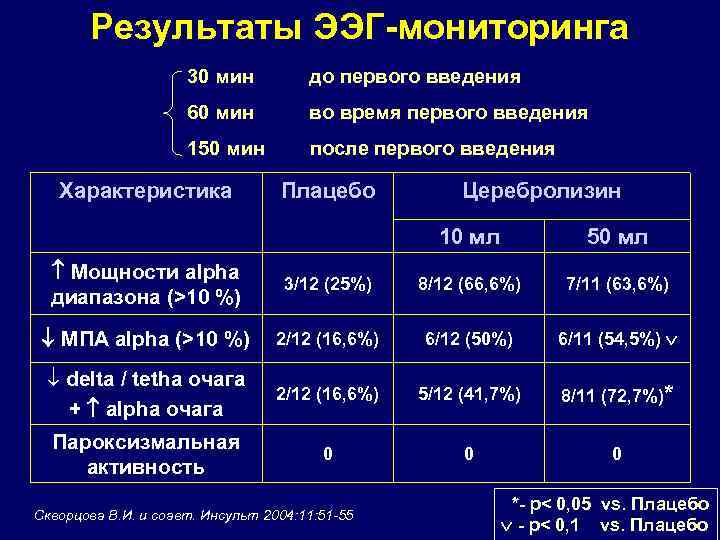
Результаты ЭЭГ-мониторинга 30 мин до первого введения 60 мин во время первого введения 150 мин после первого введения Характеристика Плацебо Церебролизин 10 мл 50 мл Мощности alpha диапазона (>10 %) 3/12 (25%) 8/12 (66, 6%) 7/11 (63, 6%) МПA alpha (>10 %) 2/12 (16, 6%) 6/12 (50%) 6/11 (54, 5%) ¯ delta / tetha очага + alpha очага 2/12 (16, 6%) 5/12 (41, 7%) 8/11 (72, 7%)* Пароксизмальная активность 0 0 0 Скворцова В. И. и соавт. Инсульт 2004: 11: 51 -55 *- р< 0, 05 vs. Плацебо - р< 0, 1 vs. Плацебо
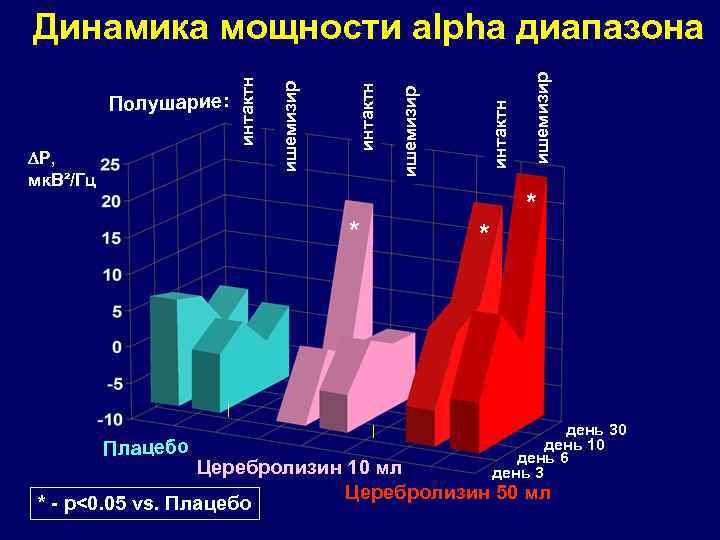
* Плацебо * ишемизир интактн P, мк. В²/Гц ишемизир Полушарие: интактн Динамика мощности alpha диапазона * день 30 день 10 день 6 день 3 Церебролизин 10 мл Церебролизин 50 мл * - p<0. 05 vs. Плацебо
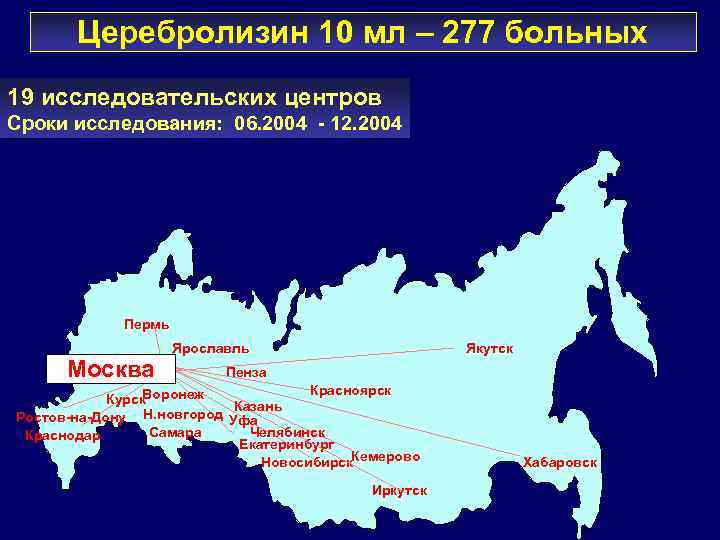
Церебролизин 10 мл – 277 больных 19 исследовательских центров Сроки исследования: 06. 2004 - 12. 2004 Пермь Москва Ярославль Якутск Пенза Красноярск Воронеж Курск Казань Ростов-на-Дону Н. новгород Уфа Самара Челябинск Краснодар Екатеринбург Новосибирск. Кемерово Иркутск Хабаровск
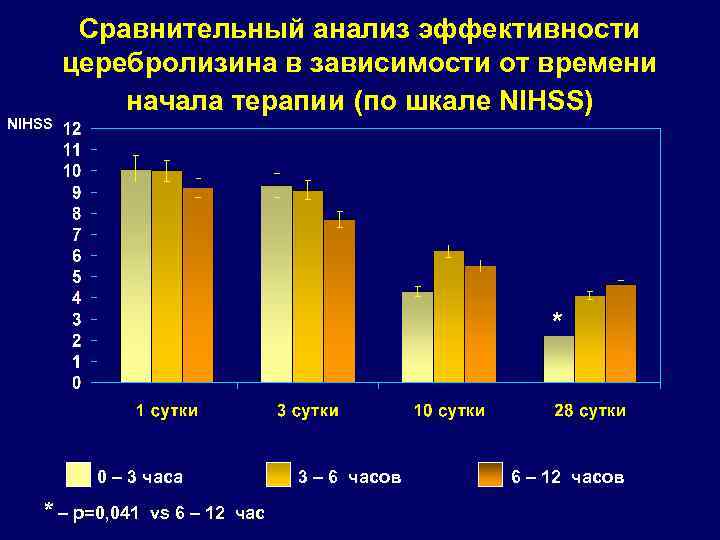
Сравнительный анализ эффективности церебролизина в зависимости от времени начала терапии (по шкале NIHSS) NIHSS * 0 – 3 часа * – р=0, 041 vs 6 – 12 час 3 – 6 часов 6 – 12 часов

Церебролизин в восстановительном периоде ишемического инсульта Церебролизин 50 мл 21 день • Значимое улучшение социальной активности, независимости • Более полный регресс очаговых симптомов (двигательных, речевых) • Раннее начало терапии улучшение функционального восстановления Коппи С. , Баролин Г. Журн. Невр. и псих. 1998: 10: 30 -35
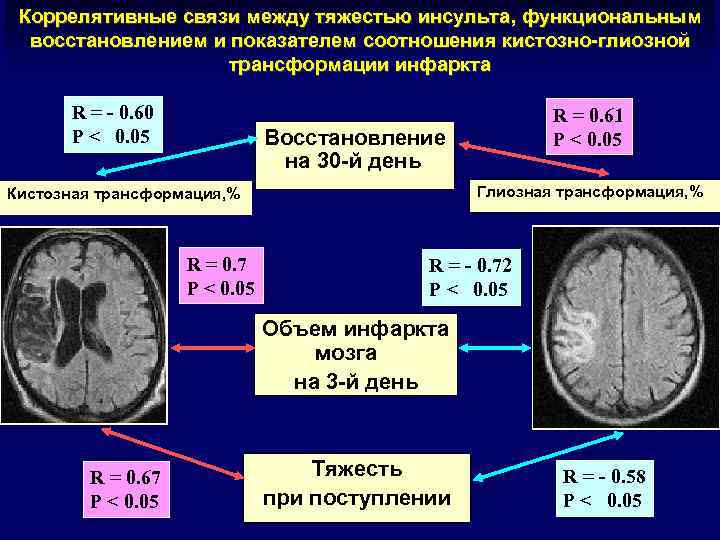
Коррелятивные связи между тяжестью инсульта, функциональным восстановлением и показателем соотношения кистозно-глиозной трансформации инфаркта R = - 0. 60 P < 0. 05 R = 0. 61 P < 0. 05 Восстановление на 30 -й день Глиозная трансформация, % Кистозная трансформация, % R = 0. 7 P < 0. 05 R = - 0. 72 P < 0. 05 Объем инфаркта мозга на 3 -й день R = 0. 67 P < 0. 05 Тяжесть при поступлении R = - 0. 58 P < 0. 05

АМИНЕРГИЧЕСКИЕ И ХОЛИНЕРГИЧЕСКИЕ МЕДИАТОРЫ (АДРЕНАЛИН, ВОЗДЕЙСТВИЕ ЭКЗОГЕННЫХ СЕРОТОНИН, АЦЕТИЛХОЛИН) РЕАБИЛИТАЦИЯ СТИМУЛИРУЮЩИХ ФАКТОРОВ ФИЗИЧЕСКАЯ И КОГНИТИВНАЯ ПЛАСТИЧНОСТЬ НЕЙРОТРОФИЧЕСКИЕ ФАКТОРЫ (NGF, BDNF, b. FGF) АМИНАЦИДЭРГИЧЕСКИЕ НЕЙРОТРАНСМИТТЕРЫ (ГЛУТАМАТ, ГАМК) НЕЙРОПЕПТИДЫ БИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА (ОКСИД АЗОТА, ЭСТРАДИОЛ И ДР. )
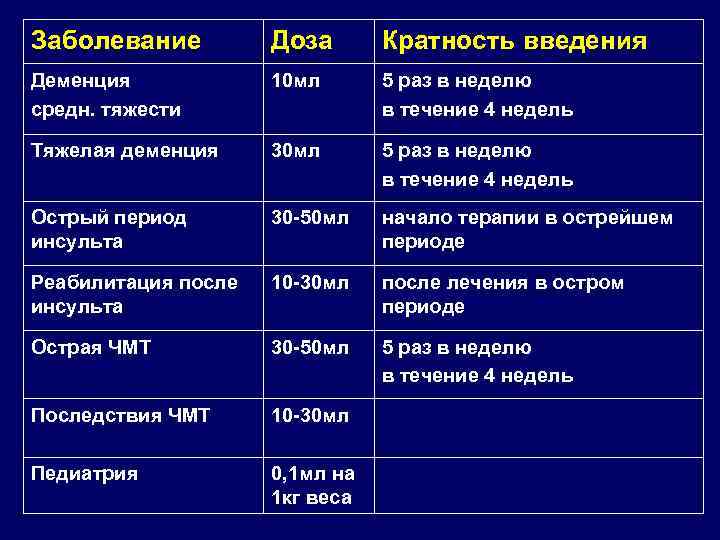
Заболевание Доза Кратность введения Деменция средн. тяжести 10 мл 5 раз в неделю в течение 4 недель Тяжелая деменция 30 мл 5 раз в неделю в течение 4 недель Острый период инсульта 30 -50 мл начало терапии в острейшем периоде Реабилитация после инсульта 10 -30 мл после лечения в остром периоде Острая ЧМТ 30 -50 мл 5 раз в неделю в течение 4 недель Последствия ЧМТ 10 -30 мл Педиатрия 0, 1 мл на 1 кг веса

Кортексин Разработан коллективом ученых Военно-медицинской академии им. С. М. Кирова под руководством академика РАМН Ф. И. Комарова

Кортексин препарат полипептидной природы, получаемый путем экстракции из коры головного мозга КРС Содержит комплекс L-аминокислот и полипептидов с молекулярной массой до 10 к. Да, а также сбалансированный для нормальной функции нейронов витаминный и минеральный состав
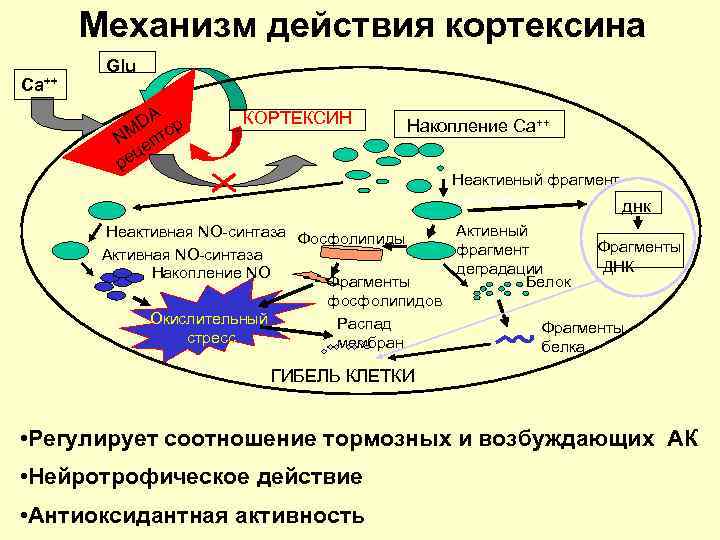
Механизм действия кортексина Са++ Glu DA ор NM епт ц ре КОРТЕКСИН Накопление Са++ Неактивный фрагмент деградации днк Активный Неактивная NO-синтаза Фосфолипиды Фрагменты фрагмент Активная NO-синтаза ДНК деградации Накопление NO Фрагменты Белок фосфолипидов Окислительный Распад Фрагменты стресс мембран белка ГИБЕЛЬ КЛЕТКИ • Регулирует соотношение тормозных и возбуждающих АК • Нейротрофическое действие • Антиоксидантная активность

Кортексин при ишемическом инсульте • церебропротекторное действие • улучшает процессы обучения и памяти • стимулирует репаративные процессы в головном мозге • ускоряет восстановление функций головного мозга после стрессорных воздействий

КОРТЕКСИН при ишемическом инсульте Мультицентровое двойное слепое плацебоконтролируемое исследование 62 пациента (50 -85 лет) с ишемическим инсультом в каротидной системе 32 пациента Кортексин 20 мг в/м в течение 10 дней 30 пациентов Плацебо 20 мл в/м в течение 10 дней А. А. Скоромец, В. И. Скворцова, А. А. Белкин и др.
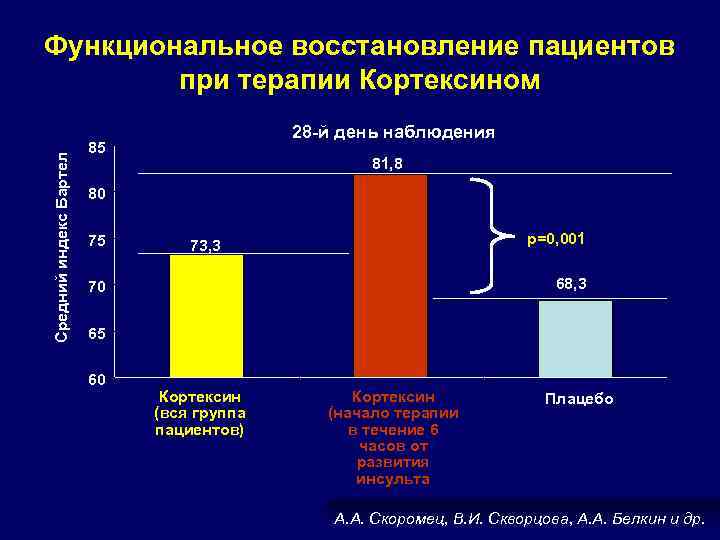
Средний индекс Бартел Функциональное восстановление пациентов при терапии Кортексином 28 -й день наблюдения 85 81, 8 80 75 р=0, 001 73, 3 68, 3 70 65 60 Кортексин (вся группа пациентов) Кортексин (начало терапии в течение 6 часов от развития инсульта Плацебо А. А. Скоромец, В. И. Скворцова, А. А. Белкин и др.
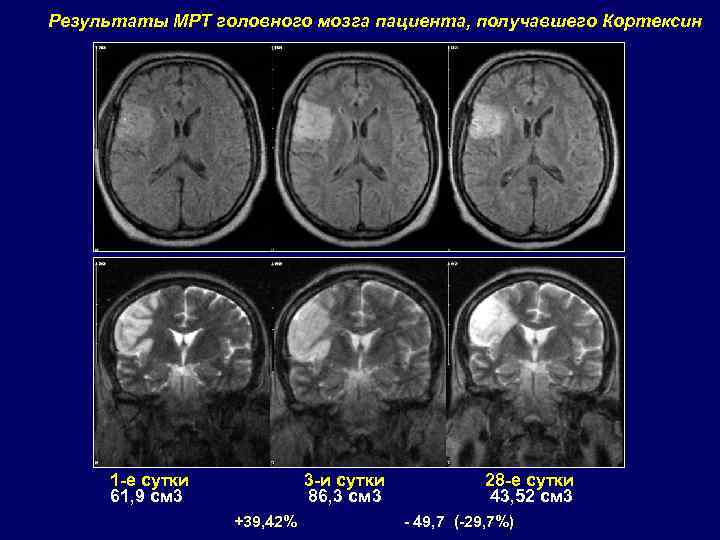
Результаты МРТ головного мозга пациента, получавшего Кортексин 1 -е сутки 61, 9 см 3 3 -и сутки 86, 3 см 3 +39, 42% 28 -е сутки 43, 52 см 3 - 49, 7 (-29, 7%)
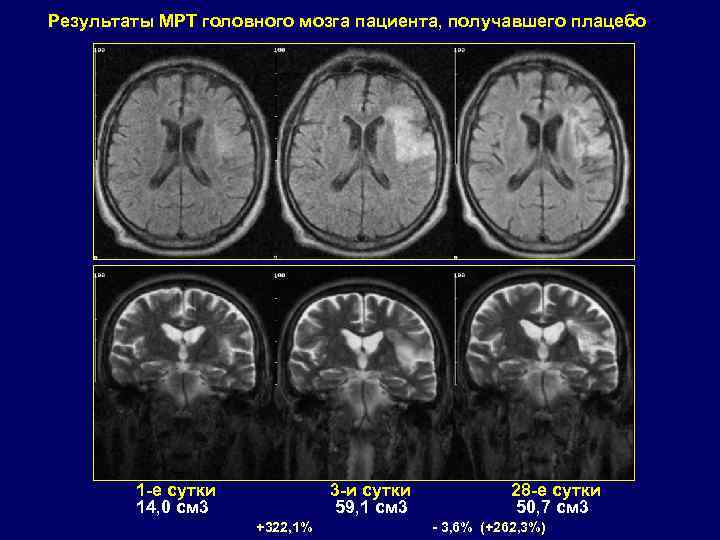
Результаты МРТ головного мозга пациента, получавшего плацебо 1 -е сутки 14, 0 см 3 3 -и сутки 59, 1 см 3 +322, 1% 28 -е сутки 50, 7 см 3 - 3, 6% (+262, 3%)

КОРТЕКСИН при геморрагическом инсульте • Снижение риска летального исхода • Достоверное ускорение регресса двигательных нарушений • Ускорение восстановления ВПФ А. П. Скороходов и др. Воронежская Госмедакадемия имени Н. Н. Бурденко
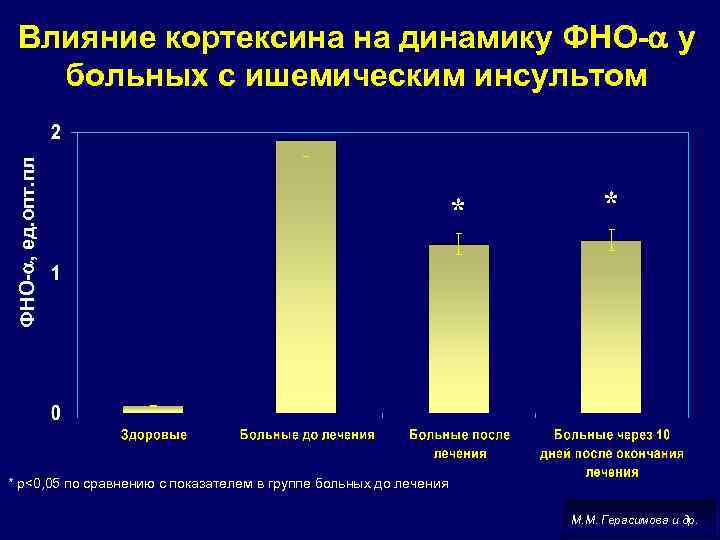
ФНО- , ед. опт. пл Влияние кортексина на динамику ФНО- у больных с ишемическим инсультом * * * р<0, 05 по сравнению с показателем в группе больных до лечения М. М. Герасимова и др.
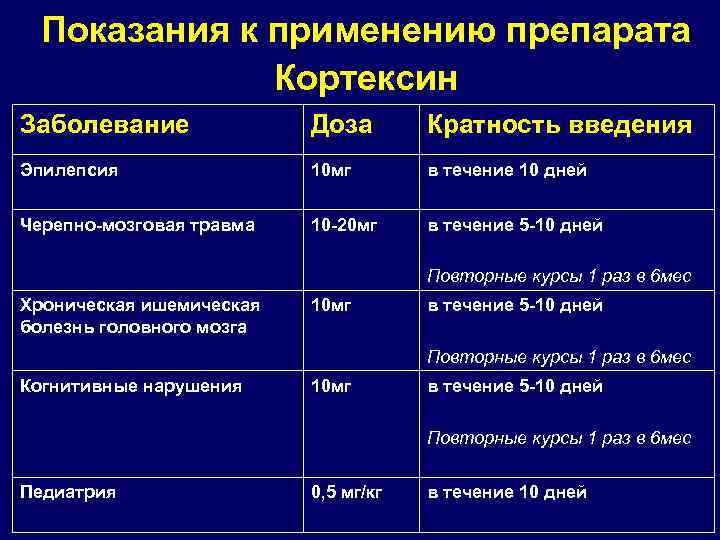
Показания к применению препарата Кортексин Заболевание Доза Кратность введения Эпилепсия 10 мг в течение 10 дней Черепно-мозговая травма 10 -20 мг в течение 5 -10 дней Повторные курсы 1 раз в 6 мес Хроническая ишемическая болезнь головного мозга 10 мг в течение 5 -10 дней Повторные курсы 1 раз в 6 мес Когнитивные нарушения 10 мг в течение 5 -10 дней Повторные курсы 1 раз в 6 мес Педиатрия 0, 5 мг/кг в течение 10 дней

ЦИТИКОЛИН цитидин-5 -дифосфохолин • Аналог эндогенного цитиколина • Донор холина в процессе синтеза АЦХ • Незаменимый метаболит в биосинтезе фосфолипидов (основных компонентов клеточных мембран)
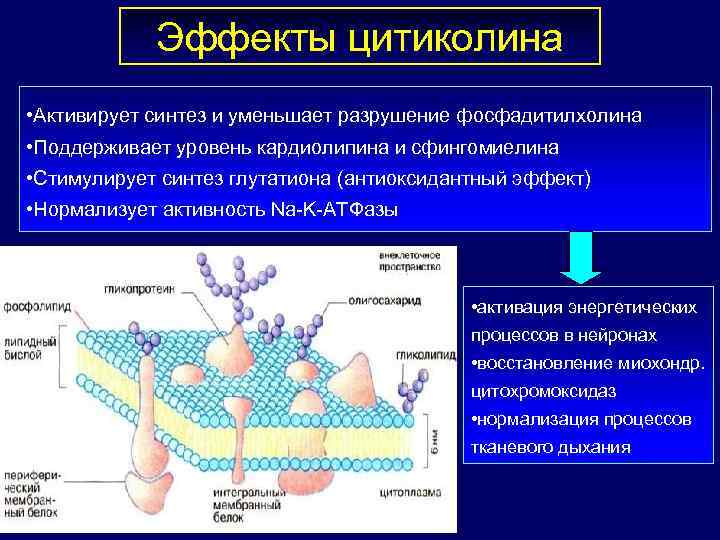
Эффекты цитиколина • Активирует синтез и уменьшает разрушение фосфадитилхолина • Поддерживает уровень кардиолипина и сфингомиелина • Стимулирует синтез глутатиона (антиоксидантный эффект) • Нормализует активность Na-K-АТФазы • активация энергетических процессов в нейронах • восстановление миохондр. цитохромоксидаз • нормализация процессов тканевого дыхания
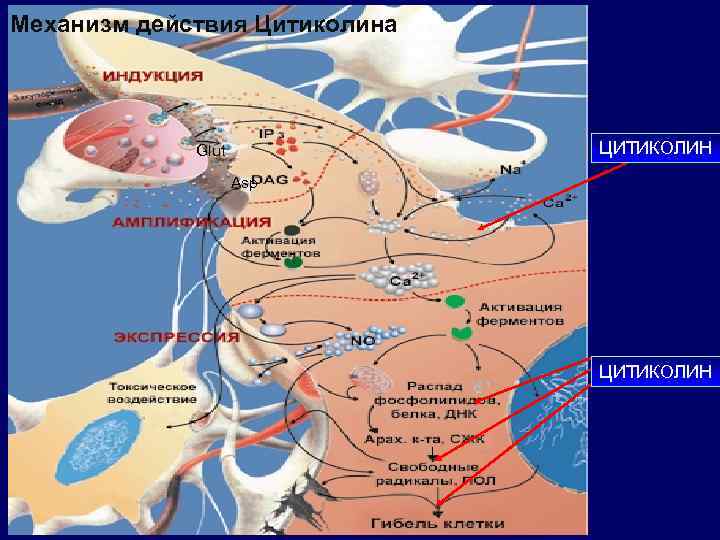
Механизм действия Цитиколина ЦИТИКОЛИН Glut Asp ЦИТИКОЛИН

Комбинированная терапия (результаты экспериментальных исследований) ЦИТИКОЛИН + rt-PA • Уменьшение объема инфаркта мозга • Улучшение функционального восстановления • Снижение частоты смертельных исходов • Защита от реперфузионной травмы Andersen M. , Overgaard K. , et al. Stroke. 1999; 30: 1464 -1471

Цитиколин при ишемическом инсульте 1000 мг/сут в течение 14 дней • Более полный регресс общемозговой и очаговой симптоматики • Достоверное улучшение функционального восстановления к концу острого периода инсульта Tazaki Y. , Sakai F. , et al. Stroke. 1988; 19: 211 -216
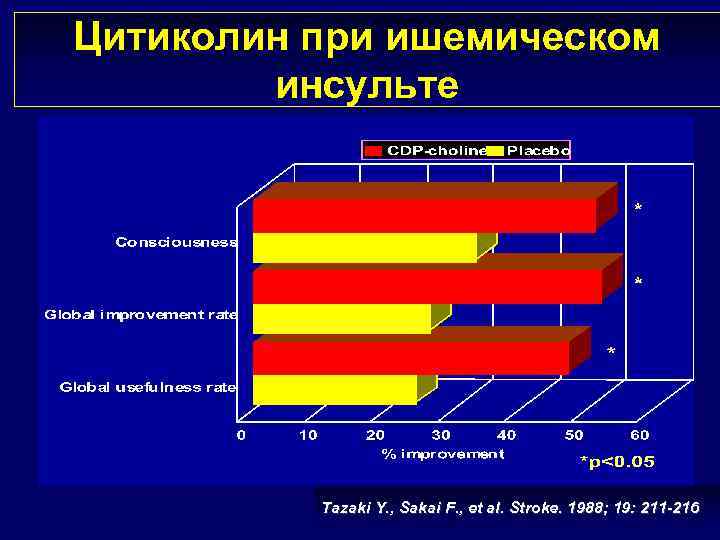
Цитиколин при ишемическом инсульте Tazaki Y. , Sakai F. , et al. Stroke. 1988; 19: 211 -216

Влияние цитиколина на объем инфаркта мозга Двойное слепое плацебо-контролируемое исследование • 100 пациентов в остром периоде ишемического инсульта • DWI и MRI на 1 -й и 12 -й неделе заболевания • 500 мг цитиколина в течение 6 недель • Хорошая переносимость и отсутствие значимых побочных эффектов • Достоверное уменьшение прироста ишемического очага в группе больных, получавших цитиколин • Более полный регресс неврологического дефицита
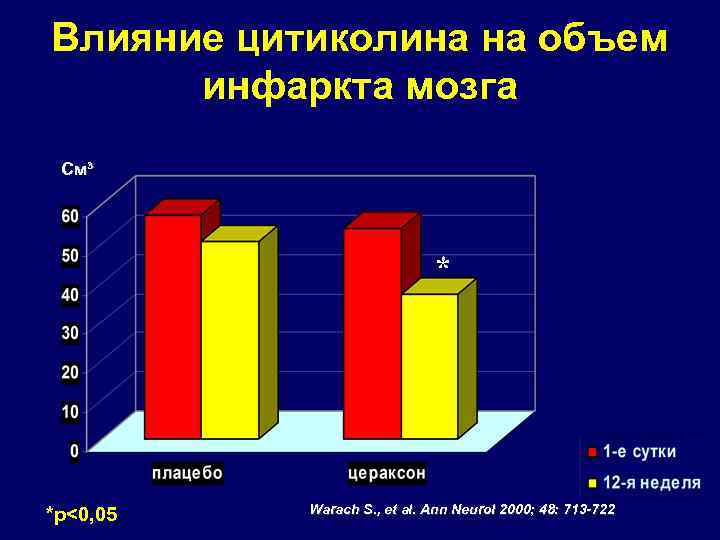
Влияние цитиколина на объем инфаркта мозга См³ * *р<0, 05 Warach S. , et al. Ann Neurol 2000; 48: 713 -722

Цитиколин Метаанализ исследований (1372 больных) • Хорошая переносимость и отсутствие значимых побочных эффектов • Значительное восстановление неврологических функций к конце 3 -го месяца в группе больных с тяжелым инсультом • Наиболее эффективная доза 2000 мг/сут • Высокая эффективность и безопасность пероральной формы
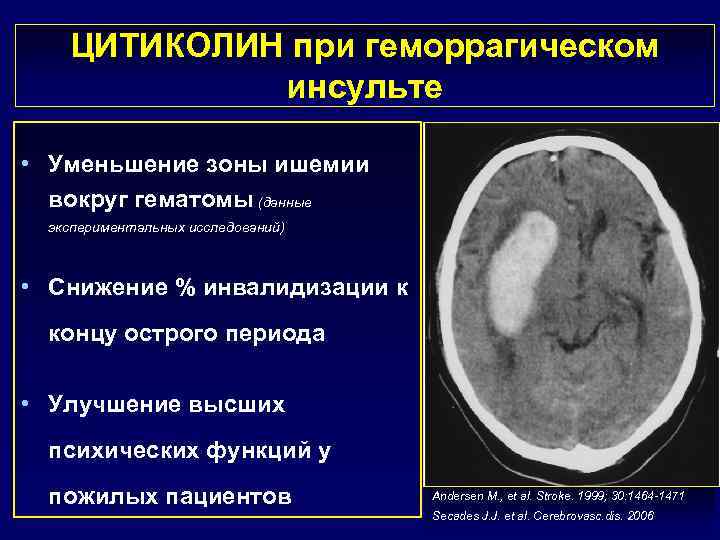
ЦИТИКОЛИН при геморрагическом инсульте • Уменьшение зоны ишемии вокруг гематомы (данные экспериментальных исследований) • Снижение % инвалидизации к концу острого периода • Улучшение высших психических функций у пожилых пациентов Andersen M. , et al. Stroke. 1999; 30: 1464 -1471 Secades J. J. et al. Cerebrovasc. dis. 2006
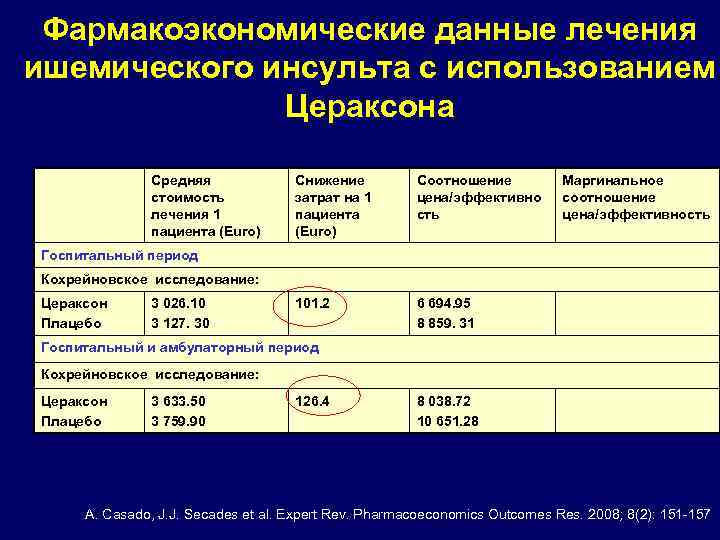
Фармакоэкономические данные лечения ишемического инсульта с использованием Цераксона Средняя стоимость лечения 1 пациента (Euro) Снижение затрат на 1 пациента (Euro) Соотношение цена/эффективно сть 101. 2 Маргинальное соотношение цена/эффективность 6 694. 95 8 859. 31 Госпитальный период Кохрейновское исследование: Цераксон Плацебо 3 026. 10 3 127. 30 Госпитальный и амбулаторный период Кохрейновское исследование: Цераксон Плацебо 3 633. 50 3 759. 90 126. 4 8 038. 72 10 651. 28 A. Casado, J. J. Secades et al. Expert Rev. Pharmacoeconomics Outcomes Res. 2008; 8(2): 151 -157
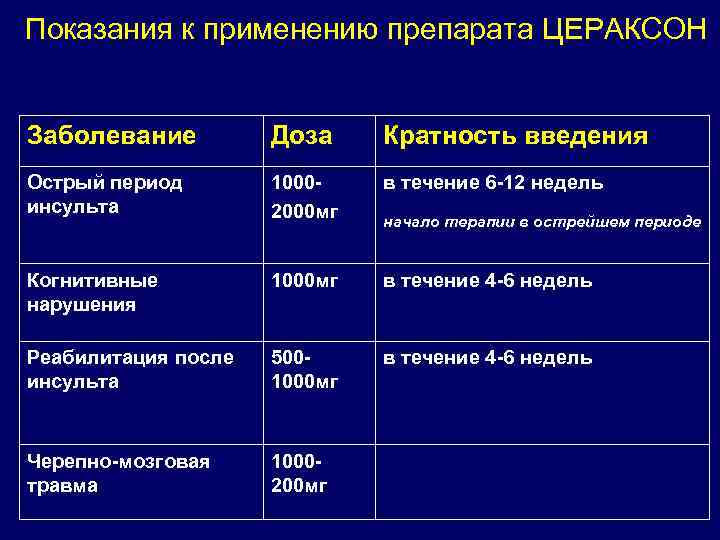
Показания к применению препарата ЦЕРАКСОН Заболевание Доза Кратность введения Острый период инсульта 10002000 мг в течение 6 -12 недель Когнитивные нарушения 1000 мг в течение 4 -6 недель Реабилитация после инсульта 5001000 мг в течение 4 -6 недель Черепно-мозговая травма 1000200 мг начало терапии в острейшем периоде

Нейропротекция при ишемическом инсульте …Мета-анализ результатов исследований выявил эффективность цитиколина, клинические исследования этого препарата продолжаются. ESO Recommendations for stroke Management – Update 2008.

Актовегин Высокоочищенный гемодиализат крови телят • Повышает обмен высокоэнергетичных фосфатов • Активирует ферменты окислительного фосфорилирования • Ускоряет распад продуктов анаэробного гликолиза • Способствует утилизации глюкозы и кислорода мозговой тканью

Показания к применению актовегина • Неврологические осложнения сахарного диабета • Черепно-мозговая травма • Трофические нарушения • Церебральный инсульт

Продление существования пенумбры • Продление времени жизни пенумбры увеличит терапевтическое окно • Потенциальные возможности «заморозить пенумбру» : 1. Гипотермия перед началом ТЛТ 2. Использование нейропротекции до начала проведения ТЛТ

Гипотермия 33 -35ºС • Улучшает выживаемость нейронов коры и глубоких слоев • Уменьшает объем повреждения мозга • Улучшает клинический исход De Georgia M. A. , et al Cooling for acute ischemic brain damage (COOL AID): A feasibility trial of endovascular cooling // Neurology. — 2004. — 63. — 312 -317.

Эндоваскулярная гипотермия N. Bornstein, 2007

Гипотермия • Умеренная и мягкая гипотермия (32 -350 C) – доказаны протективные свойства – пассивное охлаждение, лед, в/в растворы – использование катетеров • Глубокая гипотермия (< 270 C) – аритмия – кровотечения – серьезные метаболические расстройства

Гипотермия при инсульте + • Эндоваскулярная гипотермия при инсульте безопасна и хорошо переносится больными • Эндоваскулярное охлаждение до 33°C эффективно и безопасно • Уменьшает степень прироста ишемического очага • Необходимы дальнейшие исследования

Гипотермия при инсульте ? • Протокол гипотермии при инсульте • Рамки «терапевтического окна» • Оптимальная температура De Georgia M. A. , et al Cooling for acute ischemic brain damage (COOL AID): A feasibility trial of endovascular cooling // Neurology 2004. 63. — 312 -317.

Гипербарическая оксигенация

Гипербарическая оксигенация • Усиление синтеза свободных радикалов • Усиление процессов ПОЛ • Улучшение доставки О 2 к пенумбре • Увеличение функциональной активности жизнеспособной ткани • Уменьшение объема инфаркта • Улучшение функционального восстановления

Ишемическое прекондиционирование • Предшествующие эпизоды ишемии уменьшают повреждающее действие при инсульте/инфаркте миокарда • Исследовалось 1707 пациентов с инсультом и ТИА в анамнезе • Не выявлено влияния ИП на течение и прогноз инсульта ! Невозможность клинических испытаний ИП ввиду потенциального вреда Йохнстон С. К. и соавт. Stroke, 2005

ПЕРСПЕКТИВЫ развития нейропротективной терапии • Использование на фоне выверенной базисной терапии • Раннее начало (в первые минуты/часы) • Использование комбинированных препаратов, воздействующих на разные звенья патогенеза ишемии • Использование в эксперименте моделей, максимально близких к человеку • Использование на фоне реперфузионной терапии

ПЕРСПЕКТИВЫ развития нейропротективной терапии II. Использование в эксперименте моделей, максимально близких к человеку • Использование «пожилых» приматов • Ремоделирование АГ • Ремоделирование СД

New avenues in neuroprotection • Treat as early as possible • Use imaging to select appropriate candidates • Combine neuroprotectant with rt-PA • Promote recovery mechanisms (growth factors, neurotrophic factors, stem cells) • Severe strokes: hypothermia, decompression N. Bornstein, 2008

Перспективные направления нейропротективной и репаративной терапии • Генотерапия - Стабильные аналоги эндогенных нейротрофинов (рекомбинация ДНК) - Генетически модифицированные клетки - источники непрерывной доставки трофических факторов - Молекулярные эффекторы, временно выключающие апоптоз (Erks, HSP-70, bcl-2, bcl-x и др. ) - Регуляторы расщепления ДНК • Стволовые клеточные технологии - Индукция эндогенных стволовых клеток и активация путей их миграции - Трансплантация экзогенных стволовых клеток (? )
ФУВ_нейропротекция.ppt