Заняття4.ppt
- Количество слайдов: 16
 НЕІЗОГІПСИЧНІ ПЕРЕТВОРЕННЯ ФУНКЦІОНАЛЬНИХ ГРУП РЕАКЦІЇ ВІДНОВЛЕННЯ Сучасні методи органічного синтезу
НЕІЗОГІПСИЧНІ ПЕРЕТВОРЕННЯ ФУНКЦІОНАЛЬНИХ ГРУП РЕАКЦІЇ ВІДНОВЛЕННЯ Сучасні методи органічного синтезу
 Алюмогідридні реагенти Li. Al. H 4 ØВідновлює велику кількість функціональних груп ØRCOCl (та ін. ): можна зупинити на альдегіді RCOCl RCOOCOR’ RCHO RCOR’ RCOOR’ RCN RCONR’ 2 RCOOH ØОб’ємний Imines etc. ØРеакція йде гетерогенно, розчинники – етери ØЗавжди використовується у невеликому надлишку Li. Al. Н(Ot-Bu)3 ØЗа реакційною здатністю нагадує Na. BH 4 (крім деяких естерів) ØРозчинний в етерах Red-Al (Na. Al. H 2(OCH 2 OCH 3)2) ØЗа реакційною здатністю дуже нагадує Li. Al. H 4 ØРозчинний в етерах, бензені та толуені ØМожна використовувати зворотний порядок змішування 2 ØЕфективний для RCOOH, RCl(Br, I), ROSO 2 R’ RCl(Br, I) Epoxides RNO 2 RN 3
Алюмогідридні реагенти Li. Al. H 4 ØВідновлює велику кількість функціональних груп ØRCOCl (та ін. ): можна зупинити на альдегіді RCOCl RCOOCOR’ RCHO RCOR’ RCOOR’ RCN RCONR’ 2 RCOOH ØОб’ємний Imines etc. ØРеакція йде гетерогенно, розчинники – етери ØЗавжди використовується у невеликому надлишку Li. Al. Н(Ot-Bu)3 ØЗа реакційною здатністю нагадує Na. BH 4 (крім деяких естерів) ØРозчинний в етерах Red-Al (Na. Al. H 2(OCH 2 OCH 3)2) ØЗа реакційною здатністю дуже нагадує Li. Al. H 4 ØРозчинний в етерах, бензені та толуені ØМожна використовувати зворотний порядок змішування 2 ØЕфективний для RCOOH, RCl(Br, I), ROSO 2 R’ RCl(Br, I) Epoxides RNO 2 RN 3
 Борогідридні реагенти Na. BH 4 ØРозчинний в етерах RCOCl RCOOCOR’ RCHO RCOR’ RCOOR’ RCN RCONR’ 2 RCOOH ØСтандартний реагент для відновлення оксазолідинонів Еванса Imines etc. ØВідновлює найактивніші карбонільні сполуки, іміни і т. п. ØАміди: перетворення на хлороімінієві солі ØРозчинний у воді, спиртах (повільно реагує з ними) Li. BН 4 ØБільш активний за Na. BH 4 : відновлює всі естери Реагент Люше (Na. BН 4 – Ce. Cl 3) ØЗагальний реагент для селективного 1, 2 -відновлення , -ненасичених альдегідів та кетонів ØРозчинники – спирти 3 ROSO 2 R’ RCl(Br, I) Epoxides RNO 2 RN 3
Борогідридні реагенти Na. BH 4 ØРозчинний в етерах RCOCl RCOOCOR’ RCHO RCOR’ RCOOR’ RCN RCONR’ 2 RCOOH ØСтандартний реагент для відновлення оксазолідинонів Еванса Imines etc. ØВідновлює найактивніші карбонільні сполуки, іміни і т. п. ØАміди: перетворення на хлороімінієві солі ØРозчинний у воді, спиртах (повільно реагує з ними) Li. BН 4 ØБільш активний за Na. BH 4 : відновлює всі естери Реагент Люше (Na. BН 4 – Ce. Cl 3) ØЗагальний реагент для селективного 1, 2 -відновлення , -ненасичених альдегідів та кетонів ØРозчинники – спирти 3 ROSO 2 R’ RCl(Br, I) Epoxides RNO 2 RN 3
 Борогідридні реагенти Na. BH(OAc)3, Na. BH 3 CN ØРеагенти відновного амінування альдегідів та кетонів ØNa. BH(OAc)3 використовується в DCE, потрібен надлишок ØNa. BH 3 CN чутливий до р. Н (оптимально 5– 6), може використовувуватися у різних полярних розчинниках Супергідрид (Li. TEBH, Li. BНEt 3) ØНайактивніший з гідридних відновників ØРозчинний в етерах ØМає яскраво виражений нуклеофільний характер, дає чисті SN 2 реакції ØПорівняно об’ємний Селектриди ØДуже об’ємні, працюють при низьких температурах K-selectride: KBH(sec-Bu)3 4 KS-selectride: KBH(Sia)3 L-selectride: Li. BH(sec-Bu)3 LS-selectride: LBH(Sia)3 RCOCl RCOOCOR’ RCHO RCOR’ RCOOR’ RCN RCONR’ 2 RCOOH Imines etc. ROSO 2 R’ RCl(Br, I) Epoxides RNO 2 RN 3
Борогідридні реагенти Na. BH(OAc)3, Na. BH 3 CN ØРеагенти відновного амінування альдегідів та кетонів ØNa. BH(OAc)3 використовується в DCE, потрібен надлишок ØNa. BH 3 CN чутливий до р. Н (оптимально 5– 6), може використовувуватися у різних полярних розчинниках Супергідрид (Li. TEBH, Li. BНEt 3) ØНайактивніший з гідридних відновників ØРозчинний в етерах ØМає яскраво виражений нуклеофільний характер, дає чисті SN 2 реакції ØПорівняно об’ємний Селектриди ØДуже об’ємні, працюють при низьких температурах K-selectride: KBH(sec-Bu)3 4 KS-selectride: KBH(Sia)3 L-selectride: Li. BH(sec-Bu)3 LS-selectride: LBH(Sia)3 RCOCl RCOOCOR’ RCHO RCOR’ RCOOR’ RCN RCONR’ 2 RCOOH Imines etc. ROSO 2 R’ RCl(Br, I) Epoxides RNO 2 RN 3
 Алюмо/борогідридні відновники електрофільного характеру Боран (BH 3–THF, BH 3–Me 2 S, Na. BH 4–BF 3 Et 2 O) ØНітрили: до альдегідів RCOCl RCOOCOR’ RCHO RCOR’ RCOOR’ RCN RCONR’ 2 RCOOH ØЕстери: до альдегідів при – 78 С, до спиртів при 0 С Imines etc. ØЛактони: до лактолів ROSO 2 R’ RCl(Br, I) Epoxides ØВідновлює карбонові кислоти, третинні аміди, альдегіди, кетони, лактони, епоксиди, нітрили ØШвидко реагує з кратними зв’язками DIBAL (i-Bu 2 Al. H) ØСелективне 1, 2 -відновлення , -ненасичених сполук ØАльдегіди, кетони та активні похідні карбонових кислот також відновлюються – не використовується ØПриєднується до потрійних зв’язків 5 RNO 2 RN 3
Алюмо/борогідридні відновники електрофільного характеру Боран (BH 3–THF, BH 3–Me 2 S, Na. BH 4–BF 3 Et 2 O) ØНітрили: до альдегідів RCOCl RCOOCOR’ RCHO RCOR’ RCOOR’ RCN RCONR’ 2 RCOOH ØЕстери: до альдегідів при – 78 С, до спиртів при 0 С Imines etc. ØЛактони: до лактолів ROSO 2 R’ RCl(Br, I) Epoxides ØВідновлює карбонові кислоти, третинні аміди, альдегіди, кетони, лактони, епоксиди, нітрили ØШвидко реагує з кратними зв’язками DIBAL (i-Bu 2 Al. H) ØСелективне 1, 2 -відновлення , -ненасичених сполук ØАльдегіди, кетони та активні похідні карбонових кислот також відновлюються – не використовується ØПриєднується до потрійних зв’язків 5 RNO 2 RN 3
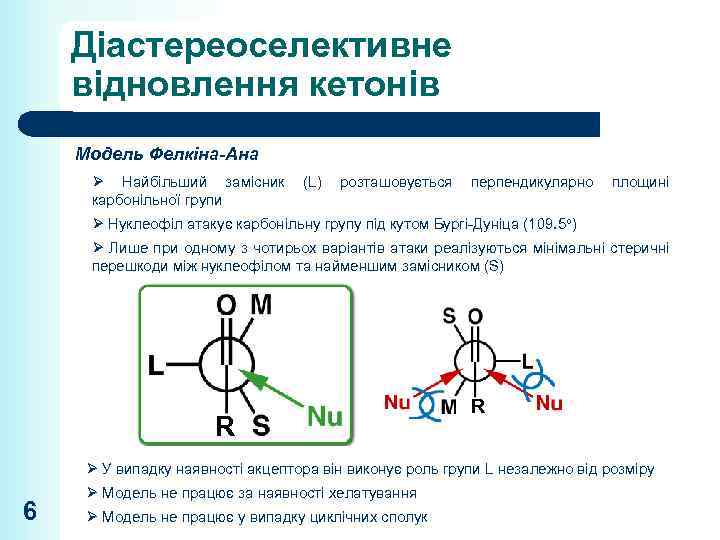 Діастереоселективне відновлення кетонів Модель Фелкіна-Ана Ø Найбільший замісник карбонільної групи (L) розташовується перпендикулярно площині Ø Нуклеофіл атакує карбонільну групу під кутом Бургі-Дуніца (109. 5 ) Ø Лише при одному з чотирьох варіантів атаки реалізуються мінімальні стеричні перешкоди між нуклеофілом та найменшим замісником (S) R R Ø У випадку наявності акцептора він виконує роль групи L незалежно від розміру 6 Ø Модель не працює за наявності хелатування Ø Модель не працює у випадку циклічних сполук
Діастереоселективне відновлення кетонів Модель Фелкіна-Ана Ø Найбільший замісник карбонільної групи (L) розташовується перпендикулярно площині Ø Нуклеофіл атакує карбонільну групу під кутом Бургі-Дуніца (109. 5 ) Ø Лише при одному з чотирьох варіантів атаки реалізуються мінімальні стеричні перешкоди між нуклеофілом та найменшим замісником (S) R R Ø У випадку наявності акцептора він виконує роль групи L незалежно від розміру 6 Ø Модель не працює за наявності хелатування Ø Модель не працює у випадку циклічних сполук
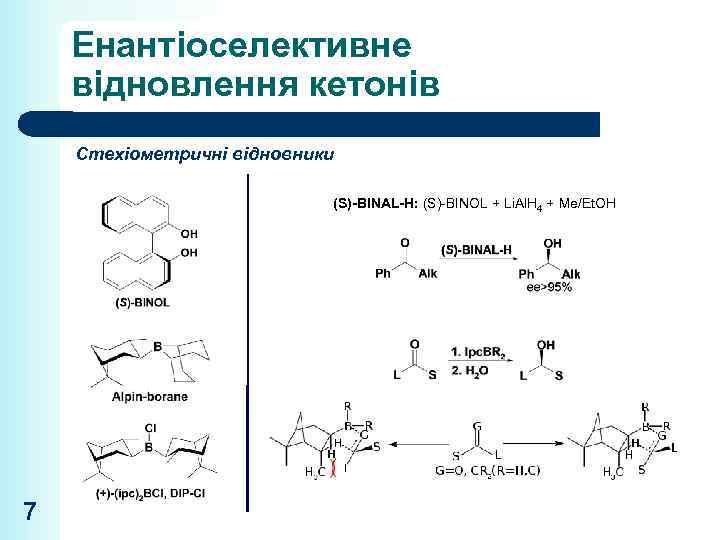 Енантіоселективне відновлення кетонів Стехіометричні відновники (S)-BINAL-H: (S)-BINOL + Li. Al. H 4 + Me/Et. OH 7
Енантіоселективне відновлення кетонів Стехіометричні відновники (S)-BINAL-H: (S)-BINOL + Li. Al. H 4 + Me/Et. OH 7
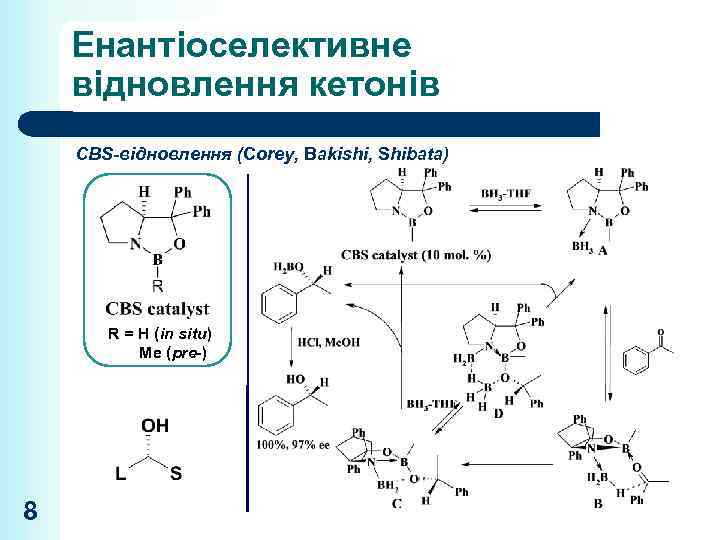 Енантіоселективне відновлення кетонів CBS-відновлення (Corey, Bakishi, Shibata) R = H (in situ) Me (pre-) 8
Енантіоселективне відновлення кетонів CBS-відновлення (Corey, Bakishi, Shibata) R = H (in situ) Me (pre-) 8
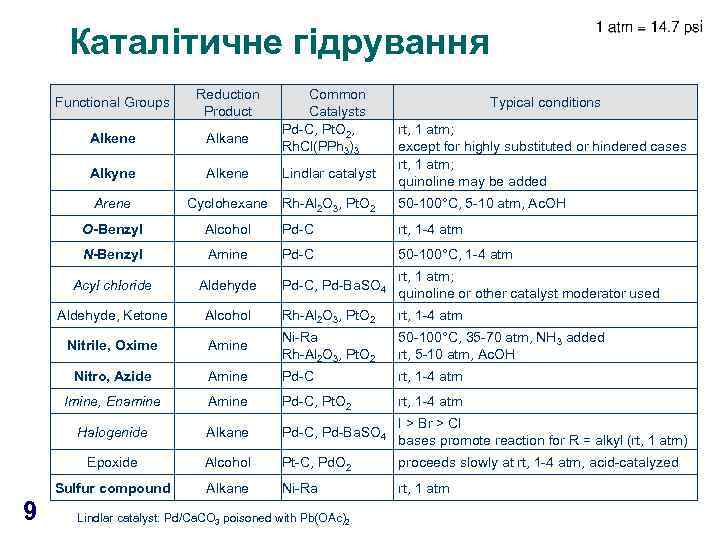 Каталітичне гідрування Functional Groups Reduction Product Alkene Alkane Alkyne Alkene Arene Common Catalysts Pd-C, Pt. O 2, Rh. Cl(PPh 3)3 Lindlar catalyst Cyclohexane Rh-Al 2 O 3, Pt. O 2 Typical conditions rt, 1 atm; except for highly substituted or hindered cases rt, 1 atm; quinoline may be added 50 -100°C, 5 -10 atm, Ac. OH O-Benzyl Pd-C rt, 1 -4 atm N-Benzyl Amine Pd-C 50 -100°C, 1 -4 atm Acyl chloride Aldehyde Pd-C, Pd-Ba. SO 4 rt, 1 atm; quinoline or other catalyst moderator used Aldehyde, Ketone Alcohol Rh-Al 2 O 3, Pt. O 2 rt, 1 -4 atm Nitrile, Oxime Amine Ni-Ra Rh-Al 2 O 3, Pt. O 2 50 -100°C, 35 -70 atm, NH 3 added rt, 5 -10 atm, Ac. OH Nitro, Azide Amine Pd-C rt, 1 -4 atm Imine, Enamine Amine Pd-C, Pt. O 2 rt, 1 -4 atm Halogenide Alkane Pd-C, Pd-Ba. SO 4 I > Br > Cl bases promote reaction for R = alkyl (rt, 1 atm) Epoxide Alcohol Pt-C, Pd. O 2 proceeds slowly at rt, 1 -4 atm, acid-catalyzed Sulfur compound 9 Alcohol Alkane Ni-Ra rt, 1 atm Lindlar catalyst: Pd/Ca. CO 3 poisoned with Pb(OAc)2
Каталітичне гідрування Functional Groups Reduction Product Alkene Alkane Alkyne Alkene Arene Common Catalysts Pd-C, Pt. O 2, Rh. Cl(PPh 3)3 Lindlar catalyst Cyclohexane Rh-Al 2 O 3, Pt. O 2 Typical conditions rt, 1 atm; except for highly substituted or hindered cases rt, 1 atm; quinoline may be added 50 -100°C, 5 -10 atm, Ac. OH O-Benzyl Pd-C rt, 1 -4 atm N-Benzyl Amine Pd-C 50 -100°C, 1 -4 atm Acyl chloride Aldehyde Pd-C, Pd-Ba. SO 4 rt, 1 atm; quinoline or other catalyst moderator used Aldehyde, Ketone Alcohol Rh-Al 2 O 3, Pt. O 2 rt, 1 -4 atm Nitrile, Oxime Amine Ni-Ra Rh-Al 2 O 3, Pt. O 2 50 -100°C, 35 -70 atm, NH 3 added rt, 5 -10 atm, Ac. OH Nitro, Azide Amine Pd-C rt, 1 -4 atm Imine, Enamine Amine Pd-C, Pt. O 2 rt, 1 -4 atm Halogenide Alkane Pd-C, Pd-Ba. SO 4 I > Br > Cl bases promote reaction for R = alkyl (rt, 1 atm) Epoxide Alcohol Pt-C, Pd. O 2 proceeds slowly at rt, 1 -4 atm, acid-catalyzed Sulfur compound 9 Alcohol Alkane Ni-Ra rt, 1 atm Lindlar catalyst: Pd/Ca. CO 3 poisoned with Pb(OAc)2
![Енантіоселективне гідрування кетонів [Ru. Cl 2(benzene)]2 10 Енантіоселективне гідрування кетонів [Ru. Cl 2(benzene)]2 10](https://present5.com/presentation/3/-30038723_129931590.pdf-img/-30038723_129931590.pdf-10.jpg) Енантіоселективне гідрування кетонів [Ru. Cl 2(benzene)]2 10
Енантіоселективне гідрування кетонів [Ru. Cl 2(benzene)]2 10
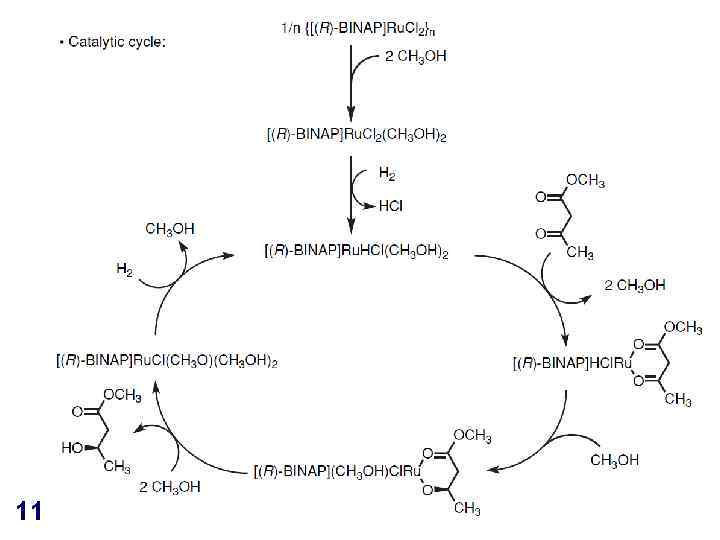 11
11
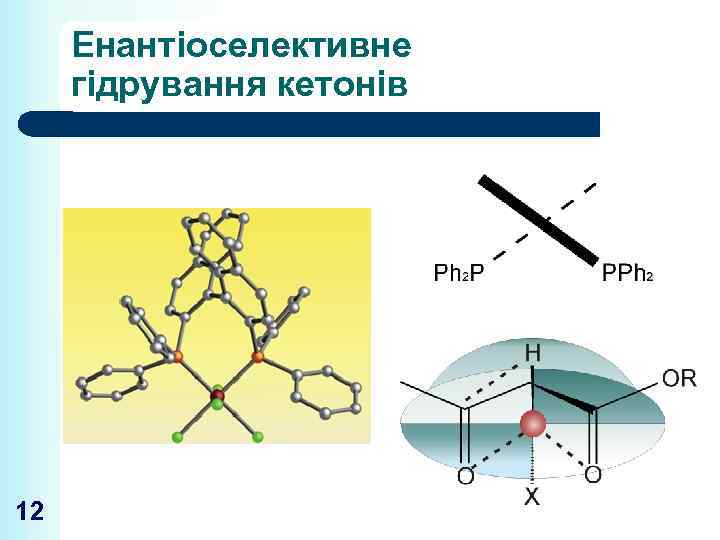 Енантіоселективне гідрування кетонів 12
Енантіоселективне гідрування кетонів 12
![Енантіоселективне гідрування кетонів 1 2 (R, R)-i-Pr-BPE (S)-[2. 2]-PHANEPHOS 3 (S, S)-DPEN 13 (S)-DAIPEN Енантіоселективне гідрування кетонів 1 2 (R, R)-i-Pr-BPE (S)-[2. 2]-PHANEPHOS 3 (S, S)-DPEN 13 (S)-DAIPEN](https://present5.com/presentation/3/-30038723_129931590.pdf-img/-30038723_129931590.pdf-13.jpg) Енантіоселективне гідрування кетонів 1 2 (R, R)-i-Pr-BPE (S)-[2. 2]-PHANEPHOS 3 (S, S)-DPEN 13 (S)-DAIPEN
Енантіоселективне гідрування кетонів 1 2 (R, R)-i-Pr-BPE (S)-[2. 2]-PHANEPHOS 3 (S, S)-DPEN 13 (S)-DAIPEN
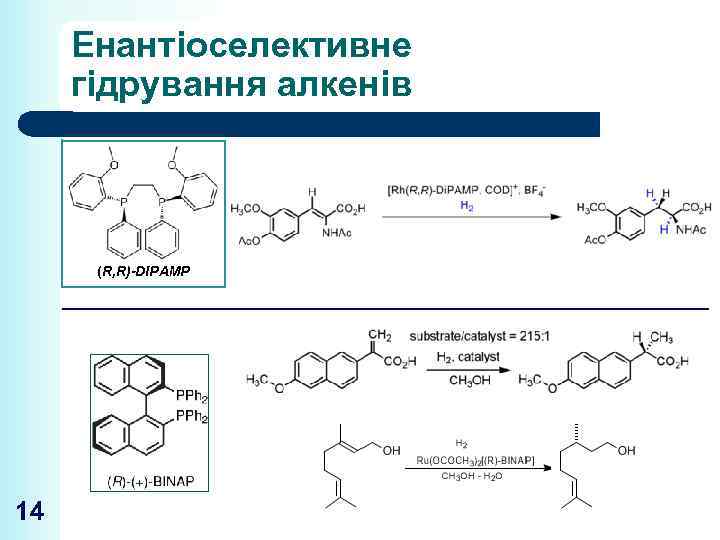 Енантіоселективне гідрування алкенів (R, R)-DIPAMP 14
Енантіоселективне гідрування алкенів (R, R)-DIPAMP 14
 Метали та їх сполуки як відновники Li/Na, RNH 2/NH 3 ØАнти-відновлення алкінів ØРеакція Берча Zn (пил), Zn-Cu ØВідновлення активованих галогенідів, дегалогенування Bu 3 Sn. H/AIBN ØСелективне відновлення галогенідів ØДеоксигенування спиртів за Бартоном (О-тіокарбонати) Амальгама алюмінію ØСелективне відновлення сульфонів 15
Метали та їх сполуки як відновники Li/Na, RNH 2/NH 3 ØАнти-відновлення алкінів ØРеакція Берча Zn (пил), Zn-Cu ØВідновлення активованих галогенідів, дегалогенування Bu 3 Sn. H/AIBN ØСелективне відновлення галогенідів ØДеоксигенування спиртів за Бартоном (О-тіокарбонати) Амальгама алюмінію ØСелективне відновлення сульфонів 15
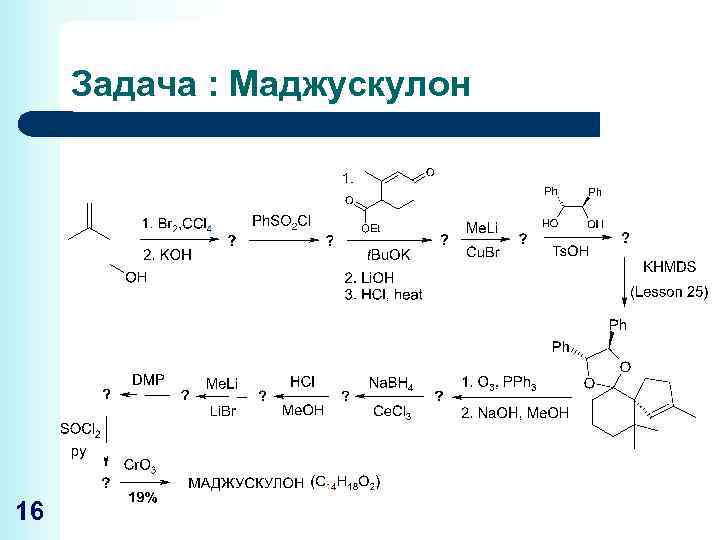 Задача : Маджускулон 16
Задача : Маджускулон 16


