Заняття3.ppt
- Количество слайдов: 19
 НЕІЗОГІПСИЧНІ ПЕРЕТВОРЕННЯ ФУНКЦІОНАЛЬНИХ ГРУП РЕАКЦІЇ ОКИСНЕННЯ Сучасні методи органічного синтезу “Modern Oxidation Methods” Ed. : Bäckvall, J. -E. Wiley-VCH, Weinheim, 2004
НЕІЗОГІПСИЧНІ ПЕРЕТВОРЕННЯ ФУНКЦІОНАЛЬНИХ ГРУП РЕАКЦІЇ ОКИСНЕННЯ Сучасні методи органічного синтезу “Modern Oxidation Methods” Ed. : Bäckvall, J. -E. Wiley-VCH, Weinheim, 2004
 Класифікація функціональних груп Рівень 0 2 Рівень 1 Рівень 2 Рівень 3
Класифікація функціональних груп Рівень 0 2 Рівень 1 Рівень 2 Рівень 3
 Окиснення спиртів ØРеагент Джонса (Cr. O 3–H 2 SO 4–ацетон, до кислоти) ØРеагент Колінза (Cr. O 3–py) ØPCC (py. H+Cr. O 3 Cl–) ØPDC ((py. H)2 Cr 2 O 7) ØРеагент Сверна (DMSO–(COCl)2) ØРеагент Паріх-Дерінга (DMSO–SO 3–py/TEA) ØРеагент Пфіцнера-Моффата (DMSO–DCC/EDC) ØMn. O 2 ØРеагент Десса-Мартіна ØIBX (2 -йодоксибензойна кислота) ØРеагент Лея (TPAP–NMO, NPr 4 Ru. O 4 – N-оксид N-метилморфоліну) ØRu. Cl 3–Na. IO 4 (до кислоти) 3 ØTEMPO–Na. Cl. O тощо (до кислоти, іноді до альдегіду)
Окиснення спиртів ØРеагент Джонса (Cr. O 3–H 2 SO 4–ацетон, до кислоти) ØРеагент Колінза (Cr. O 3–py) ØPCC (py. H+Cr. O 3 Cl–) ØPDC ((py. H)2 Cr 2 O 7) ØРеагент Сверна (DMSO–(COCl)2) ØРеагент Паріх-Дерінга (DMSO–SO 3–py/TEA) ØРеагент Пфіцнера-Моффата (DMSO–DCC/EDC) ØMn. O 2 ØРеагент Десса-Мартіна ØIBX (2 -йодоксибензойна кислота) ØРеагент Лея (TPAP–NMO, NPr 4 Ru. O 4 – N-оксид N-метилморфоліну) ØRu. Cl 3–Na. IO 4 (до кислоти) 3 ØTEMPO–Na. Cl. O тощо (до кислоти, іноді до альдегіду)
 Окиснення карбонільних сполук Окиснення альдегідів ØРеагент Джонса (Cr. O 3–H 2 SO 4–ацетон) ØAg 2 O–Na. OH ØРеагент Пінніка (Na. Cl. O 2–(Na 2 HPO 4)– 2, 3 -диметилбутен) ØMn. O 2–Na. CN Окиснення кетонів З розривом С–С зв’язку ØОкиснення за Байєром-Вілігером (MCPBA тощо) ØГалоформна реакція (Na. Cl. O/Na. Br. O) За -положенням ØОкиснення Se. O 2 Ø Окиснення за Руботтомом 4 ØОкиснення за Саегусою – Іто (Si-енолят, Pd(OAc)2–(інший окисник)) (Si-енолят, MCPBA) ØОкиснення оксазиридином Девіса
Окиснення карбонільних сполук Окиснення альдегідів ØРеагент Джонса (Cr. O 3–H 2 SO 4–ацетон) ØAg 2 O–Na. OH ØРеагент Пінніка (Na. Cl. O 2–(Na 2 HPO 4)– 2, 3 -диметилбутен) ØMn. O 2–Na. CN Окиснення кетонів З розривом С–С зв’язку ØОкиснення за Байєром-Вілігером (MCPBA тощо) ØГалоформна реакція (Na. Cl. O/Na. Br. O) За -положенням ØОкиснення Se. O 2 Ø Окиснення за Руботтомом 4 ØОкиснення за Саегусою – Іто (Si-енолят, Pd(OAc)2–(інший окисник)) (Si-енолят, MCPBA) ØОкиснення оксазиридином Девіса
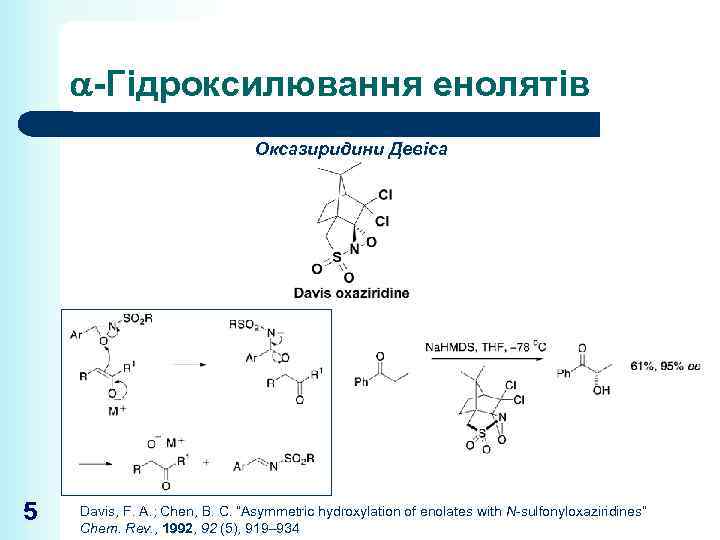 -Гідроксилювання енолятів Оксазиридини Девіса 5 Davis, F. A. ; Chen, B. C. “Asymmetric hydroxylation of enolates with N-sulfonyloxaziridines” Chem. Rev. , 1992, 92 (5), 919– 934
-Гідроксилювання енолятів Оксазиридини Девіса 5 Davis, F. A. ; Chen, B. C. “Asymmetric hydroxylation of enolates with N-sulfonyloxaziridines” Chem. Rev. , 1992, 92 (5), 919– 934
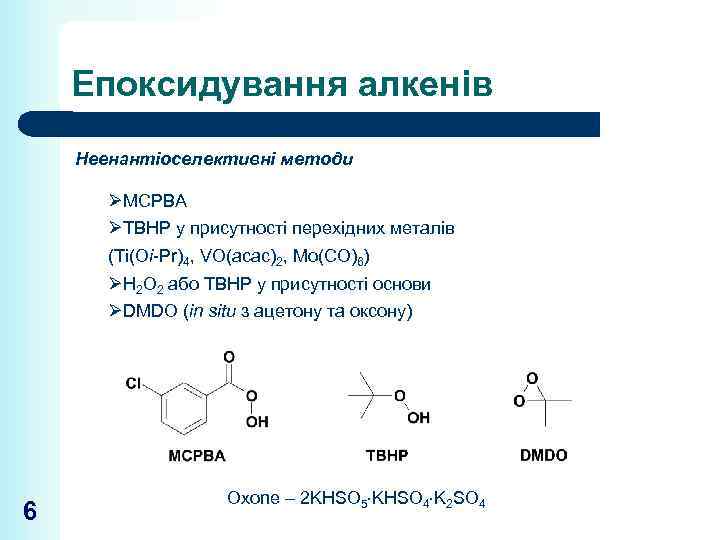 Епоксидування алкенів Неенантіоселективні методи ØMCPBA ØTBHP у присутності перехідних металів (Ti(Oi-Pr)4, VO(acac)2, Mo(CO)6) ØH 2 O 2 або TBHP у присутності основи ØDMDO (in situ з ацетону та оксону) 6 Oxone – 2 KHSO 5 KHSO 4 K 2 SO 4
Епоксидування алкенів Неенантіоселективні методи ØMCPBA ØTBHP у присутності перехідних металів (Ti(Oi-Pr)4, VO(acac)2, Mo(CO)6) ØH 2 O 2 або TBHP у присутності основи ØDMDO (in situ з ацетону та оксону) 6 Oxone – 2 KHSO 5 KHSO 4 K 2 SO 4
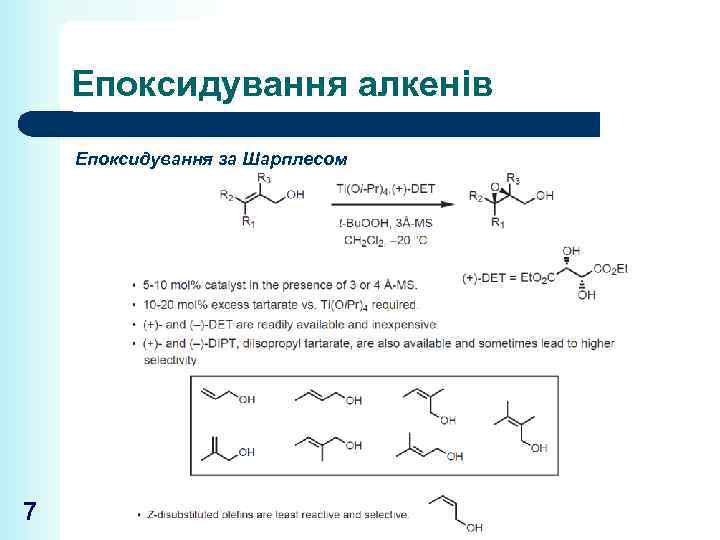 Епоксидування алкенів Епоксидування за Шарплесом 7
Епоксидування алкенів Епоксидування за Шарплесом 7
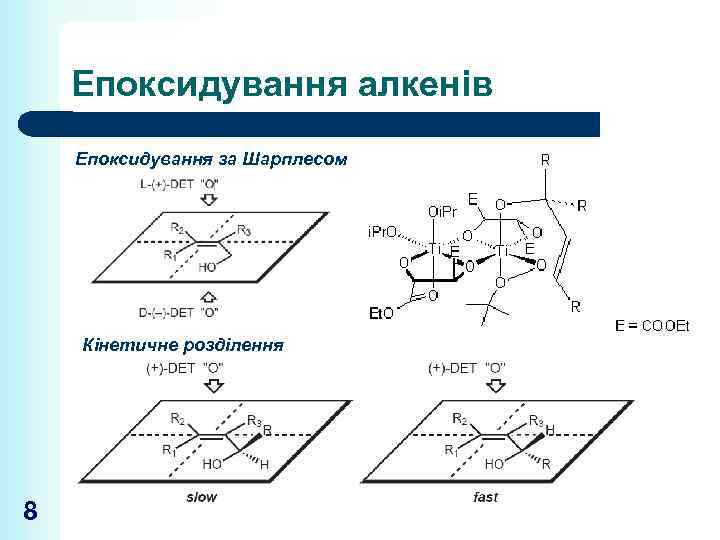 Епоксидування алкенів Епоксидування за Шарплесом Кінетичне розділення 8
Епоксидування алкенів Епоксидування за Шарплесом Кінетичне розділення 8
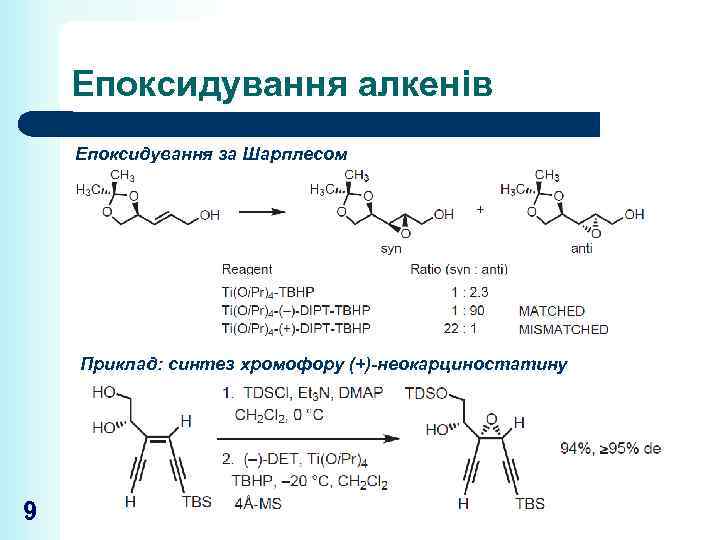 Епоксидування алкенів Епоксидування за Шарплесом Приклад: синтез хромофору (+)-неокарциностатину 9
Епоксидування алкенів Епоксидування за Шарплесом Приклад: синтез хромофору (+)-неокарциностатину 9
 Епоксидування алкенів Епоксидування за Якобсеном • Теrminal olefins are poor substrates. • A lot of trisubstituted alkenes are epoxidized with high levels of enantioselectivity • High enantioselectivities are not yet general for tetrasubstituted alkenes but may be attained in certain cases 10
Епоксидування алкенів Епоксидування за Якобсеном • Теrminal olefins are poor substrates. • A lot of trisubstituted alkenes are epoxidized with high levels of enantioselectivity • High enantioselectivities are not yet general for tetrasubstituted alkenes but may be attained in certain cases 10
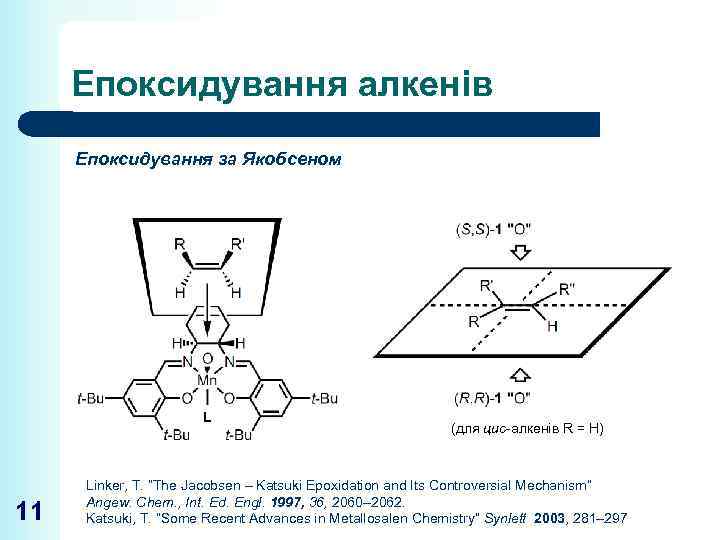 Епоксидування алкенів Епоксидування за Якобсеном L 11 (для цис-алкенів R = H) Linker, T. “The Jacobsen – Katsuki Epoxidation and Its Controversial Mechanism” Angew. Chem. , Int. Ed. Engl. 1997, 36, 2060– 2062. Katsuki, T. “Some Recent Advances in Metallosalen Chemistry” Synlett 2003, 281– 297
Епоксидування алкенів Епоксидування за Якобсеном L 11 (для цис-алкенів R = H) Linker, T. “The Jacobsen – Katsuki Epoxidation and Its Controversial Mechanism” Angew. Chem. , Int. Ed. Engl. 1997, 36, 2060– 2062. Katsuki, T. “Some Recent Advances in Metallosalen Chemistry” Synlett 2003, 281– 297
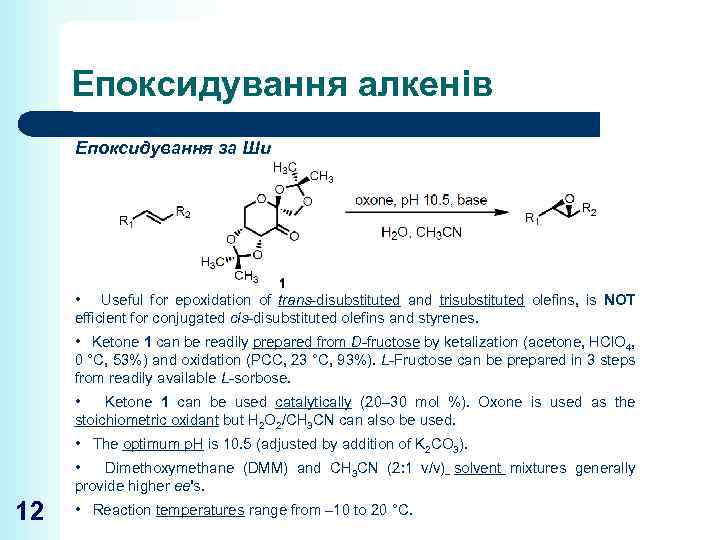 Епоксидування алкенів Епоксидування за Ши • Useful for epoxidation of trans-disubstituted and trisubstituted olefins, is NOT efficient for conjugated cis-disubstituted olefins and styrenes. • Ketone 1 can be readily prepared from D-fructose by ketalization (acetone, HCl. O 4, 0 °C, 53%) and oxidation (PCC, 23 °C, 93%). L-Fructose can be prepared in 3 steps from readily available L-sorbose. • Ketone 1 can be used catalytically (20– 30 mol %). Oxone is used as the stoichiometric oxidant but H 2 O 2/CH 3 CN can also be used. • The optimum p. H is 10. 5 (adjusted by addition of K 2 CO 3). • Dimethoxymethane (DMM) and CH 3 CN (2: 1 v/v) solvent mixtures generally provide higher ee's. 12 • Reaction temperatures range from – 10 to 20 °C.
Епоксидування алкенів Епоксидування за Ши • Useful for epoxidation of trans-disubstituted and trisubstituted olefins, is NOT efficient for conjugated cis-disubstituted olefins and styrenes. • Ketone 1 can be readily prepared from D-fructose by ketalization (acetone, HCl. O 4, 0 °C, 53%) and oxidation (PCC, 23 °C, 93%). L-Fructose can be prepared in 3 steps from readily available L-sorbose. • Ketone 1 can be used catalytically (20– 30 mol %). Oxone is used as the stoichiometric oxidant but H 2 O 2/CH 3 CN can also be used. • The optimum p. H is 10. 5 (adjusted by addition of K 2 CO 3). • Dimethoxymethane (DMM) and CH 3 CN (2: 1 v/v) solvent mixtures generally provide higher ee's. 12 • Reaction temperatures range from – 10 to 20 °C.
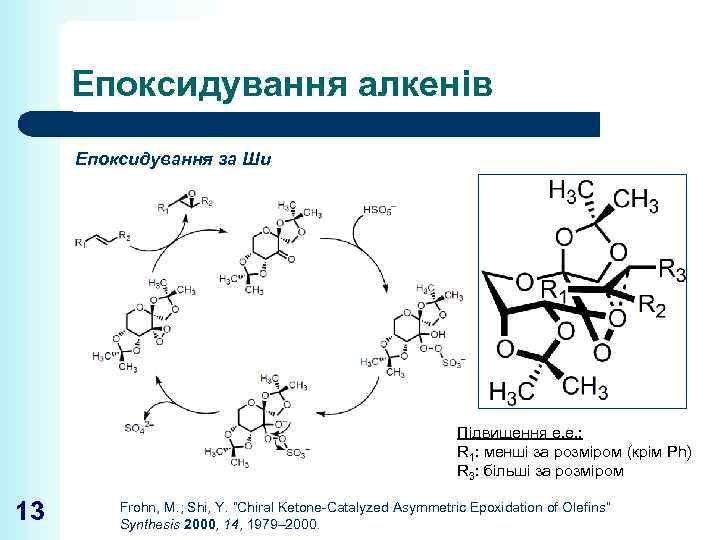 Епоксидування алкенів Епоксидування за Ши Підвищення е. е. : R 1: менші за розміром (крім Ph) R 3: більші за розміром 13 Frohn, M. ; Shi, Y. “Chiral Ketone-Catalyzed Asymmetric Epoxidation of Olefins” Synthesis 2000, 14, 1979– 2000.
Епоксидування алкенів Епоксидування за Ши Підвищення е. е. : R 1: менші за розміром (крім Ph) R 3: більші за розміром 13 Frohn, M. ; Shi, Y. “Chiral Ketone-Catalyzed Asymmetric Epoxidation of Olefins” Synthesis 2000, 14, 1979– 2000.
 Цис-гідроксилювання алкенів Неенантіоселективні методи Ø Os. O 4 – окисник, що використовується найчастіше Ø Використовується без співокисника або разом з хлоратами (KCl. O 3, Ba(Cl. O 3)2) та N-оксидами (NMO, Me 3 N+O–) Ø Іноді додають піридин або TMEDA Енантіоселектвне гідроксилювання за Шарплесом AD-mix- K 3 Fe(CN)6 (3 mmol) K 2 CO 3 (3 mmol) (DHQ)2 -PHAL (0. 01 mmol) K 2 Os. O 2(OH)4 (0. 002 mmol) AD-mix-β K 3 Fe(CN)6 (3 mmol) K 2 CO 3 (3 mmol) (DHQD)2 -PHAL (0. 01 mmol) K 2 Os. O 2(OH)4 (0. 002 mmol) Умови: алкен (1 ммоль), t-Bu. OH – H 2 O (1: 1), 0 °C, 6 – 24 h 14
Цис-гідроксилювання алкенів Неенантіоселективні методи Ø Os. O 4 – окисник, що використовується найчастіше Ø Використовується без співокисника або разом з хлоратами (KCl. O 3, Ba(Cl. O 3)2) та N-оксидами (NMO, Me 3 N+O–) Ø Іноді додають піридин або TMEDA Енантіоселектвне гідроксилювання за Шарплесом AD-mix- K 3 Fe(CN)6 (3 mmol) K 2 CO 3 (3 mmol) (DHQ)2 -PHAL (0. 01 mmol) K 2 Os. O 2(OH)4 (0. 002 mmol) AD-mix-β K 3 Fe(CN)6 (3 mmol) K 2 CO 3 (3 mmol) (DHQD)2 -PHAL (0. 01 mmol) K 2 Os. O 2(OH)4 (0. 002 mmol) Умови: алкен (1 ммоль), t-Bu. OH – H 2 O (1: 1), 0 °C, 6 – 24 h 14
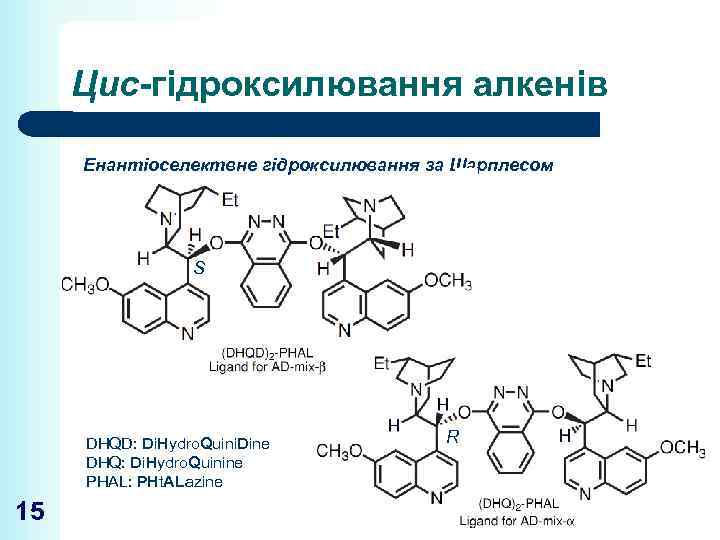 Цис-гідроксилювання алкенів Енантіоселектвне гідроксилювання за Шарплесом S DHQD: Di. Hydro. Quini. Dine DHQ: Di. Hydro. Quinine PHAL: PHt. ALazine 15 R
Цис-гідроксилювання алкенів Енантіоселектвне гідроксилювання за Шарплесом S DHQD: Di. Hydro. Quini. Dine DHQ: Di. Hydro. Quinine PHAL: PHt. ALazine 15 R
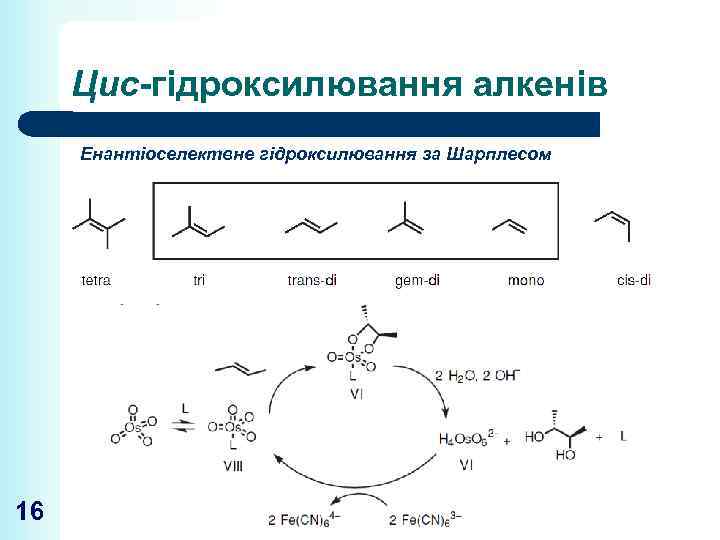 Цис-гідроксилювання алкенів Енантіоселектвне гідроксилювання за Шарплесом 16
Цис-гідроксилювання алкенів Енантіоселектвне гідроксилювання за Шарплесом 16
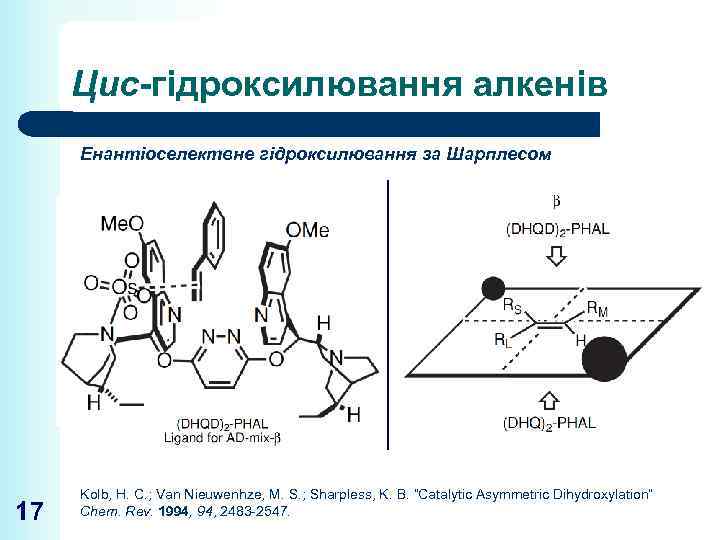 Цис-гідроксилювання алкенів Енантіоселектвне гідроксилювання за Шарплесом 17 Kolb, H. C. ; Van Nieuwenhze, M. S. ; Sharpless, K. B. “Catalytic Asymmetric Dihydroxylation” Chem. Rev. 1994, 2483 -2547.
Цис-гідроксилювання алкенів Енантіоселектвне гідроксилювання за Шарплесом 17 Kolb, H. C. ; Van Nieuwenhze, M. S. ; Sharpless, K. B. “Catalytic Asymmetric Dihydroxylation” Chem. Rev. 1994, 2483 -2547.
 Інші реакції окиснення Окиснення алкенів з розривом С=С зв’язку (а також 1, 2 -діолів тощо) ØОзон (O 3, Me 2 S) ØРеагент Лем’є – Джонсона (Os. O 4 – Na. IO 4) ØPb(OAc)4 ØRu. Cl 3–Na. IO 4 Алільне окиснення алкенів ØNBS ØSe. O 2 Окиснення ароматичних сполук до хінонів 18 ØCAN (церійамонійнітрат, (NH 4)2 Ce(NO 3)6) ØPh. I(OCOCF 3)2 ØІснує до десятка реагентів, всі не універсальні
Інші реакції окиснення Окиснення алкенів з розривом С=С зв’язку (а також 1, 2 -діолів тощо) ØОзон (O 3, Me 2 S) ØРеагент Лем’є – Джонсона (Os. O 4 – Na. IO 4) ØPb(OAc)4 ØRu. Cl 3–Na. IO 4 Алільне окиснення алкенів ØNBS ØSe. O 2 Окиснення ароматичних сполук до хінонів 18 ØCAN (церійамонійнітрат, (NH 4)2 Ce(NO 3)6) ØPh. I(OCOCF 3)2 ØІснує до десятка реагентів, всі не універсальні
 Окиснення елементорганічних сполук Окиснення сульфурвмісних сполук ØNa. IO 4 (сульфід до сульфоксиду) ØRu. Cl 3–Na. IO 4 (сульфіт до сульфату) ØMCPBA (сульфід до сульфоксиду або сульфону) ØH 2 O 2 (сульфід до сульфону) ØОксазиридин Девіса (сульфід до сульфоксиду) Окиснення за Тамао-Флемінгом 19 Fleming, I. ; Henning, R. ; Parker, D. C. ; Plaut, H. E. ; Sanderson, P. E. J. “The phenyldimethylsilyl group as a masked hydroxy group” J. Chem. Soc. Perkin Trans. 1, 1995, 317 -337
Окиснення елементорганічних сполук Окиснення сульфурвмісних сполук ØNa. IO 4 (сульфід до сульфоксиду) ØRu. Cl 3–Na. IO 4 (сульфіт до сульфату) ØMCPBA (сульфід до сульфоксиду або сульфону) ØH 2 O 2 (сульфід до сульфону) ØОксазиридин Девіса (сульфід до сульфоксиду) Окиснення за Тамао-Флемінгом 19 Fleming, I. ; Henning, R. ; Parker, D. C. ; Plaut, H. E. ; Sanderson, P. E. J. “The phenyldimethylsilyl group as a masked hydroxy group” J. Chem. Soc. Perkin Trans. 1, 1995, 317 -337


