Неидеальные растворы.ppt
- Количество слайдов: 24
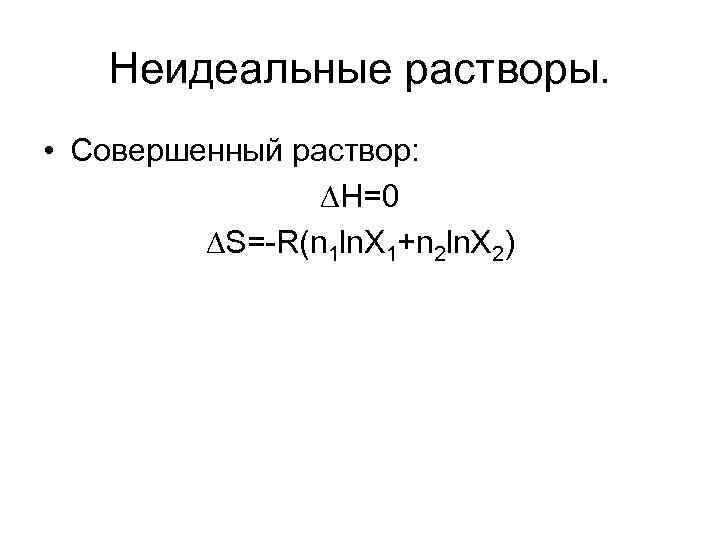 Неидеальные растворы. • Совершенный раствор: Н=0 S=-R(n 1 ln. X 1+n 2 ln. X 2)
Неидеальные растворы. • Совершенный раствор: Н=0 S=-R(n 1 ln. X 1+n 2 ln. X 2)
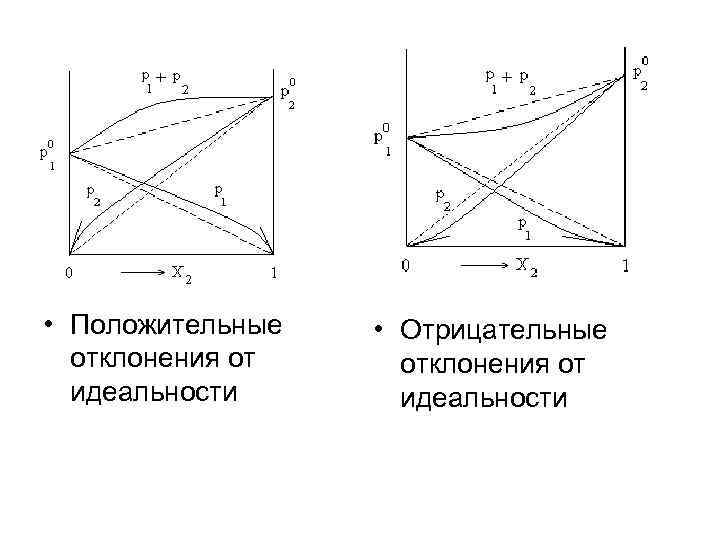 • Положительные отклонения от идеальности • Отрицательные отклонения от идеальности
• Положительные отклонения от идеальности • Отрицательные отклонения от идеальности
 • Требования к основной характеристике реальных растворов: 1) через нее должны просто выражаться все т/д свойства раствора; 2) в предельных случаях (для идеальных растворов) она должна совпадать с концентрацией, а в реальных растворах показывать степень отклонения от идеальности; 3) с ее помощью желательно сохранить форму уравнений, выражающих законы идеальных растворов.
• Требования к основной характеристике реальных растворов: 1) через нее должны просто выражаться все т/д свойства раствора; 2) в предельных случаях (для идеальных растворов) она должна совпадать с концентрацией, а в реальных растворах показывать степень отклонения от идеальности; 3) с ее помощью желательно сохранить форму уравнений, выражающих законы идеальных растворов.
 • Термодинамическая активность Химический потенциал для компонента совершенного раствора Химический потенциал для компонента разбавленного раствора Химический потенциал компонента реального раствора (1)
• Термодинамическая активность Химический потенциал для компонента совершенного раствора Химический потенциал для компонента разбавленного раствора Химический потенциал компонента реального раствора (1)
 • - химический потенциал компонента в стандартном состоянии • Для совершенных растворов • Для разбавленных растворов
• - химический потенциал компонента в стандартном состоянии • Для совершенных растворов • Для разбавленных растворов
 • Компонент находится в реальном растворе и в паре над раствором. При равновесии: Для стандартного состояния: Вычитая из первого уравнения второе, получим:
• Компонент находится в реальном растворе и в паре над раствором. При равновесии: Для стандартного состояния: Вычитая из первого уравнения второе, получим:
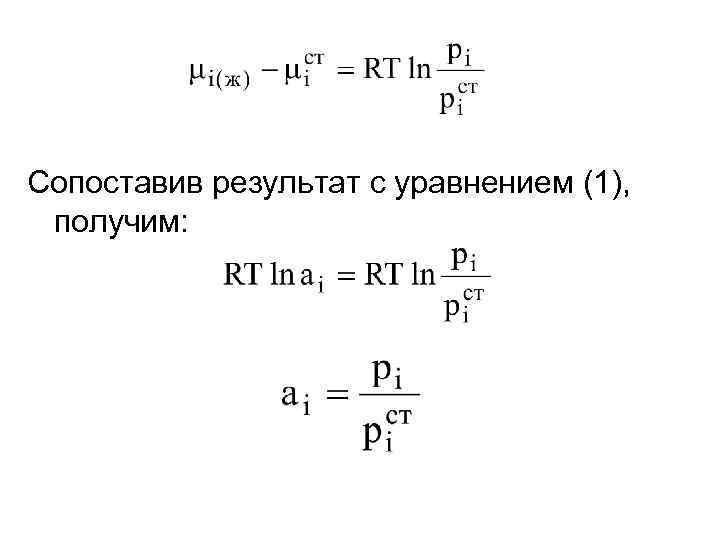 Сопоставив результат с уравнением (1), получим:
Сопоставив результат с уравнением (1), получим:
 Выбор стандартного состояния • Для совершенных растворов Сопоставим с уравнением Активность может совпадать с мольной долей только если
Выбор стандартного состояния • Для совершенных растворов Сопоставим с уравнением Активность может совпадать с мольной долей только если
 Для растворов близких к совершенным, в качестве стандартного состояния принимается чистый компонент и Степень отклонения от идеальности определяется величиной коэффициента активности ( i)
Для растворов близких к совершенным, в качестве стандартного состояния принимается чистый компонент и Степень отклонения от идеальности определяется величиной коэффициента активности ( i)
 • i>1 положительные отклонения от идеальности • 0< i<1 отрицательные отклонения от идеальности • Закон Рауля для реального раствора
• i>1 положительные отклонения от идеальности • 0< i<1 отрицательные отклонения от идеальности • Закон Рауля для реального раствора
 • Для разбавленных растворов • Для растворителя • Для растворенного в-ва Для растворителя в качестве стандартного состояния целесообразно принять этот компонент в чистом состоянии Коэффициент активности
• Для разбавленных растворов • Для растворителя • Для растворенного в-ва Для растворителя в качестве стандартного состояния целесообразно принять этот компонент в чистом состоянии Коэффициент активности
 • Для растворенного вещества выбор стандартного состояния должен быть сделан таким образом, чтобы в растворе любой концентрации соблюдался закон Генри. Сопоставим уравнения
• Для растворенного вещества выбор стандартного состояния должен быть сделан таким образом, чтобы в растворе любой концентрации соблюдался закон Генри. Сопоставим уравнения
 • Коэффициент активности • По одному из определений: активность – величина, подстановка которой вместо концентрации в термодинамические уравнения делает последние применимыми для реальных растворов.
• Коэффициент активности • По одному из определений: активность – величина, подстановка которой вместо концентрации в термодинамические уравнения делает последние применимыми для реальных растворов.
 • Закон действующих масс А=2 D При равновесии A=2 D
• Закон действующих масс А=2 D При равновесии A=2 D
 • Закон распределения частный случай закона действующих масс
• Закон распределения частный случай закона действующих масс
 Методы определения активности • Измерение давления пара Чему равна активность воды в растворе, если давление водяного пара над ним равно 700 мм рт. ст при 100 С.
Методы определения активности • Измерение давления пара Чему равна активность воды в растворе, если давление водяного пара над ним равно 700 мм рт. ст при 100 С.
 • Давление насыщенного пара меди над раствором Fe-Cu при 1600 С имеет следующие значения: XCu. O 0, 01 0, 02 0, 06 0, 21 0, 46 5 3 1 7 7 P, 8, 7 13, 3 30, 9 53, 2 59, 8 Па Определить активность и коэффициент активности меди в этих растворах.
• Давление насыщенного пара меди над раствором Fe-Cu при 1600 С имеет следующие значения: XCu. O 0, 01 0, 02 0, 06 0, 21 0, 46 5 3 1 7 7 P, 8, 7 13, 3 30, 9 53, 2 59, 8 Па Определить активность и коэффициент активности меди в этих растворах.
 Па -1 Па-1 - ХСu Г=1, 7. 10 -3 Па-3
Па -1 Па-1 - ХСu Г=1, 7. 10 -3 Па-3
 Па 0, 05 0, 09 0, 10 3 2 0, 9 0, 4 0, 2
Па 0, 05 0, 09 0, 10 3 2 0, 9 0, 4 0, 2
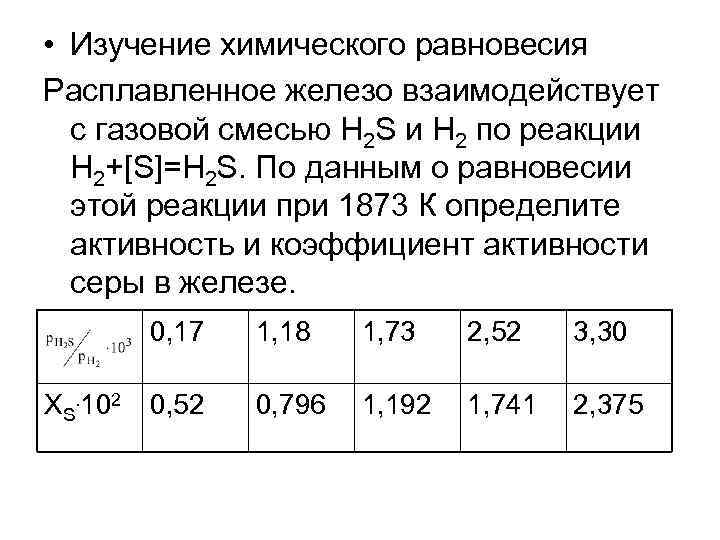 • Изучение химического равновесия Расплавленное железо взаимодействует с газовой смесью H 2 S и H 2 по реакции H 2+[S]=H 2 S. По данным о равновесии этой реакции при 1873 К определите активность и коэффициент активности серы в железе. 0, 17 XS. 102 1, 18 1, 73 2, 52 3, 30 0, 52 0, 796 1, 192 1, 741 2, 375
• Изучение химического равновесия Расплавленное железо взаимодействует с газовой смесью H 2 S и H 2 по реакции H 2+[S]=H 2 S. По данным о равновесии этой реакции при 1873 К определите активность и коэффициент активности серы в железе. 0, 17 XS. 102 1, 18 1, 73 2, 52 3, 30 0, 52 0, 796 1, 192 1, 741 2, 375
 Константа для реального раствора Константа для разбавленного раствора K* 0, 145 0, 144 0, 139
Константа для реального раствора Константа для разбавленного раствора K* 0, 145 0, 144 0, 139
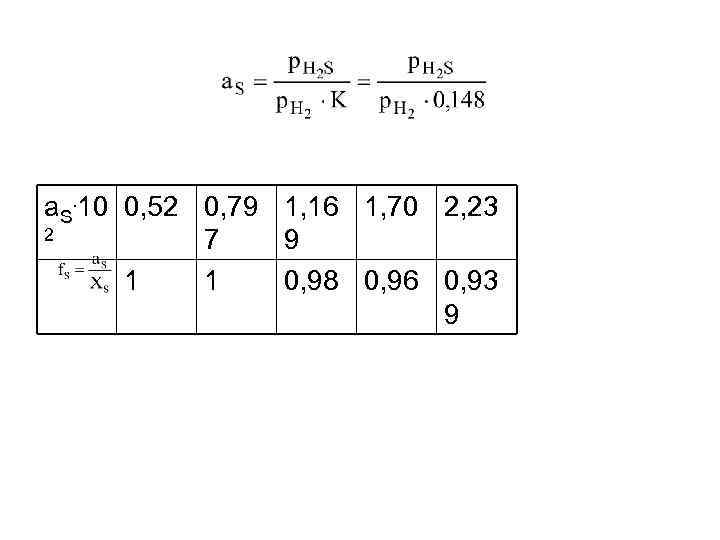 а. S. 10 0, 52 0, 79 1, 16 1, 70 2, 23 2 7 9 1 1 0, 98 0, 96 0, 93 9
а. S. 10 0, 52 0, 79 1, 16 1, 70 2, 23 2 7 9 1 1 0, 98 0, 96 0, 93 9
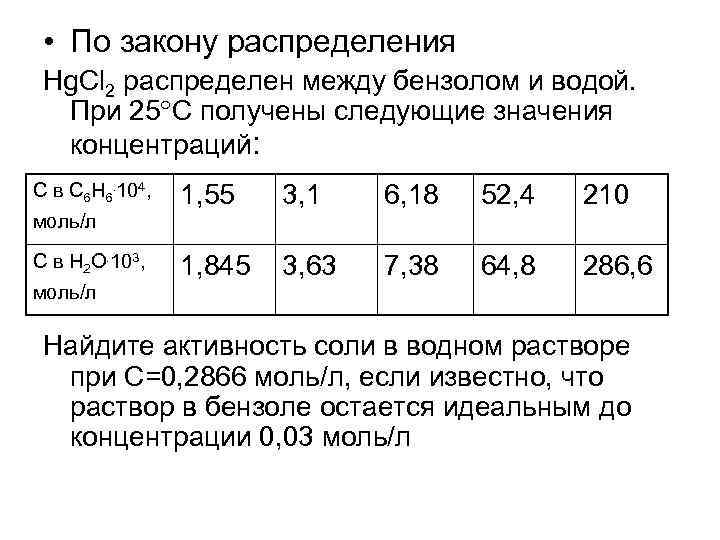 • По закону распределения Hg. Cl 2 распределен между бензолом и водой. При 25 С получены следующие значения концентраций: С в С 6 Н 6. 104, моль/л С в Н 2 О. 103, моль/л 1, 55 3, 1 6, 18 52, 4 210 1, 845 3, 63 7, 38 64, 8 286, 6 Найдите активность соли в водном растворе при С=0, 2866 моль/л, если известно, что раствор в бензоле остается идеальным до концентрации 0, 03 моль/л
• По закону распределения Hg. Cl 2 распределен между бензолом и водой. При 25 С получены следующие значения концентраций: С в С 6 Н 6. 104, моль/л С в Н 2 О. 103, моль/л 1, 55 3, 1 6, 18 52, 4 210 1, 845 3, 63 7, 38 64, 8 286, 6 Найдите активность соли в водном растворе при С=0, 2866 моль/л, если известно, что раствор в бензоле остается идеальным до концентрации 0, 03 моль/л
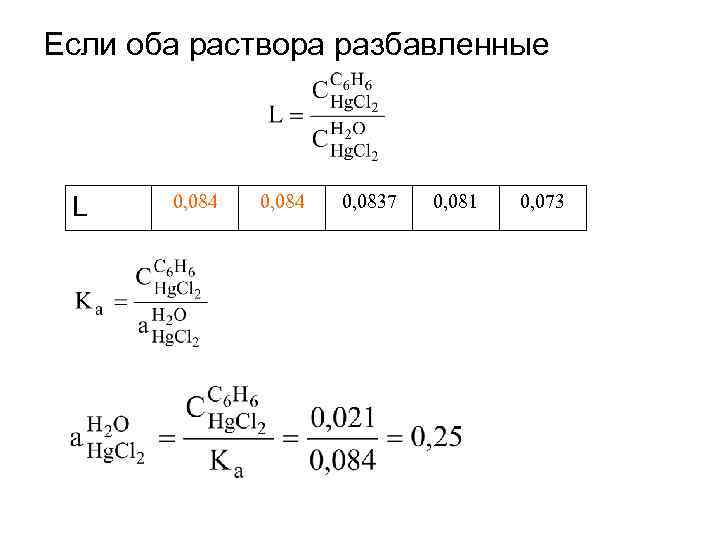 Если оба раствора разбавленные L 0, 084 0, 0837 0, 081 0, 073
Если оба раствора разбавленные L 0, 084 0, 0837 0, 081 0, 073


