Catalysis by metals-3.ppt
- Количество слайдов: 33
 Нефтепродукты первичной перегонки Легкие: Т. кип. , о. С Катализ металлами легкий бензин < 80 бензин (сырье для реформинга) керосин (топливо для реактивных двигателей) 80 -160 150 -230 газойль (дизельное топливо, печное топливо) 170 -370 Тяжелые: мазут (на отопление) >350 1
Нефтепродукты первичной перегонки Легкие: Т. кип. , о. С Катализ металлами легкий бензин < 80 бензин (сырье для реформинга) керосин (топливо для реактивных двигателей) 80 -160 150 -230 газойль (дизельное топливо, печное топливо) 170 -370 Тяжелые: мазут (на отопление) >350 1
 Реакции, протекающие при гидроочистке Катализ металлами 1. Гидрогенолиз связей C-S, C-N и др. 2. Гидрогенолиз связей С-С (гидрокрекинг) 3. Гидрирование 4. Деметаллизация (разрушение металлоорганических соединений V и Ni) 2
Реакции, протекающие при гидроочистке Катализ металлами 1. Гидрогенолиз связей C-S, C-N и др. 2. Гидрогенолиз связей С-С (гидрокрекинг) 3. Гидрирование 4. Деметаллизация (разрушение металлоорганических соединений V и Ni) 2
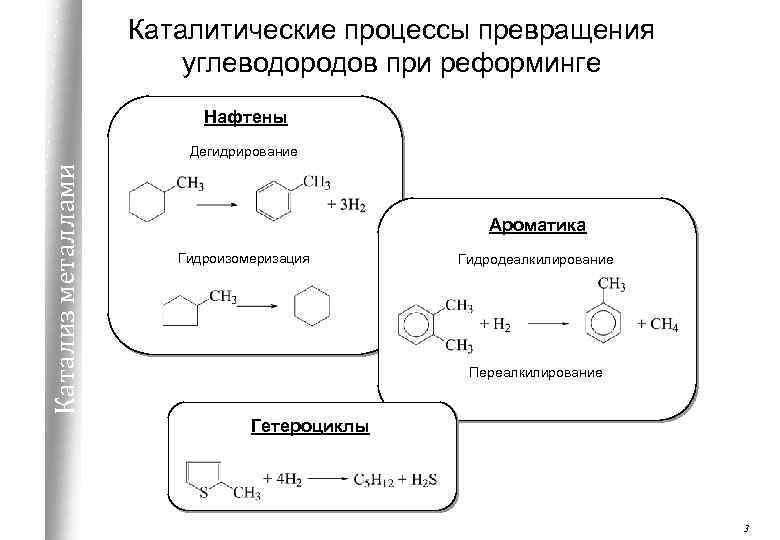 Каталитические процессы превращения углеводородов при реформинге Нафтены Катализ металлами Дегидрирование Ароматика Гидроизомеризация Гидродеалкилирование Переалкилирование Гетероциклы 3
Каталитические процессы превращения углеводородов при реформинге Нафтены Катализ металлами Дегидрирование Ароматика Гидроизомеризация Гидродеалкилирование Переалкилирование Гетероциклы 3
 Каталитические процессы: Реформинг Катализ металлами Цель: получение высокооктановых топлив и(или) ароматических углеводородов о. ч. прямогонного бензина <50 (15 -75 прямоцепных углеводородов) 4
Каталитические процессы: Реформинг Катализ металлами Цель: получение высокооктановых топлив и(или) ароматических углеводородов о. ч. прямогонного бензина <50 (15 -75 прямоцепных углеводородов) 4
 Каталитические процессы: Катализ металлами Скорость, влияние давления, тепловые эффекты Катализаторы реформинга: до 1950 г. : Cr 2 O 3, Mo. O 4 на Al 2 O 3 50 -70 -е годы: Pt/Al 2 O 3 после 1970 г. : (Pt+M)/Al 2 O 3; M=Re, Ir, Sn 5
Каталитические процессы: Катализ металлами Скорость, влияние давления, тепловые эффекты Катализаторы реформинга: до 1950 г. : Cr 2 O 3, Mo. O 4 на Al 2 O 3 50 -70 -е годы: Pt/Al 2 O 3 после 1970 г. : (Pt+M)/Al 2 O 3; M=Re, Ir, Sn 5
 Влияние состава катализатора на активность в дегидрирование циклогексана Катализ металлами ммоль С 6 Н 6/г Кт. с 34%Cr 2 O 3/Al 2 O 3 0. 5 10%Mo. O 3/Al 2 O 3 3 5%Ni/Al 2 O 3 13 5%Co/Al 2 O 3 13 1%Pd /Al 2 O 3 200 5%Ni /Al 2 O 3 320 1%Rh /Al 2 O 3 890 0. 5%Pt /Al 2 O 3 1400 -4000 6
Влияние состава катализатора на активность в дегидрирование циклогексана Катализ металлами ммоль С 6 Н 6/г Кт. с 34%Cr 2 O 3/Al 2 O 3 0. 5 10%Mo. O 3/Al 2 O 3 3 5%Ni/Al 2 O 3 13 5%Co/Al 2 O 3 13 1%Pd /Al 2 O 3 200 5%Ni /Al 2 O 3 320 1%Rh /Al 2 O 3 890 0. 5%Pt /Al 2 O 3 1400 -4000 6
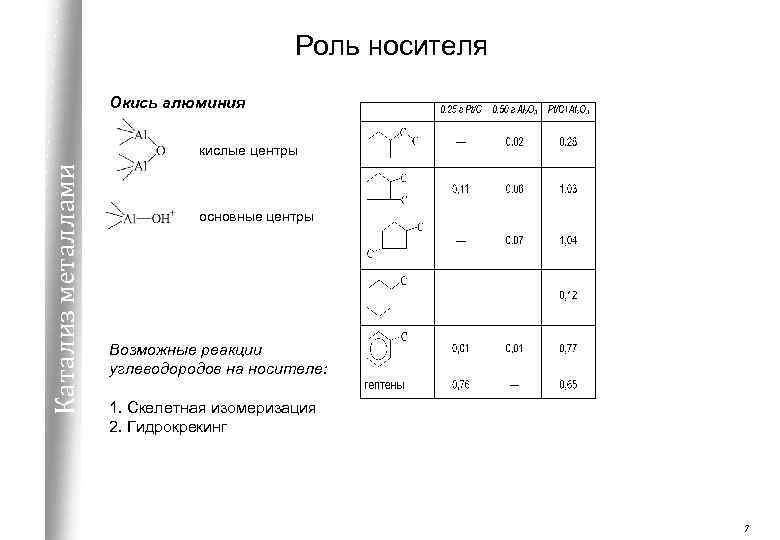 Роль носителя Окись алюминия Катализ металлами кислые центры основные центры Возможные реакции углеводородов на носителе: 1. Скелетная изомеризация 2. Гидрокрекинг 7
Роль носителя Окись алюминия Катализ металлами кислые центры основные центры Возможные реакции углеводородов на носителе: 1. Скелетная изомеризация 2. Гидрокрекинг 7
 Бифункциональный механизм действия катализаторов реформинга Катализ металлами Образование карбоний-катионов: пример: или миграция двойной связи Скелетная изомеризация: на Pt: ароматизация олефинов С 5 -циклизация изопарафинов 8
Бифункциональный механизм действия катализаторов реформинга Катализ металлами Образование карбоний-катионов: пример: или миграция двойной связи Скелетная изомеризация: на Pt: ароматизация олефинов С 5 -циклизация изопарафинов 8
 Превращение углеводородов Пути ароматизации: Катализ металлами 1) 1, 6 -циклизация 2) 1, 5 -замыкание цикла, затем превращение С 5®С 6 (расширение кольца) 3) последовательное дегидрирование: гексен ® гексадиен ® гексатриен ® бензол. Второй путь более вероятен (реакция на сплавах и отравленных катализаторах) 9
Превращение углеводородов Пути ароматизации: Катализ металлами 1) 1, 6 -циклизация 2) 1, 5 -замыкание цикла, затем превращение С 5®С 6 (расширение кольца) 3) последовательное дегидрирование: гексен ® гексадиен ® гексатриен ® бензол. Второй путь более вероятен (реакция на сплавах и отравленных катализаторах) 9
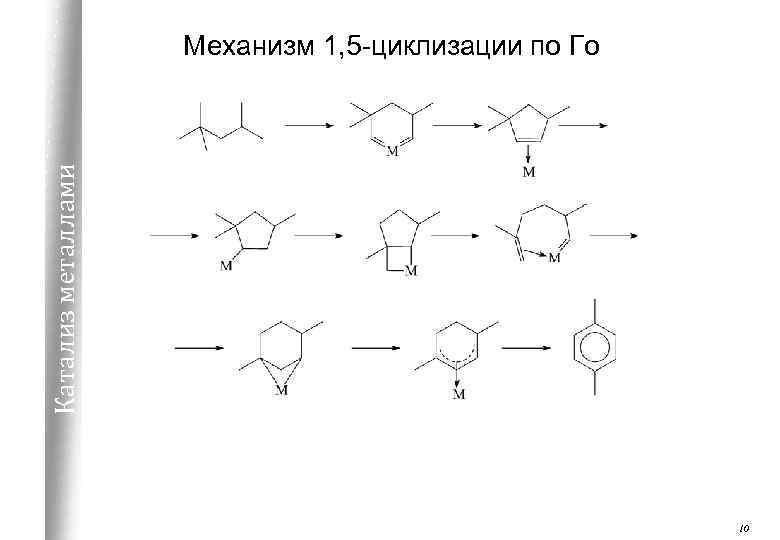 Катализ металлами Механизм 1, 5 -циклизации по Го 10
Катализ металлами Механизм 1, 5 -циклизации по Го 10
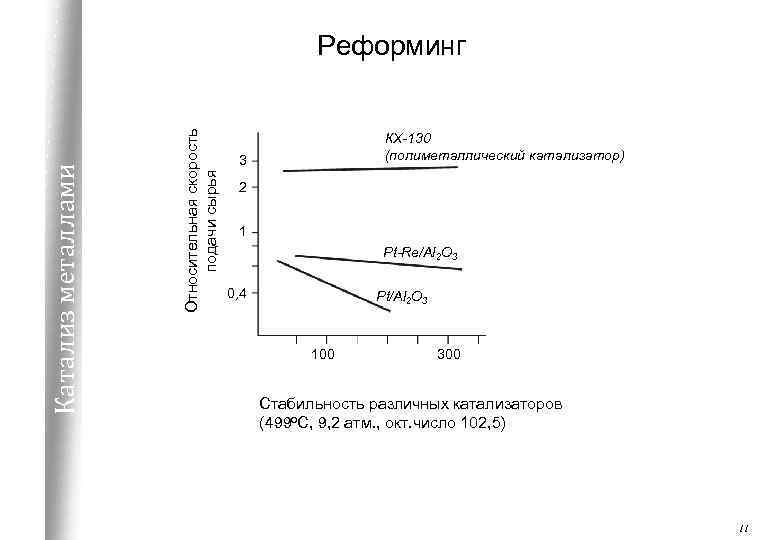 Относительная скорость подачи сырья Катализ металлами Реформинг КХ-130 (полиметаллический катализатор) 3 2 1 Pt-Re/Al 2 O 3 0, 4 Pt/Al 2 O 3 100 300 Стабильность различных катализаторов (499 о. С, 9, 2 атм. , окт. число 102, 5) 11
Относительная скорость подачи сырья Катализ металлами Реформинг КХ-130 (полиметаллический катализатор) 3 2 1 Pt-Re/Al 2 O 3 0, 4 Pt/Al 2 O 3 100 300 Стабильность различных катализаторов (499 о. С, 9, 2 атм. , окт. число 102, 5) 11
 Катализ металлами Возможные причины дезактивации 1. Агломерация частиц металла 2. Коксообразование 3. Отравление каталитическими ядами: S, P, Cl, другие металлы (Fe) 12
Катализ металлами Возможные причины дезактивации 1. Агломерация частиц металла 2. Коксообразование 3. Отравление каталитическими ядами: S, P, Cl, другие металлы (Fe) 12
 Проблема Pt-Re катализатора Катализ металлами Состояние компонентов (гипотезы) на окиси алюминия: 1. На поверхности носителя находятся ионы Re 4+; во время процесса связаны с серой. 2. На поверхности находятся частицы Reo; покрыты серой. 3. Ионы Re 4+ связаны с платиной. 4. На поверхности находятся частицы сплава Pt-Re; сера находится преимущественно на Re. 13
Проблема Pt-Re катализатора Катализ металлами Состояние компонентов (гипотезы) на окиси алюминия: 1. На поверхности носителя находятся ионы Re 4+; во время процесса связаны с серой. 2. На поверхности находятся частицы Reo; покрыты серой. 3. Ионы Re 4+ связаны с платиной. 4. На поверхности находятся частицы сплава Pt-Re; сера находится преимущественно на Re. 13
 Катализ металлами Возможные причины повышения стабильности в случае Pt-Re катализаторов 1. Ионы Re связывают частицы Pt, препятствуя их миграции. 2. Соединения Re предотвращают образование кокса. 3. Соединения Re модифицируют каталитическое действие Pt и ингибируют превращение продуктов разложения углеводородов в графит. 14
Катализ металлами Возможные причины повышения стабильности в случае Pt-Re катализаторов 1. Ионы Re связывают частицы Pt, препятствуя их миграции. 2. Соединения Re предотвращают образование кокса. 3. Соединения Re модифицируют каталитическое действие Pt и ингибируют превращение продуктов разложения углеводородов в графит. 14
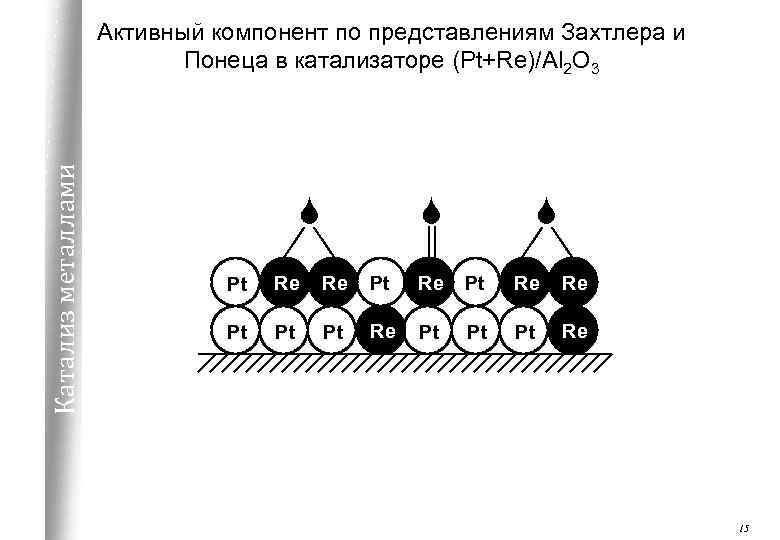 Катализ металлами Активный компонент по представлениям Захтлера и Понеца в катализаторе (Pt+Re)/Al 2 O 3 S S S Pt Re Re Pt Pt Pt Re 15
Катализ металлами Активный компонент по представлениям Захтлера и Понеца в катализаторе (Pt+Re)/Al 2 O 3 S S S Pt Re Re Pt Pt Pt Re 15
 Каталитические процессы. Реформинг, условия процесса Катализ металлами Давление 30 -50 атм: высокая скорость гидрокрекинга, низкая конверсия в ароматические углеводороды, низкий выход Н 2, низкая скорость дезактивации 8 -20 атм: высокий выход ароматических углеводородов, низкий выход продуктов крекинга, высокий выход Н 2, быстрая дезактивация. Температура 460 -520 о. С, обычно 480 -500 о. С. Повышение температуры по мере дезактивации катализатора. Объемная скорость: 1 -2 час-1 Н 2: углеводороды = 5 - 8 Необходимое содержание S в сырье <1 ppm (0, 0001%) 16
Каталитические процессы. Реформинг, условия процесса Катализ металлами Давление 30 -50 атм: высокая скорость гидрокрекинга, низкая конверсия в ароматические углеводороды, низкий выход Н 2, низкая скорость дезактивации 8 -20 атм: высокий выход ароматических углеводородов, низкий выход продуктов крекинга, высокий выход Н 2, быстрая дезактивация. Температура 460 -520 о. С, обычно 480 -500 о. С. Повышение температуры по мере дезактивации катализатора. Объемная скорость: 1 -2 час-1 Н 2: углеводороды = 5 - 8 Необходимое содержание S в сырье <1 ppm (0, 0001%) 16
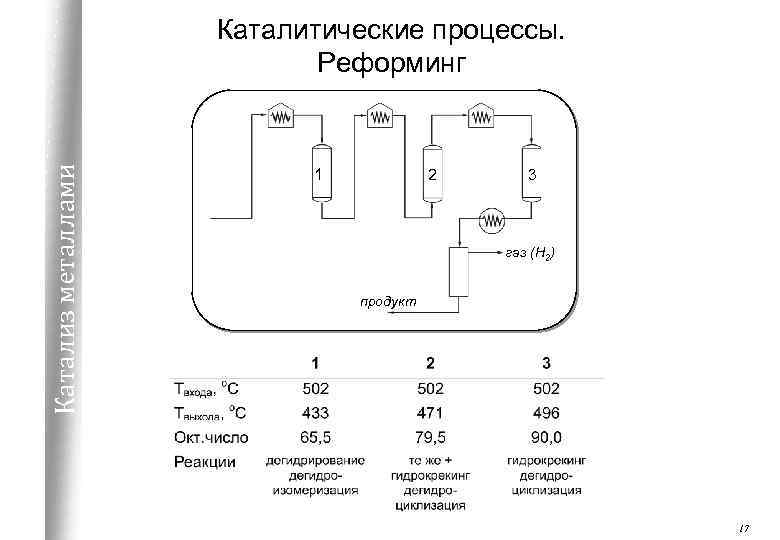 Катализ металлами Каталитические процессы. Реформинг 1 2 3 газ (Н 2) продукт 17
Катализ металлами Каталитические процессы. Реформинг 1 2 3 газ (Н 2) продукт 17
 Катализ металлами Основные процессы гидрирования в получении химического сырья 18
Катализ металлами Основные процессы гидрирования в получении химического сырья 18
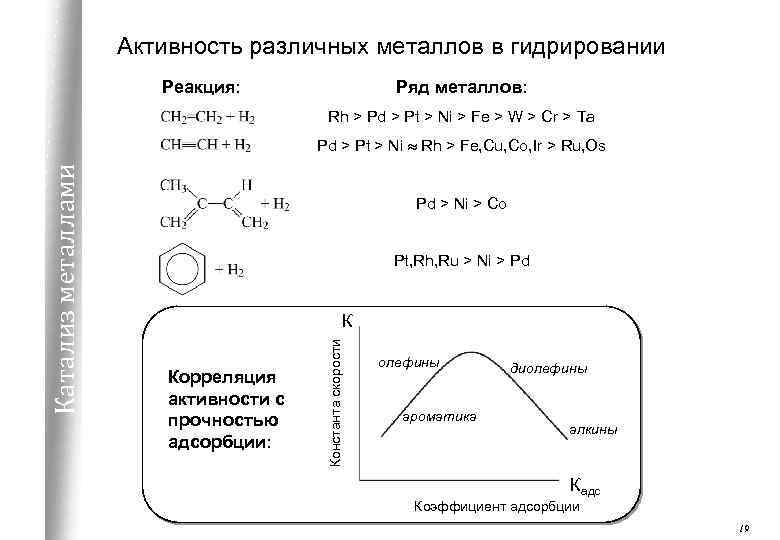 Активность различных металлов в гидрировании Реакция: Ряд металлов: Rh > Pd > Pt > Ni > Fe > W > Cr > Ta Pd > Ni > Co Pt, Rh, Ru > Ni > Pd К Корреляция активности с прочностью адсорбции: Константа скорости Катализ металлами Pd > Pt > Ni Rh > Fe, Cu, Co, Ir > Ru, Os олефины ароматика диолефины алкины Кадс Коэффициент адсорбции 19
Активность различных металлов в гидрировании Реакция: Ряд металлов: Rh > Pd > Pt > Ni > Fe > W > Cr > Ta Pd > Ni > Co Pt, Rh, Ru > Ni > Pd К Корреляция активности с прочностью адсорбции: Константа скорости Катализ металлами Pd > Pt > Ni Rh > Fe, Cu, Co, Ir > Ru, Os олефины ароматика диолефины алкины Кадс Коэффициент адсорбции 19
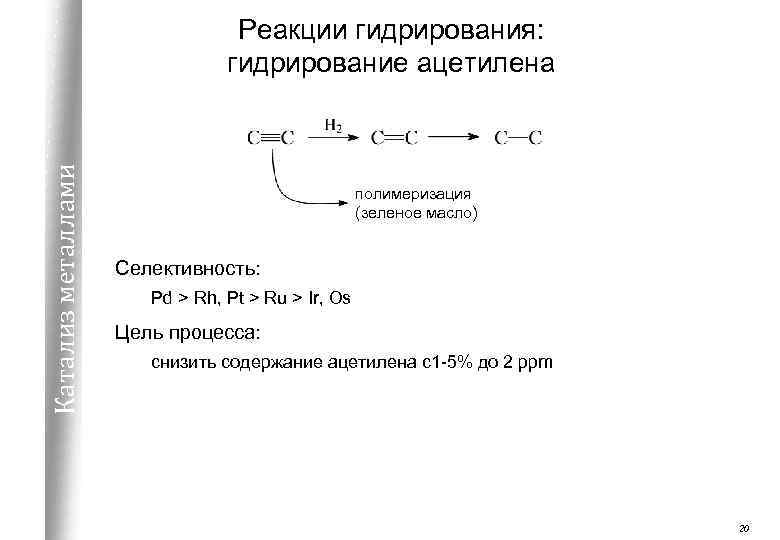 Катализ металлами Реакции гидрирования: гидрирование ацетилена полимеризация (зеленое масло) Селективность: Pd > Rh, Pt > Ru > Ir, Os Цель процесса: снизить содержание ацетилена с1 -5% до 2 ppm 20
Катализ металлами Реакции гидрирования: гидрирование ацетилена полимеризация (зеленое масло) Селективность: Pd > Rh, Pt > Ru > Ir, Os Цель процесса: снизить содержание ацетилена с1 -5% до 2 ppm 20
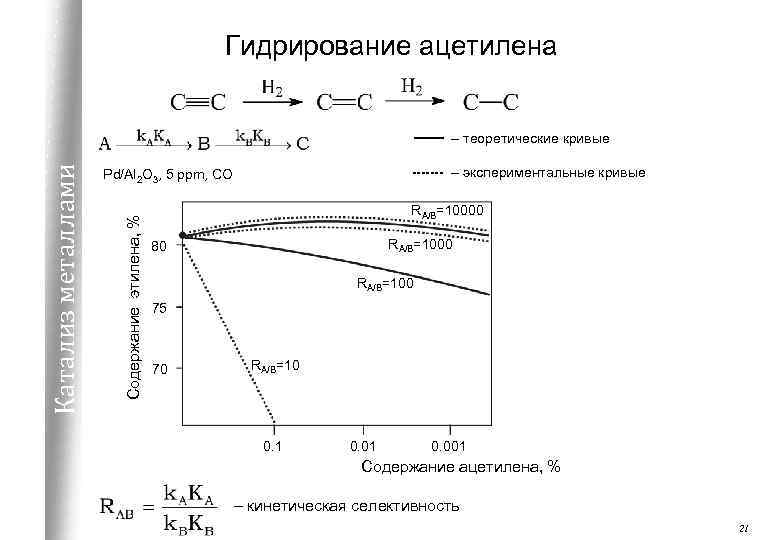 Гидрирование ацетилена – экспериментальные кривые Pd/Al 2 O 3, 5 ppm, CO Содержание этилена, % Катализ металлами – теоретические кривые RA/B=10000 RA/B=1000 80 RA/B=100 75 70 RA/B=10 0. 1 0. 001 Содержание ацетилена, % – кинетическая селективность 21
Гидрирование ацетилена – экспериментальные кривые Pd/Al 2 O 3, 5 ppm, CO Содержание этилена, % Катализ металлами – теоретические кривые RA/B=10000 RA/B=1000 80 RA/B=100 75 70 RA/B=10 0. 1 0. 001 Содержание ацетилена, % – кинетическая селективность 21
 Промышленные процессы. Синтез Фишера-Тропша Катализ металлами Восстановительная олигомеризация окиси углерода n. CO + m. H 2 Cx Hy O z 1922 г. : Фишер, Тропш; гидрирование СО на Fe+щелочи; 150 атм, 400 -450 о. С, О-содержащие продукты 1936 г. : 4 промышленных завода 1943 г. : 1 млн. т углеводородов (Co - Th. O 2 - Mg. O - Si. O 2) 46% бензина, 23% дизельного топлива, 3% смазочных масел, 28% восков 1953 г. : СССР, завод в Новочеркасске Настоящее время: ЮАР, 4 млн т в год Sasol Kellog — Synthol 22
Промышленные процессы. Синтез Фишера-Тропша Катализ металлами Восстановительная олигомеризация окиси углерода n. CO + m. H 2 Cx Hy O z 1922 г. : Фишер, Тропш; гидрирование СО на Fe+щелочи; 150 атм, 400 -450 о. С, О-содержащие продукты 1936 г. : 4 промышленных завода 1943 г. : 1 млн. т углеводородов (Co - Th. O 2 - Mg. O - Si. O 2) 46% бензина, 23% дизельного топлива, 3% смазочных масел, 28% восков 1953 г. : СССР, завод в Новочеркасске Настоящее время: ЮАР, 4 млн т в год Sasol Kellog — Synthol 22
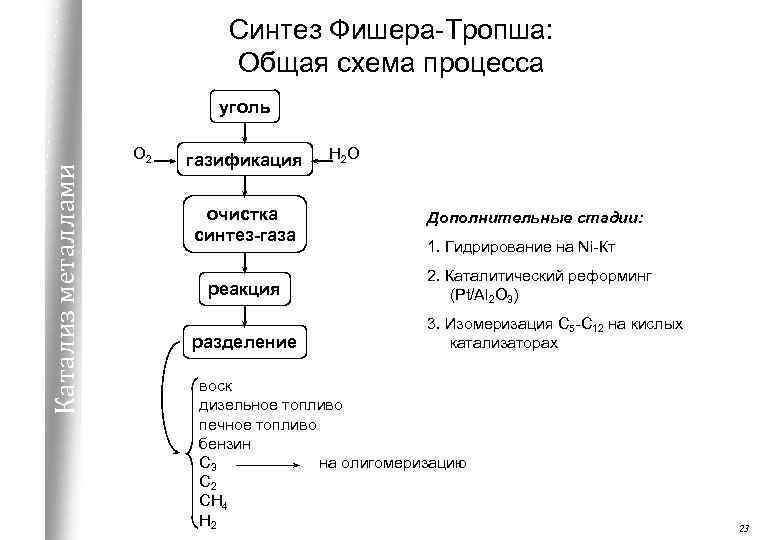 Синтез Фишера-Тропша: Общая схема процесса Катализ металлами уголь O 2 газификация H 2 O очистка синтез-газа Дополнительные стадии: реакция 2. Каталитический реформинг (Pt/Al 2 O 3) разделение 1. Гидрирование на Ni-Кт 3. Изомеризация С 5 -С 12 на кислых катализаторах воск дизельное топливо печное топливо бензин С 3 на олигомеризацию С 2 СН 4 Н 2 23
Синтез Фишера-Тропша: Общая схема процесса Катализ металлами уголь O 2 газификация H 2 O очистка синтез-газа Дополнительные стадии: реакция 2. Каталитический реформинг (Pt/Al 2 O 3) разделение 1. Гидрирование на Ni-Кт 3. Изомеризация С 5 -С 12 на кислых катализаторах воск дизельное топливо печное топливо бензин С 3 на олигомеризацию С 2 СН 4 Н 2 23
 Синтез Фишера-Тропша: Карбидный механизм Фишер, Тропш (1926), Эйдус (1947), Захтлер (1979) Катализ металлами Диссоциативная адсорбция СО: Образование СН 4: Рост цепи: Обрыв цепи: 24
Синтез Фишера-Тропша: Карбидный механизм Фишер, Тропш (1926), Эйдус (1947), Захтлер (1979) Катализ металлами Диссоциативная адсорбция СО: Образование СН 4: Рост цепи: Обрыв цепи: 24
 Синтез Фишера-Тропша: Механизм Катализ металлами Диссоциативная адсорбция СО: Эксперименты с С 13 О (Понец, Захтлер): 1. Адсорбция 13 СО 2. Вывод: частицы СНх участвуют в образовании СН 4 и высших углеводородов Мьютериз (1980): 25
Синтез Фишера-Тропша: Механизм Катализ металлами Диссоциативная адсорбция СО: Эксперименты с С 13 О (Понец, Захтлер): 1. Адсорбция 13 СО 2. Вывод: частицы СНх участвуют в образовании СН 4 и высших углеводородов Мьютериз (1980): 25
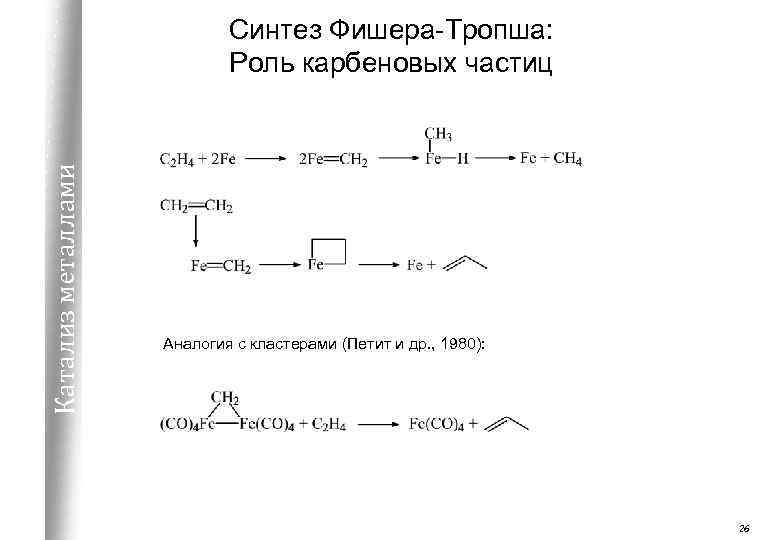 Катализ металлами Синтез Фишера-Тропша: Роль карбеновых частиц Аналогия с кластерами (Петит и др. , 1980): 26
Катализ металлами Синтез Фишера-Тропша: Роль карбеновых частиц Аналогия с кластерами (Петит и др. , 1980): 26
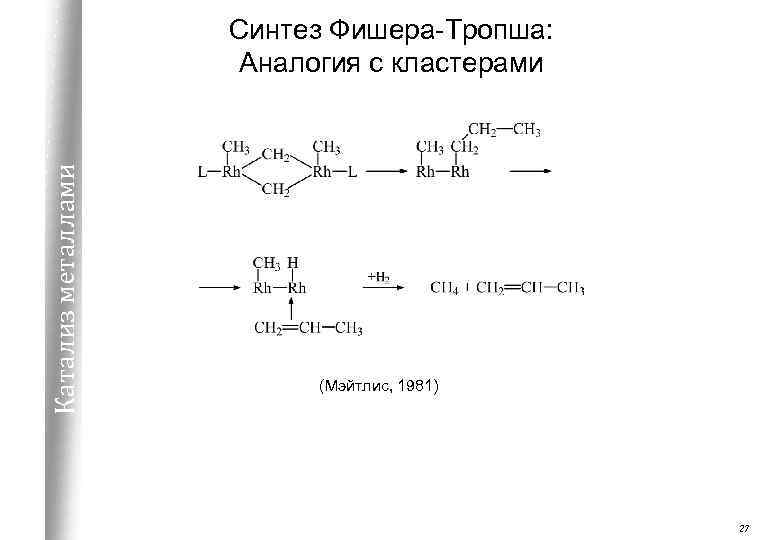 Катализ металлами Синтез Фишера-Тропша: Аналогия с кластерами (Мэйтлис, 1981) 27
Катализ металлами Синтез Фишера-Тропша: Аналогия с кластерами (Мэйтлис, 1981) 27
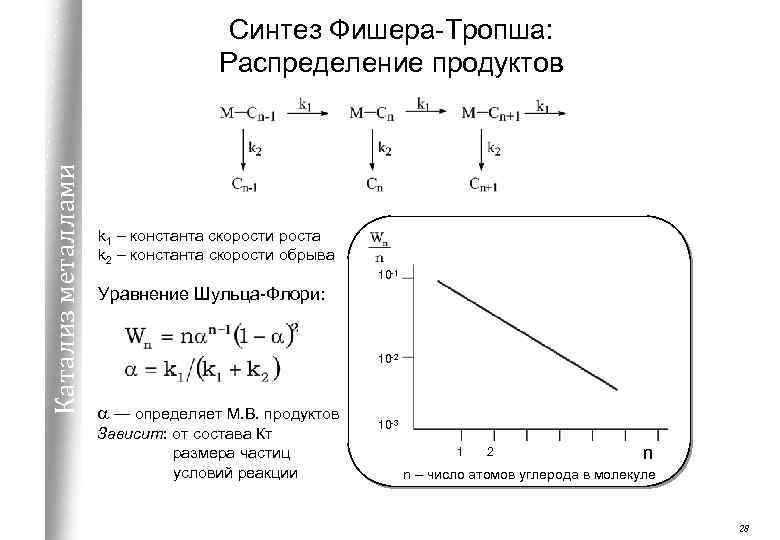 Катализ металлами Синтез Фишера-Тропша: Распределение продуктов k 1 – константа скорости роста k 2 – константа скорости обрыва 10 -1 Уравнение Шульца-Флори: 10 -2 a — определяет М. В. продуктов Зависит: от состава Кт размера частиц условий реакции 10 -3 1 2 n n – число атомов углерода в молекуле 28
Катализ металлами Синтез Фишера-Тропша: Распределение продуктов k 1 – константа скорости роста k 2 – константа скорости обрыва 10 -1 Уравнение Шульца-Флори: 10 -2 a — определяет М. В. продуктов Зависит: от состава Кт размера частиц условий реакции 10 -3 1 2 n n – число атомов углерода в молекуле 28
 Синтез Фишера-Тропша Катализ металлами Плавленый железный катализатор: 5 -10 м 2/г Степень восстановления до a-Fe: 95% В ходе реакции катализатор превращается в смесь: Fe 3 O 4 Fe 5 C 2 Fe 7 C 3 Fe 29
Синтез Фишера-Тропша Катализ металлами Плавленый железный катализатор: 5 -10 м 2/г Степень восстановления до a-Fe: 95% В ходе реакции катализатор превращается в смесь: Fe 3 O 4 Fe 5 C 2 Fe 7 C 3 Fe 29
 Синтез Фишера-Тропша Катализ металлами Катализатор для получения олефинов: Fe(100)/Mn(70) CH 4 10% C 2 H 4 31% C 3 H 6 22% C 4 H 8 17% C 2 -C 4 15% алканы Катализатор для получения спиртов: (Rh-Э)/Si. O 2 (Э: Zr, Ti, Cr, Mn) Ac. OH ~5% Ac. H ~3% Et. OH ~70% но: СН 4 30 -50% 30
Синтез Фишера-Тропша Катализ металлами Катализатор для получения олефинов: Fe(100)/Mn(70) CH 4 10% C 2 H 4 31% C 3 H 6 22% C 4 H 8 17% C 2 -C 4 15% алканы Катализатор для получения спиртов: (Rh-Э)/Si. O 2 (Э: Zr, Ti, Cr, Mn) Ac. OH ~5% Ac. H ~3% Et. OH ~70% но: СН 4 30 -50% 30
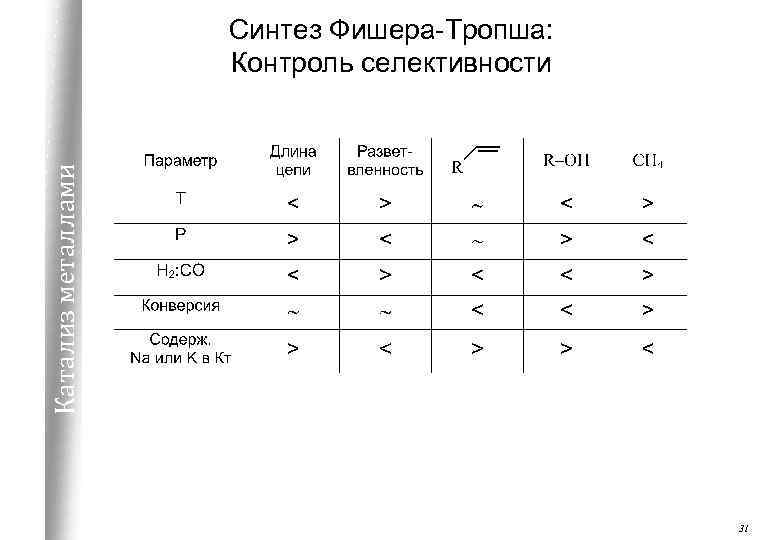 Катализ металлами Синтез Фишера-Тропша: Контроль селективности 31
Катализ металлами Синтез Фишера-Тропша: Контроль селективности 31
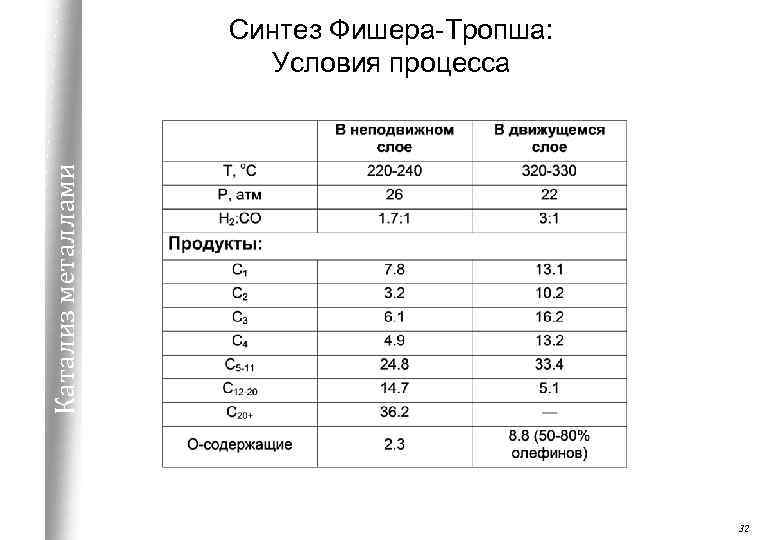 Катализ металлами Синтез Фишера-Тропша: Условия процесса 32
Катализ металлами Синтез Фишера-Тропша: Условия процесса 32
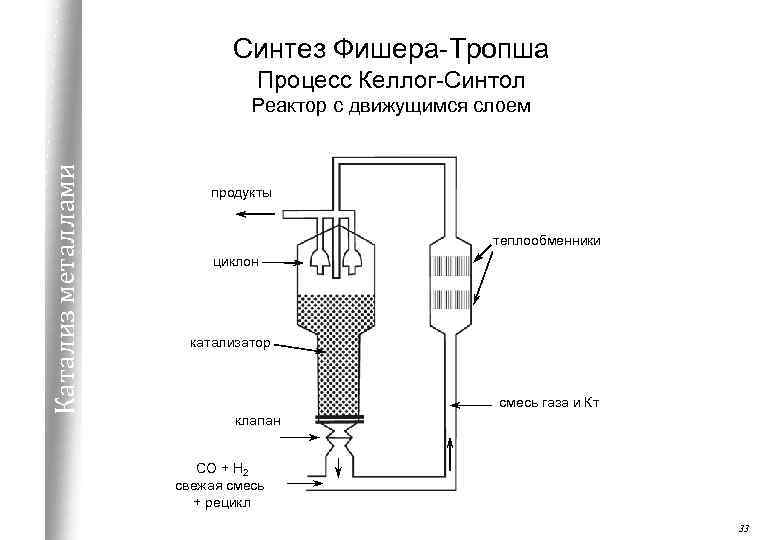 Синтез Фишера-Тропша Процесс Келлог-Синтол Катализ металлами Реактор с движущимся слоем продукты теплообменники циклон катализатор смесь газа и Кт клапан СО + Н 2 свежая смесь + рецикл 33
Синтез Фишера-Тропша Процесс Келлог-Синтол Катализ металлами Реактор с движущимся слоем продукты теплообменники циклон катализатор смесь газа и Кт клапан СО + Н 2 свежая смесь + рецикл 33


