
Nb Ta

История открытия Нио бий был открыт в 1801 г. английским учёным Ч. Хатчетом в минерале колумбите, в бассейне р. Колумбии, и потому получил название «колумбий» . В 1844 году немецкий химик Генрих Розе переименовал его в «ниобий» в честь дочери Тантала Ниобы, чем подчеркнул сходство между ниобием и танталом. Однако в некоторых странах (США, Англии) долго сохранялось первоначальное название элемента — колумбий, и только в 1950 году решением Международного союза теоретической и прикладной химии (ИЮПАК, IUPAC) элементу окончательно было присвоено название ниобий. Год спустя после того как Гатчет (1801) открыл ниобий, химик из Упсалы Экеберг занялся исследованием некоторых минералов из северных стран, в частности из Финляндии. Минералы, в которых был открыт тантал, Экеберг наименовал танталитом и иттротанталитом. В 1809 г. Волластон, подвергнув минералы колумбит и танталит тщательным исследованиям, пришел к выводу, что колумбий Гатчета и тантал Экеберга являются одним и тем же элементом. Это мнение было принято химиками всех стран до середины 40 -х годов XIX в. В 1844 г. Пластичный металлический тантал впервые получен немецким учёным В. Больтеном в 1903 г.

Область применения Применение и производство ниобия быстро возрастают, что обусловлено сочетанием таких его свойств, как тугоплавкость, способность образовывать жаропрочные, сверхпроводящие и др. сплавы, коррозионная стойкость, низкая работа выхода электронов, хорошие обрабатываемость давлением на холоде и свариваемость. Основные области применения ниобия: ракетостроение, авиационная и космическая техника, радиотехника, электроника, химическое аппаратостроение, атомная энергетика. Тантал нашел свое техническое применение довольно поздно — в начале XX века его использовали в качестве материала для нитей накаливания электроламп. Вскоре он потерял свое значение в этой области, вытесненный менее дорогим и более тугоплавким вольфрамом. В двадцатых годах XX века его стали использовать в выпрямителях переменного тока (тантал, покрытый окисной пленкой, пропускает ток лишь в одном направлении), а спустя еще год — в радиолампах. После чего металл получил признание и вскоре стал завоевывать все новые и новые области промышленности. В наше время тантал благодаря своим уникальным свойствам используется в электронике.

Основные физические характеристики и химические свойства. (ЛИТОФИЛЬНЫЕ ЭЛЕМЕНТЫ) Ниобий(Nb)- хим. элемент V гр. , период. системы, ат. номер 41, в природе один стабильный изотоп 93 Nb. Тантал(Та)- хим. элемент V гр. , период. системы, ат. номер 73, в природе один стабильный изотоп 181 Та. Атомная масса 92, 90638 а. е. м. (г/моль) Радиус атома 146 пм Ионный радиус 0, 069 нм Плотность 8, 57 г/см³ Температура плавления 2741 К Температура кипения 5015 K Теплота плавлавления 26, 8 к. Дж/моль Теплота испарения 680 к. Дж/моль Молярн. теплоёмк. 24, 44 Дж/(K·моль) Молярный объём 10, 8 см³/моль Атомная масса 180, 9479 а. е. м. (г/моль) Радиус атома 149 пм Ионный радиус 0, 068 пм Плотность 16, 654 г/см³ Температура плавления 3290 К Температура кипения 5731 К Теплота плавления 24, 7 к. Дж/моль Теплота испарения 758 к. Дж/моль Молярн. теплоёмк. 25, 39 Дж/(K·моль) Молярный объём 10, 9 см³/моль Физические свойства: Блестящий серебристо-серый металл с объемоцентрированной решеткой. Физические свойства: В чистом виде серо-стальной металл, пластичен как золото. Химические свойства: Электроотриц. 1, 6 (шкала Полинга) Cтепень окисления +5 Химические свойства: Электроотриц. 1, 5 (шкала Полинга) Стень окисления +5

Основные минералы-носители Форма нахождения ниобия в природе может быть разной: рассеянной (в породообразующих и акцессорных минералах магматических пород) и минеральной. В общей сложности известно более 100 минералов, содержащих ниобий. Из них промышленное значение имеют лишь некоторые: Колумбит-танталит (Fe, Mn)(Nb, Ta)2 O 6 содержит 82 -86% оксидов Nb и Та. При содержании ниобия выше, чем Та, минерал называется колумбитом, при обратном соотношении - танталитом. Пирохлор (Na, Ce)2(Nb, Ti)2(OH, F)O 6 обычно содержит 37, 5 -65, 6% Nb 2 O 5; Лопарит (Na, Ce, Ca, Sr. XNb, Ti)O 3 8 -10% Nb 2 O 5. Минералы ниобия слабо парамагнитны и радиоактивны из-за примесей U и Th. Минералы, содержащие ниобий в виде примесей - ильменит, касситерит, вольфрамит. В щелочных — ультраосновных породах ниобий рассеивается в минералах типа перовскита и в эвдиалите. Тантал — типично рассеянный элемент, так как изоморфен со многими химическими элементами. Известно около 20 собственно минералов тантала — серия колумбит — танталит, воджинит, лопарит, пирохлор, касситерит и другие, а также более 60 минералов, содержащих тантал. В минералах тантал всегда находится совместно с ниобием вследствие сходства их физических и химических свойств.

Ниобий и тантал имеют несколько валентных состояний: 5, 4, 3, 2 и даже 1. Наиболее типичной в химических соединениях является валентность 5. Соединения тантала низшей степени окисления образуются с большим трудом и не имеют значения в аналитической химии. Ниобий сравнительно легко восстанавливается до 3 -валентного состояния, но эти соединения изучены мало.

Поведение Nb в геологических процессах Ниобий – чрезвычайно тугоплавкий (2468°C) и высококипящий (4927°C) металл, очень стойкий во многих агрессивных средах. Устойчив против действия соляной, серной, азотной, фосфорной и органических кислот любой концентрации на холоду и при 100 — 150°С. Металл растворяется в плавиковой кислоте и особенно интенсивно в смеси плавиковой и азотной кислот. Кислоты-окислители покрывают его защитной окисной пленкой. При высоких температурах химическая активность ниобия повышается. Если при 150. . . 200°C окисляется лишь небольшой поверхностный слой металла, то при 900. . . 1200°C толщина окисной пленки значительно увеличивается. Менее устойчив ниобий в щелочах. Горячие растворы едких щелочей заметно разъедает металл, в расплавленных щелочах и соде он быстро окисляется. В хрупкое состояние ниобий переходит при температурах от — 100 до — 200°С. Из водных растворов выделить электрохимически ниобий пока не удалось. Возможно электрохимическое получение сплавов, содержащих ниобий. Электролизом безводных солевых расплавов может быть выделен металлический ниобий. Ниобий не играет никакой биологической роли

Характерное свойство ниобия — способность поглощать газы — водород, азот и кислород. При низкой температуре водород поглощается медленно, при температуре примерно 360°С водород поглощается с максимальной скоростью. Поглощённый водород придаёт металлу хрупкость, но при нагревании в вакууме выше 600°С почти весь водород выделяется и прежние механические свойства восстанавливаются. Ниобий поглощает азот при 600°С, а при более высокой температуре образуется нитрид Nb. N, который плавится при 2300°С. Углерод и углеродсодержащие газы (СН 4, СО) при высокой температуре (1200 — 1400°С) взаимодействуют с металлом с образованием твёрдого и тугоплавкого карбида Nb. C (плавится при 3500°С). С бором и кремнием ниобий образует тугоплавкий и твёрдый борид и силицид Nb. B 2 (плавится при 2900°С). В присутствии паров воды и кислорода Nb. Cl 5 и Nb. Br 5 образуют оксигалогениды Nb. OCl 3 и Nb. OBr 3 — рыхлые ватообразные вещества. При взаимодействии ниобия и графита образуются карбиды Nb 2 C и Nb. C, твердые жаропрочные соединения. В системе Nb — N существуют несколько фаз переменного состава и нитриды Nb 2 N и Nb. N. Сходным образом ведет себя ниобий в системах с фосфором и мышьяком. При взаимодействии ниобия с серой получены сульфиды: Nb. S, Nb. S 2 и Nb. S 3.

Поведение Та в геологических процессах На сегодняшний день тантал является одним из наиболее распространенных коррозионностойких металлов. Причиной высокой устойчивости тантала к коррозии является образующаяся на его поверхности при контакте с воздухом и нагревании оксидная пленка. Однако толщина оксидной пленки, в отличие от других химически активных металлов, очень невелика. Тантал не переходит в хрупкое состояние до — 211°С. Химически тантал очень инертен. Он начинает окисляться при температуре выше 300 °С, устойчив к действию сухих Вr 2 и I 2 при 150°С, взаимодействует с Сl 2 выше 200 °С, с Н 2 -выше 250 °С (интенсивно- при 300 °С), с Р 2 -выше 250 °С, с С и углеводородами- при 800 -1100 °С. Ниже 150°С не растворяется в царской водке, при обычной температуре- в соляной, фосфорной и серной кислотах, не реагирует с большинством других кислот, водным NH 3, водными растворами солей, органическими веществами. Не взаимодействует с разбавленными растворами щелочей, но медленно растворяется в их концентрированных горячих растворах. Устойчив к большинству расплавленных металлов (Li, Na, К, Си, Cd, Hg, Sn, Pb, Bi). Примеси H, N, С и О снижают пластичность и повышают твердость тантала.

Геологические барьеры Кислородный геохимический барьер характеризуется проявлением окислительной обстановки из-за наличия большого количества свободного кислорода. Интенсивность всех окислительных процессов резко возрастает. Щелочной геохимический барьер (тип D) характеризуется изменением среды в сторону снижения концентрации ионов водорода (увеличение р. Н среды). Идут процессы образования нерастворимых гидроксидов и карбонатов металлов. Сорбционный геохимический барьер возникает в тех местах биосферы, где воды соприкасаются с сорбентами веществами, способными поглощать (сорбировать) из растворов газы, ионы и молекулы. В качестве природных сорбентов обычно выступают почвы, глины, торф, илы.

Распространенность Nb В природе ниобий встречается только в виде соединений, входящих в состав различных минералов. в почве 3 -300 мг/кг в золе растений 5 10^-5% в речных водах 0, 01 мкг/л в морской воде 1· 10^− 9 мг/л в организме 0, 02 -0, 6 мг суточное потребление с пищей 0, 00062 мг Содержание в гидросфере не установлено
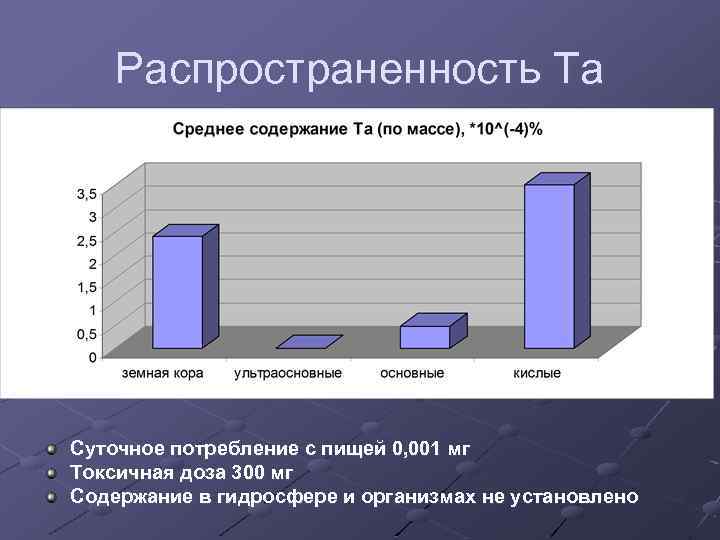
Распространенность Та Суточное потребление с пищей 0, 001 мг Токсичная доза 300 мг Содержание в гидросфере и организмах не установлено

Основные типы месторождений Колумбит встречается в изверженных пегматитах, биотитах и щелочных гранитах, иногда-в россыпных месторождениях (Нигерия), его часто добывают как побочный продукт обогащения оловянных концентратов. Пирохлор содержится в карбонатитах, щелочных породах (Канада), нефелин-сиенитовых пегматитах, в элювиальных продуктах выветривания сиенито-карбонатитов (Бразилия). Крупные залежи лопарита имеются в СССР.
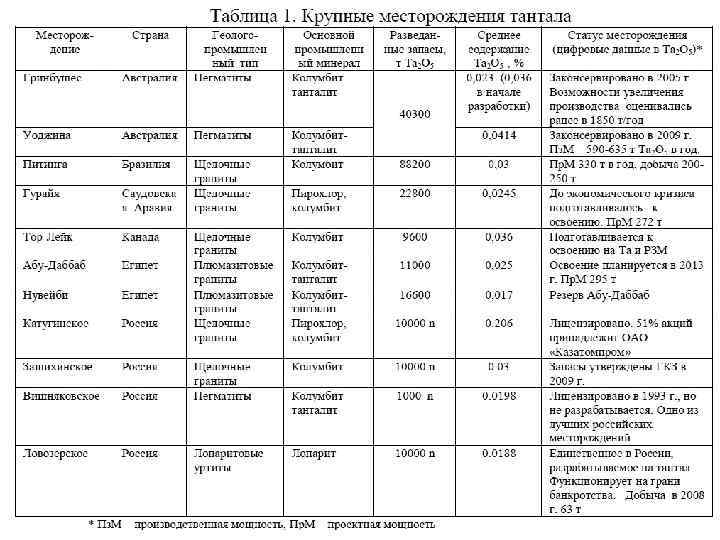
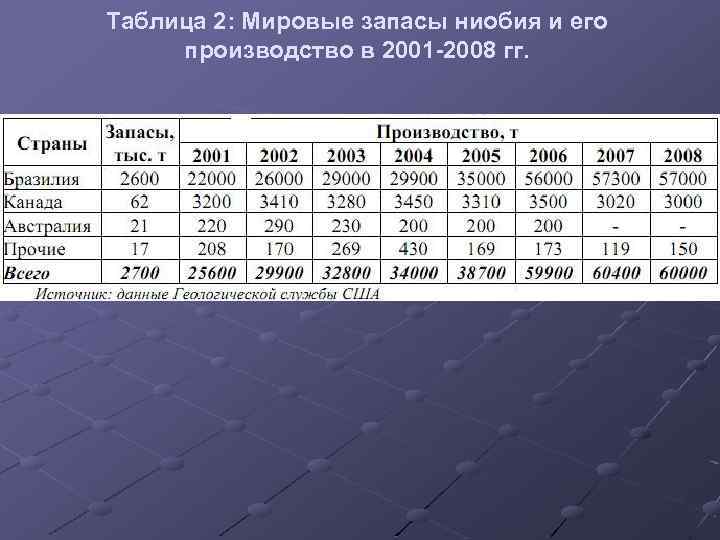
Таблица 2: Мировые запасы ниобия и его производство в 2001 -2008 гг.