Нитрозный метод получения сернойи кислоты.pptx
- Количество слайдов: 18

Название: ГБОУ СПО «ЧХТТ» Дисциплина: » Технология кислот в химической промышленности» Обучающийся: Н. А. Мусаева Преподаватель: Л. В. Белова

Производство серной кислоты нитрозным методом

Оглавление 1. Свойства сырья 2. Технологический процесс 3. Основное технологическое оборудование 4. Характеристика готового продукта 5. Техника безопасности 6. Области применения

Свойства сырья. Самородная сера В водородных и кислородных соединениях находится в составе различных ионов, образует многие кислоты и соли. Многие серосодержащие соли малорастворимы в воде. Важнейшие природные соединения серы: Fe. S 2 — железный колчедан или пирит, Zn. S — цинковая обманка или сфалерит (вюрцит), Pb. S — свинцовый блеск или галенит, Hg. S — киноварь, Sb 2 S 3 — антимонит. Кроме того, сера присутствует в нефти, природном угле, природных газах и сланцах.

Пирит (серный колчедан) Пири т — камень, высекающий огонь), серный колчедан, железный колчедан — минерал, сульфид железа химического состава Fe. S 2 (46, 6 % Fe, 53, 4 % S) Пирит является сырьём для получения серной кислоты, серы и железного купороса, но последнее время редко используется для этих целей. В последнее время всё чаще применяется в качестве корректирующей добавки производстве цементов. В огромных объёмах он извлекается при разработке гидротермальных месторождений меди, свинца, цинка, олова и других цветных металлов. Но переработка пирита в полезные компоненты обычно оказывается экономически невыгодной, и его отправляют в отвалы

Сероводород Сероводоро д (серни стый водоро д, сульфид водорода) — бесцветный газ с запахом тухлых яиц и сладковатым вкусом. Химическая формула — H 2 S. Плохо растворим в воде, хорошо — в этаноле. Ядовит. При больших концентрациях разъедает многие металлы. Концентрационные пределы воспламенения с воздухом составляют 4, 5 — 45 % сероводорода.

Сульфиды цветных металлов Сульфиды — природные сернистые соединения металлов и некоторых неметаллов. В химическом отношении рассматриваются как соли сероводородной кислоты H 2 S. Ряд элементов образует с серой полисульфиды, являющиеся солями полисернистой кислоты H 2 Sx. Главнейшие элементы, образующие сульфиды — Fe, Zn, Cu, Mo, Ag, Hg, Pb, Bi, Ni, Co, Mn, V, Ga, Ge, As, Sb.
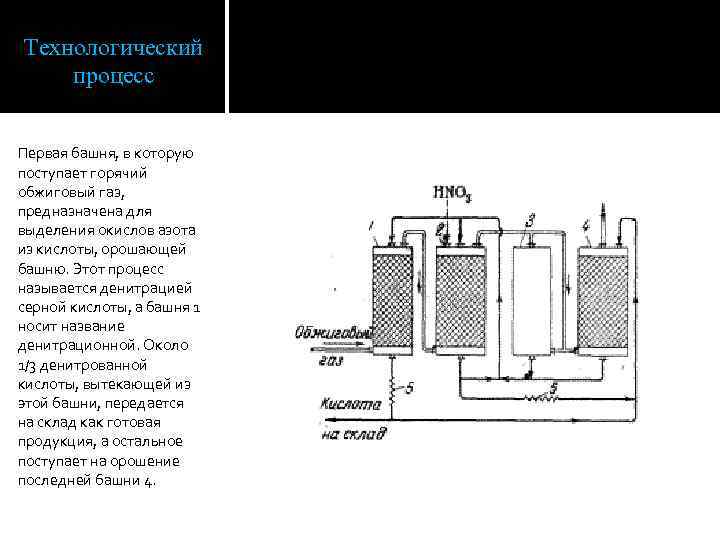
Технологический процесс Первая башня, в которую поступает горячий обжиговый газ, предназначена для выделения окислов азота из кислоты, орошающей башню. Этот процесс называется денитрацией серной кислоты, а башня 1 носит название денитрационной. Около 1/3 денитрованной кислоты, вытекающей из этой башни, передается на склад как готовая продукция, а остальное поступает на орошение последней башни 4.
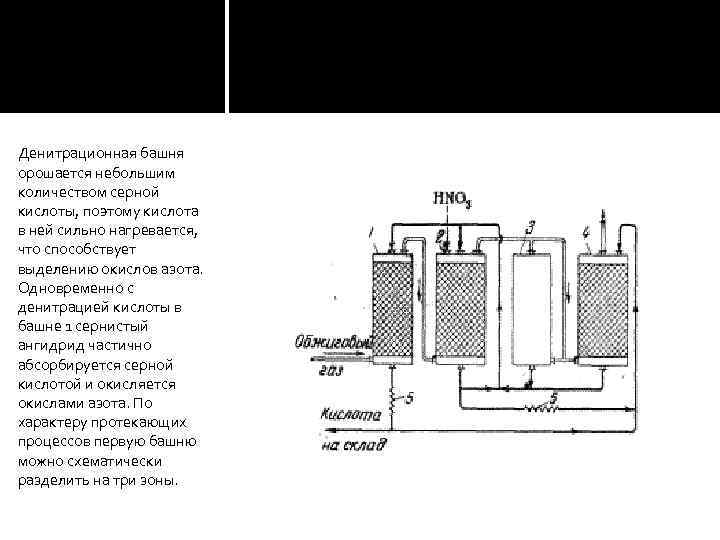
Денитрационная башня орошается небольшим количеством серной кислоты, поэтому кислота в ней сильно нагревается, что способствует выделению окислов азота. Одновременно с денитрацией кислоты в башне 1 сернистый ангидрид частично абсорбируется серной кислотой и окисляется окислами азота. По характеру протекающих процессов первую башню можно схематически разделить на три зоны.

В нижней зоне происходит упаривание серной кислоты с выделением водяных паров в газовую фазу, в средней зоне окислы азота выделяются из нитрозы вследствие наибольшего ее разбавления, в верхней зоне конденсируются поступающие снизу пары воды и, следовательно, происходит разбавление нитрозы и частичное окисление растворяющегося в ней SO 2. Строгого разделения перечисленных процессов по зонам провести нельзя, так как частично они совмещаются друг с другом. Кроме этих процессов, в первой башне из газа улавливаются также остатки пыли, поглощаются мышьяковистый ангидрид и двуокись селена, конденсируются пары серной кислоты (образуются из SO 3, присутствующего в обжиговом газе), происходит образование сернокислотного тумана и др. Туман лишь частично поглощается в первой башне, большая его часть поступает в последующие башни системы, где вследствие большой суммарной поверхности частиц тумана он существенно влияет на протекающие в башнях процессы. Готовую продукцию в башенных системах отводят только из денитрационной башни, где почти полностью улавливаются все примеси обжигового газа, поэтому башенная кислота загрязнена мышьяком, селеном, огарковой пылью и другими примесями. Основное назначение второй башни — абсорбция сернистого ангидрида из обжигового газа серной кислотой и окисление SO 2 нитрозой.
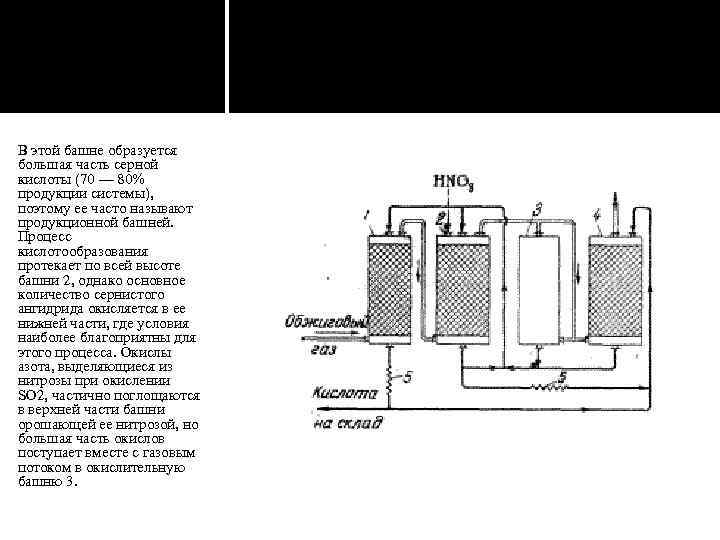
В этой башне образуется большая часть серной кислоты (70 — 80% продукции системы), поэтому ее часто называют продукционной башней. Процесс кислотообразования протекает по всей высоте башни 2, однако основное количество сернистого ангидрида окисляется в ее нижней части, где условия наиболее благоприятны для этого процесса. Окислы азота, выделяющиеся из нитрозы при окислении SO 2, частично поглощаются в верхней части башни орошающей ее нитрозой, но большая часть окислов поступает вместе с газовым потоком в окислительную башню 3.

Здесь окисляется такое количество окиси азота, которое требуется, чтобы соотношение между NO и NO 2 было наиболее благоприятным для поглощения их в абсорбционных башнях. В башне 3 NO окисляется кислородом, содержащимся в газе. Степень окисления окислов азота в этой башне регулируют, пропуская часть газа по обводному газопроводу помимо башни (байпас). Из окислительной башни газ поступает в башню 4, где окислы азота поглощаются орошающей ее серной кислотой; эту башню называют абсорбционной или поглотительной. При охлаждении обжигового газа и образовании серной кислоты выделяется большое количество тепла, поэтому в денитрационной и продукционных башнях орошающая кислота нагревается и перед возвратом на орошение ее приходится охлаждать. Для этого установлены холодильники 5. В процессе производства башенной кислоты неизбежны потери окислов азота с отходящими газами, с продукционной кислотой и др. Для восполнения этих потерь в продукционную башню 2 подается азотная кислота. Вода, необходимая для образования серной кислоты, вводится в денитрационную и продукционную башни 1 и 2.
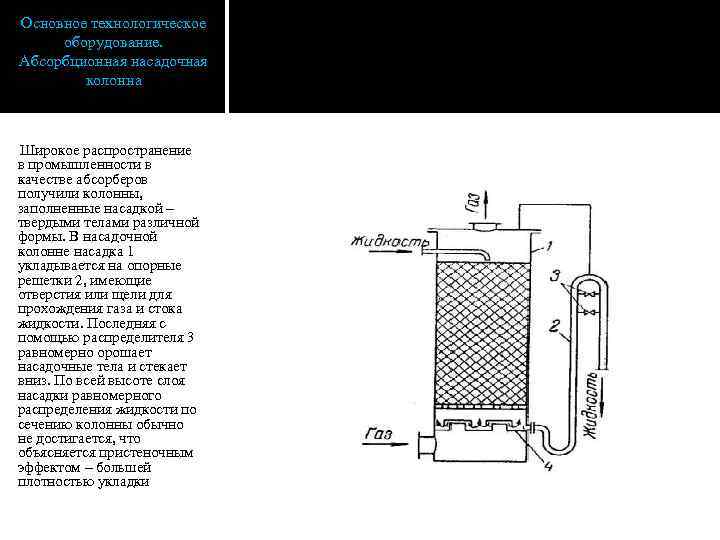
Основное технологическое оборудование. Абсорбционная насадочная колонна Широкое распространение в промышленности в качестве абсорберов получили колонны, заполненные насадкой – твердыми телами различной формы. В насадочной колонне насадка 1 укладывается на опорные решетки 2, имеющие отверстия или щели для прохождения газа и стока жидкости. Последняя с помощью распределителя 3 равномерно орошает насадочные тела и стекает вниз. По всей высоте слоя насадки равномерного распределения жидкости по сечению колонны обычно не достигается, что объясняется пристеночным эффектом – большей плотностью укладки
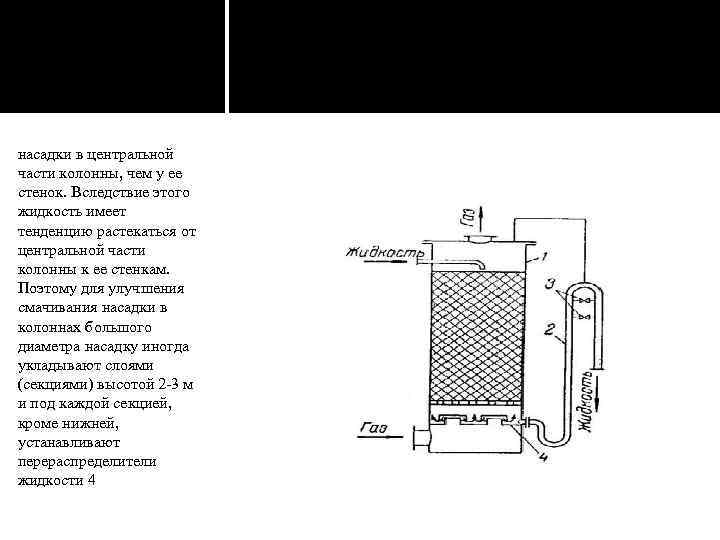
насадки в центральной части колонны, чем у ее стенок. Вследствие этого жидкость имеет тенденцию растекаться от центральной части колонны к ее стенкам. Поэтому для улучшения смачивания насадки в колоннах большого диаметра насадку иногда укладывают слоями (секциями) высотой 2 -3 м и под каждой секцией, кроме нижней, устанавливают перераспределители жидкости 4

Характеристика готового продукта Се рная кислота H 2 SO 4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха. В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO 3. Если молярное отношение SO 3: H 2 O < 1, то это водный раствор серной кислоты, если > 1, — раствор SO 3 в серной кислоте (олеум).

Техника безопасности В производстве возможны случаи отравления диоксидом серы, диоксидами азота, парами серной кислоты, в случае отравления: химические ожоги серной кислотой, олеумом, термические ожоги и опасность поражения электрическим током. Ванадиевый катализатор: опасна пыль содержащая соединения ванадия, вызывает изменения кровообращения, нарушает работу органов дыхания. ПДК не более 0. 5 мг/м 3

Сернистый ангидрид действует на дыхательные пути, приводит к появлению отдышки. ПДК 10 мл/м 3 Триоксид серы с влагой образует туман серной кислоты, которая вызывает раздражение дыхательных путей. ПДК 1 мл/м 3. При отравлении прополоскать горло раствором соды. Мышьяковистый и селенистый ангидриды: весьма ядовитые вещества. ПДК 0. 3 мл/м 3
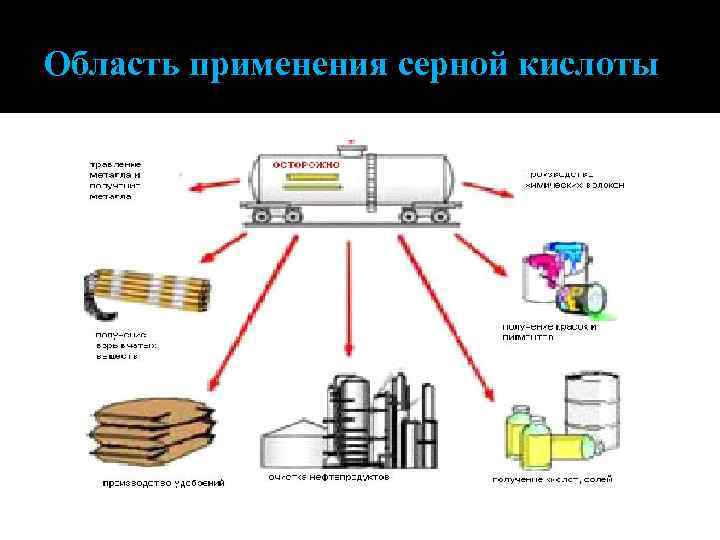
Область применения серной кислоты
Нитрозный метод получения сернойи кислоты.pptx