35 Одноатомные спирты.pptx
- Количество слайдов: 16

Назаров Б. К. представляет ОДНОАТОМНЫЕ СПИРТЫ

СПИРТЫ И ФЕНОЛЫ Спиртами называются соединения, содержащие одну или несколько гидроксильных групп (–ОН), связанных с углеводородным радикалом. Вещества, у которых гидроксил находится непосредственно у бензольного кольца, называются фенолами. В зависимости от числа гидроксильных групп спирты делят на одно-, двух- и трёхатомные. В зависимости от того, при каком углеродном атоме находится гидроксильная группа, различают спирты: первичные R–CH 2–OH, вторичные R и третичные R I I CH–OH, R’ - C–OH I I R’ R’’

Физические свойства Низшие спирты (до С 12) – жидкости, температуры кипения которых значительно выше, чем у соответствующих алканов из-за образования водородных связей за счёт полярной связи О–Н O–H …. . : O–H …… I I R R Метанол и этанол смешиваются с водой в любых соотношениях; с увеличением молекулярной массы растворимость спиртов в воде уменьшается.
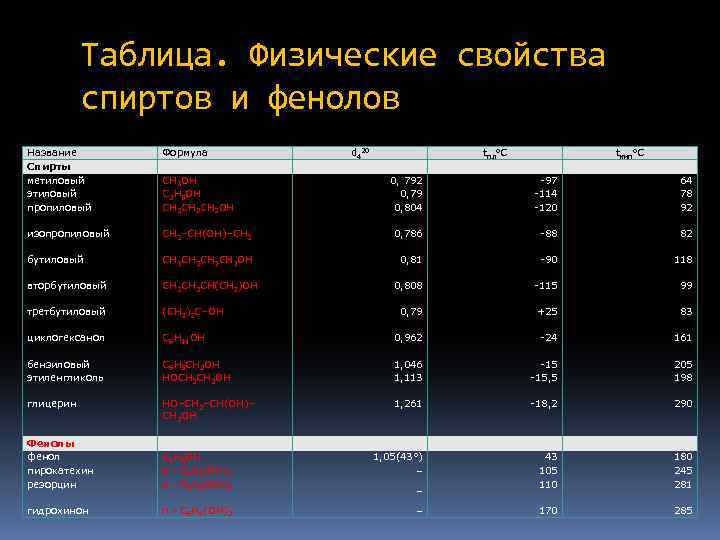
Таблица. Физические свойства спиртов и фенолов Название Спирты метиловый этиловый пропиловый Формула изопропиловый СН 3 OH С 2 Н 5 OH СН 3 СН 2 OH tпл C d 420 tкип C 0, 792 0, 79 0, 804 -97 -114 -120 64 78 92 СН 3–СН(ОH)–СH 3 0, 786 -88 82 бутиловый CH 3 CH 2 CH 2 OH 0, 81 -90 118 вторбутиловый CH 3 CH 2 CH(CH 3)OH 0, 808 -115 99 третбутиловый (СН 3)3 С–OH 0, 79 +25 83 циклогексанол С 6 Н 11 OH 0, 962 -24 161 бензиловый этиленгликоль C 6 H 5 CH 2 OH HOCH 2 OH 1, 046 1, 113 -15, 5 205 198 глицерин НО–СН 2–CH(ОН)– СН 2 OH 1, 261 -18, 2 290 43 105 110 180 245 281 170 285 Фенолы фенол пирокатехин резорцин С 6 Н 5 OH о - С 6 Н 4(OH)2 м - С 6 Н 4(OH)2 1, 05(43°) – гидрохинон n - С 6 Н 4(OH)2 – –

Одноатомные спирты Изомерия углеродного радикала (начиная с C 4 H 9 OH). Изомерия положения гидроксильной группы, (начиная с С 3 Н 7 ОН). Межклассовая изомерия с простыми эфирами (СН 3–СН 2–ОН и СН 3–О–СН 3). Название спиртов включает в себя наименование соответствующего углеводорода с добавлением суффикса -ол (положение гидроксильной группы указывают цифрой) или к названию углеводородного радикала добавляется слово "спирт"; также часто встречаются тривиальные (бытовые) названия: СН 3–ОН – метанол, метиловый спирт; СН 3–СН 2–ОН – этанол, этиловый спирт; СН 3–СН–СН 3 – пропанол-2, изопропиловый спирт. I OH

Получение В промышленности. Метанол синтезируют из синтез-газа на катализаторе (Zn. O, Сu) при 250 C и давлении 5 -10 МПа: СО + 2 Н 2 СН 3 ОН Ранее метанол получали сухой перегонкой древесины без доступа воздуха. Этанол получают: гидратацией этилена (Н 3 РО 4; 280 C; 8 МПа) СН 2=СН 2 + Н 2 О СН 3–СН 2–ОН брожением крахмала (или целлюлозы): крахмал С 6 Н 12 О 6(глюкоза) ––ферменты 2 С 2 Н 5 ОН + 2 СО 2 (источник крахмала – зерно, картофель)

В лаборатории. Гидратация алкенов (согласно правилу В. В. Марковникова): СH 3–СH=CH 2 + H 2 O ––H+ СH 3–CH– СH 3 I OH Гидролиз галогенопроизводных углеводородов: СH 3–СH 2–Br + H 2 O СH 3–CH 2–OH + HBr Чтобы сдвинуть равновесие вправо, добавляют щёлочь, которая связывает образующийся HBr.

Восстановление карбонильных соединений: Альдегиды образуют первичные спирты, а кетоны – вторичные. O II СH 3–СH 2 – C –– 2[H] СH 3–CH 2–OH I H СH 3 -- C --CH 3 –– 2[H] CH 3 --CH--СH 3 II I O OH
Химические свойства Свойства спиртов ROH определяются наличием полярных связей O -–H + и C +–O -, и неподеленных электронных пар на атоме кислорода. При реакции спиртов возможно разрушение одной из двух связей: C–OH (с отщеплением гидроксильной группы) или O–H (с отщеплением водорода). Это могут быть реакции замещения, в которых происходит замена OH или H, или элиминирование (отщепление), когда образуется двойная связь. На реакционную способность спиртов большое влияние оказывает строение радикалов, связанных с гидроксильной группой.

Реакции с разрывом связи RO–H Спирты реагируют с щелочными и щелочноземельными металлами, образуя солеобразные соединения – алкоголяты. Со щелочами спирты не взаимодействуют. 2 СH 3 CH 2 OH + 2 Na 2 СH 3 CH 2 ONa + H 2 2 СH 3 CH 2 OH + Сa (СH 3 CH 2 O)2 Ca + H 2 В присутствии воды алкоголяты гидролизуются: (СH 3)3 С–OK + H 2 O (СH 3)3 C–OH + KOH Это означает, что спирты – более слабые кислоты, чем вода.

Реакция этерификации Взаимодействие с органическими кислотами приводит к образованию сложных эфиров. O II II CH 3–C--OH + H --OC 2 H 5 H 2 SO 4 CH 3–C–O–C 2 H 5 + H 2 O (уксусноэтиловый эфир (этилацетат)) В общем виде: O II H+ II R–C--OH + H--OR’ R–C–O–R’ + H 2 O

Реакции с разрывом связи R–OH. С галогеноводородами: R–OH + HBr R–Br + H 2 O С концентрированной серной кислотой: C 2 H 5 O--H + H–O O C 2 H 5 O O // S (этилсерная кислота) + H 2 O / \ H–O O C 2 H 5–O O // S / \ C 2 H 5 O-H+ H–O O C 2 H 5 O O // S (диэтилсерная кислота(диэтилсульфат)) + H 2 O / \ C 2 H 5 O O

Реакции окисления Спирты горят: 2 С 3 H 7 ОH + 9 O 2 6 СO 2 + 8 H 2 O При действии окислителей: первичные спирты превращаются в альдегиды (или в карбоновые кислоты) (первичный R--CH 2–OH CH 3–CH 2–OH спирт) –– [O] K 2 Cr 2 O 7 –––– H 2 SO 4 O II O II R-- C (альдегид) –– [O] I H O II CH 3–C I H R-- C I OH K 2 Cr 2 O 7 –––– H 2 SO 4 O II CH 3 OH + Cu. O ––t H–C I H O II CH 3–C I OH + Cu + H 2 O (карбоновая к-та)
![Третичные спирты устойчивы к действию окислителей. R- -CH- -R’(вторичный спирт) ––[O] I OH CH Третичные спирты устойчивы к действию окислителей. R- -CH- -R’(вторичный спирт) ––[O] I OH CH](https://present5.com/presentation/69605649_132727716/image-14.jpg)
Третичные спирты устойчивы к действию окислителей. R- -CH- -R’(вторичный спирт) ––[O] I OH CH CH–CH 2–CH 3 3– I OH R- -C- -R'(кетон) II O K 2 Cr 2 O 7, H 2 SO 4 CH 3–C–CH 2–CH 3 II O

Дегидратация Внутримолекулярная дегидратация приводит к образованию алкенов CH 3–CH 2–OH ––t >140 C, H 2 SO 4 CH 2=CH 2 + H 2 O CH 3 I CH 3– C – CH 3 I I HO H t , H 2 SO 4 CH 3 I CH 3– =CH–CH 3 + H 2 O C При отщеплении воды от молекул вторичных и третичных спиртов атом водорода отрывается от соседнего наименее гидрогенизированного атома углерода; образующийся алкен содержит наибольшее число заместителей при двойной связи (правило Зайцева).

Межмолекулярная дегидратация даёт простые эфиры R--OH + H--O–R –– t , H 2 SO 4 R–O–R(простой эфир) + H 2 O CH 3–CH 2 --OH + H--O–CH 2–CH 3 ––t <140 C, H 2 SO 4 CH 3–CH 2–O–CH 2–CH 3(диэтиловый эфир) + H 2 O Обе реакции конкурируют между собой. Увеличение температуры и разбавление инертным растворителем благоприятствуют внутримолекулярному процессу.
35 Одноатомные спирты.pptx