алюминий.ppt
- Количество слайдов: 26
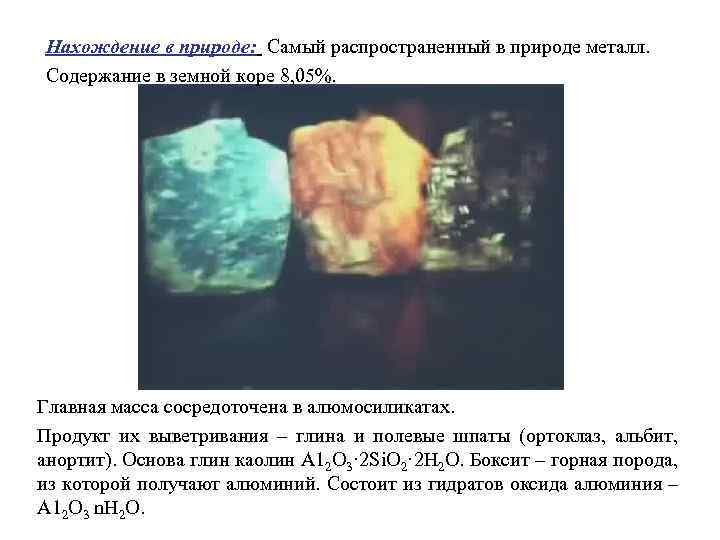 Нахождение в природе: Самый распространенный в природе металл. Содержание в земной коре 8, 05%. Главная масса сосредоточена в алюмосиликатах. Продукт их выветривания – глина и полевые шпаты (ортоклаз, альбит, анортит). Основа глин каолин А 12 О 3· 2 Si. О 2· 2 Н 2 О. Боксит – горная порода, из которой получают алюминий. Состоит из гидратов оксида алюминия – А 12 О 3 n. Н 2 О.
Нахождение в природе: Самый распространенный в природе металл. Содержание в земной коре 8, 05%. Главная масса сосредоточена в алюмосиликатах. Продукт их выветривания – глина и полевые шпаты (ортоклаз, альбит, анортит). Основа глин каолин А 12 О 3· 2 Si. О 2· 2 Н 2 О. Боксит – горная порода, из которой получают алюминий. Состоит из гидратов оксида алюминия – А 12 О 3 n. Н 2 О.
 Строение атома: На внешнем уровне три электрона: 3 s 23 p 1. Размер атома больше, а энергия ионизации меньше, чем у бора. Не металлические признаки у алюминия выражены в меньшей степени, чем у бора.
Строение атома: На внешнем уровне три электрона: 3 s 23 p 1. Размер атома больше, а энергия ионизации меньше, чем у бора. Не металлические признаки у алюминия выражены в меньшей степени, чем у бора.
 Физические свойства: Серебристо-белый мягкий металл, плавящийся при 6600 С. Пластичен, легко вытягивается в проволоку и раскатывается в листы. Обладает большой тепло- и электропроводностью. Его сплавы с различными металлами прочны и легки.
Физические свойства: Серебристо-белый мягкий металл, плавящийся при 6600 С. Пластичен, легко вытягивается в проволоку и раскатывается в листы. Обладает большой тепло- и электропроводностью. Его сплавы с различными металлами прочны и легки.
 Получение: Электролиз раствора А 12 О 3 в расплавленном криолите. Процесс ведут при 10000 С в специальных электропечах. (-)К: А 13+ + 3 е = А 1 (+)А: 4 А 1 О 33 - -12 е = 2 А 12 О 3 + 3 О 2
Получение: Электролиз раствора А 12 О 3 в расплавленном криолите. Процесс ведут при 10000 С в специальных электропечах. (-)К: А 13+ + 3 е = А 1 (+)А: 4 А 1 О 33 - -12 е = 2 А 12 О 3 + 3 О 2
 Химические свойства: Характерная степень окисления +3. 1) Химически активен, в обычных условиях покрывается очень прочной оксидной пленкой. Последняя ослабляет металлический блеск и определяет его высокую коррозионную стойкость.
Химические свойства: Характерная степень окисления +3. 1) Химически активен, в обычных условиях покрывается очень прочной оксидной пленкой. Последняя ослабляет металлический блеск и определяет его высокую коррозионную стойкость.
 2) Горит в О 2 при высоких температурах в мелко раздробленном состоянии: 4 А 1 + 3 О 2 = 2 А 12 О 3
2) Горит в О 2 при высоких температурах в мелко раздробленном состоянии: 4 А 1 + 3 О 2 = 2 А 12 О 3
 3) С йодом реагирует при нагревании или в присутствии воды как катализатора. С хлором и бромом при обычной температуре : 2 А 1 +3 Вr 2 = 2 А 1 Вr 3
3) С йодом реагирует при нагревании или в присутствии воды как катализатора. С хлором и бромом при обычной температуре : 2 А 1 +3 Вr 2 = 2 А 1 Вr 3
 4) Если с алюминия снять оксидную пленку, то он взаимодействует с кислородом воздуха: 2 А 1 + 3 О 2 + 6 Н 2 О = 4 А 1(ОН)3
4) Если с алюминия снять оксидную пленку, то он взаимодействует с кислородом воздуха: 2 А 1 + 3 О 2 + 6 Н 2 О = 4 А 1(ОН)3
 5) Очищенный от оксидной пленки взаимодействует с водой: 2 А 1 + 6 Н 2 О = 2 А 1(ОН)3 + 3 Н 2 6) Взаимодействует с серой: 2 А 1 + 3 S = А 12 S 3. 7) При 8000 2 А 1 + N 2 = 2 А 1 N 8) При 20000 4 А 1 + 3 С = А 14 С 3 9) С водородом непосредственно не взаимодействует.
5) Очищенный от оксидной пленки взаимодействует с водой: 2 А 1 + 6 Н 2 О = 2 А 1(ОН)3 + 3 Н 2 6) Взаимодействует с серой: 2 А 1 + 3 S = А 12 S 3. 7) При 8000 2 А 1 + N 2 = 2 А 1 N 8) При 20000 4 А 1 + 3 С = А 14 С 3 9) С водородом непосредственно не взаимодействует.
 10) В ряду напряжения стоит до водорода, растворяется в разбавленных Н 2 SО 4 и НС 1: 2 А 1+6 НС 1=2 А 1 С 13+3 Н 2 2 А 1+3 Н 2 SО 4=А 12(SО 4)3+3 Н 2 11) Разбавленная и концентрированная НNО 3 на холоду пассивирует А 1, но при нагревании он Значения стандартного электродного потенциала: в кислой среде: А 13+ +3 е = А 1, Е 0298 = -1, 66 В в щелочной среде А 1 О 2 -+2 Н 2 О+3 е=А 1+4 ОН-, Е 0298= -2, 35 В
10) В ряду напряжения стоит до водорода, растворяется в разбавленных Н 2 SО 4 и НС 1: 2 А 1+6 НС 1=2 А 1 С 13+3 Н 2 2 А 1+3 Н 2 SО 4=А 12(SО 4)3+3 Н 2 11) Разбавленная и концентрированная НNО 3 на холоду пассивирует А 1, но при нагревании он Значения стандартного электродного потенциала: в кислой среде: А 13+ +3 е = А 1, Е 0298 = -1, 66 В в щелочной среде А 1 О 2 -+2 Н 2 О+3 е=А 1+4 ОН-, Е 0298= -2, 35 В
 12) А 1 активно восстанавливает многие металлы из оксидов (алюмотермия): 2 А 1 + Мо. О 3 = Мо + А 12 О 3 Применяется в производстве Мn, Сr, V, W, ферросплавов.
12) А 1 активно восстанавливает многие металлы из оксидов (алюмотермия): 2 А 1 + Мо. О 3 = Мо + А 12 О 3 Применяется в производстве Мn, Сr, V, W, ферросплавов.
 Применение: 1)химическая аппаратура; 2) электрические провода; 3) конденсаторы; 4) фольга для пищевой и фармацевтической промышленности; 5)легкие сплавы используют в автомобилестроении, судостроении, авиастроении; 6) емкости для перевозки НNО 3; 7) лигирующая добавка – придает жаропрочность. Соединения с d – элементами - алюминиды, используются в качестве жаропрочных материалов.
Применение: 1)химическая аппаратура; 2) электрические провода; 3) конденсаторы; 4) фольга для пищевой и фармацевтической промышленности; 5)легкие сплавы используют в автомобилестроении, судостроении, авиастроении; 6) емкости для перевозки НNО 3; 7) лигирующая добавка – придает жаропрочность. Соединения с d – элементами - алюминиды, используются в качестве жаропрочных материалов.
 СОЕДИНЕНИЯ СТЕПЕНЬ ОКИСЛЕНИЯ +3 А 12 О 3 имеет несколько модификаций: В обычных условиях устойчив α А 12 О 3. Эта модификация встречается в природе в виде корунда. Физические свойства: Высокая прочность связи А 1 -О-А 1 и плотная кристаллическая структура придают высокую температуру плавления (20500 С), твердость, огнеупорность А 12 О 3. Применение: 1) Абразивный материал - корунд по твердости уступает только алмазу, карбарунду и эльбору и применяется в виде корундовых кругов и наждака. 2) Монокристаллы корунда используют, как опорные камни в точных механизмах. 3) Искусственные рубины используют в качестве квантовых генераторов (лазеры). Сильно прокаленный А 12 О 3 – алунда.
СОЕДИНЕНИЯ СТЕПЕНЬ ОКИСЛЕНИЯ +3 А 12 О 3 имеет несколько модификаций: В обычных условиях устойчив α А 12 О 3. Эта модификация встречается в природе в виде корунда. Физические свойства: Высокая прочность связи А 1 -О-А 1 и плотная кристаллическая структура придают высокую температуру плавления (20500 С), твердость, огнеупорность А 12 О 3. Применение: 1) Абразивный материал - корунд по твердости уступает только алмазу, карбарунду и эльбору и применяется в виде корундовых кругов и наждака. 2) Монокристаллы корунда используют, как опорные камни в точных механизмах. 3) Искусственные рубины используют в качестве квантовых генераторов (лазеры). Сильно прокаленный А 12 О 3 – алунда.
 Часто в корунде атомы А 13+ частично замещены на атомы других элементов, придающих ему окраску. Окрашенные кристаллы корунда - драгоценные камни. - рубин – примесь Сr 3+ сапфир – примесь Тi 3+ и Fе 3+ Их можно получать искусственно.
Часто в корунде атомы А 13+ частично замещены на атомы других элементов, придающих ему окраску. Окрашенные кристаллы корунда - драгоценные камни. - рубин – примесь Сr 3+ сапфир – примесь Тi 3+ и Fе 3+ Их можно получать искусственно.
 Кристаллическая модификация А 12 О 3 химически стойкая: 1) Не взаимодействует с водой и кислотами. 2) При кипячении в концентрированных растворах щелочей частично переходит в раствор. 3) А 12 О 3 переводит в раствор: А 12 О 3 + 2 КОН = 2 КА 1 О 2 + Н 2 О А 12 О 3 + 3 К 2 S 2 О 7 = 5 К 2 SО 4 + А 12(SО 4)3
Кристаллическая модификация А 12 О 3 химически стойкая: 1) Не взаимодействует с водой и кислотами. 2) При кипячении в концентрированных растворах щелочей частично переходит в раствор. 3) А 12 О 3 переводит в раствор: А 12 О 3 + 2 КОН = 2 КА 1 О 2 + Н 2 О А 12 О 3 + 3 К 2 S 2 О 7 = 5 К 2 SО 4 + А 12(SО 4)3
 При сплавлении А 12 О 3 с К 2 СО 3 образуются алюминаты, которые легко растворяются в воде: А 12 О 3 + К 2 СО 3 = 2 КА 1 О 2 + СО 2 Применение: Производство металлического алюминия. Для этого используют глинозем, который получают из бокситов и переработанной нефти.
При сплавлении А 12 О 3 с К 2 СО 3 образуются алюминаты, которые легко растворяются в воде: А 12 О 3 + К 2 СО 3 = 2 КА 1 О 2 + СО 2 Применение: Производство металлического алюминия. Для этого используют глинозем, который получают из бокситов и переработанной нефти.
 Гидроксид алюминия Получение: А 12 О 3 в воде не растворим. Отвечающий ему гидроксид получают косвенным путем (исходя из солей). А 1 С 13+3 КОН=А 1(ОН)3+3 КС 1 Кристаллический А 1(ОН)3 получают при пропускании СО 2 в щелочной раствор алюмината: Nа. А 1(ОН)4 + СО 2 = А 1(ОН)3 + Nа. НСО 3
Гидроксид алюминия Получение: А 12 О 3 в воде не растворим. Отвечающий ему гидроксид получают косвенным путем (исходя из солей). А 1 С 13+3 КОН=А 1(ОН)3+3 КС 1 Кристаллический А 1(ОН)3 получают при пропускании СО 2 в щелочной раствор алюмината: Nа. А 1(ОН)4 + СО 2 = А 1(ОН)3 + Nа. НСО 3
 Физические свойства: А 1(ОН)3 – полимерное соединение, имеет слоистую кристаллическую решетку, между слоями существует водородная связь. Объёмный, студенистый осадок белого цвета. Химические свойства: 1)нерастворим в воде. 2)Амфотерное вещество, легко растворяется в кислотах и щелочах: 2 А 1(ОН)3 + 3 Н 2 SО 4 = А 12(SО 4)3 + 6 Н 2 О А 1(ОН)3 + 3 КОН = К 3[А 1(ОН)6] Основные и особенно кислотные свойства выражены слабо. 3) В избытке NН 4 ОН не растворим. 4) При стоянии осадок постепенно (с выделением Н 2 О) переходит в кристаллический А 1(ОН)3 и теряет свою активность – ''стареет''. 5)
Физические свойства: А 1(ОН)3 – полимерное соединение, имеет слоистую кристаллическую решетку, между слоями существует водородная связь. Объёмный, студенистый осадок белого цвета. Химические свойства: 1)нерастворим в воде. 2)Амфотерное вещество, легко растворяется в кислотах и щелочах: 2 А 1(ОН)3 + 3 Н 2 SО 4 = А 12(SО 4)3 + 6 Н 2 О А 1(ОН)3 + 3 КОН = К 3[А 1(ОН)6] Основные и особенно кислотные свойства выражены слабо. 3) В избытке NН 4 ОН не растворим. 4) При стоянии осадок постепенно (с выделением Н 2 О) переходит в кристаллический А 1(ОН)3 и теряет свою активность – ''стареет''. 5)
 При прокаливании А 12 О 3·n. Н 2 О постепенно теряет Н 2 О, превращаясь в А 1 ООН (бемит) и в конечном счете в А 12 О 3. Высушенный А 1(ОН)3 не растворяется ни в щелочах, ни в кислотах (напоминает А 12 О 3). Алюмогель форма дегидратированного А 1(ОН)3. Применение: 1) адсорбент 2) очистка воды.
При прокаливании А 12 О 3·n. Н 2 О постепенно теряет Н 2 О, превращаясь в А 1 ООН (бемит) и в конечном счете в А 12 О 3. Высушенный А 1(ОН)3 не растворяется ни в щелочах, ни в кислотах (напоминает А 12 О 3). Алюмогель форма дегидратированного А 1(ОН)3. Применение: 1) адсорбент 2) очистка воды.
 Алюминаты Получение: А 1(ОН)3+КОН= КА 1 О 2+2 Н 2 О. Химические свойства: 1) Алюминаты I валентных активных металлов растворимы в воде. 2) Их растворы устойчивы только в щелочной среде, т. к. гидролизуются: КА 1 О 2+2 Н 2 О =А 1(ОН)3+КОН, р. Н>7 Алюминаты слабых оснований гидролизованы на цело. Получают их сплавление А 12 О 3 с оксидом металла. В воде нерастворимы.
Алюминаты Получение: А 1(ОН)3+КОН= КА 1 О 2+2 Н 2 О. Химические свойства: 1) Алюминаты I валентных активных металлов растворимы в воде. 2) Их растворы устойчивы только в щелочной среде, т. к. гидролизуются: КА 1 О 2+2 Н 2 О =А 1(ОН)3+КОН, р. Н>7 Алюминаты слабых оснований гидролизованы на цело. Получают их сплавление А 12 О 3 с оксидом металла. В воде нерастворимы.
 Соли иона А 13+ Ион А 13+ в растворе бесцветный. Получение: А 1(ОН)3 +3 НС 1=А 1 С 13+Н 2 О Химические свойства: 1) Производные сильных кислот в воде растворимы, и гидролизованы, среда кислая. 2) Соли слабых кислот гидролизованы ещё сильнее. Многие водой разлагаются полностью: А 12 S 3+6 Н 2 О=2 А 1(ОН)3+3 Н 2 S А 12(SО 4)3 и квасцы используют в бумажной промышленности, в кожевенной (дубление), в текстильной (крашение) и т. д.
Соли иона А 13+ Ион А 13+ в растворе бесцветный. Получение: А 1(ОН)3 +3 НС 1=А 1 С 13+Н 2 О Химические свойства: 1) Производные сильных кислот в воде растворимы, и гидролизованы, среда кислая. 2) Соли слабых кислот гидролизованы ещё сильнее. Многие водой разлагаются полностью: А 12 S 3+6 Н 2 О=2 А 1(ОН)3+3 Н 2 S А 12(SО 4)3 и квасцы используют в бумажной промышленности, в кожевенной (дубление), в текстильной (крашение) и т. д.
 Алюмосиликаты Это силикаты, в которых часть тэтраэдров Si. О 44 - заменена на тетраэдры А 1 О 45 -. Распространены полевые шпаты: ортоклаз - К[А 1 Si 3 О 8], альбит - Nа[А 1 Si 3 О 8], анортит - Са[А 12 Si 2 О 8], нефелин – (Nа, К)2[А 12 Si 2 О 8]. Используется для получения глинозема: (Nа, К)2[А 12 Si 2 О 8]+2 Са. СО 3=2 Са. Si. О 3+Nа. А 1 О 2+КА 1 О 2+2 СО 2 Nа. А 1 О 2 + КА 1 О 2 + 4 Н 2 О = Nа[А 1(ОН)4] + К[А 1(ОН)4] Nа[А 1(ОН)4]+К[А 1(ОН)4]+2 СО 2=Nа. НСО 3+КНСО 3+2 А 1(ОН)3= А 12 О 3 + 3 Н 2 О Выпариванием выделяют Nа 2 СО 3+К 2 СО 3, а шлам (Са. Si. О 3) идет на производство цемента.
Алюмосиликаты Это силикаты, в которых часть тэтраэдров Si. О 44 - заменена на тетраэдры А 1 О 45 -. Распространены полевые шпаты: ортоклаз - К[А 1 Si 3 О 8], альбит - Nа[А 1 Si 3 О 8], анортит - Са[А 12 Si 2 О 8], нефелин – (Nа, К)2[А 12 Si 2 О 8]. Используется для получения глинозема: (Nа, К)2[А 12 Si 2 О 8]+2 Са. СО 3=2 Са. Si. О 3+Nа. А 1 О 2+КА 1 О 2+2 СО 2 Nа. А 1 О 2 + КА 1 О 2 + 4 Н 2 О = Nа[А 1(ОН)4] + К[А 1(ОН)4] Nа[А 1(ОН)4]+К[А 1(ОН)4]+2 СО 2=Nа. НСО 3+КНСО 3+2 А 1(ОН)3= А 12 О 3 + 3 Н 2 О Выпариванием выделяют Nа 2 СО 3+К 2 СО 3, а шлам (Са. Si. О 3) идет на производство цемента.
 Цеолиты Их состав выражается формулой: Мх. Эу. О 2 z n. Н 2 О, где М=Са, Nа (реже Ва, Sr, К) Э=Si и А 1 в переменном соотношении.
Цеолиты Их состав выражается формулой: Мх. Эу. О 2 z n. Н 2 О, где М=Са, Nа (реже Ва, Sr, К) Э=Si и А 1 в переменном соотношении.
 Кремнекислородные и алюмокислородные тетраэдры, которые соединены друг с другом через атомы кислорода. Благодаря такому строению в кристаллах цеолитов имеются свободные полости. В этих полостях располагаются ионы М+ и М 2+, компенсирующие отрицательный заряд алюмокремнекислородных тетраэдров, и в них могут внедряться молекулы Н 2 О. Соединение воды зависит от давления водяного пара. Цеолиты способны обменивать воду на другие вещества (спирт, NН 3 и т. д. ). При удалении, и даже полное обезвоживание не приводит к разрушению кристаллической решетки цеолита. Искусственные цеолиты используются в качестве молекулярных сит. Молекулярные сита поглощают вещества, молекулы которых могут войти в их полости (d=0, 3 - 1, 3 нм). Например, одно из молекулярных сит с d=0, 35 нм) может поглотить Н 2, О 2, N 2, но не поглощают более крупные молекулы типа СН 4, или атомы Аr. Применение: 1) разделение углеводородов, 2) осушка газов и жидкостей. 3) цеолиты с внедренными d ионами являются катализаторами. 4) ионнообменники
Кремнекислородные и алюмокислородные тетраэдры, которые соединены друг с другом через атомы кислорода. Благодаря такому строению в кристаллах цеолитов имеются свободные полости. В этих полостях располагаются ионы М+ и М 2+, компенсирующие отрицательный заряд алюмокремнекислородных тетраэдров, и в них могут внедряться молекулы Н 2 О. Соединение воды зависит от давления водяного пара. Цеолиты способны обменивать воду на другие вещества (спирт, NН 3 и т. д. ). При удалении, и даже полное обезвоживание не приводит к разрушению кристаллической решетки цеолита. Искусственные цеолиты используются в качестве молекулярных сит. Молекулярные сита поглощают вещества, молекулы которых могут войти в их полости (d=0, 3 - 1, 3 нм). Например, одно из молекулярных сит с d=0, 35 нм) может поглотить Н 2, О 2, N 2, но не поглощают более крупные молекулы типа СН 4, или атомы Аr. Применение: 1) разделение углеводородов, 2) осушка газов и жидкостей. 3) цеолиты с внедренными d ионами являются катализаторами. 4) ионнообменники
 Другие соединения алюминия А 12 S 3 получают прямой синтез при температуре красного каления. Это кристаллическое вещество (tпл = 11000 С), полностью гидролизуется даже следами влаги в воздухе. А 1 На 13 - кристаллические вещества. Получают прямым синтезом. Реакционноспособные. С водой реагируют с выделением тепла, гидролизуются, но неполно и обратимо. С основными галогенидами А 1 На 13 образует галогеналюминаты. Наиболее устойчив криолит Nа 3 А 1 F 6. Производство криолита: 2 А 1(ОН)3 + 12 НF + 3 Nа 2 СО 3 = 2 Nа 3 А 1 F 6 + 3 CО 2 + 9 Н 2 О Фторалюминаты щелочных металлов в воде растворяются с трудом
Другие соединения алюминия А 12 S 3 получают прямой синтез при температуре красного каления. Это кристаллическое вещество (tпл = 11000 С), полностью гидролизуется даже следами влаги в воздухе. А 1 На 13 - кристаллические вещества. Получают прямым синтезом. Реакционноспособные. С водой реагируют с выделением тепла, гидролизуются, но неполно и обратимо. С основными галогенидами А 1 На 13 образует галогеналюминаты. Наиболее устойчив криолит Nа 3 А 1 F 6. Производство криолита: 2 А 1(ОН)3 + 12 НF + 3 Nа 2 СО 3 = 2 Nа 3 А 1 F 6 + 3 CО 2 + 9 Н 2 О Фторалюминаты щелочных металлов в воде растворяются с трудом
 Алюминий образует полимерный гидрид (алан) А 1 Н 3. Получают: 3 Li[А 1 Н 4] + А 1 С 13 = 4 А 1 Н 3 + 3 Li. С 1 А 1 Н 3 – белый порошок, разлагается при нагревании выше 1050 С с выделением водорода. При взаимодействии с основными гидридами в эфирном растворе образуются гидридоалюминаты: Li. Н + А 1 Н 3 =Li [А 1 Н 4] Это белые твердые вещества. Устойчивость меньше гидридоборатов. Водой бурно разлагаются. Сильные восстановители. Применяют в органическом синтезе.
Алюминий образует полимерный гидрид (алан) А 1 Н 3. Получают: 3 Li[А 1 Н 4] + А 1 С 13 = 4 А 1 Н 3 + 3 Li. С 1 А 1 Н 3 – белый порошок, разлагается при нагревании выше 1050 С с выделением водорода. При взаимодействии с основными гидридами в эфирном растворе образуются гидридоалюминаты: Li. Н + А 1 Н 3 =Li [А 1 Н 4] Это белые твердые вещества. Устойчивость меньше гидридоборатов. Водой бурно разлагаются. Сильные восстановители. Применяют в органическом синтезе.


