Л_01-SPA-Введение-цели и задачи НОПК.ppt
- Количество слайдов: 27
 НАУЧНЫЕ ОСНОВЫ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРОВ Николай Александрович Пахомов Кандидат химических наук, старший научный сотрудник ИК СО РАН, доцент НГУ, зам. зав. кафедрой “Катализ и адсорбция” (до 2011 г. ). Область научных интересов: научные основы приготовления катализаторов, катализ нанесенными сплавами и оксидами: разработка и исследование катализаторов для процессов дегидрирования и изомеризации низших парафинов, селективного хлорирования углеводородов и дегидрохлорирования. Педагогический стаж – 25 лет. Создал курс лекций Павел Анатольевич Симонов “Научные основы приготовления катализаторов” Кандидат химических наук, старший научный сотрудник ИК СО РАН, ассистент, зам. зав. кафедрой “Катализ и адсорбция” НГУ. Область научных интересов: научные основы приготовления нанесённых металлических катализаторов, взаимосвязь структуры и реакционной способности углеродных материалов, изучение механиз-мов взаимодействия металлокомплексов с поверхностью адсорбентов (носителей), разработка и исследование нанесённых катализаторов на основе благородных
НАУЧНЫЕ ОСНОВЫ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРОВ Николай Александрович Пахомов Кандидат химических наук, старший научный сотрудник ИК СО РАН, доцент НГУ, зам. зав. кафедрой “Катализ и адсорбция” (до 2011 г. ). Область научных интересов: научные основы приготовления катализаторов, катализ нанесенными сплавами и оксидами: разработка и исследование катализаторов для процессов дегидрирования и изомеризации низших парафинов, селективного хлорирования углеводородов и дегидрохлорирования. Педагогический стаж – 25 лет. Создал курс лекций Павел Анатольевич Симонов “Научные основы приготовления катализаторов” Кандидат химических наук, старший научный сотрудник ИК СО РАН, ассистент, зам. зав. кафедрой “Катализ и адсорбция” НГУ. Область научных интересов: научные основы приготовления нанесённых металлических катализаторов, взаимосвязь структуры и реакционной способности углеродных материалов, изучение механиз-мов взаимодействия металлокомплексов с поверхностью адсорбентов (носителей), разработка и исследование нанесённых катализаторов на основе благородных
 Лекция 1 1. Введение. История становления науки о катализе 2. Цели и задачи научных основ приготовления катализаторов (НОПК) 2. 1. Положения Г. К. Борескова о химической природе катализа 2. 2. Основные проблемы катализа 2. 3. Развитие взглядов и подходов к приготовлению катализаторов 2. 4. Классификация катализаторов. Основные типы промышленных катализаторов 2. 5. Цели и задачи научных основ приготовления и технологии катализаторов 2. 6. Связь НОПК с другими научными дисциплинами
Лекция 1 1. Введение. История становления науки о катализе 2. Цели и задачи научных основ приготовления катализаторов (НОПК) 2. 1. Положения Г. К. Борескова о химической природе катализа 2. 2. Основные проблемы катализа 2. 3. Развитие взглядов и подходов к приготовлению катализаторов 2. 4. Классификация катализаторов. Основные типы промышленных катализаторов 2. 5. Цели и задачи научных основ приготовления и технологии катализаторов 2. 6. Связь НОПК с другими научными дисциплинами
 1. Введение. История становления науки о катализе Уже древние переработки народы широко использовали для пищевых продуктов случайно обнаруженные биокаталитические приёмы, совершенно не зная их сущности 6000 лет до н. э. – использование солода для пивоварения 3000 лет до н. э. – получение вина брожением виноградного сока 2000 лет до н. э. – производство алкогольных напитков ферментацией различного углеводного сырья 800 лет до н. э. – получение сыра с использованием сычуга
1. Введение. История становления науки о катализе Уже древние переработки народы широко использовали для пищевых продуктов случайно обнаруженные биокаталитические приёмы, совершенно не зная их сущности 6000 лет до н. э. – использование солода для пивоварения 3000 лет до н. э. – получение вина брожением виноградного сока 2000 лет до н. э. – производство алкогольных напитков ферментацией различного углеводного сырья 800 лет до н. э. – получение сыра с использованием сычуга
 ► Первые упоминания о химических процессах, известных в настоящее время как каталитические VIII в. – Джабир ибн Хайам (Гебер): 1200 г. – Раймонд Люллиус: 1540 г. – Валериус Кордус: “серный эфир” “сладкий купорос” “сладкое купоросное масло” 1680 г. – Роберт Бойль 1704 г. – Исаак Ньютон 1730 г. – С. Фробениус: 1666 – А. Лефебр и Н. Лемери “эфир”
► Первые упоминания о химических процессах, известных в настоящее время как каталитические VIII в. – Джабир ибн Хайам (Гебер): 1200 г. – Раймонд Люллиус: 1540 г. – Валериус Кордус: “серный эфир” “сладкий купорос” “сладкое купоросное масло” 1680 г. – Роберт Бойль 1704 г. – Исаак Ньютон 1730 г. – С. Фробениус: 1666 – А. Лефебр и Н. Лемери “эфир”
 ► Конец 18 – середина 19 вв. : накопление фактов и первые попытки объяснения механизмов реакций 1781 – Антуан-Огюст Пармантье (Франция) 1779 -1782 – Карл Шееле (Швеция) Этерификация органич. кислот, H+ 1783 – Джон Бойтон Пристли (Англия) 1796 – Мартин ван-Марум (Голландия) 1806 – Никола Клеман и Шарль Дезорм (Франция) 1811 -1814 – Константин Киргоф (Россия) ! 1803 -1808 – Дж. Дальтон Теория кратных отношений: химическое вещество состоит из атомов, соединенных в молекулы в определенной весовой пропорции
► Конец 18 – середина 19 вв. : накопление фактов и первые попытки объяснения механизмов реакций 1781 – Антуан-Огюст Пармантье (Франция) 1779 -1782 – Карл Шееле (Швеция) Этерификация органич. кислот, H+ 1783 – Джон Бойтон Пристли (Англия) 1796 – Мартин ван-Марум (Голландия) 1806 – Никола Клеман и Шарль Дезорм (Франция) 1811 -1814 – Константин Киргоф (Россия) ! 1803 -1808 – Дж. Дальтон Теория кратных отношений: химическое вещество состоит из атомов, соединенных в молекулы в определенной весовой пропорции
 1813 -1818 – Луи Жак Тенар (Франция) 1817 – Гэмфри и Джон Дэви (Англия) 1821 – Иоганн Дёберейнер (Германия) 1820 – Эдмун Дэви (Англия), Дёберейнер (1821) 1831 – Перегрин Филлипс (Англия) 1844 – Майкл Фарадей (Англия) 1828 – А. Геннель (лаб. М. Фарадея) 1833 – Эйльхард Митчерлих (Германия) Окисление паров органических веществ на Pt при комнатной t
1813 -1818 – Луи Жак Тенар (Франция) 1817 – Гэмфри и Джон Дэви (Англия) 1821 – Иоганн Дёберейнер (Германия) 1820 – Эдмун Дэви (Англия), Дёберейнер (1821) 1831 – Перегрин Филлипс (Англия) 1844 – Майкл Фарадей (Англия) 1828 – А. Геннель (лаб. М. Фарадея) 1833 – Эйльхард Митчерлих (Германия) Окисление паров органических веществ на Pt при комнатной t
 Первые взгляды на природу обнаруженных процессов: Э. Митчерлих (1833, Германия): реакции, ускоряемые другими веществами – «контактные реакции» Якоб Берцелиус (1835, Швеция): эти вещества не поглощаются в ходе ускоряемой ими реакции, а причина их действия – в исходящей от них некой «каталитической силе» Катализ – (греч. ) – разрушение, разложение (термин введен в 16 -ом веке А. Либавиусом в учебнике «Алхимия» ) Майкл Фарадей (1840, Англия): каталитические явления можно объяснить известными свойствами материи, не снабжая ее при этом никакой новой силой А. Белани (1824) и М. Фарадей (1833) – авторы первых теорий катализа, позднее названных “адсорбционными”
Первые взгляды на природу обнаруженных процессов: Э. Митчерлих (1833, Германия): реакции, ускоряемые другими веществами – «контактные реакции» Якоб Берцелиус (1835, Швеция): эти вещества не поглощаются в ходе ускоряемой ими реакции, а причина их действия – в исходящей от них некой «каталитической силе» Катализ – (греч. ) – разрушение, разложение (термин введен в 16 -ом веке А. Либавиусом в учебнике «Алхимия» ) Майкл Фарадей (1840, Англия): каталитические явления можно объяснить известными свойствами материи, не снабжая ее при этом никакой новой силой А. Белани (1824) и М. Фарадей (1833) – авторы первых теорий катализа, позднее названных “адсорбционными”
 ► Вторая половина 19 вв. : начало систематических исследований каталитических реакций А. М. Бутлеров, М. М. Зайцев, М. Г. Кучеров, В. Н. Ипатьев, А. Е. Фаворский, Д. П. Коновалов, Н. Д. Зелинский, Л. В. Писаржевский, Д. И. Менделеев, Я. -Г. Вант-Гофф, С. А. Аррениус, М. Боденштейн, В. Ф. Оствальд, П. Сабатье, А. Гофман и др. Особенности этого периода исследований Становление науки о катализе было сопряжено, с одной стороны, с зарождением промышленного производства и насущными проблемами его развития в индустриальных странах, а с другой, – с накоплением знаний в смежных областях естествознания (физика, физическая химия, химия комплексных соединений, кристаллохимия, химия твердого тела и др. ) Исторически сложившееся разделение на гомогенный и гетерогенный катализ (и в последствии – ферментативный катализ) препятствовало поиску их общих закономерностей
► Вторая половина 19 вв. : начало систематических исследований каталитических реакций А. М. Бутлеров, М. М. Зайцев, М. Г. Кучеров, В. Н. Ипатьев, А. Е. Фаворский, Д. П. Коновалов, Н. Д. Зелинский, Л. В. Писаржевский, Д. И. Менделеев, Я. -Г. Вант-Гофф, С. А. Аррениус, М. Боденштейн, В. Ф. Оствальд, П. Сабатье, А. Гофман и др. Особенности этого периода исследований Становление науки о катализе было сопряжено, с одной стороны, с зарождением промышленного производства и насущными проблемами его развития в индустриальных странах, а с другой, – с накоплением знаний в смежных областях естествознания (физика, физическая химия, химия комплексных соединений, кристаллохимия, химия твердого тела и др. ) Исторически сложившееся разделение на гомогенный и гетерогенный катализ (и в последствии – ферментативный катализ) препятствовало поиску их общих закономерностей
 ► Конец 19 - начало 20 вв. : раскрытие сущности каталитических реакций с точки зрения их кинетики, термодинамики и механизма: Л. Плэйфейр (1848): Н. Н. Бекетов (1865), К. М. Гульберг и П. Вааге (1867): Теория нестойких промежуточных соединений Закон действующих масс Я. -Г. Вант-Гофф (1884): Молекулярность (порядок) реакций, химическое равновесие В. Ф. Оствальд (1884 -1888) С. А. Аррениус (1884 -1887) В. Ф. Нернст (1888 -1889): Теория электролитической диссоциации С. А. Аррениус (1889): Уравнение Аррениуса М. Боденштейн (1913): Принцип стационарной концентрации промежуточных продуктов реакции Й. Н. Брёнстед (1923 -1924): Г. Льюис (1924): Протонная теория кислот, связь между силой кислот и оснований и их каталитической активностью, солевые эффекты в кинетике Электронная теория кислот и реакций оснований Л. Плейфейр и П. Сабатье – авторы первых “химических” теорий катализа
► Конец 19 - начало 20 вв. : раскрытие сущности каталитических реакций с точки зрения их кинетики, термодинамики и механизма: Л. Плэйфейр (1848): Н. Н. Бекетов (1865), К. М. Гульберг и П. Вааге (1867): Теория нестойких промежуточных соединений Закон действующих масс Я. -Г. Вант-Гофф (1884): Молекулярность (порядок) реакций, химическое равновесие В. Ф. Оствальд (1884 -1888) С. А. Аррениус (1884 -1887) В. Ф. Нернст (1888 -1889): Теория электролитической диссоциации С. А. Аррениус (1889): Уравнение Аррениуса М. Боденштейн (1913): Принцип стационарной концентрации промежуточных продуктов реакции Й. Н. Брёнстед (1923 -1924): Г. Льюис (1924): Протонная теория кислот, связь между силой кислот и оснований и их каталитической активностью, солевые эффекты в кинетике Электронная теория кислот и реакций оснований Л. Плейфейр и П. Сабатье – авторы первых “химических” теорий катализа
 ► Первая половина 20 -го в. – определение катализа: В. Ф. Оствальд (1895) Катализатор – вещество, которое увеличивает скорость достижения равновесия химического процесса без существенного поглощения в ходе реакции П. Сабатье (1901) Катализатор – вещество, которое изменяет скорость реакции, участвуя в последовательности её стадий, но не превращаясь в продукты Катализ осуществляется в результате реакции, а не простого присутствия вещества Э. Абель (1913) Д. И. Менделеев (1886), Н. Д. Зелинский (1925) Каталитическое действие заключается в деформации молекул на поверхности катализатора, вследствие чего увеличивается их реакционная способность П. Рашиг (1906) Катализ представляет вызываемое внешними причинами изменение строения молекулы, имеющее следствием изменение химических свойств Л. Гурвич (1916) Каталитически действующие тела, притягивая к себе движущиеся молекулы гораздо сильнее, чем тела, лишенные каталитического действия, тем самым увеличивают силу удара, попадающих на их поверхность молекул
► Первая половина 20 -го в. – определение катализа: В. Ф. Оствальд (1895) Катализатор – вещество, которое увеличивает скорость достижения равновесия химического процесса без существенного поглощения в ходе реакции П. Сабатье (1901) Катализатор – вещество, которое изменяет скорость реакции, участвуя в последовательности её стадий, но не превращаясь в продукты Катализ осуществляется в результате реакции, а не простого присутствия вещества Э. Абель (1913) Д. И. Менделеев (1886), Н. Д. Зелинский (1925) Каталитическое действие заключается в деформации молекул на поверхности катализатора, вследствие чего увеличивается их реакционная способность П. Рашиг (1906) Катализ представляет вызываемое внешними причинами изменение строения молекулы, имеющее следствием изменение химических свойств Л. Гурвич (1916) Каталитически действующие тела, притягивая к себе движущиеся молекулы гораздо сильнее, чем тела, лишенные каталитического действия, тем самым увеличивают силу удара, попадающих на их поверхность молекул
 50 лет (1953 - 1968) Г. К. Боресков (1962) А. А. Баландин (1964) В. И. Кузнецов Феноменологически катализ – это возбуждение химических реакций или изменение их скорости под влиянием веществ – катализаторов, многократно вступающих в промежуточное химическое взаимодействие с участниками реакции и восстанавливающих после каждого цикла промежуточных взаимодействий свой состав Катализ – воздействие вещества на реакцию, избирательно изменяющее её кинетику, но сохраняющее её стехиометрические и термодинамические условия; это воздействие состоит в заменен одних элементарных процессов другими , циклическими, в которых участвует воздействующее вещество. В пределе, это вещество (катализатор) не изменяется в результате реакции и не смещает равновесия Катализ – это процессы инициирования, химической ориентации и матричной ориентации реакций, происходящие во взаимной обусловленности и являющиеся результатом взаимодействия дискретной и непрерывной форм химической организации вещества (позднее определение дополнено представлением об энергетической активации – эффекте аггравации)
50 лет (1953 - 1968) Г. К. Боресков (1962) А. А. Баландин (1964) В. И. Кузнецов Феноменологически катализ – это возбуждение химических реакций или изменение их скорости под влиянием веществ – катализаторов, многократно вступающих в промежуточное химическое взаимодействие с участниками реакции и восстанавливающих после каждого цикла промежуточных взаимодействий свой состав Катализ – воздействие вещества на реакцию, избирательно изменяющее её кинетику, но сохраняющее её стехиометрические и термодинамические условия; это воздействие состоит в заменен одних элементарных процессов другими , циклическими, в которых участвует воздействующее вещество. В пределе, это вещество (катализатор) не изменяется в результате реакции и не смещает равновесия Катализ – это процессы инициирования, химической ориентации и матричной ориентации реакций, происходящие во взаимной обусловленности и являющиеся результатом взаимодействия дискретной и непрерывной форм химической организации вещества (позднее определение дополнено представлением об энергетической активации – эффекте аггравации)
 ► Середина 20 -го в. – становление методологии исследования кинетики гетерогенных реакций: Г. Тейлор (1925 -30) Концепция активных центров катализаторов С. Брунауэр П. Эммет, Е. Теллер (1938) Создание теории полимолекулярной адсорбции и метода БЭТ для измерения удельной поверхности пористых тел Г. Дамкёлер (1937) Я. Б. Зельдович (1939) Е. В. Тиле (1939) Теоретический анализ связи массопереноса в порах катализатора с наблюдаемой скоростью реакции М. И. Тёмкин (1950) Создание безградиентного реактора W каталитическая активность, т. е. количество вещества, превращённого в единицу времени в единице объема катализатора при заданных условиях; S полная площадь поверхности катализатора в единице объема; Х доля активной поверхности в катализаторе; Ауд удельная каталитическая активность (УКА), т. е. активность единицы “активной” поверхности катализатора;
► Середина 20 -го в. – становление методологии исследования кинетики гетерогенных реакций: Г. Тейлор (1925 -30) Концепция активных центров катализаторов С. Брунауэр П. Эммет, Е. Теллер (1938) Создание теории полимолекулярной адсорбции и метода БЭТ для измерения удельной поверхности пористых тел Г. Дамкёлер (1937) Я. Б. Зельдович (1939) Е. В. Тиле (1939) Теоретический анализ связи массопереноса в порах катализатора с наблюдаемой скоростью реакции М. И. Тёмкин (1950) Создание безградиентного реактора W каталитическая активность, т. е. количество вещества, превращённого в единицу времени в единице объема катализатора при заданных условиях; S полная площадь поверхности катализатора в единице объема; Х доля активной поверхности в катализаторе; Ауд удельная каталитическая активность (УКА), т. е. активность единицы “активной” поверхности катализатора;
 2. 1. Положения Г. К. Борескова о химической природе катализа § Изменение скорости химической реакции при гетерогенном катализе вызывается промежуточным поверхностным химическим взаимодействием реагирующих веществ с катализатором. Активность твердого катализатора в отношении данной реакции определяется, в первую очередь, его химическими свойствами § Каталитическая активность присуща нормальной поверхности кристаллических твердых тел и не связана с особым состоянием или особыми структурными элементами их поверхности § Удельная каталитическая активность, УКА (активность единицы поверхности), катализаторов постоянного состава приблизительно одинакова. Основным фактором, определяющим УКА, является химический состав и химическое строение катализатора § Для катализаторов с определенной УКА мощным фактором повышения активности единицы объема, характеризующей промышленную ценность катализатора, является увеличение работающей поверхности. Это может быть достигнуто путем увеличения внутренней поверхности и создания оптимальной пористой структуры катализатора, в обеспечивающей Боресков Г. К. - В кн. : Гетерогенный катализ химической промышленности: Материалы Всесоюзного совещания. М. , 1953, поверхности высокую степень использования его внутренней М. : Госхимиздат, 1955, с. 5 -28.
2. 1. Положения Г. К. Борескова о химической природе катализа § Изменение скорости химической реакции при гетерогенном катализе вызывается промежуточным поверхностным химическим взаимодействием реагирующих веществ с катализатором. Активность твердого катализатора в отношении данной реакции определяется, в первую очередь, его химическими свойствами § Каталитическая активность присуща нормальной поверхности кристаллических твердых тел и не связана с особым состоянием или особыми структурными элементами их поверхности § Удельная каталитическая активность, УКА (активность единицы поверхности), катализаторов постоянного состава приблизительно одинакова. Основным фактором, определяющим УКА, является химический состав и химическое строение катализатора § Для катализаторов с определенной УКА мощным фактором повышения активности единицы объема, характеризующей промышленную ценность катализатора, является увеличение работающей поверхности. Это может быть достигнуто путем увеличения внутренней поверхности и создания оптимальной пористой структуры катализатора, в обеспечивающей Боресков Г. К. - В кн. : Гетерогенный катализ химической промышленности: Материалы Всесоюзного совещания. М. , 1953, поверхности высокую степень использования его внутренней М. : Госхимиздат, 1955, с. 5 -28.
 2. 2. Основные проблемы катализа • Создание теории предвидения каталитического действия (экспериментальное и квантово-химическое исследование реакционной способности веществ, глубокое изучение природы промежуточных соединений, механизмов реакций и раскрытие зависимости удельной каталитической активности от химического состава и строения катализатора на атомно-молекулярном уровне) • Разработка научных основ приготовления и технологии катализаторов (разработка теоретических и экспериментальных подходов к целенаправленному синтезу катализаторов с заданными свойствами – химическим и фазовым составом, структурой активного компонента (или активного центра) и текстурными характеристиками) • Развитие научных основ технологии каталитических процессов (изучение кинетики каталитических реакций, математическое моделирование протекания каталитических процессов для определения типа каталитического реактора, оптимальных условий процесса, технологической схемы производства)
2. 2. Основные проблемы катализа • Создание теории предвидения каталитического действия (экспериментальное и квантово-химическое исследование реакционной способности веществ, глубокое изучение природы промежуточных соединений, механизмов реакций и раскрытие зависимости удельной каталитической активности от химического состава и строения катализатора на атомно-молекулярном уровне) • Разработка научных основ приготовления и технологии катализаторов (разработка теоретических и экспериментальных подходов к целенаправленному синтезу катализаторов с заданными свойствами – химическим и фазовым составом, структурой активного компонента (или активного центра) и текстурными характеристиками) • Развитие научных основ технологии каталитических процессов (изучение кинетики каталитических реакций, математическое моделирование протекания каталитических процессов для определения типа каталитического реактора, оптимальных условий процесса, технологической схемы производства)
 2. 3. Развитие взглядов и подходов к приготовлению катализаторов § Приготовление катализаторов как “искусство”: П. А. Митташ (промышленный катализатор Fe-K 2 O-Al 2 O 3 синтеза NH 3 из N 2+H 2 в процессе Габера-Боша, Германия, 1913 -1916 гг. ) – при поиске катализатора испытано около 20 тыс. веществ. Ю. Гудри (первая промышленная установка по каталитическому крекингу тяжёлых фракций нефти на алюмосиликатном катализаторе, США, 1937 г. ) – от идеи до её практической реализации прошло 10 лет. В. Н. Ипатьев (высокоэффективный кислотный катализатор алкилирования алкенов для получения высокооктановых бензинов, США, 1940 -42 гг. ) – от анализа причины невоспроизводимости общепринятой стандартной методики выделения алкенов из смеси с алканами серной кислотой до создания катализатора прошло около 3 лет. К. В. Циглер и Дж. Натта (промышленный катализатор Al. R 3 -Ti. Cl 3 полимеризации этилена, 1952 -53 гг. ) – от анализа причин неудачных экспериментов по олиго-меризации этилена на Al. R 3 до
2. 3. Развитие взглядов и подходов к приготовлению катализаторов § Приготовление катализаторов как “искусство”: П. А. Митташ (промышленный катализатор Fe-K 2 O-Al 2 O 3 синтеза NH 3 из N 2+H 2 в процессе Габера-Боша, Германия, 1913 -1916 гг. ) – при поиске катализатора испытано около 20 тыс. веществ. Ю. Гудри (первая промышленная установка по каталитическому крекингу тяжёлых фракций нефти на алюмосиликатном катализаторе, США, 1937 г. ) – от идеи до её практической реализации прошло 10 лет. В. Н. Ипатьев (высокоэффективный кислотный катализатор алкилирования алкенов для получения высокооктановых бензинов, США, 1940 -42 гг. ) – от анализа причины невоспроизводимости общепринятой стандартной методики выделения алкенов из смеси с алканами серной кислотой до создания катализатора прошло около 3 лет. К. В. Циглер и Дж. Натта (промышленный катализатор Al. R 3 -Ti. Cl 3 полимеризации этилена, 1952 -53 гг. ) – от анализа причин неудачных экспериментов по олиго-меризации этилена на Al. R 3 до
 § Приготовление катализаторов как “наука”: 1. 1925 -1940 гг. – концепция активных центров (Г. Тейлор), стимулировавшая развитие мультиплетной теории катализа (А. А. Баландин) и теории активных ансамблей (Н. И. Кобозев). «Теория пересыщения» С. З. Рогинского – первая теория приготовления катализаторов, базирующаяся на представлении, что каталитические свойства твердого тела определяются неравновесным состоянием его поверхности, наличием на ней различного рода дефектов в виде дислокаций, катионной или анионной нестехиометрии, присутствием примесных атомов. 2. 1937 -1939 гг. – метод БЭТ для измерения удельной поверхности пористых тел, создание теории диффузионно-контролируемых химических процессов. 1940 -1950 гг. – экспериментальное обнаружение (спектральными методами) образования промежуточных соединений на поверхности катализаторов, последующее разложение которых приводило к конечным продуктам (А. Н. Теренин, Р. Эйшенс). 1950 -1953 гг. – измерение каталитической активности в безградиентных реак-торах, введение понятия об УКА и
§ Приготовление катализаторов как “наука”: 1. 1925 -1940 гг. – концепция активных центров (Г. Тейлор), стимулировавшая развитие мультиплетной теории катализа (А. А. Баландин) и теории активных ансамблей (Н. И. Кобозев). «Теория пересыщения» С. З. Рогинского – первая теория приготовления катализаторов, базирующаяся на представлении, что каталитические свойства твердого тела определяются неравновесным состоянием его поверхности, наличием на ней различного рода дефектов в виде дислокаций, катионной или анионной нестехиометрии, присутствием примесных атомов. 2. 1937 -1939 гг. – метод БЭТ для измерения удельной поверхности пористых тел, создание теории диффузионно-контролируемых химических процессов. 1940 -1950 гг. – экспериментальное обнаружение (спектральными методами) образования промежуточных соединений на поверхности катализаторов, последующее разложение которых приводило к конечным продуктам (А. Н. Теренин, Р. Эйшенс). 1950 -1953 гг. – измерение каталитической активности в безградиентных реак-торах, введение понятия об УКА и
 § Приготовление катализаторов как “наука”: 3. Конец 60 -х – начало 80 -х гг. ХХ в. – интенсивное развитие и применение физических методов для исследования структуры пористых тел и состояния их поверхности (в том числе и методов in situ). Закладка теоретических основ «традиционных» методов приготовления катализаторов – осаждения и соосаждения, нанесения (пропитка, адсорбция), механического смешения, термического разложения. 4. Конец 80 -х – по настоящее время: – усовершенствование традиционных методов приготовления, основанное на фундаментальных достижениях НОПК, – создание новых, «нетрадиционных» , методов приготовления, исходя из современных достижений в области нанотехнологий (радиационные, плазменные, электрохимические и др. методы).
§ Приготовление катализаторов как “наука”: 3. Конец 60 -х – начало 80 -х гг. ХХ в. – интенсивное развитие и применение физических методов для исследования структуры пористых тел и состояния их поверхности (в том числе и методов in situ). Закладка теоретических основ «традиционных» методов приготовления катализаторов – осаждения и соосаждения, нанесения (пропитка, адсорбция), механического смешения, термического разложения. 4. Конец 80 -х – по настоящее время: – усовершенствование традиционных методов приготовления, основанное на фундаментальных достижениях НОПК, – создание новых, «нетрадиционных» , методов приготовления, исходя из современных достижений в области нанотехнологий (радиационные, плазменные, электрохимические и др. методы).
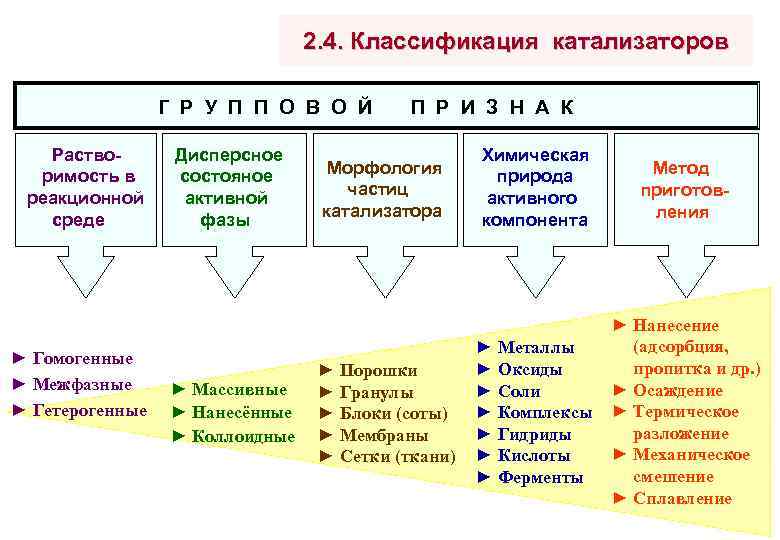 2. 4. Классификация катализаторов Г Р У П П О В О Й Растворимость в реакционной среде ► Гомогенные ► Межфазные ► Гетерогенные Дисперсное состояное активной фазы ► Массивные ► Нанесённые ► Коллоидные П Р И З Н А К Морфология частиц катализатора ► Порошки ► Гранулы ► Блоки (соты) ► Мембраны ► Сетки (ткани) Химическая природа активного компонента Метод приготовления ► Металлы ► Оксиды ► Соли ► Комплексы ► Гидриды ► Кислоты ► Ферменты ► Нанесение (адсорбция, пропитка и др. ) ► Осаждение ► Термическое разложение ► Механическое смешение ► Сплавление
2. 4. Классификация катализаторов Г Р У П П О В О Й Растворимость в реакционной среде ► Гомогенные ► Межфазные ► Гетерогенные Дисперсное состояное активной фазы ► Массивные ► Нанесённые ► Коллоидные П Р И З Н А К Морфология частиц катализатора ► Порошки ► Гранулы ► Блоки (соты) ► Мембраны ► Сетки (ткани) Химическая природа активного компонента Метод приготовления ► Металлы ► Оксиды ► Соли ► Комплексы ► Гидриды ► Кислоты ► Ферменты ► Нанесение (адсорбция, пропитка и др. ) ► Осаждение ► Термическое разложение ► Механическое смешение ► Сплавление
 Основные типы промышленных катализаторов Г Р У П П О В О Й Класс катализируемых процессов П Р И З Н А К Однокомпонентные катализаторы Катализаторы для нефтепереработки: ► Гидроочистка (400 С, 40 атм) ► Крекинг (500 С, 2 -3 атм) Pt, Cr-катализаторы ► Гидрокрекинг WS 2/Al 2 O 3 (500 С, 100 атм) ► Риформинг (500 С, 5 -15 атм) Pt/Al 2 O 3 ► Изомеризация (400 С, 5 -40 атм) цеолиты, Pt(или Pd)/Al 2 O 3( Cl−, F−) Многокомпонентные катализаторы (Co-Mo)Sx/Al 2 O 3, (Ni-Mo)Sx/Al 2 O 3 Цеолиты + редкие земли (Co-Mo)Sx/Al 2 O 3, цеолиты + Pt, Pd, Ni, Co Pt-Re-Ir/Al 2 O 3 ( Cl−, SO 42−), Pt-Sn/Al 2 O 3( Cl−)
Основные типы промышленных катализаторов Г Р У П П О В О Й Класс катализируемых процессов П Р И З Н А К Однокомпонентные катализаторы Катализаторы для нефтепереработки: ► Гидроочистка (400 С, 40 атм) ► Крекинг (500 С, 2 -3 атм) Pt, Cr-катализаторы ► Гидрокрекинг WS 2/Al 2 O 3 (500 С, 100 атм) ► Риформинг (500 С, 5 -15 атм) Pt/Al 2 O 3 ► Изомеризация (400 С, 5 -40 атм) цеолиты, Pt(или Pd)/Al 2 O 3( Cl−, F−) Многокомпонентные катализаторы (Co-Mo)Sx/Al 2 O 3, (Ni-Mo)Sx/Al 2 O 3 Цеолиты + редкие земли (Co-Mo)Sx/Al 2 O 3, цеолиты + Pt, Pd, Ni, Co Pt-Re-Ir/Al 2 O 3 ( Cl−, SO 42−), Pt-Sn/Al 2 O 3( Cl−)
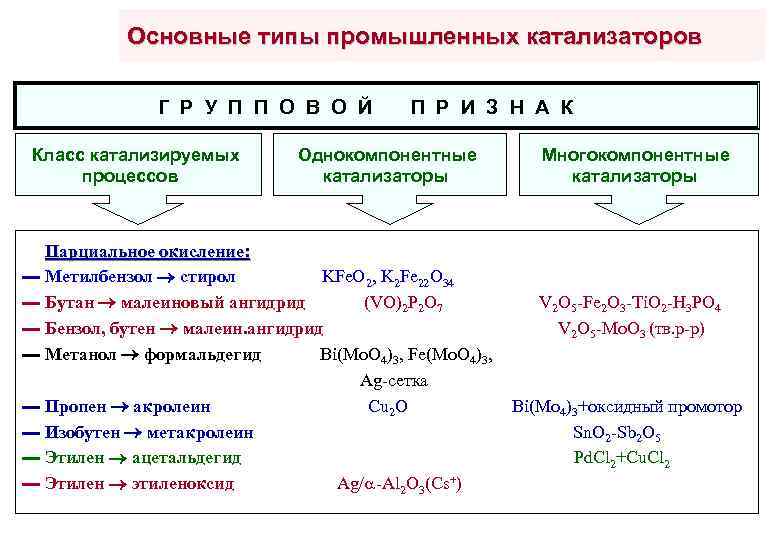 Основные типы промышленных катализаторов Г Р У П П О В О Й Класс катализируемых процессов П Р И З Н А К Однокомпонентные катализаторы Парциальное окисление: ▬ Метилбензол стирол KFe. O 2, K 2 Fe 22 O 34 ▬ Бутан малеиновый ангидрид (VO)2 P 2 O 7 ▬ Бензол, бутен малеин. ангидрид ▬ Метанол формальдегид Bi(Mo. O 4)3, Fe(Mo. O 4)3, Ag-сетка ▬ Пропен акролеин Cu 2 O ▬ Изобутен метакролеин ▬ Этилен ацетальдегид ▬ Этилен этиленоксид Ag/ -Al 2 O 3(Cs+) Многокомпонентные катализаторы V 2 O 5 -Fe 2 O 3 -Ti. O 2 -H 3 PO 4 V 2 O 5 -Mo. O 3 (тв. р-р) Bi(Mo 4)3+оксидный промотор Sn. O 2 -Sb 2 O 5 Pd. Cl 2+Cu. Cl 2
Основные типы промышленных катализаторов Г Р У П П О В О Й Класс катализируемых процессов П Р И З Н А К Однокомпонентные катализаторы Парциальное окисление: ▬ Метилбензол стирол KFe. O 2, K 2 Fe 22 O 34 ▬ Бутан малеиновый ангидрид (VO)2 P 2 O 7 ▬ Бензол, бутен малеин. ангидрид ▬ Метанол формальдегид Bi(Mo. O 4)3, Fe(Mo. O 4)3, Ag-сетка ▬ Пропен акролеин Cu 2 O ▬ Изобутен метакролеин ▬ Этилен ацетальдегид ▬ Этилен этиленоксид Ag/ -Al 2 O 3(Cs+) Многокомпонентные катализаторы V 2 O 5 -Fe 2 O 3 -Ti. O 2 -H 3 PO 4 V 2 O 5 -Mo. O 3 (тв. р-р) Bi(Mo 4)3+оксидный промотор Sn. O 2 -Sb 2 O 5 Pd. Cl 2+Cu. Cl 2
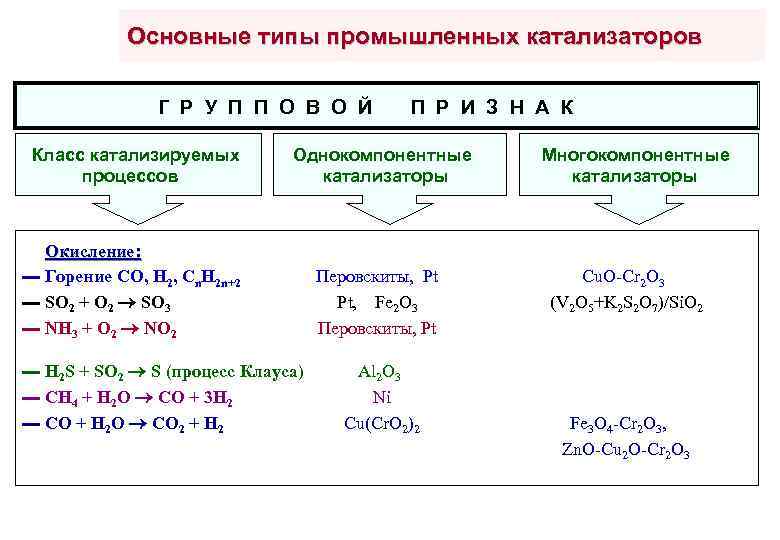 Основные типы промышленных катализаторов Г Р У П П О В О Й Класс катализируемых процессов П Р И З Н А К Однокомпонентные катализаторы Oкисление: ▬ Горение CO, H 2, Cn. H 2 n+2 ▬ SO 2 + O 2 SO 3 ▬ NH 3 + O 2 NO 2 ▬ H 2 S + SO 2 S (процесс Клауса) ▬ CH 4 + H 2 O CO + 3 H 2 ▬ CO + H 2 O CO 2 + H 2 Перовскиты, Pt Pt, Fe 2 O 3 Перовскиты, Pt Al 2 O 3 Ni Cu(Cr. O 2)2 Многокомпонентные катализаторы Cu. O-Cr 2 O 3 (V 2 O 5+K 2 S 2 O 7)/Si. O 2 Fe 3 O 4 -Cr 2 O 3, Zn. O-Cu 2 O-Cr 2 O 3
Основные типы промышленных катализаторов Г Р У П П О В О Й Класс катализируемых процессов П Р И З Н А К Однокомпонентные катализаторы Oкисление: ▬ Горение CO, H 2, Cn. H 2 n+2 ▬ SO 2 + O 2 SO 3 ▬ NH 3 + O 2 NO 2 ▬ H 2 S + SO 2 S (процесс Клауса) ▬ CH 4 + H 2 O CO + 3 H 2 ▬ CO + H 2 O CO 2 + H 2 Перовскиты, Pt Pt, Fe 2 O 3 Перовскиты, Pt Al 2 O 3 Ni Cu(Cr. O 2)2 Многокомпонентные катализаторы Cu. O-Cr 2 O 3 (V 2 O 5+K 2 S 2 O 7)/Si. O 2 Fe 3 O 4 -Cr 2 O 3, Zn. O-Cu 2 O-Cr 2 O 3
 Основные типы промышленных катализаторов Окислительное дегидрирование: ▬ Бутен + O 2 Бутадиен Bi(Mo. O 4)3, Mn. Fe 2 O 4, Zn(Cr 2 -x. Fex)O 4 ▬ NH 3 + O 2 NO 2 Перовскиты, Pt Дегидрирование: Cr 2 O 3, Cu. O, Fe 2 O 3, Mo. O 3, V 2 O 5, Co, Pt, Pd, Rh, Ag на носителях Гидрирование: Cr 2 O 3, Cu. O, Fe 2 O 3, Mo. O 3, V 2 O 5, Zn. O, Ni, Co, Pt, Pd, Rh, Ru, Ag на носителях Гидрогенолиз: Cu. O, Ni, Co, Pt, Pd, Rh, Ru, на носителях Алкилирование: Cr 2 O 3, Al 2 O 3, Fe 2 O 3, Ni. O, H 3 PO 4/Si. O 2, Al. Cl 3, Mo, Ni, Pt, Pd, Ru, Re Карбонилирование: Fe 2 O 3, Mo. O 3, Zn. O, Pd Карбоксилирование: Rh Изомеризация: Al 2 O 3, Mo. O 3, Fe 2 O 3, Cu. O-Cr 2 O 3, Al 2 O 3 -Si. O 2 Ni, Co, Pt, Pd на носителях Полимеризация: Fe 2 O 3, Pd, Ti. Cl 4+Al. R 3, Cr. O 3/Si. O 2, Al. Cl 3, BF 3 Кислотно-основной катализ: H 3 PO 4/Si. O 2, гетерополикислоты, Al 2 O 3 -Si. O 2
Основные типы промышленных катализаторов Окислительное дегидрирование: ▬ Бутен + O 2 Бутадиен Bi(Mo. O 4)3, Mn. Fe 2 O 4, Zn(Cr 2 -x. Fex)O 4 ▬ NH 3 + O 2 NO 2 Перовскиты, Pt Дегидрирование: Cr 2 O 3, Cu. O, Fe 2 O 3, Mo. O 3, V 2 O 5, Co, Pt, Pd, Rh, Ag на носителях Гидрирование: Cr 2 O 3, Cu. O, Fe 2 O 3, Mo. O 3, V 2 O 5, Zn. O, Ni, Co, Pt, Pd, Rh, Ru, Ag на носителях Гидрогенолиз: Cu. O, Ni, Co, Pt, Pd, Rh, Ru, на носителях Алкилирование: Cr 2 O 3, Al 2 O 3, Fe 2 O 3, Ni. O, H 3 PO 4/Si. O 2, Al. Cl 3, Mo, Ni, Pt, Pd, Ru, Re Карбонилирование: Fe 2 O 3, Mo. O 3, Zn. O, Pd Карбоксилирование: Rh Изомеризация: Al 2 O 3, Mo. O 3, Fe 2 O 3, Cu. O-Cr 2 O 3, Al 2 O 3 -Si. O 2 Ni, Co, Pt, Pd на носителях Полимеризация: Fe 2 O 3, Pd, Ti. Cl 4+Al. R 3, Cr. O 3/Si. O 2, Al. Cl 3, BF 3 Кислотно-основной катализ: H 3 PO 4/Si. O 2, гетерополикислоты, Al 2 O 3 -Si. O 2
 2. 5. Цели и задачи научных основ приготовления и технологии катализаторов Создание научных основ приготовления катализаторов (НОПК) подразумевает решение следующих равнозначных по важности и часто взаимосвязанных задач: § управление процессами формирования заданного химического и фазового состава катализатора, направленных на достижение требуемой структуры его активных центров, § управление процессами формирования заданной субструктуры первичных частиц, микроструктуры и текстуры их агрегатов, направленных на достижение требуемой концентрации активных центров и характера их распределения в порах катализатора, § управление процессами придания зёрнам катализатора требуемой морфологии, необходимой для достижения определенных эксплуатационных качеств катализатора
2. 5. Цели и задачи научных основ приготовления и технологии катализаторов Создание научных основ приготовления катализаторов (НОПК) подразумевает решение следующих равнозначных по важности и часто взаимосвязанных задач: § управление процессами формирования заданного химического и фазового состава катализатора, направленных на достижение требуемой структуры его активных центров, § управление процессами формирования заданной субструктуры первичных частиц, микроструктуры и текстуры их агрегатов, направленных на достижение требуемой концентрации активных центров и характера их распределения в порах катализатора, § управление процессами придания зёрнам катализатора требуемой морфологии, необходимой для достижения определенных эксплуатационных качеств катализатора
 Основная проблема не может быть создано всеобъемлющей, универсальной теории приготовления катализаторов Причины: • громадное количество катализаторов, сильно различающихся по свойствам, • широкое разнообразие методов их приготовления, • приготовление многих промышленных катализаторов, основанное в целом на известных теоретических и экспериментальных подходах, содержит в себе элементы «knowhow» Подходы к частичному решению проблемы: • рассмотрение катализаторов по признаку общности их определенных свойств и характеристик (т. е. разделение на отдельные классы и группы), • поиск общих закономерностей формирования катализаторов в рамках определенного класса или группы
Основная проблема не может быть создано всеобъемлющей, универсальной теории приготовления катализаторов Причины: • громадное количество катализаторов, сильно различающихся по свойствам, • широкое разнообразие методов их приготовления, • приготовление многих промышленных катализаторов, основанное в целом на известных теоретических и экспериментальных подходах, содержит в себе элементы «knowhow» Подходы к частичному решению проблемы: • рассмотрение катализаторов по признаку общности их определенных свойств и характеристик (т. е. разделение на отдельные классы и группы), • поиск общих закономерностей формирования катализаторов в рамках определенного класса или группы
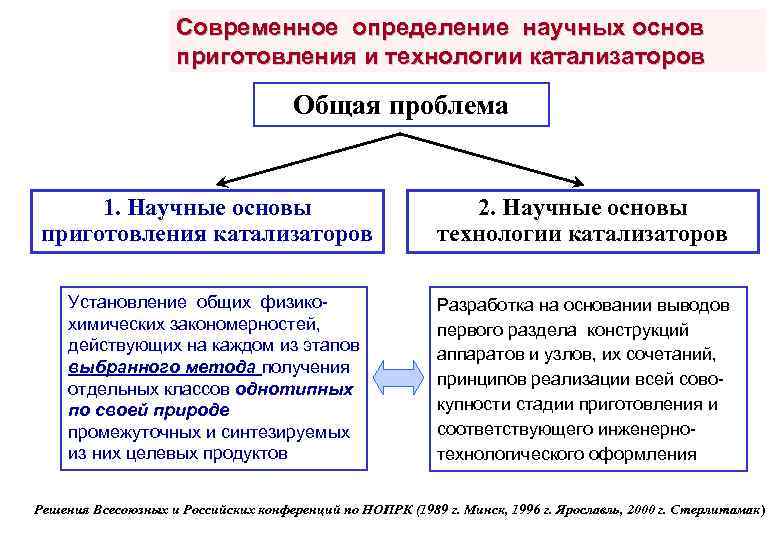 Современное определение научных основ приготовления и технологии катализаторов Общая проблема 1. Научные основы приготовления катализаторов Установление общих физикохимических закономерностей, действующих на каждом из этапов выбранного метода получения отдельных классов однотипных по своей природе промежуточных и синтезируемых из них целевых продуктов 2. Научные основы технологии катализаторов Разработка на основании выводов первого раздела конструкций аппаратов и узлов, их сочетаний, принципов реализации всей совокупности стадии приготовления и соответствующего инженернотехнологического оформления Решения Всесоюзных и Российских конференций по НОПРК (1989 г. Минск, 1996 г. Ярославль, 2000 г. Стерлитамак)
Современное определение научных основ приготовления и технологии катализаторов Общая проблема 1. Научные основы приготовления катализаторов Установление общих физикохимических закономерностей, действующих на каждом из этапов выбранного метода получения отдельных классов однотипных по своей природе промежуточных и синтезируемых из них целевых продуктов 2. Научные основы технологии катализаторов Разработка на основании выводов первого раздела конструкций аппаратов и узлов, их сочетаний, принципов реализации всей совокупности стадии приготовления и соответствующего инженернотехнологического оформления Решения Всесоюзных и Российских конференций по НОПРК (1989 г. Минск, 1996 г. Ярославль, 2000 г. Стерлитамак)
 2. 6. Связь НОПК с другими дисциплинами Научные основы приготовления ката-лизаторов новая, самостоятельная наука, возникшая на стыке ряда физико -химических и дисциплин, задачей которой является комплексное изучение процессов формирования как ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ химического и фазового состава, так и субструктуры, текстуры, морфологии и дисперсных свойств твердых веществ, и определение совокупности подходов к целенаправленному управлению ими
2. 6. Связь НОПК с другими дисциплинами Научные основы приготовления ката-лизаторов новая, самостоятельная наука, возникшая на стыке ряда физико -химических и дисциплин, задачей которой является комплексное изучение процессов формирования как ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ химического и фазового состава, так и субструктуры, текстуры, морфологии и дисперсных свойств твердых веществ, и определение совокупности подходов к целенаправленному управлению ими



