alkogol_lekts.ppt
- Количество слайдов: 35
 Наследственные варианты алкогольдегидрогеназы, альдегидрогеназы, параоксоназы Лекция 6
Наследственные варианты алкогольдегидрогеназы, альдегидрогеназы, параоксоназы Лекция 6
 Этанол • Этанол — жирорастворимая молекула • Всасывается в кровь из 12 -перстной кишки и тонкого кишечника, в меньшей степени из желудка и толстого кишечника. • Высокое содержание пищевых белков, жиров и углеводов тормозит абсорбцию этанола. • Увеличение глюкозы, фруктозы и галактозы в крови снижают его содержание, увеличивая скорость окисления. • Метаболизм происходит в желудке и в большей степени – в печени ( 75– 90 %) • Общее количество выводимого здоровым человеком этанола составляет 100– 300 мг/л/час, что эквивалентно 6– 9 г в час. • При хроническом потреблении этанола скорость его выведения увеличивается за счет индукции микросомальных этанол-окисляющих систем. • Женские половые гормоны, в особенности эстрогены, снижают максимум концентрации этанола на фармакокинетической кривой. • роль генетического компонента в различиях скорости элиминации алкоголя составляет 40 -50%
Этанол • Этанол — жирорастворимая молекула • Всасывается в кровь из 12 -перстной кишки и тонкого кишечника, в меньшей степени из желудка и толстого кишечника. • Высокое содержание пищевых белков, жиров и углеводов тормозит абсорбцию этанола. • Увеличение глюкозы, фруктозы и галактозы в крови снижают его содержание, увеличивая скорость окисления. • Метаболизм происходит в желудке и в большей степени – в печени ( 75– 90 %) • Общее количество выводимого здоровым человеком этанола составляет 100– 300 мг/л/час, что эквивалентно 6– 9 г в час. • При хроническом потреблении этанола скорость его выведения увеличивается за счет индукции микросомальных этанол-окисляющих систем. • Женские половые гормоны, в особенности эстрогены, снижают максимум концентрации этанола на фармакокинетической кривой. • роль генетического компонента в различиях скорости элиминации алкоголя составляет 40 -50%
 Метаболизм этанола • Скорость метаболизма этанола, наряду с рядом других факторов, определяется генетическими вариантами двух ферментов — цитозольной алкогольдегидрогеназы (ADH) и митохондриальной альдегидрогеназы (ALDH 2) • Оба фермента используют NAD+ как кофактор для окисления алкоголя. • Скорость окисления этанола определяется не только количеством фермента в ткани и его функциональными характеристиками, но и концентрацией кофакторов NAD+ и NADН и концентрацией этанола и ацетальдегида в клеточных структурах (цитозоле и митохондриях). • ацетальдегид проявляет выраженные свойства ингибитора реакций с участием алкогольдегидрогеназы. • Элиминация ацетальдегида – определяющий фактор скорости метаболизма этанола.
Метаболизм этанола • Скорость метаболизма этанола, наряду с рядом других факторов, определяется генетическими вариантами двух ферментов — цитозольной алкогольдегидрогеназы (ADH) и митохондриальной альдегидрогеназы (ALDH 2) • Оба фермента используют NAD+ как кофактор для окисления алкоголя. • Скорость окисления этанола определяется не только количеством фермента в ткани и его функциональными характеристиками, но и концентрацией кофакторов NAD+ и NADН и концентрацией этанола и ацетальдегида в клеточных структурах (цитозоле и митохондриях). • ацетальдегид проявляет выраженные свойства ингибитора реакций с участием алкогольдегидрогеназы. • Элиминация ацетальдегида – определяющий фактор скорости метаболизма этанола.
 Алкогольдегидрогеназа (ADH, АДГ) (Е. С. 1. 1) • димерный цитозольный фермент • определяет основной путь метаболизма этанола у млекопитающих • катализирует обратимое окисление многих первичных и вторичных спиртов в альдегиды и кетоны. • Алкоголь + NAD+ ↔ альдегид или кетон + NADH + H+
Алкогольдегидрогеназа (ADH, АДГ) (Е. С. 1. 1) • димерный цитозольный фермент • определяет основной путь метаболизма этанола у млекопитающих • катализирует обратимое окисление многих первичных и вторичных спиртов в альдегиды и кетоны. • Алкоголь + NAD+ ↔ альдегид или кетон + NADH + H+
 АDH • У человека активность АDH снижена в детском возрасте и достигает уровня взрослого к 5 годам • АДГ состоит из 2 -х субъединиц с молекулярным весом 40 000 Дальтон каждая. • Фермент содержит два атома цинка и по одному активному центру на субъединицу. • Атомы цинка существенны для проявления ферментативной активности.
АDH • У человека активность АDH снижена в детском возрасте и достигает уровня взрослого к 5 годам • АДГ состоит из 2 -х субъединиц с молекулярным весом 40 000 Дальтон каждая. • Фермент содержит два атома цинка и по одному активному центру на субъединицу. • Атомы цинка существенны для проявления ферментативной активности.
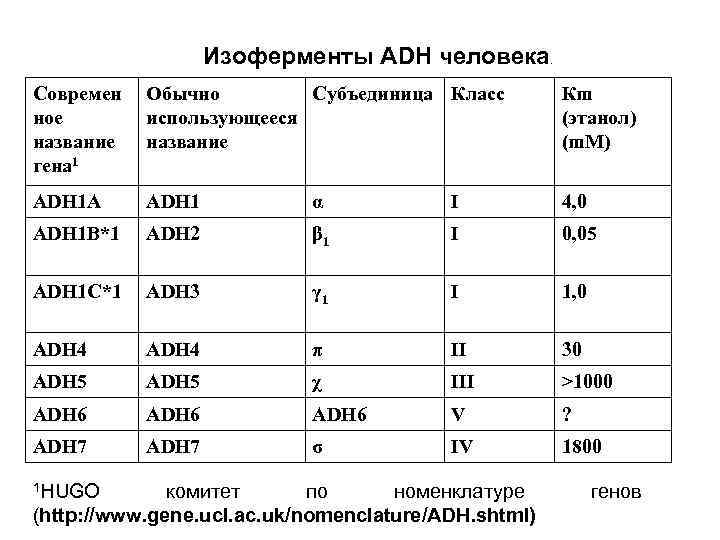 Изоферменты ADH человека. Современ ное название гена 1 Обычно Субъединица Класс использующееся название Кm (этанол) (m. M) ADH 1 A ADH 1 α I 4, 0 ADH 1 B*1 ADH 2 β 1 I 0, 05 ADH 1 C*1 ADH 3 γ 1 I 1, 0 ADH 4 π II 30 ADH 5 χ III >1000 ADH 6 V ? ADH 7 σ IV 1800 1 HUGO комитет по номенклатуре (http: //www. gene. ucl. ac. uk/nomenclature/ADH. shtml) генов
Изоферменты ADH человека. Современ ное название гена 1 Обычно Субъединица Класс использующееся название Кm (этанол) (m. M) ADH 1 A ADH 1 α I 4, 0 ADH 1 B*1 ADH 2 β 1 I 0, 05 ADH 1 C*1 ADH 3 γ 1 I 1, 0 ADH 4 π II 30 ADH 5 χ III >1000 ADH 6 V ? ADH 7 σ IV 1800 1 HUGO комитет по номенклатуре (http: //www. gene. ucl. ac. uk/nomenclature/ADH. shtml) генов
 класс I АDH • наиболее важен для метаболизма этанола. • Изоэнзимы класса формируются за счет димерной ассоциации любых их трех типов полипептидных субъединиц α, β 1 и γ 1, контролируемых 3 -мя отдельными генными локусами ADH 1 A (АDH 1), ADH 1 B*1 (АDH 2), ADH 1 C*1 (АDH 3), соответственно. • имеют более 93% идентичных последовательностей и могут образовывать как гомо-, так и гетеродимеры, тогда как ферменты других классов – только гомодимеры.
класс I АDH • наиболее важен для метаболизма этанола. • Изоэнзимы класса формируются за счет димерной ассоциации любых их трех типов полипептидных субъединиц α, β 1 и γ 1, контролируемых 3 -мя отдельными генными локусами ADH 1 A (АDH 1), ADH 1 B*1 (АDH 2), ADH 1 C*1 (АDH 3), соответственно. • имеют более 93% идентичных последовательностей и могут образовывать как гомо-, так и гетеродимеры, тогда как ферменты других классов – только гомодимеры.
 АDH класса II (АDH 4) • кодируются на локусе АDH 4 • Субстраты - алифатические и содержащие длинные цепи ароматические спирты • участие в метаболизме этанола незначительно • не способны окислять метанол.
АDH класса II (АDH 4) • кодируются на локусе АDH 4 • Субстраты - алифатические и содержащие длинные цепи ароматические спирты • участие в метаболизме этанола незначительно • не способны окислять метанол.
 АDH класса III (АDH 5) • в физиологических условиях в окислении этанола не участвуют • субстратами являются спирты средней длины с числом атомов углерода > 4 • есть данные, что ферменты класса идентичны формальдегидрогеназе.
АDH класса III (АDH 5) • в физиологических условиях в окислении этанола не участвуют • субстратами являются спирты средней длины с числом атомов углерода > 4 • есть данные, что ферменты класса идентичны формальдегидрогеназе.
 ADH класса IV (ADH 7) • имеют высокую Кm для этанола • при обычно достигающихся концентрациях этанола в плазме не происходит их насыщение субстратом • насыщение может быть достигнуто при высокой концентрации этанола в желудке • ADH 7 представлены в желудке • окисляют ретинол в ретиналь. Эта реакция — одно из звеньев образования ретиноевой кислоты. • ADH 7 экспрессируется в соответствующих тканях в период эмбрионального развития и участвует в процессе развития. • Имеется гипотеза, что субстратная конкуренция этанола и ретинола за ADH 7 может приводить к нарушениям развития плода, определяемым как алкогольный синдром плода.
ADH класса IV (ADH 7) • имеют высокую Кm для этанола • при обычно достигающихся концентрациях этанола в плазме не происходит их насыщение субстратом • насыщение может быть достигнуто при высокой концентрации этанола в желудке • ADH 7 представлены в желудке • окисляют ретинол в ретиналь. Эта реакция — одно из звеньев образования ретиноевой кислоты. • ADH 7 экспрессируется в соответствующих тканях в период эмбрионального развития и участвует в процессе развития. • Имеется гипотеза, что субстратная конкуренция этанола и ретинола за ADH 7 может приводить к нарушениям развития плода, определяемым как алкогольный синдром плода.
 Полиморфизм АDH класса I • «Атипичная» форма фермента кодируется локусом АDH 2 • содержит β 2 субъединицу вместо обычной β 1 • Вариант β 2 отличается от β 1 транзицией CGC → CAC, что ведет к замене в 47 позиции аргинина на гистидин • Мутация ведет к повышению скорости окисления этанола • Каталитическая активность димеров - β 2 > β 2 β 1 > β 1. • «Атипичная» форма фермента по-разному представлена в популяциях.
Полиморфизм АDH класса I • «Атипичная» форма фермента кодируется локусом АDH 2 • содержит β 2 субъединицу вместо обычной β 1 • Вариант β 2 отличается от β 1 транзицией CGC → CAC, что ведет к замене в 47 позиции аргинина на гистидин • Мутация ведет к повышению скорости окисления этанола • Каталитическая активность димеров - β 2 > β 2 β 1 > β 1. • «Атипичная» форма фермента по-разному представлена в популяциях.
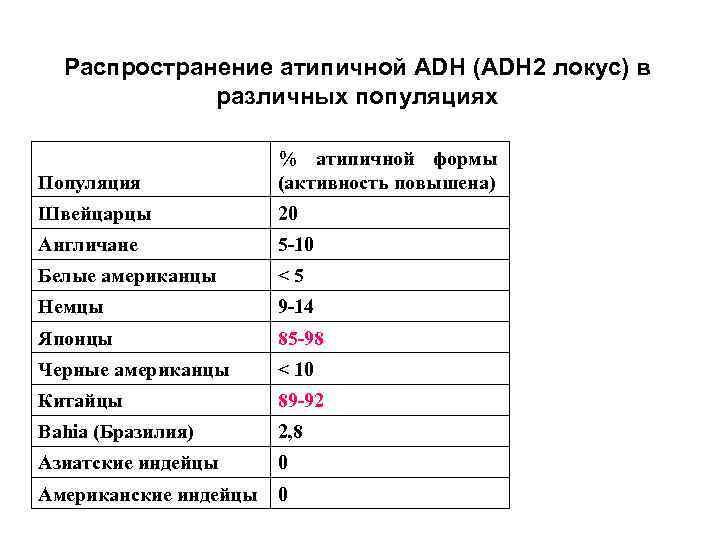 Распространение атипичной АDH (АDH 2 локус) в различных популяциях Популяция % атипичной формы (активность повышена) Швейцарцы 20 Англичане 5 -10 Белые американцы <5 Немцы 9 -14 Японцы 85 -98 Черные американцы < 10 Китайцы 89 -92 Bahia (Бразилия) 2, 8 Азиатские индейцы 0 Американские индейцы 0
Распространение атипичной АDH (АDH 2 локус) в различных популяциях Популяция % атипичной формы (активность повышена) Швейцарцы 20 Англичане 5 -10 Белые американцы <5 Немцы 9 -14 Японцы 85 -98 Черные американцы < 10 Китайцы 89 -92 Bahia (Бразилия) 2, 8 Азиатские индейцы 0 Американские индейцы 0
 Значение полиформизма алкогольдегидрогеназ • Определяется широкой субстратной специфичностью. • Субстраты - первичные и вторичные алифатические спирты, диоли, циклические и ароматические спирты, омега-гидрокси жирные кислоты, диеновые кислоты и их альдегиды. • При нейтральных р. Н АDH катализируют необратимое восстановление альдегидов со скоростью в 40 раз большей, чем окисление спиртов • Имеет значение для регуляции важных для зрения взаимопревращений ретинола в ретиналь, в метаболизме стероидов, желчных кислот, коротких спиртов, определяющих запах пищи. • Медицинское значение имеет метаболизм метанола, этиленгликоля, 1, 2 пропандиола. • Окисление АDH полиэтиленгликоля в ди- и гидроксикислотные метаболиты может приводить к ацидозу и почечной недостаточности.
Значение полиформизма алкогольдегидрогеназ • Определяется широкой субстратной специфичностью. • Субстраты - первичные и вторичные алифатические спирты, диоли, циклические и ароматические спирты, омега-гидрокси жирные кислоты, диеновые кислоты и их альдегиды. • При нейтральных р. Н АDH катализируют необратимое восстановление альдегидов со скоростью в 40 раз большей, чем окисление спиртов • Имеет значение для регуляции важных для зрения взаимопревращений ретинола в ретиналь, в метаболизме стероидов, желчных кислот, коротких спиртов, определяющих запах пищи. • Медицинское значение имеет метаболизм метанола, этиленгликоля, 1, 2 пропандиола. • Окисление АDH полиэтиленгликоля в ди- и гидроксикислотные метаболиты может приводить к ацидозу и почечной недостаточности.
 Значение полиформизма алкогольдегидрогеназ • АDH печени человека участвуют в метаболизме сердечных гликозидов - дигоксин, дигитоксин, превращая их в кетопроизводные. • при конкуренции с этанолом окисление сердечных гликозидов снижается, обусловливая их токсический эффект. • полиморфизм АDH определяет индивидуальную скорость окисления этанола. У потребляющих спиртные напитки людей поражения печени и другие расстройства чаще возникают при высоких уровнях активности АDH. • Ацетальдегид, обусловливающий токсическое действие этанола, интенсивнее накапливается у восточных этнических групп, что совпадает с географией распространения атипичного фермента АDH 2.
Значение полиформизма алкогольдегидрогеназ • АDH печени человека участвуют в метаболизме сердечных гликозидов - дигоксин, дигитоксин, превращая их в кетопроизводные. • при конкуренции с этанолом окисление сердечных гликозидов снижается, обусловливая их токсический эффект. • полиморфизм АDH определяет индивидуальную скорость окисления этанола. У потребляющих спиртные напитки людей поражения печени и другие расстройства чаще возникают при высоких уровнях активности АDH. • Ацетальдегид, обусловливающий токсическое действие этанола, интенсивнее накапливается у восточных этнических групп, что совпадает с географией распространения атипичного фермента АDH 2.
 Альдегидрогеназа (ALDH E. C. 1. 2. 1. 3). • Ферментативное удаление альдегидов у человека опосредуется системой неспецифических ферментов, таких как альдегидоксидаза, ксантиноксидаза и альдегидрогеназа. • в печени основной объем окисления альдегидов катализируется NAD-зависимой альдегидрогеназой • Ацетальдегид – первый продукт окисления этанола в печени человека, значительно более токсичен, чем этанол, и обусловливает его многие как фармакологические, так и токсические эффекты.
Альдегидрогеназа (ALDH E. C. 1. 2. 1. 3). • Ферментативное удаление альдегидов у человека опосредуется системой неспецифических ферментов, таких как альдегидоксидаза, ксантиноксидаза и альдегидрогеназа. • в печени основной объем окисления альдегидов катализируется NAD-зависимой альдегидрогеназой • Ацетальдегид – первый продукт окисления этанола в печени человека, значительно более токсичен, чем этанол, и обусловливает его многие как фармакологические, так и токсические эффекты.
 Дегидрирование альдегидов в карбоксильные кислоты ALDH RCHO + NAD+ + (P) + ½ O 2 RCOO - + NAD (P)H Реакции, катализируемые АЛДГ необратимы
Дегидрирование альдегидов в карбоксильные кислоты ALDH RCHO + NAD+ + (P) + ½ O 2 RCOO - + NAD (P)H Реакции, катализируемые АЛДГ необратимы
 ALDH • делится на 7 классов • более характерны для человека ALDH классов I и II. • Класс I - высокая Km для ацетальдегида, локализован в цитозоле. • Класс II с низкой Km, локализован преимущественно в митохондриях. • Изоэнзимы ALDH 1 (ALDH 1 А 1) и ALDH 2 являются гомотетрамерами, состоящими из субъединиц с молекулярным весом около 54000 дальтон • эритроциты человека содержат ALDH, идентичную цитозольной в печени.
ALDH • делится на 7 классов • более характерны для человека ALDH классов I и II. • Класс I - высокая Km для ацетальдегида, локализован в цитозоле. • Класс II с низкой Km, локализован преимущественно в митохондриях. • Изоэнзимы ALDH 1 (ALDH 1 А 1) и ALDH 2 являются гомотетрамерами, состоящими из субъединиц с молекулярным весом около 54000 дальтон • эритроциты человека содержат ALDH, идентичную цитозольной в печени.
 ALDH • Гены ALDH 1 и ALDH 2 расположены в различных хромосомах: 9 q 21 и 12 q 24. 2, соответственно. • Выяснение последовательности ДНК выявило 66 % идентичности кодирующих их участков • ген ALDH 2 состоит из 44 килобаз, содержит как минимум 13 экзонов, кодирующих полипептид из 517 аминокислот • Ген атипичной ALDH 2 имеет единичную транзицию G→A в экзоне 12, что ведет к замене в 487 положении Glu на Lys • Эта мутация локализована близко к С-концевому участку, определяющему структуру активного центра, ведет к снижению ферментативной активности.
ALDH • Гены ALDH 1 и ALDH 2 расположены в различных хромосомах: 9 q 21 и 12 q 24. 2, соответственно. • Выяснение последовательности ДНК выявило 66 % идентичности кодирующих их участков • ген ALDH 2 состоит из 44 килобаз, содержит как минимум 13 экзонов, кодирующих полипептид из 517 аминокислот • Ген атипичной ALDH 2 имеет единичную транзицию G→A в экзоне 12, что ведет к замене в 487 положении Glu на Lys • Эта мутация локализована близко к С-концевому участку, определяющему структуру активного центра, ведет к снижению ферментативной активности.
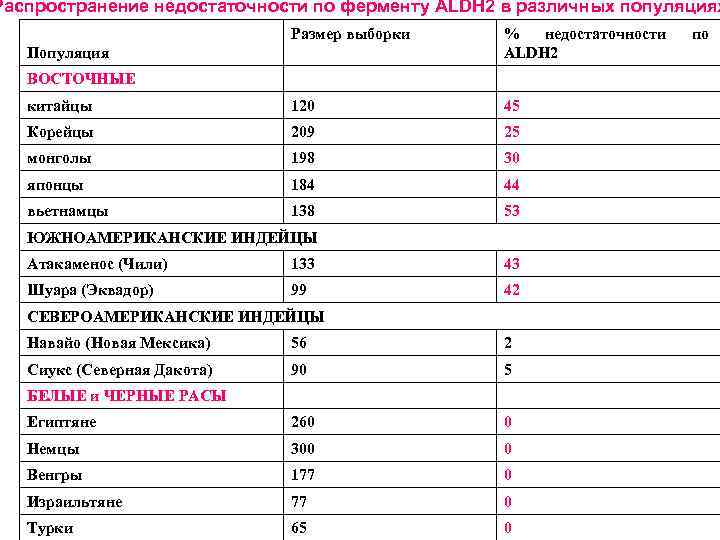 Распространение недостаточности по ферменту АLDH 2 в различных популяциях Размер выборки % недостаточности ALDH 2 китайцы 120 45 Корейцы 209 25 монголы 198 30 японцы 184 44 вьетнамцы 138 53 Популяция ВОСТОЧНЫЕ ЮЖНОАМЕРИКАНСКИЕ ИНДЕЙЦЫ Атакаменос (Чили) 133 43 Шуара (Эквадор) 99 42 СЕВЕРОАМЕРИКАНСКИЕ ИНДЕЙЦЫ Навайо (Новая Мексика) 56 2 Сиукс (Северная Дакота) 90 5 Египтяне 260 0 Немцы 300 0 Венгры 177 0 Израильтяне 77 0 Турки 65 0 БЕЛЫЕ и ЧЕРНЫЕ РАСЫ по
Распространение недостаточности по ферменту АLDH 2 в различных популяциях Размер выборки % недостаточности ALDH 2 китайцы 120 45 Корейцы 209 25 монголы 198 30 японцы 184 44 вьетнамцы 138 53 Популяция ВОСТОЧНЫЕ ЮЖНОАМЕРИКАНСКИЕ ИНДЕЙЦЫ Атакаменос (Чили) 133 43 Шуара (Эквадор) 99 42 СЕВЕРОАМЕРИКАНСКИЕ ИНДЕЙЦЫ Навайо (Новая Мексика) 56 2 Сиукс (Северная Дакота) 90 5 Египтяне 260 0 Немцы 300 0 Венгры 177 0 Израильтяне 77 0 Турки 65 0 БЕЛЫЕ и ЧЕРНЫЕ РАСЫ по
 Значение полиморфизма ALDH 2 • биогенные амины, превращаясь в альдегиды через свои моноамино- и диаминооксидазные системы, образуют субстраты для ALDH. • Альдегиды образуются при перекисном окислении липидов • Ряд фармакологических средств также образует альдегиды в процессе биотрансформации. • нагрузка этанолом, приводящая к увеличению концентраций ацетальдегида, вызывает субстратную конкуренцию, обусловливая токсическое действие других нераспавшихся альдегидов • Повышение уровня ацетальдегида ингибирует реакции, катализируемые алкогольдегидрогеназой, таким образом замедляется элиминация алкоголя.
Значение полиморфизма ALDH 2 • биогенные амины, превращаясь в альдегиды через свои моноамино- и диаминооксидазные системы, образуют субстраты для ALDH. • Альдегиды образуются при перекисном окислении липидов • Ряд фармакологических средств также образует альдегиды в процессе биотрансформации. • нагрузка этанолом, приводящая к увеличению концентраций ацетальдегида, вызывает субстратную конкуренцию, обусловливая токсическое действие других нераспавшихся альдегидов • Повышение уровня ацетальдегида ингибирует реакции, катализируемые алкогольдегидрогеназой, таким образом замедляется элиминация алкоголя.
 Ацетальдегид • накапливается в печени и в крови • ковалентно связывается с различными белками, вызывает нарушение их функций, включая активность многих ферментов • Связываясь с белками, образует эпитопы – вещества с антигенной активностью. • Возникающие к ним антитела еще в большей степени усиливают нарушения в печени • Высокая активность альдегидрогеназ в роговице и хрусталике отражает значение детоксикации альдегидов для зрительной функции • Наличие мутантного гена, обусловливающего недостаточность ALDH 2, вызывает усугубление всех этих формирующих патологию процессов, особенно при избытке ацетальдегида
Ацетальдегид • накапливается в печени и в крови • ковалентно связывается с различными белками, вызывает нарушение их функций, включая активность многих ферментов • Связываясь с белками, образует эпитопы – вещества с антигенной активностью. • Возникающие к ним антитела еще в большей степени усиливают нарушения в печени • Высокая активность альдегидрогеназ в роговице и хрусталике отражает значение детоксикации альдегидов для зрительной функции • Наличие мутантного гена, обусловливающего недостаточность ALDH 2, вызывает усугубление всех этих формирующих патологию процессов, особенно при избытке ацетальдегида
 Ацетальдегид • Одним из эффектов алкоголя является сосудорасширяющее действие, опосредуемое центральной нервной системой. • симпатомиметический эффект этанола у человека обусловлен преимущественно ацетальдегидом • Ацетальдегид реагирует с хромаффинными клетками, способствуя выбросу катехоламинов • Реагирует с тучными клетками, выделяющими кинины и гистамин • У некоторых людей вызывает развитие flush (вспышка) - синдрома
Ацетальдегид • Одним из эффектов алкоголя является сосудорасширяющее действие, опосредуемое центральной нервной системой. • симпатомиметический эффект этанола у человека обусловлен преимущественно ацетальдегидом • Ацетальдегид реагирует с хромаффинными клетками, способствуя выбросу катехоламинов • Реагирует с тучными клетками, выделяющими кинины и гистамин • У некоторых людей вызывает развитие flush (вспышка) - синдрома
 flush–синдром • проявляется в покраснении лица, тахикардии, аритмии, ощущении жара в желудке, мышечной слабости и др. • Еще в 1962 г в ранних исследованиях Kalow, применив метод фотоплетизмографии для регистрации flush-синдрома, показал, что в популяции японцев выделяются подгруппы высоко-, умеренно- и низкорезистентных к этанолу лиц. • Wolf в 1972 г показал, что подобный ответ на алкоголь в белой популяции встречается в 5%, в то время как у монголоидов и американских индейцев в 80%.
flush–синдром • проявляется в покраснении лица, тахикардии, аритмии, ощущении жара в желудке, мышечной слабости и др. • Еще в 1962 г в ранних исследованиях Kalow, применив метод фотоплетизмографии для регистрации flush-синдрома, показал, что в популяции японцев выделяются подгруппы высоко-, умеренно- и низкорезистентных к этанолу лиц. • Wolf в 1972 г показал, что подобный ответ на алкоголь в белой популяции встречается в 5%, в то время как у монголоидов и американских индейцев в 80%.
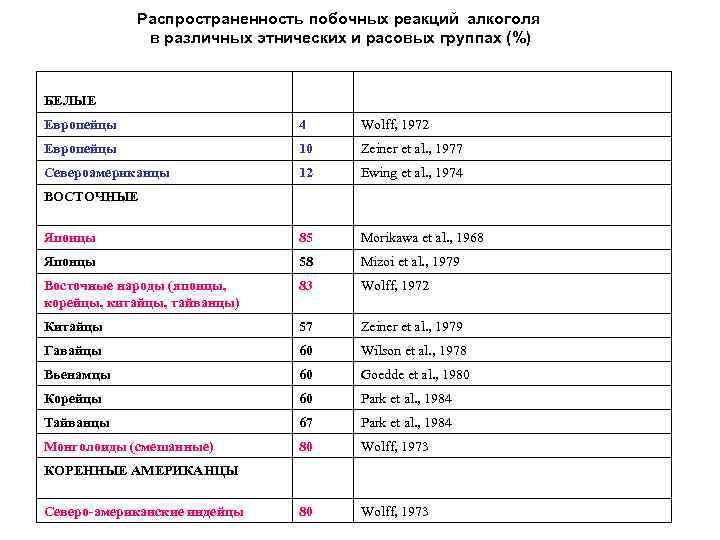 Распространенность побочных реакций алкоголя в различных этнических и расовых группах (%) БЕЛЫЕ Европейцы 4 Wolff, 1972 Европейцы 10 Zeiner et al. , 1977 Североамериканцы 12 Ewing et al. , 1974 Японцы 85 Morikawa et al. , 1968 Японцы 58 Mizoi et al. , 1979 Восточные народы (японцы, корейцы, китайцы, тайванцы) 83 Wolff, 1972 Китайцы 57 Zeiner et al. , 1979 Гавайцы 60 Wilson et al. , 1978 Вьенамцы 60 Goedde et al. , 1980 Корейцы 60 Park et al. , 1984 Тайванцы 67 Park et al. , 1984 Монголоиды (смешанные) 80 Wolff, 1973 ВОСТОЧНЫЕ КОРЕННЫЕ АМЕРИКАНЦЫ Северо-американские индейцы
Распространенность побочных реакций алкоголя в различных этнических и расовых группах (%) БЕЛЫЕ Европейцы 4 Wolff, 1972 Европейцы 10 Zeiner et al. , 1977 Североамериканцы 12 Ewing et al. , 1974 Японцы 85 Morikawa et al. , 1968 Японцы 58 Mizoi et al. , 1979 Восточные народы (японцы, корейцы, китайцы, тайванцы) 83 Wolff, 1972 Китайцы 57 Zeiner et al. , 1979 Гавайцы 60 Wilson et al. , 1978 Вьенамцы 60 Goedde et al. , 1980 Корейцы 60 Park et al. , 1984 Тайванцы 67 Park et al. , 1984 Монголоиды (смешанные) 80 Wolff, 1973 ВОСТОЧНЫЕ КОРЕННЫЕ АМЕРИКАНЦЫ Северо-американские индейцы
 Распространенность недостаточности изофермента ALDH 2 и потребление алкоголя у здоровых людей в Японии Район Размер выборки ALDH 2 дефицит Потребление алкоголя л/год на человека Sendai 47 25, 5% 6, 25 Gifu 65 52, 3% 3, 82 1989 г Agarval и Gooll
Распространенность недостаточности изофермента ALDH 2 и потребление алкоголя у здоровых людей в Японии Район Размер выборки ALDH 2 дефицит Потребление алкоголя л/год на человека Sendai 47 25, 5% 6, 25 Gifu 65 52, 3% 3, 82 1989 г Agarval и Gooll
 ALDH*2/*2 • заболеваемость ассоциированным с этанолом раком с локализацией в ЖКТ значительно увеличена у представителей азиатских групп, имеющих гомозиготный фенотип ALDH*2/*2, соответствующий низкой активности фермента. • выше риск алкогольного поражения печени
ALDH*2/*2 • заболеваемость ассоциированным с этанолом раком с локализацией в ЖКТ значительно увеличена у представителей азиатских групп, имеющих гомозиготный фенотип ALDH*2/*2, соответствующий низкой активности фермента. • выше риск алкогольного поражения печени
 ALDH*2/*2 • наличие мутантной формы ALDH*2/*2, некоторым образом «защищает» от злоупотребления алкоголем. • Но лица, имеющие сниженную активность ALDH и при этом злоупотребляющие алкоголем, более подвержены развитию алкогольного поражения печени и злокачественных опухолей ЖКТ
ALDH*2/*2 • наличие мутантной формы ALDH*2/*2, некоторым образом «защищает» от злоупотребления алкоголем. • Но лица, имеющие сниженную активность ALDH и при этом злоупотребляющие алкоголем, более подвержены развитию алкогольного поражения печени и злокачественных опухолей ЖКТ
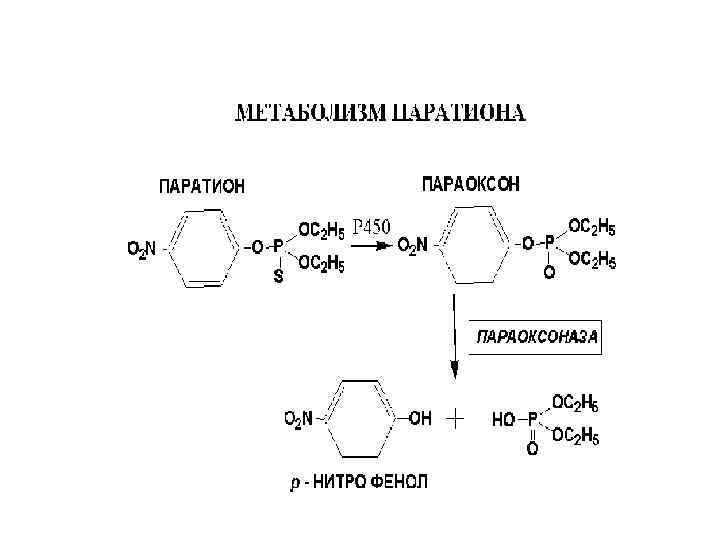
 Параоксоназы / арилэстеразы (Е. С. 3. 1. 8. 1) • арилэстераза, которая гидроксилирует • параоксон в р-нитрофенол • Паратион (тиофос) используется как инсектицид более 50 лет. В результате его микросомального окисления в печени человека и других млекопитающих образуется параоксон, мощный антихолинэстеразный агент.
Параоксоназы / арилэстеразы (Е. С. 3. 1. 8. 1) • арилэстераза, которая гидроксилирует • параоксон в р-нитрофенол • Паратион (тиофос) используется как инсектицид более 50 лет. В результате его микросомального окисления в печени человека и других млекопитающих образуется параоксон, мощный антихолинэстеразный агент.
 Фармакогенетика параоксоназы • Бимодальное распределение по активности параоксоназы человека было впервые установлено Krish в 1968 г • Генетический контроль высокой и низкой активности параоксоназы изучен группой Playfer в 1976 г. • установлено простое менделевское наследование, детерминируемое двумя аллелями одного локуса. Низкая активность наследуется рецессивно. • В белых популяциях обнаружено бимодальное распределение. • В монголоидной и негроидной популяциях выявлено унимодальное распределение.
Фармакогенетика параоксоназы • Бимодальное распределение по активности параоксоназы человека было впервые установлено Krish в 1968 г • Генетический контроль высокой и низкой активности параоксоназы изучен группой Playfer в 1976 г. • установлено простое менделевское наследование, детерминируемое двумя аллелями одного локуса. Низкая активность наследуется рецессивно. • В белых популяциях обнаружено бимодальное распределение. • В монголоидной и негроидной популяциях выявлено унимодальное распределение.
 Фармакогенетика параоксоназы • В кодирующих регионах параоксоназы сыворотки человека высокой (А) и низкой (В) активности выявлено два полиморфных участка Leu/Met в кодоне 54 и Arg/Gln в кодоне 191. • Leu/Met полиморфизм не коррелировал с фенотипом активности • по Arg/Gln в 191 позиции обнаружено четкое соответствие активности • А фенотип имеет в 191 положении глицин, а В – аргинин. • Семейный анализ подтвердил, что гетерозиготы Arg/Gln ассоциируются с АВ фенотипом.
Фармакогенетика параоксоназы • В кодирующих регионах параоксоназы сыворотки человека высокой (А) и низкой (В) активности выявлено два полиморфных участка Leu/Met в кодоне 54 и Arg/Gln в кодоне 191. • Leu/Met полиморфизм не коррелировал с фенотипом активности • по Arg/Gln в 191 позиции обнаружено четкое соответствие активности • А фенотип имеет в 191 положении глицин, а В – аргинин. • Семейный анализ подтвердил, что гетерозиготы Arg/Gln ассоциируются с АВ фенотипом.
 Методы фенотипирования • высокоактивная параоксоназа стимулируется 1 M Nа. Cl в 2 -3 раза сильнее, чем низкоактивная (Eckerson, 1983) • 0, 1 м. М хлорпромазин подавляет низкоактивный фермент в большей степени, чем высокоактивную форму • Определение р-нитрофенола в плазме после инкубации с параоксоном (Playfer et al. , 1976) р-нитрофенол в щелочной среде дает желтое окрашивание
Методы фенотипирования • высокоактивная параоксоназа стимулируется 1 M Nа. Cl в 2 -3 раза сильнее, чем низкоактивная (Eckerson, 1983) • 0, 1 м. М хлорпромазин подавляет низкоактивный фермент в большей степени, чем высокоактивную форму • Определение р-нитрофенола в плазме после инкубации с параоксоном (Playfer et al. , 1976) р-нитрофенол в щелочной среде дает желтое окрашивание
 Значение полиморфизма параоксоназы • Картирование гена параоксоназы показало его локализацию в 7 q 21– 22 вблизи гена кистозного фиброза. Поиски связи этого заболевания с активностью фермента положительных результатов пока не дали. • Другой аспект изучения параоксоназы возник в связи с обнаружением ее активности в составе липопротеинов высокой плотности. Однако до настоящего времени значение этого феномена, возможно только физико-химического, не ясно. • Не выяснено, какой конкретный эндогенный субстрат параоксоназа метаболизирует. • Тем не менее, типирование по параоксоназе уже сейчас может представлять интерес для профессионального отбора
Значение полиморфизма параоксоназы • Картирование гена параоксоназы показало его локализацию в 7 q 21– 22 вблизи гена кистозного фиброза. Поиски связи этого заболевания с активностью фермента положительных результатов пока не дали. • Другой аспект изучения параоксоназы возник в связи с обнаружением ее активности в составе липопротеинов высокой плотности. Однако до настоящего времени значение этого феномена, возможно только физико-химического, не ясно. • Не выяснено, какой конкретный эндогенный субстрат параоксоназа метаболизирует. • Тем не менее, типирование по параоксоназе уже сейчас может представлять интерес для профессионального отбора
 Некоторые вещества, являющиеся субстратами сывороточной параоксоназы/арилэстеразы человека Вещество Органофосфаты параоксон метил параоксон DFP хлорпирифос оксон дихлорвос хлортрион оксон пиримфос-метил оксон зарин зоман табун
Некоторые вещества, являющиеся субстратами сывороточной параоксоназы/арилэстеразы человека Вещество Органофосфаты параоксон метил параоксон DFP хлорпирифос оксон дихлорвос хлортрион оксон пиримфос-метил оксон зарин зоман табун
 органофосфонаты ЕРN –оксон (О-этил-О-4 -нитробензин) фосфонат Армин (этил-р-нитрофенил-этилфосфонат карбаматы Севин (3 -изопропил) фенил-N-метилкарбамат N-диметилкарбамилфлуорид Эфиры карбоксильной кислоты фенилацетат тиофенилацетат 2 -нафтилацетат 2 -нитрофенилацетат 4 -нитрофенилацетат дельта-циклогексенилацетат дельта-циклопентинилацетат 3 -пиридилацетат Изопропенилацетат винилацетат
органофосфонаты ЕРN –оксон (О-этил-О-4 -нитробензин) фосфонат Армин (этил-р-нитрофенил-этилфосфонат карбаматы Севин (3 -изопропил) фенил-N-метилкарбамат N-диметилкарбамилфлуорид Эфиры карбоксильной кислоты фенилацетат тиофенилацетат 2 -нафтилацетат 2 -нитрофенилацетат 4 -нитрофенилацетат дельта-циклогексенилацетат дельта-циклопентинилацетат 3 -пиридилацетат Изопропенилацетат винилацетат


