Направления инвагинации мембраны Формы мембранных структур, встречающиеся в

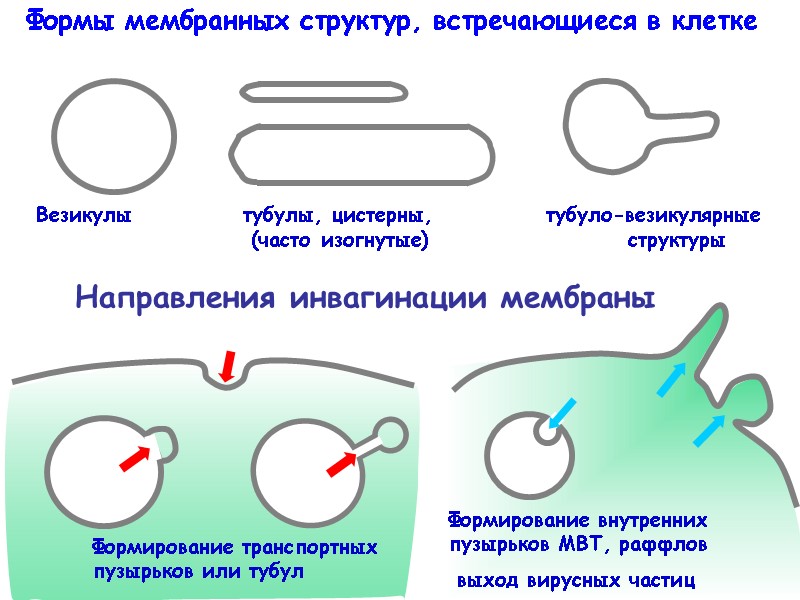
Направления инвагинации мембраны Формы мембранных структур, встречающиеся в клетке
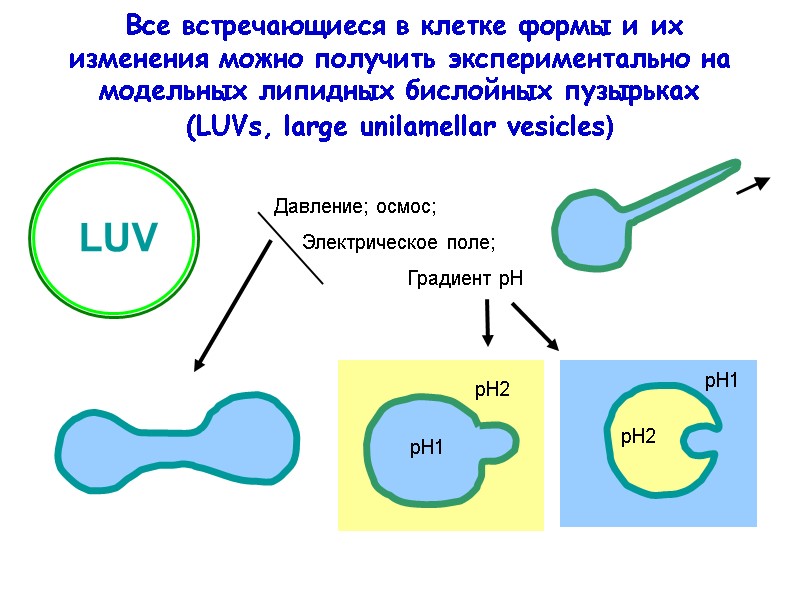
Все встречающиеся в клетке формы и их изменения можно получить экспериментально на модельных липидных бислойных пузырьках (LUVs, large unilamellar vesicles) Давление; осмос; Электрическое поле; Градиент рН

изменения формы мембраны определяются их физико-химическими свойствами Формирование транспортных везикул может происходить и без участия белков

COPI и COPII –окаймления “клатриновые” окаймления: АР1, АР2, АР3, АР4 GGA1, GGA2, GGA3 ??? Окаймления (coats)
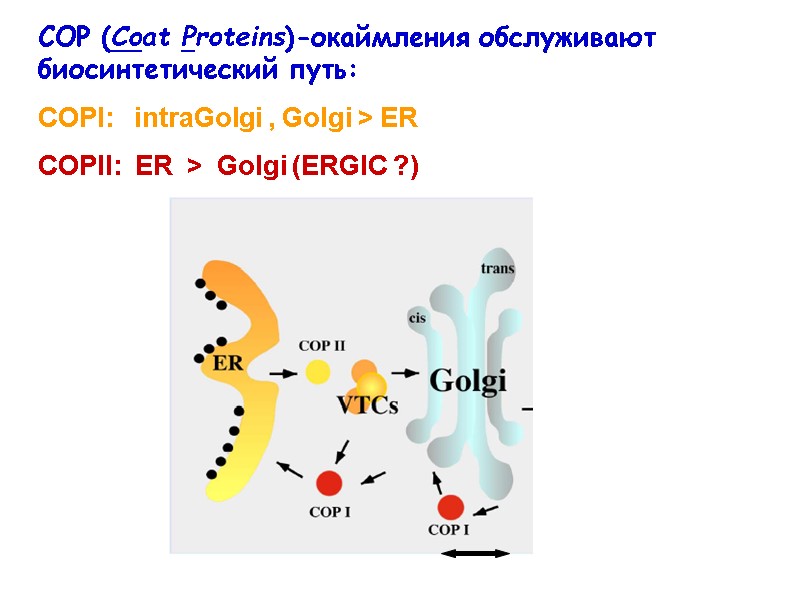
COP (Coat Proteins)-окаймления обслуживают биосинтетический путь: COPI: intraGolgi , Golgi > ER COPII: ER > Golgi (ERGIC ?)
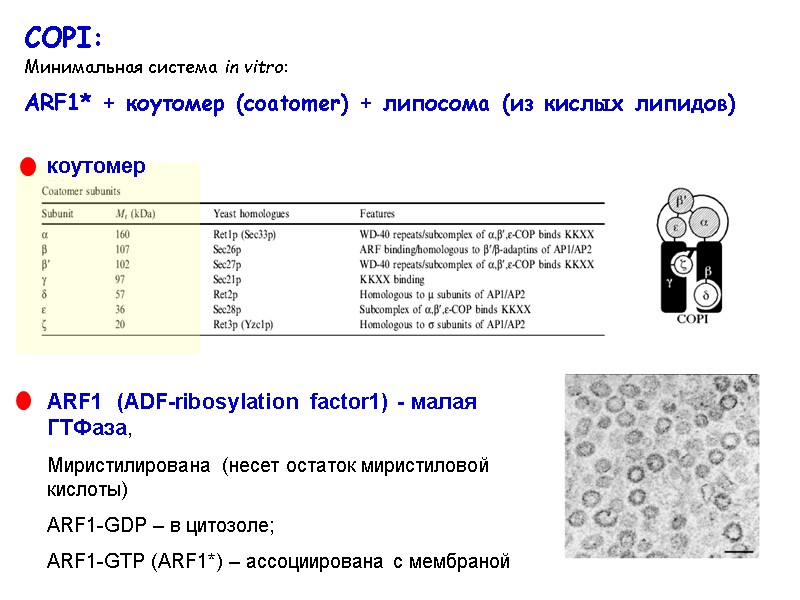
COPI: Минимальная система in vitro: ARF1* + коутомер (coatomer) + липосома (из кислых липидов)
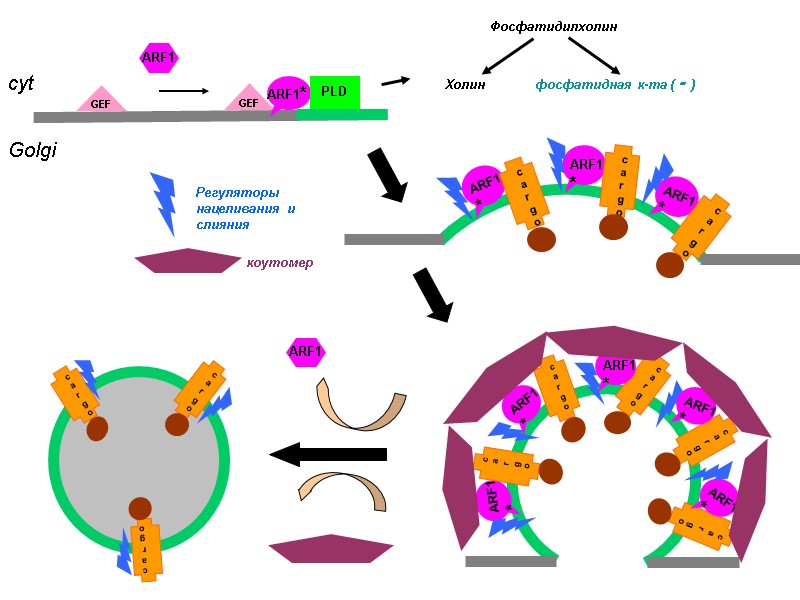
cyt Golgi

Грузы селектируются за счет взаимодействия со своими мембранными рецепторами, узнающими определенные последовательности в молекулах грузов (напр., KDEL, KKXX etc.) На роль мембранных рецепторов претендуют белки семейства р24:

В жизненном цикле COPI-везикулы присутствуют 2 GAP-активности Медленная – циклы гидролиза ГТФ на ARF1 под ее действием необходимы для накопления груза; Она создает временное окно, в течение которого пузырек заполняется грузом Быстрая - после полной сборки окаймления следует быстрый гидролиз ГТФ на ARF1, отделение пузырька и разборка окаймления; коутомер не является ARFGAP, тем не менее его ассоциация с везикулой значительно ускоряет гидролиз ГТФ.

COPI на эндосомах: 1. Нет - и -субъединиц 2. -COP посттрансляционно модифицирован (фосфорилирован?) 3. COPI на эндосомах мало по сравнению с мембранами АГ 4. Дефекты по -COP препятствуют образованию мультивезикулярных тел 5. Ассоциация с мембраной зависит от Rab-белков , а не ARF1 ARF6-GTP - локализован на ПМ ARF6-GDP – локализован на рециклирующих эндосомах ARF 6 взаимодействует с Rac1 и участвует в реорганизации кортикального актинового цитоскелета COPI на других органеллах
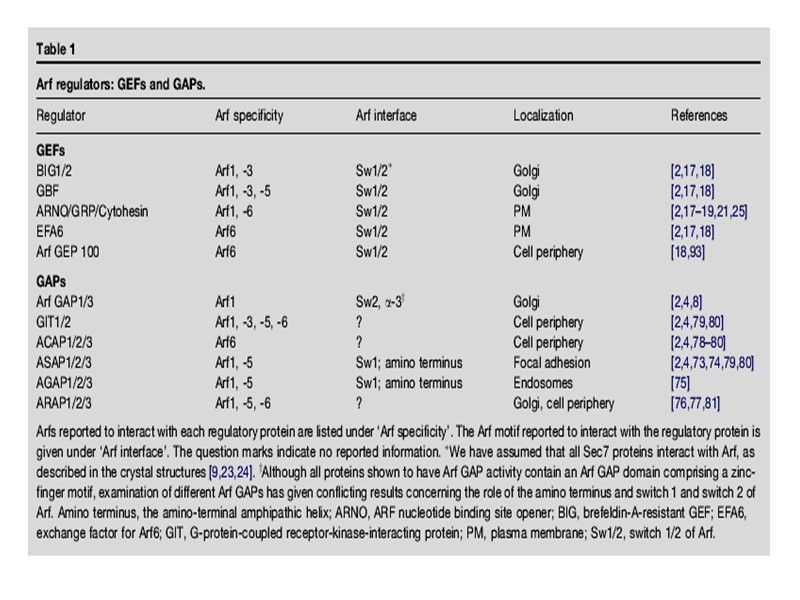
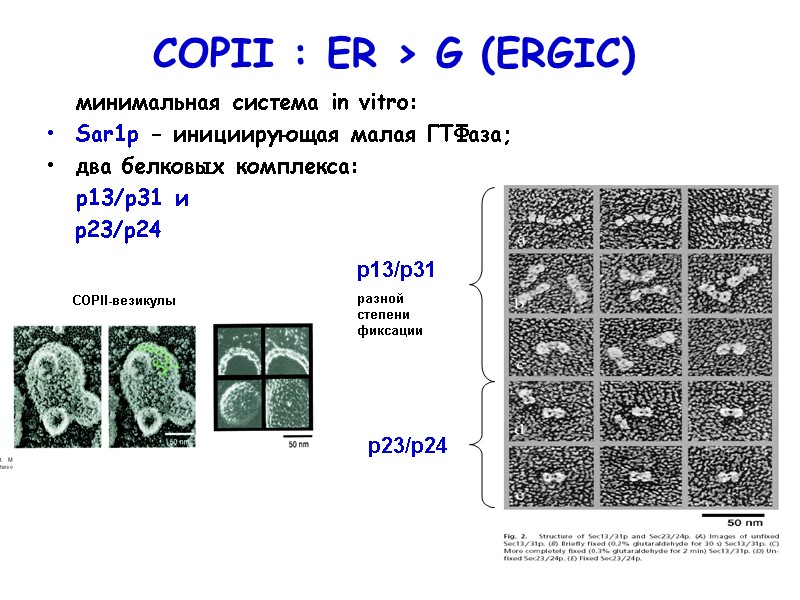
COPII : ER > G (ERGIC) минимальная система in vitro: Sar1p - инициирующая малая ГТФаза; два белковых комплекса: р13/р31 и р23/р24 СOPII-везикулы
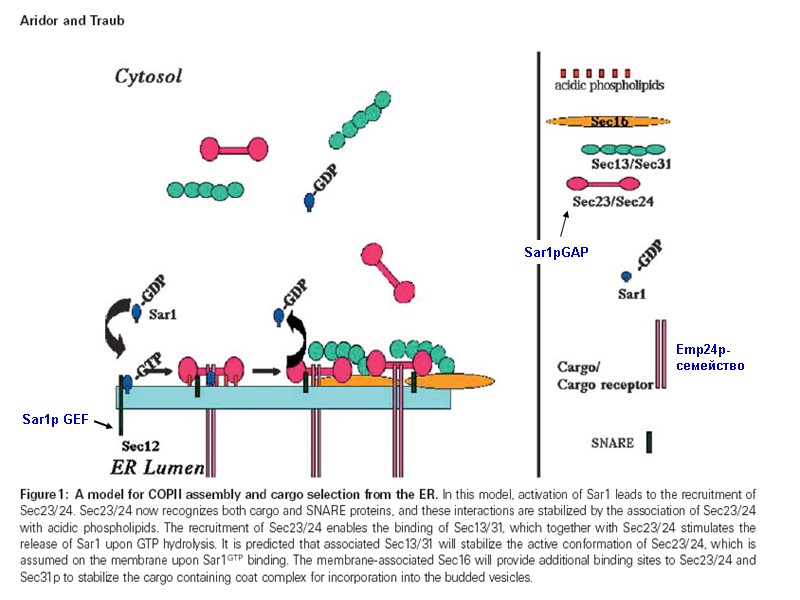
Sar1pGAP Sar1p GEF Emp24p-семейство
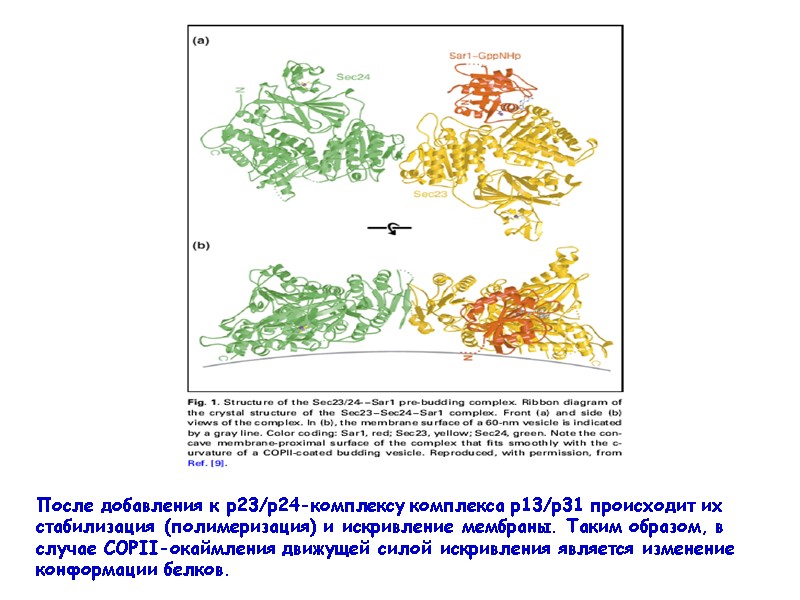
После добавления к р23/р24-комплексу комплекса р13/р31 происходит их стабилизация (полимеризация) и искривление мембраны. Таким образом, в случае COPII-окаймления движущей силой искривления является изменение конформации белков.
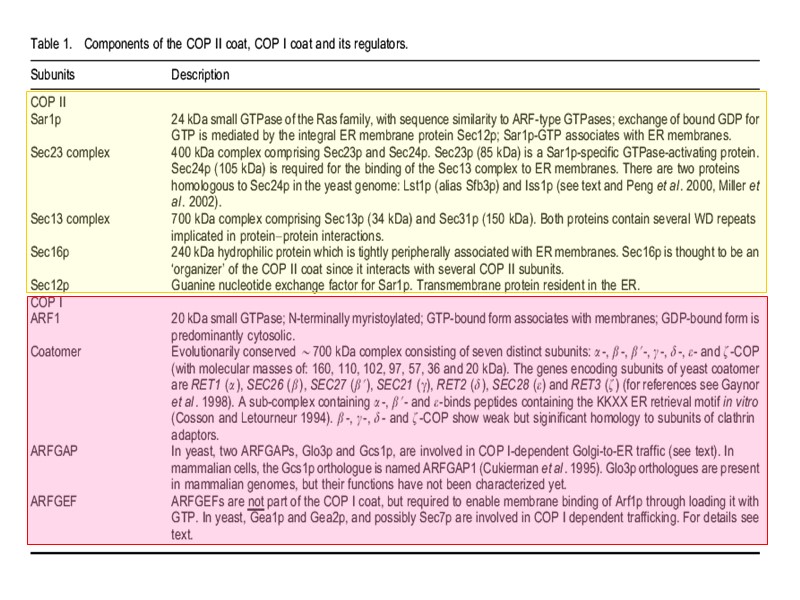
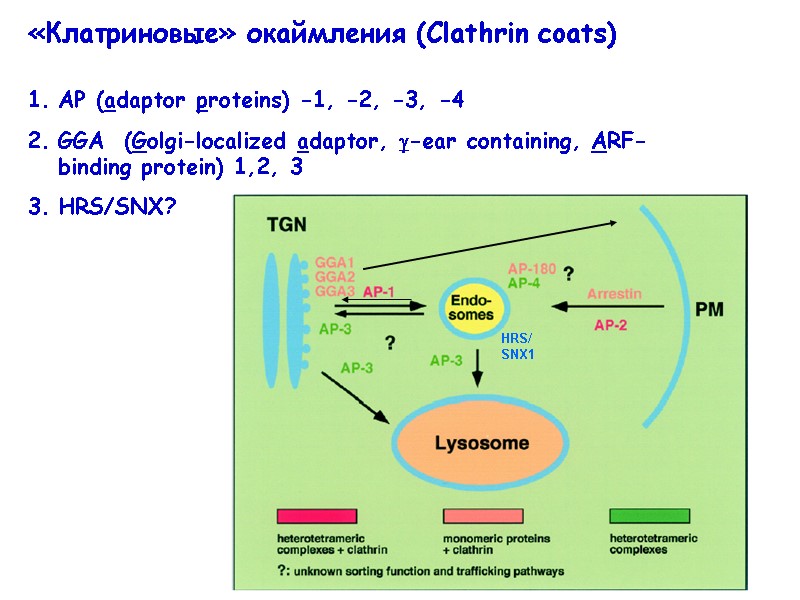
«Клатриновые» окаймления (Clathrin coats) АР (adaptor proteins) -1, -2, -3, -4 GGA (Golgi-localized adaptor, -ear containing, ARF- binding protein) 1,2, 3 HRS/SNX?
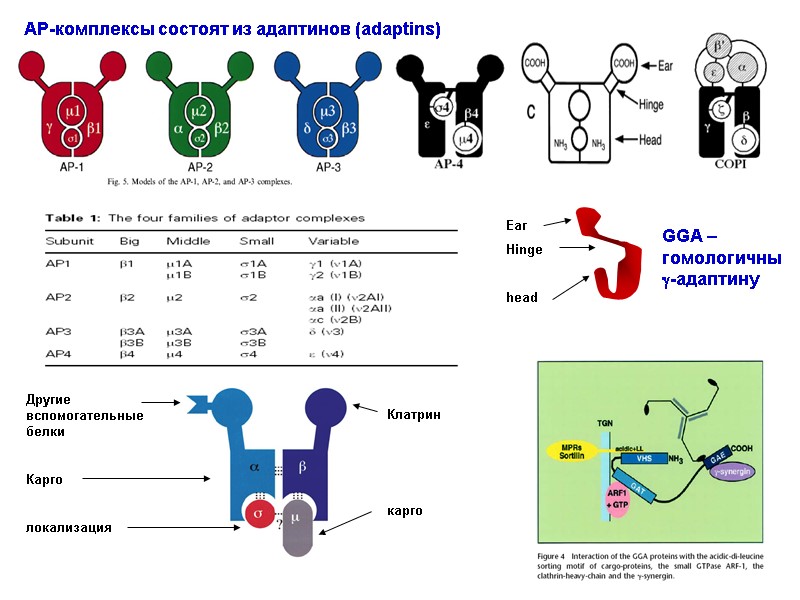
Клатриновые окаймления AP-комплексы состоят из адаптинов (adaptins)
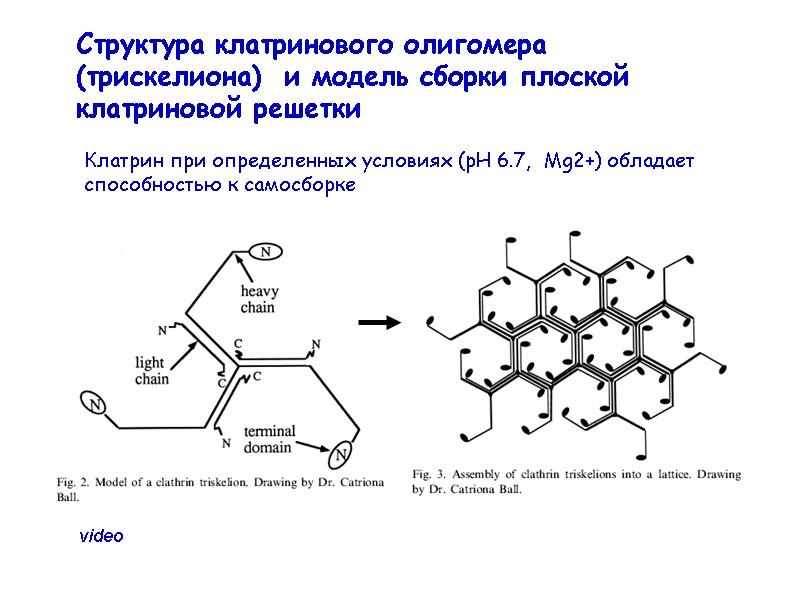
Структура клатринового олигомера (трискелиона) и модель сборки плоской клатриновой решетки video Клатрин при определенных условиях (рН 6.7, Mg2+) обладает способностью к самосборке
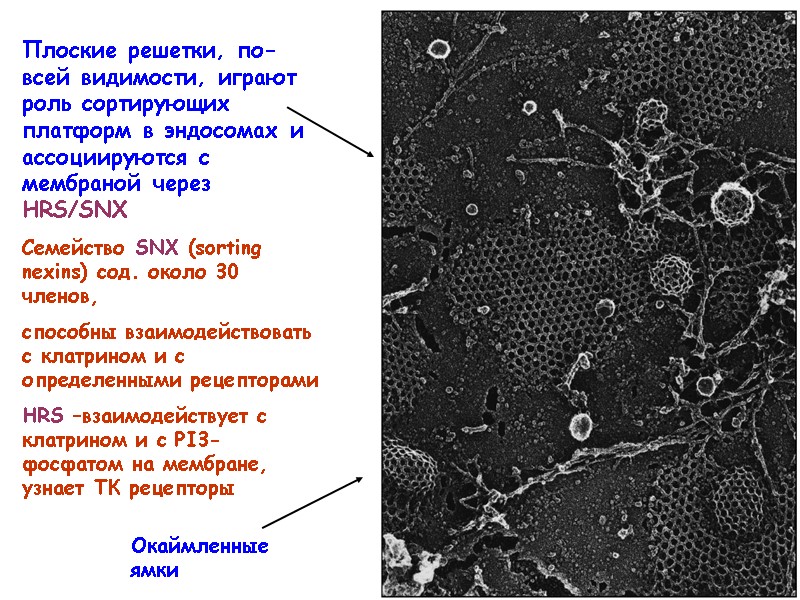
Плоские решетки, по-всей видимости, играют роль сортирующих платформ в эндосомах и ассоциируются с мембраной через HRS/SNX Cемейство SNX (sorting nexins) сод. около 30 членов, способны взаимодействовать с клатрином и с определенными рецепторами HRS –взаимодействует с клатрином и с PI3-фосфатом на мембране, узнает ТК рецепторы Окаймленные ямки
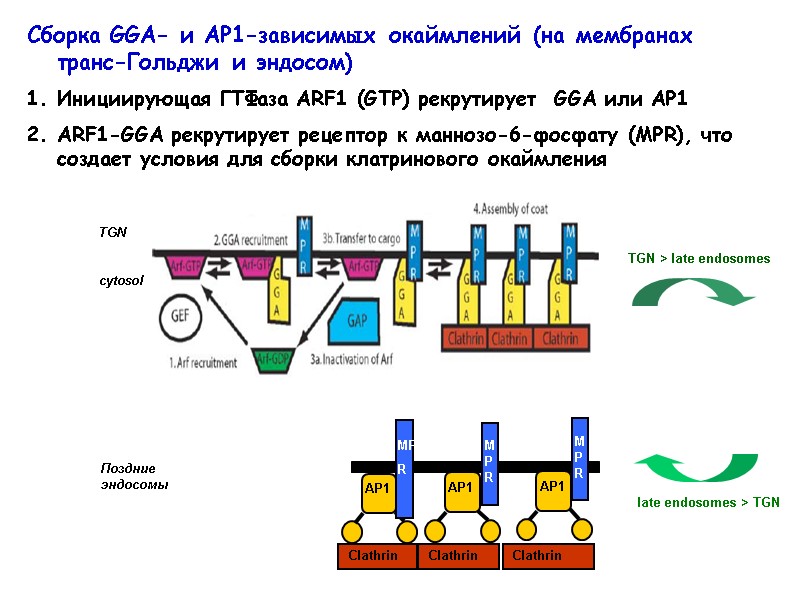
TGN cytosol Сборка GGA- и AP1-зависимых окаймлений (на мембранах транс-Гольджи и эндосом) Инициирующая ГТФаза ARF1 (GTP) рекрутирует GGA или АР1 ARF1-GGA рекрутирует рецептор к маннозо-6-фосфату (MPR), что создает условия для сборки клатринового окаймления
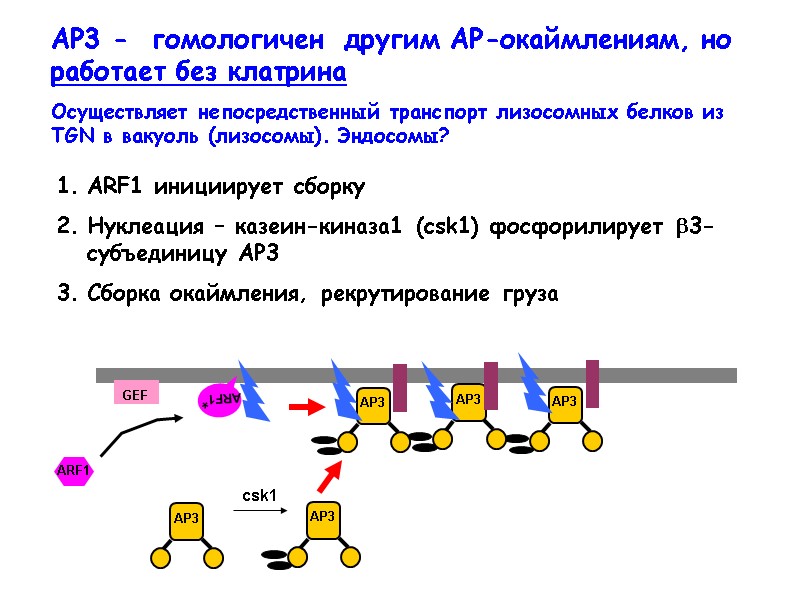
AP3 - гомологичен другим АР-окаймлениям, но работает без клатрина Осуществляет непосредственный транспорт лизосомных белков из TGN в вакуоль (лизосомы). Эндосомы? ARF1 инициирует сборку Нуклеация – казеин-киназа1 (csk1) фосфорилирует 3-субъединицу АР3 Сборка окаймления, рекрутирование груза


Как инициируется сборка АР-2 окаймления? Сборку инициируют рецепторы-грузы Но: в одни и те же ямки могут попадать рецепторы различной природы (метаболические и сигнальные) 2. Сборка идет конститутивно Фибробласты : 2-3 тыс ОЯ/мин Оказалось, что на мембране существуют области, «разрешенные» для формирования окаймленных ямок, именно в пределах такой области и может инициироваться сборка новых окаймлений Большую роль в стабилизации «зон эндоцитоза» играет актиновый цитоскелет На роль инициаторов претендуют PI(4,5) P2 и синаптотагмин
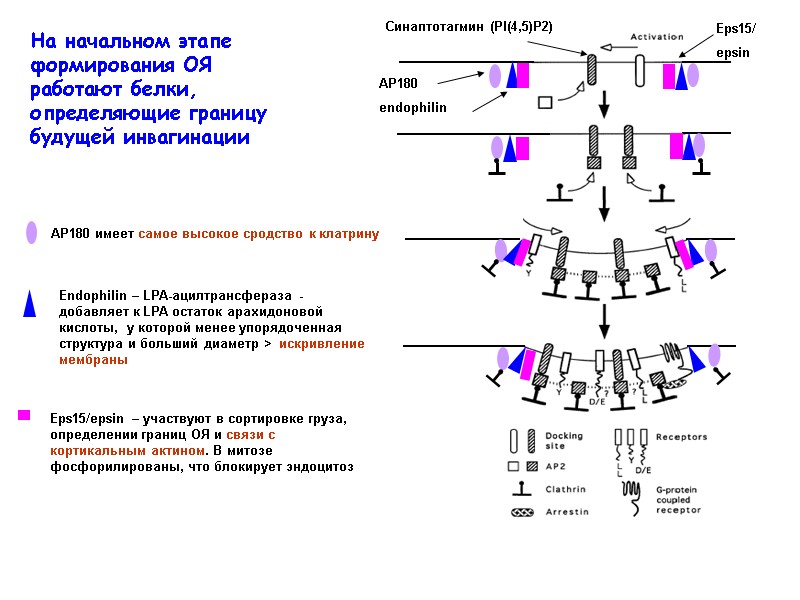
AP180 имеет самое высокое сродство к клатрину Endophilin – LPA-ацилтрансфераза - добавляет к LPA остаток арахидоновой кислоты, у которой менее упорядоченная структура и больший диаметр > искривление мембраны Eps15/epsin – участвуют в сортировке груза, определении границ ОЯ и связи с кортикальным актином. В митозе фосфорилированы, что блокирует эндоцитоз На начальном этапе формирования ОЯ работают белки, определяющие границу будущей инвагинации
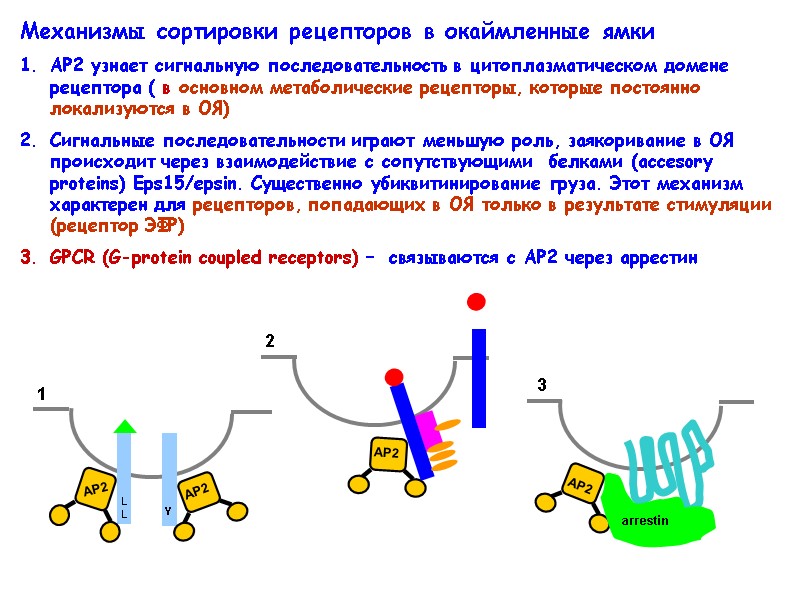
Механизмы сортировки рецепторов в окаймленные ямки АР2 узнает сигнальную последовательность в цитоплазматическом домене рецептора ( в основном метаболические рецепторы, которые постоянно локализуются в ОЯ) Сигнальные последовательности играют меньшую роль, заякоривание в ОЯ происходит через взаимодействие с сопутствующими белками (accesory proteins) Eps15/epsin. Существенно убиквитинирование груза. Этот механизм характерен для рецепторов, попадающих в ОЯ только в результате стимуляции (рецептор ЭФР) GPCR (G-protein coupled receptors) – связываются с АР2 через аррестин LL Y 1 2
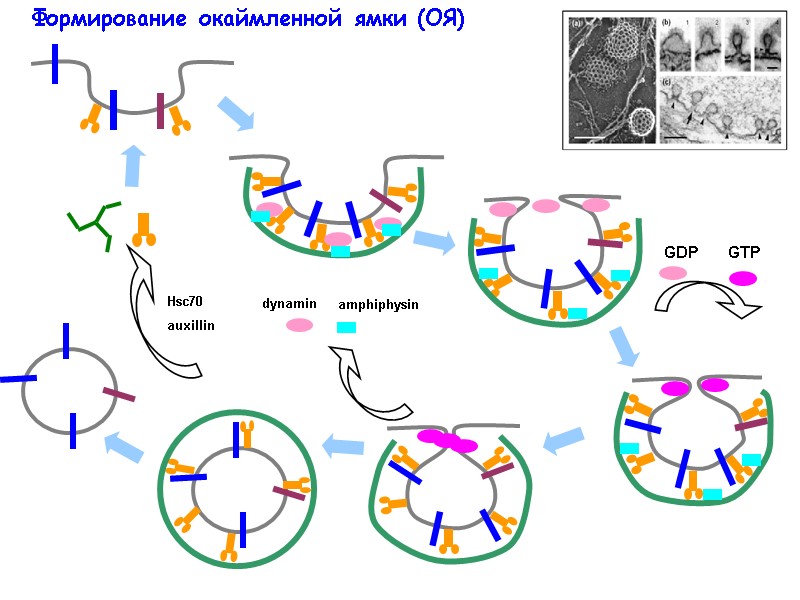
Формирование окаймленной ямки (ОЯ)
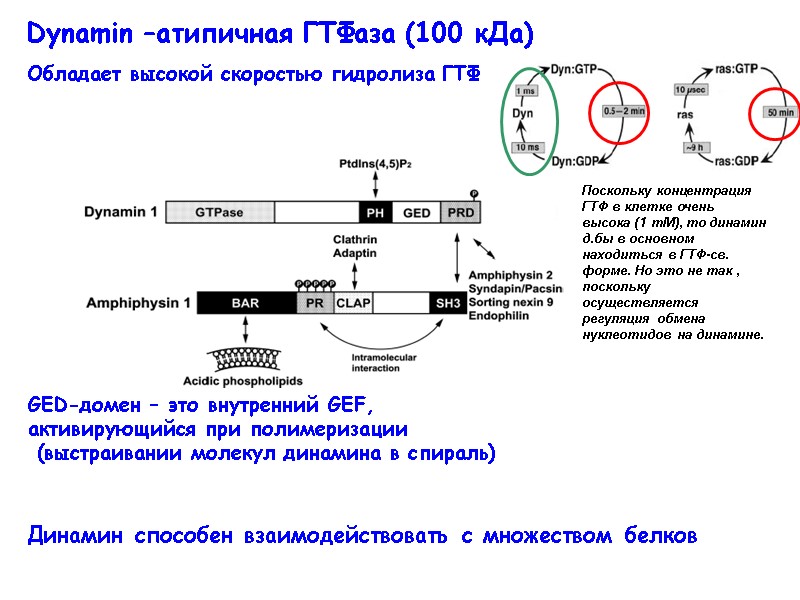
Dynamin –атипичная ГТФаза (100 кДа) Обладает высокой скоростью гидролиза ГТФ Динамин способен взаимодействовать с множеством белков Поскольку концентрация ГТФ в клетке очень высока (1 mM), то динамин д.бы в основном находиться в ГТФ-св. форме. Но это не так , поскольку осуществляется регуляция обмена нуклеотидов на динамине.
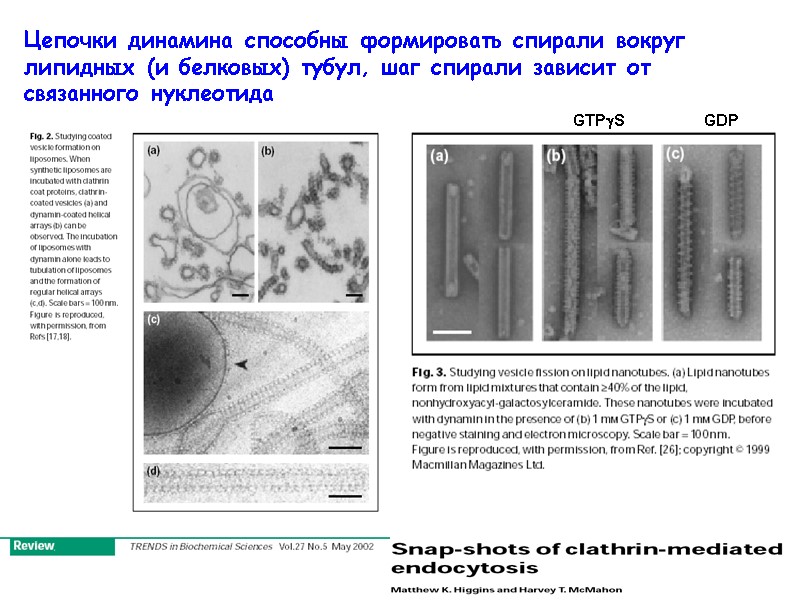
Цепочки динамина способны формировать спирали вокруг липидных (и белковых) тубул, шаг спирали зависит от связанного нуклеотида GTPS GDP
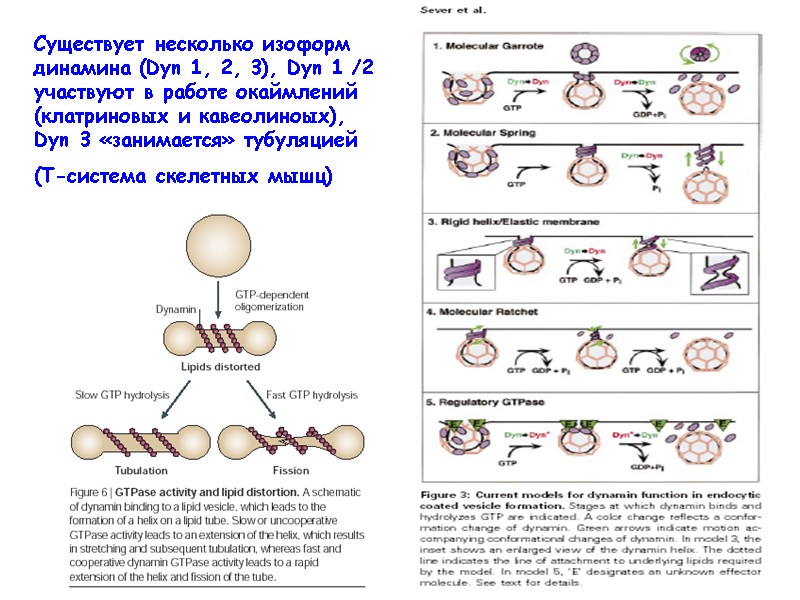
Существует несколько изоформ динамина (Dyn 1, 2, 3), Dyn 1 /2 участвуют в работе окаймлений (клатриновых и кавеолиноых), Dyn 3 «занимается» тубуляцией (Т-система скелетных мышц)
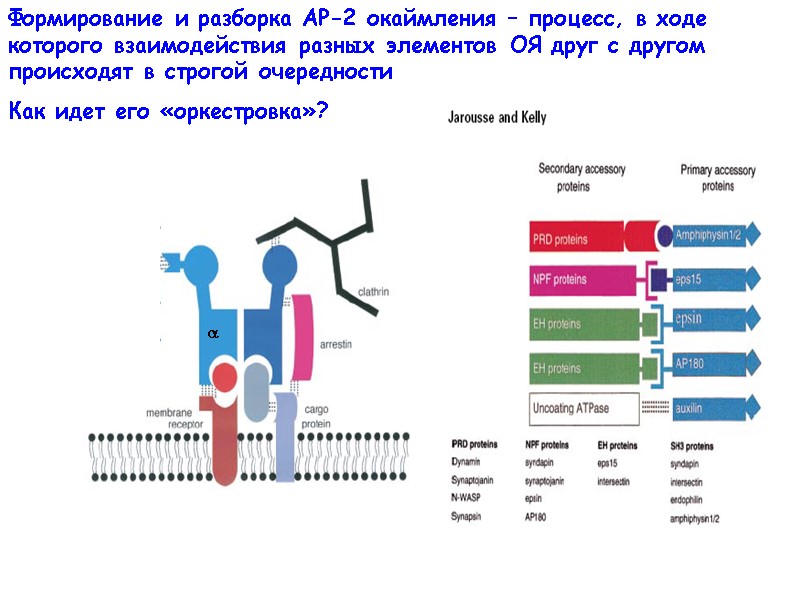
Формирование и разборка АР-2 окаймления – процесс, в ходе которого взаимодействия разных элементов ОЯ друг с другом происходят в строгой очередности Как идет его «оркестровка»?
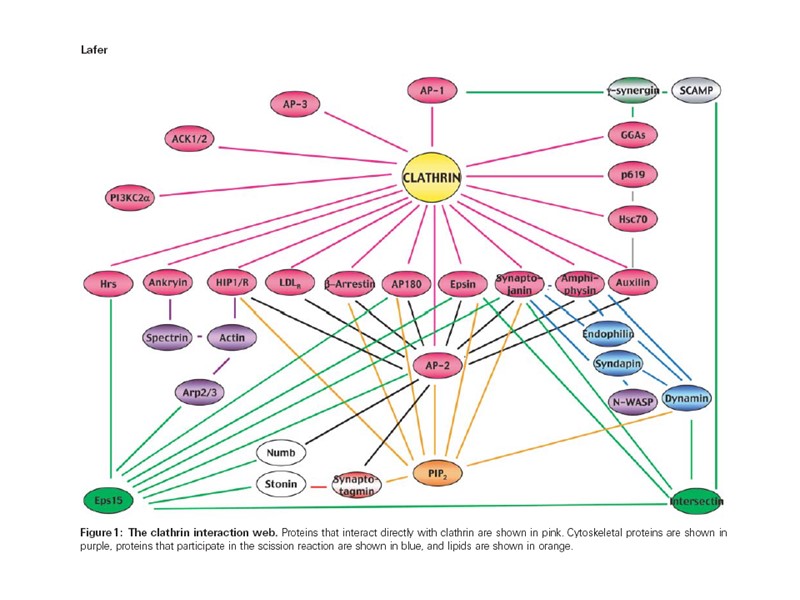
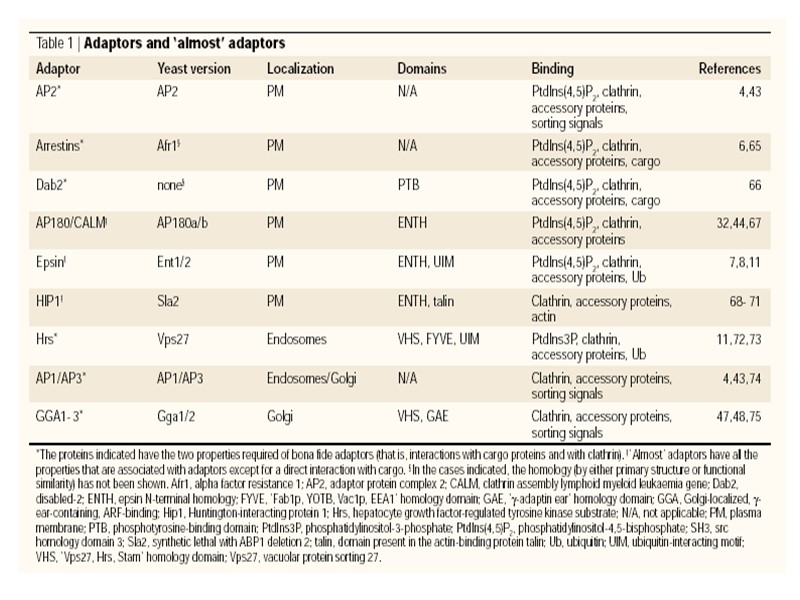

По-видимому, большинство белков в клетках выполняют более чем одну функцию (уже известную нам), другая (или другие) может оказаться весьма неожиданной
39186-vezikulyarnyy_transport_lecture3-coats.ppt
- Количество слайдов: 33

