Направление химических реакций Лекция 14 по курсу «Общая


Направление химических реакций Лекция 14 по курсу «Общая химия»
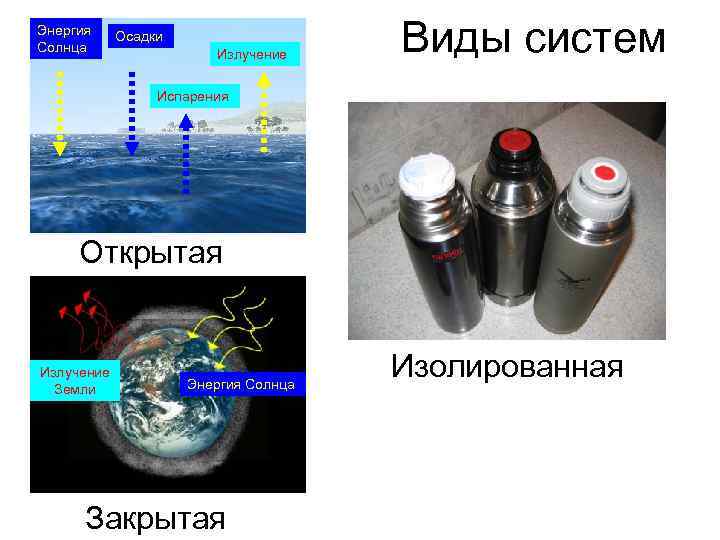
Энергия Солнца Осадки Излучение Виды систем Испарения Открытая Излучение Энергия Солнца Изолированная Земли Закрытая
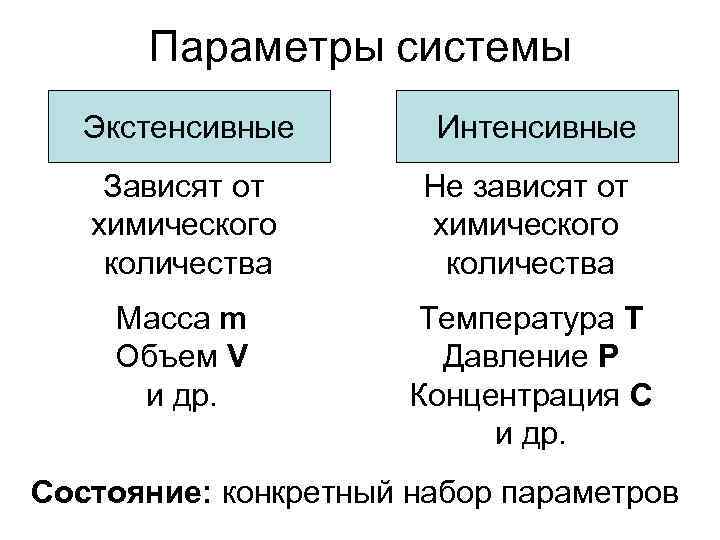
Параметры системы Экстенсивные Интенсивные Зависят от Не зависят от химического количества Масса m Температура T Объем V Давление P и др. Концентрация C и др. Состояние: конкретный набор параметров

Функции состояния Величины, зависящие от параметров (V, T, P, C…), но не от пути достижения состояния Для каждого состояния – только одно значение функции! Примеры функций состояния: Энтальпия H, константы равновесия KC и KP Обычно рассматривают процессы при двух неизменных параметрах P = const, T = const: изобарно-изотермический V = const, T = const: изохорно-изотермический

Внутренняя энергия U Сумма кинетической и потенциальной энергии частиц, составляющих систему U = Eк + Eп (но не энергия самой системы по отношению к внешней среде!) Пример: сжатая пружина. U состоит из: 1) Энергии теплового движения частиц (Eк) 2) Энергии взаимодействия частиц (Eп)

Первый закон термодинамики Для квазистатических (равновесных) процессов Количество теплоты, полученное системой, идёт на изменение её внутренней энергии и совершение работы против внешних сил. Q = U + W или U = Q – W Закон сохранения энергии! Энтальпия: H = U + PV, или H = U + P V В химии чаще применяется H, в физике U

Направление химических реакций: первые гипотезы M. Бертло Ю. Томсен Принцип Бертло-Томсена: самопроизвольно протекают экзотермические реакции Всегда ли верен?

Примеры самопроизвольных неэкзотермических процессов Расширение газа, H = 0 Растворение KNO 3, H > 0 Вывод: есть какой-то дополнительный фактор!

Энтропия S. Второй закон термодинамики Первоначальное определение: S = Q/T Мера неупорядоченности в системе Л. Больцман Второй закон термодинамики: Энтропия изолированной системы не может уменьшаться ( S 0)

Термодинамическая вероятность S = k. Bln Термодинамическая Постоянная вероятность Больцмана Количество микросостояний, 1. 38· 10− 23 Дж/К которыми может быть реали- зовано данное макросостояние Макросостояние – состояние всей системы Микросостояние – каждой отдельной частицы Одному и тому же макросостоянию соответствует много микросостояний!
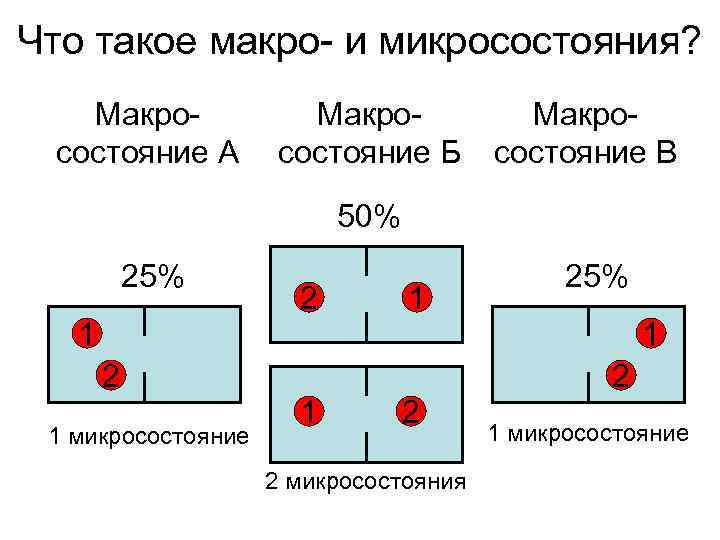
Что такое макро- и микросостояния? Макро- состояние А состояние Б состояние В 50% 25% 2 1 1 2 1 2 1 микросостояние 2 микросостояния

Третий закон термодинамики Энтропия идеальных кристаллов при абсолютном нуле равна 0 Нет движения нет выбора микросостояний В. Нернст

Свободная энергия Гиббса G = H – TS G = H – T S G < 0 – процесс самопроизволен G > 0 – процесс несамопроизволен (а обратный – самопроизволен) G = 0 – состояние равновесия По справочным данным рассчитывают стандартное G: для T = 298 K, P = 105 Па, Сm = 1 моль/кг В «нестандартных» условиях G другое!

Самопроизвольность реакций H и S сильно зависят от Т, но H и S – слабо! 1. H < 0, S > 0 G < 0 при любой T. Процесс всегда самопроизволен 2. H < 0, S < 0 G < 0 при T < H/ S Процесс самопроизволен при низких Т 3. H > 0, S > 0 G < 0 при T > H/ S Процесс самопроизволен при высоких Т 4. H > 0, S < 0 G > 0 при любой T. Процесс всегда несамопроизволен

Предсказание направления реакции CO 2(г) + H 2(г) = CO(г) + H 2 O(ж) f. H 0298, -393. 51 0 -110. 52 -285. 83 к. Дж/моль S 0298 213. 68 130. 52 197. 54 70. 08 Дж/моль·К H 0298 = -110. 52 + (-285. 83) – (-393. 51) = -2, 84 (к. Дж/моль) S 0298 = 70. 08 + 197. 54 – 213. 68 – 130. 52 = -76, 58 (Дж/моль·К) G 0298 = -2, 84 – 298·(-76, 58/1000) = 19. 98 (к. Дж/моль) При стандартных условиях несамопроизволен прямой процесс, самопроизволен обратный

Предсказание температурного интервала самопроизвольности G = H – T S Для самопроизвольной G < 0 Для несамопроизвольной G > 0 Если G = 0, то H = T S При H < 0, S < 0 реакция самопроизвольна ниже этой температуры При H > 0, S > 0 – наоборот
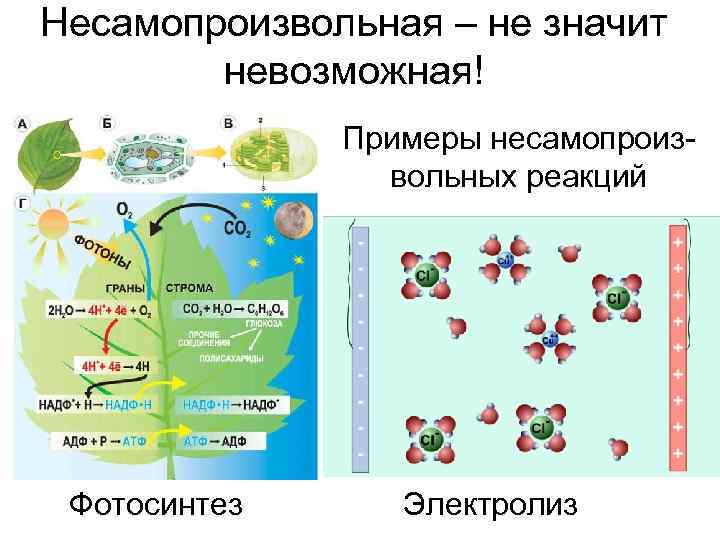
Несамопроизвольная – не значит невозможная! Примеры несамопроиз- вольных реакций Фотосинтез Электролиз
14_Направление химических реакций.ppt
- Количество слайдов: 17

