Строение вещества 6 л 2016.ppt
- Количество слайдов: 30
 Наночастицы на основе углерода Аллотропные модификации – различные структурные формы одного элемента. Углерод – один из самых распространённых элементов – не перестаёт удивлять появлением всё новых и новых форм. Широко распространенными модификациями углерода являются графит и алмаз, известен также карбин. Их разнообразие обусловлено способностью углеродного атома принимать тетраэдрическую sp 3 - (алмаз), тригональную sp 2 – (графит, фуллерен, нанотрубки) или линейную sp- (карбин) гибридизации.
Наночастицы на основе углерода Аллотропные модификации – различные структурные формы одного элемента. Углерод – один из самых распространённых элементов – не перестаёт удивлять появлением всё новых и новых форм. Широко распространенными модификациями углерода являются графит и алмаз, известен также карбин. Их разнообразие обусловлено способностью углеродного атома принимать тетраэдрическую sp 3 - (алмаз), тригональную sp 2 – (графит, фуллерен, нанотрубки) или линейную sp- (карбин) гибридизации.
 Ничего другого кроме атомов С в таких разных «простых» веществах, как графит, алмаз и сажа обнаружить не удавалось. В углероде заложена способность к созданию в трехмерном мире химически стабильных двумерных мембран толщиной в один атом. Это свойство углерода имеет важное значение для химии и технологического развития в целом.
Ничего другого кроме атомов С в таких разных «простых» веществах, как графит, алмаз и сажа обнаружить не удавалось. В углероде заложена способность к созданию в трехмерном мире химически стабильных двумерных мембран толщиной в один атом. Это свойство углерода имеет важное значение для химии и технологического развития в целом.
 Фуллерены – новые аллотропные модификации углерода В 1985 г. произошло важное открытие в химии одного из наиболее изученных элементов – углерода. Коллектив авторов: Крото (Англия), Хит, О’Брайен, Керл и Смолли (США), исследуя масс-спектры паров графита, полученных при лазерном облучении (импульсный эксимерный лазер Ar. F, λ=193 нм, энергия 6, 4 э. В) твердого образца, обнаружили пики, соответствующие массам 720 и 840. Они предположили, что данные пики соответствуют индивидуальным молекулам С 60 и С 70.
Фуллерены – новые аллотропные модификации углерода В 1985 г. произошло важное открытие в химии одного из наиболее изученных элементов – углерода. Коллектив авторов: Крото (Англия), Хит, О’Брайен, Керл и Смолли (США), исследуя масс-спектры паров графита, полученных при лазерном облучении (импульсный эксимерный лазер Ar. F, λ=193 нм, энергия 6, 4 э. В) твердого образца, обнаружили пики, соответствующие массам 720 и 840. Они предположили, что данные пики соответствуют индивидуальным молекулам С 60 и С 70.
 • Исследования углеродных кластеров были предприняты с целью определить могут ли углеродные цепочки типа HC 7 N (обнаруженные радиоастрономами в межзвёздной среде) быть получены в лабораторных условиях. Ar. F лазер осуществлял ионизацию. Образованные при этом ионы ускорялись в постоянном электрическом поле и попадали в дрейфовую трубку время-пролётного масс-спектрометра.
• Исследования углеродных кластеров были предприняты с целью определить могут ли углеродные цепочки типа HC 7 N (обнаруженные радиоастрономами в межзвёздной среде) быть получены в лабораторных условиях. Ar. F лазер осуществлял ионизацию. Образованные при этом ионы ускорялись в постоянном электрическом поле и попадали в дрейфовую трубку время-пролётного масс-спектрометра.
 Фуллерен С 60 принадлежит к тем редким химическим структурам, которые обладают наивысшей точечной симметрией, а именно симметрией икосаэдра Ih. Сферическая оболочка из 60 атомов образована пяти- и шестичленными циклами. Каждый пятичленный цикл соединен с пятью шестичленными. В молекуле отсутствуют пятичленные циклы, соединенные друг с другом. Всего в молекуле 12 пентагонов и 20 гексагонов. В 1996 г. Крото, Керл и Смолли были удостоены Нобелевской премии по химии за открытие, разработку методов получения и исследование фуллеренов, причем Нобелевский комитет сравнил это открытие по значимости не более не менее как с открытием Америки Колумбом.
Фуллерен С 60 принадлежит к тем редким химическим структурам, которые обладают наивысшей точечной симметрией, а именно симметрией икосаэдра Ih. Сферическая оболочка из 60 атомов образована пяти- и шестичленными циклами. Каждый пятичленный цикл соединен с пятью шестичленными. В молекуле отсутствуют пятичленные циклы, соединенные друг с другом. Всего в молекуле 12 пентагонов и 20 гексагонов. В 1996 г. Крото, Керл и Смолли были удостоены Нобелевской премии по химии за открытие, разработку методов получения и исследование фуллеренов, причем Нобелевский комитет сравнил это открытие по значимости не более не менее как с открытием Америки Колумбом.
 Рис. 2. Изомер С 60 в виде "початка". Заштрихованные области показывают смещение -электронного облака относительно атомов молекулы, образующих боковую поверхность структуры
Рис. 2. Изомер С 60 в виде "початка". Заштрихованные области показывают смещение -электронного облака относительно атомов молекулы, образующих боковую поверхность структуры
 Правило изолированных пятиугольников • На основе анализа большого эмпирического материала было установлено, что наиболее устойчивыми являются те фуллерены, в которых каждая пятиугольная грань окружена шестиугольниками.
Правило изолированных пятиугольников • На основе анализа большого эмпирического материала было установлено, что наиболее устойчивыми являются те фуллерены, в которых каждая пятиугольная грань окружена шестиугольниками.
 • Молекулы фуллеренов являются трехмерными аналогами ароматических структур. В фуллерене С 60 плоская углеродная сетка свернута и сшита в замкнутую сферу радиусом 0, 357 нм. Из правильных шестиугольников можно выложить плоскую поверхность, однако ими нельзя сформировать замкнутую поверхность. Поэтому в фуллерене часть шестиугольников преобразуется в пятиугольники, образуя усеченный икосаэдр. Расстояние С-С в пятиугольнике составляет 0, 143 нм, в шестиугольнике 0, 139 нм.
• Молекулы фуллеренов являются трехмерными аналогами ароматических структур. В фуллерене С 60 плоская углеродная сетка свернута и сшита в замкнутую сферу радиусом 0, 357 нм. Из правильных шестиугольников можно выложить плоскую поверхность, однако ими нельзя сформировать замкнутую поверхность. Поэтому в фуллерене часть шестиугольников преобразуется в пятиугольники, образуя усеченный икосаэдр. Расстояние С-С в пятиугольнике составляет 0, 143 нм, в шестиугольнике 0, 139 нм.
 Молекулы были названы фуллеренами по имени архитектора Фуллера, автора сетчатых ажурных конструкций (павильон США на Всемирной выставки ЭКСПО-67 в Монреале и др. ).
Молекулы были названы фуллеренами по имени архитектора Фуллера, автора сетчатых ажурных конструкций (павильон США на Всемирной выставки ЭКСПО-67 в Монреале и др. ).
 Зависимость масс-спектров фуллеренов от условий кластеризации Было обнаружено, что относительная интенсивность пика С 60 зависит от условий, увеличиваясь при повышении температуры. Следовательно, изомер (или изомеры), ответственный за высокую интенсивность пика, должен обладать повышенной химической стабильностью, чтобы «выживать» при увеличении числа соударений. Изомеры с висячими углеродными связями будут обладать высокой реакционной способностью и не смогут выжить при столкновениях. Роль химически активных столкновений проявляется в том, что в масс-спектрах наблюдаются только фуллерены с четным числом атомов углерода (С 60, С 70 и др. ).
Зависимость масс-спектров фуллеренов от условий кластеризации Было обнаружено, что относительная интенсивность пика С 60 зависит от условий, увеличиваясь при повышении температуры. Следовательно, изомер (или изомеры), ответственный за высокую интенсивность пика, должен обладать повышенной химической стабильностью, чтобы «выживать» при увеличении числа соударений. Изомеры с висячими углеродными связями будут обладать высокой реакционной способностью и не смогут выжить при столкновениях. Роль химически активных столкновений проявляется в том, что в масс-спектрах наблюдаются только фуллерены с четным числом атомов углерода (С 60, С 70 и др. ).
 Правила стабилизации полиэдрических структур Моделирование электронного строения таких структур привело к ряда правил, необходимых для их стабилизации: • Стабильные кластеры углерода имеют вид полиэдров, в которых каждый атом углерода имеет координационное число 3. • Более стабильны карбополиэдры, содержащие только пяти- и шестичленные циклы. • Более симметричные кластеры углерода – стабильнее. • Пятичленные циклы в полиэдрах должны быть изолированными. • Форма карбополиэдра должна быть сферической.
Правила стабилизации полиэдрических структур Моделирование электронного строения таких структур привело к ряда правил, необходимых для их стабилизации: • Стабильные кластеры углерода имеют вид полиэдров, в которых каждый атом углерода имеет координационное число 3. • Более стабильны карбополиэдры, содержащие только пяти- и шестичленные циклы. • Более симметричные кластеры углерода – стабильнее. • Пятичленные циклы в полиэдрах должны быть изолированными. • Форма карбополиэдра должна быть сферической.
 Метод получения макроскопических количеств фуллеренов • Интенсивно свойства фуллеренов стали изучаться только после разработки в 1990 г. Кречмером простого и эффективного метода получения граммовых (макроскопических) количеств фуллеренов. Основой метода является использование дугового электрического разряда с графитовыми электродами в атмосфере инертного газа. В результате в массе полученной «сажи» выход фуллеренов ~ 15%.
Метод получения макроскопических количеств фуллеренов • Интенсивно свойства фуллеренов стали изучаться только после разработки в 1990 г. Кречмером простого и эффективного метода получения граммовых (макроскопических) количеств фуллеренов. Основой метода является использование дугового электрического разряда с графитовыми электродами в атмосфере инертного газа. В результате в массе полученной «сажи» выход фуллеренов ~ 15%.
 Наиболее интенсивны линии фуллеренов С 60 и С 70, что свидетельствует о наибольшей их устойчивости.
Наиболее интенсивны линии фуллеренов С 60 и С 70, что свидетельствует о наибольшей их устойчивости.
 Структура С 70 получается при введении в экваториальную область С 60 пояса, состоящего из пяти шестиугольников.
Структура С 70 получается при введении в экваториальную область С 60 пояса, состоящего из пяти шестиугольников.
 • В саже пламени углеводородов с помощью электронной микроскопии были обнаружены различные фуллереновые наноструктуры: фуллерены, нанотрубки и вложенные друг в друга фуллерены, напоминающие русские матрешки. Эти наблюдения подтверждают, что углерод имеет сильную склонность к образованию подобных структур в совершенно различных с точки зрения химии ситуациях.
• В саже пламени углеводородов с помощью электронной микроскопии были обнаружены различные фуллереновые наноструктуры: фуллерены, нанотрубки и вложенные друг в друга фуллерены, напоминающие русские матрешки. Эти наблюдения подтверждают, что углерод имеет сильную склонность к образованию подобных структур в совершенно различных с точки зрения химии ситуациях.
 Спектральные свойства фуллеренов Важнейшими структурно-энергетическими характеристиками соединения являются его колебательные и электронные спектры (а-гексан, б-бензол).
Спектральные свойства фуллеренов Важнейшими структурно-энергетическими характеристиками соединения являются его колебательные и электронные спектры (а-гексан, б-бензол).
 • Вследствие очень высокой симметрии С 60 в его ИК-спектрах проявляются только 4 сильные линии. Спектр КР более богат и содержит 10 частот. • Наличие развитого спектра поглощения в видимой области (что делает эти растворы окрашенными) делает его похожим на спектры органических красителей. • Электронные спектры поглощения фуллеренов в УФ- и видимой области (200 -800 нм) используются в аналитических целях при получении, разделении и очистке фуллеренов. • Фуллерены обладают и люминесценцией, но с очень низким квантовым выходом.
• Вследствие очень высокой симметрии С 60 в его ИК-спектрах проявляются только 4 сильные линии. Спектр КР более богат и содержит 10 частот. • Наличие развитого спектра поглощения в видимой области (что делает эти растворы окрашенными) делает его похожим на спектры органических красителей. • Электронные спектры поглощения фуллеренов в УФ- и видимой области (200 -800 нм) используются в аналитических целях при получении, разделении и очистке фуллеренов. • Фуллерены обладают и люминесценцией, но с очень низким квантовым выходом.
 Сольватохромия фуллеренов • Растворы фуллеренов обладают сольватохромией, что свидетельствует о проявлении межмолекулярных взаимодействий (ММВ) не только специфического характера (что свойственно замещенным фуллеренам), но и универсальной природы. Это касается прежде всего фуллеренов эллипсоидного типа (С 70, С 84) и их производных.
Сольватохромия фуллеренов • Растворы фуллеренов обладают сольватохромией, что свидетельствует о проявлении межмолекулярных взаимодействий (ММВ) не только специфического характера (что свойственно замещенным фуллеренам), но и универсальной природы. Это касается прежде всего фуллеренов эллипсоидного типа (С 70, С 84) и их производных.
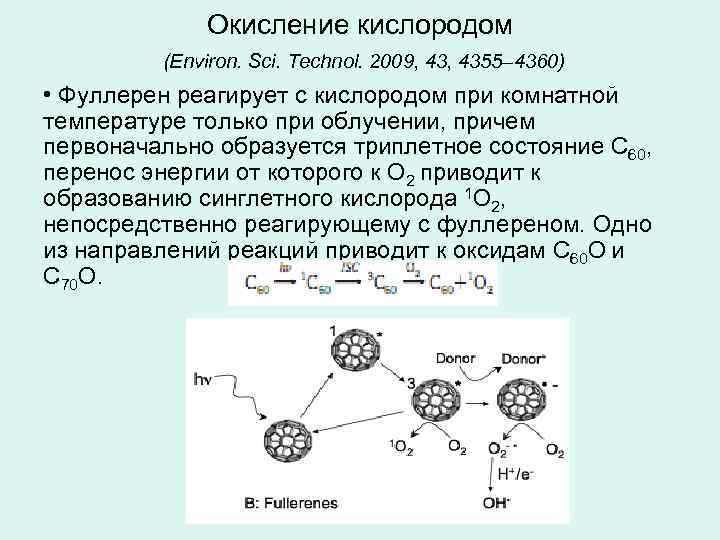 Окисление кислородом (Environ. Sci. Technol. 2009, 4355– 4360) • Фуллерен реагирует с кислородом при комнатной температуре только при облучении, причем первоначально образуется триплетное состояние С 60, перенос энергии от которого к О 2 приводит к образованию синглетного кислорода 1 О 2, непосредственно реагирующему с фуллереном. Одно из направлений реакций приводит к оксидам С 60 О и С 70 О.
Окисление кислородом (Environ. Sci. Technol. 2009, 4355– 4360) • Фуллерен реагирует с кислородом при комнатной температуре только при облучении, причем первоначально образуется триплетное состояние С 60, перенос энергии от которого к О 2 приводит к образованию синглетного кислорода 1 О 2, непосредственно реагирующему с фуллереном. Одно из направлений реакций приводит к оксидам С 60 О и С 70 О.
 Одно- и двухфотонное поглощение, приводящее к фотосенсибилизированному образованию 1 О 2 триплетными состояниями
Одно- и двухфотонное поглощение, приводящее к фотосенсибилизированному образованию 1 О 2 триплетными состояниями
 Фуллерен в атмосфере аргона • Молекула С 60 стабильна в инертной атмосфере аргона вплоть до температур порядка 1700 К, но в присутствии кислорода при 500 К наблюдается её значительное окисление с образованием СО и СО 2 • Молекулы фуллеренов являются трёхмерными аналогами ароматических структур.
Фуллерен в атмосфере аргона • Молекула С 60 стабильна в инертной атмосфере аргона вплоть до температур порядка 1700 К, но в присутствии кислорода при 500 К наблюдается её значительное окисление с образованием СО и СО 2 • Молекулы фуллеренов являются трёхмерными аналогами ароматических структур.
 Химическая связь в объемных карбофуллеренах • Если построить карту распределения электронной плотности, то можно увидеть, что эта плотность заметно выше внутри сферы, чем вне ее. В результате и создается направленная к центру стягивающая электронноядерная сила. Такая ситуация вообще должна быть характерна для каркасных молекул. Увеличение электронной плотности внутри сферы объясняется кривизной поверхности.
Химическая связь в объемных карбофуллеренах • Если построить карту распределения электронной плотности, то можно увидеть, что эта плотность заметно выше внутри сферы, чем вне ее. В результате и создается направленная к центру стягивающая электронноядерная сила. Такая ситуация вообще должна быть характерна для каркасных молекул. Увеличение электронной плотности внутри сферы объясняется кривизной поверхности.
 • Сферические фуллерены представляют собой класс соединений, само существование которых целиком определяется только объемными π – составляющими расположенного внутри сферы электронного облака. • В молекуле С 60 из-за кривизны поверхности углеродного каркаса перекрывание σ- и π -типа отлично от нуля. Поэтому в фуллерене отсутствуют валентные МО, имеющие ясно выраженный σ- или π – характер, что свойственно плоским молекулам. • Понятие ароматичности, выработанное для классических сопряженных молекул вряд ли стоит распространять на молекулы типа фуллерена. Если же нужно подчеркнуть образование единой ρэлектронной делокализованной системы (аналог πсистемы), лучше пользоваться термином «псевдоароматичность» .
• Сферические фуллерены представляют собой класс соединений, само существование которых целиком определяется только объемными π – составляющими расположенного внутри сферы электронного облака. • В молекуле С 60 из-за кривизны поверхности углеродного каркаса перекрывание σ- и π -типа отлично от нуля. Поэтому в фуллерене отсутствуют валентные МО, имеющие ясно выраженный σ- или π – характер, что свойственно плоским молекулам. • Понятие ароматичности, выработанное для классических сопряженных молекул вряд ли стоит распространять на молекулы типа фуллерена. Если же нужно подчеркнуть образование единой ρэлектронной делокализованной системы (аналог πсистемы), лучше пользоваться термином «псевдоароматичность» .
 Замещенные фуллерены • Фуллерены сочетают в себе свойства диенов и ароматических колец. Присоединение функциональных групп по двойным связям преобразует электронную структуру фуллерена. Простейшим замещенным фуллереном является С 60 Нn, при этом наблюдаются формы С 60 Н 2, С 60 Н 4, С 60 Н 18 и С 60 Н 36. Однако гидриды фуллеренов отличаются низкой устойчивостью. Гораздо большей устойчивостью, а потому и применимостью для создания материалов на их основе, обладают галогениды фуллеренов, устойчивость которых нарастает в ряду: С 60 Ix, С 60 Clx, С 60 Brx, С 60 Fx.
Замещенные фуллерены • Фуллерены сочетают в себе свойства диенов и ароматических колец. Присоединение функциональных групп по двойным связям преобразует электронную структуру фуллерена. Простейшим замещенным фуллереном является С 60 Нn, при этом наблюдаются формы С 60 Н 2, С 60 Н 4, С 60 Н 18 и С 60 Н 36. Однако гидриды фуллеренов отличаются низкой устойчивостью. Гораздо большей устойчивостью, а потому и применимостью для создания материалов на их основе, обладают галогениды фуллеренов, устойчивость которых нарастает в ряду: С 60 Ix, С 60 Clx, С 60 Brx, С 60 Fx.
 Галогензамещенные производные фуллеренов • Получены фторфуллерены С 60 FX, С 70 FX, где X- только чётное число. Увеличение содержания фтора на поверхности фуллерена приводит к снижению энергии связи C-F в связи с нарастанием стерических напряжений в высокофторированных фуллеренах. К наиболее стабильным фуллеренам относится С 60 F 18, из которого выращены молекулярные кристаллы и определена их структура.
Галогензамещенные производные фуллеренов • Получены фторфуллерены С 60 FX, С 70 FX, где X- только чётное число. Увеличение содержания фтора на поверхности фуллерена приводит к снижению энергии связи C-F в связи с нарастанием стерических напряжений в высокофторированных фуллеренах. К наиболее стабильным фуллеренам относится С 60 F 18, из которого выращены молекулярные кристаллы и определена их структура.
 Металлокомплексы фуллеренов • Известно, что неустойчивые фуллерены могут существовать в виде эндоэдральных металлокомплексов (ЭМК), представляющих собой фуллерен, внутрь оболочки которого внедрен кластер, содержащий атом металла. Lu 2@C 76 Согласно ЭПР измерениям, все 6 валентных электроны лютеция в данном ЭМК находятся в фуллереновой оболочке. В первом приближении можно полагать, что валентные электроны внедренного металла не приводят к существенному изменению энергетического спектра исходного фуллерена. Вследствие этого можно считать, что электронное строение ЭМК определяется энергетическим спектром чистого фуллерена, в котором имеются "избыточные электроны".
Металлокомплексы фуллеренов • Известно, что неустойчивые фуллерены могут существовать в виде эндоэдральных металлокомплексов (ЭМК), представляющих собой фуллерен, внутрь оболочки которого внедрен кластер, содержащий атом металла. Lu 2@C 76 Согласно ЭПР измерениям, все 6 валентных электроны лютеция в данном ЭМК находятся в фуллереновой оболочке. В первом приближении можно полагать, что валентные электроны внедренного металла не приводят к существенному изменению энергетического спектра исходного фуллерена. Вследствие этого можно считать, что электронное строение ЭМК определяется энергетическим спектром чистого фуллерена, в котором имеются "избыточные электроны".
 Соединения включения: в 1985 г. - первый эндоэдральный фуллерен La. С 60 Внутри С 60 имеется полость диаметром почти 0, 4 нм, способная вместить любой атом. • Было проведено лазерное испарение графита низкой плотности, вымоченного в водном растворе La. Cl 3. С помощью лазерной фрагментации было доказано, что атомы входят во внутреннюю полость фуллерена. • Далее были получены эндоэдральные металлофуллерены, содержащие атомы щелочных металлов K и Cs.
Соединения включения: в 1985 г. - первый эндоэдральный фуллерен La. С 60 Внутри С 60 имеется полость диаметром почти 0, 4 нм, способная вместить любой атом. • Было проведено лазерное испарение графита низкой плотности, вымоченного в водном растворе La. Cl 3. С помощью лазерной фрагментации было доказано, что атомы входят во внутреннюю полость фуллерена. • Далее были получены эндоэдральные металлофуллерены, содержащие атомы щелочных металлов K и Cs.
 • При таком изменении структуры энергия ионизации эндоэдрального фуллерена становится заметно меньше, а сродство к электрону, несмотря на отрицательный заряд на углеродном каркасе, больше, чем у полого аналога фуллерена. Действительно, эксперименты на эндоэдральных фуллеренах свидетельствуют о том, что они легче отдают и принимают электрон, чем простые фуллерены.
• При таком изменении структуры энергия ионизации эндоэдрального фуллерена становится заметно меньше, а сродство к электрону, несмотря на отрицательный заряд на углеродном каркасе, больше, чем у полого аналога фуллерена. Действительно, эксперименты на эндоэдральных фуллеренах свидетельствуют о том, что они легче отдают и принимают электрон, чем простые фуллерены.
 Химический димер
Химический димер
 Что касается фуллеренов, то в настоящее время стало ясно, что именно модифицированные фуллерены, т. е. фуллерены с различными функциональными группами наиболее перспективны для создания новых материалов. Фуллерен С 60, обладая высокой электроотрицательностью, легко образует комплексы с переносом заряда, где выступает акцептором электронов. В системах, состоящих из фуллерена в качестве акцептора, ковалентно связанного с фотоактивным донором, происходит фотоиндуцированный электронный переход. Фуллерены с азотсодержащими лигандами использованы для создания солнечных батарей. Для медицинских применений необходимы водорастворимые фуллерены – фуллеренолы С 60 Оy(OH)x.
Что касается фуллеренов, то в настоящее время стало ясно, что именно модифицированные фуллерены, т. е. фуллерены с различными функциональными группами наиболее перспективны для создания новых материалов. Фуллерен С 60, обладая высокой электроотрицательностью, легко образует комплексы с переносом заряда, где выступает акцептором электронов. В системах, состоящих из фуллерена в качестве акцептора, ковалентно связанного с фотоактивным донором, происходит фотоиндуцированный электронный переход. Фуллерены с азотсодержащими лигандами использованы для создания солнечных батарей. Для медицинских применений необходимы водорастворимые фуллерены – фуллеренолы С 60 Оy(OH)x.


