Надлежащие практики в фармации Лекция 1.ppt
- Количество слайдов: 22
 Надлежащие практики в фармации Кафедра промышленной фармации Национального фармацевтического университета Доктор фармацевтических наук ГЛАДУХ Евгений Владимирович 1
Надлежащие практики в фармации Кафедра промышленной фармации Национального фармацевтического университета Доктор фармацевтических наук ГЛАДУХ Евгений Владимирович 1
 ОСНОВНОЙ ПРИНЦИП GMP Владелец лицензии на производство должен производить ЛС так, чтобы обеспечить их соответствие своему назначению, требованиям регистрационного досье и исключить риск для пациентов, связанный с недостаточной безопасностью, качеством или эффективностью ЛС. 2
ОСНОВНОЙ ПРИНЦИП GMP Владелец лицензии на производство должен производить ЛС так, чтобы обеспечить их соответствие своему назначению, требованиям регистрационного досье и исключить риск для пациентов, связанный с недостаточной безопасностью, качеством или эффективностью ЛС. 2
 ОПРЕДЕЛЕНИЕ l. Система качества – совокупность организационных мероприятий, предпринимаемых в целях гарантии соответствия качества ЛС их назначению 3
ОПРЕДЕЛЕНИЕ l. Система качества – совокупность организационных мероприятий, предпринимаемых в целях гарантии соответствия качества ЛС их назначению 3
 Система обеспечения качества, предназначенная для производства лекарственных средств, должна гарантировать что: 1. ЛС разработаны и исследованы с учетом требований НПП и НЛП; 2. операции по изготовлению и контролю качества ясно специфицированы и соответствуют НПП; 3. четко определены ответственность и обязанности руководства; 4. осуществлены мероприятия по производству, поставке и использованию надлежащего исходного сырья и упаковочных материалов; 4
Система обеспечения качества, предназначенная для производства лекарственных средств, должна гарантировать что: 1. ЛС разработаны и исследованы с учетом требований НПП и НЛП; 2. операции по изготовлению и контролю качества ясно специфицированы и соответствуют НПП; 3. четко определены ответственность и обязанности руководства; 4. осуществлены мероприятия по производству, поставке и использованию надлежащего исходного сырья и упаковочных материалов; 4
 5. проведен весь необходимый контроль промежуточной продукции, любой другой производственный контроль и валидация; 6. готовая продукция правильно произведена и проверена в соответствии с установленными методиками; 7. ЛС не будут проданы и поставлены до того, как Уполномоченное лицо не удостоверит, что каждая серия продукции была изготовлена и проконтролирована в соответствии требованиями регистрационного досье и любыми другими предписаниями в отношении изготовления, контроля и выпуска лекарственных средств; 8. осуществлены достаточные мероприятия, гарантирующие, что качество ЛС поддерживается в течение всего срока годности при их хранении, распространении и последующем обращении; 9. имеется методика проведения самоинспекции или аудита качества, по которой регулярно оценивают эффективность и 5 пригодность системы обеспечения качества.
5. проведен весь необходимый контроль промежуточной продукции, любой другой производственный контроль и валидация; 6. готовая продукция правильно произведена и проверена в соответствии с установленными методиками; 7. ЛС не будут проданы и поставлены до того, как Уполномоченное лицо не удостоверит, что каждая серия продукции была изготовлена и проконтролирована в соответствии требованиями регистрационного досье и любыми другими предписаниями в отношении изготовления, контроля и выпуска лекарственных средств; 8. осуществлены достаточные мероприятия, гарантирующие, что качество ЛС поддерживается в течение всего срока годности при их хранении, распространении и последующем обращении; 9. имеется методика проведения самоинспекции или аудита качества, по которой регулярно оценивают эффективность и 5 пригодность системы обеспечения качества.
 Для создания на предприятии системы управления качеством организация должна: l определить процессы, необходимые для системы управления качеством, и их использование на всех уровнях в организации; l определить последовательность и взаимодействие этих процессов; l определить критерии и методы, необходимые для поддерживания функционирования этих процессов и управление ими; l обеспечить наличие ресурсов и информации, необходимых для поддержания функционирования и мониторинга этих процессов; l осуществлять мониторинг, измерения и анализ этих процессов; l внедрять методы, необходимые для достижения запланированных результатов и постоянного улучшения этих процессов 6
Для создания на предприятии системы управления качеством организация должна: l определить процессы, необходимые для системы управления качеством, и их использование на всех уровнях в организации; l определить последовательность и взаимодействие этих процессов; l определить критерии и методы, необходимые для поддерживания функционирования этих процессов и управление ими; l обеспечить наличие ресурсов и информации, необходимых для поддержания функционирования и мониторинга этих процессов; l осуществлять мониторинг, измерения и анализ этих процессов; l внедрять методы, необходимые для достижения запланированных результатов и постоянного улучшения этих процессов 6
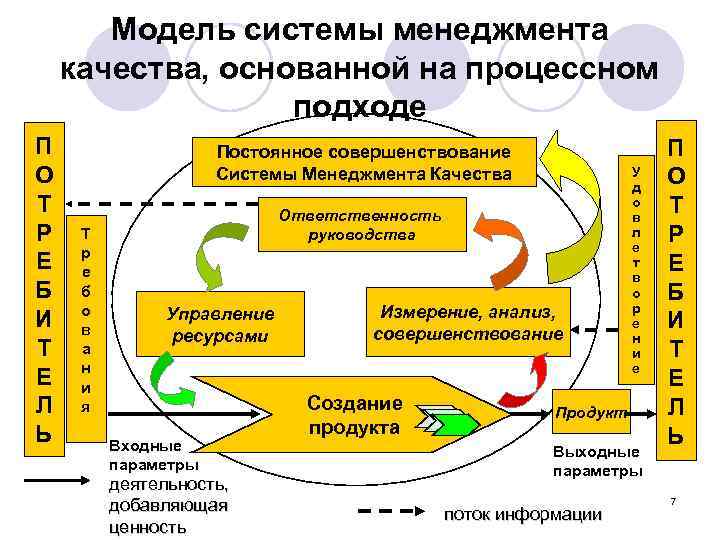 Модель системы менеджмента качества, основанной на процессном подходе П О Т Р Е Б И Т Е Л Ь Постоянное совершенствование Системы Менеджмента Качества Т р е б о в а н и я Ответственность руководства Управление ресурсами Входные параметры деятельность, добавляющая ценность Измерение, анализ, совершенствование Создание продукта У д о в л е т в о р е н и е Продукт Выходные параметры поток информации П О Т Р Е Б И Т Е Л Ь 7
Модель системы менеджмента качества, основанной на процессном подходе П О Т Р Е Б И Т Е Л Ь Постоянное совершенствование Системы Менеджмента Качества Т р е б о в а н и я Ответственность руководства Управление ресурсами Входные параметры деятельность, добавляющая ценность Измерение, анализ, совершенствование Создание продукта У д о в л е т в о р е н и е Продукт Выходные параметры поток информации П О Т Р Е Б И Т Е Л Ь 7
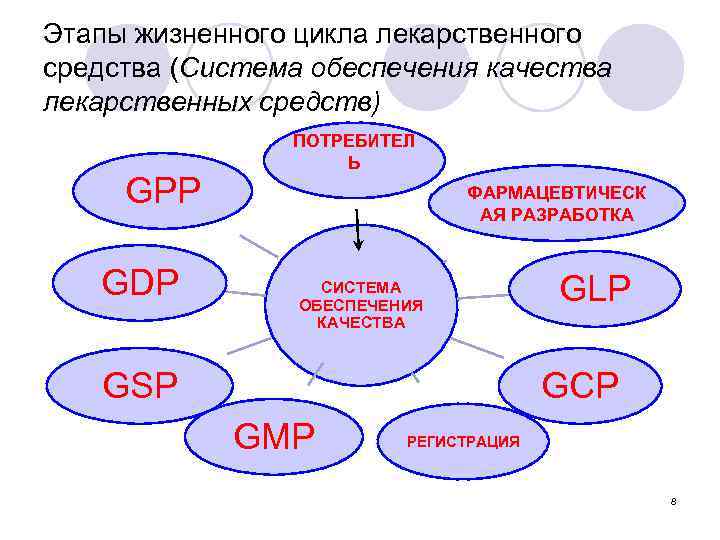 Этапы жизненного цикла лекарственного средства (Система обеспечения качества лекарственных средств) GPP GDP ПОТРЕБИТЕЛ Ь ФАРМАЦЕВТИЧЕСК АЯ РАЗРАБОТКА СИСТЕМА ОБЕСПЕЧЕНИЯ КАЧЕСТВА GSP GLP GCP GMP РЕГИСТРАЦИЯ 8
Этапы жизненного цикла лекарственного средства (Система обеспечения качества лекарственных средств) GPP GDP ПОТРЕБИТЕЛ Ь ФАРМАЦЕВТИЧЕСК АЯ РАЗРАБОТКА СИСТЕМА ОБЕСПЕЧЕНИЯ КАЧЕСТВА GSP GLP GCP GMP РЕГИСТРАЦИЯ 8
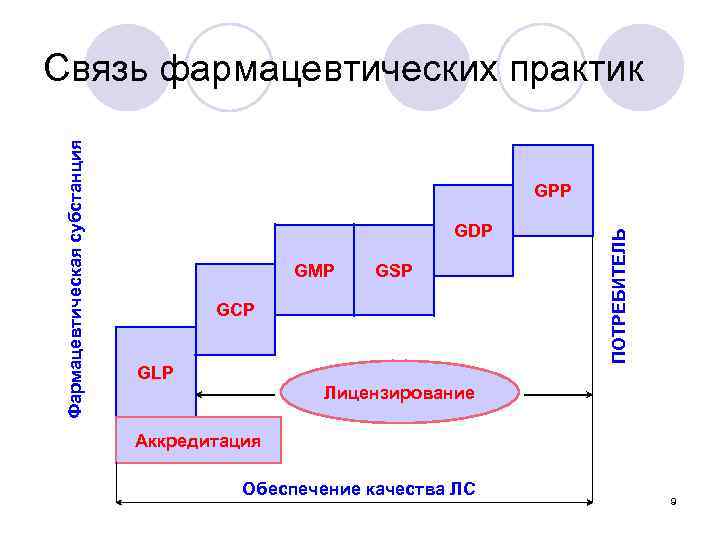 GPP GDP GMP GSP GCP GLP ПОТРЕБИТЕЛЬ Фармацевтическая субстанция Связь фармацевтических практик Лицензирование Аккредитация Обеспечение качества ЛС 9
GPP GDP GMP GSP GCP GLP ПОТРЕБИТЕЛЬ Фармацевтическая субстанция Связь фармацевтических практик Лицензирование Аккредитация Обеспечение качества ЛС 9
 Нормативные документы СТ-Н МОЗУ 42 -1. 0: 2005 Фармацевтична продукція. Система стандартизації. Основні положення СТ-Н МОЗУ 42 -3. 0: 2011 Настанова. Лікарські засоби. Фармацевтична розробка (ІСН Q 8) СТ-Н МОЗУ 42 -3. 1: 2004 Настанова. Лікарські засоби. Фармацевтична розробка СТ-Н МОЗУ 42 -3. 2: 2004 Настанова. Лікарські засоби. Специфікації: контрольні випробування та критерії прийнятності СТ-Н МОЗУ 42 -3. 3: 2004 Настанова. Лікарські засоби. Випробування стабільності СТ-Н МОЗУ 42 -3. 4: 2004 Настанова. Лікарські засоби. Виробництво готових лікарських засобів СТ-Н МОЗУ 42 -3. 5: 2004 Настанова. Лікарські засоби. Валідація процесів СТ-Н МОЗУ 42 -3. 6: 2004 Настанова. Лікарські засоби. Допоміжні речовини СТ-Н МОЗУ 42 -4. 0: 2011 Настанова. Лікарські засоби. Належна виробнича практика СТ-Н МОЗУ 42 -4. 1: 2011 Настанова. Лікарські засоби. Досьє виробничої дільниці 10
Нормативные документы СТ-Н МОЗУ 42 -1. 0: 2005 Фармацевтична продукція. Система стандартизації. Основні положення СТ-Н МОЗУ 42 -3. 0: 2011 Настанова. Лікарські засоби. Фармацевтична розробка (ІСН Q 8) СТ-Н МОЗУ 42 -3. 1: 2004 Настанова. Лікарські засоби. Фармацевтична розробка СТ-Н МОЗУ 42 -3. 2: 2004 Настанова. Лікарські засоби. Специфікації: контрольні випробування та критерії прийнятності СТ-Н МОЗУ 42 -3. 3: 2004 Настанова. Лікарські засоби. Випробування стабільності СТ-Н МОЗУ 42 -3. 4: 2004 Настанова. Лікарські засоби. Виробництво готових лікарських засобів СТ-Н МОЗУ 42 -3. 5: 2004 Настанова. Лікарські засоби. Валідація процесів СТ-Н МОЗУ 42 -3. 6: 2004 Настанова. Лікарські засоби. Допоміжні речовини СТ-Н МОЗУ 42 -4. 0: 2011 Настанова. Лікарські засоби. Належна виробнича практика СТ-Н МОЗУ 42 -4. 1: 2011 Настанова. Лікарські засоби. Досьє виробничої дільниці 10
 Нормативные документы СТ-Н МОЗУ 42 -4. 2: 2011 Настанова. Лікарські засоби. Управління ризиками для якості (ІСН Q 9) СТ-Н МОЗУ 42 -4. 3: 2011 Настанова. Лікарські засоби. Фармацевтична система якості (ІСН Q 10) СТ-Н МОЗУ 42 -4. 4: 2011 Настанова. Лікарські засоби. Міжнародні гармонізовані вимоги щодо сертифікації серії НАСТАНОВА 42 -01 -2003 Настанова. Лікарські засоби. Технологічний процес. Документація СТ-Н МОЗУ 42 -5. 0: 2008 Настанова. Лікарські засоби. Належна практика дистрибуції СТ-Н МОЗУ 42 -5. 1: 2011 Настанова. Лікарські засоби. Належна практика зберігання СТ-Н МОЗУ 42 -6. 0: 2008 Настанова. Лікарські засоби. Належна лабораторна практика СТ-Н МОЗУ 42 -7. 0: 2008 Настанова. Лікарські засоби. Належна клінічна практика СТ-Н МОЗУ 42 -7. 1: 2005 Настанова. Лікарські засоби. Дослідження біодоступності та біоеквівалентності 11
Нормативные документы СТ-Н МОЗУ 42 -4. 2: 2011 Настанова. Лікарські засоби. Управління ризиками для якості (ІСН Q 9) СТ-Н МОЗУ 42 -4. 3: 2011 Настанова. Лікарські засоби. Фармацевтична система якості (ІСН Q 10) СТ-Н МОЗУ 42 -4. 4: 2011 Настанова. Лікарські засоби. Міжнародні гармонізовані вимоги щодо сертифікації серії НАСТАНОВА 42 -01 -2003 Настанова. Лікарські засоби. Технологічний процес. Документація СТ-Н МОЗУ 42 -5. 0: 2008 Настанова. Лікарські засоби. Належна практика дистрибуції СТ-Н МОЗУ 42 -5. 1: 2011 Настанова. Лікарські засоби. Належна практика зберігання СТ-Н МОЗУ 42 -6. 0: 2008 Настанова. Лікарські засоби. Належна лабораторна практика СТ-Н МОЗУ 42 -7. 0: 2008 Настанова. Лікарські засоби. Належна клінічна практика СТ-Н МОЗУ 42 -7. 1: 2005 Настанова. Лікарські засоби. Дослідження біодоступності та біоеквівалентності 11
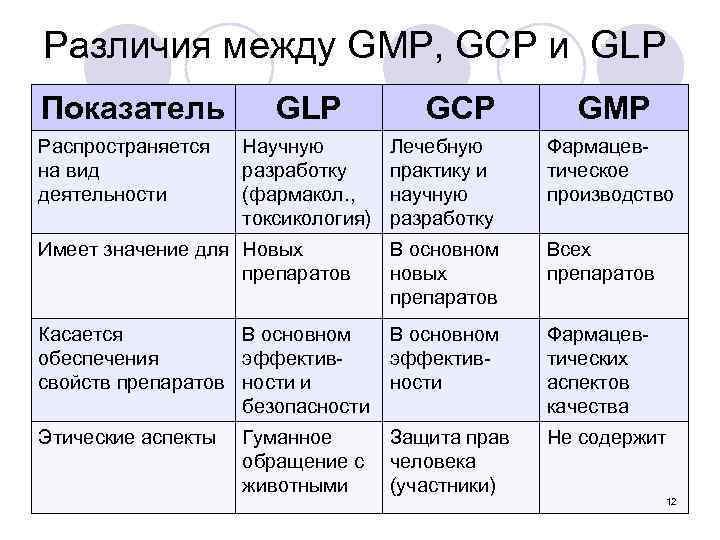 Различия между GMP, GСP и GLP Показатель Распространяется на вид деятельности GLP Научную разработку (фармакол. , токсикология) GСP GMP Лечебную практику и научную разработку Фармацевтическое производство Имеет значение для Новых препаратов В основном новых препаратов Всех препаратов Касается В основном обеспечения эффективсвойств препаратов ности и безопасности В основном эффективности Фармацевтических аспектов качества Этические аспекты Защита прав человека (участники) Не содержит Гуманное обращение с животными 12
Различия между GMP, GСP и GLP Показатель Распространяется на вид деятельности GLP Научную разработку (фармакол. , токсикология) GСP GMP Лечебную практику и научную разработку Фармацевтическое производство Имеет значение для Новых препаратов В основном новых препаратов Всех препаратов Касается В основном обеспечения эффективсвойств препаратов ности и безопасности В основном эффективности Фармацевтических аспектов качества Этические аспекты Защита прав человека (участники) Не содержит Гуманное обращение с животными 12
 Основные принципы l Управление качеством l Персонал l Помещения и оборудование l Документация l Производство l Контроль качества l Производство по контракту l Отзыв продукции l Самоинспекция 13
Основные принципы l Управление качеством l Персонал l Помещения и оборудование l Документация l Производство l Контроль качества l Производство по контракту l Отзыв продукции l Самоинспекция 13
 Управление качеством l Основополагающий принцип GMP гласит, что производитель лекарственных средств должен создать и внедрить эффективную систему обеспечения качества, включая активное участие дирекции и всего персонала. l Система качества – это совокупность организационной структуры, методик, процессов и ресурсов, необходимых для осуществления управления качеством. l Стандарт GMP предназначен для построения систем качества на предприятиях, которые производят лекарственные средства. 14
Управление качеством l Основополагающий принцип GMP гласит, что производитель лекарственных средств должен создать и внедрить эффективную систему обеспечения качества, включая активное участие дирекции и всего персонала. l Система качества – это совокупность организационной структуры, методик, процессов и ресурсов, необходимых для осуществления управления качеством. l Стандарт GMP предназначен для построения систем качества на предприятиях, которые производят лекарственные средства. 14
 Персонал l Основной принцип в отношении персонала гласит, что поскольку система качества и производство зависят от людей, то штат должен быть укомплектован достаточным количеством квалифицированного персонала, который способен на должном уровне решать все задачи, находящиеся в сфере ответственности предприятия. 15
Персонал l Основной принцип в отношении персонала гласит, что поскольку система качества и производство зависят от людей, то штат должен быть укомплектован достаточным количеством квалифицированного персонала, который способен на должном уровне решать все задачи, находящиеся в сфере ответственности предприятия. 15
 Помещения и оборудование l Следующий принцип касается помещений и оборудования, которые необходимо проектировать, располагать, конструировать, оснащать, приспосабливать, а также содержать и обслуживать таким образом, чтобы они соответствовали своему назначению и были пригодны для предусмотренных работ. Их размер, конструкция и расположение должны сводить к минимуму риск ошибок при производстве и обеспечивать возможность проведения эффективной уборки и эксплуатации с целью исключения перекрестной контаминации, накопления пыли или грязи, а также всех других факторов, которые могут отрицательно повлиять на качество продукции 16
Помещения и оборудование l Следующий принцип касается помещений и оборудования, которые необходимо проектировать, располагать, конструировать, оснащать, приспосабливать, а также содержать и обслуживать таким образом, чтобы они соответствовали своему назначению и были пригодны для предусмотренных работ. Их размер, конструкция и расположение должны сводить к минимуму риск ошибок при производстве и обеспечивать возможность проведения эффективной уборки и эксплуатации с целью исключения перекрестной контаминации, накопления пыли или грязи, а также всех других факторов, которые могут отрицательно повлиять на качество продукции 16
 Документация l Следующий принцип касается качественной документации, которая является важной частью системы обеспечения качества. l Она должна регламентировать все аспекты производства и контроля качества лекарственных средств. На каждом предприятии должен быть необходимый комплект документов 17
Документация l Следующий принцип касается качественной документации, которая является важной частью системы обеспечения качества. l Она должна регламентировать все аспекты производства и контроля качества лекарственных средств. На каждом предприятии должен быть необходимый комплект документов 17
 Производство l Следующий принцип гласит, что производство лекарственных средств должно осуществляться по технологическим регламентам с учетом принципов и правил надлежащей производственной практики (GMP), что необходимо для получения готовой продукции требуемого качества в соответствии с регистрационной и лицензионной документацией. 18
Производство l Следующий принцип гласит, что производство лекарственных средств должно осуществляться по технологическим регламентам с учетом принципов и правил надлежащей производственной практики (GMP), что необходимо для получения готовой продукции требуемого качества в соответствии с регистрационной и лицензионной документацией. 18
 Контроль качества l Контроль качества включает работы, которые связаны с отбором проб, нормативной документацией (спецификациями) и испытаниями; а также с методиками организации этих работ, их документированием и выдачей в установленном порядке разрешений, которые гарантируют, что все необходимые соответствующие испытания действительно проведены. Исходное сырье, материалы, полупродукты и промежуточная продукция не разрешаются для использования, а готовая продукция не допускается к реализации до тех пор, пока их качество не будет признано удовлетворительным. 19
Контроль качества l Контроль качества включает работы, которые связаны с отбором проб, нормативной документацией (спецификациями) и испытаниями; а также с методиками организации этих работ, их документированием и выдачей в установленном порядке разрешений, которые гарантируют, что все необходимые соответствующие испытания действительно проведены. Исходное сырье, материалы, полупродукты и промежуточная продукция не разрешаются для использования, а готовая продукция не допускается к реализации до тех пор, пока их качество не будет признано удовлетворительным. 19
 Производство по контракту l Основной принцип гласит, что при анализе контракта все условия производства и/или испытаний должны быть четко и всесторонне определены, согласованы и проконтролированы во избежание недоразумений и несоответствий, которые могут стать причиной неудовлетворительного качества продукции, выполняемых работ или испытаний. Требуется наличие письменного контракта (договора), который заключается в установленном порядке между двумя юридическими лицами 20
Производство по контракту l Основной принцип гласит, что при анализе контракта все условия производства и/или испытаний должны быть четко и всесторонне определены, согласованы и проконтролированы во избежание недоразумений и несоответствий, которые могут стать причиной неудовлетворительного качества продукции, выполняемых работ или испытаний. Требуется наличие письменного контракта (договора), который заключается в установленном порядке между двумя юридическими лицами 20
 Отзыв продукции l Следующий принцип гласит, что все рекламации и другая информация относительно несоответствия качества потенциально бракованной продукции должны тщательно проверяться в соответствии со стандартной рабочей методикой. На предприятии-производителе должна быть организована система, позволяющая, при необходимости, быстро и эффективно отзывать реализованную продукцию, у которой установлены или предполагаются дефекты качества. 21
Отзыв продукции l Следующий принцип гласит, что все рекламации и другая информация относительно несоответствия качества потенциально бракованной продукции должны тщательно проверяться в соответствии со стандартной рабочей методикой. На предприятии-производителе должна быть организована система, позволяющая, при необходимости, быстро и эффективно отзывать реализованную продукцию, у которой установлены или предполагаются дефекты качества. 21
 Самоинспекции l И, наконец, последний незыблемый принцип – на предприятии должна осуществляться самоинспекция и аудит качества, назначение которых состоит во всестороннем надзоре за выполнением правил GMP, и при необходимости, в выработке рекомендаций по проведению предупреждающих и корректирующих действий 22
Самоинспекции l И, наконец, последний незыблемый принцип – на предприятии должна осуществляться самоинспекция и аудит качества, назначение которых состоит во всестороннем надзоре за выполнением правил GMP, и при необходимости, в выработке рекомендаций по проведению предупреждающих и корректирующих действий 22


