Латышев. А. М..pptx
- Количество слайдов: 18
 Национальный исследовательский Томский государственный университет з Институт Физики Прочности и Материаловедения СО РАН СОРБЦИЯ И ДИФФУЗИЯ КИСЛОРОДА В СПЛАВЕ Ti. Al 3 А. М. Латышев Научный руководитель: проф. д. ф. -м. н. C. Е. Кулькова А. В. Бакулин
Национальный исследовательский Томский государственный университет з Институт Физики Прочности и Материаловедения СО РАН СОРБЦИЯ И ДИФФУЗИЯ КИСЛОРОДА В СПЛАВЕ Ti. Al 3 А. М. Латышев Научный руководитель: проф. д. ф. -м. н. C. Е. Кулькова А. В. Бакулин
 Введение Ø Сплавы Ti-Al обладают уникальными свойствами, такими как высокая температура плавления и высокая прочность, а также являются более легкими, по сравнению с другими материалами. Ø Главным недостатком данных сплавов является недостаточная коррозионная стойкость при высоких температурах, что ограничивает их практическое применение. Ø Экспериментальные исследования показали, что вместо плотной защитной пленки оксида алюминия на поверхности формируются смешанные оксидные структуры на основе Al 2 O 3 и Ti. O 2. Ø Легирование сплавов Ti-Al и изменение их химического состава может влиять на механизм окисления. Например, сплав Ti. Al 3 имеет наибольшую коррозионную стойкость из всех алюминидов титана. Цель работы: Изучение сорбции и диффузии кислорода в сплаве Ti. Al 3. 2
Введение Ø Сплавы Ti-Al обладают уникальными свойствами, такими как высокая температура плавления и высокая прочность, а также являются более легкими, по сравнению с другими материалами. Ø Главным недостатком данных сплавов является недостаточная коррозионная стойкость при высоких температурах, что ограничивает их практическое применение. Ø Экспериментальные исследования показали, что вместо плотной защитной пленки оксида алюминия на поверхности формируются смешанные оксидные структуры на основе Al 2 O 3 и Ti. O 2. Ø Легирование сплавов Ti-Al и изменение их химического состава может влиять на механизм окисления. Например, сплав Ti. Al 3 имеет наибольшую коррозионную стойкость из всех алюминидов титана. Цель работы: Изучение сорбции и диффузии кислорода в сплаве Ti. Al 3. 2
 Метод расчета o Расчеты производились методом псевдопотенциала, реализованном программным кодом VASP с обобщенным градиентным приближением для обменно-корреляционного функционала (GGA). o Энергия обрезания для плоских волн составляла 550 э. В. o Атомные позиции релаксировались до достижения сил на атомах ~0. 01 э. В/Å. o Интегрирование по зоне Бриллюэна при расчете электронной структуры объемного сплава проводилась по сетке k-точек 15 15 7, генерируемой по схеме Монхорста-Пака. o Энергия молекулы кислорода была равна 8. 23 э. В. Энергия адсорбции вычислялась по формуле: где и – полные энергии систем с кислородом и без него, а полная энергия молекулы кислорода. Энергия связи вычислялась по формуле: 3
Метод расчета o Расчеты производились методом псевдопотенциала, реализованном программным кодом VASP с обобщенным градиентным приближением для обменно-корреляционного функционала (GGA). o Энергия обрезания для плоских волн составляла 550 э. В. o Атомные позиции релаксировались до достижения сил на атомах ~0. 01 э. В/Å. o Интегрирование по зоне Бриллюэна при расчете электронной структуры объемного сплава проводилась по сетке k-точек 15 15 7, генерируемой по схеме Монхорста-Пака. o Энергия молекулы кислорода была равна 8. 23 э. В. Энергия адсорбции вычислялась по формуле: где и – полные энергии систем с кислородом и без него, а полная энергия молекулы кислорода. Энергия связи вычислялась по формуле: 3
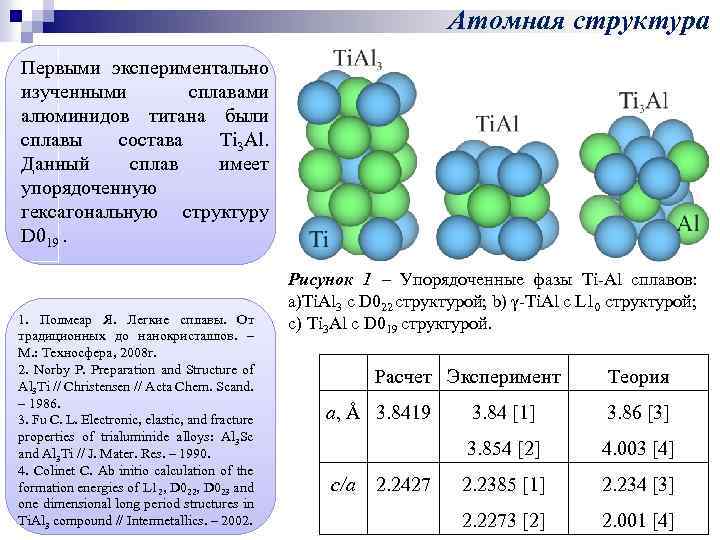 Атомная структура Первыми экспериментально изученными сплавами алюминидов титана были сплавы состава Ti 3 Al. Данный сплав имеет упорядоченную гексагональную структуру D 019. 1. Полмеар Я. Легкие сплавы. От традиционных до нанокристаллов. – М. : Техносфера, 2008 г. 2. Norby P. Preparation and Structure of Al 3 Ti // Christensen // Acta Chem. Scand. – 1986. 3. Fu C. L. Electronic, elastic, and fracture properties of trialuminide alloys: Al 3 Sc and Al 3 Ti // J. Mater. Res. – 1990. 4. Colinet C. Ab initio calculation of the formation energies of L 12, D 023 and one dimensional long period structures in Ti. Al 3 compound // Intermetallics. – 2002. Рисунок 1 – Упорядоченные фазы Ti-Al сплавов: a)Ti. Al 3 с D 022 структурой; b) γ-Ti. Al с L 10 структурой; с) Ti 3 Al c D 019 структурой. Расчет Эксперимент a, Å 3. 8419 Теория 2. 2427 3. 86 [3] 3. 854 [2] c/a 3. 84 [1] 4. 003 [4] 2. 2385 [1] 2. 234 [3] 2. 2273 [2] 2. 001 [4]
Атомная структура Первыми экспериментально изученными сплавами алюминидов титана были сплавы состава Ti 3 Al. Данный сплав имеет упорядоченную гексагональную структуру D 019. 1. Полмеар Я. Легкие сплавы. От традиционных до нанокристаллов. – М. : Техносфера, 2008 г. 2. Norby P. Preparation and Structure of Al 3 Ti // Christensen // Acta Chem. Scand. – 1986. 3. Fu C. L. Electronic, elastic, and fracture properties of trialuminide alloys: Al 3 Sc and Al 3 Ti // J. Mater. Res. – 1990. 4. Colinet C. Ab initio calculation of the formation energies of L 12, D 023 and one dimensional long period structures in Ti. Al 3 compound // Intermetallics. – 2002. Рисунок 1 – Упорядоченные фазы Ti-Al сплавов: a)Ti. Al 3 с D 022 структурой; b) γ-Ti. Al с L 10 структурой; с) Ti 3 Al c D 019 структурой. Расчет Эксперимент a, Å 3. 8419 Теория 2. 2427 3. 86 [3] 3. 854 [2] c/a 3. 84 [1] 4. 003 [4] 2. 2385 [1] 2. 234 [3] 2. 2273 [2] 2. 001 [4]
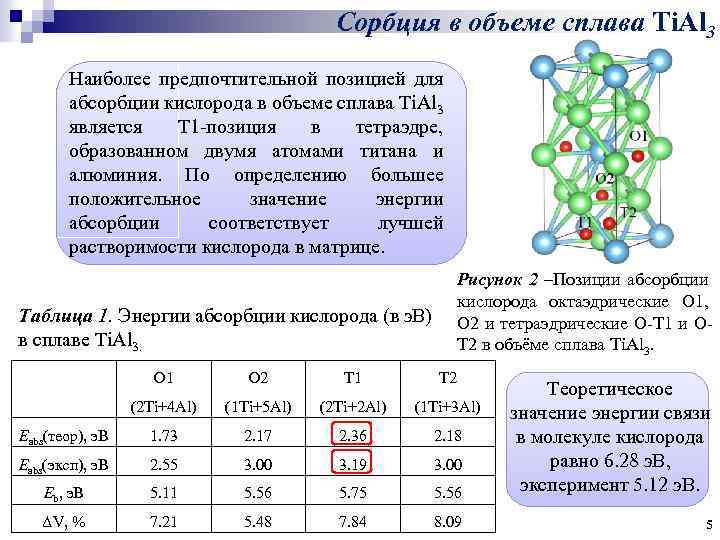 Сорбция в объеме сплава Ti. Al 3 Наиболее предпочтительной позицией для абсорбции кислорода в объеме сплава Ti. Al 3 является T 1 -позиция в тетраэдре, образованном двумя атомами титана и алюминия. По определению большее положительное значение энергии абсорбции соответствует лучшей растворимости кислорода в матрице. Рисунок 2 –Позиции абсорбции кислорода октаэдрические O 1, O 2 и тетраэдрические O-T 1 и OT 2 в объёме сплава Ti. Al 3. Таблица 1. Энергии абсорбции кислорода (в э. В) в сплаве Ti. Al 3. O 1 O 2 T 1 T 2 (2 Ti+4 Al) (1 Ti+5 Al) (2 Ti+2 Al) (1 Ti+3 Al) Eabs(теор), э. В 1. 73 2. 17 2. 36 2. 18 Eabs(эксп), э. В 2. 55 3. 00 3. 19 3. 00 Eb, э. В 5. 11 5. 56 5. 75 5. 56 Теоретическое значение энергии связи в молекуле кислорода равно 6. 28 э. В, эксперимент 5. 12 э. В. ΔV, % 7. 21 5. 48 7. 84 8. 09 5
Сорбция в объеме сплава Ti. Al 3 Наиболее предпочтительной позицией для абсорбции кислорода в объеме сплава Ti. Al 3 является T 1 -позиция в тетраэдре, образованном двумя атомами титана и алюминия. По определению большее положительное значение энергии абсорбции соответствует лучшей растворимости кислорода в матрице. Рисунок 2 –Позиции абсорбции кислорода октаэдрические O 1, O 2 и тетраэдрические O-T 1 и OT 2 в объёме сплава Ti. Al 3. Таблица 1. Энергии абсорбции кислорода (в э. В) в сплаве Ti. Al 3. O 1 O 2 T 1 T 2 (2 Ti+4 Al) (1 Ti+5 Al) (2 Ti+2 Al) (1 Ti+3 Al) Eabs(теор), э. В 1. 73 2. 17 2. 36 2. 18 Eabs(эксп), э. В 2. 55 3. 00 3. 19 3. 00 Eb, э. В 5. 11 5. 56 5. 75 5. 56 Теоретическое значение энергии связи в молекуле кислорода равно 6. 28 э. В, эксперимент 5. 12 э. В. ΔV, % 7. 21 5. 48 7. 84 8. 09 5
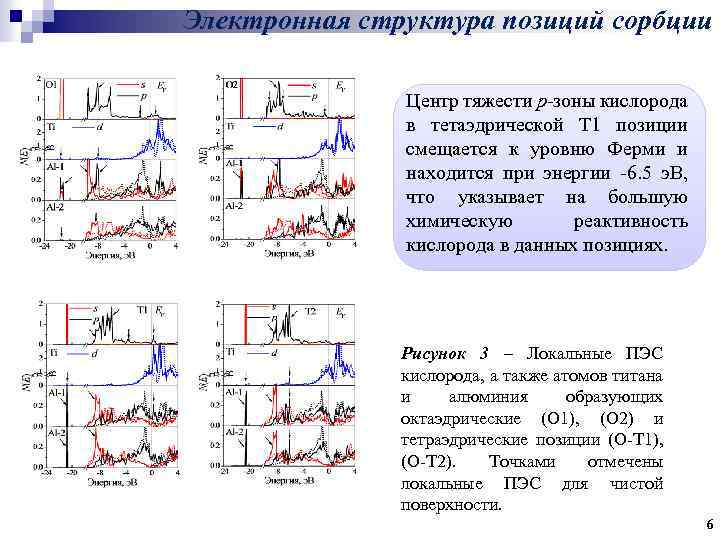 Электронная структура позиций сорбции Центр тяжести р-зоны кислорода в тетаэдрической T 1 позиции смещается к уровню Ферми и находится при энергии -6. 5 э. В, что указывает на большую химическую реактивность кислорода в данных позициях. Рисунок 3 – Локальные ПЭС кислорода, а также атомов титана и алюминия образующих октаэдрические (O 1), (O 2) и тетраэдрические позиции (O-T 1), (O-T 2). Точками отмечены локальные ПЭС для чистой поверхности. 6
Электронная структура позиций сорбции Центр тяжести р-зоны кислорода в тетаэдрической T 1 позиции смещается к уровню Ферми и находится при энергии -6. 5 э. В, что указывает на большую химическую реактивность кислорода в данных позициях. Рисунок 3 – Локальные ПЭС кислорода, а также атомов титана и алюминия образующих октаэдрические (O 1), (O 2) и тетраэдрические позиции (O-T 1), (O-T 2). Точками отмечены локальные ПЭС для чистой поверхности. 6
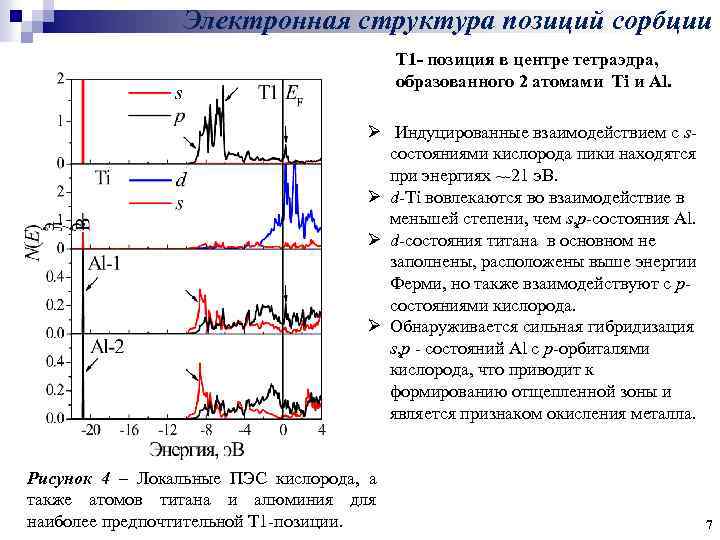 Электронная структура позиций сорбции Т 1 - позиция в центре тетраэдра, образованного 2 атомами Ti и Al. Ø Индуцированные взаимодействием с sсостояниями кислорода пики находятся при энергиях ~-21 э. В. Ø d-Ti вовлекаются во взаимодействие в меньшей степени, чем s, p-состояния Al. Ø d-состояния титана в основном не заполнены, расположены выше энергии Ферми, но также взаимодействуют с рсостояниями кислорода. Ø Обнаруживается сильная гибридизация s, p - состояний Al с р-орбиталями кислорода, что приводит к формированию отщепленной зоны и является признаком окисления металла. Рисунок 4 – Локальные ПЭС кислорода, а также атомов титана и алюминия для наиболее предпочтительной Т 1 -позиции. 7
Электронная структура позиций сорбции Т 1 - позиция в центре тетраэдра, образованного 2 атомами Ti и Al. Ø Индуцированные взаимодействием с sсостояниями кислорода пики находятся при энергиях ~-21 э. В. Ø d-Ti вовлекаются во взаимодействие в меньшей степени, чем s, p-состояния Al. Ø d-состояния титана в основном не заполнены, расположены выше энергии Ферми, но также взаимодействуют с рсостояниями кислорода. Ø Обнаруживается сильная гибридизация s, p - состояний Al с р-орбиталями кислорода, что приводит к формированию отщепленной зоны и является признаком окисления металла. Рисунок 4 – Локальные ПЭС кислорода, а также атомов титана и алюминия для наиболее предпочтительной Т 1 -позиции. 7
 Адсорбция на поверхности (001) Сплав Ti. Al 3 имеет тетрагональную структуру D 022, поэтому для поверхности (001) возможно два типа окончания. Сплав может заканчиваться слоем алюминия Ti. Al 3(001)Al или слоем, содержащим атомы титана и алюминия в равных пропорциях Ti. Al 3(001)Ti. Al. Рисунок 5 – позиции адсорбции кислорода на нестехиометрической поверхности (100) Таблица 2. Энергия адсорбции кислорода (в э. В) на поверхности Ti. Al 3(001). Позиция HTi B TAl TTi Ti. Al 3(001)Al Рисунок 6– Диаграмма стабильности поверхности сплава Ti. Al 3 HAl 4. 63 3. 79 – 2. 21 – Ti. Al 3(001)Ti. Al 4. 71 – 4. 60 2. 88 3. 78 8
Адсорбция на поверхности (001) Сплав Ti. Al 3 имеет тетрагональную структуру D 022, поэтому для поверхности (001) возможно два типа окончания. Сплав может заканчиваться слоем алюминия Ti. Al 3(001)Al или слоем, содержащим атомы титана и алюминия в равных пропорциях Ti. Al 3(001)Ti. Al. Рисунок 5 – позиции адсорбции кислорода на нестехиометрической поверхности (100) Таблица 2. Энергия адсорбции кислорода (в э. В) на поверхности Ti. Al 3(001). Позиция HTi B TAl TTi Ti. Al 3(001)Al Рисунок 6– Диаграмма стабильности поверхности сплава Ti. Al 3 HAl 4. 63 3. 79 – 2. 21 – Ti. Al 3(001)Ti. Al 4. 71 – 4. 60 2. 88 3. 78 8
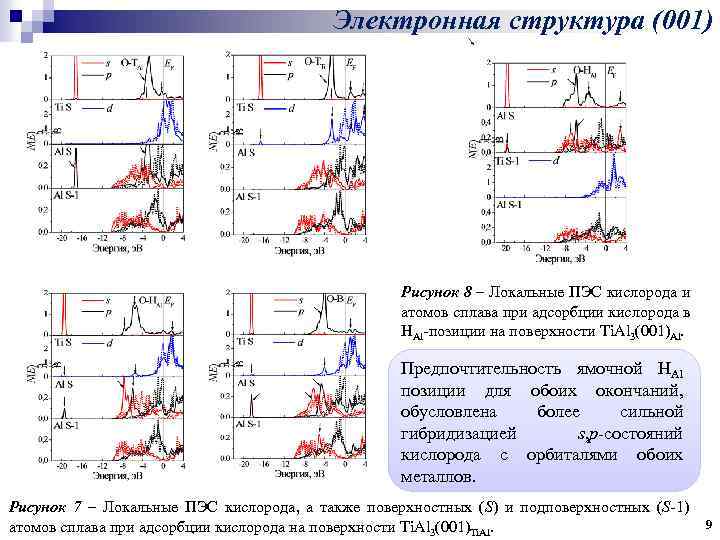 Электронная структура (001) Рисунок 8 – Локальные ПЭС кислорода и атомов сплава при адсорбции кислорода в HAl-позиции на поверхности Ti. Al 3(001)Al. Предпочтительность ямочной HAl позиции для обоих окончаний, обусловлена более сильной гибридизацией s, p-состояний кислорода с орбиталями обоих металлов. Рисунок 7 – Локальные ПЭС кислорода, а также поверхностных (S) и подповерхностных (S-1) атомов сплава при адсорбции кислорода на поверхности Ti. Al 3(001)Ti. Al. 9
Электронная структура (001) Рисунок 8 – Локальные ПЭС кислорода и атомов сплава при адсорбции кислорода в HAl-позиции на поверхности Ti. Al 3(001)Al. Предпочтительность ямочной HAl позиции для обоих окончаний, обусловлена более сильной гибридизацией s, p-состояний кислорода с орбиталями обоих металлов. Рисунок 7 – Локальные ПЭС кислорода, а также поверхностных (S) и подповерхностных (S-1) атомов сплава при адсорбции кислорода на поверхности Ti. Al 3(001)Ti. Al. 9
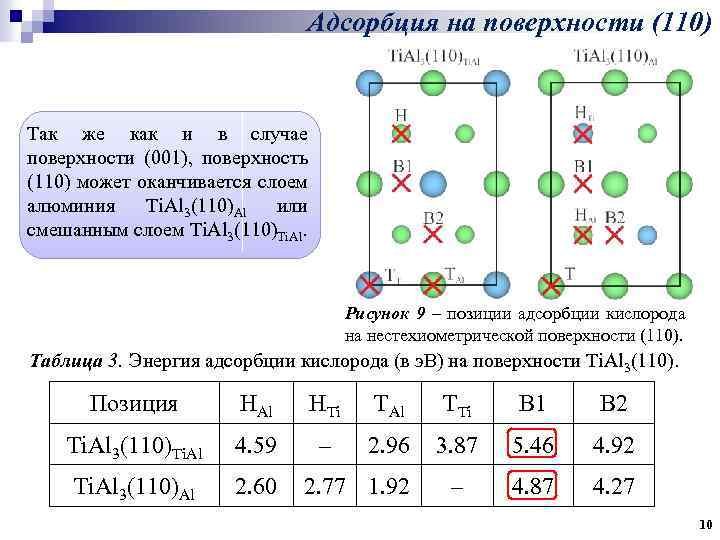 Адсорбция на поверхности (110) Так же как и в случае поверхности (001), поверхность (110) может оканчивается слоем алюминия Ti. Al 3(110)Al или смешанным слоем Ti. Al 3(110)Ti. Al. Рисунок 9 – позиции адсорбции кислорода на нестехиометрической поверхности (110). Таблица 3. Энергия адсорбции кислорода (в э. В) на поверхности Ti. Al 3(110). Позиция HAl HTi TAl TTi B 1 B 2 Ti. Al 3(110)Ti. Al 4. 59 – 2. 96 3. 87 5. 46 4. 92 Ti. Al 3(110)Al 2. 60 – 4. 87 4. 27 2. 77 1. 92 10
Адсорбция на поверхности (110) Так же как и в случае поверхности (001), поверхность (110) может оканчивается слоем алюминия Ti. Al 3(110)Al или смешанным слоем Ti. Al 3(110)Ti. Al. Рисунок 9 – позиции адсорбции кислорода на нестехиометрической поверхности (110). Таблица 3. Энергия адсорбции кислорода (в э. В) на поверхности Ti. Al 3(110). Позиция HAl HTi TAl TTi B 1 B 2 Ti. Al 3(110)Ti. Al 4. 59 – 2. 96 3. 87 5. 46 4. 92 Ti. Al 3(110)Al 2. 60 – 4. 87 4. 27 2. 77 1. 92 10
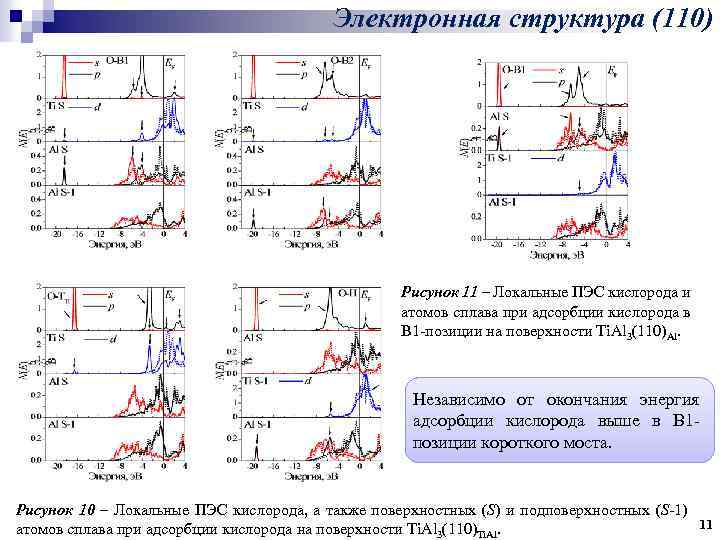 Электронная структура (110) Рисунок 11 – Локальные ПЭС кислорода и атомов сплава при адсорбции кислорода в B 1 -позиции на поверхности Ti. Al 3(110)Al. Независимо от окончания энергия адсорбции кислорода выше в В 1 позиции короткого моста. Рисунок 10 – Локальные ПЭС кислорода, а также поверхностных (S) и подповерхностных (S-1) 11 атомов сплава при адсорбции кислорода на поверхности Ti. Al 3(110)Ti. Al.
Электронная структура (110) Рисунок 11 – Локальные ПЭС кислорода и атомов сплава при адсорбции кислорода в B 1 -позиции на поверхности Ti. Al 3(110)Al. Независимо от окончания энергия адсорбции кислорода выше в В 1 позиции короткого моста. Рисунок 10 – Локальные ПЭС кислорода, а также поверхностных (S) и подповерхностных (S-1) 11 атомов сплава при адсорбции кислорода на поверхности Ti. Al 3(110)Ti. Al.
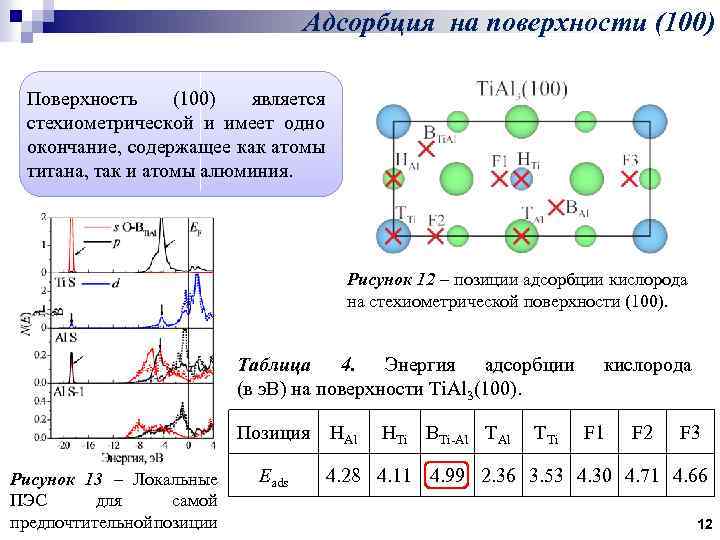 Адсорбция на поверхности (100) Поверхность (100) является стехиометрической и имеет одно окончание, содержащее как атомы титана, так и атомы алюминия. Рисунок 12 – позиции адсорбции кислорода на стехиометрической поверхности (100). Таблица 4. Энергия адсорбции (в э. В) на поверхности Ti. Al 3(100). Позиция HAl Рисунок 13 – Локальные ПЭС для самой предпочтительной позиции Еads HTi BTi-Al TTi кислорода F 1 F 2 F 3 4. 28 4. 11 4. 99 2. 36 3. 53 4. 30 4. 71 4. 66 12
Адсорбция на поверхности (100) Поверхность (100) является стехиометрической и имеет одно окончание, содержащее как атомы титана, так и атомы алюминия. Рисунок 12 – позиции адсорбции кислорода на стехиометрической поверхности (100). Таблица 4. Энергия адсорбции (в э. В) на поверхности Ti. Al 3(100). Позиция HAl Рисунок 13 – Локальные ПЭС для самой предпочтительной позиции Еads HTi BTi-Al TTi кислорода F 1 F 2 F 3 4. 28 4. 11 4. 99 2. 36 3. 53 4. 30 4. 71 4. 66 12
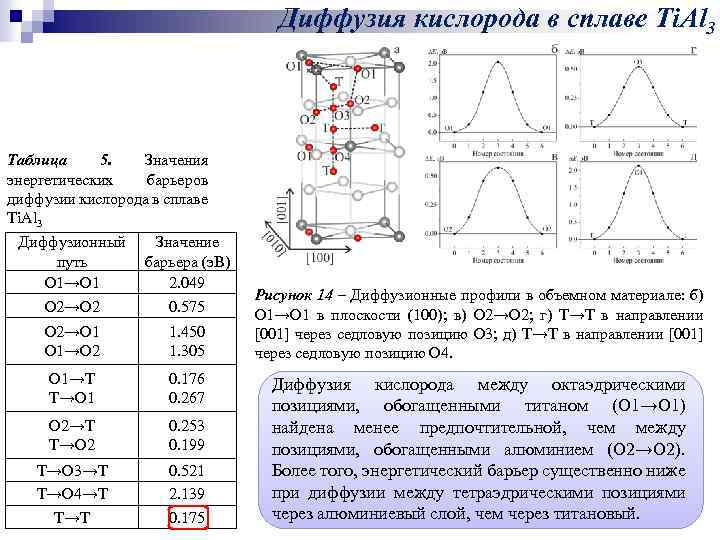 Диффузия кислорода в сплаве Ti. Al 3 Таблица 5. Значения энергетических барьеров диффузии кислорода в сплаве Ti. Al 3 Диффузионный путь O 1→O 1 O 2→O 2 Значение барьера (э. В) 2. 049 0. 575 O 2→O 1 O 1→O 2 1. 450 1. 305 O 1→T T→O 1 0. 176 0. 267 O 2→T T→O 2 0. 253 0. 199 T→O 3→Т T→O 4→T T→T 0. 521 2. 139 0. 175 Рисунок 14 – Диффузионные профили в объемном материале: б) О 1→О 1 в плоскости (100); в) О 2→О 2; г) Т→Т в направлении [001] через седловую позицию О 3; д) Т→Т в направлении [001] через седловую позицию О 4. Диффузия кислорода между октаэдрическими позициями, обогащенными титаном (О 1→О 1) найдена менее предпочтительной, чем между позициями, обогащенными алюминием (О 2→О 2). Более того, энергетический барьер существенно ниже при диффузии между тетраэдрическими позициями через алюминиевый слой, чем через титановый.
Диффузия кислорода в сплаве Ti. Al 3 Таблица 5. Значения энергетических барьеров диффузии кислорода в сплаве Ti. Al 3 Диффузионный путь O 1→O 1 O 2→O 2 Значение барьера (э. В) 2. 049 0. 575 O 2→O 1 O 1→O 2 1. 450 1. 305 O 1→T T→O 1 0. 176 0. 267 O 2→T T→O 2 0. 253 0. 199 T→O 3→Т T→O 4→T T→T 0. 521 2. 139 0. 175 Рисунок 14 – Диффузионные профили в объемном материале: б) О 1→О 1 в плоскости (100); в) О 2→О 2; г) Т→Т в направлении [001] через седловую позицию О 3; д) Т→Т в направлении [001] через седловую позицию О 4. Диффузия кислорода между октаэдрическими позициями, обогащенными титаном (О 1→О 1) найдена менее предпочтительной, чем между позициями, обогащенными алюминием (О 2→О 2). Более того, энергетический барьер существенно ниже при диффузии между тетраэдрическими позициями через алюминиевый слой, чем через титановый.
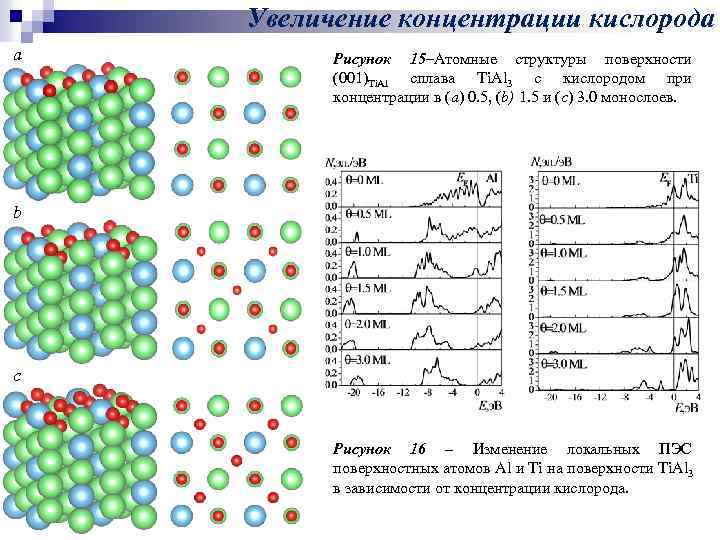 Увеличение концентрации кислорода a Рисунок 15–Атомные структуры поверхности (001)Ti. Al сплава Ti. Al 3 c кислородом при концентрации в (a) 0. 5, (b) 1. 5 и (c) 3. 0 монослоев. b c Рисунок 16 – Изменение локальных ПЭС поверхностных атомов Al и Ti на поверхности Ti. Al 3 в зависимости от концентрации кислорода.
Увеличение концентрации кислорода a Рисунок 15–Атомные структуры поверхности (001)Ti. Al сплава Ti. Al 3 c кислородом при концентрации в (a) 0. 5, (b) 1. 5 и (c) 3. 0 монослоев. b c Рисунок 16 – Изменение локальных ПЭС поверхностных атомов Al и Ti на поверхности Ti. Al 3 в зависимости от концентрации кислорода.
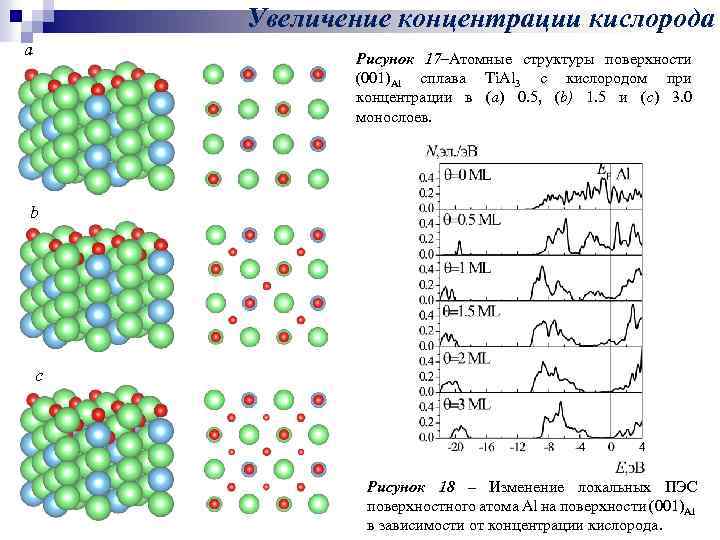 Увеличение концентрации кислорода a Рисунок 17–Атомные структуры поверхности (001)Al сплава Ti. Al 3 c кислородом при концентрации в (a) 0. 5, (b) 1. 5 и (c) 3. 0 монослоев. b c Рисунок 18 – Изменение локальных ПЭС поверхностного атома Al на поверхности (001)Al в зависимости от концентрации кислорода.
Увеличение концентрации кислорода a Рисунок 17–Атомные структуры поверхности (001)Al сплава Ti. Al 3 c кислородом при концентрации в (a) 0. 5, (b) 1. 5 и (c) 3. 0 монослоев. b c Рисунок 18 – Изменение локальных ПЭС поверхностного атома Al на поверхности (001)Al в зависимости от концентрации кислорода.
 Выводы Ø Показано, что независимо от окончании поверхности Ti. Al 3(001) адсорбция наиболее предпочтительна в HAlпозиции, что обусловлено более сильной гибридизацией s, pсостояний кислорода с орбиталями обоих металлов. Ø На поверхности (110) кислород предпочитает позицию короткого моста, тогда как на поверхности (100) наиболее выгодной также является мостиковая позиция между атомами титана и алюминия. Ø Показано, что диффузия кислорода наиболее предпочтительна между тетраэдрическими позициями в области между алюминиевым и смешанным слоем, в слое алюминия, а также через алюминиевый слой. Ø Написать про изменение концентрации кислорода на поверхности (001) 16
Выводы Ø Показано, что независимо от окончании поверхности Ti. Al 3(001) адсорбция наиболее предпочтительна в HAlпозиции, что обусловлено более сильной гибридизацией s, pсостояний кислорода с орбиталями обоих металлов. Ø На поверхности (110) кислород предпочитает позицию короткого моста, тогда как на поверхности (100) наиболее выгодной также является мостиковая позиция между атомами титана и алюминия. Ø Показано, что диффузия кислорода наиболее предпочтительна между тетраэдрическими позициями в области между алюминиевым и смешанным слоем, в слое алюминия, а также через алюминиевый слой. Ø Написать про изменение концентрации кислорода на поверхности (001) 16
 Спасибо за внимание!
Спасибо за внимание!
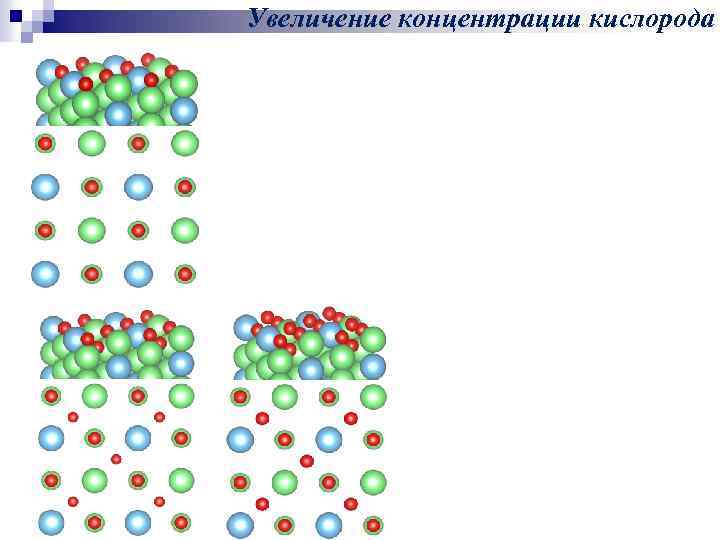 Увеличение концентрации кислорода
Увеличение концентрации кислорода


