Бакалавры_Металлурги 2014_весна_лекция 1.ppt
- Количество слайдов: 60
 Национальный исследовательский технологический университет «МИСи. С» МАТЕРИАЛОВЕДЕНИЕ Курс лекций для бакалавров-металлургов Лектор – доцент, к. ф. -м. н. Перминов Александр Сергеевич, кафедра физического материаловедения
Национальный исследовательский технологический университет «МИСи. С» МАТЕРИАЛОВЕДЕНИЕ Курс лекций для бакалавров-металлургов Лектор – доцент, к. ф. -м. н. Перминов Александр Сергеевич, кафедра физического материаловедения
 Материаловедение - наука о связи состава, строения и свойств материалов, их изменениях при механических, тепловых, химических и других видах воздействия. Металловедение - раздел материаловедения, рассматривающий металлические материалы
Материаловедение - наука о связи состава, строения и свойств материалов, их изменениях при механических, тепловых, химических и других видах воздействия. Металловедение - раздел материаловедения, рассматривающий металлические материалы
 ЗАДАЧИ КУРСА дать представление об основных закономерностях структурообразования в металлах и сплавах обучить основам формирования микроструктуры в сплавах научить выбору составов и режимов термической обработки сплавов научить прогнозировать структуру и свойства сплавов на основе представлений о фазовом равновесии и механизмах фазовых превращений
ЗАДАЧИ КУРСА дать представление об основных закономерностях структурообразования в металлах и сплавах обучить основам формирования микроструктуры в сплавах научить выбору составов и режимов термической обработки сплавов научить прогнозировать структуру и свойства сплавов на основе представлений о фазовом равновесии и механизмах фазовых превращений
 РАСПРЕДЕЛЕНИЕ УЧЕБНОГО ВРЕМЕНИ Семестр 1 Лекции 34 Лабораторные работы 17 Практические занятия 34 Самостоятельная работа 57 Семестровый контроль Экзамен
РАСПРЕДЕЛЕНИЕ УЧЕБНОГО ВРЕМЕНИ Семестр 1 Лекции 34 Лабораторные работы 17 Практические занятия 34 Самостоятельная работа 57 Семестровый контроль Экзамен
 ПРОГРАММА КУРСА • Тема 1 Основы строения и свойства материалов. • Тема 2 Фазовые превращения в металлических сплавах. (коллоквиум № 1) • Тема 3 Железо и сплавы на его основе. (коллоквиум № 2) • Тема 4 Основы термической обработки и поверхностного упрочнения сплавов. • Тема 5 Цветные металлы и сплавы • Тема 6 Неметаллические и композиционные материалы (контрольная работа № 1)
ПРОГРАММА КУРСА • Тема 1 Основы строения и свойства материалов. • Тема 2 Фазовые превращения в металлических сплавах. (коллоквиум № 1) • Тема 3 Железо и сплавы на его основе. (коллоквиум № 2) • Тема 4 Основы термической обработки и поверхностного упрочнения сплавов. • Тема 5 Цветные металлы и сплавы • Тема 6 Неметаллические и композиционные материалы (контрольная работа № 1)
 Основные учебники к курсу • Новиков И. И. , Строганов Г. Б. , Новиков А. И. Металловедение, термообработка и рентгенография. М. , МИСи. С, 1994, 479 с. • Новиков И. И. Теория термической обработки металлов. М. , Металлургия. 1986, 480 с.
Основные учебники к курсу • Новиков И. И. , Строганов Г. Б. , Новиков А. И. Металловедение, термообработка и рентгенография. М. , МИСи. С, 1994, 479 с. • Новиков И. И. Теория термической обработки металлов. М. , Металлургия. 1986, 480 с.
 Литература к практикуму • Микроструктура металлических сплавов. Лабораторный практикум. /Под ред. Р. И. Малинина и В. Ю. Введенского – М. , МИСи. С, Учеба, 2007, 198 С. № 1165 • Лилеев А. С. , Малютина Е. С. Фазовые равновесия и структурообразование. Двухкомпонентные диаграммы фазового равновесия. Сборник задач. – М. , МИСи. С, 2012. № 2197 • Малинина Р. И. , Шуваева Е. А, Ушакова О. Ю. , Перминов А. С. , Введенский В. Ю. Материаловедение. Сплавы Fe-C. Сборник задач. ‑ М. : «Издательский Дом МИСи. С» , 2013. № 2163 • Шуваева Е. А, Перминов А. С. Материаловедение: неметаллические и композиционные материалы: курс лекций. ‑ М. : «Издательский Дом МИСи. С» , 2013, 77 с. № 2162
Литература к практикуму • Микроструктура металлических сплавов. Лабораторный практикум. /Под ред. Р. И. Малинина и В. Ю. Введенского – М. , МИСи. С, Учеба, 2007, 198 С. № 1165 • Лилеев А. С. , Малютина Е. С. Фазовые равновесия и структурообразование. Двухкомпонентные диаграммы фазового равновесия. Сборник задач. – М. , МИСи. С, 2012. № 2197 • Малинина Р. И. , Шуваева Е. А, Ушакова О. Ю. , Перминов А. С. , Введенский В. Ю. Материаловедение. Сплавы Fe-C. Сборник задач. ‑ М. : «Издательский Дом МИСи. С» , 2013. № 2163 • Шуваева Е. А, Перминов А. С. Материаловедение: неметаллические и композиционные материалы: курс лекций. ‑ М. : «Издательский Дом МИСи. С» , 2013, 77 с. № 2162
 Дополнительные учебники к курсу • Лившиц Б. Г. Металлография. М. , Металлургия, 1990, 334 с. • Захаров А. М. Диаграммы состояния двойных и тройных систем. М. , Металлургия, 1990, 240 с.
Дополнительные учебники к курсу • Лившиц Б. Г. Металлография. М. , Металлургия, 1990, 334 с. • Захаров А. М. Диаграммы состояния двойных и тройных систем. М. , Металлургия, 1990, 240 с.
 СВЯЗЬ МАТЕРИАЛОВЕДЕНИЯ С ДРУГИМИ ПРЕДМЕТАМИ ФИЗИКА ФИЗИЧЕСКАЯ ХИМИЯ МАТЕРИАЛОВЕДЕНИЕ ХИМИЯ МЕТАЛЛУРГИЯ МАШИНОСТРОЕНИЕ
СВЯЗЬ МАТЕРИАЛОВЕДЕНИЯ С ДРУГИМИ ПРЕДМЕТАМИ ФИЗИКА ФИЗИЧЕСКАЯ ХИМИЯ МАТЕРИАЛОВЕДЕНИЕ ХИМИЯ МЕТАЛЛУРГИЯ МАШИНОСТРОЕНИЕ
 Тема 1 Структура металла § 1 Понятие структуры и её градации Структура – (от лат. строение, порядок, расположение) – совокупность устойчивых связей объекта, обеспечивающих его целостность и тождественность самому себе. [Большая Советская Энциклопедия] Структурирование - способ модельного описания чеголибо, посредством разделения на повторяющиеся структурные частисоставляющие, описание которых более просто
Тема 1 Структура металла § 1 Понятие структуры и её градации Структура – (от лат. строение, порядок, расположение) – совокупность устойчивых связей объекта, обеспечивающих его целостность и тождественность самому себе. [Большая Советская Энциклопедия] Структурирование - способ модельного описания чеголибо, посредством разделения на повторяющиеся структурные частисоставляющие, описание которых более просто
 Например, структура человека Она может иметь различные приближения – масштабы, уровни или градации: 1) Как состоящего из частей тела 2) Как состоящего из тканей 3) Как состоящего из клеток 4) Как состоящего из атомов
Например, структура человека Она может иметь различные приближения – масштабы, уровни или градации: 1) Как состоящего из частей тела 2) Как состоящего из тканей 3) Как состоящего из клеток 4) Как состоящего из атомов
 структура металлических тел 1 Макроструктура – структура, наблюдаемая невооруженным взглядом или при увеличении до 25 раз Фото сечения слитка сплава Pb-50%Sb (по массе) Высота слитка 2 см
структура металлических тел 1 Макроструктура – структура, наблюдаемая невооруженным взглядом или при увеличении до 25 раз Фото сечения слитка сплава Pb-50%Sb (по массе) Высота слитка 2 см
 структура металлических тел 2 Микроструктура – структура, наблюдаемая при металлографическом исследовании с помощью светового микроскопа, т. е. при увеличении до 1600 раз; Фото микроструктуры сплава Sb+30% Cu (по массе) УВЕЛИЧЕНО, Ø=0. 64 мм
структура металлических тел 2 Микроструктура – структура, наблюдаемая при металлографическом исследовании с помощью светового микроскопа, т. е. при увеличении до 1600 раз; Фото микроструктуры сплава Sb+30% Cu (по массе) УВЕЛИЧЕНО, Ø=0. 64 мм
 структура металлических тел 3 Атомнокристаллическая структура (чаще используют термин строение) – на изучении этого уровня мы остановимся далее подробнее
структура металлических тел 3 Атомнокристаллическая структура (чаще используют термин строение) – на изучении этого уровня мы остановимся далее подробнее
 структура металлических тел 4 Электронная структура – структура, изучающая особенности взаимодействие частиц сравнимых по размеру с электроном в веществе. Этот уровень и более глубокие уровни структуры в данном курсе мы изучать практически не будем
структура металлических тел 4 Электронная структура – структура, изучающая особенности взаимодействие частиц сравнимых по размеру с электроном в веществе. Этот уровень и более глубокие уровни структуры в данном курсе мы изучать практически не будем
 § 2 Атомно-кристаллическое строение твердых тел При описании атомнокристаллического строения твердое тело рассматривается как состоящее из атомов, которые уложены в параллелепипеды, которые многократно повторяются в пространстве. Вершины параллелепипедов совпадают с центрами атомов.
§ 2 Атомно-кристаллическое строение твердых тел При описании атомнокристаллического строения твердое тело рассматривается как состоящее из атомов, которые уложены в параллелепипеды, которые многократно повторяются в пространстве. Вершины параллелепипедов совпадают с центрами атомов.
 Пример
Пример
 ХАРАКТЕРИСТИКИ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ Пространственная решетка характеризуется элементарной Пространственная ячейкой – минимальным по объему параллелепипедом. Длины элементарной ячейки называются ребер элементарной называются периодами решетки. Элементарная ячейка в трехмерном пространстве характеризуется тремя периодами решетки – a, b, c и характеризуется тремя периодами решетки – a, и тремя углами: a – между и c; b – между ребрами a и c; g – тремя углами: ребрами b и c; b – между ребрами a и c; g между ребрами a и b. b. – между ребрами a и
ХАРАКТЕРИСТИКИ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ Пространственная решетка характеризуется элементарной Пространственная ячейкой – минимальным по объему параллелепипедом. Длины элементарной ячейки называются ребер элементарной называются периодами решетки. Элементарная ячейка в трехмерном пространстве характеризуется тремя периодами решетки – a, b, c и характеризуется тремя периодами решетки – a, и тремя углами: a – между и c; b – между ребрами a и c; g – тремя углами: ребрами b и c; b – между ребрами a и c; g между ребрами a и b. b. – между ребрами a и
 Элементарная ячейка
Элементарная ячейка
 Пример
Пример
 ТИПЫ КРИСТАЛЛИЧЕСКИХ РЕШЕТОК Пространственные решетки различных металлических материалов можно разделить на семь систем – сингоний, отличающихся соотношением величин сторон и углов Сингония Соотношение сторон Соотношение углов Кубическая а=b=с a=b=g=90 о Гексагональная а=b¹с a=b=90 о; g=120 о Тетрагональная а=b¹с a=b=g=90 о Тригональная (ромбоэдрическая) а=b=с a=b=g¹ 90 о Ромбическая а¹b¹с a=b=g=90 о Моноклинная а¹b¹с a=g=90 о; b¹ 90 о Триклинная а¹b¹с a¹b¹g¹ 90 о
ТИПЫ КРИСТАЛЛИЧЕСКИХ РЕШЕТОК Пространственные решетки различных металлических материалов можно разделить на семь систем – сингоний, отличающихся соотношением величин сторон и углов Сингония Соотношение сторон Соотношение углов Кубическая а=b=с a=b=g=90 о Гексагональная а=b¹с a=b=90 о; g=120 о Тетрагональная а=b¹с a=b=g=90 о Тригональная (ромбоэдрическая) а=b=с a=b=g¹ 90 о Ромбическая а¹b¹с a=b=g=90 о Моноклинная а¹b¹с a=g=90 о; b¹ 90 о Триклинная а¹b¹с a¹b¹g¹ 90 о
 Решетки Бравэ Помимо соотношения сторон и углов можно выделить четыре способа укладки атомов в элементарной ячейке или, как говорят, четыре типа решеток Браве. У примитивной решетки Браве (обозначается Р) атомы имеются только на вершинах параллелепипеда элементарной ячейки.
Решетки Бравэ Помимо соотношения сторон и углов можно выделить четыре способа укладки атомов в элементарной ячейке или, как говорят, четыре типа решеток Браве. У примитивной решетки Браве (обозначается Р) атомы имеются только на вершинах параллелепипеда элементарной ячейки.
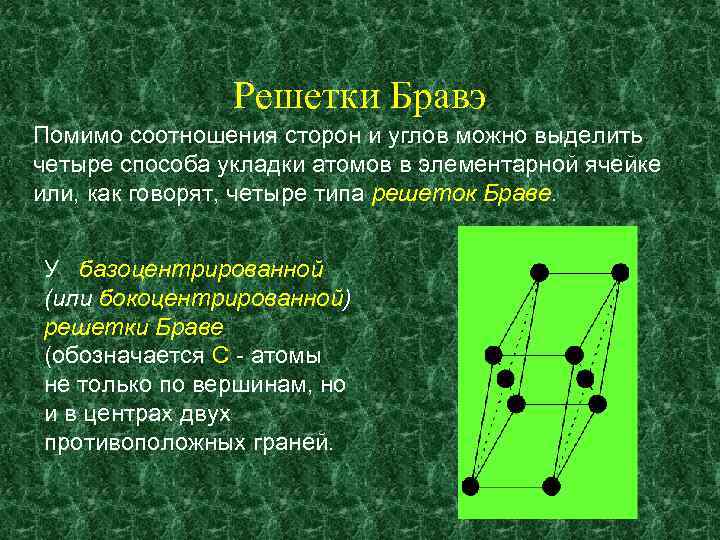 Решетки Бравэ Помимо соотношения сторон и углов можно выделить четыре способа укладки атомов в элементарной ячейке или, как говорят, четыре типа решеток Браве. У базоцентрированной (или бокоцентрированной) решетки Браве (обозначается С - атомы не только по вершинам, но и в центрах двух противоположных граней.
Решетки Бравэ Помимо соотношения сторон и углов можно выделить четыре способа укладки атомов в элементарной ячейке или, как говорят, четыре типа решеток Браве. У базоцентрированной (или бокоцентрированной) решетки Браве (обозначается С - атомы не только по вершинам, но и в центрах двух противоположных граней.
 Решетки Бравэ Помимо соотношения сторон и углов можно выделить четыре способа укладки атомов в элементарной ячейке или, как говорят, четыре типа решеток Браве. У объемноцентрированной решетки Браве (обозначается I) -кроме атомов по вершинам имеется атом в центре объема элементарной ячейки.
Решетки Бравэ Помимо соотношения сторон и углов можно выделить четыре способа укладки атомов в элементарной ячейке или, как говорят, четыре типа решеток Браве. У объемноцентрированной решетки Браве (обозначается I) -кроме атомов по вершинам имеется атом в центре объема элементарной ячейки.
 Решетки Бравэ Помимо соотношения сторон и углов можно выделить четыре способа укладки атомов в элементарной ячейке или, как говорят, четыре типа решеток Браве. У гранецентрированной решетки Браве (обозначается F) атомы по вершинам и в центре каждой грани элементарной ячейки.
Решетки Бравэ Помимо соотношения сторон и углов можно выделить четыре способа укладки атомов в элементарной ячейке или, как говорят, четыре типа решеток Браве. У гранецентрированной решетки Браве (обозначается F) атомы по вершинам и в центре каждой грани элементарной ячейки.
 Решетки Браве в 7 сингониях Тип решетки Браве Сингония Р Кубическая Гексагональная Тетрагональная Тригональная (ромбоэдрическая) Ромбическая Моноклинная Триклинная С + + + F + + + I + + + Итого 14 типов элементарной ячейки +
Решетки Браве в 7 сингониях Тип решетки Браве Сингония Р Кубическая Гексагональная Тетрагональная Тригональная (ромбоэдрическая) Ромбическая Моноклинная Триклинная С + + + F + + + I + + + Итого 14 типов элементарной ячейки +
 Комментарий: Элементарная ячейка – параллелепипед минимального объема. 14 типов решетки из 28 не используется, т. к. эти решетки можно описать параллелепипедом меньшего объема Например: тетрагональная базоцентрированная решетка может быть описана примитивной тетрагональной решеткой меньшего объема
Комментарий: Элементарная ячейка – параллелепипед минимального объема. 14 типов решетки из 28 не используется, т. к. эти решетки можно описать параллелепипедом меньшего объема Например: тетрагональная базоцентрированная решетка может быть описана примитивной тетрагональной решеткой меньшего объема
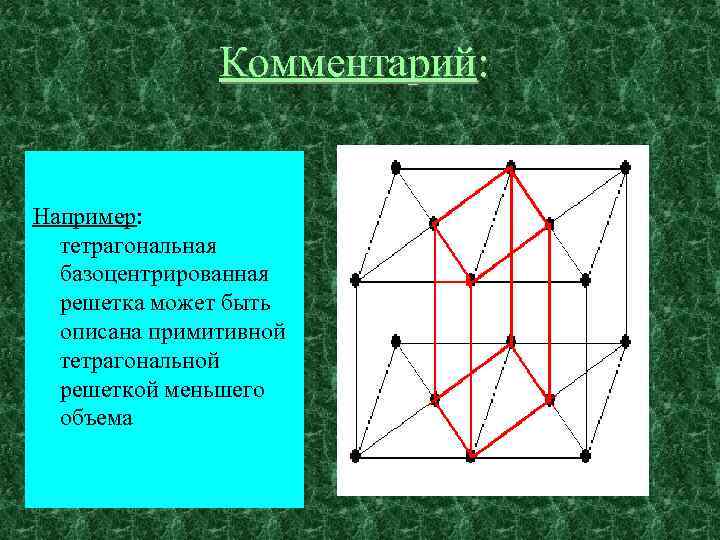 Комментарий: Например: тетрагональная базоцентрированная решетка может быть описана примитивной тетрагональной решеткой меньшего объема
Комментарий: Например: тетрагональная базоцентрированная решетка может быть описана примитивной тетрагональной решеткой меньшего объема
 Вывод Кристаллическое тело не монолитно имеет пустоты, причем количество пустот в различных направлениях различно, т. е. кристаллическое тело анизотропно, его характеристики и свойства различны в разных направлениях
Вывод Кристаллическое тело не монолитно имеет пустоты, причем количество пустот в различных направлениях различно, т. е. кристаллическое тело анизотропно, его характеристики и свойства различны в разных направлениях
 Внешняя огранка квазикристаллов Al-Cu-Fe ( и др. ) имеет ту же, т. е. икосаэдрическую симметрию Внешняя огранка кристаллов отражает их внутреннее строение (принцип Гаюи, 18 век)
Внешняя огранка квазикристаллов Al-Cu-Fe ( и др. ) имеет ту же, т. е. икосаэдрическую симметрию Внешняя огранка кристаллов отражает их внутреннее строение (принцип Гаюи, 18 век)
 § 3 Другие характеристики элементарной ячейки Кроме геометрических характеристик используются характеристики, отражающие уровень сил связи в решетки и плотность заполнения решетки веществом.
§ 3 Другие характеристики элементарной ячейки Кроме геометрических характеристик используются характеристики, отражающие уровень сил связи в решетки и плотность заполнения решетки веществом.
 Координационное число (КЧ) – число ближайших соседей, окружающих данный атом на равных расстояниях
Координационное число (КЧ) – число ближайших соседей, окружающих данный атом на равных расстояниях
 Для примитивной кубической решетки КЧ=6 Минимальное расстояние между атомами а
Для примитивной кубической решетки КЧ=6 Минимальное расстояние между атомами а
 Для ОЦКрешетки КЧ=8 Минимальное расстояние между атомами
Для ОЦКрешетки КЧ=8 Минимальное расстояние между атомами
 Для ГЦК-решетки КЧ=12 Минимальное расстояние между атомами
Для ГЦК-решетки КЧ=12 Минимальное расстояние между атомами
 Число атомов на ячейку (nяч) – число атомов в данной элементарной ячейке. При этом атом рассматривается как сфера
Число атомов на ячейку (nяч) – число атомов в данной элементарной ячейке. При этом атом рассматривается как сфера
 В примитивной кубической решетке на 1 ячейку приходится 1 атом 8 вершин ⅛ атома в вершине = 1
В примитивной кубической решетке на 1 ячейку приходится 1 атом 8 вершин ⅛ атома в вершине = 1
 В ОЦК-решетке на 1 ячейку приходится 2 атома 8 вершин ⅛ атома в вершине + 1 атом в центре = 2
В ОЦК-решетке на 1 ячейку приходится 2 атома 8 вершин ⅛ атома в вершине + 1 атом в центре = 2
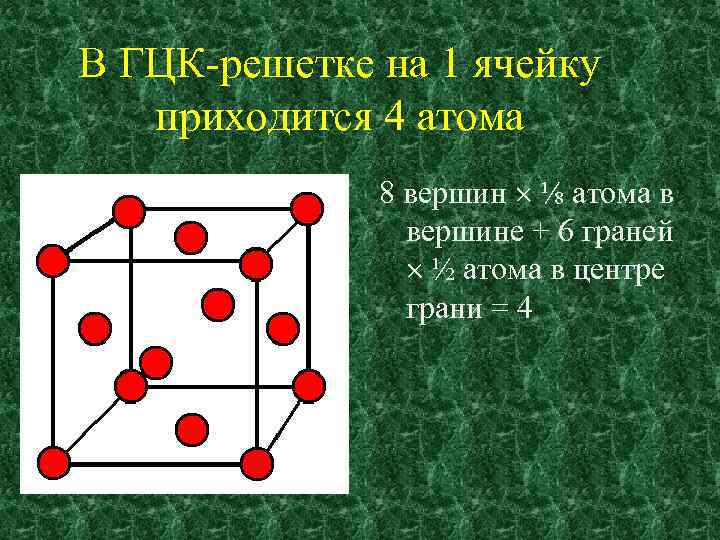 В ГЦК-решетке на 1 ячейку приходится 4 атома 8 вершин ⅛ атома в вершине + 6 граней ½ атома в центре грани = 4
В ГЦК-решетке на 1 ячейку приходится 4 атома 8 вершин ⅛ атома в вершине + 6 граней ½ атома в центре грани = 4
 Коэффициент заполнения решетки веществом ( ) – отношение суммарного объема атомов в элементарной ячейке к объему элементарной ячейки, выраженное в процентах =
Коэффициент заполнения решетки веществом ( ) – отношение суммарного объема атомов в элементарной ячейке к объему элементарной ячейки, выраженное в процентах =
 Коэффициент заполнения решетки веществом в примитивной кубической решетке В примитивной решетке атомы плотнее всего располагаются по ребрам куба, причем параметр решетки а равен 2 радиусам атома a = 2 r Тогда = =52%
Коэффициент заполнения решетки веществом в примитивной кубической решетке В примитивной решетке атомы плотнее всего располагаются по ребрам куба, причем параметр решетки а равен 2 радиусам атома a = 2 r Тогда = =52%
 Коэффициент заполнения решетки веществом в ОЦК решетке В ОЦК решетке атомы плотнее всего располагаются по диагонали куба, которая проходит через 3 атома. Параметр решетки а можно оценить по длине диагонали куба, которая равна 4 радиусам атома Тогда = a = 4 r =68%
Коэффициент заполнения решетки веществом в ОЦК решетке В ОЦК решетке атомы плотнее всего располагаются по диагонали куба, которая проходит через 3 атома. Параметр решетки а можно оценить по длине диагонали куба, которая равна 4 радиусам атома Тогда = a = 4 r =68%
 Коэффициент заполнения решетки веществом в ГЦК решетке В ГЦК решетке атомы плотнее всего располагаются по диагонали грани куба, которая проходит через 3 атома. Параметр решетки а можно оценить по длине диагонали грани куба, которая равна 4 радиусам атома Тогда = a = 4 r =74%
Коэффициент заполнения решетки веществом в ГЦК решетке В ГЦК решетке атомы плотнее всего располагаются по диагонали грани куба, которая проходит через 3 атома. Параметр решетки а можно оценить по длине диагонали грани куба, которая равна 4 радиусам атома Тогда = a = 4 r =74%
 СРАВНЕНИЕ ХАРАКТЕРИСТИК ЭЛЕМЕНТАРНЫХ ЯЧЕЕК КУБИЧЕСКОЙ СИНГОНИИ Примитивная Тип решетки кубическая ОЦК ГЦК КЧ 6 8 12 nяч 1 2 4 , % 52 68 74
СРАВНЕНИЕ ХАРАКТЕРИСТИК ЭЛЕМЕНТАРНЫХ ЯЧЕЕК КУБИЧЕСКОЙ СИНГОНИИ Примитивная Тип решетки кубическая ОЦК ГЦК КЧ 6 8 12 nяч 1 2 4 , % 52 68 74
 § 4 Поры в решетке В кристаллических решетках существуют пустоты или как их называют – поры. Поры играют существенную роль в формировании свойств кристаллического тела: – т. к. являются местом расположения примесных атомов. – движение атомов по порам – один из путей диффузии Различают тетрапоры и октапоры.
§ 4 Поры в решетке В кристаллических решетках существуют пустоты или как их называют – поры. Поры играют существенную роль в формировании свойств кристаллического тела: – т. к. являются местом расположения примесных атомов. – движение атомов по порам – один из путей диффузии Различают тетрапоры и октапоры.
 Тетрапора – пустота между 4 атомами, уложенными в тетраэдр Пример – тетрапора на грани ОЦК решетки
Тетрапора – пустота между 4 атомами, уложенными в тетраэдр Пример – тетрапора на грани ОЦК решетки
 Октапора – пустота между шестью атомами, уложенными в октаэдр Пример – октапора на грани ОЦК решетки
Октапора – пустота между шестью атомами, уложенными в октаэдр Пример – октапора на грани ОЦК решетки
 § 5 Индицирование – наиболее удобный способ описания пространственного расположения плоскостей и направлений путем приписывании им определенных индексов Различают индексы направлений и плоскостей
§ 5 Индицирование – наиболее удобный способ описания пространственного расположения плоскостей и направлений путем приписывании им определенных индексов Различают индексы направлений и плоскостей
 Индексы плоскостей • В случае плоскости за индексы принимаются три числа h, k, l, равные обратным величинам отрезков, отсекаемых данной плоскостью (hkl) на осях x, y, z, умноженные на общий коэффициент, приводящий все числа h, k, l к целым и простым числам • Для обозначения плоскостей пользуются обозначением (hkl) – для одной плоскости; и {hkl} – для семейства эквивалентных по структуре плоскостей.
Индексы плоскостей • В случае плоскости за индексы принимаются три числа h, k, l, равные обратным величинам отрезков, отсекаемых данной плоскостью (hkl) на осях x, y, z, умноженные на общий коэффициент, приводящий все числа h, k, l к целым и простым числам • Для обозначения плоскостей пользуются обозначением (hkl) – для одной плоскости; и {hkl} – для семейства эквивалентных по структуре плоскостей.
 Индексы плоскостей а) (323); б) (320)
Индексы плоскостей а) (323); б) (320)
 Семейство плоскостей В кристаллах можно выделить несколько непараллельных, но полностью идентичных кристаллографических плоскостей с одинаковым расположением атомов. Совокупность таких плоскостей называют семейством и обозначают {hkl}.
Семейство плоскостей В кристаллах можно выделить несколько непараллельных, но полностью идентичных кристаллографических плоскостей с одинаковым расположением атомов. Совокупность таких плоскостей называют семейством и обозначают {hkl}.
 Семейство плоскостей Самым простым примером является грань куба – во всех трех гранях куба, различающихся по пространственной ориентации и перпендикулярных другу, атомы расположены одинаково. В семейство плоскостей {100} входят плоскости (100), (010), (001).
Семейство плоскостей Самым простым примером является грань куба – во всех трех гранях куба, различающихся по пространственной ориентации и перпендикулярных другу, атомы расположены одинаково. В семейство плоскостей {100} входят плоскости (100), (010), (001).
 Семейство плоскостей В семейство плоскостей {110} входит шесть плоскостей – (110), (101), (011), которые проходят через диагонали граней куба.
Семейство плоскостей В семейство плоскостей {110} входит шесть плоскостей – (110), (101), (011), которые проходят через диагонали граней куба.
![Индексы направлений • За индексы направления [uvw] принимаются координаты атома, через который из начала Индексы направлений • За индексы направления [uvw] принимаются координаты атома, через который из начала](https://present5.com/presentation/-42583223_280053664/image-54.jpg) Индексы направлений • За индексы направления [uvw] принимаются координаты атома, через который из начала координат проходит это направление, приведенные к трем наименьшим целым числам делением на общий делитель • Аналогично семейству плоскостей существует и семейство направлений – в семейство направлений
Индексы направлений • За индексы направления [uvw] принимаются координаты атома, через который из начала координат проходит это направление, приведенные к трем наименьшим целым числам делением на общий делитель • Аналогично семейству плоскостей существует и семейство направлений – в семейство направлений
![Индексы направлений примеры индицирования направлений в двумерном случае [31] Индексы направлений примеры индицирования направлений в двумерном случае [31]](https://present5.com/presentation/-42583223_280053664/image-55.jpg) Индексы направлений примеры индицирования направлений в двумерном случае [31]
Индексы направлений примеры индицирования направлений в двумерном случае [31]
![Семейство направлений В семейство направлений <uvw> входят все направления [uvw] c одинаковым расположением атомов Семейство направлений В семейство направлений <uvw> входят все направления [uvw] c одинаковым расположением атомов](https://present5.com/presentation/-42583223_280053664/image-56.jpg) Семейство направлений В семейство направлений
Семейство направлений В семейство направлений
 Примеры
Примеры
 Плотноупакованные направления и плоскости Обратим внимание на тот факт, что расстояние между атомами в направлениях, принадлежащих разным семействам, существенно различаются. Так в случае примитивной кубической решетки для направлений <100> оно равно а, для направлений <110> - a , для направлений <111> - a. Расположение атомов в плоскостях с разными индексами различно.
Плотноупакованные направления и плоскости Обратим внимание на тот факт, что расстояние между атомами в направлениях, принадлежащих разным семействам, существенно различаются. Так в случае примитивной кубической решетки для направлений <100> оно равно а, для направлений <110> - a , для направлений <111> - a. Расположение атомов в плоскостях с разными индексами различно.
 Плотноупакованные направления и плоскости в кубической сингонии Решетка Кубическая примитивная ОЦК ГЦК Плоскость {100} {111} Направление <100> <111> <110>
Плотноупакованные направления и плоскости в кубической сингонии Решетка Кубическая примитивная ОЦК ГЦК Плоскость {100} {111} Направление <100> <111> <110>
 Анизотропия кристаллической решетки Так как в разных направлениях расстояние между атомами различается, следовательно, различается и уровень сил связей между атомами в различных направлениях. Это означает, что и свойства кристаллического тела вдоль различных направлений (с разным расстоянием между атомами) будут различаться. Это явление различия свойств вдоль различных направлений получило название анизотропии свойств
Анизотропия кристаллической решетки Так как в разных направлениях расстояние между атомами различается, следовательно, различается и уровень сил связей между атомами в различных направлениях. Это означает, что и свойства кристаллического тела вдоль различных направлений (с разным расстоянием между атомами) будут различаться. Это явление различия свойств вдоль различных направлений получило название анизотропии свойств


