 На рукомойнике моём Позеленела медь, Но так играет луч на нём, Что весело глядеть.
На рукомойнике моём Позеленела медь, Но так играет луч на нём, Что весело глядеть.
 От латинского “Corrosion” – разъедать, разрушать. Коррозия – это процесс перехода металла в то природное, естественное состояние, в котором мы встречаем его в земной коре»
От латинского “Corrosion” – разъедать, разрушать. Коррозия – это процесс перехода металла в то природное, естественное состояние, в котором мы встречаем его в земной коре»
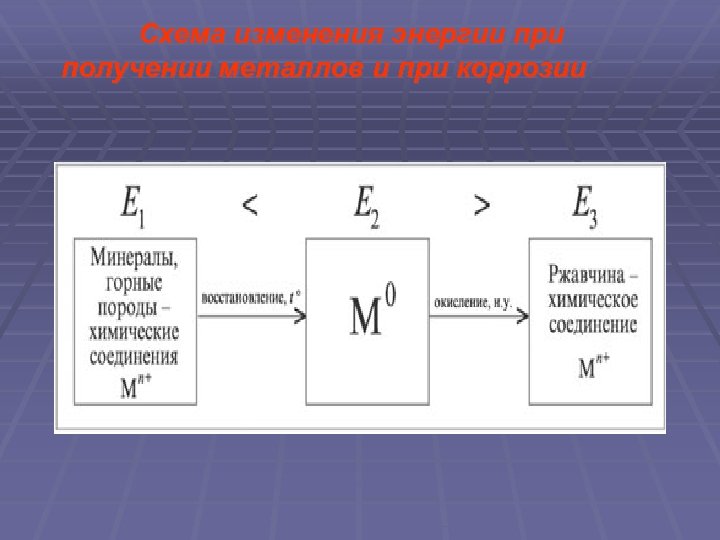 Схема изменения энергии при получении металлов и при коррозии
Схема изменения энергии при получении металлов и при коррозии
 Процессы катодного восстановления Среда Кислотная (p. H<7) Щелочная или нейтральная (p. H>7) При отсутствии кислорода в электролите В присутствии кислорода в электролите
Процессы катодного восстановления Среда Кислотная (p. H<7) Щелочная или нейтральная (p. H>7) При отсутствии кислорода в электролите В присутствии кислорода в электролите
 Задача 1. а) какие вещества образуются при повреждении листов оцинкованного железа во влажном атмосферном воздухе? Приведите электронные и молекулярные уравнения протекающих процессов. б) какие вещества образуются при коррозии луженого оловом железа при повреждени покрытия в морской воде?
Задача 1. а) какие вещества образуются при повреждении листов оцинкованного железа во влажном атмосферном воздухе? Приведите электронные и молекулярные уравнения протекающих процессов. б) какие вещества образуются при коррозии луженого оловом железа при повреждени покрытия в морской воде?
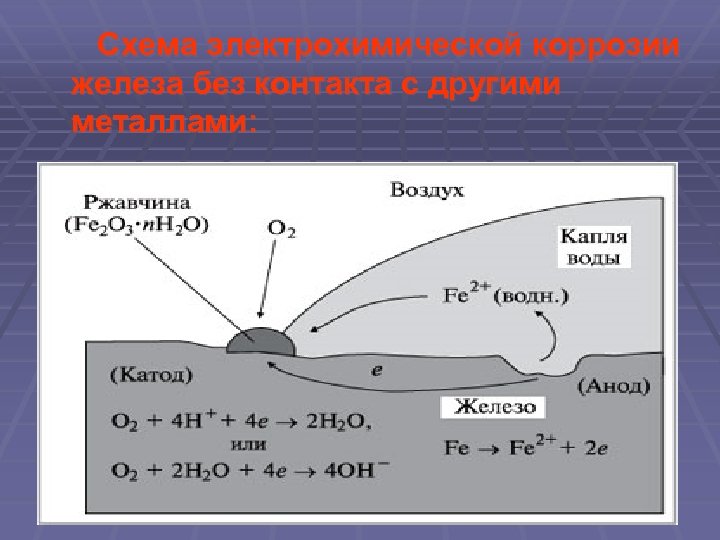 Схема электрохимической коррозии железа без контакта с другими металлами:
Схема электрохимической коррозии железа без контакта с другими металлами:
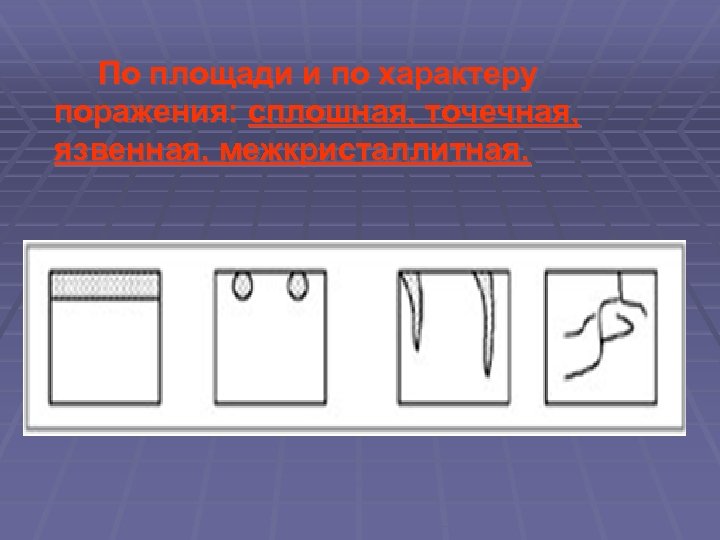 По площади и по характеру поражения: сплошная, точечная, язвенная, межкристаллитная.
По площади и по характеру поражения: сплошная, точечная, язвенная, межкристаллитная.
 Межкристаллитная коррозия: (для хромистых и хромовоникелевых сталей, никелевые и алюминиевые сплавы)
Межкристаллитная коррозия: (для хромистых и хромовоникелевых сталей, никелевые и алюминиевые сплавы)
 Кутубская колонна в Дели. Метеоритное железо
Кутубская колонна в Дели. Метеоритное железо
 Скорость электрохимической коррозии зависит: 1) От природы электролита (в щелочной среде, где p. H > 9 -10 железо не корродирует) 2) От разности активности металлов, образующих гальванические пары. 3) От природы примесей в металле 4) От температуры, с увеличением температуры скорость коррозии увеличивается.
Скорость электрохимической коррозии зависит: 1) От природы электролита (в щелочной среде, где p. H > 9 -10 железо не корродирует) 2) От разности активности металлов, образующих гальванические пары. 3) От природы примесей в металле 4) От температуры, с увеличением температуры скорость коррозии увеличивается.
 Сульфовосстанавливающие анаэробные бактерии из рода Desulfovibrio.
Сульфовосстанавливающие анаэробные бактерии из рода Desulfovibrio.
 Физкульминутка
Физкульминутка
 Задание 2 Будет ли защищена железная конструкция от электрохимической коррозии в воде, если на ней укрепить пластинку из другого металла: а) магния; б) свинца; в) никеля?
Задание 2 Будет ли защищена железная конструкция от электрохимической коррозии в воде, если на ней укрепить пластинку из другого металла: а) магния; б) свинца; в) никеля?
 Задание 4. Человек поставил на зуб золотую коронку, по истечении некоторого времени возникла необходимость в ещё одной коронке. Возможен ли вариант, чтобы поставить на зуб стальную коронку?
Задание 4. Человек поставил на зуб золотую коронку, по истечении некоторого времени возникла необходимость в ещё одной коронке. Возможен ли вариант, чтобы поставить на зуб стальную коронку?
 Задание 3. Почему цинк не используют при изготовлении консервных банок для покрытия им железа, а используют олово.
Задание 3. Почему цинк не используют при изготовлении консервных банок для покрытия им железа, а используют олово.
 - Что такое коррозия? Каковы причины коррозии? Какие виды коррозии бывают? От каких факторов зависит скорость коррозии? Перечислите основные способы защиты металлов от коррозии? Где можно использовать процессы коррозии?
- Что такое коррозия? Каковы причины коррозии? Какие виды коррозии бывают? От каких факторов зависит скорость коррозии? Перечислите основные способы защиты металлов от коррозии? Где можно использовать процессы коррозии?
 1. Склепаны два металла. Укажите, какой из металлов подвергается коррозии: а) Mn – Al ; б) Sn – Cu. 2. Какие из нижеперечисленных металлов выполняют для свинца роль анодного покрытия: Pt, Al, Cu, Hg ? 3. Какие из нижеперечисленных металлов выполняют для свинца роль катодного покрытия: Zn, Mn, Ag, Cr ?
1. Склепаны два металла. Укажите, какой из металлов подвергается коррозии: а) Mn – Al ; б) Sn – Cu. 2. Какие из нижеперечисленных металлов выполняют для свинца роль анодного покрытия: Pt, Al, Cu, Hg ? 3. Какие из нижеперечисленных металлов выполняют для свинца роль катодного покрытия: Zn, Mn, Ag, Cr ?
 На дом: Стр. 259, задачи 16, 17, 20. Подготовить сообщение о вкладе русских учёных в формирование электрохимической теории коррозии металлов.
На дом: Стр. 259, задачи 16, 17, 20. Подготовить сообщение о вкладе русских учёных в формирование электрохимической теории коррозии металлов.