Лекция по органике_7.ppt
- Количество слайдов: 46
 На предыдущей лекции…
На предыдущей лекции…
 Электрофильное присоединение по Марковникову Получается только вещество А. Фактором, определяющим направление присоединения, является устойчивость промежуточного карбокатиона, в стабилизации которого участвуют алкильные или арильные заместители. Чем устойчивее катион, тем ниже его энергия и, следовательно, тем легче он образуется.
Электрофильное присоединение по Марковникову Получается только вещество А. Фактором, определяющим направление присоединения, является устойчивость промежуточного карбокатиона, в стабилизации которого участвуют алкильные или арильные заместители. Чем устойчивее катион, тем ниже его энергия и, следовательно, тем легче он образуется.
 Пероксидный эффект Хараша В присутствии пероксидов присоединение бромистого водорода к алкенам идет против правила Марковникова. Из двух радикалов А и Б в основном образуется первый, как более устойчивый. Аналогично электрофильному, радикальное присоединение к алкенам протекает через стадию образования наиболее стабильного радикала.
Пероксидный эффект Хараша В присутствии пероксидов присоединение бромистого водорода к алкенам идет против правила Марковникова. Из двух радикалов А и Б в основном образуется первый, как более устойчивый. Аналогично электрофильному, радикальное присоединение к алкенам протекает через стадию образования наиболее стабильного радикала.
 Электрофильное замещение в ароматических системах Лекция 7
Электрофильное замещение в ароматических системах Лекция 7
 Качественные реакции на ненасыщенность для алкенов и алкинов 1) Обесцвечивание бромной воды 2) Обесцвечивание раствора перманганата калия (реакция Вагнера): 3 CH 2 = CH 2 + 2 КМn. О 4 + 4 H 2 О 3 НОCH 2 - CH 2 ОН + Мn. О 2↓+ 2 КОН Для аренов не характерны реакции присоединения, свойственные алкенам и алкинам
Качественные реакции на ненасыщенность для алкенов и алкинов 1) Обесцвечивание бромной воды 2) Обесцвечивание раствора перманганата калия (реакция Вагнера): 3 CH 2 = CH 2 + 2 КМn. О 4 + 4 H 2 О 3 НОCH 2 - CH 2 ОН + Мn. О 2↓+ 2 КОН Для аренов не характерны реакции присоединения, свойственные алкенам и алкинам
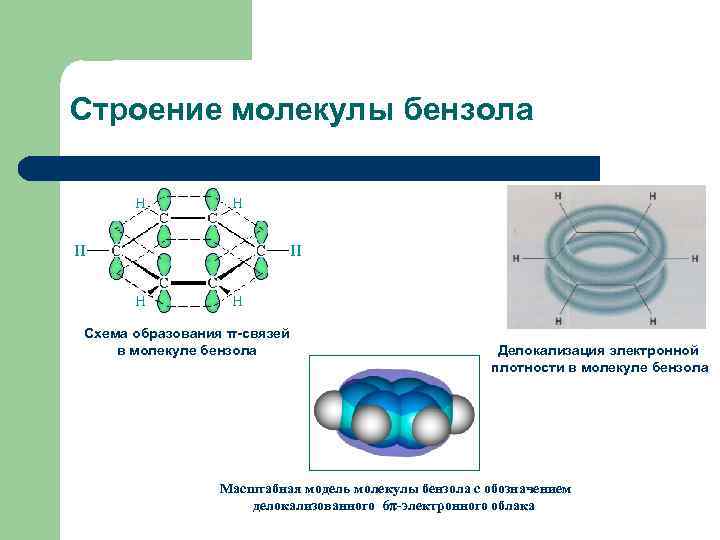 Строение молекулы бензола Схема образования π-связей в молекуле бензола Делокализация электронной плотности в молекуле бензола Масштабная модель молекулы бензола с обозначением делокализованного 6 -электронного облака
Строение молекулы бензола Схема образования π-связей в молекуле бензола Делокализация электронной плотности в молекуле бензола Масштабная модель молекулы бензола с обозначением делокализованного 6 -электронного облака
 Арены и алкены: действие электрофилов Для ароматических соединений характерные реакции электрофильного замещения (SE) + +
Арены и алкены: действие электрофилов Для ароматических соединений характерные реакции электрофильного замещения (SE) + +
 Электрофилы + Электрофильные реагенты (Е, Е ) – это частицы, образующие новые ковалентные связи за счет пары электронов партнера - положительно заряженные ионы H+ Hal+ протон NO 2+ галоген-катионы нитроил-катион NO+ нитрозил-катион карбокатион - нейтральные молекулы, имеющие электронодефицитный центр δ+ Х Х – группа с – I- и/или – М-эффектом SO 3 BF 3, BCl 3, Fe. Br 3, Al. Cl 3 Триоксид серы Кислоты Льюиса
Электрофилы + Электрофильные реагенты (Е, Е ) – это частицы, образующие новые ковалентные связи за счет пары электронов партнера - положительно заряженные ионы H+ Hal+ протон NO 2+ галоген-катионы нитроил-катион NO+ нитрозил-катион карбокатион - нейтральные молекулы, имеющие электронодефицитный центр δ+ Х Х – группа с – I- и/или – М-эффектом SO 3 BF 3, BCl 3, Fe. Br 3, Al. Cl 3 Триоксид серы Кислоты Льюиса
 Сила электрофилов 1. 1. Сильные электрофилы NO 2+(Ион нитрония, нитроил-катион); комплексы Cl 2 или Br 2 с различными кислотами Льюиса (Fe. Cl 3, Al. Br 3, Al. Cl 3, Sb. Cl 5 и т. д. ); H 2 OCl + , H 2 OBr + , RSO 2+ , HSO 3+ , H 2 S 2 O 7. 1. 2. Электрофилы средней силы Комплексы алкилгалогенидов или ацилгалогенидов с кислотами Льюиса (RCl·Al. Cl 3, RBr·Ga. Br 3, RCOCl·Al. Cl 3 и др. ); комплексы спиртов с сильными кислотами Льюиса и Бренстеда (ROH·BF 3, ROH·H 3 PO 4, ROH·HF). 1. 3. Слабые электрофилы Катионы диазония Ar. NN+, иминия CH 2=N+H 2, нитрозония NO+ (нитрозоил-катион); оксид углерода (IV) СО 2 (один из самых слабых электрофилов).
Сила электрофилов 1. 1. Сильные электрофилы NO 2+(Ион нитрония, нитроил-катион); комплексы Cl 2 или Br 2 с различными кислотами Льюиса (Fe. Cl 3, Al. Br 3, Al. Cl 3, Sb. Cl 5 и т. д. ); H 2 OCl + , H 2 OBr + , RSO 2+ , HSO 3+ , H 2 S 2 O 7. 1. 2. Электрофилы средней силы Комплексы алкилгалогенидов или ацилгалогенидов с кислотами Льюиса (RCl·Al. Cl 3, RBr·Ga. Br 3, RCOCl·Al. Cl 3 и др. ); комплексы спиртов с сильными кислотами Льюиса и Бренстеда (ROH·BF 3, ROH·H 3 PO 4, ROH·HF). 1. 3. Слабые электрофилы Катионы диазония Ar. NN+, иминия CH 2=N+H 2, нитрозония NO+ (нитрозоил-катион); оксид углерода (IV) СО 2 (один из самых слабых электрофилов).
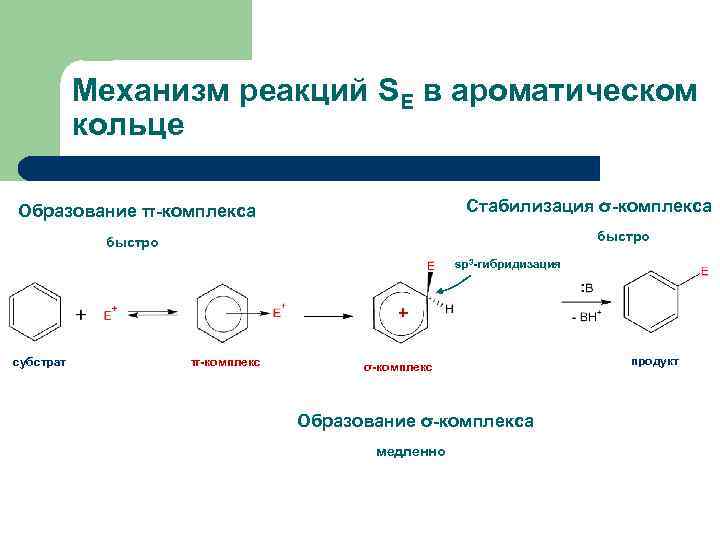 Механизм реакций SE в ароматическом кольце Стабилизация σ-комплекса Образование π-комплекса быстро sp 3 -гибридизация + субстрат π-комплекс σ-комплекс Образование σ-комплекса медленно продукт
Механизм реакций SE в ароматическом кольце Стабилизация σ-комплекса Образование π-комплекса быстро sp 3 -гибридизация + субстрат π-комплекс σ-комплекс Образование σ-комплекса медленно продукт
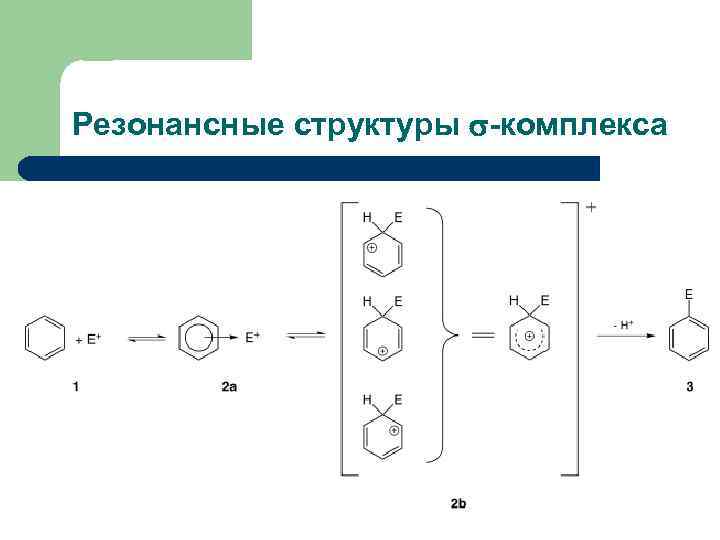 Резонансные структуры -комплекса
Резонансные структуры -комплекса
![Энергетическая диаграмма реакции SE в ароматическом кольце V = k[Ar. H][E+] Реакция второго порядка Энергетическая диаграмма реакции SE в ароматическом кольце V = k[Ar. H][E+] Реакция второго порядка](https://present5.com/presentation/3/-76738116_378809809.pdf-img/-76738116_378809809.pdf-12.jpg) Энергетическая диаграмма реакции SE в ароматическом кольце V = k[Ar. H][E+] Реакция второго порядка
Энергетическая диаграмма реакции SE в ароматическом кольце V = k[Ar. H][E+] Реакция второго порядка
 Устойчивость аренониевых ионов Устойчивость -комплексов растет при наличии в ароматическом ядре электронодонорных заместителей, участвующих в делокализации положительного заряда, а также при наличии комплексных противоионов типа BF 4 - или Sb. F 6 - (слабые основания). Мезитилен образует аренониевый ион при взаимодействии с HF в присутствии BF 3, устойчивый до -30 о. С. Этот -комплекс имеет желтую окраску и полностью разлагается на исходные компоненты уже при -15 о. С. При использовании в качестве кислоты Льюиса Sb. F 5 образуется соль с противоионом Sb. F 6 -, которая более стабильна и не разлагается даже при +50 о. С.
Устойчивость аренониевых ионов Устойчивость -комплексов растет при наличии в ароматическом ядре электронодонорных заместителей, участвующих в делокализации положительного заряда, а также при наличии комплексных противоионов типа BF 4 - или Sb. F 6 - (слабые основания). Мезитилен образует аренониевый ион при взаимодействии с HF в присутствии BF 3, устойчивый до -30 о. С. Этот -комплекс имеет желтую окраску и полностью разлагается на исходные компоненты уже при -15 о. С. При использовании в качестве кислоты Льюиса Sb. F 5 образуется соль с противоионом Sb. F 6 -, которая более стабильна и не разлагается даже при +50 о. С.
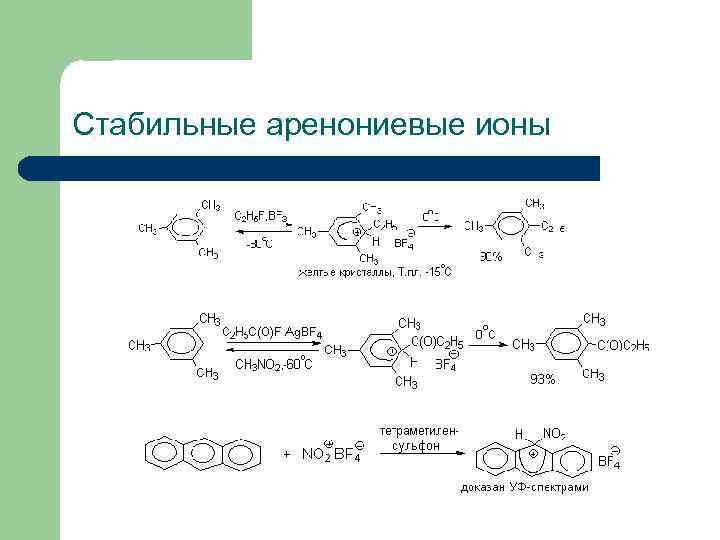 Стабильные аренониевые ионы
Стабильные аренониевые ионы
 Влияние строения субстрата на SE 1) Как заместитель в бензольном кольце влияет на скорость SE в целом? 2) Как заместитель в бензольном кольце влияет на направление атаки электрофильного агента (региоспецифичность реакций SE)?
Влияние строения субстрата на SE 1) Как заместитель в бензольном кольце влияет на скорость SE в целом? 2) Как заместитель в бензольном кольце влияет на направление атаки электрофильного агента (региоспецифичность реакций SE)?
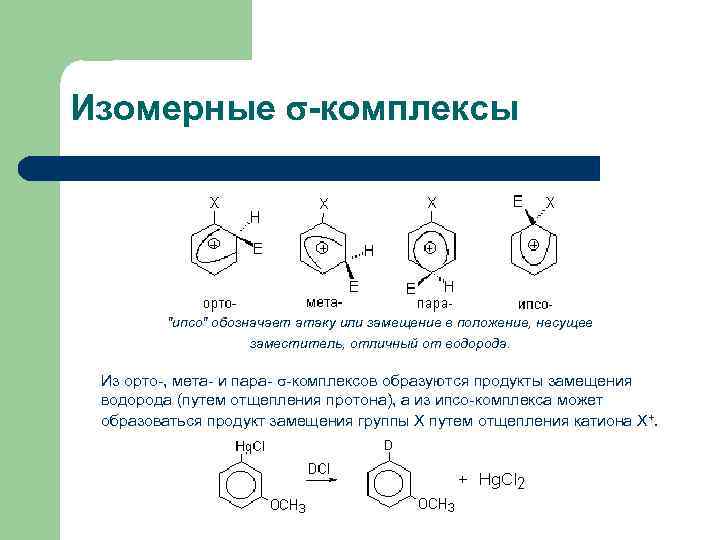 Изомерные -комплексы "ипсо" обозначает атаку или замещение в положение, несущее заместитель, отличный от водорода. Из орто-, мета- и пара- -комплексов образуются продукты замещения водорода (путем отщепления протона), а из ипсо-комплекса может образоваться продукт замещения группы Х путем отщепления катиона Х+.
Изомерные -комплексы "ипсо" обозначает атаку или замещение в положение, несущее заместитель, отличный от водорода. Из орто-, мета- и пара- -комплексов образуются продукты замещения водорода (путем отщепления протона), а из ипсо-комплекса может образоваться продукт замещения группы Х путем отщепления катиона Х+.
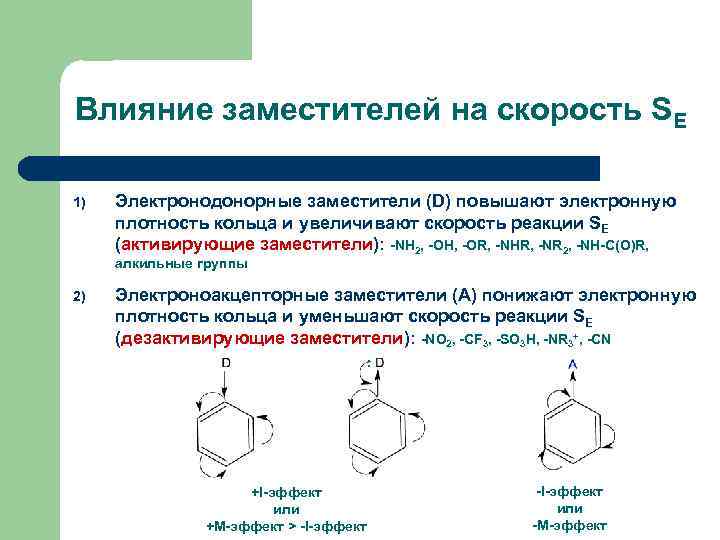 Влияние заместителей на скорость SE 1) Электронодонорные заместители (D) повышают электронную плотность кольца и увеличивают скорость реакции SE (активирующие заместители): -NH 2, -OH, -OR, -NHR, -NR 2, -NH-C(O)R, алкильные группы 2) Электроноакцепторные заместители (А) понижают электронную плотность кольца и уменьшают скорость реакции SE (дезактивирующие заместители): -NO 2, -CF 3, -SO 3 H, -NR 3+, -CN : +I-эффект или +М-эффект > -I-эффект или -М-эффект
Влияние заместителей на скорость SE 1) Электронодонорные заместители (D) повышают электронную плотность кольца и увеличивают скорость реакции SE (активирующие заместители): -NH 2, -OH, -OR, -NHR, -NR 2, -NH-C(O)R, алкильные группы 2) Электроноакцепторные заместители (А) понижают электронную плотность кольца и уменьшают скорость реакции SE (дезактивирующие заместители): -NO 2, -CF 3, -SO 3 H, -NR 3+, -CN : +I-эффект или +М-эффект > -I-эффект или -М-эффект
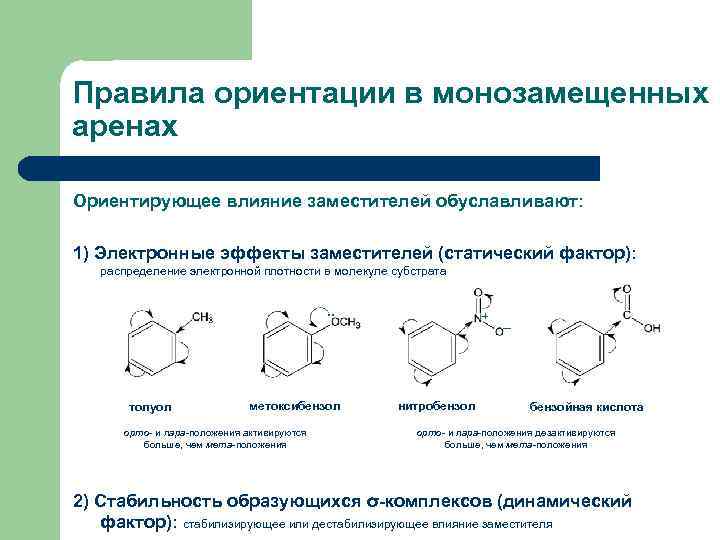 Правила ориентации в монозамещенных аренах Ориентирующее влияние заместителей обуславливают: 1) Электронные эффекты заместителей (статический фактор): распределение электронной плотности в молекуле субстрата . . толуол метоксибензол орто- и пара-положения активируются больше, чем мета-положения + нитробензол _ бензойная кислота орто- и пара-положения дезактивируются больше, чем мета-положения 2) Стабильность образующихся σ-комплексов (динамический фактор): стабилизирующее или дестабилизирующее влияние заместителя
Правила ориентации в монозамещенных аренах Ориентирующее влияние заместителей обуславливают: 1) Электронные эффекты заместителей (статический фактор): распределение электронной плотности в молекуле субстрата . . толуол метоксибензол орто- и пара-положения активируются больше, чем мета-положения + нитробензол _ бензойная кислота орто- и пара-положения дезактивируются больше, чем мета-положения 2) Стабильность образующихся σ-комплексов (динамический фактор): стабилизирующее или дестабилизирующее влияние заместителя
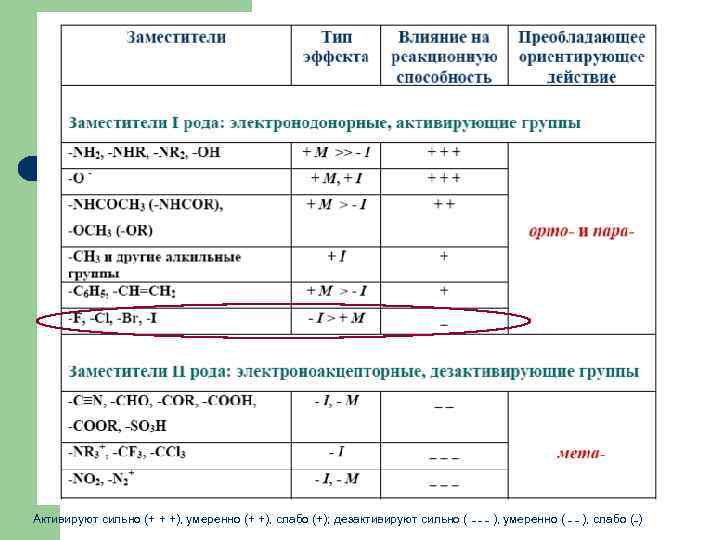 Активируют сильно (+ + +), умеренно (+ +), слабо (+); дезактивируют сильно ( _ _ _ ), умеренно ( _ _ ), слабо (_)
Активируют сильно (+ + +), умеренно (+ +), слабо (+); дезактивируют сильно ( _ _ _ ), умеренно ( _ _ ), слабо (_)
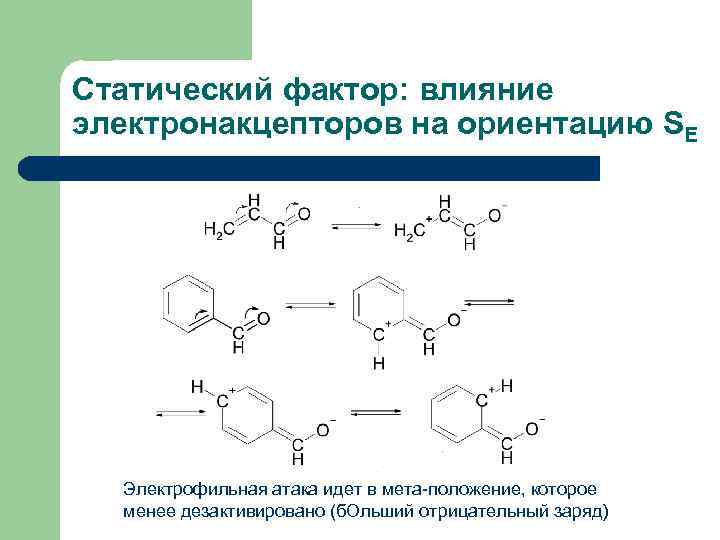 Статический фактор: влияние электронакцепторов на ориентацию SE Электрофильная атака идет в мета-положение, которое менее дезактивировано (б. Ольший отрицательный заряд)
Статический фактор: влияние электронакцепторов на ориентацию SE Электрофильная атака идет в мета-положение, которое менее дезактивировано (б. Ольший отрицательный заряд)
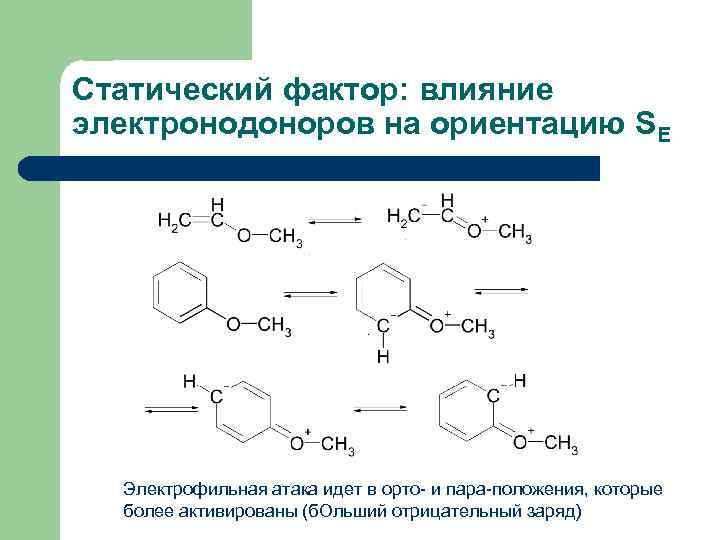 Статический фактор: влияние электронодоноров на ориентацию SE Электрофильная атака идет в орто- и пара-положения, которые более активированы (б. Ольший отрицательный заряд)
Статический фактор: влияние электронодоноров на ориентацию SE Электрофильная атака идет в орто- и пара-положения, которые более активированы (б. Ольший отрицательный заряд)
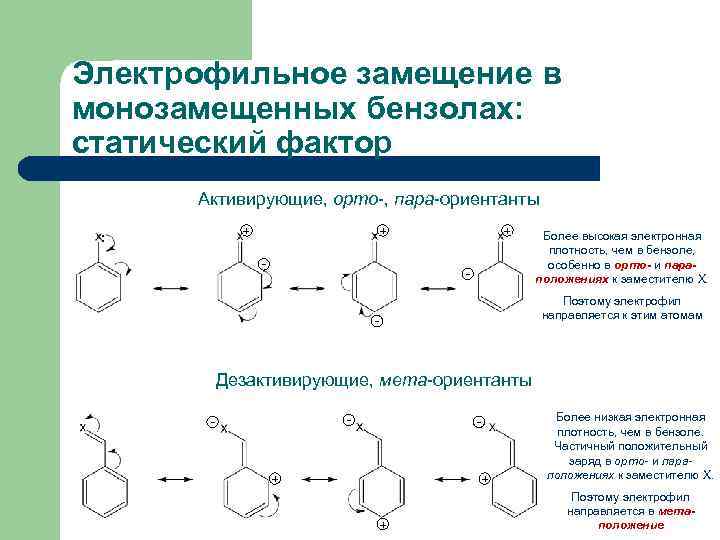 Электрофильное замещение в монозамещенных бензолах: статический фактор Активирующие, орто-, пара-ориентанты + : + - Более высокая электронная плотность, чем в бензоле, особенно в орто- и параположениях к заместителю Х. Поэтому электрофил направляется к этим атомам - Дезактивирующие, мета-ориентанты - - - + + + Более низкая электронная плотность, чем в бензоле. Частичный положительный заряд в орто- и параположениях к заместителю Х. Поэтому электрофил направляется в метаположение
Электрофильное замещение в монозамещенных бензолах: статический фактор Активирующие, орто-, пара-ориентанты + : + - Более высокая электронная плотность, чем в бензоле, особенно в орто- и параположениях к заместителю Х. Поэтому электрофил направляется к этим атомам - Дезактивирующие, мета-ориентанты - - - + + + Более низкая электронная плотность, чем в бензоле. Частичный положительный заряд в орто- и параположениях к заместителю Х. Поэтому электрофил направляется в метаположение
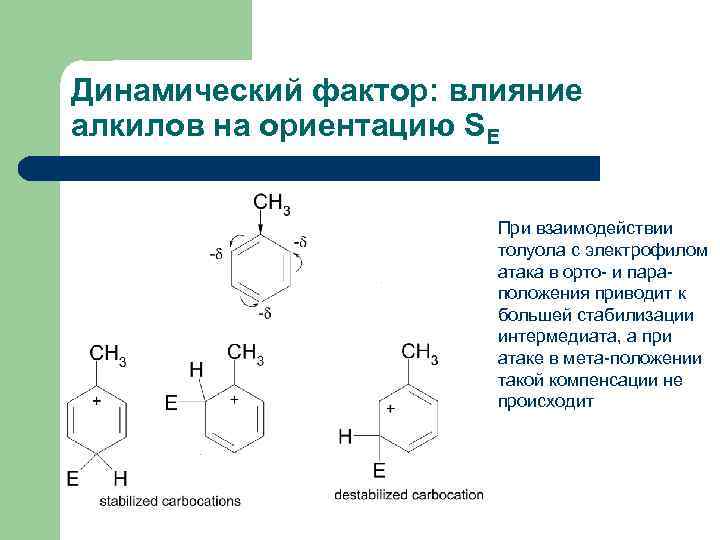 Динамический фактор: влияние алкилов на ориентацию SE При взаимодействии толуола с электрофилом атака в орто- и параположения приводит к большей стабилизации интермедиата, а при атаке в мета-положении такой компенсации не происходит
Динамический фактор: влияние алкилов на ориентацию SE При взаимодействии толуола с электрофилом атака в орто- и параположения приводит к большей стабилизации интермедиата, а при атаке в мета-положении такой компенсации не происходит
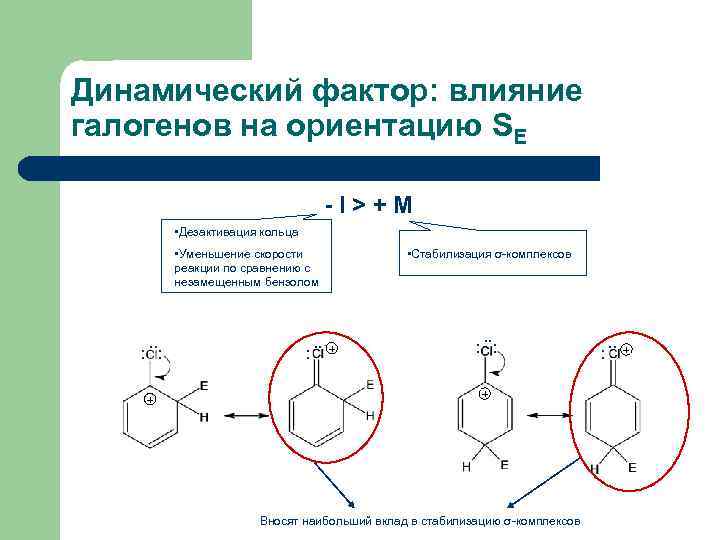 Динамический фактор: влияние галогенов на ориентацию SE - I > + M • Дезактивация кольца • Уменьшение скорости реакции по сравнению с незамещенным бензолом . . : : + : . . + • Стабилизация σ-комплексов . . : : + Вносят наибольший вклад в стабилизацию σ-комплексов : . . +
Динамический фактор: влияние галогенов на ориентацию SE - I > + M • Дезактивация кольца • Уменьшение скорости реакции по сравнению с незамещенным бензолом . . : : + : . . + • Стабилизация σ-комплексов . . : : + Вносят наибольший вклад в стабилизацию σ-комплексов : . . +
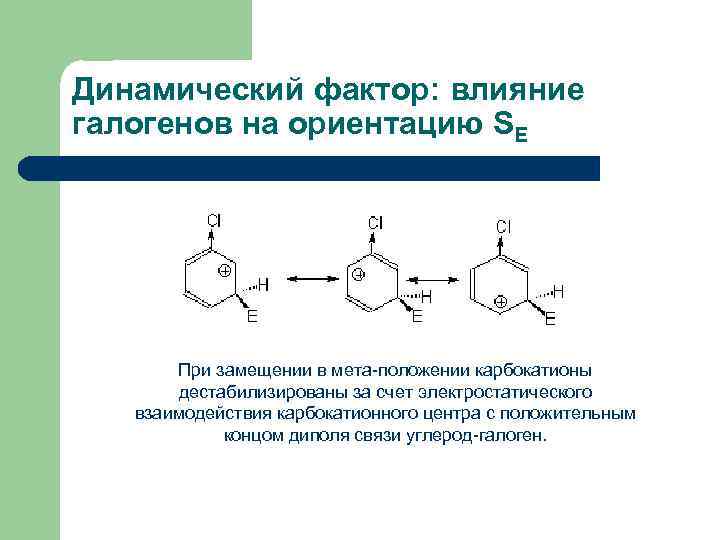 Динамический фактор: влияние галогенов на ориентацию SE При замещении в мета-положении карбокатионы дестабилизированы за счет электростатического взаимодействия карбокатионного центра с положительным концом диполя связи углерод-галоген.
Динамический фактор: влияние галогенов на ориентацию SE При замещении в мета-положении карбокатионы дестабилизированы за счет электростатического взаимодействия карбокатионного центра с положительным концом диполя связи углерод-галоген.
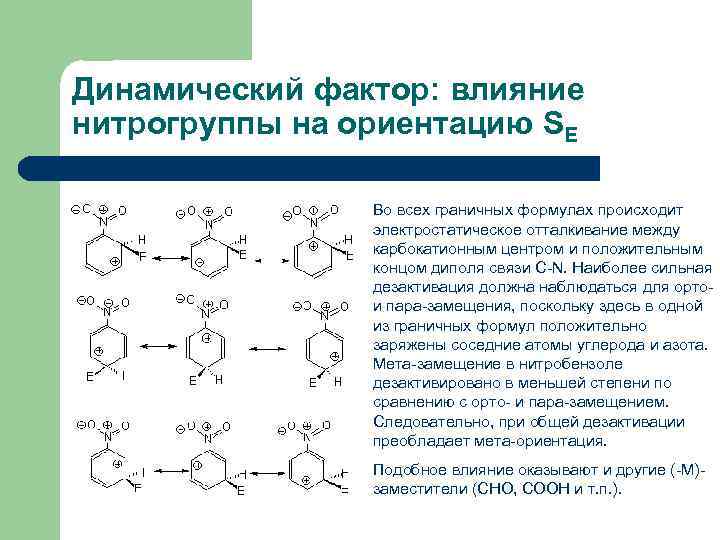 Динамический фактор: влияние нитрогруппы на ориентацию SE Во всех граничных формулах происходит электростатическое отталкивание между карбокатионным центром и положительным концом диполя связи С-N. Наиболее сильная дезактивация должна наблюдаться для орто- и пара-замещения, поскольку здесь в одной из граничных формул положительно заряжены соседние атомы углерода и азота. Мета-замещение в нитробензоле дезактивировано в меньшей степени по сравнению с орто- и пара-замещением. Следовательно, при общей дезактивации преобладает мета-ориентация. Подобное влияние оказывают и другие (-М)заместители (СНО, СООН и т. п. ).
Динамический фактор: влияние нитрогруппы на ориентацию SE Во всех граничных формулах происходит электростатическое отталкивание между карбокатионным центром и положительным концом диполя связи С-N. Наиболее сильная дезактивация должна наблюдаться для орто- и пара-замещения, поскольку здесь в одной из граничных формул положительно заряжены соседние атомы углерода и азота. Мета-замещение в нитробензоле дезактивировано в меньшей степени по сравнению с орто- и пара-замещением. Следовательно, при общей дезактивации преобладает мета-ориентация. Подобное влияние оказывают и другие (-М)заместители (СНО, СООН и т. п. ).
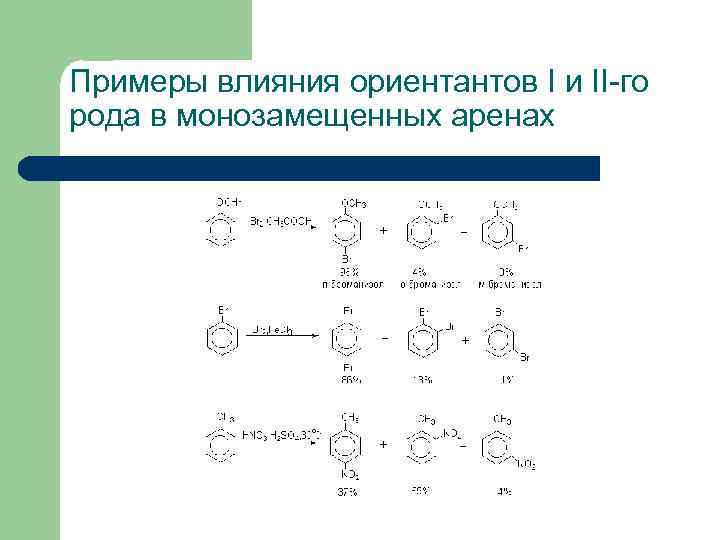 Примеры влияния ориентантов I и II-го рода в монозамещенных аренах
Примеры влияния ориентантов I и II-го рода в монозамещенных аренах
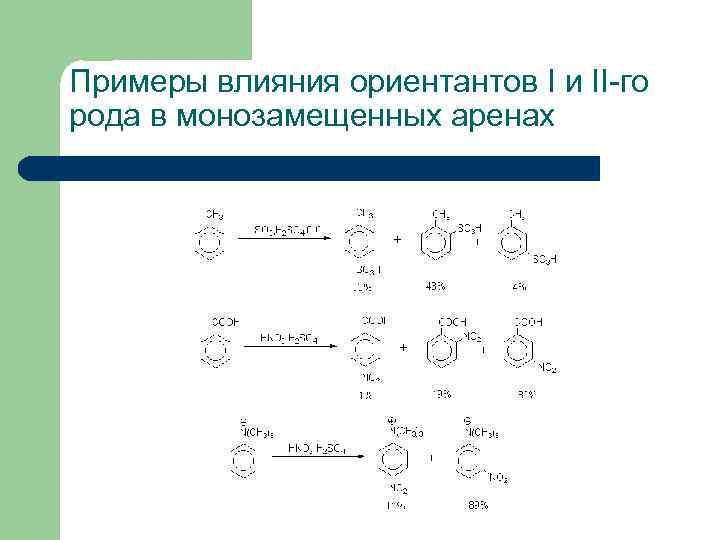 Примеры влияния ориентантов I и II-го рода в монозамещенных аренах
Примеры влияния ориентантов I и II-го рода в монозамещенных аренах
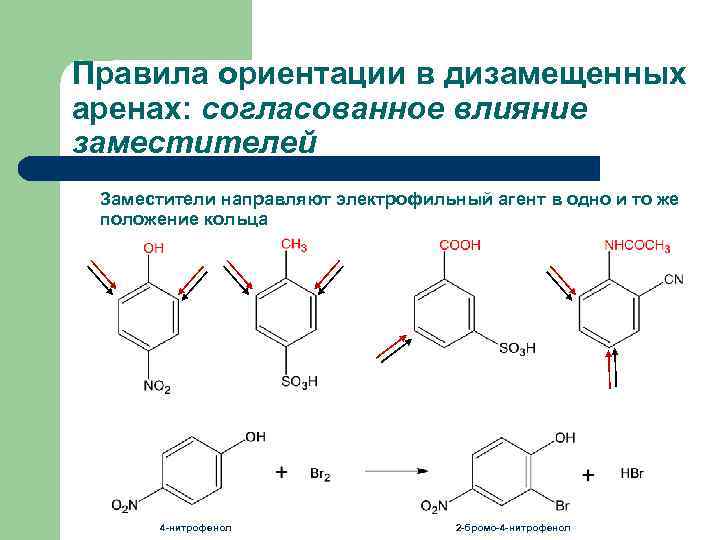 Правила ориентации в дизамещенных аренах: согласованное влияние заместителей Заместители направляют электрофильный агент в одно и то же положение кольца 4 -нитрофенол 2 -бромо-4 -нитрофенол
Правила ориентации в дизамещенных аренах: согласованное влияние заместителей Заместители направляют электрофильный агент в одно и то же положение кольца 4 -нитрофенол 2 -бромо-4 -нитрофенол
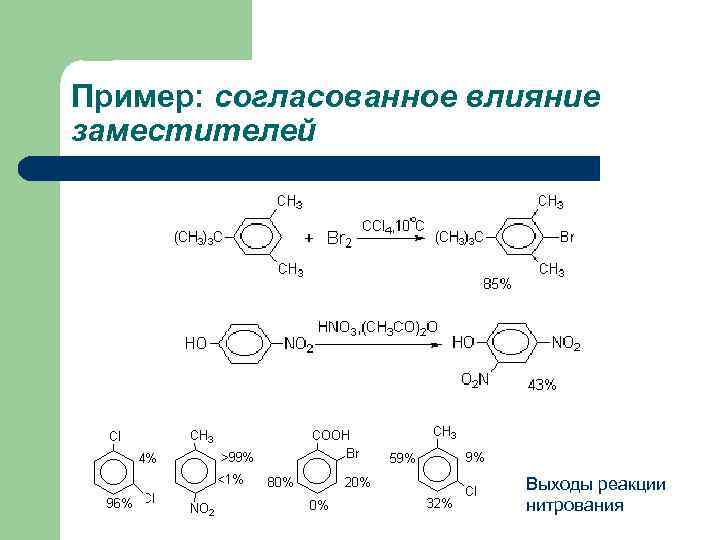 Пример: согласованное влияние заместителей Выходы реакции нитрования
Пример: согласованное влияние заместителей Выходы реакции нитрования
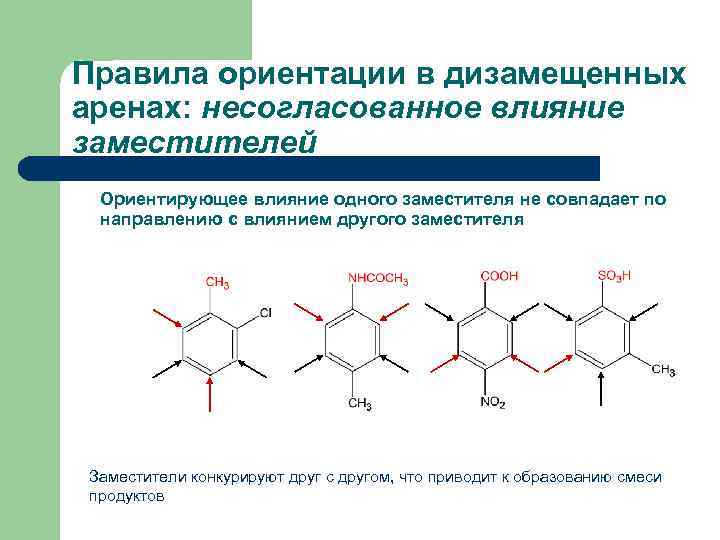 Правила ориентации в дизамещенных аренах: несогласованное влияние заместителей Ориентирующее влияние одного заместителя не совпадает по направлению с влиянием другого заместителя Заместители конкурируют друг с другом, что приводит к образованию смеси продуктов
Правила ориентации в дизамещенных аренах: несогласованное влияние заместителей Ориентирующее влияние одного заместителя не совпадает по направлению с влиянием другого заместителя Заместители конкурируют друг с другом, что приводит к образованию смеси продуктов
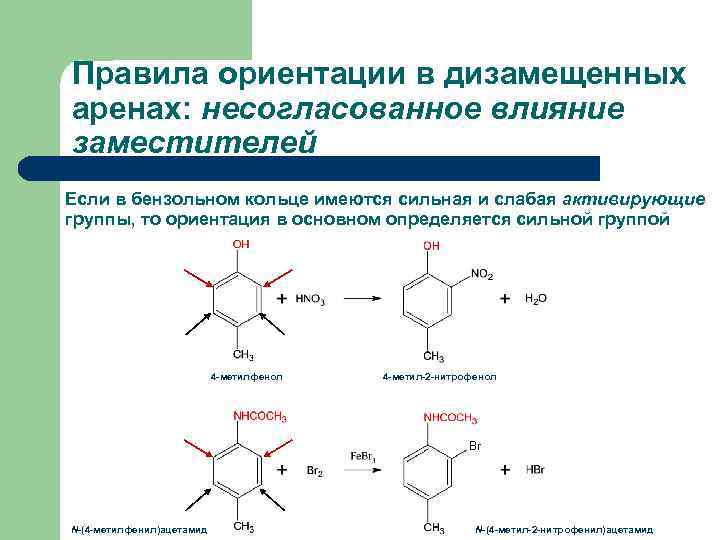 Правила ориентации в дизамещенных аренах: несогласованное влияние заместителей Если в бензольном кольце имеются сильная и слабая активирующие группы, то ориентация в основном определяется сильной группой 4 -метилфенол 4 -метил-2 -нитрофенол Br N-(4 -метилфенил)ацетамид N-(4 -метил-2 -нитрофенил)ацетамид
Правила ориентации в дизамещенных аренах: несогласованное влияние заместителей Если в бензольном кольце имеются сильная и слабая активирующие группы, то ориентация в основном определяется сильной группой 4 -метилфенол 4 -метил-2 -нитрофенол Br N-(4 -метилфенил)ацетамид N-(4 -метил-2 -нитрофенил)ацетамид
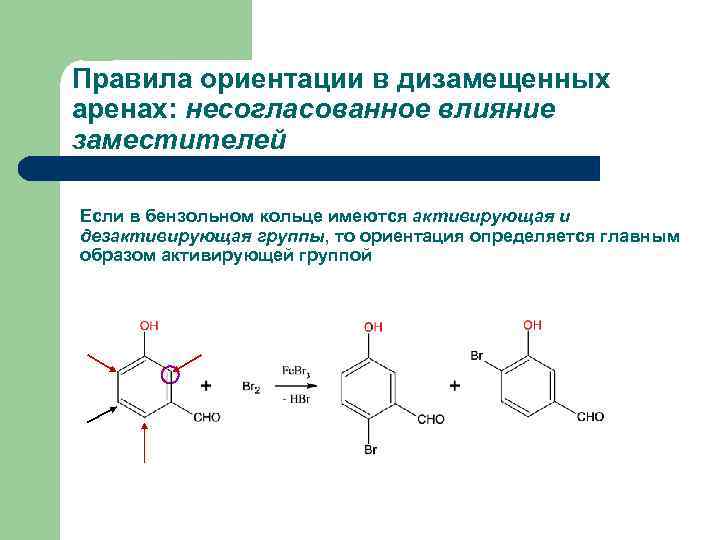 Правила ориентации в дизамещенных аренах: несогласованное влияние заместителей Если в бензольном кольце имеются активирующая и дезактивирующая группы, то ориентация определяется главным образом активирующей группой
Правила ориентации в дизамещенных аренах: несогласованное влияние заместителей Если в бензольном кольце имеются активирующая и дезактивирующая группы, то ориентация определяется главным образом активирующей группой
 Реакции электрофильного замещения (SE) аренов 1) Галогенирование 2) Нитрование 3) Сульфирование 4) Алкилирование 5) Ацилирование
Реакции электрофильного замещения (SE) аренов 1) Галогенирование 2) Нитрование 3) Сульфирование 4) Алкилирование 5) Ацилирование
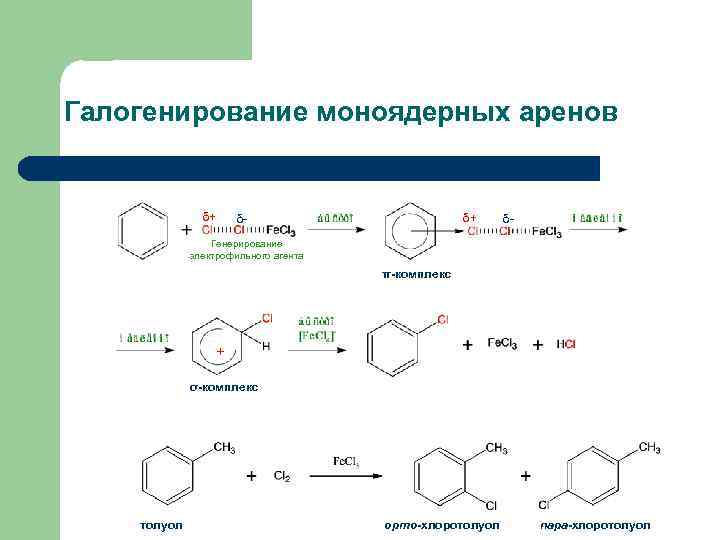 Галогенирование моноядерных аренов δ+ δ+ δ- δ- Генерирование электрофильного агента π-комплекс + σ-комплекс толуол орто-хлоротолуол пара-хлоротолуол
Галогенирование моноядерных аренов δ+ δ+ δ- δ- Генерирование электрофильного агента π-комплекс + σ-комплекс толуол орто-хлоротолуол пара-хлоротолуол
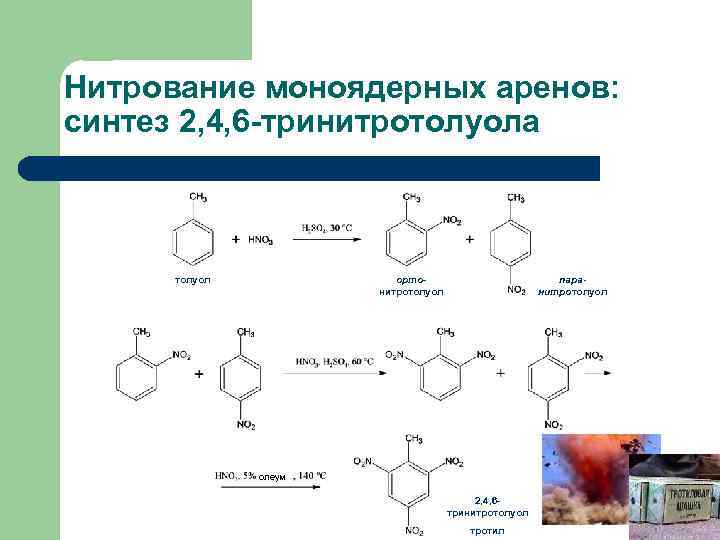 Нитрование моноядерных аренов: синтез 2, 4, 6 -тринитротолуола толуол ортонитротолуол паранитротолуол олеум 2, 4, 6 тринитротолуол тротил
Нитрование моноядерных аренов: синтез 2, 4, 6 -тринитротолуола толуол ортонитротолуол паранитротолуол олеум 2, 4, 6 тринитротолуол тротил
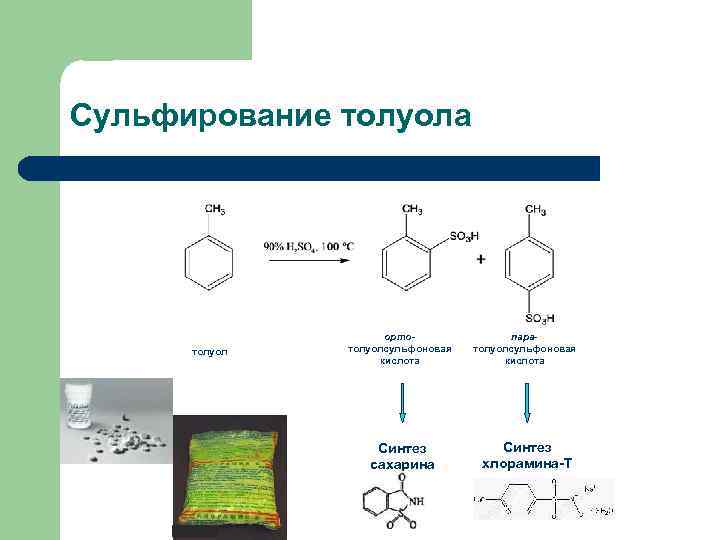 Сульфирование толуола толуол ортотолуолсульфоновая кислота паратолуолсульфоновая кислота Синтез сахарина Синтез хлорамина-Т
Сульфирование толуола толуол ортотолуолсульфоновая кислота паратолуолсульфоновая кислота Синтез сахарина Синтез хлорамина-Т
 Реакция Фриделя-Крафтса Введение в бензольное кольцо алкильных или ацильных групп Алкилирующие реагенты: галогеноалканы, алкены, спирты Ацилирующие реагенты: хлорангидриды и ангидриды кислот Осуществляется в присутствии кислот Льюиса Синтез: l l Поверхностно-активных веществ Душистых веществ Этилбензола этилбензол Кумола, тимола стирол Ароматических кетонов (промежуточные продукты в производстве фармацевтических препаратов и красителей) l кетон Михлера кумол
Реакция Фриделя-Крафтса Введение в бензольное кольцо алкильных или ацильных групп Алкилирующие реагенты: галогеноалканы, алкены, спирты Ацилирующие реагенты: хлорангидриды и ангидриды кислот Осуществляется в присутствии кислот Льюиса Синтез: l l Поверхностно-активных веществ Душистых веществ Этилбензола этилбензол Кумола, тимола стирол Ароматических кетонов (промежуточные продукты в производстве фармацевтических препаратов и красителей) l кетон Михлера кумол
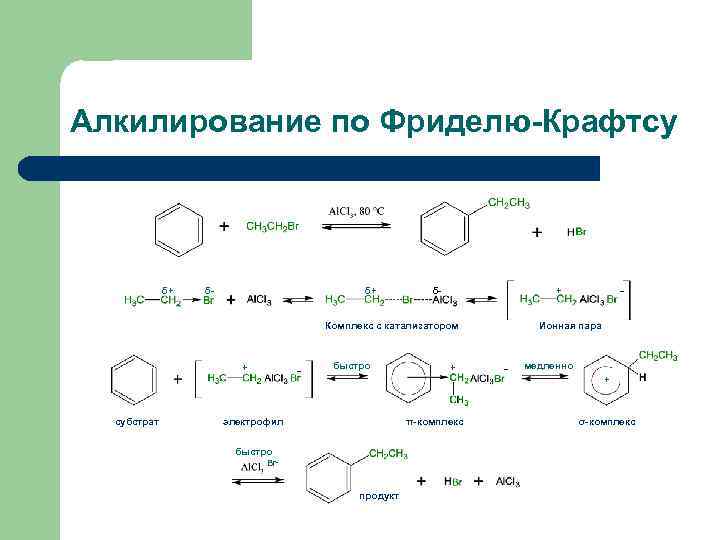 Алкилирование по Фриделю-Крафтсу δ+ δ- + Комплекс с катализатором + субстрат - быстро электрофил + π-комплекс быстро Br- продукт - Ионная пара - медленно + σ-комплекс
Алкилирование по Фриделю-Крафтсу δ+ δ- + Комплекс с катализатором + субстрат - быстро электрофил + π-комплекс быстро Br- продукт - Ионная пара - медленно + σ-комплекс
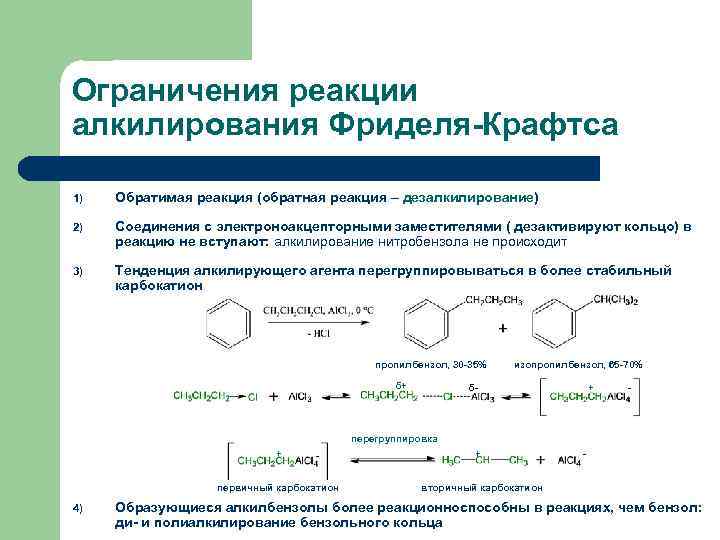 Ограничения реакции алкилирования Фриделя-Крафтса 1) Обратимая реакция (обратная реакция – дезалкилирование) 2) Соединения с электроноакцепторными заместителями ( дезактивируют кольцо) в реакцию не вступают: алкилирование нитробензола не происходит 3) Тенденция алкилирующего агента перегруппировываться в более стабильный карбокатион пропилбензол, 30 -35% δ+ изопропилбензол, 65 -70% δ- + - перегруппировка + - первичный карбокатион 4) + - вторичный карбокатион Образующиеся алкилбензолы более реакционноспособны в реакциях, чем бензол: ди- и полиалкилирование бензольного кольца
Ограничения реакции алкилирования Фриделя-Крафтса 1) Обратимая реакция (обратная реакция – дезалкилирование) 2) Соединения с электроноакцепторными заместителями ( дезактивируют кольцо) в реакцию не вступают: алкилирование нитробензола не происходит 3) Тенденция алкилирующего агента перегруппировываться в более стабильный карбокатион пропилбензол, 30 -35% δ+ изопропилбензол, 65 -70% δ- + - перегруппировка + - первичный карбокатион 4) + - вторичный карбокатион Образующиеся алкилбензолы более реакционноспособны в реакциях, чем бензол: ди- и полиалкилирование бензольного кольца
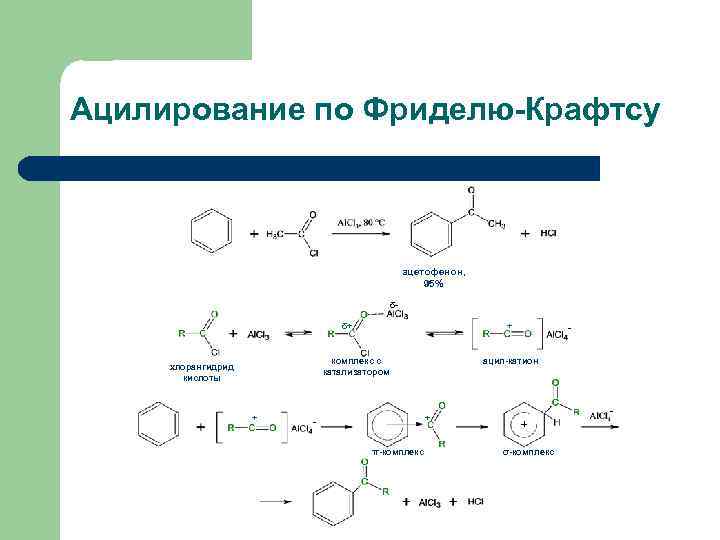 Ацилирование по Фриделю-Крафтсу ацетофенон, 95% δδ+ + комплекс с катализатором хлорангидрид кислоты + ацил-катион + π-комплекс - - + σ-комплекс
Ацилирование по Фриделю-Крафтсу ацетофенон, 95% δδ+ + комплекс с катализатором хлорангидрид кислоты + ацил-катион + π-комплекс - - + σ-комплекс
 Реакции SE конденсированных аренов и небензоидных ароматических систем 1. Электрофильное замещение в соединениях данного типа также протекает с частичным нарушением ароматической системы на стадии образования -комплекса. Потери энергии стабилизации в этом случае существенно ниже, чем в случае бензола или соединений с изолированными бензольными ядрами. 2. Нафталин, антрацен и фенантрен легче вступают в реакции электрофильного замещения, чем бензол и соединения с изолированными бензольными ядрами.
Реакции SE конденсированных аренов и небензоидных ароматических систем 1. Электрофильное замещение в соединениях данного типа также протекает с частичным нарушением ароматической системы на стадии образования -комплекса. Потери энергии стабилизации в этом случае существенно ниже, чем в случае бензола или соединений с изолированными бензольными ядрами. 2. Нафталин, антрацен и фенантрен легче вступают в реакции электрофильного замещения, чем бензол и соединения с изолированными бензольными ядрами.
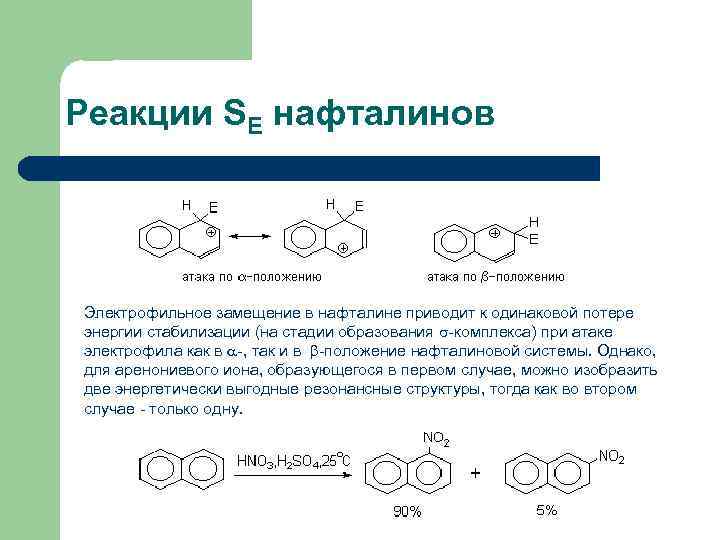 Реакции SE нафталинов Электрофильное замещение в нафталине приводит к одинаковой потере энергии стабилизации (на стадии образования -комплекса) при атаке электрофила как в -, так и в -положение нафталиновой системы. Однако, для аренониевого иона, образующегося в первом случае, можно изобразить две энергетически выгодные резонансные структуры, тогда как во втором случае - только одну.
Реакции SE нафталинов Электрофильное замещение в нафталине приводит к одинаковой потере энергии стабилизации (на стадии образования -комплекса) при атаке электрофила как в -, так и в -положение нафталиновой системы. Однако, для аренониевого иона, образующегося в первом случае, можно изобразить две энергетически выгодные резонансные структуры, тогда как во втором случае - только одну.
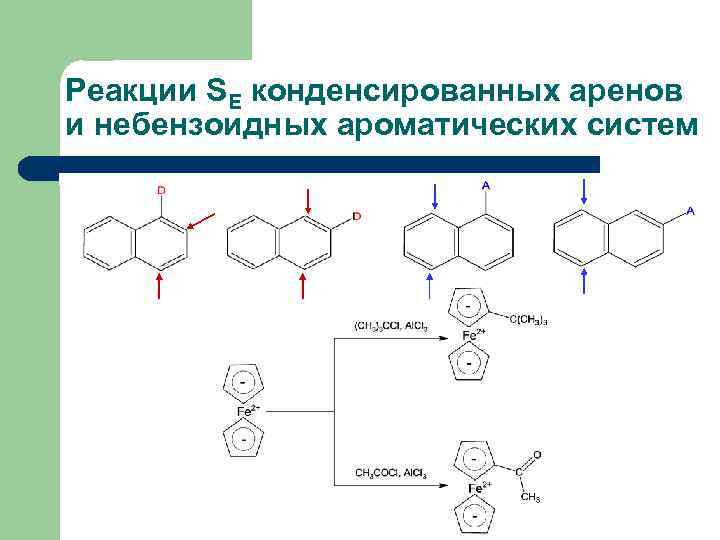 Реакции SE конденсированных аренов и небензоидных ароматических систем
Реакции SE конденсированных аренов и небензоидных ароматических систем
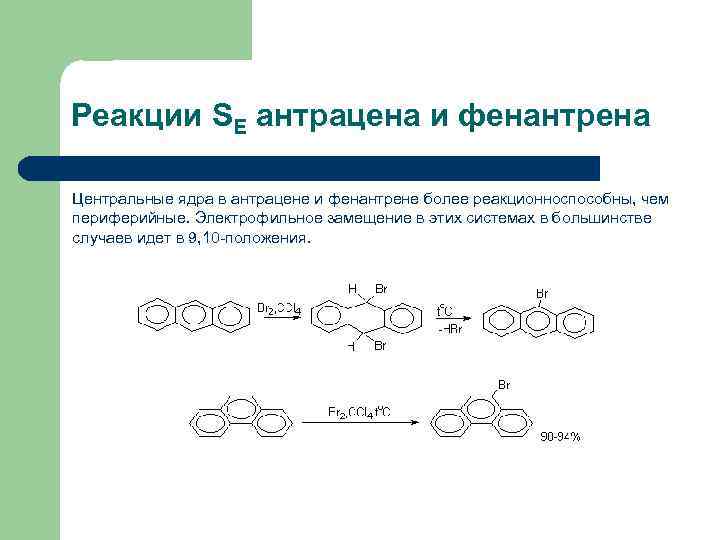 Реакции SE антрацена и фенантрена Центральные ядра в антрацене и фенантрене более реакционноспособны, чем периферийные. Электрофильное замещение в этих системах в большинстве случаев идет в 9, 10 -положения.
Реакции SE антрацена и фенантрена Центральные ядра в антрацене и фенантрене более реакционноспособны, чем периферийные. Электрофильное замещение в этих системах в большинстве случаев идет в 9, 10 -положения.
 Благодарю за внимание!
Благодарю за внимание!


