Обмен белков4.ppt
- Количество слайдов: 47
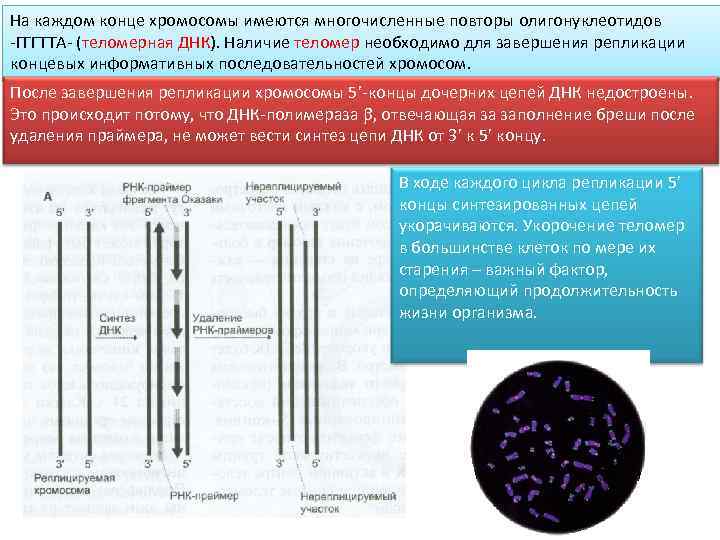 На каждом конце хромосомы имеются многочисленные повторы олигонуклеотидов -ГГГТТА- (теломерная ДНК). Наличие теломер необходимо для завершения репликации концевых информативных последовательностей хромосом. После завершения репликации хромосомы 5’-концы дочерних цепей ДНК недостроены. Это происходит потому, что ДНК-полимераза , отвечающая за заполнение бреши после удаления праймера, не может вести синтез цепи ДНК от 3’ к 5’ концу. В ходе каждого цикла репликации 5’ концы синтезированных цепей укорачиваются. Укорочение теломер в большинстве клеток по мере их старения – важный фактор, определяющий продолжительность жизни организма.
На каждом конце хромосомы имеются многочисленные повторы олигонуклеотидов -ГГГТТА- (теломерная ДНК). Наличие теломер необходимо для завершения репликации концевых информативных последовательностей хромосом. После завершения репликации хромосомы 5’-концы дочерних цепей ДНК недостроены. Это происходит потому, что ДНК-полимераза , отвечающая за заполнение бреши после удаления праймера, не может вести синтез цепи ДНК от 3’ к 5’ концу. В ходе каждого цикла репликации 5’ концы синтезированных цепей укорачиваются. Укорочение теломер в большинстве клеток по мере их старения – важный фактор, определяющий продолжительность жизни организма.
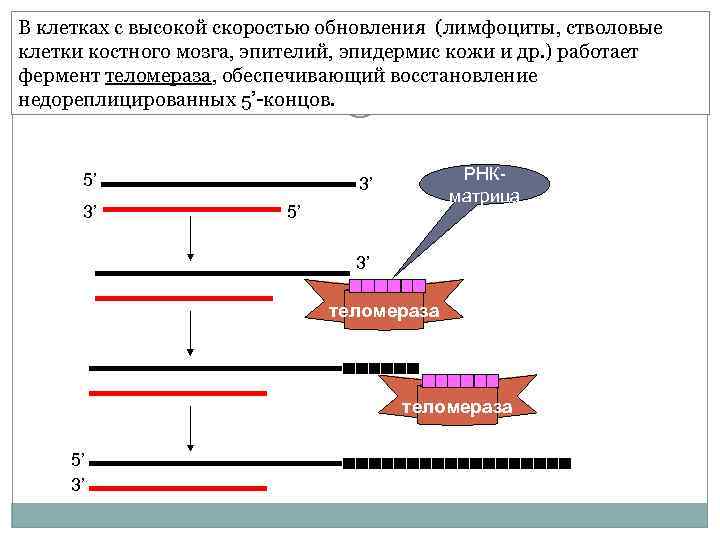 В клетках с высокой скоростью обновления (лимфоциты, стволовые клетки костного мозга, эпителий, эпидермис кожи и др. ) работает фермент теломераза, обеспечивающий восстановление недореплицированных 5’-концов. 5’ 3’ РНКматрица 3’ 5’ 3’ теломераза 5’ 3’
В клетках с высокой скоростью обновления (лимфоциты, стволовые клетки костного мозга, эпителий, эпидермис кожи и др. ) работает фермент теломераза, обеспечивающий восстановление недореплицированных 5’-концов. 5’ 3’ РНКматрица 3’ 5’ 3’ теломераза 5’ 3’
 После завершения репликации происходит метилирование нуклеотидных остатков вновь образованных цепей ДНК. Количество метилированных оснований 1 -8%. Источник метильных групп – S-аденозилметионин. Это необходимо для формирования структуры хромосом и регуляции транскрипции генов, защиты от расщепления рестриктазами.
После завершения репликации происходит метилирование нуклеотидных остатков вновь образованных цепей ДНК. Количество метилированных оснований 1 -8%. Источник метильных групп – S-аденозилметионин. Это необходимо для формирования структуры хромосом и регуляции транскрипции генов, защиты от расщепления рестриктазами.
 В настоящее время синтезировано много аналогов д. НТФ, которые включаются ДНК- полимеразами в ДНК и ингибируют репликацию. Мощные противоопухолевые препараты. Их действие основано на том, что 1) через «запасные» пути из них образуются нуклеотиды, которые блокируют тимидилат синтазу - 5 -фторурацил (аналог урацила), 2) тот же эффект, но путем имитации фолиевой кислоты (метотрексат, аминоптерин) или 3) ингибировать ДНКполимеразу – цитозинарабинозид (цитарабин). Антивирусные и антибактериальные препараты: азидотимидин (ретровирусная инфекция – ВИЧ), 5 -йоддезоксиуридин (вирус герпеса), азатиоприн (в организме превращается в 6 -меркаптопурин, оказывающий мощное иммуносупрессорное действие)
В настоящее время синтезировано много аналогов д. НТФ, которые включаются ДНК- полимеразами в ДНК и ингибируют репликацию. Мощные противоопухолевые препараты. Их действие основано на том, что 1) через «запасные» пути из них образуются нуклеотиды, которые блокируют тимидилат синтазу - 5 -фторурацил (аналог урацила), 2) тот же эффект, но путем имитации фолиевой кислоты (метотрексат, аминоптерин) или 3) ингибировать ДНКполимеразу – цитозинарабинозид (цитарабин). Антивирусные и антибактериальные препараты: азидотимидин (ретровирусная инфекция – ВИЧ), 5 -йоддезоксиуридин (вирус герпеса), азатиоприн (в организме превращается в 6 -меркаптопурин, оказывающий мощное иммуносупрессорное действие)
 Репарация или репаративный синтез ДНК (исправление повреждений) Все репарационные механизмы основаны на том, что ДНК – двухцепочечная молекула. Если нуклеотидная последовательность одной из двух цепей оказывается поврежденной (измененной), информацию можно восстановить, так как вторая (комплементарная) цепь сохранена. Спонтанные и индуцируемые повреждения. Спонтанные – ошибки репликации, депуринизация, дезаминирование Ошибки репликации – в дочернюю цепь ДНК включаются нуклеотиды, некомплементарные нуклеотидам матричной цепи. Частота – 1 раз на 105 -106 нуклеотидных остатков. Депуринизация. ДНК каждой клетки человека теряет за сутки около 5000 пуриновых остатков вследствие разрыва N-гликозидной связи между пурином и дезоксирибозой. Тогда в молекуле ДНК на месте этих оснований образуется участок, лишенный азотистых оснований, названный апуриновый сайт. Реакции дезаминирования цитозина и превращение его в урацил, аденина в гипоксантин, гуанина в ксантин происходят значительно реже, чем депуринизация, и составляют 10 реакций на 1 геном в сутки
Репарация или репаративный синтез ДНК (исправление повреждений) Все репарационные механизмы основаны на том, что ДНК – двухцепочечная молекула. Если нуклеотидная последовательность одной из двух цепей оказывается поврежденной (измененной), информацию можно восстановить, так как вторая (комплементарная) цепь сохранена. Спонтанные и индуцируемые повреждения. Спонтанные – ошибки репликации, депуринизация, дезаминирование Ошибки репликации – в дочернюю цепь ДНК включаются нуклеотиды, некомплементарные нуклеотидам матричной цепи. Частота – 1 раз на 105 -106 нуклеотидных остатков. Депуринизация. ДНК каждой клетки человека теряет за сутки около 5000 пуриновых остатков вследствие разрыва N-гликозидной связи между пурином и дезоксирибозой. Тогда в молекуле ДНК на месте этих оснований образуется участок, лишенный азотистых оснований, названный апуриновый сайт. Реакции дезаминирования цитозина и превращение его в урацил, аденина в гипоксантин, гуанина в ксантин происходят значительно реже, чем депуринизация, и составляют 10 реакций на 1 геном в сутки
 Основные механизмы исправления повреждений: Прямая репарация (при депуринизации) Этот тип повреждений устраняет фермент ДНК инсертаза, который может присоединять к дезоксирибозе основание в соответствии с правилом комплементарности. В этом случае нет необходимости разрезать цепь ДНК, вырезать неправильный нуклеотид и репарировать разрыв.
Основные механизмы исправления повреждений: Прямая репарация (при депуринизации) Этот тип повреждений устраняет фермент ДНК инсертаза, который может присоединять к дезоксирибозе основание в соответствии с правилом комплементарности. В этом случае нет необходимости разрезать цепь ДНК, вырезать неправильный нуклеотид и репарировать разрыв.
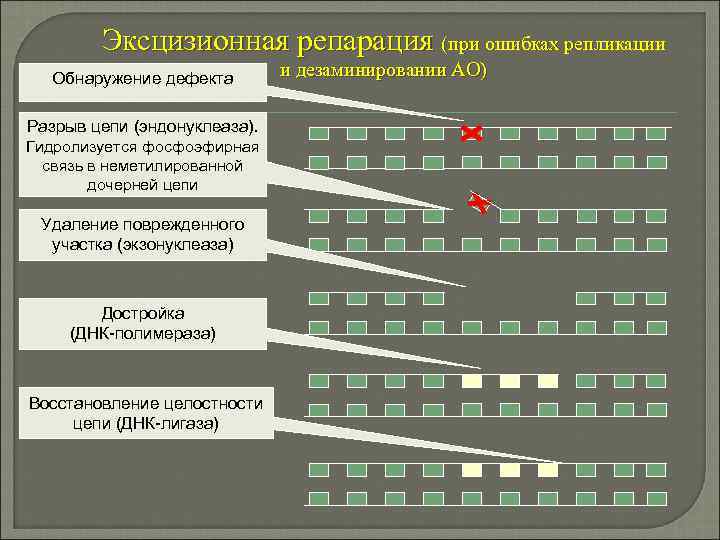 Эксцизионная репарация (при ошибках репликации Обнаружение дефекта Разрыв цепи (эндонуклеаза). Гидролизуется фосфоэфирная связь в неметилированной дочерней цепи Удаление поврежденного участка (экзонуклеаза) Достройка (ДНК-полимераза) Восстановление целостности цепи (ДНК-лигаза) и дезаминировании АО)
Эксцизионная репарация (при ошибках репликации Обнаружение дефекта Разрыв цепи (эндонуклеаза). Гидролизуется фосфоэфирная связь в неметилированной дочерней цепи Удаление поврежденного участка (экзонуклеаза) Достройка (ДНК-полимераза) Восстановление целостности цепи (ДНК-лигаза) и дезаминировании АО)
 C нарушением процессов репарации и накоплением повреждений в ДНК связаны Ø Апоптоз Ø Старение Ø Канцерогенез
C нарушением процессов репарации и накоплением повреждений в ДНК связаны Ø Апоптоз Ø Старение Ø Канцерогенез
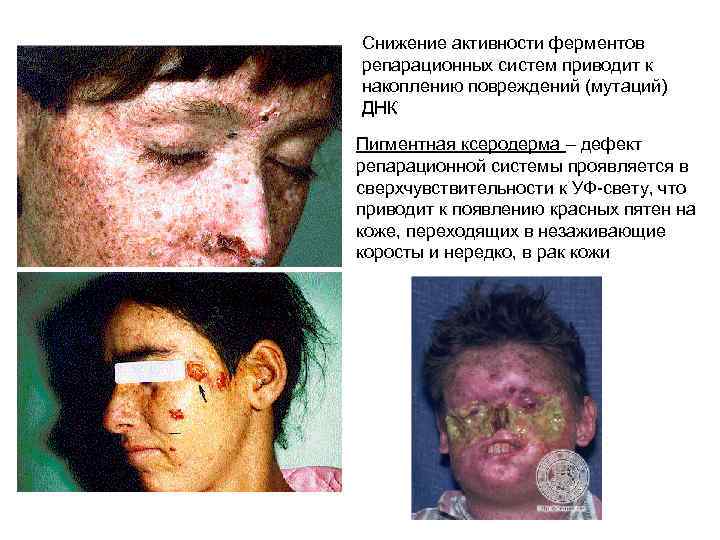 Снижение активности ферментов репарационных систем приводит к накоплению повреждений (мутаций) ДНК Пигментная ксеродерма – дефект репарационной системы проявляется в сверхчувствительности к УФ-свету, что приводит к появлению красных пятен на коже, переходящих в незаживающие коросты и нередко, в рак кожи
Снижение активности ферментов репарационных систем приводит к накоплению повреждений (мутаций) ДНК Пигментная ксеродерма – дефект репарационной системы проявляется в сверхчувствительности к УФ-свету, что приводит к появлению красных пятен на коже, переходящих в незаживающие коросты и нередко, в рак кожи
 Апоптоз Это механизм программируемой и регулируемой гибели клеток. Он включается при повреждениях систем репарации ДНК и накопления повреждений ДНК. Эти изменения активируют ряд специфических протеаз в клетке, которые, в свою очередь, активируют эндонуклеазы. Эндонуклеазы гидролизуют ДНК сначала на крупные фрагменты, а затем – на мелкие (размер участка ДНК в нуклеосоме). Далее клетка распадается на мембранные везикулы (апоптозные тельца), содержащие фрагментированную ДНК; везикулы поглощаются и разрушаются фагоцитирующими клетками. Так устраняются клетки, размножение которых может быть опасным для организма, например, привести к развитию раковой опухоли. Другая функция апоптоза – уничтожение клеток, завершивших свою роль (исчезновение хвоста у головастика при превращении в лягушку и др. )
Апоптоз Это механизм программируемой и регулируемой гибели клеток. Он включается при повреждениях систем репарации ДНК и накопления повреждений ДНК. Эти изменения активируют ряд специфических протеаз в клетке, которые, в свою очередь, активируют эндонуклеазы. Эндонуклеазы гидролизуют ДНК сначала на крупные фрагменты, а затем – на мелкие (размер участка ДНК в нуклеосоме). Далее клетка распадается на мембранные везикулы (апоптозные тельца), содержащие фрагментированную ДНК; везикулы поглощаются и разрушаются фагоцитирующими клетками. Так устраняются клетки, размножение которых может быть опасным для организма, например, привести к развитию раковой опухоли. Другая функция апоптоза – уничтожение клеток, завершивших свою роль (исчезновение хвоста у головастика при превращении в лягушку и др. )
 Центральная догма молекулярной биологии ДНК РНК БЕЛОК
Центральная догма молекулярной биологии ДНК РНК БЕЛОК
 ТРАНСКРИПЦИЯ 1. Синтез РНК начинается в определенных последовательностях (сайтах) ДНК, которые называют промоторы, и завершается в терминирующих участках (сайты терминации). 2. Участок ДНК, ограниченный промотором и сайтом терминации, представляет собой единицу транскрипции – транскриптон (у прокариот – оперон). У эукариотов в составе транскриптона – 1 ген, у прокариотов несколько. 3. В каждом транскриптоне транскрибируется только одна из двух цепей ДНК, которая называется матричной, вторая, комплементарная ей цепь, называется кодирующей. 4. Синтез цепи РНК идет от 5’ – к 3’ концу, при этом матричная цепь ДНК всегда антипараллельна синтезируемой нуклеиновой кислоте В ядрах эукариот 3 РНК-полимеразы: РНК-полимераза I, синтезирующая пре-р. РНК; РНК-полимераза II, ответственная за синтез пре-м. РНК; РНКполимераза III, синтезирующая пре-т. РНК.
ТРАНСКРИПЦИЯ 1. Синтез РНК начинается в определенных последовательностях (сайтах) ДНК, которые называют промоторы, и завершается в терминирующих участках (сайты терминации). 2. Участок ДНК, ограниченный промотором и сайтом терминации, представляет собой единицу транскрипции – транскриптон (у прокариот – оперон). У эукариотов в составе транскриптона – 1 ген, у прокариотов несколько. 3. В каждом транскриптоне транскрибируется только одна из двух цепей ДНК, которая называется матричной, вторая, комплементарная ей цепь, называется кодирующей. 4. Синтез цепи РНК идет от 5’ – к 3’ концу, при этом матричная цепь ДНК всегда антипараллельна синтезируемой нуклеиновой кислоте В ядрах эукариот 3 РНК-полимеразы: РНК-полимераза I, синтезирующая пре-р. РНК; РНК-полимераза II, ответственная за синтез пре-м. РНК; РНКполимераза III, синтезирующая пре-т. РНК.
 Транскрипция Фермент – РНК-полимераза. Требует наличия: • матрицы • субстратов для синтеза цепи РНК (АТФ, ГТФ, ЦТФ, УТФ) • ионов Mg 2+ и Mn 2+ (!) Не требует праймера
Транскрипция Фермент – РНК-полимераза. Требует наличия: • матрицы • субстратов для синтеза цепи РНК (АТФ, ГТФ, ЦТФ, УТФ) • ионов Mg 2+ и Mn 2+ (!) Не требует праймера
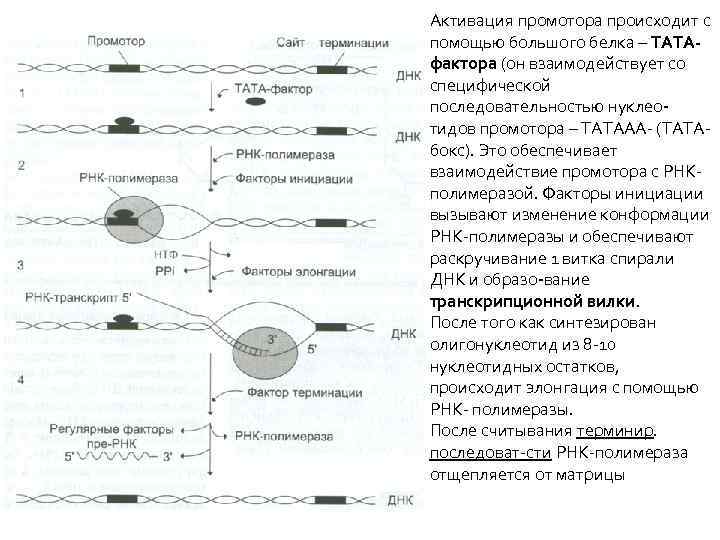 Активация промотора происходит с помощью большого белка – ТАТАфактора (он взаимодействует со специфической последовательностью нуклеотидов промотора – ТАТААА- (ТАТАбокс). Это обеспечивает взаимодействие промотора с РНКполимеразой. Факторы инициации вызывают изменение конформации РНК-полимеразы и обеспечивают раскручивание 1 витка спирали ДНК и образо-вание транскрипционной вилки. После того как синтезирован олигонуклеотид из 8 -10 нуклеотидных остатков, происходит элонгация с помощью РНК- полимеразы. После считывания терминир. последоват-сти РНК-полимераза отщепляется от матрицы
Активация промотора происходит с помощью большого белка – ТАТАфактора (он взаимодействует со специфической последовательностью нуклеотидов промотора – ТАТААА- (ТАТАбокс). Это обеспечивает взаимодействие промотора с РНКполимеразой. Факторы инициации вызывают изменение конформации РНК-полимеразы и обеспечивают раскручивание 1 витка спирали ДНК и образо-вание транскрипционной вилки. После того как синтезирован олигонуклеотид из 8 -10 нуклеотидных остатков, происходит элонгация с помощью РНК- полимеразы. После считывания терминир. последоват-сти РНК-полимераза отщепляется от матрицы
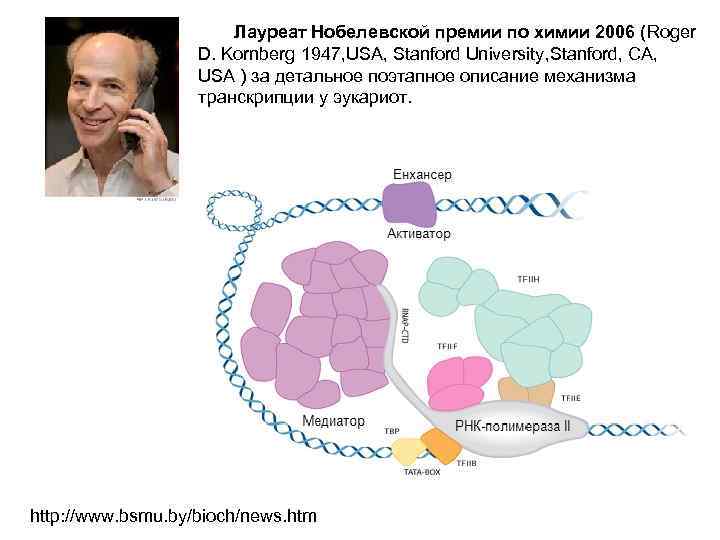 Лауреат Нобелевской премии по химии 2006 (Roger D. Kornberg 1947, USA, Stanford University, Stanford, CA, USA ) за детальное поэтапное описание механизма транскрипции у эукариот. http: //www. bsmu. by/bioch/news. htm
Лауреат Нобелевской премии по химии 2006 (Roger D. Kornberg 1947, USA, Stanford University, Stanford, CA, USA ) за детальное поэтапное описание механизма транскрипции у эукариот. http: //www. bsmu. by/bioch/news. htm
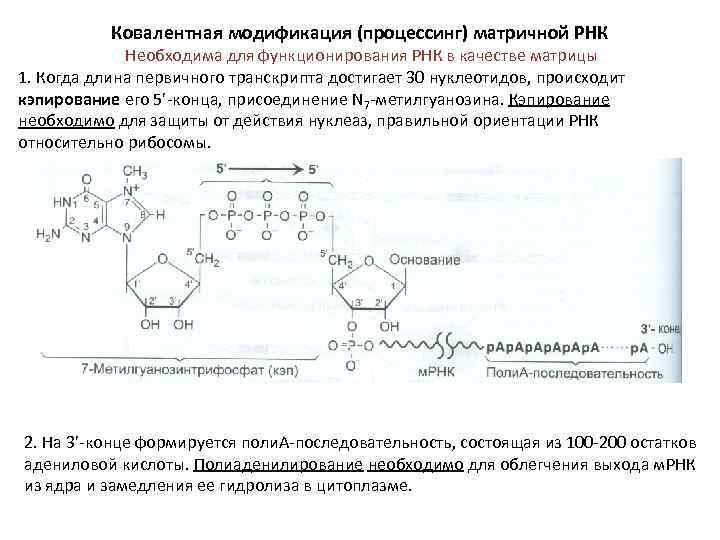 Ковалентная модификация (процессинг) матричной РНК Необходима для функционирования РНК в качестве матрицы 1. Когда длина первичного транскрипта достигает 30 нуклеотидов, происходит кэпирование его 5’-конца, присоединение N 7 -метилгуанозина. Кэпирование необходимо для защиты от действия нуклеаз, правильной ориентации РНК относительно рибосомы. 2. На 3’-конце формируется поли. А-последовательность, состоящая из 100 -200 остатков адениловой кислоты. Полиаденилирование необходимо для облегчения выхода м. РНК из ядра и замедления ее гидролиза в цитоплазме.
Ковалентная модификация (процессинг) матричной РНК Необходима для функционирования РНК в качестве матрицы 1. Когда длина первичного транскрипта достигает 30 нуклеотидов, происходит кэпирование его 5’-конца, присоединение N 7 -метилгуанозина. Кэпирование необходимо для защиты от действия нуклеаз, правильной ориентации РНК относительно рибосомы. 2. На 3’-конце формируется поли. А-последовательность, состоящая из 100 -200 остатков адениловой кислоты. Полиаденилирование необходимо для облегчения выхода м. РНК из ядра и замедления ее гидролиза в цитоплазме.
 3. Сплайсинг первичных транскриптов м. РНК – происходит в ядре • Некодирующие последовательности нуклеотидов - интроны (80 -1000 нуклеотидов), кодирующие последовательности нуклеотидов - экзоны. • Соотношение информативной и неинформативной частей в транскриптонах эукариотов 1: 9 (у прокариотов 9: 1) • Последовательности интронов вырезаются из первичного транскрипта, концы экзонов соединяются – сплайсинг. Процесс вырезания интронов протекает при участии мя. РНК в комплексе с белками Каталитическая функция сплайсосом обусловлена РНКсоставляющими, такие РНК называют «рибозимы»
3. Сплайсинг первичных транскриптов м. РНК – происходит в ядре • Некодирующие последовательности нуклеотидов - интроны (80 -1000 нуклеотидов), кодирующие последовательности нуклеотидов - экзоны. • Соотношение информативной и неинформативной частей в транскриптонах эукариотов 1: 9 (у прокариотов 9: 1) • Последовательности интронов вырезаются из первичного транскрипта, концы экзонов соединяются – сплайсинг. Процесс вырезания интронов протекает при участии мя. РНК в комплексе с белками Каталитическая функция сплайсосом обусловлена РНКсоставляющими, такие РНК называют «рибозимы»
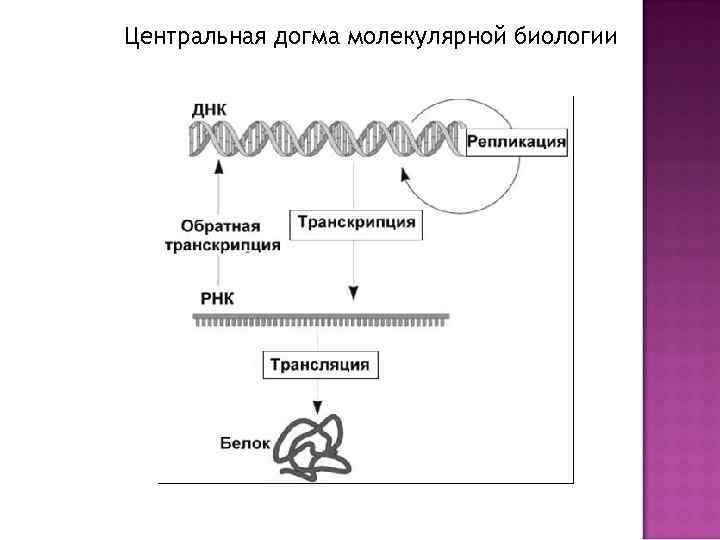 Центральная догма молекулярной биологии
Центральная догма молекулярной биологии
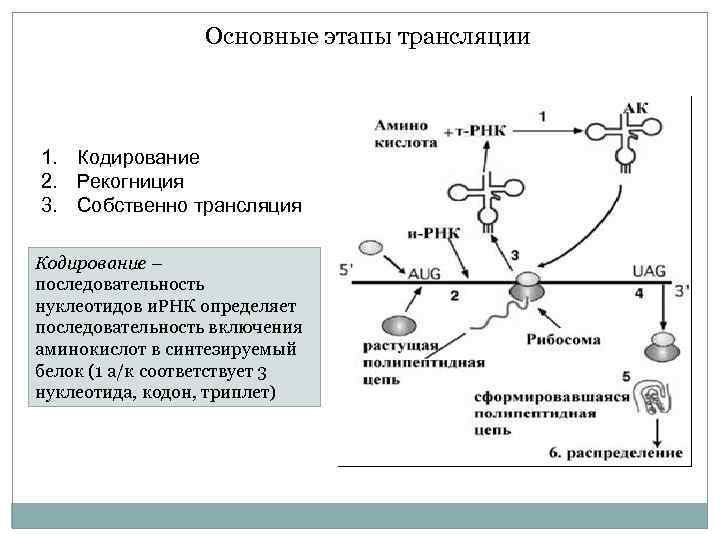 Основные этапы трансляции 1. Кодирование 2. Рекогниция 3. Собственно трансляция Кодирование – последовательность нуклеотидов и. РНК определяет последовательность включения аминокислот в синтезируемый белок (1 а/к соответствует 3 нуклеотида, кодон, триплет)
Основные этапы трансляции 1. Кодирование 2. Рекогниция 3. Собственно трансляция Кодирование – последовательность нуклеотидов и. РНК определяет последовательность включения аминокислот в синтезируемый белок (1 а/к соответствует 3 нуклеотида, кодон, триплет)
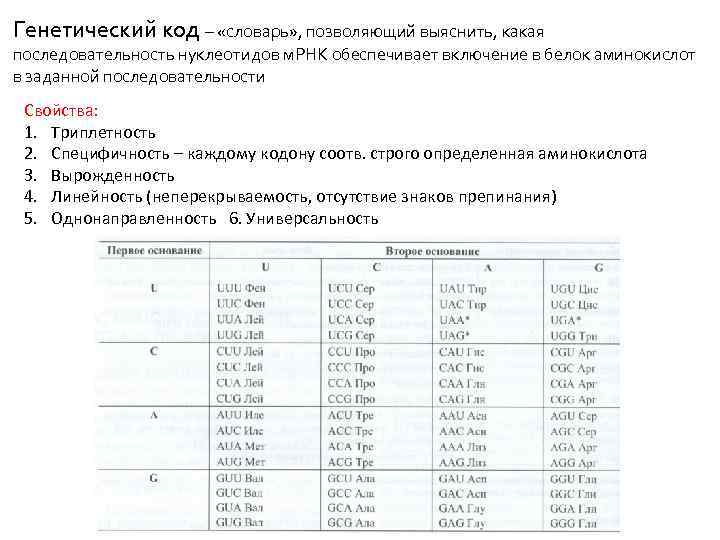 Генетический код – «словарь» , позволяющий выяснить, какая последовательность нуклеотидов м. РНК обеспечивает включение в белок аминокислот в заданной последовательности Свойства: 1. Триплетность 2. Специфичность – каждому кодону соотв. строго определенная аминокислота 3. Вырожденность 4. Линейность (неперекрываемость, отсутствие знаков препинания) 5. Однонаправленность 6. Универсальность
Генетический код – «словарь» , позволяющий выяснить, какая последовательность нуклеотидов м. РНК обеспечивает включение в белок аминокислот в заданной последовательности Свойства: 1. Триплетность 2. Специфичность – каждому кодону соотв. строго определенная аминокислота 3. Вырожденность 4. Линейность (неперекрываемость, отсутствие знаков препинания) 5. Однонаправленность 6. Универсальность
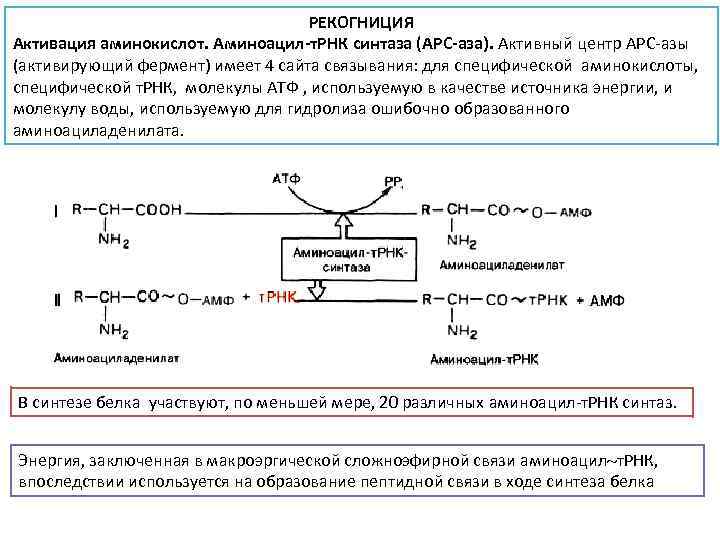 РЕКОГНИЦИЯ Активация аминокислот. Аминоацил-т. РНК синтаза (АРС-аза). Активный центр АРС-азы (активирующий фермент) имеет 4 сайта связывания: для специфической аминокислоты, специфической т. РНК, молекулы АТФ , используемую в качестве источника энергии, и молекулу воды, используемую для гидролиза ошибочно образованного аминоациладенилата. В синтезе белка участвуют, по меньшей мере, 20 различных аминоацил-т. РНК синтаз. Энергия, заключенная в макроэргической сложноэфирной связи аминоацил т. РНК, впоследствии используется на образование пептидной связи в ходе синтеза белка
РЕКОГНИЦИЯ Активация аминокислот. Аминоацил-т. РНК синтаза (АРС-аза). Активный центр АРС-азы (активирующий фермент) имеет 4 сайта связывания: для специфической аминокислоты, специфической т. РНК, молекулы АТФ , используемую в качестве источника энергии, и молекулу воды, используемую для гидролиза ошибочно образованного аминоациладенилата. В синтезе белка участвуют, по меньшей мере, 20 различных аминоацил-т. РНК синтаз. Энергия, заключенная в макроэргической сложноэфирной связи аминоацил т. РНК, впоследствии используется на образование пептидной связи в ходе синтеза белка
 В ходе синтеза белка прочтение информации м. РНК идет в направлении от 5’- к 3’-концу, обеспечивая синтез пептида от Nк С-концу. На включение одной аминокислоты в растущую полипептидную цепь клетка затрачивает 4 макроэргические связи: 2 из АТФ в ходе реакции, катализируемой аа-т. РНК синтазой (в процессе активации АТФ расщепляется на АМФ и Фн. Фн) и 2 молекулы ГТФ (одна используется на связывание аа-т. РНК в А-центре рибосомы, а вторая затрачивается на стадию транслокации). Еще 2 макроэргические связи молекул АТФ и ГТФ расходуются на инициацию и терминацию синтеза полипептидной цепи. 3 этапа на рибосоме – инициация, элонгация, терминация
В ходе синтеза белка прочтение информации м. РНК идет в направлении от 5’- к 3’-концу, обеспечивая синтез пептида от Nк С-концу. На включение одной аминокислоты в растущую полипептидную цепь клетка затрачивает 4 макроэргические связи: 2 из АТФ в ходе реакции, катализируемой аа-т. РНК синтазой (в процессе активации АТФ расщепляется на АМФ и Фн. Фн) и 2 молекулы ГТФ (одна используется на связывание аа-т. РНК в А-центре рибосомы, а вторая затрачивается на стадию транслокации). Еще 2 макроэргические связи молекул АТФ и ГТФ расходуются на инициацию и терминацию синтеза полипептидной цепи. 3 этапа на рибосоме – инициация, элонгация, терминация
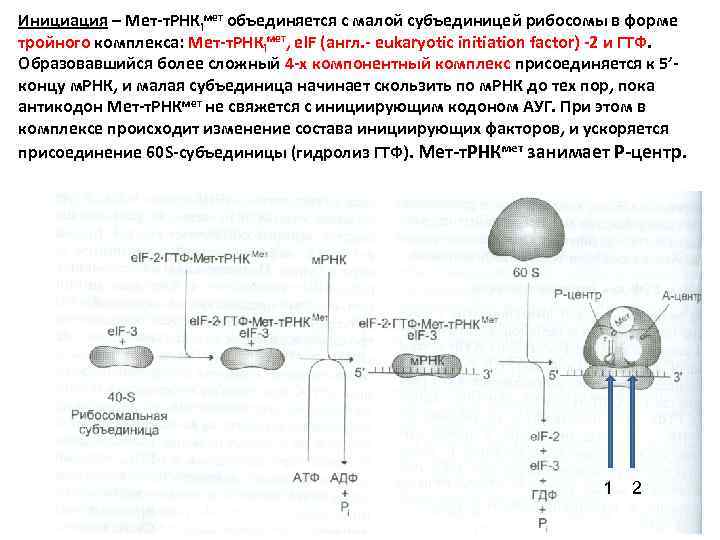 Инициация – Мет-т. РНКiмет объединяется с малой субъединицей рибосомы в форме тройного комплекса: Мет-т. РНКiмет, el. F (англ. - eukaryotic initiation factor) -2 и ГТФ. Образовавшийся более сложный 4 -х компонентный комплекс присоединяется к 5’концу м. РНК, и малая субъединица начинает скользить по м. РНК до тех пор, пока антикодон Мет-т. РНКмет не свяжется с инициирующим кодоном АУГ. При этом в комплексе происходит изменение состава инициирующих факторов, и ускоряется присоединение 60 S-субъединицы (гидролиз ГТФ). Мет-т. РНКмет занимает Р-центр. 1 2
Инициация – Мет-т. РНКiмет объединяется с малой субъединицей рибосомы в форме тройного комплекса: Мет-т. РНКiмет, el. F (англ. - eukaryotic initiation factor) -2 и ГТФ. Образовавшийся более сложный 4 -х компонентный комплекс присоединяется к 5’концу м. РНК, и малая субъединица начинает скользить по м. РНК до тех пор, пока антикодон Мет-т. РНКмет не свяжется с инициирующим кодоном АУГ. При этом в комплексе происходит изменение состава инициирующих факторов, и ускоряется присоединение 60 S-субъединицы (гидролиз ГТФ). Мет-т. РНКмет занимает Р-центр. 1 2
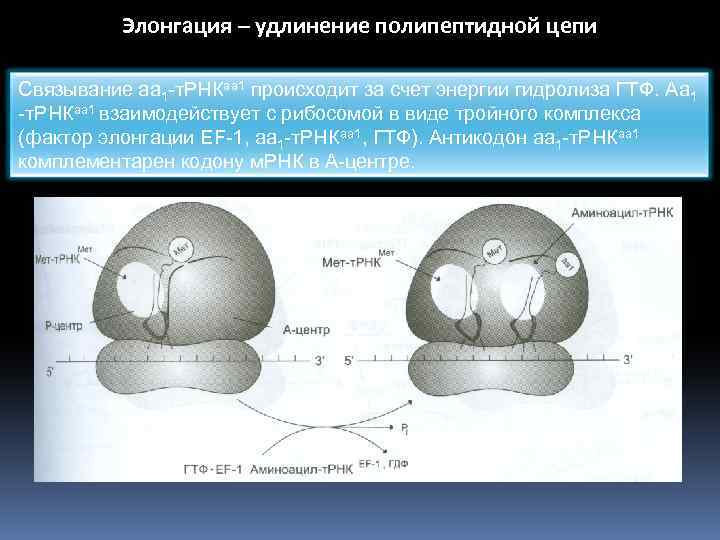 Элонгация – удлинение полипептидной цепи Связывание аа 1 -т. РНКаа 1 происходит за счет энергии гидролиза ГТФ. Aа 1 -т. РНКаа 1 взаимодействует с рибосомой в виде тройного комплекса (фактор элонгации EF-1, аа 1 -т. РНКаа 1, ГТФ). Антикодон аа 1 -т. РНКаа 1 комплементарен кодону м. РНК в А-центре.
Элонгация – удлинение полипептидной цепи Связывание аа 1 -т. РНКаа 1 происходит за счет энергии гидролиза ГТФ. Aа 1 -т. РНКаа 1 взаимодействует с рибосомой в виде тройного комплекса (фактор элонгации EF-1, аа 1 -т. РНКаа 1, ГТФ). Антикодон аа 1 -т. РНКаа 1 комплементарен кодону м. РНК в А-центре.
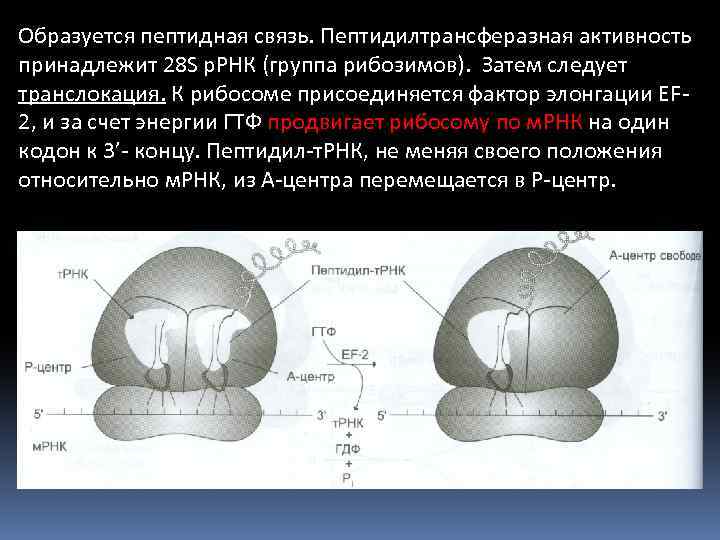 Образуется пептидная связь. Пептидилтрансферазная активность принадлежит 28 S р. РНК (группа рибозимов). Затем следует транслокация. К рибосоме присоединяется фактор элонгации ЕF 2, и за счет энергии ГТФ продвигает рибосому по м. РНК на один кодон к 3’- концу. Пептидил-т. РНК, не меняя своего положения относительно м. РНК, из А-центра перемещается в Р-центр.
Образуется пептидная связь. Пептидилтрансферазная активность принадлежит 28 S р. РНК (группа рибозимов). Затем следует транслокация. К рибосоме присоединяется фактор элонгации ЕF 2, и за счет энергии ГТФ продвигает рибосому по м. РНК на один кодон к 3’- концу. Пептидил-т. РНК, не меняя своего положения относительно м. РНК, из А-центра перемещается в Р-центр.
 Резюме элонгации Включение каждой аминокислоты в белок происходит в 3 стадии: (1)аа-т. РНК каждой входящей в белок аминокислоты связывается с А-центром рибосомы; (2)пептид от пептидил-т. РНК, находящейся в Р-центре, присоединяется к NH 2 -группе аминокислотного остатка аа-т. РНК А-центра с образованием новой пептидной связи; (3)удлиненная на один аминокислотный остаток пептидил-т. РНК перемещается из А-центра в Р-центр в результате транслокации рибосомы.
Резюме элонгации Включение каждой аминокислоты в белок происходит в 3 стадии: (1)аа-т. РНК каждой входящей в белок аминокислоты связывается с А-центром рибосомы; (2)пептид от пептидил-т. РНК, находящейся в Р-центре, присоединяется к NH 2 -группе аминокислотного остатка аа-т. РНК А-центра с образованием новой пептидной связи; (3)удлиненная на один аминокислотный остаток пептидил-т. РНК перемещается из А-центра в Р-центр в результате транслокации рибосомы.
 Терминация трансляции наступает, когда в А-центр рибосомы попадает один из стоп-кодонов: УАГ, УАА или УГА. Тогда к рибосоме присоединяются 2 белковых фактора (RF, англ. releasing factor). Один из них катализирует гидролитическое отщепление синтезированного пептида от т. РНК. Другой за счет энергии гидролиза ГТФ вызывает диссоциацию рибосомы на субъединицы. Каждая рибосома занимает на м. РНК участок длиной около 80 нуклеотидов, поэтому рибосомы располагаются на м. РНК с интервалом около 100 нуклеотидов (полисомы)
Терминация трансляции наступает, когда в А-центр рибосомы попадает один из стоп-кодонов: УАГ, УАА или УГА. Тогда к рибосоме присоединяются 2 белковых фактора (RF, англ. releasing factor). Один из них катализирует гидролитическое отщепление синтезированного пептида от т. РНК. Другой за счет энергии гидролиза ГТФ вызывает диссоциацию рибосомы на субъединицы. Каждая рибосома занимает на м. РНК участок длиной около 80 нуклеотидов, поэтому рибосомы располагаются на м. РНК с интервалом около 100 нуклеотидов (полисомы)
 Пострибосомальный период «созревания» белковой молекулы 2 типа рибосом у эукариотов – «свободные» , обнаруживаемые в цитоплазме клеток, и связанные с ЭПР. Белки, синтезируемые свободными рибосомами, содержат специфичные аминокислотные последовательности (то есть, сигнальные последовательности) на своих N - концевых отделах. Они обеспечивают встраивание белка в мембраны, выполняют роль сигналов, которые способствуют точному и целенаправленному переносу белка к месту его функционирования. N - концевая последовательность удаляется во время этого транспорта. Важную роль в механизме переноса таких белков принадлежит специальному классу белков - шаперонам. Белки при взаимодействии с шаперонами остаются развернутыми и доставляются к участку рецептора на мембране органеллы. Наиболее хорошо изученные шапероны - члены семейства белков " теплового шока"(HSP). Они классифицируются по молекулярной массе. Различают семейства HSP 70, HSP 60 и т. д.
Пострибосомальный период «созревания» белковой молекулы 2 типа рибосом у эукариотов – «свободные» , обнаруживаемые в цитоплазме клеток, и связанные с ЭПР. Белки, синтезируемые свободными рибосомами, содержат специфичные аминокислотные последовательности (то есть, сигнальные последовательности) на своих N - концевых отделах. Они обеспечивают встраивание белка в мембраны, выполняют роль сигналов, которые способствуют точному и целенаправленному переносу белка к месту его функционирования. N - концевая последовательность удаляется во время этого транспорта. Важную роль в механизме переноса таких белков принадлежит специальному классу белков - шаперонам. Белки при взаимодействии с шаперонами остаются развернутыми и доставляются к участку рецептора на мембране органеллы. Наиболее хорошо изученные шапероны - члены семейства белков " теплового шока"(HSP). Они классифицируются по молекулярной массе. Различают семейства HSP 70, HSP 60 и т. д.
 Белки, синтезируемые на рибосомах, связанных с ЭПР (полисомы), предназначены для клеточных мембран, лизосом, или для внеклеточного транспорта и используют специальную систему сортировки, ШЭР и комплекс Гольджи. Благодаря гидрофобной лидирующей N-концевой последовательности аминокислот новосинтезированная полипептидная цепь проходит через мембрану ЭПР В ЭПР происходит фолдинг полипептидных цепей после посттрансляционной их модификации. В чем она заключается?
Белки, синтезируемые на рибосомах, связанных с ЭПР (полисомы), предназначены для клеточных мембран, лизосом, или для внеклеточного транспорта и используют специальную систему сортировки, ШЭР и комплекс Гольджи. Благодаря гидрофобной лидирующей N-концевой последовательности аминокислот новосинтезированная полипептидная цепь проходит через мембрану ЭПР В ЭПР происходит фолдинг полипептидных цепей после посттрансляционной их модификации. В чем она заключается?
 1. Частичный протеолиз. Удаление инициирующего метионина, сигнальных пептидов, образование акт. форм ферментов и гормонов 2. Присоединение углеводов – гликозилирование 3. Ацилирование помогает белкам встраиваться в мембраны (доноры этой модификации – ацетил-Ко. А и миристоил-Ко. А), пример - гистоны 4. Метилирование аминокислотных остатков в белках - встречается редко 5. Реакции фосфорилирования белков составляют часть механизмов регуляции биологической активности белка и являются обратимыми. Другие формы ковалентной модификации (гидроксилирование, иодирование, карбоксилирование) 6. Остатки тирозина в некоторых белках могут сульфатироваться (фибриноген, гастрин). Донором сульфата является 3 '-фосфоаденозил-5 'фосфосульфат (ФАФС). 7. Присоединение 15 углеродной фарнезильной или 20 углеродной геранильной групп к акцепторным белкам – пренилирование (Gбелки).
1. Частичный протеолиз. Удаление инициирующего метионина, сигнальных пептидов, образование акт. форм ферментов и гормонов 2. Присоединение углеводов – гликозилирование 3. Ацилирование помогает белкам встраиваться в мембраны (доноры этой модификации – ацетил-Ко. А и миристоил-Ко. А), пример - гистоны 4. Метилирование аминокислотных остатков в белках - встречается редко 5. Реакции фосфорилирования белков составляют часть механизмов регуляции биологической активности белка и являются обратимыми. Другие формы ковалентной модификации (гидроксилирование, иодирование, карбоксилирование) 6. Остатки тирозина в некоторых белках могут сульфатироваться (фибриноген, гастрин). Донором сульфата является 3 '-фосфоаденозил-5 'фосфосульфат (ФАФС). 7. Присоединение 15 углеродной фарнезильной или 20 углеродной геранильной групп к акцепторным белкам – пренилирование (Gбелки).
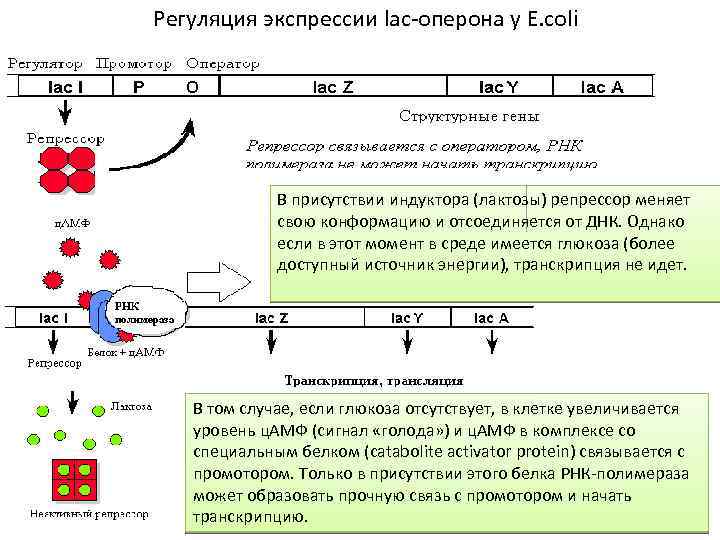 Регуляция экспрессии lac-оперона у E. coli В присутствии индуктора (лактозы) репрессор меняет свою конформацию и отсоединяется от ДНК. Однако если в этот момент в среде имеется глюкоза (более доступный источник энергии), транскрипция не идет. В том случае, если глюкоза отсутствует, в клетке увеличивается уровень ц. АМФ (сигнал «голода» ) и ц. АМФ в комплексе со специальным белком (catabolite activator protein) связывается с промотором. Только в присутствии этого белка РНК-полимераза может образовать прочную связь с промотором и начать транскрипцию.
Регуляция экспрессии lac-оперона у E. coli В присутствии индуктора (лактозы) репрессор меняет свою конформацию и отсоединяется от ДНК. Однако если в этот момент в среде имеется глюкоза (более доступный источник энергии), транскрипция не идет. В том случае, если глюкоза отсутствует, в клетке увеличивается уровень ц. АМФ (сигнал «голода» ) и ц. АМФ в комплексе со специальным белком (catabolite activator protein) связывается с промотором. Только в присутствии этого белка РНК-полимераза может образовать прочную связь с промотором и начать транскрипцию.
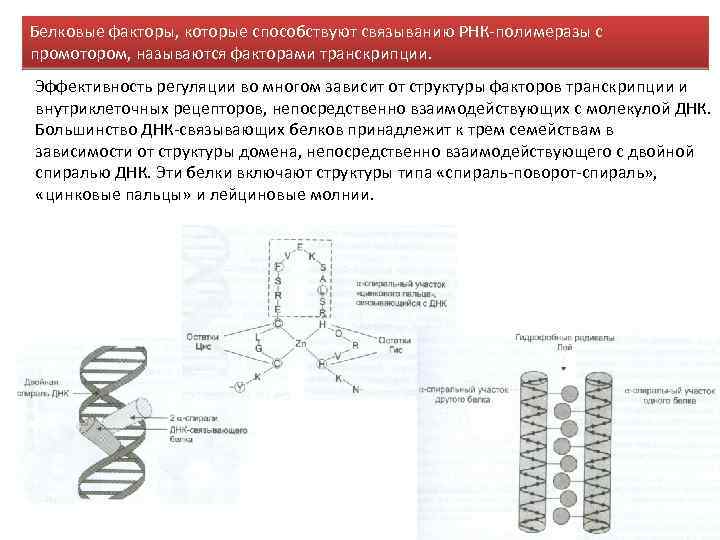 Белковые факторы, которые способствуют связыванию РНК-полимеразы с промотором, называются факторами транскрипции. Эффективность регуляции во многом зависит от структуры факторов транскрипции и внутриклеточных рецепторов, непосредственно взаимодействующих с молекулой ДНК. Большинство ДНК-связывающих белков принадлежит к трем семействам в зависимости от структуры домена, непосредственно взаимодействующего с двойной спиралью ДНК. Эти белки включают структуры типа «спираль-поворот-спираль» , «цинковые пальцы» и лейциновые молнии.
Белковые факторы, которые способствуют связыванию РНК-полимеразы с промотором, называются факторами транскрипции. Эффективность регуляции во многом зависит от структуры факторов транскрипции и внутриклеточных рецепторов, непосредственно взаимодействующих с молекулой ДНК. Большинство ДНК-связывающих белков принадлежит к трем семействам в зависимости от структуры домена, непосредственно взаимодействующего с двойной спиралью ДНК. Эти белки включают структуры типа «спираль-поворот-спираль» , «цинковые пальцы» и лейциновые молнии.
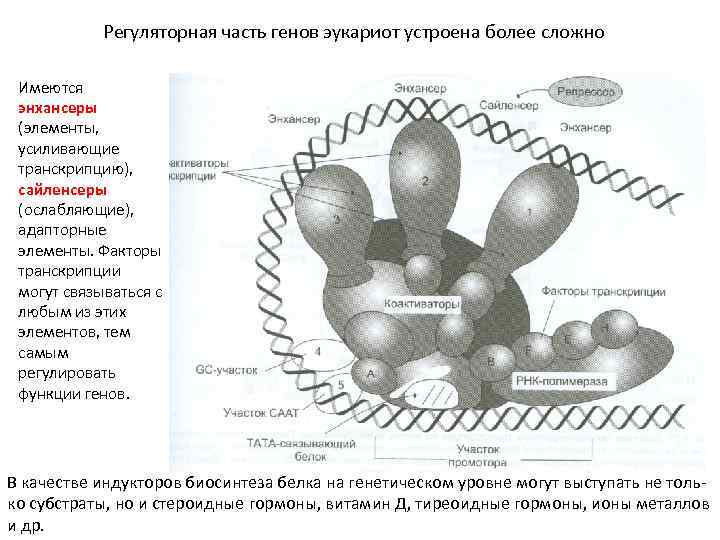 Регуляторная часть генов эукариот устроена более сложно Имеются энхансеры (элементы, усиливающие транскрипцию), сайленсеры (ослабляющие), адапторные элементы. Факторы транскрипции могут связываться с любым из этих элементов, тем самым регулировать функции генов. В качестве индукторов биосинтеза белка на генетическом уровне могут выступать не только субстраты, но и стероидные гормоны, витамин Д, тиреоидные гормоны, ионы металлов и др.
Регуляторная часть генов эукариот устроена более сложно Имеются энхансеры (элементы, усиливающие транскрипцию), сайленсеры (ослабляющие), адапторные элементы. Факторы транскрипции могут связываться с любым из этих элементов, тем самым регулировать функции генов. В качестве индукторов биосинтеза белка на генетическом уровне могут выступать не только субстраты, но и стероидные гормоны, витамин Д, тиреоидные гормоны, ионы металлов и др.

 Дифтерийный токсин Под действием протеолитических ферментов клеток хозяина белок распадается на два фрагмента. Один фрагмент представляет собой фермент АДФ-рибозилтрансферазу, катализирующий модификацию фактора элонгации EF 2. Такой фактор элонгации теряет способность участвовать в транслокации рибосомы, и трансляция прекращается. Рицин Смертельный растительный лектин. Найден в касторовом семени, катализирует распад р. РНК большой субъединицы рибосом эукариот -аманитин Токсичное начало бледной поганки. Блокирует синтез м. РНК, осуществляемый РНК-полимеразой II, но не влияет на синтез РНК у прокариот. Интерфероны Индуцируют синтез фермента, который синтезирует олигонуклеотид, последний активирует РНК-азу, которая разрушает м. РНК
Дифтерийный токсин Под действием протеолитических ферментов клеток хозяина белок распадается на два фрагмента. Один фрагмент представляет собой фермент АДФ-рибозилтрансферазу, катализирующий модификацию фактора элонгации EF 2. Такой фактор элонгации теряет способность участвовать в транслокации рибосомы, и трансляция прекращается. Рицин Смертельный растительный лектин. Найден в касторовом семени, катализирует распад р. РНК большой субъединицы рибосом эукариот -аманитин Токсичное начало бледной поганки. Блокирует синтез м. РНК, осуществляемый РНК-полимеразой II, но не влияет на синтез РНК у прокариот. Интерфероны Индуцируют синтез фермента, который синтезирует олигонуклеотид, последний активирует РНК-азу, которая разрушает м. РНК
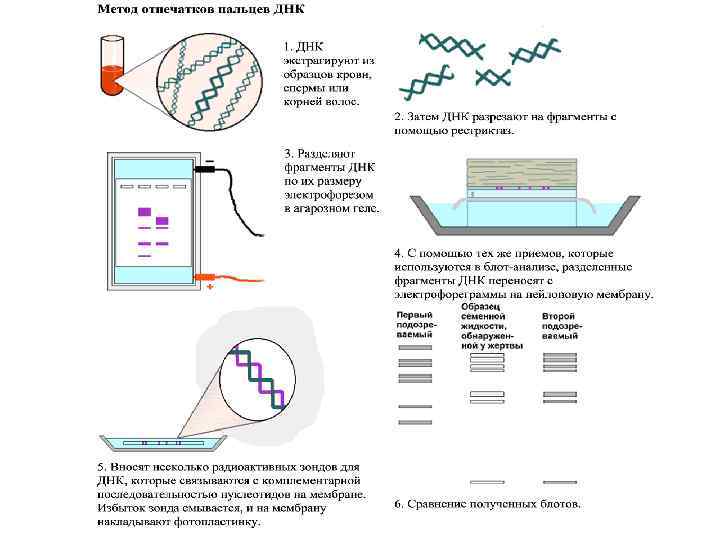
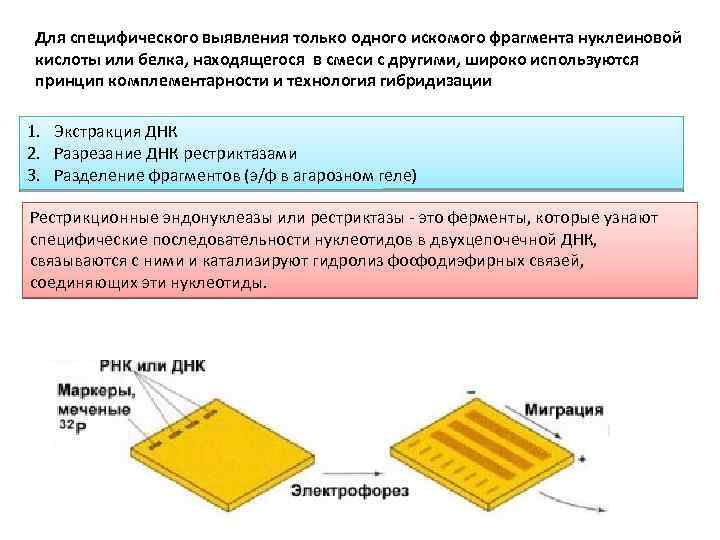 Для специфического выявления только одного искомого фрагмента нуклеиновой кислоты или белка, находящегося в смеси с другими, широко используются принцип комплементарности и технология гибридизации 1. Экстракция ДНК 2. Разрезание ДНК рестриктазами 3. Разделение фрагментов (э/ф в агарозном геле) Рестрикционные эндонуклеазы или рестриктазы - это ферменты, которые узнают специфические последовательности нуклеотидов в двухцепочечной ДНК, связываются с ними и катализируют гидролиз фосфодиэфирных связей, соединяющих эти нуклеотиды.
Для специфического выявления только одного искомого фрагмента нуклеиновой кислоты или белка, находящегося в смеси с другими, широко используются принцип комплементарности и технология гибридизации 1. Экстракция ДНК 2. Разрезание ДНК рестриктазами 3. Разделение фрагментов (э/ф в агарозном геле) Рестрикционные эндонуклеазы или рестриктазы - это ферменты, которые узнают специфические последовательности нуклеотидов в двухцепочечной ДНК, связываются с ними и катализируют гидролиз фосфодиэфирных связей, соединяющих эти нуклеотиды.
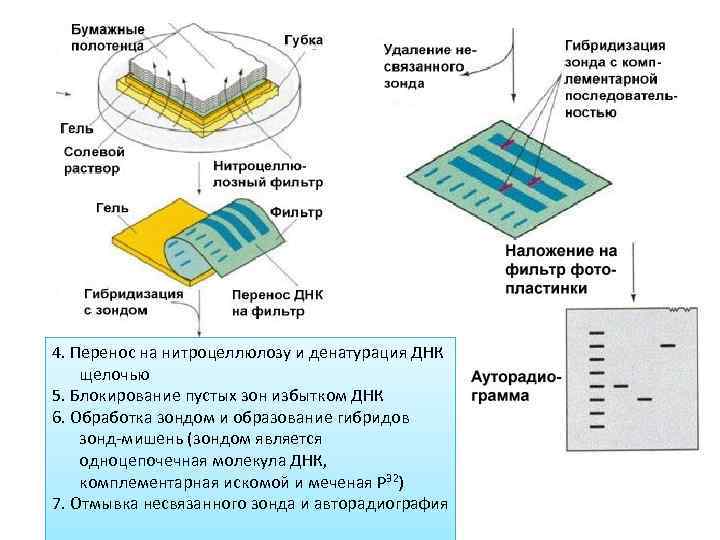 4. Перенос на нитроцеллюлозу и денатурация ДНК щелочью 5. Блокирование пустых зон избытком ДНК 6. Обработка зондом и образование гибридов зонд-мишень (зондом является одноцепочечная молекула ДНК, комплементарная искомой и меченая Р 32) 7. Отмывка несвязанного зонда и авторадиография
4. Перенос на нитроцеллюлозу и денатурация ДНК щелочью 5. Блокирование пустых зон избытком ДНК 6. Обработка зондом и образование гибридов зонд-мишень (зондом является одноцепочечная молекула ДНК, комплементарная искомой и меченая Р 32) 7. Отмывка несвязанного зонда и авторадиография
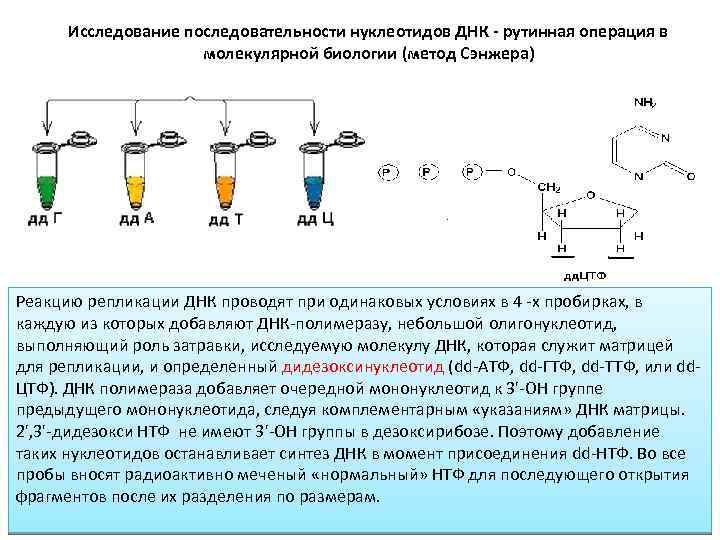 Исследование последовательности нуклеотидов ДНК - рутинная операция в молекулярной биологии (метод Сэнжера) Реакцию репликации ДНК проводят при одинаковых условиях в 4 -х пробирках, в каждую из которых добавляют ДНК-полимеразу, небольшой олигонуклеотид, выполняющий роль затравки, исследуемую молекулу ДНК, которая служит матрицей для репликации, и определенный дидезоксинуклеотид (dd-АТФ, dd-ГТФ, dd-ТТФ, или dd. ЦТФ). ДНК полимераза добавляет очередной мононуклеотид к 3'-ОН группе предыдущего мононуклеотида, следуя комплементарным «указаниям» ДНК матрицы. 2', 3'-дидезокси НТФ не имеют 3'-ОН группы в дезоксирибозе. Поэтому добавление таких нуклеотидов останавливает синтез ДНК в момент присоединения dd-НТФ. Во все пробы вносят радиоактивно меченый «нормальный» НТФ для последующего открытия фрагментов после их разделения по размерам.
Исследование последовательности нуклеотидов ДНК - рутинная операция в молекулярной биологии (метод Сэнжера) Реакцию репликации ДНК проводят при одинаковых условиях в 4 -х пробирках, в каждую из которых добавляют ДНК-полимеразу, небольшой олигонуклеотид, выполняющий роль затравки, исследуемую молекулу ДНК, которая служит матрицей для репликации, и определенный дидезоксинуклеотид (dd-АТФ, dd-ГТФ, dd-ТТФ, или dd. ЦТФ). ДНК полимераза добавляет очередной мононуклеотид к 3'-ОН группе предыдущего мононуклеотида, следуя комплементарным «указаниям» ДНК матрицы. 2', 3'-дидезокси НТФ не имеют 3'-ОН группы в дезоксирибозе. Поэтому добавление таких нуклеотидов останавливает синтез ДНК в момент присоединения dd-НТФ. Во все пробы вносят радиоактивно меченый «нормальный» НТФ для последующего открытия фрагментов после их разделения по размерам.
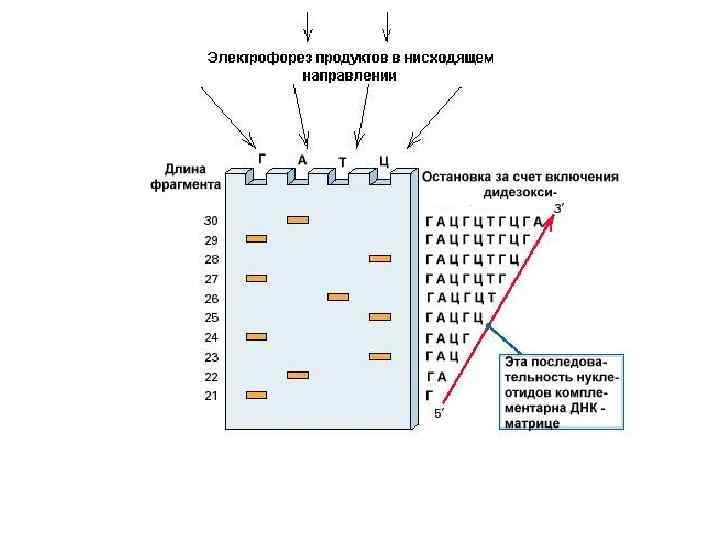
 ПЦР – полимеразная цепная реакция 1. Интересующий участок ДНК 2. ДНК денатурирована 3. Праймеры присоединены к каждой цепи 4. За праймером на каждой цепи синтезируется новая цепь ДНК 5. В следующем цикле происходит денатурация вновь образованных молекул ДНК. Затем присоединяются праймеры, и количество цепей ДНК опять удваивается. Три этапа полимеразной реакции проводятся в одном и том же сосуде, но при разной температуре. (1) Вначале двойную спираль ДНК разделяют на две цепи. Эту достигается нагреванием до 90 -950 С в течение 30 сек. Праймер не может связываться при такой высокой температуре с цепями ДНК. (2) Поэтому сосуд охлаждают до 550 С. Охлаждение вызывает «отжиг» праймера. Он присоединяется к концам цепей ДНК. Процедура занимает около 20 сек. (3) Затем в дело вступает Taq полимераза. Ее температурный оптимум - 750 С (температура горячего источника, где была открыта бактерия). Фермент начинает катализировать присоединение нуклеотидов к праймеру и таким образом постепенно образует копию матрицы. На этом полимеразный цикл завершается.
ПЦР – полимеразная цепная реакция 1. Интересующий участок ДНК 2. ДНК денатурирована 3. Праймеры присоединены к каждой цепи 4. За праймером на каждой цепи синтезируется новая цепь ДНК 5. В следующем цикле происходит денатурация вновь образованных молекул ДНК. Затем присоединяются праймеры, и количество цепей ДНК опять удваивается. Три этапа полимеразной реакции проводятся в одном и том же сосуде, но при разной температуре. (1) Вначале двойную спираль ДНК разделяют на две цепи. Эту достигается нагреванием до 90 -950 С в течение 30 сек. Праймер не может связываться при такой высокой температуре с цепями ДНК. (2) Поэтому сосуд охлаждают до 550 С. Охлаждение вызывает «отжиг» праймера. Он присоединяется к концам цепей ДНК. Процедура занимает около 20 сек. (3) Затем в дело вступает Taq полимераза. Ее температурный оптимум - 750 С (температура горячего источника, где была открыта бактерия). Фермент начинает катализировать присоединение нуклеотидов к праймеру и таким образом постепенно образует копию матрицы. На этом полимеразный цикл завершается.
 PCR-SSCP анализ генов нормального и серповидноклеточного -глобина
PCR-SSCP анализ генов нормального и серповидноклеточного -глобина
 Биочипы будут составлять основу биомедицины 21 века Что такое биочипы? Точнее всего их описывает английское название DNA-microarrays, т. е. это организованное размещение молекул ДНК на небольшой площади специального носителя и считывать с этой площади информацию с помощью флуоресцентного микроскопа или специального лазерного устройства для чтения. Изготовленный таким образом биочип в дальнейшем гибридизуют с молекулами ДНК, мечеными красителем. Сравнивают, например, ДНК, выделенную из здоровых клеток, и ДНК, выделенную из раковых клеток. Часто сравнивают ДНК, выделенную из материала разных больных. После гибридизации на биочипе возникают причудливые узоры. Эти узоры бывают разными у нормальных и у раковых клеток или сильно различаются при различных видах лейкозов. В России разработали биочипы, которые применяются для диагностики оспы, холеры, гепатита, СПИДа, венерических заболеваний, выявления других особо опасных инфекций, вирусологического анализа донорской крови и так далее.
Биочипы будут составлять основу биомедицины 21 века Что такое биочипы? Точнее всего их описывает английское название DNA-microarrays, т. е. это организованное размещение молекул ДНК на небольшой площади специального носителя и считывать с этой площади информацию с помощью флуоресцентного микроскопа или специального лазерного устройства для чтения. Изготовленный таким образом биочип в дальнейшем гибридизуют с молекулами ДНК, мечеными красителем. Сравнивают, например, ДНК, выделенную из здоровых клеток, и ДНК, выделенную из раковых клеток. Часто сравнивают ДНК, выделенную из материала разных больных. После гибридизации на биочипе возникают причудливые узоры. Эти узоры бывают разными у нормальных и у раковых клеток или сильно различаются при различных видах лейкозов. В России разработали биочипы, которые применяются для диагностики оспы, холеры, гепатита, СПИДа, венерических заболеваний, выявления других особо опасных инфекций, вирусологического анализа донорской крови и так далее.
 Клонирование - способ получения больших количеств идентичных молекул нуклеиновых кислот или их фрагментов Известны несколько основных классов векторов, позволяющих встраивать исследуемый нуклеотидный фрагмент в геном клетки хозяина. К ним относятся плазмиды, ламбда бактериофаги, хромосомы дрожжей или бактерий. Выбор определяется размерами переносимого фрагмента. Плазмиды могут переносить фрагменты менее 10000 пар оснований, бактериофаги –до 25000. Для переноса более крупных фрагментов используют векторы - химеры (плазмида-ламбда вектор), называемые космидами. Еще более крупные фрагменты, необходимые для работы с геномом человека, переносят с использованием хромосомы дрожжей.
Клонирование - способ получения больших количеств идентичных молекул нуклеиновых кислот или их фрагментов Известны несколько основных классов векторов, позволяющих встраивать исследуемый нуклеотидный фрагмент в геном клетки хозяина. К ним относятся плазмиды, ламбда бактериофаги, хромосомы дрожжей или бактерий. Выбор определяется размерами переносимого фрагмента. Плазмиды могут переносить фрагменты менее 10000 пар оснований, бактериофаги –до 25000. Для переноса более крупных фрагментов используют векторы - химеры (плазмида-ламбда вектор), называемые космидами. Еще более крупные фрагменты, необходимые для работы с геномом человека, переносят с использованием хромосомы дрожжей.
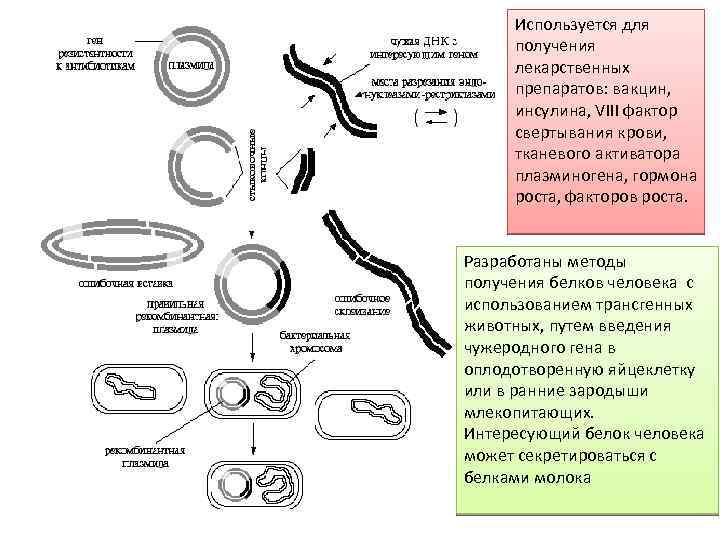 Используется для получения лекарственных препаратов: вакцин, инсулина, VIII фактор свертывания крови, тканевого активатора плазминогена, гормона роста, факторов роста. Разработаны методы получения белков человека с использованием трансгенных животных, путем введения чужеродного гена в оплодотворенную яйцеклетку или в ранние зародыши млекопитающих. Интересующий белок человека может секретироваться с белками молока
Используется для получения лекарственных препаратов: вакцин, инсулина, VIII фактор свертывания крови, тканевого активатора плазминогена, гормона роста, факторов роста. Разработаны методы получения белков человека с использованием трансгенных животных, путем введения чужеродного гена в оплодотворенную яйцеклетку или в ранние зародыши млекопитающих. Интересующий белок человека может секретироваться с белками молока
 Генная терапия Лечение наследственных и инфекционных заболеваний путем введения в соматические клетки пациентов генов, которые обеспечивают исправление генных дефектов или придают клеткам новые функции. Первый клинический опыт в 1990 г. В г. Бетесда (США) на 4 -хлетней девочке, страдавшей наследственным иммунодефицитом, вызванным мутацией в гене аденозиндезаминазы. Две задачи для успешного результата: • обеспечить эффективную доставку чужеродного гена в клетки-мишени • создать условия длительной экспрессии гена в этих клетках В геном пациента чужеродная ДНК может вводиться либо в культуре клеток (ex vivo), либо непосредственно в организм больного (in vivo) Из 175 уже одобренных протоколов клинических испытаний по генотерапии более 120 основаны на применении ретровирусных векторов Современный уровень знаний не позволяет проводить коррекцию генных дефектов на уровне половых клеток и клеток ранних доимплантационных зародышей человека в связи с опасностью засорения генофонда
Генная терапия Лечение наследственных и инфекционных заболеваний путем введения в соматические клетки пациентов генов, которые обеспечивают исправление генных дефектов или придают клеткам новые функции. Первый клинический опыт в 1990 г. В г. Бетесда (США) на 4 -хлетней девочке, страдавшей наследственным иммунодефицитом, вызванным мутацией в гене аденозиндезаминазы. Две задачи для успешного результата: • обеспечить эффективную доставку чужеродного гена в клетки-мишени • создать условия длительной экспрессии гена в этих клетках В геном пациента чужеродная ДНК может вводиться либо в культуре клеток (ex vivo), либо непосредственно в организм больного (in vivo) Из 175 уже одобренных протоколов клинических испытаний по генотерапии более 120 основаны на применении ретровирусных векторов Современный уровень знаний не позволяет проводить коррекцию генных дефектов на уровне половых клеток и клеток ранних доимплантационных зародышей человека в связи с опасностью засорения генофонда


