Н. Заболоцкий Не позволяй душе


Н. Заболоцкий Не позволяй душе лениться! Чтоб воду в ступе не толочь, Душа обязана трудиться, И день, и ночь, и день, и ночь!

Вариант-1 Вариант-2 Водород является продуктом Водород в лаборатории получают А взаимодействия: 1) Cu + HCl; 2) Zn + HCl; взаимодействием: 1)железа с водой; 3) Cu + H 2 O; 4) S + Na. OH 2) 2) натрия с водой; 3) оксида кальция с водой; 4) цинка с соляной кислотой. Укажите валентность фосфора в Индивидуальным веществом является: Б водородном соединении: 1) I; 2) II; 1) чугун; 2) водород; 3) III; 4) V 3) соляная кислота; 4) воздух. Водород реагирует с: Водород не реагирует с: В 1) Н 2 О; 3) Cl 2; 2) SO 3; 4) Au 1) N 2; 3) O 2; 2) S; 4) HCl В промышленности водород Водород реагирует: Г получают : 1) Из метана ; 1) только с простыми веществами; 2) с простыми и сложными 2) железа с водой; веществами; 3) электролизом воды; 3) только со сложными 4) цинка с соляной кислотой. веществами;

Вариант-1 Вариант-2 Водород является продуктом Водород в лаборатории получают А взаимодействия: 1) Cu + HCl; 2) Zn + HCl; взаимодействием: 1)железа с водой; 3) Cu + H 2 O; 4) S + Na. OH 2) 2) натрия с водой; 3) оксида кальция с водой; 4) цинка с соляной кислотой. Укажите валентность фосфора в Индивидуальным веществом является: Б водородном соединении: 1) I; 2) II; 1) чугун; 2) водород; 3) III; 4) V 3) соляная кислота; 4) воздух. Водород реагирует с: Водород не реагирует с: В 1) Н 2 О; 3) Cl 2; 2) SO 3; 4) Au 1) N 2; 3) O 2; 2) S; 4) HCl В промышленности водород Водород реагирует: Г получают : 1) Из метана 1) только с простыми веществами; 2) с простыми и сложными 2) железа с водой; веществами; 3) электролизом воды; 3) только со сложными 4) цинка с соляной кислотой. веществами;

Тема урока:

Цели урока: • рассмотреть положение галогенов в Периодической Системе Д. И. Менделеева; • рассмотреть строение их атомов и характерные степени окисления; • изучить физические и химические свойства; • ознакомиться с характерными способами получения галогенов.

Пункты назначения: 1. Положение в ПС ↓ 2. Строение атомов и характерные степени окисления ↓ 3. Физические свойства ↓ 4. Способы получения ↓ 5. Химические свойства

Положение в ПСХЭ, строение атома, физические свойства
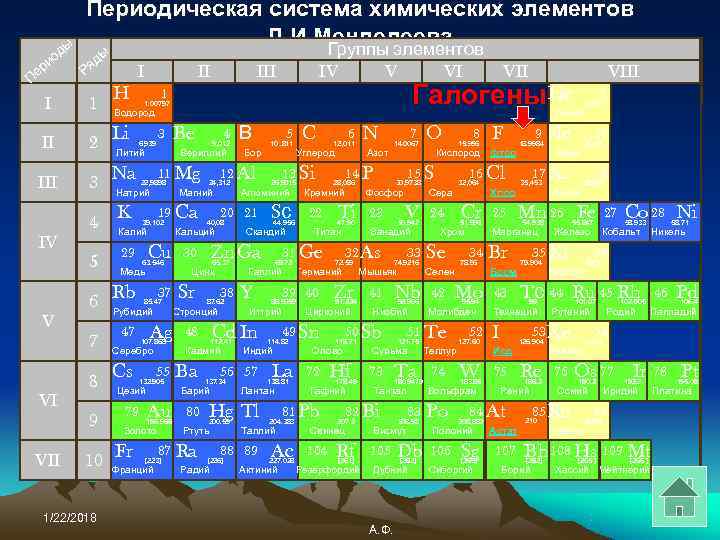
Периодическая система химических элементов ы Д. И. Менделеева Группы элементов од д ы ри Ря III IV VII VIII Пе I 1 H Водород 1. 00797 1 Галогены He Гелий 4, 003 2 II 2 Li 6, 939 3 Be 4 9, 012 В 5 10. 811 C 12, 011 6 N 7 14. 0067 O 8 15. 996 F 9 18. 9984 Ne 20, 18 10 Литий Вериллий Бор Углерод Азот Кислород фтор Неон III 3 Na 22, 9898 11 Mg 12 Al 24, 312 13 Si 26, 9815 14 P 28, 086 15 S 30, 9738 16 Cl 32, 064 17 Ar 35, 453 39, 948 18 Натрий Магний Алюминий Кремний Фосфор Сера Хлор Аргон 4 K 39. 102 19 Ca 40, 08 20 21 Sс 44. 956 22 Ti 47. 90 23 V 50. 942 24 Cr 51. 996 25 Mn 26 Fe 54. 938 55. 847 27 Co 28 Ni 58. 933 58. 71 Калий Кальций Скандий Титан Ванадий Хром Марганец Железо Кобальт Никель IV 5 29 Cu 63. 546 30 Zn Ga 65. 37 31 Ge 69. 72 32 As 72. 59 33 74. 9216 Se 34 78. 96 Br 35 Kr 79. 904 83, 8 36 Медь Цинк Галлий Германий Мышьяк Селен Бром Криптон 6 Rb 85. 47 37 Sr 87. 62 38 Y 39 40 88. 9059 Zr 91. 224 41 Nb 92. 906 42 Mo 95. 94 43 Tс 44 Ru 45 Rh 99 101. 07 102. 905 46 Pd 106. 4 Рубидий Стронций Иттрий Цирконий Ниобий Молибден Технеций Рутений Родий Палладий V 7 47 Ag 107. 868 48 Cd In 112. 41 49 Sn 114. 82 50 Sb 118. 71 51 Te 121. 75 52 127. 60 I 53 Xe 126. 904 131, 3 54 Серебро Кадмий Индий Олово Сурьма Теллур Иод Ксенон 8 Cs 55 132. 905 Ba 137. 34 56 57 La 138. 81 72 Hf 178. 49 73 Ta 180. 9479 74 W 183. 85 75 Re 186. 2 76 Os 77 Ir 78 Pt 190. 2 192. 2 195. 09 Цезий Барий Лантан Гафний Тантал Вольфрам Рений Осмий Иридий Платина VI 9 79 Au 196. 966 80 Hg Tl 200. 59 81 Pb 204. 383 82 Bi 207. 2 83 208. 98 Po 84 At 208. 982 210 85 Rn [222] 86 Золото Ртуть Таллий Свинец Висмут Полоний Астат Радон VII 10 Fr 87 Ra [223] [226] 88 89 Ac 227. 028 104 Rf [261] 105 Db [262] 106 Sg [263] 107 Bh 108 Hs 109 Mt [262] [265 ] [266 ] Франций Радий Актиний Резерфордий Дубний Сиборгий Борий Хассий Мейтнерий 1/22/2018 А. Ф.

Периодическая система химических элементов ы Д. И. Менделеева Группы элементов од д ы ри Ря I III IV V VI VIII Пе I 1 Фтор/Fluorum (F) Внешний вид Бледно-жёлтый газ. II 2 простого вещества Очень ядовит. III 3 Электронная [He] 2 s 2 2 p 5 4 коефигуранция IV ЭО 3, 98 5 (по Полингу) Степень окисления − 1 6 V Плотность (при − 189 °C)1, 108 7 г/см ³ Температура 53, 53 К 8 плавления VI 9 Температура 85, 01 К кипения VII 10 1/22/2018 А. Ф.

F 2 Анри Муассан в 1866 г. – фр. ученый(греч. - фторос – разрушающий)

История открытия фтора В 1886 году французский химик А. Муассан, используя электролиз жидкого фтороводорода, охлажденного до температуры – 23°C (в жидкости должно содержаться немного фторида калия, который обеспечивает ее электропроводимость), смог на аноде получить первую порцию нового, газа. В первых опытах для получения фтора Анри Муассан использовал очень дорогой Муассан электролизер, изготовленный из платины и (1852 – иридия. При этом каждый грамм 1907) полученного фтора «съедал» до 6 г платины. 1/22/2018 А. Ф.

Периодическая система химических элементов ы Д. И. Менделеева Группы элементов од д ы ри Ря I III IV V VII VIII Пе I 1 Хлор / Chlorum (Cl) Внешний вид Газ жёлто-зеленого II 2 простого вещества цвета с резким III 3 запахом. Ядовит. Электронная [Ne] 3 s 2 3 p 5 4 коефигуранция IV ЭО 3. 16 5 (по Полингу) 6 Степень окисления 7, 6, 5, 4, 3, 1, − 1 V Плотность (при − 33. 6 °C)1, 56 7 г/см ³ Температура 172. 2 К 8 VI плавления 9 Температура 238. 6 К кипения VII 10 1/22/2018 А. Ф.

Cl 2 Карл Шееле в 1774 г. – шведский ученый (греч. - хлорос – желто- зеленый
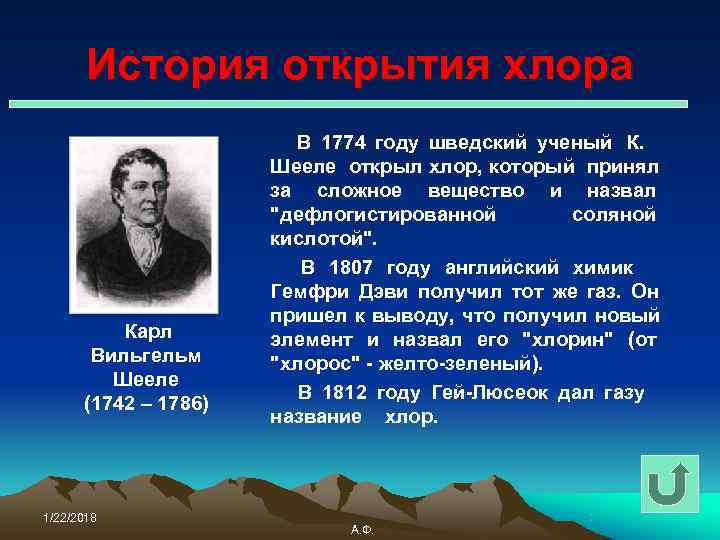
История открытия хлора В 1774 году шведский ученый К. Шееле открыл хлор, который принял за сложное вещество и назвал "дефлогистированной соляной кислотой". В 1807 году английский химик Гемфри Дэви получил тот же газ. Он пришел к выводу, что получил новый Карл элемент и назвал его "хлорин" (от Вильгельм "хлорос" - желто-зеленый). Шееле В 1812 году Гей-Люсеок дал газу (1742 – 1786) название хлор. 1/22/2018 А. Ф.

Периодическая система химических элементов ы Д. И. Менделеева Группы элементов од д ы ри Ря I III IV V VI VIII Пе I 1 Бром / Bromum (Br) Внешний вид красно-бурая II 2 простого вещества жидкость с III 3 сильным неприятным 4 запахом IV Электронная [Ar] 3 d 10 4 s 2 4 p 5 конфигуранция 6 ЭО 2, 96 V (по Полингу) 7 Степень окисления 7, 5, 3, 1, -1 Плотность 3, 12 г/см³ 8 VI Температура 265, 9 К 9 плавления Температура 331, 9 К VII 10 кипения 1/22/2018 А. Ф.

Br 2 Балар в 1826 г. – фр. ученый ( греч. – бромос – зловонный)

История открытия брома В 1825 году французский химик А. Ж. Балар при изучении маточных рассолов выделил темно-бурую жидкость, который он назвал - "мурид" (от латинского слова muria, означающего "рассол"). Комиссия Академии, проверив это сообщение, подтвердила открытие Балара и предложила назвать элемент Антуан Жером бромом (от "бромос", с греческого Балар "зловонный"). (1802 – 1876) 1/22/2018 А. Ф.
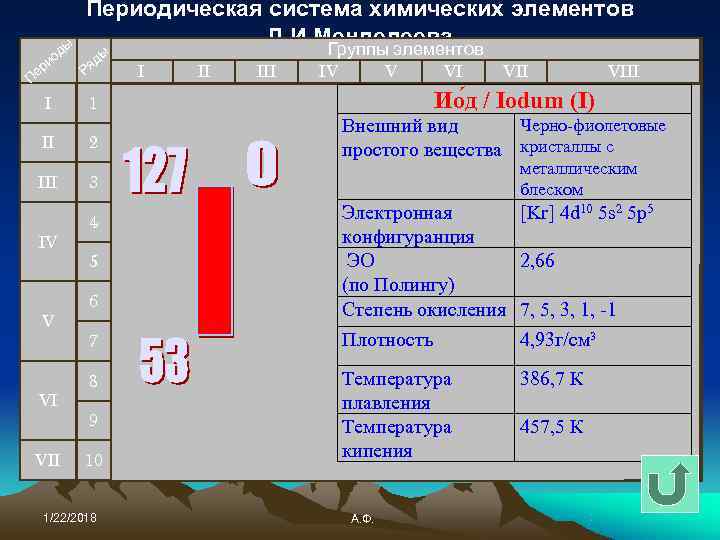
Периодическая система химических элементов ы Д. И. Менделеева Группы элементов од д ы ри Ря I III IV V VIII Пе I 1 Ио д / Iodum (I) Внешний вид Черно-фиолетовые II 2 простого вещества кристаллы с металлическим III 3 блеском 4 Электронная [Kr] 4 d 10 5 s 2 5 p 5 IV конфигуранция 5 ЭО 2, 66 (по Полингу) 6 Степень окисления 7, 5, 3, 1, -1 V 7 Плотность 4, 93 г/см³ 8 Температура 386, 7 К VI плавления 9 Температура 457, 5 К VII 10 кипения 1/22/2018 А. Ф.

I 2 Куртуа в 1811 г. – фр. ученый (греч. иодэс – фиолетовый)

История открытия йода В 1811 году французский химик Бернар Куртуа открыл иод путём перегонки маточных растворов от своего азотнокислого кальция с серной кислотой Чтобы другие химики могли изучать новое вещество, Б. Куртуа подарил его (правда, очень небольшое количество) фармацевтической Бернар Куртуа фирме в Дижоне. (1777 – 1838 ) В 1813 году Ж. -Л. Гей-Люссак подробно изучил этот элемент и дал ему современное название. Название "иод" происходит от греческого слова "иодэс" - "фиолетовый" (по цвету паров). 1/22/2018 А. Ф.
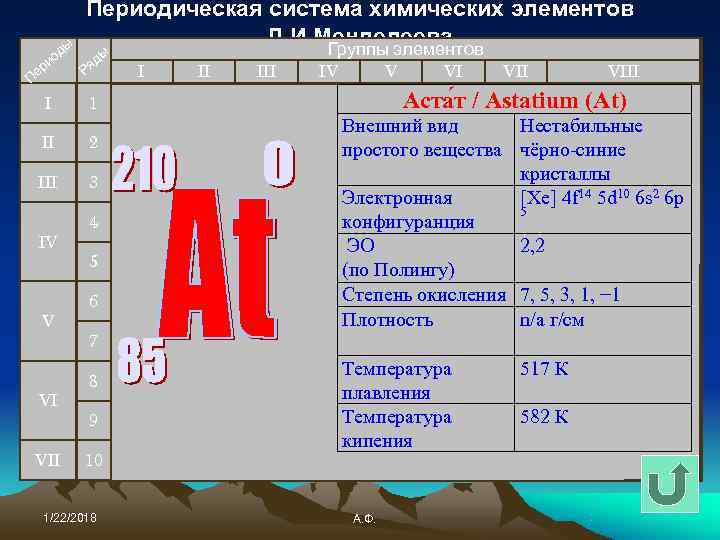
Периодическая система химических элементов ы Д. И. Менделеева Группы элементов од д ы ри Ря I III IV V VII VIII Пе I 1 Аста т / Astatium (At) Внешний вид Нестабильные II 2 простого вещества чёрно-синие III 3 кристаллы Электронная [Xe] 4 f 14 5 d 10 6 s 2 6 p 5 4 конфигуранция IV ЭО 2, 2 5 (по Полингу) 6 Степень окисления 7, 5, 3, 1, − 1 V Плотность n/a г/см 7 Температура 517 К 8 VI плавления 9 Температура 582 К кипения VII 10 1/22/2018 А. Ф.

Аt Был предсказан Менделеевым Д. И. под названием «ЭКАИОД» . Синтезировали его американские ученые в 1940 г. Корсон, Маккензи и Сегре по ядерной реакции (греч. – астатос – неустойчивый)

Строение атомов галогенов На Только F R -1, 0 окисли атома внешнем тель энергети Cl ческом +7, +5, уровне +3, +1, Br 7 0, -1 электро I нов At Окислител ьные свойства

Способы получения 1. Электролиз расплава соли: 2 Na. Cl → 2 Na + Cl 2 2. Окисление хлороводорода оксидом марганца 4 Mn. O 2 +4 HCl → Cl 2 + Mn. Cl 2 + 2 H 2 O 3. Окисление иодида перекисью водорода H 2 O 2 + 2 KI + H 2 SO 4 → I 2 + K 2 SO 4 + 2 H 2 O

Химические свойства галогенов + Н 2 +1 -1 HHal 2 +не. Ме +n -1 не. Ме. Haln +Ме +n -1 Ме. Haln

Химические свойства Cl 2 - сильно реакционноспособен (искл. C, O 2, N 2 и некот. др. ) С простыми веществами: С металлами С неметаллами Fe + Cl 2 → Cu + Cl 2 → H 2 + Cl 2 → P + Cl 2 → с сурьмой. mpg Cl 2+K. wmv Со сложными веществами: отбел-е. wmv H 2 O + Cl 2 → Na. OH + Cl 2 → KBr + Cl 2 → KI + Cl 2 → 1/22/2018 А. Ф.

Химические свойства 45 F 2 -наиболее реакционноспособен , реакции идут на холоду, при нагревании – даже с участием Au, Pt. С простыми веществами: С металлами С неметаллами Na + F 2 → H 2 + F 2 → Mo + F 2 → Xe + F 2 → Со сложными веществами: H 2 O + F 2 → KCl + F 2 → KBr + F 2 → KI + F 2 → Проверить 1/22/2018 А. Ф.

Химические свойства 45 F 2 -наиболее реакционноспособен , реакции идут на холоду, при нагревании – даже с участием Au, Pt. С простыми веществами: С металлами С неметаллами 2 Na + F 2 → 2 Na. F H 2 + F 2 → 2 HF Mo + 3 F 2 → Mo. F 6 Xe + 2 F 2 → Xe. F 4 Со сложными веществами: 2 H 2 O + F 2 → 4 HF + O 2 2 KCl + F 2 → Cl 2 + 2 Na. F 2 KBr + F 2 → Br 2 + 2 КF 2 KI + F 2 → I 2 + 2 КF 1/22/2018 А. Ф. А. Ф.

Химические свойства Br 2 - реакционноспособен С простыми веществами: С металлами С неметаллами Al+Br 2. wmv H 2 + Br 2 → Cu + Br 2 → P + Br 2 → Со сложными веществами: Br 2 + H 2 O → KI + Br 2 → Проверить 1/22/2018 А. Ф.

Химические свойства I 2 - химически наименее активен С простыми веществами: С металлами С неметаллами Hg + I 2 → H 2 + I 2 → Al+J 2. wmv P + Br 2 → Со сложными веществами: Действие крахмала на I 2 + H 2 O → йод 080290. mpg Проверить 1/22/2018 А. Ф.

Химические свойства I 2 - химически наименее активен С простыми веществами: С металлами С неметаллами Hg + I 2 → Hg. I 2 H 2 + I 2 → 2 HCl (tº) 2 Al + 3 I 2 → 2 Al. I 3 2 P + 3 Br 2 → 2 PI 3 Со сложными веществами: I 2 + H 2 O → HI + HIO I 2 + р-р крахмала → темно-синее окрашивание 1/22/2018 А. Ф.
F Сl Кости, зубы Кровь, желудочный сок Br I Регуляция нервных обмена веществ процессов 1/22/2018 А. Ф.
Тефлон Фтор Заменител ь крови Фториды Фреон в зубных пастах Окислитель ракетного топлива 1/22/2018 А. Ф.

Дезинфекция Органические воды раствори- Отбеливатели тели Лекарственные Применени Хлорирование препараты органических е хлора веществ Производство Получение HCl неорганических брома, йода хлоридов 1/22/2018 А. Ф.
Лекарственные препараты Ветеренарные Фотографи препараты я Применени е брома Присадки Красители к бензину Ингибиторы 1/22/2018 А. Ф.
Лекарственные Дезинфекци препараты я одежды Применение йода Фотография Красители Электролампы 1/22/2018 А. Ф.

Химические свойства галогенов Найди соответствие между исходными веществами и продуктами реакций 2 H 2 O + 2 F 2 = 2 Na. OH + H 2 +Cl 2 Xe + 2 F 2 = 2 Na. Cl + I 2 H 2 + F 2 = 2 Au. Cl 3 2 Au + 3 Cl 2 = Xe. F 4 2 Na. Cl + 2 H 2 O = 4 HF + O 2 2 Na. I + Cl 2 = 2 HF 1/22/2018

Спасибо за урок! Благодарю за сотрудничество. 1/22/2018 А. Ф.

