водно минеральный обмен, гормоны.ppt
- Количество слайдов: 193

n Водно-минеральный обмен ПОНЯТИЕ О ГОМЕОСТАЗЕ Слово «гомеостаз» означает постоянство внутренней среды организма (кровь, лимфу, межклеточная жидкость и др), химический состав которых примерно одинаков. Важнейшей особенностью внутренней среды организма является удивительное постоянство ее основных биохимических показателей. n Названные биологические жидкости представляют собой водные растворы органических (белки, глюкоза, разнообразные продукты промежуточного обмена и др. ) и неорганических (минеральных) веществ, каждое из которых выполняет свои специфические функции.

n ОБМЕН ВОДЫ В количественном отношении вода является самой значительной составной частью организма. Все реакции обмена веществ протекают в водной среде, в ней существуют и поддерживают взаимосвязь клетки организма. Вода составляет основу всех биологических жидкостей от крови до мочи. В среднем вода составляет 2/3 массы тела человека, но это количество может существенно меняться с возрастом. У 4 месячного эмбриона в клетках содержится 94%, а у взрослых — 50 — 60% воды. Ее уровень также зависит от пола: в организме мужчин воды больше, чем у женщин. Кроме того, различные ткани и органы отличаются по количеству содержащейся в них воды: кости, соединительная ткань бедны водой, тогда как в крови и мышцах ее много.

Вся жидкость организма подразделяется на внутри- и внеклеточную. Внутриклеточная жидкость составляет около 2/3 всей воды организма и во всех клетках имеет примерно одинаковый состав. В ней преобладают ионы калия, анионы белка и фосфатов. Внеклеточная вода (1/3 часть всей воды) образует в организме единую фазу и содержит высокие концентрации хлоридов и бикарбонатов натрия. У здорового человека существует водное равновесие. Потребность в воде меняется с возрастом: взрослому человеку необходимо воды около 15 мл/кг в сутки, а ребенку — в 3 раза больше, что зависит, прежде всего, от интенсивности обмена веществ.

В водном обмене принимают участие почки, легкие, кожа, пищеварительная система, эндокринные железы и т. д. Почки являются главным органом, участвующим в обмене воды. В условиях недостатка воды они выделяют небольшое количество сильно концентрированной мочи. При избытке воды в организме выводится большой объем сильно разбавленной мочи. Нарушение способности почек концентрировать мочу наблюдается при тяжелых почечных заболеваниях. Легкие выделяют воду в виде водяных паров, которыми насыщен воздух в альвеолах. Количество воды, выводимой легкими, зависит от активности обмена, частоты дыхания, температуры тела. При усиленной мышечной деятельности, лихорадочных состояниях, возбуждении увеличивается объем дыхания и соответственно возрастает количество выводимой воды.

Кожа участвует в водном обмене путем выделения и испарения пота, что зависит от разницы температуры тела и окружающего воздуха. При высокой температуре окружающего воздуха у человека, не прошедшего акклиматизацию, выделяется пот, богатый ионами натрия и хлора, состав которого приближается к составу плазмы крови. У акклиматизированных людей в этом случае выделяется сильно разведенный пот. Выделение пота разного состава является приспособительной реакцией организма.

ОБМЕН МИНЕРАЛЬНЫХ ВЕЩЕСТВ Минеральные вещества относятся к незаменимым факторам питания, поскольку они не синтезируются в организме, но необходимы для деятельности любой его клетки. n Они участвуют в построении органоидов, входят в состав ферментов, гормонов, участвуют в мышечном сокращении, нервной проводимости, поддержании осмотического давления, в обеспечении постоянства р. Н внутренней среды организма и т. д. Содержание их в органах и тканях различно, Са, Р, Мg в основном концентрируются в костях, К преобладает в мышцах, мозге, почках, Nа является основным компонентом плазмы и т. д.

В составе живого вещества найдено более 70 элементов. Элементы необходимые организму для построения и жизнедеятельности клеток и органов, называют биогенными элементами. Существует несколько классификаций биогенных элементов:

А) По их функциональной роли: 1) органогены, в организме их 97, 4% (С, Н, О, N, Р, S), 2) элементы электролитного фона (Na, К, Ca, Mg, Сl). Данные ионы металлов составляют 99% общего содержания металлов в организме; 3) Микроэлементы – это биологически активные атомы центров ферментов, гормонов (переходные металлы). Б) По концентрации элементов в организме биогенные элементы делят: 1) макроэлементы; 2) микроэлементы; 3) ультрамикроэлементы. Биогенные элементы, содержание которых превышает 0, 01% от массы тела, относят к макроэлементам. К ним отнесены 12 элементов: органогены, ионы электролитного фона и железо. Они составляют 99, 99% живого субстрата. Еще более поразительно, что 99% живых тканей содержат только шесть элементов: С, Н, О, N, Р, Ca.

Каждый макроэлемент выполняет свои функции. Так, Na, K, Cl участвуют в поддержании осмотического давления, активируют ряд ферментов, входят в состав органоидов клеток. Кальций является одним из основных структурных компонентов костей, участвует в процессах мышечного сокращения, проведении нервных импульсов, обеспечении проницаемости мембран, свертывании крови. Он обладает способностью накапливаться в местах повреждений тканей, например в легочной ткани, при благоприятном течении туберкулеза, чем способствует рубцеванию очагов поражения. Последнее послужило основанием для применения солей кальция в качестве лекарственных средств при туберкулезе и других заболеваниях.

Р широко представлен в организме как в свободной форме, так и в соединении с различными веществами (белками, жирами, углеводами). Он входит в состав фосфопротеидов, фосфолипидов, мононуклеотидов (АТФ, ГТФ и др. ), фосфатной буферной системы организма. Все это подтверждает важнейшее значение фосфора в процессах обмена веществ. Элементы К, Na, Mg, Fe, Сl, S относят к олигобиогенным элементам. Содержание их колеблется от 0, 1 до 1%. Биогенные элементы, суммарное содержание которых составляет величину порядка 0, 01%, относят к микроэлементам. Содержание каждого из них - 0, 001%.

К важнейшим микроэлементам относится Fe, которое является жизненно важным элементом. Оно входит в состав гемоглобина, миоглобина, окислительно-восстановительных ферментов (каталазы, пероксидазы, цитохромов и др. ). Большая часть железа содержится в эритроцитах, а в печени оно запасается в виде ферритина (комплекса железа со специфическим белком). Mg регулирует нервно-мышечную возбудимость, работу сердца, активирует деятельность ряда ферментов. Из других микроэлементов важную роль выполняют медь, цинк, йод, кобальт, молибден и др. Их основное значение заключается в обеспечении деятельности ферментов, но они имеют и свои особые функции. Так, кобальт входит в состав витамина В улучшает процессы всасывания в кишечнике, способствует синтезу белков мышц и т. д.

Марганец участвует в обмене углеводов, оказывает определенное влияние на половое развитие и размножение. М е д ь участвует в процессах кроветворения, в повышении иммунологической устойчивости и сопротивляемости организма к вредным воздействиям внешней среды. И о д входит в состав гормонов щитовидной железы и т. д. -5 Элементы, содержание которых меньше чем 10 %, относят к ультрамикроэлементам. Данные о количестве и биологической роли многих элементов невыяснены до конца. Некоторые из них постоянно содержатся в организме животных и человека: Ga, Ti, F, Al, As, Cr, Ni, Se, Ge, Sn и другие. Биологическая роль их мало выяснена. Их относят к условно биогенным элементам. Потребность человека в минеральных веществах зависит от различных факторов: пола, возраста, рода трудовой деятельности и т. д. При этом имеет значение не только их общее количество в пище, но и соотношение между отдельными элементами.

Поступлению в организм химических элементов также способствует питание и потребляемая вода. Организм состоит из воды на 60%, 34% приходится на органические вещества и 6% на неорганические. Основными компонентами органических веществ являются С, Н, О. В их состав входят также N, P, S. В составе неорганических веществ обязательно присутствуют 22 химических элемента. Например, если вес человека составляет 70 кг, то в нём содержится (в граммах): Са - 1700, К - 250, Na – 70, Mg - 42, Fe - 5, Zn - 3. На долю металлов приходится 2, 1 кг. Столько же химических элементов должно выводиться, поскольку их содержание в организме находится в относительном постоянстве. При недостаточном поступлении элемента в организм наносится существенный ущерб росту и развитию организма. Это объясняется снижением активности ферментов, в состав которых входит элемент.

Содержание минеральных веществ в растительных продуктах в значительной степени зависит от состава почвы, на которой они произрастают. Недостаток каких-либо элементов в почве и соответственно в продуктах питания отражается на обеспеченности организма. Такие территории с необычным содержанием в почве минеральных веществ названы биогеохимическими провинциями.

Например, в горных районах обнаружены зоны с пониженным содержанием йода, что проявляется развитием у проживающих здесь людей эндемического зоба, а избыточное содержание молибдена в почвах характеризуется широким распространением в этой местности подагры и т. д. Соответственно в таких зонах проводятся определенные профилактические и лечебные мероприятия по нормализации минерального питания.

ХАРАКТЕРИСТИКА ВОДНО-МИНЕРАЛЬНОГО ОБМЕНА В организме человека обмена воды и минеральных веществ тесно связаны в единый водно-минеральный, или водно-солевой обмен, который в значительной мере обеспечивает гомеостаз — постоянство внутренней среды организма (осмотическое давление, р. Н среды и т. д. Осмотическое давление любой биологической жидкости (крови, лимфы и др. ) определяется молярной концентрацией растворенных в ней веществ, называемых осмотически активными. К ним относятся как неэлектролиты (белки, мочевина, глюкоза и др. ), так и различные соли— электролиты (Na. Cl, Na. HPO 4 и др. ). Последние в большей степени, чем неэлектролиты, влияют на величину осмотического давления, что определяется диссоциацией солей на осмотически активные ионы. При этом катионы и анионы создают равное другу осмотическое давление. Суммарное осмотическое давление, создаваемое в биологических жидкостях электролитами и неэлектролитами при 37 °С, составляет 7, 7— 8, 1 атм.

Осмотическое давление имеет важное физиологическое значение, так как нормальная его величина в крови и лимфе, омывающих все клетки человеческого организма, определяет их форму и функции (проницаемость мембран и др. ). Постоянство осмотического давления поддерживается деятельностью эндокринных желез, почек и другими регуляторными механизмами.

Составной частью осмотического давления является так называемое онкотическое или коллоидоосмотическое давление, создаваемое белками. Оно имеет значение для удержания воды в сосудистом русле. Поэтому при гипопротеинемии возникает разница в онкотическом давлении крови и тканевых жидкостей, и вода устремляется в сторону более высокого давления, т. е. в ткани, чаще всего в подкожную клетчатку, где накапливается и вызывает развитие отеков.

Реакция среды определяется показателем р. Н — водородным показателем, представляющим собой отрицательный десятичный логарифм концентрации водородных ионов. Концентрацию водородных ионов определяют исходя из того, что в 1 л воды в диссоцированном состоянии находятся 1 х10 -14 молей ионов воды. Как известно, вода содержит равное количество ионов гидроксила и протонов, каждого из которых в данном случае содержится 1 х10 -7 молей. Такая реакция среды является нейтральной, и ее р. Н соответствует 7. При уменьшении концентрации протонов соответственно возрастает уровень ионов гидроксила, т. е. среда становится щелочной, и наоборот. Кислотность среды характеризуется величинами р. Н от 0 до 7, а щелочность — от 7 до 14. Величина р. Н крови отличается постоянством и находится в пределах 7, 36— 7, 4, несмотря на различные вещества кислого или основного характера, регулярно поступающие с пищей или образующиеся в обменных процессах.

Изменение р. Н крови более чем на 0, 07 свидетельствует о развитии патологического процесса. Сдвиг р. Н в кислую сторону называется ацидозом, а в щелочную — алкалозом. В организме поддержание равновесия кислот и оснований, а, следовательно, и постоянства р. Н крови обеспечивается б у ф е р н ы м и с т е м а м и, к которым относится гемоглобиновая, белковая, бикарбонатная и фосфатная. Общее представление о механизме действия буферов рассмотрим на примере бикарбонатного. Буферная система состоит из двух компонентов: слабой кислоты и ее соли, образованной сильным основанием. В данном случае слабой кислотой является H 2 CO 3, ее солью Na. HCO 3. При накоплении в организме кислых продуктов (например, соляной кислоты) они вступают в реакцию нейтрализации с Тiа. НСО с образованием хлорида натрия и угольной кислоты: Nа. НСО 3 + НСI — Na. Cl + Н 2 CO 3, которая легко диссоциирует на Н 2 O и СО 2.

Углекислый газ с помощью гемоглобиновой буферной системы переносится в легкие, откуда выводится наружу. Образовавшийся избыток Nа. СI выводится из организма почками, и р. Н в организме не изменяется. При увеличении содержания в крови основных компонентов (например, Na. OH они связываются с угольной кислотой: H 2 CO 3 +Na. OH = Na. HCO 3 +H 2 O Nа. НСОз пополняет буферную бикарбонатную систему. Действие фосфатного буфера связано с деятельностью почек.

n Регуляция водно-солевого обмена При увеличении в плазме натрия и хлора возрастает приток воды в кровь из тканей, что обеспечивает поддержание нормального уровня осмотического давления. Уменьшение в плазме натрия приводит к обезвоживанию организма. Натрий и калий тесно связаны в своем обмене. Повышение концентрации натрия в плазме приводит к снижению в ней содержания калия. Кроме того, в почках избыток калия и водорода активно секретируется и выводится с мочой из организма, тогда как ионы натрия реабсорбируются.

Регуляция водно-соленого обмена осуществляется под контролем нервной системы и других факторов, в том числе гормонов. Так, в а з о п р е с с и н (гормон задней доли гипофиза) обладает антидиуретическим действием, т. е. способствует обратному всасыванию воды в почках. Поэтому в клинике его чаще называют антидиуретическим гормоном (АДГ). Секреция вазопрессина контролируется величиной осмотического давления, повышение которого усиливает выработку гормона. В результате увеличивается реабсорбция воды в почках, концентрация осмотически активных веществ в крови снижается и давление нормализуется. При этом выделяется небольшое количество сильно концентрированной мочи. При понижении осмотического давления активируется выработка а л ь д о с т е р о н а (гормона коркового вещества надпочечников), который усиливает реабсорбцию натрия в почках. Уровень натрия в крови повышается, и осмотическое давление приходит к норме. Таким образом, вазопрессин и альдостерон регулируют осмотическое давление при его снижении выработка альдостерона активируется, а вазопрессина — тормозится. Повышение осмотического давления характеризуется обратным явлением: активацией образования вазопрессина и торможением альдостерона.

Витамины - биологически активные вещества, необходимые для нормальной жизнедеятельности организма. Они способствуют правильному обмену веществ, повышают работоспособность, выносливость, устойчивость к инфекциям. Они не синтезируются в организме и поступают только с пищей. В отличие от белков, жиров, углеводов потребность в них не превышает нескольких тысячных, сотых долей грамма. Витамины очень нестойки и разрушаются во время варки продуктов. Отсутствие витаминов в пище может приводить к тяжелым расстройствам в организме, которые в настоящее время встречаются редко. Часто отмечается снижение обеспеченности организма теми или иными витаминами (гиповитаминозы). Гиповитаминозы носят сезонный характер, наблюдаются чаще всего в зимне-весеннее время, и для них характерны повышение утомляемости, снижение трудоспособности, подверженность различным простудным заболеваниям. Повышенная потребность в витаминах возникает при усиленной физической нагрузке, переохлаждении организма, при заболеваниях желудочно-кишечного тракта (гастритах, колитах), у женщин во время беременности и т. д.

Витамины являются катализаторами (ускорителями) действия ферментов и гормонов. Так, витамины группы В образуют активный центра многих ферментов и коферментов. При отсутствии или недостатке в пище тех или иных витаминов возникают гиповитаминозы. Сходство и различие витаминов и гормонов (табл. 1) Витамины классифицируются на: 1. Жирорастворимые: А (ретинол), D (эргостерол), Е (токоферол), К (к 1 -филлохинон, к 2 -метахинон), F (антихолестериновый вит). 2. Водорастворимые: группа В (тиамин), РР (ниацин, никотиновая к-та), Н (биотин), С (аскорбиновая к-та) , В 2 (рибофлавин), В 3 (пантотеновая кислота), В 6 (пиридоксаль), В 9 (фолиевая к-та), В 12 (кобаламин).

сходство И гормоны и витамины регулируют метаболизм в организме человека через ферменты Витамины входят в состав ферментов и являются коферментами или кофакторами Гормоны или регулируют активность уже имеющихся ферментов в клетке, или являются индукторами или репрессорами в биосинтезе необходимых ферментов Различие 1. Витамины — экзогенные факторы регуляции метаболизма и поступают с пищей извне; гормоны — эндогенные факторы, синтезирующиеся в эндокринных железах организма в ответ на изменение внешней или внутренней среды организма человека, и также регулируют метаболизм. 2. Витамины — низкомолекулярные органические соединения, гормоны — высокомолекулярные органические соединения взаимосвязь Витамин Е в организме человека служит субстратом для биосинтеза гормона кальцитриола

Витамин А выполняет самостоятельную антиоксидантную функцию, а также превращается в организме человека в витамин А, с дефицитом которого связано развитие различных патологических состояний. Одно из ранних проявлений недостаточности витамина А в организме - ослабление темновой адаптации ("куриная слепота" или гемеролапия), проявляющаяся снижением остроты зрения при слабой освещенности. Витамин А участвует в окислительно-восстановительных реакциях в организме, изменяет проницаемость мембран клеток и тканей; усиливает биосинтез гликопротеинов мембран клеток. Витамин А усиливает и функциональную активность иммунной системы, при его дефиците снижается способность лейкоцитов к фагоцитозу, уменьшается выработка антител.

В организм человека чистый витамин А поступает лишь с продуктами животного происхождения. Много витамина А содержится в печени рыб (трески, морского окуня, камбалы, минтая, палтуса), в говяжьей печени. Много его в сливочном масле, яичном желтке. Провитамин А - каротин имеется в продуктах растительного происхождения. Очень много каротина в моркови, тыкве, петрушке, красном перце, укропе, помидорах, зеленом луке, абрикосах, апельсинах, лимонах, персиках, рябине, плодах шиповника, урюке, малине. Из-за того, что витамин А является жирорастворимым, он значительно лучше усваивается вместе с жиром. Для лучшего всасывания в кишечнике витамина А и каротина желательно использовать растительные масла или сметану. Витамин А устойчив к нагреванию, но неустойчив к кислороду и к действию ультрафиолетовых лучей. Поэтому овощи, содержащие каротин, рекомендуется хранить в темном помещении, а при кулинарной обработке измельчить непосредственно перед использованием. Суточная физиологическая потребность в витамине А здорового человека составляет 1, 5 мг, в каротине - 3 мг.

Витамин Е - токоферол - означает "несущий потомство". Он оказывает положительное влияние на функции половых желез, и недостаточное поступление этого витамина в период полового созревания может в дальнейшем стать причиной нарушения репродуктивной функции. Следующая важнейшая функция витамина Е - антиоксидантная: стабилизация и защита ненасыщенных липидов клеточных мембран от свободнорадикальных процессов перекисного окисления. Однако, витамин Е является не только естественным барьером для предотвращения разрушительного действия на организм высокотоксичных и реакционноспособных перекисных соединений, но и контролирует другие важнейшие свойства клеточных мембран: работу встроенных в них ферментов, сопротивляемость бактериям и вирусам, проницаемость для различных веществ.

Суточная потребность которого в организме составляет 5 мг. Источники: растительные масла (подсолнечное, кукурузное и т. д. ), семена злаков, капуста, мясо, сливочное масло, яичный желток. Гипо- и авитаминоз Е: у детей — гемолитическая желтуха, у взрослых — дегенеративные процессы в репродуктивных органах, выкидыши беременных, жировая дегенерация печени и дистрофические изменения в скелетных мышцах.

Витамин D (эргостерол). Дефицит этого витамина приводит к развитию рахита. Начальными признаками рахита являются изменения со стороны нервной системы. Ребенок становится раздражительным, часто плачет, потеет. У него долго не зарастают роднички, наблюдается размягчение костей черепа, ребер, грудина выступает вперед. На местах соединения ребер с реберными хрящами появляются рахитические четки. В результате грудная клетка деформируется. Одним из следствий деформации грудной клетки отмечаются застойные явления в печени и воротной вене, которые приводят к ухудшению всасывания в кишечнике. Увеличиваются размеры живота. Вследствие дефицита витамина D нарушается всасывание через стенку кишечника кальция.

Снижение уровня кальция в крови стимулирует функцию паращитовидных желез и усиление секреции гормона этой железы, который способствует разрушению белковой основы костной ткани и выведению из костей солей кальция, магния, фосфора, натрия и других элементов. Костная ткань становится ломкой, и наряду с рахитом у детей и у взрослых возникает остеопороз (рассасывание костей). Большое количество витамина D сосредоточено в печени морских рыб, в сливочном масле, молоке, яичном желтке, икре рыб. Богаты витамином D дрожжи. В качестве источника витамина D используется витаминизированный рыбий жир. В настоящее время выделена эндогенная (образующаяся в коже и почках) форма витамина D. Активность эндогенного витамина D повышается под влиянием ультрафиолетового облучения. Суточная потребность в витамине D для ребенка составляет 500 - 1000 МЕ (международных единиц).

Витамин К (к 1 -филлохинон, К 2 -метахинон). При гипотаминозе возникают кровоточивость, кровоизлияния в кожу даже при самой незначительной травме. Наблюдается также кровоизлияния в суставы, сетчатку глаза, носовые кровотечения, кровоточивость десен при жевании твердой пищи, чистке зубов. Витамин синтезируется бактериями толстой кишки, поэтому гиповитаминоз К может возникнуть при поносах, остром хроническом поражении печени, приеме медикаментов, которые блокируют синтез витамина К (сульфаниламиды, салициловокислый натрий, аспирин и др. ). Витамин К содержится в зеленых листьях салата, шпината, в белокачанной и цветной капусте, моркови, томатах, ягодах рябины. Суточная потребность взрослого человека в витамине К - 1 -2 мг.

Витамин F - антихолестериновый витамин (ненасыщенные жирные кислоты линолевая, линоленовая и арахидоновая) – жирорастворимый витамин, состоит из ненасыщенных жирных кислот, получаемых из пищи. Суточная потребность витамина F в организме составляет 10— 3 О г.

Гипо- и авитаминоз F приводит к снижению биосинтеза эфиров холестерина, простагландинов, лейкотриенов, тромбоксанов. Следствием этого является сухость кожи и слизистых, шелушение кожи, выпадение волос, ломкость ногтей. Витамин F участвует в регуляции обмена липидов. Особенно важно, что непредельные ВЖК способствуют выведению из организма животных и человека холестерина, а это препятствует развитию атеросклероза. Отмечено также положительное действие витамина на состояние кожного и волосяного покровов. Арахидоновая кислота служит субстратом для биосинтеза простагландинов, тромбоксанов, в организме человека.

Витамины, растворимые в воде Витамины группы B. Эта группа витаминов самая многочисленная. В ней насчитывается более 20 различных веществ. Правда, одни из них изучены хорошо, другие - в меньшей степени. Наиболее важное значение имеют следующие витамины группы B: B 1 (или тиамин), B 2 (или рибофлавин), B 6 (или пиридоксин), PP (или никотинамид), B 5 (или пантотеновая кислота), витамин B 12 (или цианокобаламин), B (фолиевая кислота). Витамин B 1 (тиамин) является антиневрическим витамином. Для гиповитаминоза характерны поражения нервной сердечной и мышечной систем, желез внутренней секреции и пищеварительного тракта, вялость, развитие параличей, расстройство походки. Витамин В 1 регулирует углеводный, жировой, водно-солевый обмены, деятельность клеточного дыхания, нервной, сердечно-сосудистой систем, органов пищеварения. В основе нарушений при недостатке витамина В 1 лежат ферментативные сдвиги.

Витамин В 1 в виде тиалиндифосфата входит в состав ряда ферментных систем, поэтому при дефиците витамина В 1 возникает ферментная недостаточность, нарушается сгорание глюкозы в организме, пентофосфатный путь превращения глюкозы (неокислительная ветвь), образование белков. Недостаток витамина В 1 приводит к накоплению пировиноградной кислоты, которая раздражает нервные окончания, способствует развитию полиневритов и других вышеотмеченных изменений. Недостаток витамина B 1 способствует развитию слабости родовой деятельности, затягиванию родов, развитию послеродовых осложнений. Витамин B 1 в значительных количествах находится в продуктах растительного происхождения: злаках, муке темного помола, отрубях, неочищенном рисе, дрожжах, корнеплодах, фруктах, бобах, орехах. Из внутренних органов животных витамином B 1 богаты печень, почки, сердце. Суточная потребность которого в организме человека составляет – 1, 2 – 2, 2 мг.

Витамин B 2 (рибофлавин) - всасывается слизистой кишечника после окончания реакция его взаимодействия с фосфором, выводится из организма почками. У здоровых людей не возникает дефицита этого витамина, так как он в достаточном количестве вырабатывается бактериями, населяющими кишечник. Ежедневная потребность в рибофлавине составляет 1. 5 -2. 5 мг. Дефицит витамина В 2 (рибофлавин, лактофлавин) вызывает прекращение роста организма, выпадение волос, заболевание глаз с зудом и светобоязнью. Язык становится шероховатым, пурпурно-красным, в уголках рта появляются мокнущие трещины. Витамин В 2 входит в состав ферментов, необходимых для клеточного дыхания, регуляции центральной нервной системы. Витамин В 2 входит в состав молока и других молочных продуктов, мяса, печени, почек, сердца, яичного желтка, грибов, пекарских и пивных дрожжей. n

Витамин PP (ниацин): Положительно влияет на деятельность нервной системы, желудка, кишечника и др. При дефиците витамина РР возникает пеллагра (шершавая кожа). Для этой болезни характерны дерматит (воспаление кожи), понос, нарушение психики. Ниацин входит в состав комплексного витамина В 2 и не относится к собственно витаминам. Ниацин содержится в пшеничной муке, в почках и печени животных, встречается также в рыбе и мясе, бобовых и фруктах. В организме человека ниацин синтезируется из аминокислоты триптофана. Ниацин играет важную роль в процессе метаболизма и участвует в синтезе жирных кислот и холестерина. Дефицит ниацина – явление достаточно редкое – проявляется в виде воспалительных процессов в кожной и слизистой тканях, а также нарушает работу нервной системы. Ниацин стимулирует клеточное дыхание и участвует в формировании кожных покровов.

Гиповитаминоз возникает при одностороннем питании кукурузой, полированным рисом, вареным горохом, сухарями и другими продуктами, не содержащими триптофана, из которого синтезируется никотиновая кислота. При недостатке никотиновой кислоты нарушается образование ферментов, осуществляющих окислительно-восстановительные реакции и клеточное дыхание. Для более полного обеспечения витамином РР имеет значение достаточное поступление в организм полноценного белка, содержащего одну из незаменимых аминокислот - триптофан, необходимый для синтеза никотиновой кислоты. Никотиновая кислота находится в дрожжах, печени, мясе, в бобовых растениях, гречневой крупе, картофеле, орехах. Суточная потребность взрослого человека в витамине РР- 15 -20 мг.

Витамин В 3 (Пантотеновая кислота). При недостатке пантотеновой кислоты в организме человека и животных развиваются разнообразные патологические явления: поражение кожных покровов и слизистых оболочек внутренних органов, дегенеративные изменения ряда органов и тканей (особенно страдают при недостатке пантотеновой кислоты железы внутренней секреции), потеря волосяного покрова и депигментация волос и т. д. Наиболее ярким симптомом В 3 -авитаминоза у человека является онемение пальцев ног, сопровождающееся покалыванием; затем возникает жгучая боль в пальцах и подошвах, распространяющаяся до голени (нога). Все это объясняется тем, что пантотеновая кислота входит в состав исключительно важного органического соединения — коэнзима А, который занимает ключевые позиции в синтезе и расщеплении жирных кислот и обеспечивает осуществление реакций, необходимых для взаимопревращения углеводов и жиров (кофермент ацилирования). Суточная потребность — 5— 10 мг. Пантотеновая кислота в том или ином количестве содержится во всех пищевых продуктах, но больше всего ее в молоке (0, 5 мг), сыре (около 0, 3 мг) и в цветной капусте (0, 8 мг).

n Витамин B 6 (пиридоксин): входит в состав многих ферментов, участвующих в обмене аминокислот, ненасыщенных жирных кислот, холестерина. Пиридоксаль используется для улучшения регуляции обмена липидов при атеросклерозе. Благотворно влияет на функции нервной системы, печени, кроветворения и др. Этот витамин синтезируется у человека кишечной микрофлорой. Гипо- и авитаминоз В 6 приводит к нарушению биосинтеза заменимых аминокислот, белка, гема, сфингомиелинов, НАД и НАДФ+ , биогенных аминов, обезвреживания биогенных аминов, нарушению распада гликогена. Витамин В 6 содержится в пшенице, ржи, овощах, мясе, рыбе, молоке, в печени крупного рогатого скота, яичном желтке, дрожжах, нежирном твороге, сыре, капусте белокочанной, гречневой крупе, рисе, картофеле. Суточная потребность в пиридоксале взрослого человека - 2, 5 мг. Потребность взрослого человека в витамине B 6 составляет 1, 82 мг в сутки.

n Витамин B 9 (фолацин, фолиевая кислота) участвует в синтезе некоторых аминокислот, оказывает стимулирующее влияние на кроветворение, способствует лучшему усвоению витамина В 12. Гипо- и авитаминоз фолиевой кислоты приводит к нарушению биосинтеза серина, метионина, белков и нуклеиновых кислот, что сопровождается задержкой роста, анемией, лейкопенией. Антагонистами фолацина являются 4 -аминоптерин и 2 -бро- мурацил, использующиеся в лечении опухолей (тормозят биосинтез нуклеиновых кислот). В организме человека не синтезируется. Наиболее богаты фолиевой кислотой из продуктов животного происхождения печень и почки, а из растительных - зелень. Лучшими источниками фолиевой кислоты являются салаты из пищевой зелени. Содержится она и в капусте, свекле, моркови, картофеле, во многих фруктах. Содержание витамина B 9 в некоторых продуктах (в мкг на 100 г продукта): хлеб пшеничный — 20; хлеб пшеничный грубого помола — 25; капуста белокочанная — 22; петрушка — 110; салат — 48. Потребность в нем составляет 200 мкг в сутки.
n Витамин B 12 (кобаламин): Этот витамин используется в образовании нуклеиновых кислот, аминокислот (холина). Он необходим для нормального кроветворения, созревания эритроцитов, активации свертывающей системы крови, принимает участие в обмене углеводов, жиров. Оказывает влияние на рост организма. Этот витамин синтезируется у человека с участием кишечной микрофлоры, но в незначительном количестве, поэтому кобаламин должен поступать в организм с пищей. Витамин В 12 накапливается в синезеленых водорослях в некоторых бактериях. Хорошим источником витамина B 12 являются молочные продукты, например нежирный творог (в 100 г творога содержится 1 мкг витамина В 12), молоко (0, 4 мкг). Витамин В 12 содержится в печени, мясе, яйцах, рыбе, дрожжах. Гиповитаминоз В 12 возникает при заболевании желудка, кишечника. Наблюдается анемия, которая характеризуется резким снижением числа эритроцитов в периферической крови, появлением в крови молодых, незрелых форм эритроцитов. Суточная потребность — 2 -3 мкг.

Витамин C (аскорбиновая кислота): Необходим для общего укрепления человеческого организма. Он повышает трудоспособность и сопротивляемость различного рода заболеваниям. Витамин C в организме не синтезируется и не накапливается, поэтому он должен ежедневно поступать с пищей. Витамин С присутствует почти во всех высших растениях, главным образом в листьях, меньше в плодах, корнях и стеблях. Иногда его количество в плодах бывает значительно выше, чем в листьях, например у черной смородины, актинидии, некоторых видов шиповника и в незрелых плодах грецкого ореха. Витамин С отсутствует, как правило, в зрелых семенах, но появляется в них при прорастании. Чаще всего, говоря о нехватке витаминов в организме, имеют в виду витамин С. Организм человеческий сам витамин этот вырабатывать не может, в отличие, кстати, от организмов многих животных.

Витамин С способствует кроветворению, повышает иммунитет, препятствует образованию канцерогенов, регулирует работу центральной нервной системы. При недостатке этого витамина резко снижается работоспособность, поражаются десны, что в конце концов может привести к цинге. Содержится он в основном в фруктах, овощах и ягодах. Но следует учитывать, что при хранении, а также при термической обработке витамин С быстро исчезает из вышеуказанных продуктов. Витамин D (кальциферол): Играет важную роль в процессе формирования костей. Витамины группы D, так же как и А, не содержатся в растениях, но все растения содержат стерины — провитамины D, которые в коже человека под действием ультрафиолетовых лучей превращаются в витамин D. Суточная потребность в этом витамине у взрослых людей составляет 2, 5 мкг. Содержание витамина D в некоторых продуктах питания (в мкг на 100 г продукта): сливочное масло летом — 2, 5 -0, 75; молоко — 0, 125.

Витамин H (биотин): Дефицит вит Н вызывает мышечные боли, высыпание на коже, ведет к выпадению волос и истощению, а также зачастую является причиной заболеваний кишечника. Биотин играет важную роль в процессе усвоения углеводов и жиров. Здоровый человек не нуждается в рекомендациях относительно минимальной ежедневной потребности в биотине, так как бактерии, населяющие здоровый кишечник, сами синтезируют биотин. Гипо- и авитаминоз витамина Н приводит к на рушению биосинтеза нуклеиновых кислот, мочевины, ВЖК, а также к нарушению глюконеогенеза. Антагонистом биосинтеза является авидин гликопротеид, содержащийся в сыром яичном белке, который взаимодействует с биотином и препятствует его всасыванию в желудочно-кишечном тракте. Достаточным количеством считаются 30 -60 мг в сутки. Биотин синтезируется микрофлорой кишечника, поэтому его недостаточность у человека встречается редко. Суточная потребность в биотине — 0, 150, 3 мг. Содержание витамина H в продуктах (в мг на 100 г продукта): соя — 0, 06; кукуруза — 0, 02; крупа овсяная — 0, 02; горох — 0, 02; творог нежирный — 0, 01.

ФЕРМЕНТЫ Ферменты – вещества белковой природы, обеспечивающие специфический высокоскоростной катализ биохимических реакций. Синтезируются клетками организма. Некоторые клетки могут содержать до 1 000 различных ферментов. Свойства ферментов 1. Все ферменты — белковой природы (простые и сложные). Конферментами сложных ферментов являются или витамины, или металлы. 2. Все ферменты — термолабильны, т. е. оптимум действия 0 -45 °С. 3. Ферменты специфичны; различают абсолютную, относительную и стереохимическую специфичность. n 4. Ферменты для своего действия требуют строго определенного значения р. Н среды для создания активного центра фермента. 5. Ферменты обладают высокой каталитической активностью (например, холинэстераза за 1 секунду расщепляет 300 000 молекул ацетилхолина).

Классификация ферментов Международным биохимическим союзом были введены номенклатуры: систематическая и тривиальная. Основные черты систематической номенклатуры состоят в следующем: n 1. Ферменты по типу реакций, которые они катализируют, подразделяются на шесть классов, в каждом из которых имеется несколько подклассов (от 4 до 13); 2. Название ферментов состоит из 2 частей: на звания субстрата + типа катализируёмой реакции + окончания аза Каждый фермент имеет шифр, состоящий из четырех чисел, разделенных точками. Первое число определяет главный класс, второе — указывает под класс, третье — подподкласс, четвертое — номер фермента в пределах подподкласса.

класс: оксвдоредуктазы — катализируют окислительновосстановительные реакции. Процессы окисления могут протекать: 1) с участием кислорода 2) без участия кислорода; дегидрогеназы катализируют дегидрирование (удаление водорода) субстрата. 1 -й 2 -й класс: трансферазы — катализируют реакции переноса химических групп. Названия ферментов данного класса складываются из названий: субстрата-донора + переносимой группы + «аза» . На пример, если переносится метильная группа, то к названию субстрата добавляется метилтрансфераза; аминогруппа — добавляется аминотрансфераза; ацильная группа — ацилтрансфераза. Но если переносится остаток фосфорной кислоты от нуклеозидтрифосфатов, то фермент называют — киназа. 3 -й класс: гидролазы — катализируют гидролиз сложных соединений с присоединением по концам расщепленной связи остатков воды. Название фермента часто складывается из названия связи, которая гидролизуется, и окончания «аза» . Например: гидролиз пептидной связи осуществляют пептидазы, гликозидазной — гликозидазы.

4 -й класс: лиазы катализируют все реакции негидролитического расщепления веществ и образование новых связей без участия энергии, выделяющейся при гидролизе АТФ. Например, если при разрыве связей выделяется углекислый газ, то фермент — декарбоксилаза (при удалении веществ добавляется приставка «де) удаляется вода — де гидратаза. 5 -й класс изомеразы — катализируют реакции взаимопревращения изомеров. Например: глюкозо-6 -фосфат фруктозо-б-фосфат; реакция осуществляется под действием фермента: глюкозо-бфосфатизомераза. б-й класс: лигазы — катализируют соединение более простых молекул в сложные, сопряженное с распадом АТФ. Для того чтобы назвать фермент, необходимо к названию продукта реакции добавить — синтетаза. Например: аминокислота + т. РНК + АТФ = аминокислота — т. РНК + АДФ; фермент: аминокислота — т. РНКсинтетаза.

n Классификация ферментов по сложности строения молекулы 1. Ферменты-протомеры представляют собой белки с третичной структурой. Например, все ферменты переваривания в желудочно-кишечном тракте человека — пепсин, трипсин и др. 2. Олигомеры — это ферменты, состоящие из белков, имеющих четвертичную структуру: в целую молекулу белка входят несколько протомеров (субъединиц), которые могут выполнять различные функции, — каталитические субъединицы и регуляторные (аллостерические) субъединицы

З Мультиферментные комплексы — это ферменты, объединяющие в своем составе несколько надмолекулярных структур, различных по действию ферментов, катализирующих в определенном порядке какой-либо один биохимический процесс. Например — синтаза ВЖК, состоящая из 6 различных по действию ферментов и 7 -го компонента — ацилпереносящего белка, занимающего центральную часть комплекса. 4. Ферментные ансамбли — комплекс различных по действий ферментов, фиксированных на мембранах клеточных органелл в определенном по рядке, обусловливая строгую последовательность стадий одного биохимического процесса. Например, ансамбль ферментов дыхательной цепи на внутренней мембране митохондрий, обеспечивающий процесс окислительного фосфорилирования для получения АТФ.

ЗНАЧЕНИЕ ДЛЯ МЕДИЦИНЫ Жизнедеятельность любого организма обеспечивается постоянным и строго последовательным течением тысяч химических реакций, катализируемых ферментами. Вот почему в основе любых нарушений функций организма лежат расстройства деятельности ферментов (ферментопатии). n Механизмы возникновения подобных отклонений, роль ферментов в развития заболеваний, диагностике и лечении — все эти вопросы входят в самостоятельный раздел биохимии — медицинскую ферментологию.

Ферментопатии (энзимопатии) — заболевания, связанные с нарушением деятельности ферментов. В зависимости от причин, вызывающих эти нарушения, выделяют несколько видов ферментопатий. Прежде всего — это наследственные ферментопатии, которые в основе своей имеют нарушения синтеза ферментов. Эти заболевания сохраняются всю жизнь и передаются по наследству. Причина их находится в повреждениях генетического аппарата клеток. Впервые этот термин ввел А. Гаррод (1908), назвав их «врожденные ошибки метаболизма» . В настоящее время выявлено около 1500 наследственных эвзимопатий; для 100 из них выяснена причина. К ним относится, например, фенилпировиноградная олигофрения, в основе которой лежит нарушение синтеза фермента, превращающего фенилаланин в тирозин. При этом в организме идет накопление фенилаланина который распадается с образованием токсических продуктов, нарушающих обмен веществ в организме, особенно в мозге. У больного ребенка замедляется развитие, обнаруживается психическая неполноценность.

Причинами других энзимопатий могут стать недостаточность обеспечения организма незаменимыми факторами питания, например витаминами — составными частями ферментов (алиментарные энзимопатии), действие токсинов, тормозящих деятельность ферментов (токсические энзимопатии) и некоторые другие. Однако некоторые ферменты вырабатываются в различных тканях, поэтому приходится учитывать их активность и количественные соотношения. Так, в сердце отмечено преобладание Ас. АТ по сравнению с Ал. АТ, а в печени отмечено обратное соотношение. В связи с этим для данных ферментов введен так называемый коэффициент де Ритиса — отношение Ас. АТ/Ал. АТ, которое в сердце здорового человека равно 1 , З 3.

Возможность использования ферментов с диагностическими целями основана на следующем: во первых, каждый орган или ткань имеет характерный для них набор (спектр) ферментов и появление их в крови позволяет локализовать патологию. Так, для сердечной мышцы среди большой группы ферментов наиболее специфичными являются креатинкиназа (КК), аспартатаминотрансфераза (Ас. АТ) и лактатдегидрогеназа (ЛДГ); в печени преобладает аланинаминотраисфераза (Ал. АТ), ЛДГ, щелочная фос фатаза (ЩФ) и Ас. АТ; в скелетных мышцах - ЛДГ, КК и в меньшей степени Ас. АТ; в почках — ЛДГ, Щф и значительно меньше Ас. АТ; в костях ЩФ; в предстательной железе — кислая фосфатаза (КФ); в поджелудочной железе — α-амилаза и т. д. Для изоферментов также определена их локализация. Например, ЛДГ-1 преобладает в сердце, а ЛДГ-4 и 5 — в печени и т. д.

Второй причиной, определяющей возможность использования ферментов в диагностике, является то, что в организме здорового человека поддерживается состояние динамического равновесия между процессами катаболизма и анаболизма. Поэтому содержание в крови ферментов является величиной относительно постоянной, а увеличение или снижение активности ферментов свидетельствует о патологических процессах. При инфаркте миокарда отмечено существенное увеличение активности КК, Ас. АТ и ЛДГ; при заболеваниях печени возрастает активность Ал. АТ, альдолазы, ЛДГ и сорбитолдегидрогеназы; для воспаления поджелудочной железы характерно повышение активности а-амилазы; при злокачественных опухолях костей отмечается повышение активности щелочной фосфатазы; рак простаты сопровождается увеличением активности кислой фосфатазы.

Выход ферментов в кровь происходит не только при разрушении клеток, но и при повышении проницаемости клеточных мембран. Последнее, как правило, отмечается в самом начале развития патологического процесса, часто до развития клинической картины. Этот факт еще более подчеркивает значимость ферментной диагностики. Так, активность КК увеличивается уже через 2— 4 ч, Ас. АТ — через 4— 6 ч после инфаркта миокарда; активность амилазы возрастает в несколько раз через З ч после начала приступа острого панкреатита, активность аминотрансферазы и ЛДГ существенно увеличиваются ещё в доклинический период острого инфекционного гепатита, когда другие признаки заболевания отсутствуют, такие же изменения активности ЩФ происходят при рахите и т.

Отмечена прямая зависимость между активностью ферментов и количеством поврежденных клеток: чем выше активность фермента, тем больше зона повреждения ткани, а снижение его активности свидетельствует об ограничении некротического очага. Так, Например, при остром гепатите, характеризующемся диффузным характером воспалительного процесса, активность Ал. АТ в крови возрастает в 50— 100 раз по сравнению с нормой и удерживается на этом уровне в течение 2— 3 нед. В то же время при инфаркте миокарда, представляющем собой поражёние ограниченного участка сердечной мышцы, активность КК и Ас. АТ в крови достигает максимума на 3— 5 -ё сутки, после чего снижается.

n Активирование и ингибирование ферментов Основу регуляции каталитической активности ферментов составляет их конформационная лабильность. Различают 5 основных путей регуляции каталитической активности ферментов: I— путь ковалентной модификации; II — путь нековалентной модификации; III — ингибирование ферментов; IУ — репрессия или индукция генов: изменение биосинтеза ферментов; У — компартментализация. I. Регуляция путем ковалентной модификации К этому пути относятся: 1) частичный протеолиз; 2) ассоциация — диссоциация; n

З) фосфорилирование — дефосфорилирование. 1) Частичный протеолиз. Некоторые ферменты первоначально синтезируются в клетке в неактивной форме и, будучи секретированными из клетки, переходят в активную форму. Неактивный предшественник фермента называется проферментом, или зимогеном. Проферменты неактивны, так как в них не сформирован активный центр: аминокислотные остатки, его образующие, присутствуют, но они не расположены должным образом. Активация профермента заключается в формировании активного центра фермента, которое происходит в результате отщепления участка полипептидной цепи, что приводит к изменению первичной структуры белка с одновременным изменением его трехмерной структуры. Синтез в форме неактивных проферментов является характерным свойством пищеварительных ферментов, а также ферментов системы свертывания крови и фибринолиза.

2) Ассоциация — диссоциация. Некоторые ферментыолигомеры могут изменять свою активность за счет ассоциации — диссоциации протомеров, входящих в их состав. Например, фермент протеинкиназа является олигомером, состоящим из 4 протомеров двух типов каталитического и регуляторного. В одном протомере, находится активный центр, а в другом — регуляторный, который может связываться с ц. АМФ. В ассоциированном виде фермент неактивен, так как его активный центр закрыт регуляторной субъединицей, а в диссоциированном активный центр открывается и может реагировать с субстратом. Когда в клетке образуется ц. АМФ, то происходит его связывание с регуляторным центром, фермент диссоциирует на субъединицы, что приводит к его активации. При уменьшении концентрации ц. АМФ он покидает регуляторный центр, что вызывает объединение субъединиц (ассоциацию) и инактивацию фермента.

3) Фосфорилирование — дефосфорилиробание. Данный способ регулирования активности (принцип «включено — выключено» основан на изменении структуры фермента. Некоторые ферменты, присоединяя (процесс фосфорилирования) или отщепляя (процесс дефосфорилирования) остаток фосфорной кислоты, могут изменять свою активность. Фосфорилирование ферментов в клетке происходит под действием фермента протеинкиназы, когда он находится в активном состоянии. Остаток фосфорной кислоты чаще всего связывается с боковой группой остатков серина или треонина: фермент—СН 2 ОН + АТФ фермент — СН 2 ОРО 3 +АДФ дефосфорилированная форма Если в клетке активна фосфатаза, то протекает противоположный процесс (дефосфорилирование): фермент — СН 2 РО 3 Н 2 + Н 2 О фермент — СН 2 ОН + Н 3 РО 4 фосфорилированная дефосфорилированная форма

В зависимости от природы фермента фосфорилирование может его активизировать или, наоборот, инактивировать. Например, активность ферментов гликогенсинтазы (регуляторный фермент биосинтеза гликогена) и гликогенфосфорилазьг (регуляторный фермент распада гликогена) регулируется путем фосфорилирования — дефосфорилирования. Природа данных ферментов такова, что фосфорилированная форма гликогенфосфорилазы активна (а гликогенсинтазы — неактивна). При дефосфорилировании их активность меняется на противоположную. Биологический смысл заключается в том, что, когда происходит биосинтез гликогена, его распад ингибируется, и наоборот

II Путь нековалентной модификации Регуляция по типу обратной связи. В состав ферментов кроме активного центра может входить иной центр — аллостерический, к которому могут присоединяться низкомолекулярные вещества и изменять активность ферментов. n 1) Аллостерический (или регуляторный) центр — участок молекулы фермента, с которым связываются низкомолекулярные вещества-эффекторы (активаторы или ингибиторы). Их структура отлична от структуры субстрата. Присоединяясь к аллостерическому центру, эти вещества (эффекторы) могут изменять третичную или четвертичную структуры молекулы фермента и соответственно структуру активного центра, вызывая увеличение или уменьшение его активности.

Таким образом, связывание фермента с эффектором в одном участке белка вызывает изменение структуры и, следовательно, активности — в другом. Активаторы увеличивают активность ферментов, а ингибиторы уменьшают. Часто биохимический процесс состоит из нескольких стадий, которые катализируются своими ферментами. В таких системах есть хотя бы один фермент — регуляторный, который определяет скорость всей последовательности реакций. Регуляторные ферменты под действием эффекторов способны включать и выключать целые цепи реакций метаболизма. Соединения, действующие как ингибиторы этих ферментов, обычно являются конечными продуктами всей цепи реакций. Систему регуляции этого типа, когда избыток продукта одной из последовательных реакций биохимического пути ингибирует активность фермента одной из ранних стадий, блокируя эту и все последующие стадии, называют ингибированием по типу обратной связи. Таким образом, накопление избытка продукта ведет к торможению его биосинтеза.

III Типы ингибирования Различают обратимое и необратимое ингибирование ферментов. Ингибирование является необратимым, если ингибитор необратимо связывается с ферментом (образованный комплекс субстрат-ингибитор не распадается). Многие ингибиторы необратимо связываются с ферментами, изменяя их структуру. Этим объясняется токсичное действие ионов металлов: Hg+, Zn 2+, Аg+ и др. n в противном случае наблюдается обратимое ингибирование. Обратимое ингибирование может быть конкурентное и неконкурентное. 1) Конкурентное ингибирование наблюдается, когда ингибитор и субстрат имеют сходные структуры и конкурируют за связывание с активным центром фермента.

Если к ферменту Е добавить конкурентный ингибитор 1 и субстрат З, то одновременно образуется два комплекса: фермент-ингибитор (ЕI) и фермент-субстратный (ЕS). Образование комплекса ЕI не приводит к образованию продуктов реакции. Скорость реакции уменьшается, потому что присоединении ингибитора к активному центру субстрата уменьшается число активных центров фермента, способных взаимодействовать с природным субстратом. Поскольку конкурентный ингибитор связывается обратимо с ферментом, то уменьшить его действие можно, увеличивая концентрацию субстрата, так как при этом увеличивается вероятность связывания фермента с субстратом. 2) Неконкурентное ингибирование - наблюдается, когда ингибитор и фермент не сходны по структуре и ингибитор присоединяется к регуляторному центру фермента. При этом образуется тройной комплекс: фермент-ингибитор-субстрат, который не приводит к образованию продуктов реакции. В данном типе ингибирования влияние ингибитора не может быть преодолено повышением концентрации субстрата.

IV. Регуляция путем изменения биосинтеза ферментов Рассмотренные ранее способы изменения скорости протекания реакций направлены на изменение активности уже имеющихся ферментов. Существует другой способ регуляции — изменение содержания ферментов. В организме имеются вещества, которые, присоединяясь к белку — регулятору оперона, могут изменять скорость биосинтеза белков-ферментов: наблюдается либо усиление биосинтеза ферментов (индукция генов), либо замедление (репрессия генов).

V. Компартментализация (отделение, отсек) в клетке Этот способ регуляции характерен только для высших форм живых организмов и позволяет осуществить наиболее тонкую регуляцию метаболизма. Он направлен на снижение скорости процесса за счет разъединения субстрата с ферментами с по мощью мембраны. Перенос групп атомов и субстратов осуществляется за счет челночных механизмов, переводящих субстрат в форму, которая способна проникать через мембрану. Затем по другую сторону мембраны происходит обратное их превращение в первоначальную форму.

«Эндокринологией» называют науку, изучающую эндокринные железы. Клетки эндокринных желез вырабатывают вещества (гормоны), которые секретируются непосредственно в кровоток. Гормон – это химическое вещество, поступающее в кровь, которая разносит его к различным клеткам-мишеням, где оно и оказывает свое действие, необходимое для организма в целом. Термин «гормон» впервые использовали Бейлис и Старлинг в 1905 г. Считается, что этот термин – производное от греческого слова, означающего «побуждение» . Эндокринная система является одной из основных регулирующих систем организма. Свои функции гормоны реализуют через их влияние на обмен веществ в организме. Главными функциями эндокринной системы являются: -обеспечение роста, физического, полового и интеллектуального развития - обеспечение адаптации организма в различных условиях - поддержание гомеостаза

Железы внутренней секреции, или эндокринные железы (от греч. endon - внутрь , krinein – выделять) – железы, которые не имеют выводных протоков и выделяют образующиеся в них секреты во внутренние среды организма (кровь, лимфу, тканевую жидкость). Строение их различно, но все они обладают очень развитой кровеносной системой, а стенки этих кровеносных сосудов отличаются особенной тонкостью и проницаемостью. Раньше их называли кровяными железами.

История развития эндокринологии В 1830 г. Мюллер сформулировал понятие о железе внутренней секреции в своём трактате о железах и в учебнике физиологии. В 1849 году Бертольд экспериментально обосновал внутреннюю секрецию (эксперименты с каплунами). В 1855 году Клод Бернар* ввёл термин «внутренняя секреция» , классифицировал железы на две группы – внешней и внутренней секреции. 1 июня 1889 г (день, когда Броун-Секар сделал свой сенсационный доклад) – день рождения науки эндокринологии. В 1905 г. – E. H. Starling ввёл термин «гормон» .

При рассмотрении структурно - функциональной организации эндокринной системы выделяют следующие железы, соответствующие разным уровням регуляции: Центральные уровни регуляции эндокринной системы: - гипоталамус - гипофиз Периферические железы эндокринной системы: - надпочечники - щитовидная железа - половые железы (яички у мужчин и яичники у женщин) - поджелудочная железа
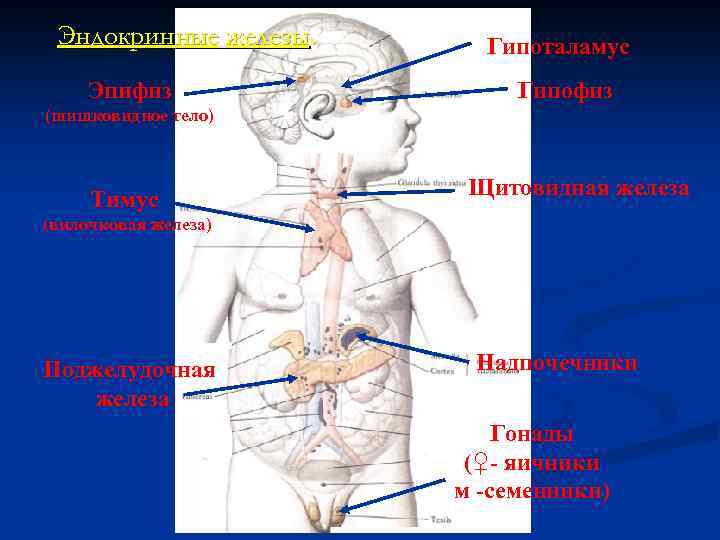
Эндокринные железы. Эпифиз Гипоталамус Гипофиз (шишковидное тело) Тимус Щитовидная железа (вилочковая железа) Поджелудочная железа Надпочечники Гонады (♀- яичники м -семенники)

Свойства гормонов: Обладают высокой биологической активностью (1 г. адреналина достаточно, чтобы усилить работу 100 000 изолированных сердец лягушек; 1 г. инсулина способен понизить уровень сахара в крови 125 000 кроликов); n n Строгая направленность действия (каждый гормон изменяет только определённые функции); n Отсутствие видовой специфичности (имеет практическое значение, так как позволяет недостаток того или иного гормона в организме человека компенсировать введением гормональных препаратов, получаемых из соответствующих желёз животных). n Избирательность действия (Воздействуют только на те клетки-мишени, которые обладают специальными рецепторами, реагирующими с данным гормоном).
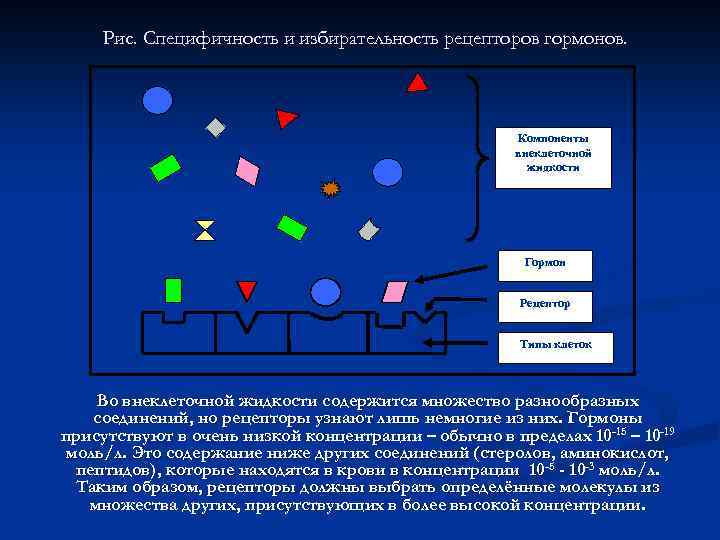
Рис. Специфичность и избирательность рецепторов гормонов. Компоненты внеклеточной жидкости Гормон Рецептор Типы клеток Во внеклеточной жидкости содержится множество разнообразных соединений, но рецепторы узнают лишь немногие из них. Гормоны присутствуют в очень низкой концентрации – обычно в пределах 10 -15 – 10 -19 моль/л. Это содержание ниже других соединений (стеролов, аминокислот, пептидов), которые находятся в крови в концентрации 10 -5 - 10 -3 моль/л. Таким образом, рецепторы должны выбрать определённые молекулы из множества других, присутствующих в более высокой концентрации.

Химические типы гормонов: n Белковые и полипептидные (менее 75 аминокислот) - с открытой цепью: АКТГ, СТГ, ЛТГ, меланоцитостимулирующий гормон, паратиреоидный, тиреокальцитонин, инсулин, глюкагон, пролактин циклические пептиды (нонапептиды) – вазопрессин и окситоцин. Гликопротеиды , содержащие углеводные остатки. ФСГ и ЛГ, : ТТГ, тиреоглобулин. n Стероидные гормоны , имеющие липидную природу– производные n Смешанная группа гормонов производные аминокислот, однако легко прони через плазматические мембраны холестерина - гормоны коры надпочечников (кортикостероиды кортикостерон, кортизол, альдостерон), половые гормоны (прогестерон, эстрадиол, эстрон, эстриол, тестостерон), простагландины. - тирозина – гормоны щитовидной железы (Т 3 и Т 4), а также гормоны мозгового слоя надпочечников (адреналин и норадреналин). триптофана – гормон эпифиза - мелатонин.
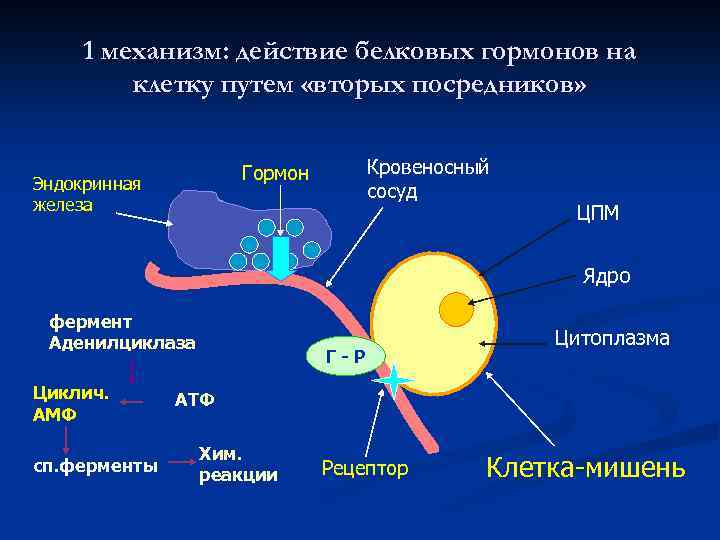
1 механизм: действие белковых гормонов на клетку путем «вторых посредников» Кровеносный сосуд Гормон Эндокринная железа ЦПМ Ядро фермент Аденилциклаза Циклич. АМФ сп. ферменты Г-Р Цитоплазма АТФ Хим. реакции Рецептор Клетка-мишень
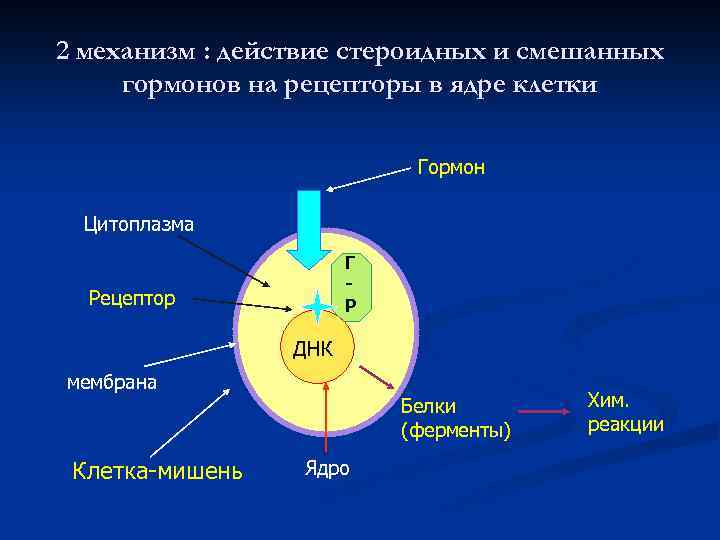
2 механизм : действие стероидных и смешанных гормонов на рецепторы в ядре клетки Гормон Цитоплазма Г Р Рецептор ДНК мембрана Клетка-мишень Белки (ферменты) Ядро Хим. реакции

ГИПОТАЛАМО-ГИПОФИЗАРНАЯ ОСЬ Гипоталамус состоит из нервной ткани под серым бугром головного мозга и связан нервными волокнами с другими отделами центральной нервной системы. В нем содержится большое число групп нервных клеток (гипоталамические ядра). К основным гипоталамическим ядрам, продуцирующим гормоны, относятся: паравентрикулярное, супраоптическое, супрахиазматическое, заднее, вентромедиальное, аркуатное ядра. Гипоталамические нейроны могут выделять свои продукты либо в синаптические щели, откуда они влияют на другие нейроны и, следовательно, представляют собой истинные нейротрансмиттеры, либо в кровь, которая доставляет их к клеткам-мишеням (например, в гипофиз), и в этом случае они, несомненно, являются гормонами. Эта важнейшая область взаимодействия эндокринной и нервной систем получила название «нейроэндокринология» .
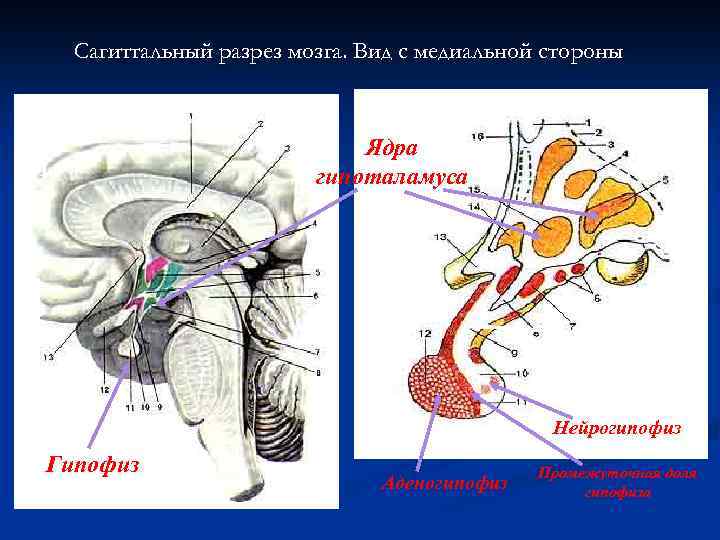
Сагиттальный разрез мозга. Вид с медиальной стороны. Б А Ядра гипоталамуса Воронка гипофиза. Нейрогипофиз Гипофиз Аденогипофиз Промежуточная доля гипофиза

Эндокринная функция гипоталамуса тесно связана с деятельностью гипофиза и осуществляется посредством выделения гипоталамическими нейронами различных гормонов, которые поступают в кровеносную систему, связывающую гипоталамус с аденогипофизом (передней долей гипофиза), либо с нейрогипофизом (задней доли гипофиза). Выделение гормонов из нервных окончаний гипоталамуса в кровь называется нейросекрецией.
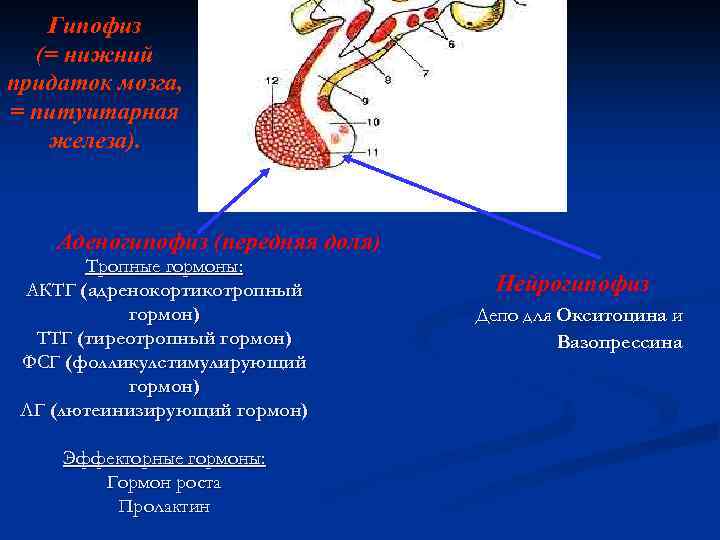
Гипофиз (= нижний придаток мозга, = питуитарная железа). Аденогипофиз (передняя доля) Тропные гормоны: АКТГ (адренокортикотропный гормон) ТТГ (тиреотропный гормон) ФСГ (фолликулстимулирующий гормон) ЛГ (лютеинизирующий гормон) Эффекторные гормоны: Гормон роста Пролактин Нейрогипофиз Депо для Окситоцина и Вазопрессина
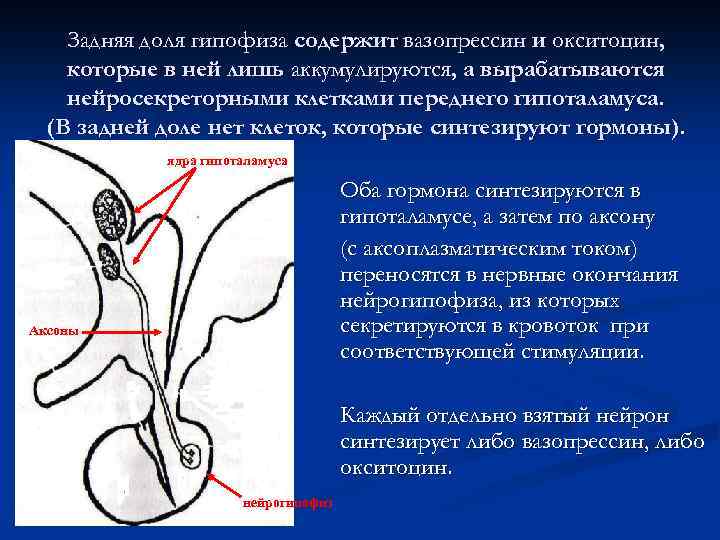
Задняя доля гипофиза содержит вазопрессин и окситоцин, которые в ней лишь аккумулируются, а вырабатываются нейросекреторными клетками переднего гипоталамуса. (В задней доле нет клеток, которые синтезируют гормоны). ядра гипоталамуса Оба гормона синтезируются в гипоталамусе, а затем по аксону (с аксоплазматическим током) переносятся в нервные окончания нейрогипофиза, из которых секретируются в кровоток при соответствующей стимуляции. Аксоны Каждый отдельно взятый нейрон синтезирует либо вазопрессин, либо окситоцин. нейрогипофиз

Структурно – функциональная организация эндокринной системы: КТРГ Гипоталамус кортикотропинрилизинг гормон ТРГ тиреотропинрилизинг гормон ГТРГ гонадотропин – рилизинг гормон Гипофиз СТГ АКТГ ТТГ Пролактин Гонадо. Адренокортико- тиреотропный тропные тропный гормоны гормон ФСГ и ЛГ Кора Щитовидная Пери- надпочечников: железа: ферические кортизол Т 3 - трийодтиронин железы тестостерон Т 4 - тироксин эстрадиол прогестерон Половые железы (гонады) тестостерон эстрадиол прогестерон Поджелудочная железа Инсулин

Названия гормонов гипоталамуса зависят от названия гормонов гипофиза, на которые они оказывают стимулирующее или ингибирующее влияние. К настоящему времени выделены и охарактеризованы различные гипоталамические гормоны, которые в зависимости от своего эффекта носят название рилизинг или либеринов (высвобождающих) и статинов (ингибирующих) гормонов. К ним относятся следующие гормоны: - тиреотропин-рилизинг гормон (ТРГ) – гормон гипоталамуса, стимулирующий секрецию тиреотропного гормона (ТТГ, тиреотропин) и пролактина; - гонадотропин-рилизинг гормон (Гн. РГ) – гормон гипоталамуса, стимулирующий секрецию фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гормонов; - кортикотропин-рилизинг гормон (КРГ, кортиколиберин) – гормон гипоталамуса, стимулирующий секрецию адренокортикотропного гормона (АКТГ, кортикотропина);

- соматотропин-рилизинг гормон (СРГ, соматолиберин, рилизинггормона роста, РГГР) – гормон гипоталамуса, стимулирующий секрецию соматотропного гормона (СТГ, соматотропин, гормон роста); - соматостатин (СС, соматотропинингибирующий гормон) – гормон гипоталамуса, ингибирующий секрецию соматотропина (СТГ, гормона роста) и тиреотропина (ТТГ) и, в определенных условиях) кортикотропина (АКТГ) и пролактина, а также инсулина и глюкагона. - дофамин – гормон гипоталамуса, угнетающий секрецию гипофизарного пролактина и, в меньшей степени, тиреотропина (ТТГ), а также, вероятно, в зависимости от дозы, оказывающий модулирующий эффект на синтез Гн. РГ. - вазопрессин (антидиуретический гормон, АДГ) –– гормон гипоталамуса, стимулирующий секрецию АКТГ гипофизом.

Центральная нервная система способна оказывать мощное регуляторное воздействие на многочисленные метаболические и другие функции организма, изменяя синтез и секрецию гипоталамических гормонов, которые, действуя на клетки-мишени аденогипофиза, контролируют секрецию аденогипофизарных гормонов. Этим-то, вероятно, и объясняется отчетливое влияние внешних раздражителей (изменений окружающей среды, эмоций и стресса) на функцию аденогипофиза.

Гипофиз (нижний мозговой придаток) – эндокринная железа, которая лежит в костной полости, называемой «турецким седлом» , у основания головного мозга. Гипофиз образован из двух совершенно разных по гистологическому строению частей: аденогипофиза и нейрогипофиза, которые функционируют как две различные эндокринные железы. Гормоны аденогипофиза можно разделить на две группы: 1 – гормоны, влияющие на ткани-мишени, это - соматотропин (СТГ) и пролактин. 2 – гормоны, чей эффект заключается в стимуляции секреции гормонов периферических эндокринных желез, это – тиреотропин (ТТГ), кортикотропин (АКТГ), гонадотропины (ЛГ и ФСГ). Основное действие тиреотропина (ТТГ) заключается в стимуляции синтеза и выделения в кровь гормонов щитовидной железы: трийодтиронина (Т 3) и тироксина (Т 4).

Ростостимулирующий эффект соматотропина обуславливается ускорением синтеза белка за счет действия гормона на ядерном уровне и усилением транспорта аминокислот через клеточные мембраны. Соматотропин действует на липолиз (распад жиров), стимулируя поглощение мышцами неэстерифицированных жирных кислот (НЭЖК) и усиливая их мобилизацию из жировой ткани. Вследствие стимуляции СТГ гликогенолиза (синтез гликогена) в печени и противодействия влиянию инсулина на поглощение глюкозы периферическими клетками, уровень глюкозы в крови может возрастать. Многие виды воздействия СТГ на линейный рост опосредуются соматомединами, которые под его действием синтезируются в различных тканях, но в основном – в печени. Соматомедины (инсулиноподобные факторы роста – ИФР-1 и ИФР-2) стимулируют пролиферацию и дифференцировку клеток. ИФР-1 обладает большей ростстимулирующей активностью, а ИФР– 2 – большей инсулиноподобной активностью.

Следует отметить, что рост и поддержание целости тканей за счет восполнения их клеточного состава при участии СТГ являются непрерывными процессами, в которых участвуют и другие гормоны: йодтиронины, инсулин, андрогены и эстрогены. Действие соматотропина и инсулина на рост оказывается взаимно дополняющим, поскольку оба гормона обладают анаболическими эффектами в сфере синтеза белка и стимулируют транспорт аминокислот в периферические клетки. В то же время эффекты их на уровень глюкозы в крови противодействуют другу. Ситуацию еще больше осложняют инсулиноподобные эффекты ИФР-1 и ИФР-2, которые способствуют поглощению глюкозы и снижению ее концентрации в крови. Общий эффект избытка СТГ сводится к увеличению инсулинорезистентности тканей и гипергликемии, которая может быть постоянной (сахарный диабет).

Немалый интерес представляет возможное влияние СТГ на сердечно-сосудистую систему, что может быть актуально для пожилых людей, у которых продукция СТГ часто снижена. Снижение уровня СТГ также выявлено при гиперкортицизме. Повышение концентрации СТГ отмечается также при стрессе, физической нагрузке, длительном голодании. Известно, что эмоциональный и хирургический стресс, повышенная температура тела действуют на продукцию СТГ через нервные связи гипоталамуса. Предполагается влияние СТГ на иммунную систему, т. к. он усиливает пролиферацию Т-лимфоцитов

Аденогипофизарные гормоны-исполнители. СОМАТОТРОПНЫЙ ГОРМОН (СТГ), или ГОРМОН РОСТА (ГР). Нормальный уровень в сыворотке крови (м. МЕ/л): Дети Мужчины n n 0, 4 -4, 0 женщины n 2, 0 -20, 0 4, 0 -20, 0 Ф. э. : стимулирует процессы роста всех тканей и органов; стимулирует рост трубчатых костей; под действием СТГ происходит усиление эритропоэза.

Избыточная секреция соматотропина в раннем детстве приводит к развитию гигантизма , а в более зрелом возрасте – к акромегалии (из-за непропорционального роста чрезмерно увеличиваются кисти и стопы, нос, язык, челюсти, сахарный диабет). Причиной обычно является опухоль аденогипофиза.

При дефиците гормона роста в детском возрасте происходит задержка роса – карликовость (гипофизарный нанизм человек на всю ), , ) жизнь остаётся карликом: телосложение у таких людей относительно пропорционально, однако кисти и стопы малы, пальцы тонкие, окостенение скелета запаздывает, половые органы недоразвиты, вторичные половые признаки слаборазвиты; плохо переносят инфекционные и др. виды заболеваний, поэтому часто умирают молодыми; у мужчин отмечается импотенция, у женщин - стерильность; у взрослого человека недостаток соматотропина вызывает тяжелейшее истощение – кахексию.

Аденогипофизарные гормоны-исполнители. ПРОЛАКТИН, или ЛАКТОТРОППЫЙ ГОРМОН (ЛТГ) Нормальный уровень в сыворотке крови (м. МЕ/л): Дети 85 -300 Мужчины 90 -500 Женщины 100 -600 Ф. э. заключается в стимуляции развития молоч желез и лактации у женщин; У мужчин функция пролактина до конца не вы У женщин, кроме того, уровень пролактина зависит от фазы менструального цикла. Содержание пролактина выше в лютеиновую фазу.

Инъекции пролактина могут вызвать лактацию и у самцов. Однако для этого нужно предварительно вводить им в течение некоторого времени эстрогены и прогестероны, т. к. молочные железы у самцов находятся в рудиментарном состоянии и не могут лактировать, если не стимулировать искусственным путём развитие их железистой ткани. Введение пролактина девочкам даже до достижения половой зрелости вызывает формирование материнского инстинкта.

Вызывают увеличение уровня пролактина: n стресс , n физические упражнения, механические раздражения сосков, сексуальные контакты, гипогликемия. n n n
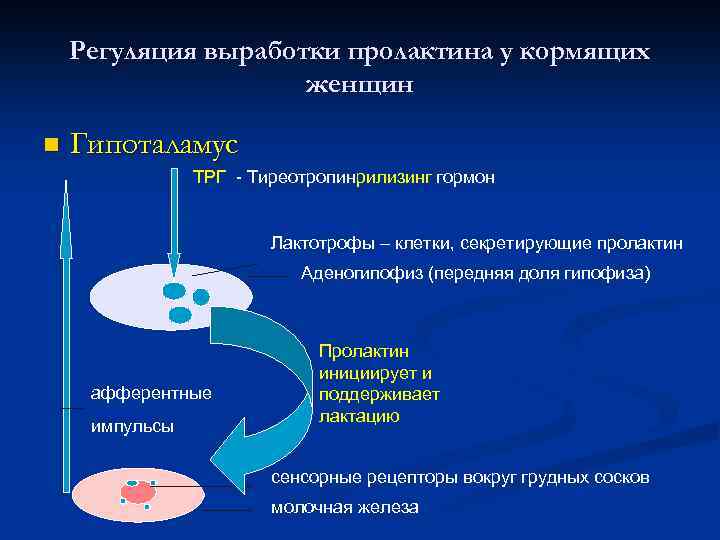
Регуляция выработки пролактина у кормящих женщин n Гипоталамус ТРГ - Тиреотропинрилизинг гормон Лактотрофы – клетки, секретирующие пролактин Аденогипофиз (передняя доля гипофиза) афферентные импульсы Пролактин инициирует и поддерживает лактацию сенсорные рецепторы вокруг грудных сосков молочная железа

ПРОЛАКТИН Пролактин - белковый гормон гипофиза, стимулирующий рост и развитие молочных желез, инициирующий и поддерживающий лактацию у женщин после родов. Однако, эти эффекты требуют присутствия и других гормонов – эстрогенов, кортикостероидов и инсулина. Пролактин принимает участие в регуляции функции половых желез: стимулирует синтез рецепторов ЛГ в половых железах, как мужчин, так и женщин. Парадоксальным является тот факт, что гиперпролактинемия сопровождается снижением репродуктивной функции: импотенцией, снижением либидо, может иметь место бесплодие, а у женщин часто отмечается аменорея (полное) или олигоменорея (частичное отсутствие менструальных циклов). Во время беременности и в первые месяцы интенсивной лактации наблюдается физиологическая гиперпролактинемия, которая, по всей вероятности, и определяет задержку восстановления менструальных циклов после родов. Важно, что пульсирующий характер секреции пролактина способствует тому, что возможно наличие периодов, когда отсутствует его контрацептивное действие, что объясняет редкие случаи возникновения беременности в период лактации.

Метаболические эффекты пролактина сходны с эффектами СТГ, он является анаболическим гормоном, но его роль в регуляции обмена веществ остается неясной. Пролактин влияет на иммунную систему, стимулируя пролиферацию лимфоцитов. Секреция пролактина контролируется, главным образом, гипоталамусом, который получает афферентные импульсы от сенсорных рецепторов, расположенных, в основном, вокруг грудных сосков кормящих женщин. Гипоталамические нейроны выделяют меньше дофамина и, вероятно, больше тиреотропинрилизинг гормона, стимулирующего лактотрофы гипофиза. В результате чего акт сосания уже через несколько минут после начала приводит к повышению концентрации пролактина в крови. Секрецию пролактина стимулируют и различные стрессоры, влияние которых опосредуется, возможно, гистаминергическими нейронами. На секрецию пролактина влияют эстрогены, которые увеличивают число рецепторов ТРГ в клетках гипофиза и стимулируют экспрессию гена пролактина, поэтому у женщин концентрация пролактина в сыворотке крови выше, чем у мужчин.

Вазопрессин, или антидиуретический гормон (АДГ). • вызывает сужение сосудов (вазоконстрикцию), повышая кровяное давление; • стимулирует реабсорбцию воды, в результате чего образуется концентрированная моча и уменьшается диурез.

Нарушение секреции или действия АДГ приводит к несахарному диабету (несахарное мочеизнурение), который характеризуется частым выделением больших объёмов разбавленной мочи и сильной жаждой. n Также характерными для несахарного диабета являются слабость, нарушение сна и аппетита, головные боли, уменьшение потоотделения, сухость кожи, сексуальные нарушения у взрослых людей и отставание в развитии у детей. n Как правило, симптомы данного заболевания возникают внезапно, однако, точную причину возникновения несахарного диабета установить достаточно трудно. Несахарный диабет может развиваться при повреждении гипоталамо-гипофизарного тракта вследствие перелома основания черепа, опухоли инфекции; может иметь и наследственную природу.

Окситоцин обнаружен у всех млекопитающих и многих видах птиц, пресмыкающихся, амфибий и костных рыб. Окситоцин, по-видимому, образуется и в яичниках. Окситоцин отличается от вазопрессина только тем, что в кольце у него фенилаланин замещён на изолейцин, а в концевой группе вместо аргинина находится лейцин.

Окситоцин вызывает сокращение гладких мышц матки (в фармакологических дозах используется для стимуляции родовой деятельности у женщин). n n При родах окситоцин может возрастать в 30 -50 раз, способствуя снижению ответа ЦНС на боль. n n n При сосании груди у кормящей матери увеличивается в 8 -10 раз (возможно, гормон стимулирует выброс молока из молочной железы). У мужчин окситоцин стимулирует эякуляцию.

Психологи установили, что, попадая в стрессовую ситуацию, женщины ведут себя более мобильно и справляются со стрессами лучше мужчин. У женщин содержание окситоцина выше. Благодаря этому гормону в стрессовых ситуациях женщины интуитивно ищут контакта с другими людьми для разрешения своей проблемы. У мужчин при стрессе так же образуется окситоцин, но его действие блокируется тестостероном.
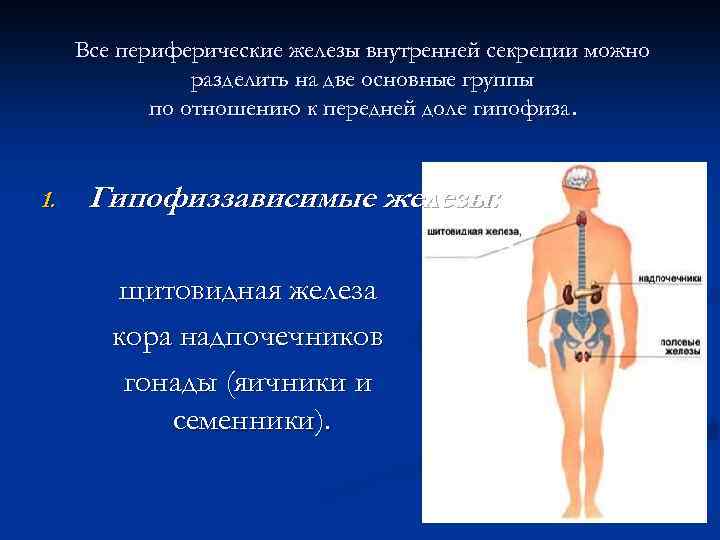
Все периферические железы внутренней секреции можно разделить на две основные группы по отношению к передней доле гипофиза. 1. Гипофиззависимые железы: щитовидная железа кора надпочечников гонады (яичники и семенники).

2. Независимые от передней доли гипофиза жел Околощитовидные железы; Хромаффинные клетки мозговой части надпочечников; Островки Лангерганса поджелудочной железы; Энтерохромаффинные и аргирофильные клетки желудка и кишечника; Клубочковая зона коры надпочечников; К-клетки щитовидной железы. Независимые железы рассматриваются как саморегулирующиеся.

КОРА НАДПОЧЕЧНИКОВ Кору надпочечников можно рассматривать как эндокринную железу, совершенно отличную от мозгового вещества надпочечников. Эти клетки секретируют гормоны (кортикостероиды), которые регулируют водносолевой баланс (минералокортикоиды) и метаболические процессы (глюкокортикоиды). Кроме того, кора надпочечников в норме секретирует небольшое количество эстрогенов и андрогенов, которые также представляют собой стероидные гормоны. Удаление коры надпочечников быстро приводит к смерти. Таким образом, корковый слой надпочечников играет ключевую роль в регуляции гомеостаза и многих жизненно важных физиологических функций. Все гормоны коры надпочечников (прогестерон, минералокортикоиды, глюкокортикоиды, андрогены и эстрогены) являются производными холестерина и состоят из углеродных цепей, являясь по своей химической структуре стероидами.

Коротко (надпочечники)

Надпочечники Мозговое вещество надпочечников. Катехоламины. Кора надпочечников. Глюкокортикоиды (кортизол). Минералокортикоиды (альдостерон).
кора надпочечника мозговое вещество надпочечника

Этапы стрессовой реакции в организме в ответ на раздражитель (этапы общего адаптационного синдрома) 1 этап – активация симпатической и парасимпатической нервной системы n 2 этап – активация мозгового слоя надпочечника с выбросом катехоламинов в кровь (80% адреналина и 20% норадреналина и дофамина) n симпатоадреналовая реакция. 3 этап – активация других звеньев эндокринной системы (адренокортикального, тиреоидного и соматотропного)
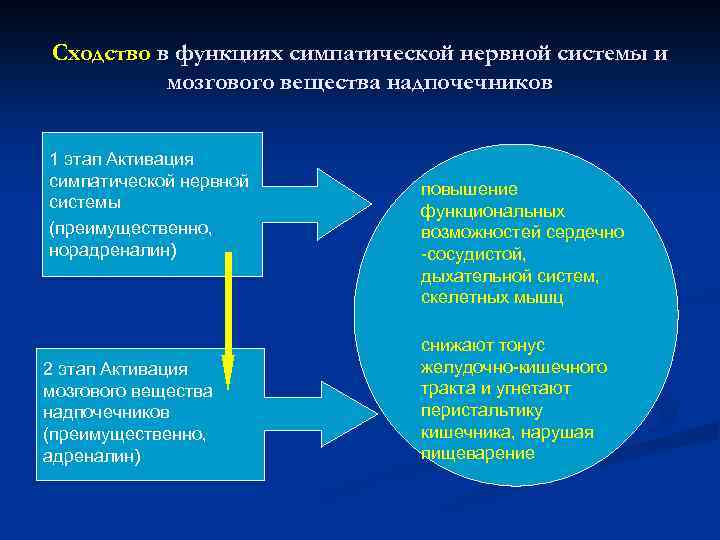
Сходство в функциях симпатической нервной системы и мозгового вещества надпочечников 1 этап Активация симпатической нервной системы (преимущественно, норадреналин) 2 этап Активация мозгового вещества надпочечников (преимущественно, адреналин) повышение функциональных возможностей сердечно -сосудистой, дыхательной систем, скелетных мышц снижают тонус желудочно-кишечного тракта и угнетают перистальтику кишечника, нарушая пищеварение
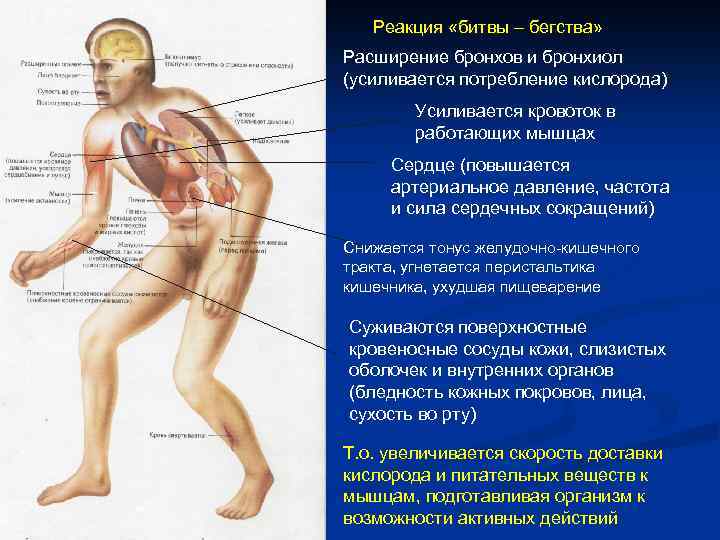
Реакция «битвы – бегства» Расширение бронхов и бронхиол (усиливается потребление кислорода) Усиливается кровоток в работающих мышцах Сердце (повышается артериальное давление, частота и сила сердечных сокращений) Снижается тонус желудочно-кишечного тракта, угнетается перистальтика кишечника, ухудшая пищеварение Суживаются поверхностные кровеносные сосуды кожи, слизистых оболочек и внутренних органов (бледность кожных покровов, лица, сухость во рту) Т. о. увеличивается скорость доставки кислорода и питательных веществ к мышцам, подготавливая организм к возможности активных действий

Метаболические эффекты адреналина (на обмен веществ в организме) n 1. Повышают уровень глюкозы в крови за счет распада гликогена. 2. Усиливают распад жира с образованием свободных жирных кислот n Повышение концентрации энергетических субстратов в крови

3 этап стресс – реакции – адренокортикальный механизм (активация коры надпочечников) Кора надпочечника синтезирует стероидные гормоны (производные холестерина) имеющие название кортикостероиды: 1. глюкокортикоиды, регулирующие метаболические процессы (обмен веществ: белков, жиров, углеводов, в частности, стимулирующие синтез глюкозы (кортизол), 2. минералокортикоиды, регулирующие водно - солевой баланс (альдостерон). 3. небольшое количество (тестостерон, эстрадиол), половых гормонов
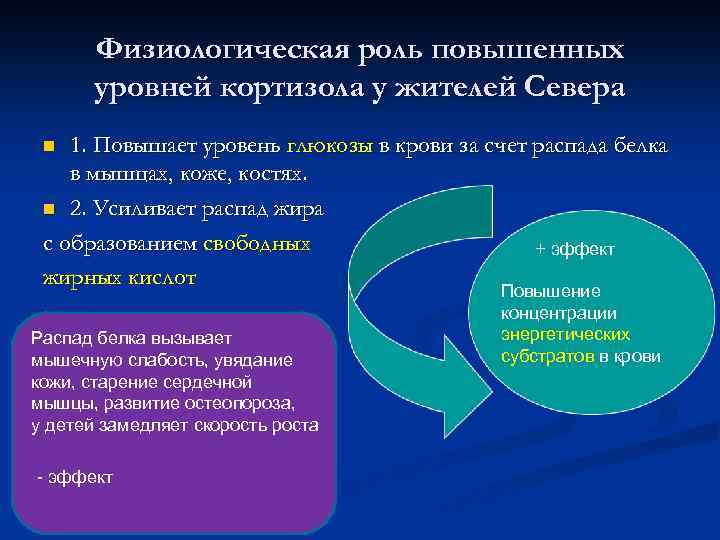
Физиологическая роль повышенных уровней кортизола у жителей Севера 1. Повышает уровень глюкозы в крови за счет распада белка в мышцах, коже, костях. n 2. Усиливает распад жира с образованием свободных + эффект жирных кислот n Распад белка вызывает мышечную слабость, увядание кожи, старение сердечной мышцы, развитие остеопороза, у детей замедляет скорость роста - эффект Повышение концентрации энергетических субстратов в крови

Неблагоприятные последствия повышенных уровней кортизола «Плата за адаптацию» n n n 1. Снижается интенсивность иммунных механизмов (иммуносупрессивный эффект) 2. Возрастает риск развития инфаркта миокарда (за счет спазма сосудов) 3. Снижается всасывание кальция из кишечника, что приводит к развитию остеопороза (хрупкости костей) 4. Снижается репродуктивная функция 5. Увеличивается количество свободных радикалов (при реакции перекисного окисления липидов), которые нарушают жизнедеятельность клетки

Профилактические мероприятия при повышенном уровне кортизола 1. Прием витамина С, который затрачивается на синтез кортизола n 2. Прием антиоксидантов – витамины С, А, Е n 3. Снижение уровня стрессированности организма: - мышечная, психологическая релаксация или медитация, дыхательная гимнастика (повышается парасимпатическая активность) - терапевтическое обучение пациента (разъяснение природы стресса, выявление его причин, аутотренинг) n 4. Ведение здорового образа жизни - рациональное и регулярное питание - достаточный сон - организованная без штурмовщины и аврала работа и учеба - общеукрепляющие процедуры умеренная физическая нагрузка (повышает тонус парасимпатической нервной системы) 5. Фармакологические методы, психотерапия, гипноз n
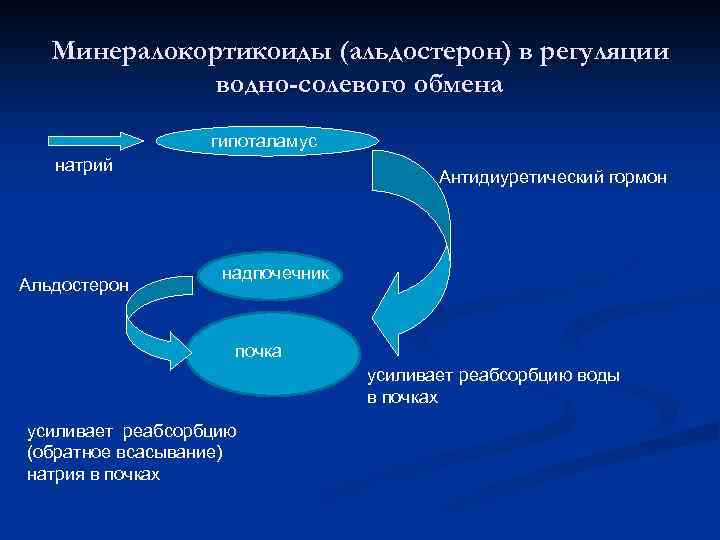
Минералокортикоиды (альдостерон) в регуляции водно-солевого обмена гипоталамус натрий Альдостерон Антидиуретический гормон надпочечник почка усиливает реабсорбцию воды в почках усиливает реабсорбцию (обратное всасывание) натрия в почках

Развернутая (надпочечники)

На первых стадиях синтеза из холестерина образуются прегненолон и прогестерон, причем последний является полноценным гормоном. Главный минералокортикоид у человека – альдостерон, синтезирующийся из прогестерона. Кортизол, являющийся у человека главным глюкокортикоидом, синтезируется также из прогестерона. Среди продуцируемых корой надпочечников андрогенов самым важным является дегидроэпиандростерон (ДГЭА). ГЛЮКОКОРТИКОИДЫ Наиболее важными из природных глюкокортикоидов, присутствующих в плазме человека, являются кортизол и кортикостерон; потенциально важен и кортизон, который сам по себе неактивен, но в печени и других тканях может превращаться в кортизол. n Основные физиологические эффекты глюкокортикоидов проявляются в сфере углеводного, белкового и (в меньшей степени) жирового обмена.

Эти гормоны играют важную роль в формировании резистентности к действию различных повреждающих факторов (стрессоров). В избыточном количестве эти соединения оказывают иммуносупрессивное, противовоспалительное и противоаллергическое действие, что имеет большое значение при некоторых клинических состояниях. Кортизол обладает многими эффектами в сфере углеводного обмена, в результате которых возрастает концентрация глюкозы в крови. Кортизол тормозит поглощение аминокислот и синтез белка вне печени, но в печени он стимулирует эти процессы. В таких периферических тканях, как мышцы, кожа, кости кортизол оказывает мощное катаболическое действие (распад белка). При его избыточной продукции может развиться резкая мышечная слабость.

В печень при этом поступает повышенное количество аминокислот, которые выполняют здесь роль предшественников глюконеогенеза. Вследствие стимулирующего влияния стероидов на синтез белка в печени увеличивается и концентрация белка в плазме. Кортизол влияет и на жировой обмен, особенно когда синтезируется в избыточных количествах. Следствием усиления липолиза (распада жира) в жировой ткани является ускорение мобилизации жирных кислот. Это эффект отчасти определяется потенцированием липолитического действия других гормонов, таких как соматотропин и катехоламины. Глюкокортикоиды оказывают влияние на водный обмен, в частности, на способность организма экскретировать водную нагрузку путем повышения скорости клубочковой фильтрации, возможно, вследствие прямого сосудорасширяющего действия глюкокортикоидов на сосуды почек.

Под влиянием глюкокортикоидов повышается сосудистый тонус; возможно, эти гормоны потенцируют сосудосуживающий эффект других вазоактивных соединений, таких как катехоламины и вазопрессин. При избыточном содержании глюкокортикоидов в крови у детей замедляется скорость роста. Этот эффект отчасти объясняется тормозящим действием глюкокортикоидов на секрецию соматотропина, но глюкокортикоиды и прямо ингибируют продукцию инсулиноподобного фактора роста (ИФР- I), а также общий синтез белка. Разнообразные стрессоры, в том числе тяжелая травма, кровотечение, острая гипогликемия, повышение температуры тела и эмоциональные переживания приводят к резкому повышению концентраций АКТГ и кортизола в крови.

Избыточные количества глюкокортикоидов угнетают воспалительный процесс (противовоспалительное действие). Кортизол в высоких концентрациях блокирует все стадии этого процесса, тем самым препятствуя нормальному заживлению раны. Высокие концентрации глюкокортикоидов вызывают противоаллергический эффект, который связан с торможением синтеза гистамина, выделяющегося при взаимодействии антигена с антителом из тучных клеток. Иммуносупрессивный эффект больших количеств кортизола обусловлен постепенным разрушением лимфоидной ткани, что сопровождается снижением образования антител, уменьшением количества лимфоцитов, базофилов, эозинофилов в крови.

Влияние глюкокортикоидов на иммунную систему проявляется не только тогда, когда он присутствует в избыточных количествах при введении их с терапевтической целью или при эндогенной гиперсекреции (синдром Кушинга), но и в нормальных условиях как часть физиологического регуляторного действия, препятствующего разрушительному действию чрезмерной активности иммунной системы на организм. Вполне вероятно, что взаимодействие между кортизолом и иммунной системой является важнейшей функцией гипоталамогипофизарно-надпочечниковой оси. Кортизол оказывает влияние на обмен кальция и костную ткань. Большие количества кортизола препятствуют действию метаболитов витамина D на всасывание кальция из кишечника и усиливают экскрецию его почками вследствие повышения скорости клубочковой фильтрации.

Торможение избыточными количествами кортизола секреции соматотропина, а также его влияние на кальциевый и белковый обмен определяет, вероятно, развитие остеопороза – частого симптома гиперпродукции глюкокортикоидов. Кортизол тормозит секрецию АКТГ по механизму отрицательной обратной связи, замыкающейся на уровне аденогипофиза или гипоталамуса и/или другими отделами головного мозга (например, гиппокампом). Все эти отрицательные обратные связи делятся на быстрые, отставленные и поздние, которые реализуются, вероятно, посредством разных механизмов.

ЩИТОВИДНАЯ ЖЕЛЕЗА Щитовидная железа секретирует два гормона, оказывающих разнообразные генерализованные влияния на обмен веществ и имеющих особое значение для нормального роста и развития. n Гормоны щитовидной железы (тиреоидные гормоны) представляют собой йодированные молекулы, называемые йодтиронинами: это трийодтиронин (Т 3) и тетрайодтиронин (Т 4, тироксин). Еще один гормон – тиреокальцитонин (или кальцитонин, КТ) принимает участие в регуляции обмена кальция. Изменения метаболизма в чувствительных к тиреоидным гормонам тканях затрагивают углеводный, жировой и белковый обмен, что определяет влияние Т 3 и Т 4 на рост и развитие организма.

КОРОТКО (щитовидная железа)

Различают тиреоидные гормоны (йодтиронины) – тироксин (Т 4) и трийодтиронин(Т 3). Соотношение Т 4 и Т 3 равно 7: 1; но Т 3 обладает более высокой активностью (превосходя в 5 -10 раз по влиянию на метаболизм).

Ф. э. тиреоидные гормоны : - повышение основного обмена веществ в организме, что связано с увеличением числа и размеров митохондрий в клетках организма; это приводит к росту потребления кислорода и увеличению теплопродукции. При снижении уровня йодтиронинов уменьшается устойчивость к холоду.

Метаболические эффекты (действие на обмен веществ) тиреоидных гормонов в организме n 1. Белковый обмен – усиливают синтез и распад белка, что важно для роста и развития организма n 2. Углеводный обмен – усиливают все стороны углеводного обмена n 3. Жировой обмен – усиливают синтез и распад липидов n Т. е. обеспечивают нормальный рост, развитие и сохранение целостности тканей организма. n Принято считать, что у жителей Севера уровни гормонов щитовидной железы повышены, особенно у женщин.

Последствия для организма повышения уровней гормонов щитовидной железы n n n 1. Возрастание потребности в витаминах, которые являются коферментами биохимических реакций 2. Усиливается потребность в микроэлементах, т. к. при избытке тиреоидных гормонов наблюдается деминерализация костей с повышением риска переломов и развитием остеопороза. 3. Увеличивается потребность тканей в кислороде 4. Увеличивается теплопродукция и теплоотдача через кожу – снижается переносимость тепла. 5. Влияют на силу сердечных сокращений, увеличивая ее, а при длительном повышении гормонов – уменьшая за счет усиления распада белков сердечной мышцы.
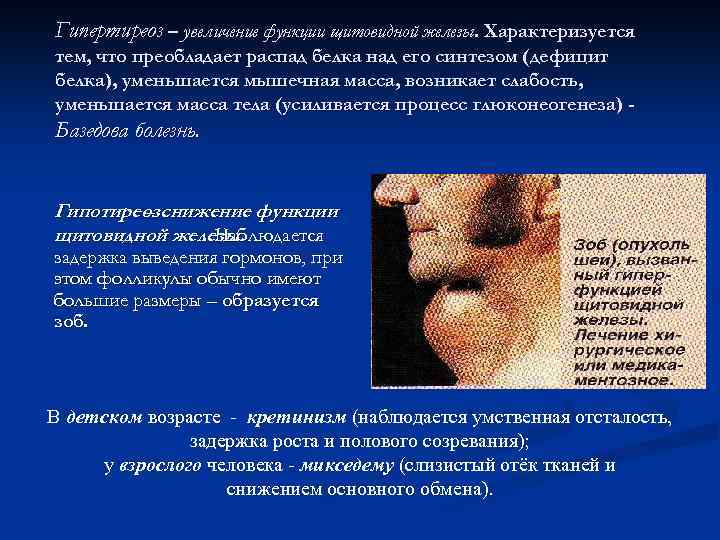
Гипертиреоз – увеличение функции щитовидной железы. Характеризуется тем, что преобладает распад белка над его синтезом (дефицит белка), уменьшается мышечная масса, возникает слабость, уменьшается масса тела (усиливается процесс глюконеогенеза) - Базедова болезнь. Гипотиреоз снижение функции – щитовидной железы. Наблюдается задержка выведения гормонов, при этом фолликулы обычно имеют большие размеры – образуется зоб. В детском возрасте - кретинизм (наблюдается умственная отсталость, задержка роста и полового созревания); у взрослого человека - микседему (слизистый отёк тканей и снижением основного обмена).
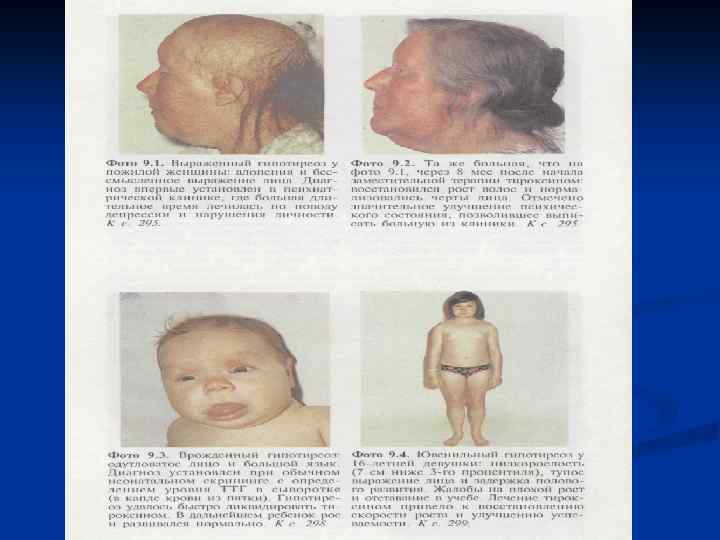

n Развернутая (щитовидная железа)

Наиболее известный эффект этих гормонов – повышение основного обмена (скорости метаболизма) во многих тканях, что означает рост потребления кислорода и увеличение теплопродукции (калоригенный эффект). Возрастание основного обмена связано с увеличением числа и размеров митохондрий и повышением внутриклеточной концентрации многих ферментов, увеличением транспорта натрия и калия через клеточную мембрану. Возрастание основного обмена сопровождается некоторым повышением температуры тела и снижением переносимости тепла, что стимулирует механизмы теплоотдачи. При снижении уровня йодтиронинов крови уменьшается толерантность к холоду.

Влияние йодтиронинов на белковый обмен особенно важно для роста и развития организма. Тиреоидные гормоны усиливают как анаболические, так и катаболические процессы в сфере белкового обмена. При гипо- и гипертиреозе обычно нарушаются рост, развитие и структурная целостность тканей. При избыточном их содержании в крови распад белка преобладает над его синтезом. Это обуславливает дефицит белка, что проявляется уменьшением мышечной массы и слабостью, а также снижением массы тела. При распаде белка в печень поступает большое количество аминокислот – субстратов глюконеогенеза, в результате чего процесс глюконеогенеза усиливается (эффекты, сходные с избыточным содержанием кортизола в крови).

При падении уровня тиреоидных гормонов задержка азота (белка) превышает его выведение из организма (положительный азотистый баланс), что связано, в основном, с изменением процесса распада белка. При этом состоянии тормозится и синтез белка, а также замедляется его кругооборот. Йодтиронины усиливают все стороны углеводного обмена. Под их влиянием возрастают всасывание глюкозы в желудочнокишечном тракте, поглощение глюкозы периферическими клетками (мышечной и жировой ткани), а также гликолиз, глюконеогенез и гликогенолиз. Одновременно усиливается эффект инсулина, стимулирующий гликогенез. Некоторые из этих эффектов, вероятно, связаны с потенцированием действия других гормонов, таких как катехоламины и инсулин. Многие эффекты йодтиронинов в сфере углеводного обмена оказываются дозозависимыми, чем и объясняется их двухфазное действие.

Вследствие общего повышения метаболической активности клеток под действием йодтиронинов в жировой ткани и других клетках усиливается липолиз, что должно было бы приводить к росту концентрации свободных жирных кислот в плазме. Однако, эти гормоны стимулируют и окисление жирных кислот в клетках. Таким образом, хотя Т 3 и Т 4 усиливают и синтез, и мобилизацию, и распад липидов, при повышении их уровня преобладает эффект общего уменьшения запасов жира в организме, похудение и снижение концентрации липидов (триглицеридов, холестерина и фосфолипидов) в крови. При снижении же уровня тиреоидных гормонов концентрация холестерина и других липидов в плазме возрастает, а масса тела увеличивается. Таким образом, не только ростстимулирующие гормоны, такие как соматотропин и инсулин, но и тиреоидные гормоны играют важнейшую роль в обеспечении нормального роста, развития и целостности тканей. Кроме того, йодтиронины оказывают многообразное влияние на функцию соматотропинсоматомединовой оси.

Одним из результатов общих метаболических эффектов тиреоидных гормонов является возрастание потребности в витаминах, которые играют важнейшую роль в качестве коферментов. Поэтому при гипертиреозе, несмотря на повышенный аппетит, без дополнительного введения витаминов развиваются авитаминозы. Тиреоидные гормоны стимулируют синтез, но, в большей степени, резорбцию костной ткани. При избытке Т 3 или Т 4 наблюдаются деминерализация костей с повышением риска переломов, гиперкальциемия и потеря кальция и фосфора с мочой и калом, ускоряется кругооборот белкового (коллагенового) матрикса кости. В результате возрастания основного обмена увеличивается потребность тканей в кислороде и теплопродукция. Эти факторы играют определенную роль в повышении минутного объема и увеличения кровотока по поверхностным сосудам, что способствует теплоотдаче через кожу.

Помимо этих влияний на сердечно-сосудистую систему, тиреоидные гормоны могут действовать на сердце как прямо, так и путем усиления эффектов катехоламинов. При небольшом повышении уровня тиреоидных гормонов в плазме сила сердечных сокращений возрастает, при значительном и длительном повышении их концентрации сила сердечных сокращений уменьшается, вероятно, вследствие усиления распада белков сердечной мышцы. Йодтиронины необходимы для психического развития человека. При их недостаточности в период между рождением и половой зрелостью ребенок остается не только физически, но и умственно отсталым (кретинизм) из-за недостаточного развития межклеточных контактов в головном мозге, гипоплазии нейронов коры больших полушарий и задержки миелинизации нервных волокон.

Если гормональную недостаточность не ликвидировать в первые недели после рождения, изменения становятся необратимыми. Гипотиреоз у взрослых характеризуется замедлением умственных процессов, ослаблением памяти, потерей инициативности, увеличивается время расслабления рефлексов, могут наблюдаться нарушения психики. Зобом называют любое увеличение щитовидной железы, а зобогенными веществами – те, которые вызывают образование зоба. Так, некоторые ионы (тиоцинат и перхлорат) ингибируют захват йода щитовидной железой, в результате чего уменьшение секреции Т 3 и Т 4 приводит к усилению секреции ТТГ, который стимулирует рост щитовидной железы. Ряд зобогенных веществ встречается в природе, так в капусте, например, найдены тиоцинаты

Зоб может развиться и при недостатке йодида в диете, что снижает его поступление в щитовидную железу. С другой стороны введение больших количеств йодида тормозит его органификацию. Фармакологические дозы йодида снижают секрецию Т 3 и Т 4 щитовидной железой. Заболевания щитовидной железы у женщин встречаются чаще, чем у мужчин, однако уровень йодтиронинов в плазме, их продукция и обмен не имеют половых различий, исключая особую ситуацию – беременность. Эстрогены уменьшают печеночный клиренс тиреоидных гормонов и усиливают синтез ТСГ в печени, что приводит к увеличению количества йодтиронинов в крови, например, при беременности. ПОДЖЕЛУДОЧНАЯ ЖЕЛЕЗА Поджелудочная железа обладает как экзокринной, так и эндокринной функцией. Продукты эндокринной секреции поджелудочной железы (панкреатические гормоны – инсулин, глюкагон, соматостатин, панкреатический полипептид (ПП) играют важнейшую роль, особенно в регуляции уровня глюкозы в крови. n

КОРОТКО в схемах (поджелудочная железа)
Поджелудочная железа - вторая по величине железа пищеварительного тракта, которая является железой смешанной секреции. Эндокринная часть (1 -2% от объёма железы) представлена клетками, которые расположены преимущественн о в области хвоста железы.
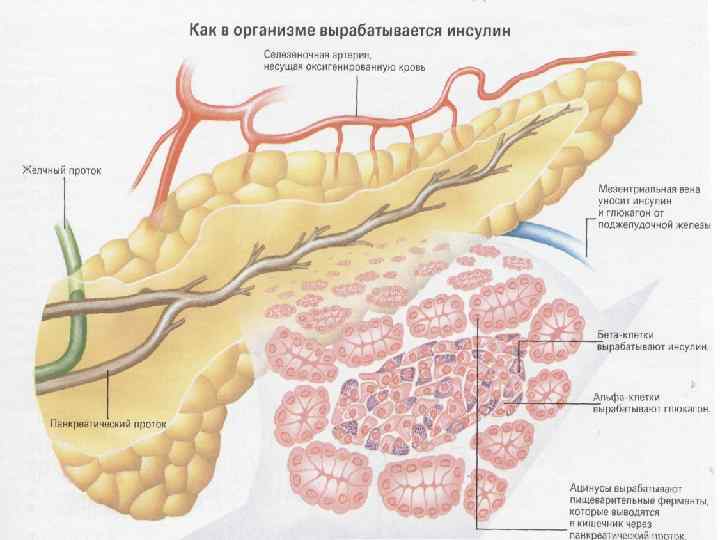

Инсулин. Образуется в b-клетках из его предшественника – проинсулина Функции: n n - Снижает концентрацию глюкозы в кровиусиливая ее , поглощение тканями и стимулирует синтез гликогена (запас глюкозы) в печени - Стимулирует синтез белка и липидов анаболический эффект), что приводит к увеличению белковых и жировых запасов в клетке и определяют роль инсулина в регуляции процессов роста и развития.

Инсулинзависимый диабет I типа – поджелудочная железа не способна вырабатывать инсулин; n обычно наблюдается с рождения и с подросткового возраста (аутоиммунное заболевание). n Дети уже в раннем возрасте учатся делать себе инъекции инсулина.
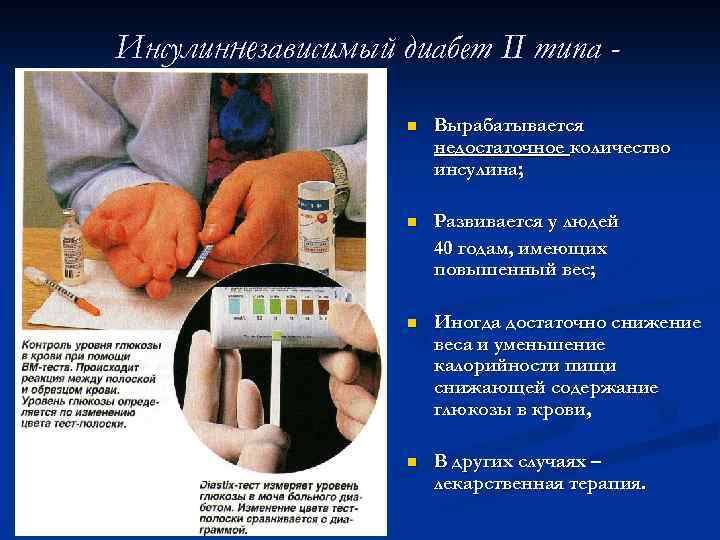
Инсулиннезависимый диабет II типа n Вырабатывается недостаточное количество инсулина; n Развивается у людей 40 годам, имеющих повышенный вес; n Иногда достаточно снижение веса и уменьшение калорийности пищи снижающей содержание глюкозы в крови, n В других случаях – лекарственная терапия.

Сахарный диабет (сахарное мочеизнурение) – заболевание, связанное с абсолютной или относительной недостаточностью инсулина. n n n n Характеристики: избыточное выделение мочи, гипергликемия, повышенное содержание сахара в моче (глюкозурия), жажда, потеря жидкости, физическая слабость, кома и, если не лечить, смерть.
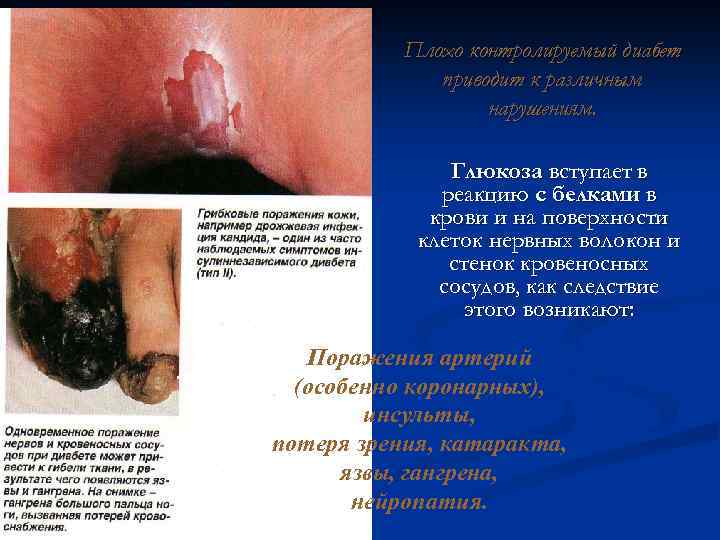
Плохо контролируемый диабет приводит к различным нарушениям. Глюкоза вступает в реакцию с белками в крови и на поверхности клеток нервных волокон и стенок кровеносных сосудов, как следствие этого возникают: Поражения артерий (особенно коронарных), инсульты, потеря зрения, катаракта, язвы, гангрена, нейропатия.

Глюкагон. Ф. э. : n запускает процессы превращения гликогена в глюкозу и поступление её в кровяное русло; n стимулирует липолиз, что повышает в крови количество свободных жирных кислот, которые используются в качестве энергетического материала; n стимулирует выделение жидкости. Во время голодания уровень инсулина в крови снижается, а глюкагона – повышается, особенно на 3 -5 й день голодания (примерно в 3 -5 раз).
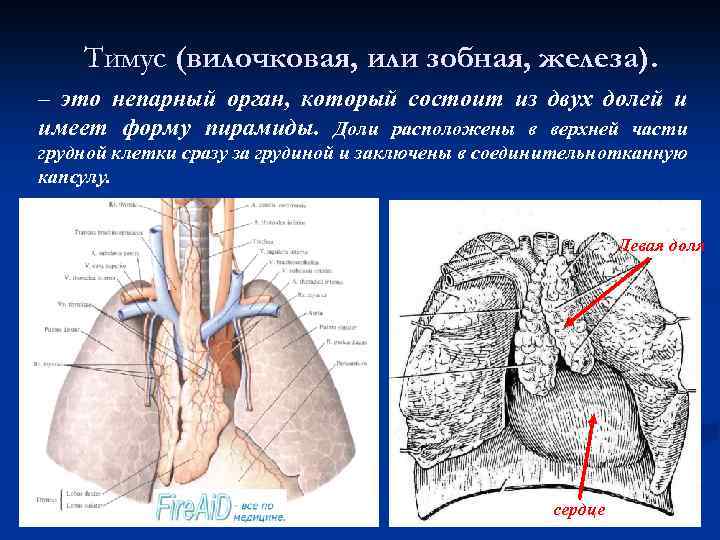
Тимус (вилочковая, или зобная, железа). – это непарный орган, который состоит из двух долей и имеет форму пирамиды. Доли расположены в верхней части грудной клетки сразу за грудиной и заключены в соединительнотканную капсулу. Левая доля сердце

Из тимуса был выделен ряд полипептидов (тимические гормоны) - тимозин, тимопоэтин, тимулин, тимусный гуморальный фактор и др. Остаётся неясным, отвечают ли эти вещества критериям гормонов и можно ли в связи с этим считать тимус эндокринной железой.
Ф. э. : n участвуют в обмене ионов фосфора и кальция; (стимулируют связывание Р и Са 2+ костной тканью); n участвуют в метаболизме железа, активируя эритропоэз (при удалении - анемия), n стимулируют лимфопоэз; n стимулируют синтез гликогена; n снижают содержание липидов. Наибольших размеров по отношению к весу тела тимус человека достигает к моменту рождения; затем он продолжает расти, хотя гораздо медленнее; в период полового созревания тимус достигает максимального веса, после чего начинается инволюция железы.

Использованная литература: n n Гайворонская И. В. , Ничипорук Г. И. Функциональная анатомия эндокринной системы. СПб. : «ЭЛБИ-СПб» , 2006, - 56 с. Климин В. Г. , Черешнев В. А. , Черешнева М. В. , Юшков Б. Г. Эндокринная регуляция физиологических функций (Избранные разделы физиологии). Учебное пособие. Екатеринбург: Ур. О РАН, 2001, - 103 с. Физиология человека / Под ред. Г. И. Косицкого. – 3 -е изд. , перераб. и доп. – М. : Медицина, 1985, - 544 с. , ил. Medinfo. ru

Развернутая форма (поджелудочная железа)

Главным стимулом к секреции инсулина служит повышение концентрации глюкозы в крови. При возрастании ее уровня выше 4 ммоль/л усиливается синтез и секреция инсулина. Мощными стимуляторами секреции инсулина являются и некоторые аминокислоты (например, аргинин). Жирные кислоты у человека обладают лишь слабым стимулирующим эффектом и вряд ли играют существенную роль в регуляции секреции инсулина. Стимуляция симпатических нервов, в основном, угнетает секрецию инсулина, а парасимпатических – усиливает. Торможение секреции инсулина при стрессе опосредуется, по всей вероятности, повышением симпатической активности. Упомянутые эфферентные пути опосредуют влияние центральной нервной системы на секрецию инсулина и тем самым на уровень глюкозы в крови. Поскольку стресс сопровождается повышенной секрецией глюкогенных гормонов (катехоламинов, кортизола, соматотропина), которые повышают концентрацию глюкозы в крови, неудивительно, что секреция инсулина (противодействующего влиянию этих гормонов) при этом тормозится.

На секрецию инсулина косвенно влияют многие гормоны, которые повышают концентрацию глюкозы в крови, например, соматотропин, усиливающий секрецию инсулина. Стимулирующим действием на секрецию инсулина обладают глюкокортикоиды, эстрогены и прогестерон. Их эффект отчасти связан со снижением чувствительности периферических тканей к инсулину, в результате чего возрастает уровень глюкозы в крови, который стимулирует синтез и секрецию инсулина. Инсулин прежде всего регулирует процессы обмена веществ, главным образом – концентрацию глюкозы в крови. Инсулин стимулирует процесс облегченной диффузии глюкозы в клетки, оказывая влияние на мембранные процессы. Инсулин влияет и на внутриклеточные процессы обмена веществ, влияя на изменение активности ферментов.

Так, инсулин стимулирует синтез гликогена, фосфорилирование глюкозы, ингибирует дефосфорилирование глюкозы с образованием свободной глюкозы, что обусловливает снижение продукции глюкозы. Снижение продукции глюкозы наряду с поглощением глюкозы периферическими клетками определяют снижение уровня глюкозы в крови под влиянием инсулина. Возрастающая под действием инсулина утилизация глюкозы клетками обеспечивает сохранение запасов других внутриклеточных энергетических субстратов (жиров и белков). Необходимо помнить, что при любом снижении секреции или ослаблении действия инсулина концентрация глюкозы в крови возрастает. Именно недостаточность инсулина чаще всего обусловливает сахарный диабет, основным проявлением которого является повышенная концентрация глюкозы в крови.

Это заболевание обычно характеризуется либо снижением продукции инсулина, либо нарушением чувствительности тканей к этому гормону (инсулиннезависимый сахарный диабет II). Инсулин стимулирует транспорт аминокислот в периферические клетки и синтез белка. Синтез белка усиливается и вследствие возрастания количества поступающих в клетку аминокислот. Возрастание утилизации глюкозы при действии инсулина замедляет распад белка. Ускорение синтеза и замедление распада белка под влиянием инсулина приводят к увеличению белковых запасов в клетке. Эффекты инсулина на белковый обмен определяют важнейшую роль инсулина в регуляции процессов роста и развития.

Инсулин стимулирует поглощение и окисление глюкозы клетками жировой ткани, стимулирует синтез ферментов, участвующих в гидролизе триглицеридов и способствует поступлению жирных кислот в адипоциты. Наряду с прямой стимуляцией липогенеза в печени и жировой ткани, а также ингибирования липолиза это приводит к увеличению запасов жира. Присутствие инсулина необходимо для поддержания внутриклеточной концентрации ионов калия. Этот эффект, по всей вероятности, является следствием прямого влияния гормона на клеточную мембрану. ГОНАДЫ (ПОЛОВЫЕ ЖЕЛЕЗЫ) Яички К мужским половым железам относятся яички. Яички взрослого человека выполняют две важные функции: - выработку зрелых мужских гамет (сперматозоидов) - сперматогенез - продуцирование стероидных гормонов – стероидогенез Полноценное осуществление этих функций начинается обычно в период полового созревания (12 -14 лет) и протекает до глубокой старости. n

Использованная литература: n n Гайворонская И. В. , Ничипорук Г. И. Функциональная анатомия эндокринной системы. СПб. : «ЭЛБИ-СПб» , 2006, - 56 с. Климин В. Г. , Черешнев В. А. , Черешнева М. В. , Юшков Б. Г. Эндокринная регуляция физиологических функций (Избранные разделы физиологии). Учебное пособие. Екатеринбург: Ур. О РАН, 2001, - 103 с. Физиология человека / Под ред. Г. И. Косицкого. – 3 -е изд. , перераб. и доп. – М. : Медицина, 1985, - 544 с. , ил. Medinfo. ru

Коротко (половые гормоны)

Гонады (половые железы). Яички. Яичники. Эстрогены (гормоны яичников). Андрогены.
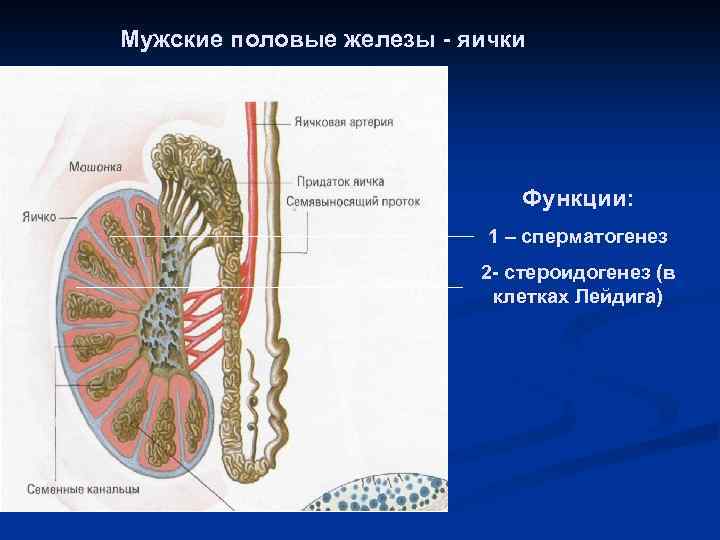
Мужские половые железы - яички Функции: 1 – сперматогенез 2 - стероидогенез (в клетках Лейдига)
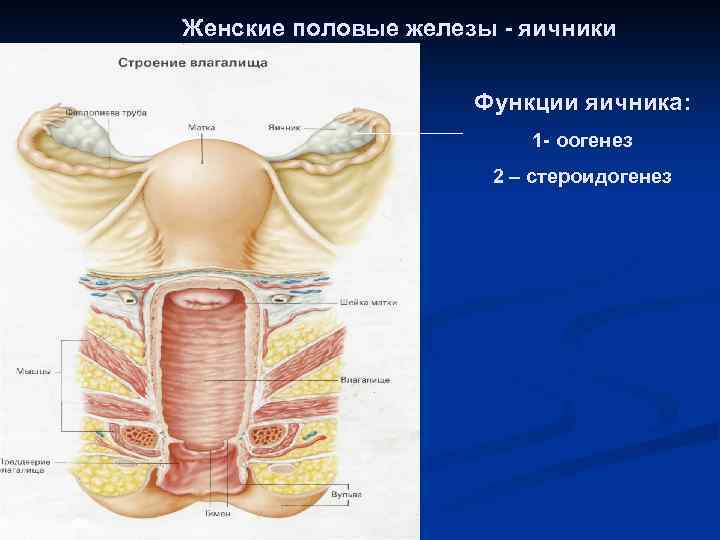
Женские половые железы - яичники Функции яичника: 1 - оогенез 2 – стероидогенез
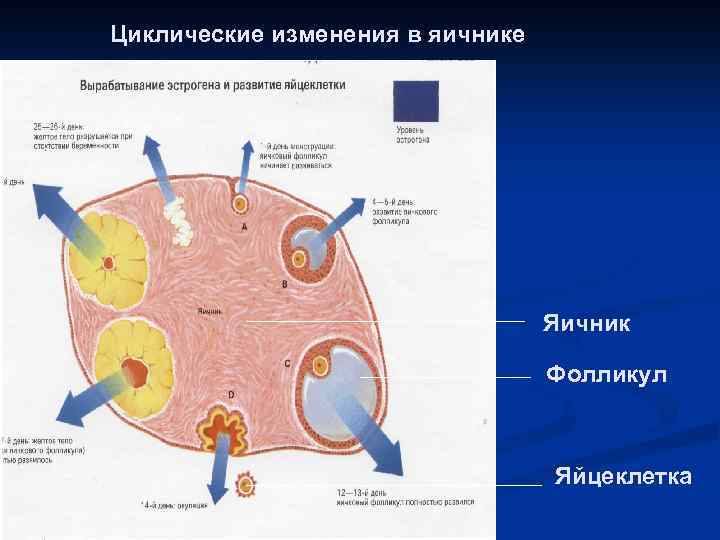
Циклические изменения в яичнике Яичник Фолликул Яйцеклетка

Фазы менструального цикла (изменения в яичнике) Фолликулярная фаза n Овуляция n Лютеиновая фаза n

Эндометриальные циклы (изменения в матке) 1. Пролиферативня фаза n 2. Секреторная фаза n

Развернутая форма (половые гормоны)

Стероидогенез заключается в синтезе стероидных гормонов, необходимых для развития и сохранения способности мужчин к размножению. Гормоны, индуцирующие рост и поддержание развития мужского полового тракта, называются андрогенами. В количественном отношении первое место среди продуцируемых яичками андрогенов занимает тестостерон, 95% которого синтезируется в яичках, а остальная часть – в коре надпочечников. Пути биосинтеза тестостерона в яичках и коре надпочечников одинаковы. Исходным веществом служит холестерин. Интенсивность синтеза тестостерона лимитируется превращением холестерина в прегненолон и контролируется лютеинизирующим гормоном гипофиза (ЛГ). Тестостерон способен превращаться во многих клетках-мишенях в более активный андроген – дигидротестостерон (ДГТ).

В ряде периферических тканей и в яичках происходит ароматизация тестостерона в эстрадиол. В качестве побочных продуктов клетки яичек постоянно секретируют небольшие количества эстрадиола и прогестерона, хотя роль этих гормонов в развитии и поддержании функции размножения у мужчин до настоящего времени не выяснена. Андрогены стимулируют рост и развитие мужского полового тракта, в который входят яички, система мужских протоков и добавочные органы (секреторные железы: предстательная железа, семенные пузырьки и бульбоуретральные железы, а также половой член). Все эти органы принимают участие в транспорте сперматозоидов или продуцировании необходимых компонентов семенной жидкости. В ростовой фазе полового созревания андрогены стимулируют увеличение объема мошонки, а также под их влиянием она становится морщинистой и пигментированной. Тестостерон необходим и для нормального сперматогенеза.

Андрогены определяют также внешний вид и развитие вторичных половых признаков у мужчин. К таким признакам относится мужское телосложение – развитая мускулатура и более высокий рост, что связано, главным образом, со стимуляцией синтеза белка. Андрогены обладают мощным анаболическим действием и стимулируют клеточное деление. Во время полового созревания они ускоряют линейный рост тела (действуя совместно с гипофизарным соматотропином – гормоном роста), но одновременно способствуют и остановке роста, так как стимулируют сращение эпифизов длинных костей с их стволами. Андрогены усиливают рост волос на лице и теле, обусловливают лобное облысение и снижают тембр голоса вследствие утолщения голосовых связок и увеличения объема гортани.

Андрогены, по все вероятности, определяют появление либидо и поддерживают его, а также влияют на половое поведение, хотя не совсем ясно, насколько это зависит от гормонов, а насколько – от факторов окружающей среды (социальных условий, ролевых установок и т. п. ). Характерные для мужчин поведенческие реакции агрессивность) обусловлены, по-видимому, гормональных и средовых влияний. (например, сочетанием К другим эффектам андрогенов относятся стимуляция секреции сальных желез, что часто вызывает появление угревой сыпи у мальчиков в период пубертата, и некоторая задержка в организме различных ионов (натрия, калия и кальция) и воды.

Яичники К женским половым железам относятся яичники, которые выполняют две важнейшие функции, аналогичные функциям яичек: - выработка зрелых гамет (яйцеклеток) – оогенез - продукция стероидных гормонов – стероидогенез. n Зрелые яичники функционируют циклично. Эти циклы, называемые менструальными, поскольку имеют примерно месячную периодичность, устанавливаются в пубертатном возрасте и прекращаются в менопаузальном возрасте. Циклические изменения в яичниках называются овариальными циклами, которые включают созревание фолликулов, овуляцию, образование желтого тела и продуцирование гормонов, которые определяют изменения в матке. Каждый овариальный цикл состоит из двух фаз – фолликулярной и лютеиновой, которые разделены процессом овуляции (выхода яйцеклетки).

Циклические изменения в матке называют эндометриальными циклами, включающими подготовку эндометрия к возможной имплантации оплодотворенной яйцеклетки. n Эстрогены Женские половые гормоны - эстрогены продуцируются клетками фолликулов в зрелых яичниках, желтым телом, фетоплацентарным комплексом (во время беременности) и, в небольшой степени, надпочечниками. Образование яичниковых эстрогенов в фолликулярную фазу предполагает синтез андрогенов (андростендиона, который может превращаться в тестостерон) из прогестерона. Андрогены, продуцируемые клетками фолликула, подвергаются ароматизации с образованием эстрогенов в клетках фолликула. Во время лютеиновой фазы эстрогены синтезируются клетками желтого тела. Важную роль в превращении андрогенов (главным образом, андростендиона) в эстрогены (эстрон) играет жировая ткань.

Она оказывается главным источником эстрогенов в крови у женщин после наступления менопаузы, когда продуцирование этих гормонов яичниками прекращается. Это объясняется способностью жировой ткани превращать андростендион в эстрон, что компенсирует выпадение яичниковой продукции эстрадиола. На протяжении менструального цикла содержание эстрогенов в плазме претерпевает резкие колебания. В фолликулярной фазе уровень эстрадиола возрастает до преовуляторного пика, затем он снижается, но в середине лютеиновой фазы наблюдается второй, обычно меньший пик. Эстрогены во многом определяют изменения, происходящие во время менструального цикла, влияя на аденогипофиз и, вероятно, на гипоталамус по механизмам отрицательной и положительной обратной связи.

Эстрогены обеспечивают развитие и поддерживают структуру матки, фаллопиевых труб, шейки матки, влагалища, малых и больших половых губ и молочных желез. Они имеют большое значение для роста эндометрия, а также для синтеза рецепторов прогестерона в ткани матки. Эстрогены стимулируют секрецию более водянистой и щелочной слизи шейкой матки, что способствует сохранению и транспорту сперматозоидов, изменяют цитологию влагалища, усиливая ороговение эпителия за счет повышенного синтеза кератина, увеличивают подвижность фаллопиевых труб и повышают возбудимость маточной мышцы. Во время беременности эстрогены стимулируют рост и развитие системы протоков молочных желез, рост миометрия (увеличение содержания в нем гликогена и актомиозина) и придают ему чувствительность к действию окситоцина.

Развитие вторичных половых признаков у женщин (широкие бедра, отложение жира в области молочных желез и ягодиц и меньшее оволосение тела) определяется соотношением между эстрогенами и андрогенами. По всей вероятности, эстрогены, как и андрогены, влияют на центральную нервную систему и в какой-то мере определяют половое влечение и различные другие аспекты женского поведения. В разных отделах мозга присутствуют рецепторы и эстрогенов, и андрогенов, и гестагенов. Влияние этих гормонов на развитие мозга и их поведенческие эффекты активно изучаются в настоящее время. Эстрогены обладают слабым анаболическим эффектом, но снижают содержание холестерина в крови. Последний эффект, возможно, связан с увеличением синтеза липопротеинов высокой плотности (ЛВП), которые уменьшают риск развития сердечно-сосудистых заболеваний, и уменьшением синтеза липопротеинов низкой плотности (ЛНП), играющие роль в генезе сердечно-сосудистых заболеваний.

Это может быть одним из факторов, определяющих меньшую частоту атеросклероза и сердечных заболеваний у женщин предменопаузального возраста. Эти гормоны могут вызывать некоторую задержку соли и воды в организме. Они способствуют также выходу электролитов и воды из сосудистого русла, что иногда вызывает увеличение массы тела и повышение чувствительности молочных желез перед менструацией. Это в какой-то степени объясняет раздражительность и чувство напряжения в предменструальный период ( «предменструальное напряжение» ). Еще один защитный эффект эстрогенов, исчезающий после наступления менопаузы, заключается в поддержании массы костной ткани. Механизм этого эффекта не совсем ясен.

n Прогестерон Наиболее активным природным гестагеном в женском организме является прогестерон. Прогестерон не только обладает собственными эндокринными эффектами, но и служит предшественником других стероидов во всех стероидпродуцирующих тканях. Прогестерон секретируется, главным образом, желтым телом во время лютеиновой фазы менструального цикла и фетоплацентарным комплексом во время беременности. Однако, в небольших количествах он также вырабатывается у того и другого пола корой надпочечников. В фолликулярной фазе менструального цикла концентрация прогестерона в плазме обычно составляет менее 5 нмоль/л, а в лютеиновой – достигает максимума – 40 -50 нмоль/л. У мужчин его уровень в плазме гораздо ниже – примерно 1 нмоль/л.

Секреция прогестерона сопровождается повышением базальной температуры тела, которое происходит сразу после овуляции и сохраняется на протяжении большей части лютеиновой фазы, пока уровень прогестерона не начнет снижаться. Повышение температуры часто считают результатом прямого влияния прогестерона на терморегуляторный центр в гипоталамусе, но эта точка зрения сегодня оспаривается. Прогестерон обусловливает секреторные изменения в эндометрии, изменяет секреторную активность шеечного и влагалищного эпителия, стимулирует рост и развитие альвеолярной системы молочных желез, что имеет особое значение для лактации. Его влияние на миометрий во время беременности противоположно влиянию эстрогенов: возбудимость мышцы снижается.

Прогестерон, вероятно, оказывает влияние на центральную нервную систему (например, участие в регуляции ее развития и определение особенностей поведения индивида), но эти эффекты еще недостаточно изучены, хотя наличие рецепторов прогестерона в определенных участках головного мозга не вызывает сомнений. Поведенческие и другие психологические сдвиги в предменструальный период могут быть связаны с изменением секреции прогестерона. В высоких концентрациях прогестерон обладает натрийуретическим действием. Натрийурез приводит к усилению секреции альдостерона и натриевый баланс нормализуется. Компенсаторное увеличение секреции альдостерона наряду с сользадерживающим влиянием эстрогенов может определять характерные симптомы в предменструальный период.

Андрогены В норме в женском организме вырабатывается гораздо меньше андрогенов, чем в мужском и их основным источником являются надпочечники. Тем не менее в ходе менструального цикла синтез андрогенов клетками фолликулов возрастает, хотя их эффекты остаются неизвестными. n Показана основная их роль в качестве предшественников синтеза эстрогенов. При чрезмерном возрастании соотношения «андрогены/эстрогены» у женщин появляются признаки маскулинизации, например, вирилизация и гирсутизм с нарушение менструального цикла. Концентрация тестостерона в плазме у женщин в норме составляет 0, 5 -2, 5 нмоль/л, во время беременности она возрастает до 3 -6 нмоль/л.

водно минеральный обмен, гормоны.ppt