+Лек1,2.Фитоиммунитет-2014.pptx
- Количество слайдов: 157



n В лекции будут рассмотрены также вопросы: -Краткие итоги изучения устойчивости растений к болезням в морфолого-цитологическом, физиолого-биохимическом и популяционно-генетическом аспектах, теория ген-на-ген. -Молекулярно-биологический подход к анализу структуры и функций генов авирулентности патогенов и резистентности растений, R-гены в роли «будильника» хозяина. -Специфичность взаимодействия в системе растение−патоген; индукция, суппрессия, модификация сверхчувствительности (апоптоза) и/или включение в клетке механизмов защиты. -Врожденный иммунитет. Двухуровневая (межвидовая и расосортовая) система распознавания растением чужеродного. -Дупликация и кластеризация R-генов, расположение их на разных хромосомах. Хромосомные карты с R-генами. -Вероятные онтогенетические функции R-генов. -Системный иммунитет и система иммунитета у растений. -Представление о фитоиммунитете как эволюционной разновидности общебиологического феномена.

Иммунитет растений является научной проблемой, которая теснейшим образом связана с практическими задачами сельскохозяйственного растениеводства, лесного хозяйства и фармакологии. Руководство Республики Беларусь, как и других государств, уделяет этим задачам первостепенное внимание, поскольку они входят в ряд важнейших вопросов, таких как «Биосырьевой потенциал» и «Продовольственная безопасность» – стратегических направлений обеспечения жизнеспособности нации. ►Т. о. , изучение распространения инфекционных заболеваний, ежегодные изменения расового состава популяций фитопатогенов и выявление условий и признаков эпифитотий – не только биологическая (фитопатологическая) проблема, но и хозяйственная и военно-политическая проблема – составная часть обеспечения безопасности государства.

Во время так назыв. «холодной войны» − противостояния СССР и США, часть научных исследований в области фитозащиты была закрыта. Да и в настоящее время в военных ведомствах стран, претендующ. на лидирующ. роль в мире, рассматривается возможность поражения инфекциями важнейших продовольств. культур потенциального противника. В связи с вышесказанным, как альтернатива подобным возможностям, в мире ведется интенсивное изучение основ болезнеустойчивости растений к важнейшим возбудителям инфекций, создаются устойчивые сорта и разрабатываются все новые средства и приемы защиты культур. После открытия в начале 20 в. наследственных основ взаимоотношений растения-хозяина и патогена проводилась большая работа по непрерывной селекции устойчивых сортов и физиологич. влияниям на растение, повышающим его сопротивляемость инфекции, что позволило обеспечить его продолжительную невосприимчивость, либо выносливость к возбудителям заболеваний. Центральной частью этих исследований является всестороннее изучение иммунитета растений.

В мире ведется интенсивное изучение основ болезнеустойчивости растений к важнейшим возбудителям инфекций, создаются устойчивые сорта и разрабатываются все новые средства и приемы защиты культур. n Центральной частью этих исследований является всестороннее изучение иммунитета растений как биологического феномена: эволюционных основ его происхождения, химической природы участвующих молекул, структурных и функциональных механизмов их действия, возможность наследования и приобретения этих механизмов, возможность оказания на них регулирующего влияния.

Касаясь самым кратким образом основных вех в истории становления фитоиммунологии как науки надо отметить, что первые этапы ее развития и первые достижения сделаны с использованием трех главных подходов: описательного, микроскопического и химического. n n n Несмотря на то что описательный подход является самым древним и первоначально связан с характеристикой макроскопических проявлений заболеваний растений, тем не менее он используется широко и теперь для изложения экспериментальных данных, полученных с применением новых методик. Микроскопический метод в исследовании различных аспектов инфекционной природы заболеваний растений и проявлений защиты важен и сыграл свою роль потому, что большинство возбудителей имеет микроскопические размеры, различимые только с помощью оптических или электронных микроскопов. Этот подход в его новых преломлениях таких как флуоресцентный анализ, спетрофотометрия в сочетании со световой и электронной микроскопией, иммуногистохимией, молекулярной биологией и другими используется теперь и имеет будущее. Химический анализ арсенала нападения фитопатогенов и защиты растений представлял и представляет важную составную часть современных исследований в области фитоиммунитета, проводимых на уровне молекул, органелл, клеток и тканей, а также целых растений и их ассоциаций.

n n А. Декандоль в 1832 г. болезни растений рассматривал как последствия отклонений от нормальных физиологических функций под влиянием окружающей среды или паразитов, поселяющихся в тканях. Хотя определение фитопатогенеза это точно, оно не может провести четкую грань между больным и здоровым состоянием, т. к. у многих сортов, полученных путем гибридизации, отмечали отклонения в химическом составе или функциях от уровня родительских. Приоритет в установлении инфекционной грибной патологии растений отдают Б. Прево и А. Де Бари, которые в 1807 и 1853 гг. на головневых и ржавчинных патогенах злаков и в 1861 г. на фитофторе – возбудителе картофеля, показали детальные стадии инфекционного процесса в этих комбинациях растение/патоген. А. Де Бари первый стал изучать динамику болезни растения, ее стадии. С конца 70 -х гг. в. началось исследование бактериальных инфекций (Е. Ф. Смит, 1893 г. ). Вирусные болезни были известны давно, но вначале их выделяли в особый разряд заболеваний (А. Майер, 1886, Д. Ивановский, 1892, М. Бейеринк, 1898), этиология же стала изучаться только с развитием техники.

М. Уорд (1890), ученик А. Де Бари, стал рассматривать фитопатогенез как определенное физиологическое состояние растительного организма, связанное с изменением его основных функций, но еще не представляющем смерть. Это состояние «предсмерти» хозяина часто продолжительно и используется паразитом. n n Были также выдвинуты теории иммунитета: механическая (М. Уорд, 1890, В. Фаррер, 1898, О. Комес, 1909); физиологическая (Ю. Эрикссон и Э. Хеннинг, 1896); хемотропическая (В. Пфеффер, 1884, Д. Масси, 1905); фагоцитарная (Н. Бернар, 1909, Комаров В. Л. , 1915, Ж. Дюффренуа, 1929, Мечников И. И. , 1950). Первые три связывали фитоустойчивость с определенными морфо-анатомическими особенностями растений – опушенностью листа, толщиной кутикулы, расположением устьиц, выделяемыми факторами хемотропизма р. Н клеточного сока. Хотя главный смысл термина фагоцитоз как раз означает внутриклеточное переваривание, завершающий акт захвата бактерии в клетку, но Ноэль Бернар феномен фагоцитоза у сем. орхидных рассматривал прежде всего как защитную реакцию, а не как способ питания растений. Он акцентировал внимание на том, что при фагоцитозе может возникать состояние взаимотерпимости – симбиоза, которое может быть достаточно продолжительным. Эта физиологическая реакция защиты растений к инфекции и способность к симбиозу позволила Н. Бернару сравнить ее с вирулентностью патогенных микроорганизмов.

Н. Бернар рассматривал иммунитет как результат длительной сопряженной эволюции паразита и хозяина. Такой эволюционный подход позволил ему удержаться от ошибки основателей прочих теорий иммунитета: он вовсе не рассматривал фагоцитоз как единственную причину иммунитета растений, но, наоборот, всячески подчеркивал, что этих причин несколько. n Его последователь Дюффренуа называет следующие три причины создающие иммунитет растений: • механическое сопротивление клеточной стенки, • фагоцитоз и • гуморальные факторы. Аналогичные причины ответственны за иммунитет животных, что приводит Дюффренуа к выводу о применимости всех теорий иммунитета из общей патологии к царству растений. Впоследствии выявили высокую степень общности генома, химического строения клеток, метаболизма и физиол. реакций. n

Развитие представлений о природе иммунитета растений в 20 в. n Фитонцидная теория (Токин Б. П. , 1928, 1940, Вердеревский Д. Д. , 1957, Горленко М. В. 1957, Новотельнов Н. В. , 1957, Van Sumere, 1971): фитонциды – летучие (1 -я линия обороны) и нелетучие (2 -я линия) в-ва, растительные аналоги антибиотиков, действующие против микроорганизмов; это – эфирные масла, кумарины, хиноны, глюкозиды, бальзамы, смолы, непредельные жирные кислоты, антоцианы, флавоноиды, фитостероиды, сапонины, дубильные вещества, алкалоиды). n Фитоалексинная теория (Мюллер К. , Бергер Х. /Оффорд. Г. , 1940, Метлицкий ЛВ. , Дьяков ЮТ. , Озерецковская ОЛ. , 1973 – факторы физиологического иммунитета, образуемые живыми клетками растений в ответ на действие индуктора из патогена, продукта взаимодествия его с клетками растения, или же некоторого химического иммуноиндуктора – это терпеноиды и фенольные соединения разной степени сложности). n Питательно-тормозящая (Гарбер Е. Д. , 1956, Эфроисон В. П. , 1961, Сухоруков К. Т. , 1959). n Оксидаз, белковых комплементарных систем и др. (Бах А. Н. , 1912, Палладин В. И. , 1913, Федотова Т. И. , 1935, Рубин Б. А. , 1940, Дунин М. С. , 1946, Страхов Т. Д. , 1959, Ван дер Планк Я. , 1961, 1980).

Р а н е е, до конца 80 х годов ХХ в. , Иммунитетом называли высшую степень устойчивости растений к заражению патогенами, т. е. практически полное отсутствие живых клеток возбудителя внутри тканей и органов растения. В этом определении содержится лишь констатация факта, результат явления, без указаний на его основы, механизм осуществления. Твердо установленным считалось отсутствие иммунитета и системы обеспечения явления в традиционном медицинском понимании в отношении растений, и любая постановка вопроса о возможных аналогиях рассматривалась как попытка возрождения лженаучных представлений и пресекалась. Однако И. И. Мечников, создатель общебиологической Мечников теории иммунитета (1902) определил устойчивость к инфекционным заболеваниям как общую систему явлений, свойственную растениям и животным, благодаря которым организм выдерживает нападение патогенных организмов. К последним относят: вирусы, бактерии, грибы, нематоды, некот. насекомые и их личинки.

В современном понимании иммунитет – способ защиты организма от живых тел и веществ, несущих на себе признаки генетической чужеродности (Р. В. Петров, 1987 г. ) ►Основной функцией иммунитета считается охрана постоянства внутренней среды организма в течение его жизни на основе способности отличать «свои» молекулы и клетки от «чужих» . Это – закон охраны индивидуальности. Наследственность охраняет ее в нисходящем ряду поколений, иммунитет – на протяжении индивидуальной жизни организма Свойства резистентности, наследуемые от предков, относят к наследственному, конститутивному иммунитету. Если устойчивость вырабатывается в процессе жизни самим организмом, иммунитет относят к приобретенному.

По механизму действия выделяют факторы − конституционные, фагоцитарные и лимфоидные. У человека и высших животных способность развивать иммунный ответ не есть некое общее свойство всего организма. Иммунологическую (т. е. защитную, гомеостатическую) функцию выполняет специализированная система лимфоидных клеток, тканей и органов. Общее число лимфоидных клеток 1012, а масса этого диффузного органа у человека равна 1, 5 2 кг. У нее 3 главные особенности: ►она генерализована по всему телу, ► ее клетки постоянно рециркулируют по телу через кровоток, и ► она обладает уникальной способностью вырабатывать сугубо специфические молекулы антител против каждого антигена. Антигены – вещества, которые несут признаки генетической чужеродности и при введении в организм вызывают развитие специфических иммунологических реакций. Или: антигены – вещества, которые при введении в организм вызывают в нем образование антител.

Все биологические полимеры обладают разной степенью антигенности, которая присуща белкам, полисахаридам, липопо лисахаридам гликопротеинам, нуклеопротеидам и полипептидам, а также некоторым искусственным соединениям. Простые элементы – железо, медь, сера, фосфор и др. , не могут быть антигенами. То же относится и к таким органическим молекулам как моно и ди сахара, аминокислоты и даже макромолекулам: нуклеиновые кислоты и липиды без примесей других веществ. Однако, в целом, специфичность проявляется на уровне организации круп ных биологических молекул. Аминокислоты, соединяясь в цепь пептидов некоторой длины и сложности, приобретают антигенность. Гомопептиды из одной аминокислоты неантигенны и не обнаруживают специфического узора генетической чужеродности. Но ди и особенно трипептиды со случайной последовательностью аминокислот − антигенны. Антигенность пептидов неодинакова, она определяется соотношением аминокислот и их расположением в цепи. Антигенны лишь полипептиды из L-, но не из D-аминокислот. Включение ароматических аминокислот (тирозина, триптофана, фенил-аланина) повышает антигенность цепи пептида или ведет к появлению новой специфичности. Фенол-производные играют роль гаптенов, повышающих уровень антигенности молекул. Антигенность по является у денатурированной и однонитчатых ДНК, у ДНК с протеидом, у липидов, связанных с белками или углеводами. Сложные молекулы могут иметь 2 и больше антигенные специфичности.

Главная – видовая специфичность молекул, которая отличае представители одного вида от другого. Многие макромолекулы организма несут признаки видо-специфичности. Альбумины и глобулины выполняют разные функции и различаются иммунологически. Это – функциональная специфичность. Реакции взаимодействия антиген–антитело проявляются в форме: а) агглютинации (склеивания), б) прецепитации (помутнения и осаждения). В случае переизбытка антигена или антитела агрегация и прецепитация не наблюдается, а образуется растворимый комплекс антиген–антитело. Есть 5 классов иммуноглобулинов человека: Ig. M, Ig. G, Ig. A, Ig. E, Ig. D. Они имеют молекулярную массу от 150000 до 90000, различаясь по физико-химическим и функциональным, а также по антигенным свойствам тяжелых полипетидных цепей− µ, γ, α, ε, δ и легких − κ или λ. У тяжелой и легкой цепей на поверхности находятся 2 активные группы, вследствие чего молекула антитела может соединять антигены в конгломераты различной

Основную массу сывороточных иммуноглобулинов составляет далее идут Ig. A (10 -15%) и мало (около 0, 2%). Ig. G (70 -80%), Ig. M (5 -10%); иммуноглобулинов классов E и D очень После рождения ребенка в его крови преобладает (до 99%) Ig. G Секреторные иммуноглобулины класса А выходят за пределы слизистых оболочек в просвет кишечника, дыхательных путей и др. , являясь «первой линией обороны» организма. После введения антигена в организм взрослого человека первыми в крови появляются Ig. M, затем Ig. G; Ig. A появляются позже. Филогенетически наиболее ранней формой антител является Ig. M Рыбы последние в филогенетическом ряду организмы, способные хоть и слабо, синтезировать антитела в ответ на введение антигенов. Система комплемента (алексина) также участвует а специфических алексина реакциях, обеспечивая лизис клеток бактерий. Фагоциты участвуют в кооперации Т и В лимфоцитов – т. е. тимусзависимых и не зависимых в своем развитии от вилочковой железы. Цитотоксические Т лимфоциты при контакте с чужой клеткой убивают ее, образуя пору в оболочке.

Что отличает растительный организм от животного? Это – прикрепленный образ жизни, отсутствие подвижности в вегетативной форме существования; наличие жесткой клеточной стенки; присутствие центральной вакуоли; наличие хлоропластов и отсутствие специальной жидкости, клеточных элементов и циркуляторной системы, тесно связанных с защитой всего организма от инфекции. « …. в вопросе поиска у растений антител заметного прогресса нет и сомнительно, будет ли он в будущем. Структура растений так отлична от животных, особенно касательно сообщающейся системы, что надо думать о глубоких различиях между иммунными системами царств животных и растений» . (Owens, 1928).

Итак, у растений такой сложной, как у животных, системы защиты организма нет. Но это не значит, что иммунитет растений характеризуется чрезвычайно простым устройством и механизмом функционирования.

В системе воззрений Н. И. Вавилова на фитоиммунитет можно выделить несколько положений. n Первое – о специализации взаимоотношений паразита и растения, исключающей конкуренцию между популяциями и определяющей существование иммунных форм, т. е. чем ýже специализация паразита в выборе растений-хозяев, тем выше вероятность нахождения устойчивых разновидностей. n Важным является второе положение – о генотипической (наследственной) природе фитоиммунитета – конституционном иммунитете. n Третье положение – о географической локализации генов растений, объясняющей групповую устойчивость/восприимчивость растений к болезням и вредителям в местах их сопряженной эволюции; n четвертое – о связи реакции сортов и разновидностей на поражение с влияние условий среды; n пятое – о практической направленности группового (комплексного) иммунитета; n шестое – о возможности прогнозирования и принципах поиска иммунных форм, т. е. о сходстве генетически близких родов и видов растений и сопряженности их с эволюцией патогенов в ареалах происхождения, позволяющих выстраивать их в гомологические ряды. Проследим за путем, как эта новая идея Н. И. Вавилова получала подтверждение и пробивала себе дорогу среди преобладающих представлений.

Убедительные доказательства того, что иммунитет растения связан не только с механическими особенностями покровной ткани, а главным образом определяется внутренней жизнедеятельностью клеток, их активной реакцией на проникновение гиф гриба были приведены в начале 20 в. в работах Ward и его учеников (P. Evans и др. ). Они считали, что 1 -м барьером на пути паразита являются клеточ. стенки, а затем уже протоплазма, активно противостоящая энзимам и ядам, выделяемым гифами грибов. Интересна и отмеченная Уордом аналогия прорастания спор патогенных грибов на поверхности растения и пыльцы на рыльце пестика в явлениях инфекции и оплодотворения, соответственно. В обоих случаях в несоответствующих сочетаниях наблюдается реакция отторжения грибных и пыльцевых ростковых трубок.
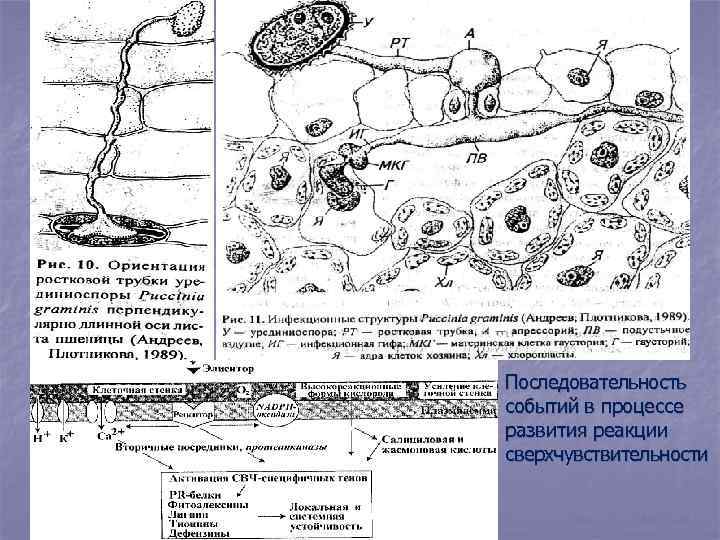
Последовательность событий в процессе развития реакции сверхчувствительности

n n n Были проведены цитологические и гистохимические исследования в различных комбинациях растение−патоген, которые подтвердили активную реакцию растительных клеток против проникающих патогенных грибов, в том числе некротрофных на ранних стадиях взаимодействия. Эти исследования выявили образование папиллы с отложениями каллозы, пероксидазы, фенольных соединений и признаками лигнификации на поверхности растительных клеток в местах проникновения патогенов. В корнях растений с эндомикоризой обнаружено образование клубков гиф в клетках около камбиального слоя (с интенсивной митотической активностью), который задерживал проникновение гриба в неколонизированные им участки корня.



n. При поражении корней и стеблей растений паразитными видами выявили образование каллусов при начальном врастании, проникновение паразита в проводящую систему растенияхозяина, завершающемся полным срастанием их сосудистых систем в совместимых комбинациях (как и в эффективных комбинациях подвой–привой) или отторжением в несовместимых комбинациях хозяин–паразит (и аналогичным отторжением в неэффективных комбинациях подвой–привой). n Соприкосновение дедифференцированных каллусов на питательной среде in vitro завершается взаимоотторжением тканей, сопровождающемся сверхчувствительной некротизацией клеток одной из культур. n. Это свидетельствует о врожденной способности растительных клеток распознавать при контакте присутствие чужеродных клеток и молекул и реагировать на проникновение таких клеток или их метаболитов в стенки и в межклетники каллусной массы. n В местах несовместимой реакции клеток развивается окислительный и лизосомальный взрыв, т. е. чрезвычайно бурная реакция на присоединение к клеточной поверхности «чужих» молекул.

Врастание корня растения-паразита в корень

Согласно И. И. Мечникову, существует 2 типа реакций сопротивления инфекции: а) направленные на обезвреживание токсинов, выделяемых патогенами, б) направленным против самого возбудителя болезни. n n n Антитоксическая реакция имеет большое значение у заболеваний, вызываемых факультативными паразитами и полусапротрофами. Например, у восприимчивого сорта капусты при поражении грибом Botrytis есть большая разница в размерах площади, занятой мицелием и пораженной вырабатываемым им токсином (потемневшая ткань), а у устойчивого сорта наблюдается почти полное совпадение размеров этих территорий. Т. е. у восприимчивого сорта влияние токсина распространяется на значительное расстояние от границы проникновения гиф в растительную ткань, а у устойчивого сорта эти границы почти совпадают. Реакциям непосредственно против патогена И. И. Мечников отводил основную роль. В 1911 г. Ноэль Бернар пришел к выводу, что иммунитет у орхидей, контролирующий скорость распространения микоризного гриба по растительным тканям, как и в случае животных, может быть 2 типов: клеточным (фагоцитоз) – в случае естественного врожденного иммунитета, и гуморальным – в случае приобретенного. В. Л. Комаров, долго и упорно изучавший взаимоотношения микоризного гриба и орхидей, в 1915 г. заключил: «Гриб своими выделениями вызывает в клетке, его приютившей, образование антител, совершенно парализующих его деятельность и отдающих его во власть энзимов-растворителей. Наблюдающееся при этом изменение формы и размеров ядра и особенно распределения в нем хроматина как бы указывает на то, что ядро − физиологический орган, участвующий в выработке энзимов и антител. Разрушение головневых грибов в тканях растений, похожее на переваривание у насекомоядных растений, описал Т. Д. Страхов.

n Эти идеи впоследствии были развиты некоторыми другими учеными. В. И. Палладин (1913) выдвинул «гипотезу антиферментов» , согласно которой ферменты паразита, проникшего в клетку устойчивого растения инактивируются энзимами и белковыми ингибиторами последнего. Т. И. Федотовой (1935) эти идеи были преобазованы в представления об «иммунологическом сродстве белков возбудителей и растений-хозяев» . n Позже эти взгляды легли в основу гипотезы «сополимеризации белков патогена и хозяина» Я. Ван дер Планка. n Было установлено, что пораженные растительные клетки дышат в 2 раза интенсивнее здоровых. Однако роль окислительных процессов в явлениях фитоиммунитета получила неоднозначную оценку. n К. Т. Сухоруков (1952) заключил, что при заражении хлопчатника вилтом повышенная активность пероксидазы благоприятствует распространению некрозов клеток вблизи сосудистого пучка и распространению там патогенного гриба. n Альтернативная точка зрения была выдвинута А. Н. Бахом и стала развиваться его учеником Б. А. Рубиным. Согласно ей, в борьбе растения с патогеном окислительные процессы играют важную роль, поскольку уровень активирования дыхания после инфицирования грибом у устойчивых растений выше, чем у восприимчивых; кроме того, энергетическая эффективность дыхания (сопряженность дыхания с фосфорилированием) у устойчивых сортов обычно выше, чем у восприимчивых.

n. Изучение процессов фотосинтеза В. Ф. Купревичем, З. Я. Серовой выявило повышение этих процессов на первой стадии патогенеза при инфекциях, вызываемых биотрофными патогенами, которое стали трактовать как физиологическую стимуляцию в фотосинтезирующих клетках хозяина, выгодную самому паразиту. n. Результаты хорошо увязывались с «гипотезой хемотропизма» (поддерживаемую учеными: нем. В. Пфеффером, яп. М. Майоши и фр. Д. Масси), согласно которой вещества, выделяемые из клеток растения играют роль аттрактантов, направляющей рост гиф грибов по градиенту питательных веществ и вызывающих процесс образования внутриклеточных гаусториев. n


§ Факторами устойчивости против проникновения гаусториев патогена считали прочность клеточной стенки и тургорность вакуолей. § Tatcher (1940) были проведены замеры давления в клетках растений и гаусториев патогенов и показана взаимосвязь степени устойчивости с превышением давления в растительных клетках по сравнению с гаусториями и, наоборот, степени восприимчивости с превышением давления в гаусториях относительно растительных клеток. § Е. Д. Гарбер в 1956 г. предложил «питательно-тормозящую гипотезу фитоиммунитета» , основанную на экологическом подходе. Разновидностью «питательно-тормозящей гипотезы» «стала «гипотеза неполной среды» В. П. Эфроимсона (1961 г. ). § В преломлении К. Т. Сухорукова в питательно-тормозящей гипотезе смыкаются две теории – питательная и фитонцидная.

Согласно Л. В. Метлицкому, в растениях существует две группы физиологически активных веществ, оказывающих влияние на развитие патогенов: 1) присутствуют в растительных тканях еще до контакта с патогеном (фитонциды), 2) вещества, возникающие в клетках растений после контакта с патогеном (фитоалексины). Обе группы в-в включают соединения преимущественно низкомолекулярные, широкого типа действия, но фитоалексины специализированы для вида растения. n Теорию фитоалекисинов как главных факторов иммунитета растений разрабатывал Мюллер (1940 г. ). n Согласно Оффорду, ингибирующее влияние на активность ферментов отмечено у ряда окисленных форм фенолов, флавоноидов, хлорогеновой кислоты: целлюлаза, каталаза, пероксидаза, амилазы, протеиназы дегидрогеназы, липазы, декарбоксилазы, фосфатазы – все ингибируются танином. n


Изучив большой и разнообразный набор устойчивых и неустойчивых форм картофеля и их взаимодействия с фитофторой Müller е. а. (1940 г. ) пришли к заключению, что подавление роста гриба в клубнях устойчивых сортов связано с окислительными превращениями фенолов. Важное значение при этом имеет скорость защитной реакции (быстрая реакция названа «сверхчувствительной» ); у восприимчивых сортов устойчивость, как правило, также проявляется, но с большой задержкой, т. е. здесь характерно заторможенное, медленное наступление защитной реакции растения-хозяина. Переход окраски клеток в коричневый, а затем почти в черный цвет связан с отмиранием пораженной клетки. Считалось, что реакция сверхчувствительности направлена прежде всего и преимущественно против облигатных паразитов, питающихся за счет живых клеток растения-хозяина, но как показали более поздние исследования (Müller, 1959; Tomiyama, 1956, 1969), реакция сверхчувствительности широко распространена в растительном мире и является важным фактором видового и сортового иммунитета растений и к факультативным паразитам, в том числе грибам и бактериям, гибель которых наступает в результате отравления образующимися токсическими соединениями. Реакция защиты растения, независимо от того, направлена она против микроорганизма или против выделяемых ими токсических веществ, представляет собой комплекс биохимических процессов, возникающих в клетках растенияхозяина под воздействием инфекции.

§ Последующие исследования показали разнообразную химическую природу фитоалексинов в растениях. Сюда относятся и фенольные вещества достаточно простого строения, лигнины и лигнаны, сапонины, танины, флавоноиды, терпеноиды, стероиды, алкалоиды и др. классы соединений. § Изучение широкого химического спектра этих веществ и направлений их действия привело к выводу, что они поражают такие клеточные структуры и звенья обмена веществ, которые являются общими у живых существ. § Рассматривая иммунитет растений, обусловленный образованием фитоалексинов, как пример приобретенного иммунитета, Müller предостерегал от начавшейся тенденции сравнивать образование фитоалексинов с антителами у животных по двум причинам: 1) фитоалексины – низкомолекулярные вещества небелковой природы, что резко отличает их от алексинов животного происхождения, 2) в отличие от антител, обнаруживаемых в любой части организма животных, даже самые неспецифические фитоалексины ограничены в своем образовании и накоплении лишь местами поражения и действуют только против вызвавшего их появление патогена. § Здесь следует уточнить. Есть работы, показывающие, что фитоалексины синтезируются не в непосредственно инфицируемой растительной клетке, а в соседних с ней и перемещаются в пораженную, где и вызывают присущие им эффекты. § Роль фитонцидов и фитоалексинов в растениях изучали в СССР Б. Токин, Д. Вердеревский, Л. Метлицкий, М. Горленко, В. Иванюк, О. Озерецковская и др.

Известен набор различных механизмов защиты растений от грибных патогенов: - морфологические барьеры (папиллы, лигнификация клеточных стенок); - локальная гибель инфицированных клеток; - биосинтез фитоалексинов; - синтез ферментов, разрушающих клеточные стенки патогена (хитиназ, глюканаз, пероксидаз и др. PR-белков); - синтез порообразующих в-в (дефензинов), - образование рибосоминактивирующих белков, и другие. В выборе и эффективности защитных механизмов растения от инфекции важное значение имеет способ питания микроорганизма. По типу питания их разделяют на сапротрофов, некро-трофов и био-трофов. Первые извлекают питательные в-ва из мертвых тканей, т. е. являются сапрофитами, вторые и третьи – паразиты.

Однако некротрофы прежде чем оккупировать какой-либо участок растения, убивают его своими токсичными выделениями, т. е. фактически, как и сапротрофы, питаются содержимым мертвых клеток, а биотрофы извлекают питательные в-ва непосредственно из живых клеток хозяина. Различия между ними заключаются в соотношении скоростей гибели зараженной ткани (некроза) и развития паразита в растении. Если некроз опережает распространение паразита, следовательно, тип питания некро-трофный, если же рост гиф паразита опережает некроз, – питание биотрофное. Существуют и переходные формы между некротрофами и биотрофами – называемые гемибиотрофами, которые имеют смешанное питание. Сначала они питаются био-трофно, затем, после гибели зараженной ткани, продолжают развиваться в ней, питаясь некротрофно. Однако у гемибиотрофных и некротрофных патогенов первая фаза внедрения в растение может индуцировать у него тоже сверхчувствительную ответную реакцию, которая полностью или частично останавливает развитие фитопатогена в таких сверчувствительно некротизированных клетках. В этом случае возникает необходи мость отличать сверхчувствительный некроз от некроза, вызы ваемого токсинами, ксенобитиками и другими причинами. Эти отличия рассмотрим чуть позже.

§ Одновременно с физиолого-биохимическим и цитологичес- ким направлением исследований по природе фитоустойчивости к инфекциям развивалось и популяционно-генетическое направление, которое начинают рассматривать обычно с работ американского фитопатолога Стэкмена (Stackman, 1918). Он занимался изучением паразитической специализации у ржавчинных грибов и подразделил их на подвиды (специализированные к питающим растениям формы), а затем и на расы, которые имеют наследственные детерминанты, обнаруживаемые с помощью растенийидентификаторов, а также по результатам скрещивания. § В 1946 г. голландский фитопатолог H. Flor, проводя генетический анализ льна на заболевание ржавчиной, увидел закономерность, которая легла в основу его концепции «ген-на-ген» и, таким образом, заложил фундамент методологии, переводящей фитопатологические исследования с геномного уровня на генный.

► Возникли модели взаимоотношений продуктов «комплементарных» генов хозяина и паразита, изображаемых в виде квадратных сеток (рис. 1 а), и был поставлен вопрос о необходимости изучения генетики партнеров только во взаимодействии – т. е. о межорганизменной генетике (Loegering, 1978). Возникновение межорганизменной генетики как отдельной дисциплины сделало возможным связать биохимические исследования факторов устойчивости растений и вирулентности паразитов с генетическими исследованиями, т. е. перейти к анализу биохимических факторов устойчивости и вирулентности.

H. Flor, 1946 А) Генотипы штаммов паразита Генотипы линий растения-хозяина R 1 r 1 Аvr 1 / R 1 Аvr 1 / r 1 Unsusceptibility (=Resistance) Resistance Susceptibility (=Compatibility) Compatibility avr 1 / R 1 avr 1 Б) Генотипы штаммов паразита avr 1 / R 1 Susceptibility (=Compatibility) Compatibility avr 1 / r 1 Susceptibility (=Compatibility) Compatibility Генотипы линий растения-хозяина R 1 r 1 Аvr 1 / R 1 Аvr 1 / r 1 Susceptibility (=Compatibility) Compatibility Unsusceptibility (=Resistance) Resistance avr 1 / R 1 Unsusceptibility (=Resistance) Resistance avr 1 / r 1 Unsusceptibility (=Resistance) Resistance

n n Из приведенных данных следует, что взаимодействие продуктов доминантных генов устойчивости (резистентности -R) и авирулентности (Avr) приводит к несовместимости (unsusceptibility), в то время как потеря или изменение одним из партнеров (или обоими) доминантного гена изменяет реакцию на совместимую (susceptibility). Наиболее простая биохимическая интерпретация этих данных заключается в предположении, что какие-то структуры растения-хозяина, синтезируемые под контролем доминантных генов устойчивости, узнают структуры или метаболиты паразита, контролируемые комплементарными доминантными аллелями генов вирулентности (генами авирулентности), как чужие и запускают защитные реакции. Отсутствие у хозяина узнающей структуры (рецептора) вследствие изменения или потери гена устойчивости или отсутствие у паразита метаболита, связываемого рецептором, вследствие изменения или потери гена авирулентности приводит к тому, что паразит перестает узнаваться хозяином как чужой, и защитные реакции не включаются (или включаются слишком поздно), и отношения между партнерами становятся совместимыми.

n n n При экспериментах, проводимых на разных объектах, обнаружились факты, не укладывающиеся в исходную концепцию. Во-1 -х, индукцию защитных реакций вызывал не какой-либо один метаболит паразита, а многие метаболиты, локализованные в разных компартментах клеток (стенке, плазматической мембране, периплазме, цитозоле) и относящиеся к разным классам химических соединений (углеводам, белкам, липидам, жирным и нуклеиновым кислотам и т. д. ). Во-2 -х, элиситорные соединения обнаруживали как у вирулентных, так и у авирулентных рас и даже у сапротрофных грибов. В-3 -х, эти элиситоры вызывали защитные реакции как у устойчивых, так и у восприимчивых сортов растений, в том числе у видов и сортов, не имеющих генов устойчивости к данному паразиту. Неспецифичность большинства изолированных элиситоров патогенов привела многих биохимиков, занимающихся изучением механизмов иммунитета растений, к представлениям о том, что индукция паразитом защитных реакций и их протекание в растении неспецифичны. Специфичны же суппрессия (подавление) защитных реакций паразитом и отзывчивость хозяина на суппрессор ( Daly, 1976; Ouchi, 1983, и др. ). В соответствии с этим, вытекающая из теории Флора диаллельная схема взаимодействия хозяина и паразита оказалась «перевернутой» , т. е. с обратным смыслом (рис. 1 б). В некоторых комбинациях растениепатоген подобные схемы получили экспериментальное подтверждение, и специфические суппрессоры были идентифицированы.


n Если растение устойчиво, то ответные реакции в нем носят быстрый, сильный, взрывной характер; токсические вещества в зоне заражения накапливаются быстро и в высоких концентрациях, происходит быстрая гибель зараженных клеток и находящихся в них инфекционных структур паразита – гаусториев. n Остается неясным вопрос: обусловлена ли гибель патогена метаболическим отмиранием пораженной и соседних клеток, или же оба организма отмирают по другой причине – например, образования в тканях растений токсических фитоалексинов. n. Как уже говорилось, отчетливое проявление устойчивости наблюдается только в случае взаимодействия растения и патогена с определенным сочетанием комплементарных генов, а именно – доминантных генов устойчивости растения и доминантных генов авирулентности паразитического гриба. Тогда возникает полная несовместимость в системе растение-патоген и происходит наиболее сильная и быстрая, лавинообразная ответная защитная реакция, которая внешне, на поверхности листа проявляется как мелкие точечные некрозы; она носит название реакции сверхчувствительности. n В любых других случаях сочетания этих генов растение будет восприимчиво. Если растение восприимчиво, ответные реакции на заражение протекают в нем вяло, антибиотические соединения в пораженных тканях образуются медленно и в низких концентрациях, так что паразит успевает сформировать инфекционные гифы и гаустории, накопить достаточное количество питательных веществ для образования новых спор, т. е. пройти полный паразитический цикл.

Микроорганизмы, патогенные для животных и растений, выделяют в зараженные ткани и клетки метаболиты – иммуномодуляторы. Одних из них – индукторы или элиситоры – хозяин использует для распознавания чужого и индукции в организме защитных реакций. Другие иммуномодуляторы – иммуносупрессоры или импедины, – наоборот подавляют защитные реакции и снижают иммунные свойства растения-хозяина. Большинство полисахаридных иммуномодуляторов представляют собой линейные или разветвленные Р-глюканы или маннаны.

Неспецифический элиситор Phytophthora infestans арахидоновая к-та в клетках картофеля включается в состав фосфолипидов, окисляется липооксигеназой до эйкозаноидов, вызывает окислительный взрыв, синтез фенолов и фитоалексинов, индуцирует апоптоз. Сфинголипидные патотоксины фитопатогенных грибов Alternaria alternata f. sp. lycopersici (AAL-токсин) и паразита кукурузы Fusаrium moniliforme (фумонизин) ингибируют церамидсинтетазу, подавляя синтез церамида из 2 -х молекул сфинганина и фосфорилируя ретинобластому – регулятор клеточного цикла (перехода G 1 в S) и апоптоза. Апоптоз клеток томата и арабидопсиса, вызванный фумонизином, требует участия сигнальных путей, идущих с участием салициловой и жасмоновой кислот.

n n В индукции защитных – прежде всего, сверхчувствительных – реакций у растений важное, или даже определяющее, значение имеют молекулы, назывемые элиситорами. Они могут быть продуктами клеток самих патогенов (белковыми, хитиновыми или глюкановыми компонентами их клеточных стенок, экзоферментами, токсинами, белками цитоскелета или иными метаболитами возбудителя) или веществами, образующимися в клетках и тканях растений при взаимодействии с патогеном (также пектиновыми, гемицеллюлозными или иными фрагментами клеточных стенок, либо продуктами расщепления клеточных мембран − веществами типа арахидоновой кислоты, пептидами и т. д. ). В каждой комбинации растение-патоген изучение их (элиситоров) образования, химической природы или роли во взаимоотношениях – интересная задача. Анализ уже полученных данных показывает, что эти элиситоры могут быть как неспецифическими, присущими многим патосистемам, так и высокоспецифическими. Последние обнаружены в вирусных, бактериальных и грибных фитопатосистемах. В частности, установлено, что специфическим элиситором для гена N табака является капсидный белок вируса (ВТМ) со свойствами РНК-полимеразы.

другом случае, определение avr-генов Pseudomons savostanoi (pv. glycinea и pv. tomato) выявило 2 гомологичных белка с уровнем гомологии в 86% (а по рамке считывания – в 98 %). В структуре этого продукта гена авирулентности отсутствуют участки, необходимые для трансмембранного переноса из цитоплазмы в окружающую среду (лидерный пептид и гидрофобный домен), т. е. это был внутриклеточный белок бактерий. Поскольку фрагмент, кодируемый avr. D, представляет собой первую из пяти рамок считывания, то предположили, что весь белок является ферментом, важным для вторичного метаболизма. Элиситорную активность этого avr. D удалось установить только после включения кодирующего гена в геном кишечной палочки, в результате чего последняя стала выделять в ростовую среду метаболит, вызывающий сверхчувствительность у сортов сои с геном Rpg 4. n Элиситором оказался низкомолекулярный С-гликозилированный липид сиринголид, а весь белок – ферментом, катализирующим синтез сиринголидов – индукторов споруляции и образования антибиотиков бактериями. n. В

Грибные циклические пептиды являются мощными иммуносупрессорами, как растений, так и животных. Циклический пептид HV-токсин (викторин) подавляет иммунный ответ клеток восприимчивых растений. Его рецептор – глинциндекарбоксилаза – центральный фермент катаболизма азота у растений и животных. Продукт гена авирулентности бактерии Xanthomonas vesicatoria (avr. Rxv), поражающей томаты и перцы, гомологичен фактору вирулентности вызывающей кишечные инфекции бактерии Yersinia pseudotuberculosum (yaupj). Компоненты наружной мембраны грам-отрицательных бактерий – липополисахариды (LPS) играют важную роль в прикреплении патогенов к их хозяевам. Другой компонент поверхности бактериальных клеток – пили IV типа обнаружены у патогенов растений и животных Pseudomonas syringae pv. tomato и P. aeruginosa. Они нужны для адгезии к клетками растений и животных. Еще один компонент – белок жгутиков бактерий флагеллин также необходим для адгезии на поверхности. Устойчивые растения и животные узнают флагеллин как элиситор. Транспорт этих, как и др. белков через бактериальные мембраны осуществляют специальные белки (продукты hrp-генов) секреторной системы III типа, гомологичные у фитопатогенных бактерий и паразитов человека из родов Shigella, Salmonella, Yersinia и др. (грам-отрицательных).

Бактериальные пептиды флагеллины являются лигандами, связывающимися иммунными молекулами растений (R-белок FLS 2 -киназа с LRR-рецепторным мотивом) и животных (Тоll-подобным рецептором также имеющем LRR-мотив – TLR 5). Супрессоры иммунных ответов восприимчивых растений циклические тетрапептиды НС- и АМ-токсины являются гомологами ингибитора гистонов в клетках животных – трапоксина. Циклоспорин, продуцируемый многими грибами, является иммуносупрессором позвоночных животных и человека и используется в фармакологии, как супрессор иммунных реакций отторжения чужеродных пересаженных органов.

Для распространения в растении паразиту необходимо: 1) подавить защитные свойства не отдельной клетки, а ткани; 2) изменить метаболизм раст-я в нужную паразиту сторону. Рассматривая суппрессоры защитных реакций растения мы имеем ввиду обычно и прежде всего вещества биотрофов. Но существует еще некротрофные фитопатогены, убивающие живые клетки растения-хозяина прежде чем используют их для паразитизма. Какие же ‘инструменты’ они применяют для достижения этих целей? Гидролитические ферменты, разрушающие клеточную стенку, не годятся, так как, будучи высокомолекулярными соединениями, они не способны мигрировать по растению. Эти ферменты – оружие ближнего боя. Веществами, мигрирующими от места инфекции по растению и выполняющими роль суппрессоров механизмов защиты и создающих тем самым плацдармы для дальнейшей оккупации растения паразитом, являются токсины. Среди них выделяют 1) хозяин-неспецифические вивотоксины и 2) хозяин-специфические патотоксины.

Вивотоксины вызывают повреждения не только хозяина данного паразита, но и видов растений, находящихся за пределами его пищевой специализации. Поэтому вивотоксины относят к факторам неспецифической (горизонтальной) патосистемы. По химической природе вивотоксины разделяют на несколько групп: а) органические кислоты, например, щавелевая к-та возбудителя белой гнили Sclerotinia sclerotiorum; б) полисахариды (токсин бактерий Xanthomonas campestris); в) полипептиды, например, цератоульмин – 13 к. Да токсин возбудителя голландской болезни ильмов Ophiostoma ulmi; г) гликопептиды, такие как токсины Clavibacter michiganense (возбудитель бактериального рака томатов) и Phoma tracheophylla (возбудитель мальсекко цитрусовых); д) циклические пептиды, состоящие из нескольких аминокислот, замкнутых в кольцо – фазеолотоксин (продуцент Pseudomonas savastanoi pv. phaseolicola), тентоксин A. tenuis (syn. A. altemata) и др. ; е) циклические ароматические соединения (кумарины, азотсодержащие алкалоиды и др. ). Таковы альтернариевая к-та (продуцент – Alternaria solani), фузариевая к-та (Fusarium oxysporum) и др. ; По механизму действия выделяют несколько групп токсинов: ингибиторы синтеза белка, ингибиторы ферментов растений, генераторы активных форм кислорода, мембранноактивные вещества и др. Роль токсинов в фитопатогенезе разнообразна и до конца не расшифрована. Для многих паразитов установлены выделение токсинов в зараженное растение и их миграция по растению, опережающая рост самих возбудителей. Это характерно гл. образом для более мелких молекул патотоксинов, и менее для более крупных молекул вивотоксинов.
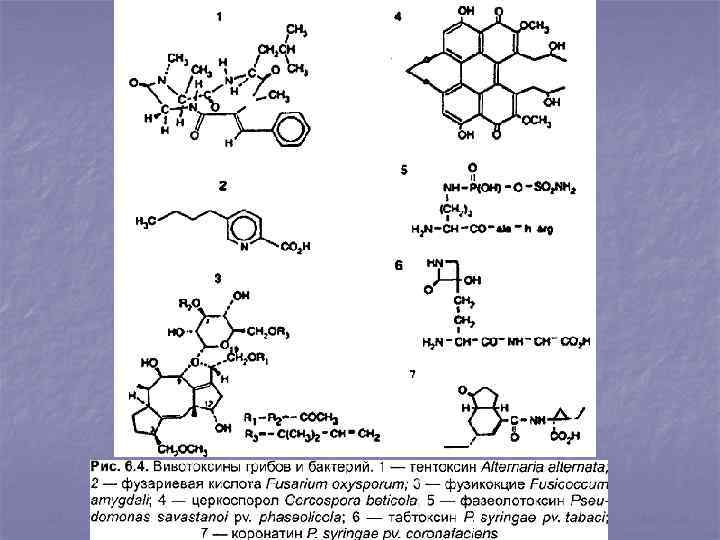

В отличие от неспецифических вивотоксинов, патотоксины повреждают только определенные виды или даже сорта растений. Некоторые из них являются первичными факторами патогенности (без токсина организм не способен быть паразитом) и получили название «токсины специфичные для хозяев» . Низкая летальная доза и высокая селективность указывают на рецепторный механизм специфичности (устойчивые растения не имеют сайта связывания токсина). Первые симптомы, наблюдаемые уже через несколько минут после обработки клеток чувствительных растений токсинами, выражаются в утечке метаболитов и электролитов, деполяризации мембранного потенциала, инвагинации мембран. Поэтому считают, что рецепторы патотоксинов расположены на мембранах. АК-, HS-, AF-, АСТ-токсины связываются с цитоплазматической мембраной, Т-, РМ-, ACR-токсины – с мембраной митохондрий, АМ-токсин – с плазмалеммой и мембраной хлоропластов. По химич. составу патотоксины объединяют в несколько групп: циклические пептиды, линейные поликетолы, гликозиды и др.


Паразиты растений имеют различные типы специализации. Филогенетическая специализация — это специализация по таксонам растений-хозяев. На этом основании выделяют монофагов, поражающих растения в пределах одного рода (или нескольких близких родов), олигофагов, специализированных в пределах семейства растений-хозяев, и полифагов, поражающих растения из многих семейств, порядков и даже классов. Био трофы концентрируются среди моно-фагов, некро трофы– среди олиго- и поли-фагов. Онтогенетическая специализация проявляется в приуроченности паразита к отдельным этапам развития растения-хозяина. Изучению онтогенетической специа-лизации паразитов большое значение придавал известн. фитопатолог М. С. Дунин. Тканевая (гистотропная) и органотропная специализации. Некоторые паразиты развиваются только в определенных органах и тканях растений. Так, одни вирусы поражают флоэму, другие – паренхиму. Грибы и бактерии, вызывающие инфекционное увядание (вилт), находятся в ксилеме растений и нарушают транспорт воды из корней в надземные части Многие грибы и бактерии, вызывающие образование пятен, поражают только или главным образом листья; мицелий распространяется внутри листа на небольшое расстояние, после чего развивается спороношение. Головневые грибы заражают формирующиеся семена или молодые всходы злаков и развиваются внутри растения системно.

Патогенность – осн. свойство фитопатогенных организмов. Качественная сторона патогенности – вирулентность, – способность данного штамма паразита развиваться за счет образца растения-хозяна. По вирулентности виды фитопатогенных организмов дифференцируют на специализированные формы и расы. Агрессивность – количественный компонент патогенности: способность вызвать эпифитотию. Одновременно с физиолого-биохимическим и цитологическим вектором исследований по природе фитоустойчивости к инфекциям развивалось и популяционно-генетическое направление, к-рое начинают рассматривать обычно с работ американского фитопатолога E. Stakman (1918), занимавшегося изучением паразитической специализации у ржавчинных грибов. Он подразделил их на подвиды (специализированные к питающим растениям формы), а затем и на расы, имеющие наследственные детерминанты, обнаруживаемые с помощью растений – сортов-идентификаторов, а также по результатам скрещивания.

В 1946 г. голландский фитопатолог H. Flor, проводя генетический анализ льна на заболевание ржавчиной, увидел закономерность, которая легла в основу его концепции «ген-на-ген» и, таким образом, заложил фундамент методологии, переводящей фитопатологические исследования с геномного уровня на генный. Возникли модели взаимоотношений продуктов «комплементарных» генов хозяина и паразита, изображаемых в виде квадратных сеток, и встал вопрос о необходимости изучения генетики партнеров только во взаимодействии – т. е. о межорганизменной генетике (Loegering, 1978).

Возникновение межорганизменной генетики как отдельной дисциплины дало возможность связать биохимические исследования факторов устойчивости растений и вирулентности паразитов с генетическими исследованиями, т. е. перейти к анализу биохимич. факторов устойчивости и вирулентности Из генетических данных следует, что взаимодействие продуктов доминантных генов устойчивости (R) и авирулентности (Avr) приводит к несовместимости (unsusceptibility), в то время как потеря или изменение одним из партнеров (или обоими) доминантного гена изменяет реакцию на совместимую (susceptibility). Наиболее простая биохимическая интерпретация этих данных заключается в предположении, что какие-то структуры растенияхозяина, синтезируемые под контролем доминантных генов устойчивости (индукторы, или элиситоры), узнают структуры или метаболиты паразита, контролируемые комплементарными доминантными аллелями генов вирулентности (генами авирулентности), как чужие и запускают р-и защиты. Отсутствие у хозяина узнающей структуры (рецептора) вследствие изменения или потери гена устойчивости или отсутствие у паразита метаболита, связываемого рецептором, вследствие изменения или потери гена авирулен тности приводит к тому, что паразит перестает узнаваться хозяином как чужой, и защитные реакции не включаются (или включаются поздно), и отношения между партнерами становятся совместимыми.

Четкое проявление устойчивости наблюдается только в случае взаимодействия растения и патогена с определенным сочетанием комплементарных генов, а именно – доминантных генов устойчивости растения и генов авирулентности паразитического гриба. Тогда возникает полная несовместимость в системе растение-патоген и происходит наиболее сильная и быстрая, лавинообразная ответная защитная реакция, которая внешне, на поверхности листа проявляется как мелкие точечные некрозы; она носит название реакции сверхчувствительности. В любых других случаях сочетания этих генов растение будет восприимчиво. Если растение восприимчиво, ответные реакции на заражение протекают в нем вяло, антибиотические соед-я в пораженных тканях образуются медленно и в низких конц-ях, так что гриб успевает развивать инфекционные гифы и гаустории, накопить достаточное количество питательных в-в для образования новых спор, т. е. пройти полный паразитический цикл. Это, в частности, иллюстрируют следующие схемы.
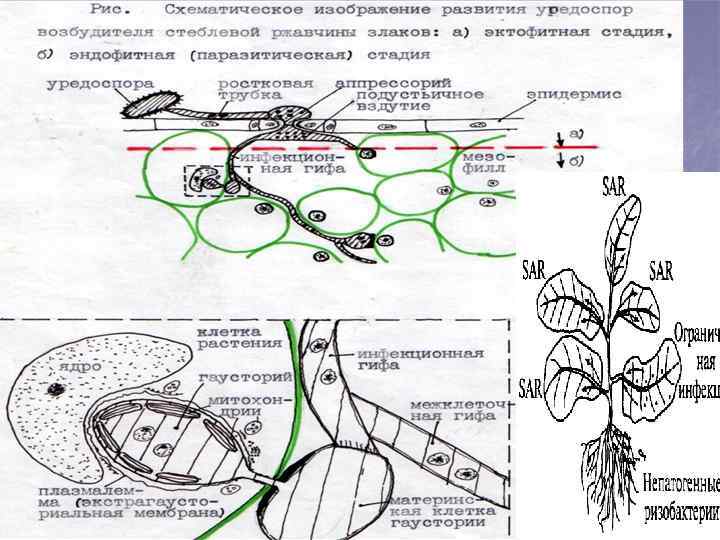


n n Т. о. , было получено доказательство опосредованного участия генов авирулентности во взаимодействии паразита и хозяина (т. е. фермент-опосредованном изготовлении внеклеточных элиситоров фитопатогенных бактерий) и освобождении этого элиситора только in planta – под влиянием метаболитов растения. Примером элиситора сверхчувствительной реакции томатов к фитопатогенному грибу Cladosporium fulvum может быть продукт гена Avr 9. Как обнаружили голландские ученые (P. de Wit e. a. ), ген avr 9 экспрессируется in vitro и in planta только при низкой концентрации N в среде. Значительная экспрессия этого гена авирулентности наблюдается у гриба после внедрения в межклеточное пространство листа томатов, причем около сосудов бóльшая, чем в мезофилле. Структура элиситора сходна с регуляторным белком метаболизма азота у грибов Aspergillus nidulans и Neurospora crassa. Все это указывает на то, что, по-видимому, ген avr 9 участвует в поступлении азота в мицелий фитопатогена C. fulvum из растения.

§ Аналогичный ген Xanthomonas oryzae avr 10, комплемен- тарный гену устойчивости риса Xa 10, кодирует белок на 80% гомологичный белку pho S E. coli − периплазматичес-кому белку, связывающему фосфаты. Продукт avr 10 имеет лидерный пептид, который экскретируется через клеточную мембрану и может быть непосредственным элиситором сверхчувствительной реакции у риса. § Клонирование генов авирулентности фитопатогенных грибов подтвердило предположение о «плюс» -функциях генов авирулентности и наличии специфических элиситоров, оперирующих в системе ген-на-ген. § Данные показывают, что появление в ходе совместной эволюции паразита и растения комплементарных наследственных систем, где доминантный ген авирулентности определяет характер взаимоотношений возбудителя заболеваний с растением-хозяином (его системой устойчивости) есть не нонсенс, а функционально оправданная ситуация. Делеция или мутация гена авирулентности фенотипически проявляется как вирулентность – одна из жизненно важных потребностей паразита, обеспечивающих его выживание.

§ Исследование другого компонента фитопатосистемы – растения – привело ученых к предположению, что комплементарные генам авирулентности патогенов гены устойчивости растений несут по крайней мере две функции: 1) рецепторов, узнающих (воспринимающих) элиситоры патогенов, и 2) медиаторов, передающих сигналы с поверхности клетки на геном ядра.


Молекулярное изучение структуры и функций генов устойчивости растений, – или R-генов, – оказалось более трудной задачей, чем исследование генов avr – авирулентности патогенов. n Это во многом определяется тем, что у растений обнаруживается много хромосом, и лишь концентрация усилий ученых всего мира на таких модельных объектах как Arabidopsis thaliana – растении-резушке, имеющей только 3 хромосомы в гаплоидном наборе (1. 108 пар оснований, ~100 генов устойчивости) продвинуло вперед эти исследования. n Впоследствии были получены данные о молекулярном строении генов устойчивости и на других растениях: Linum (7. 108 пар оснований), Triticum (1, 7. 1010 пар оснований) и других. n Для изоляции генов устойчивости были применены следующие методы и их сочетания: 1) мечение генов устойчивости перекрывающимися сегментами разрезанной рестриктазами ДНК (RLFP-локусами) в расщепляющемся потомстве F 2; 2) маркирование локусов устойчивости транспозонным мутагенезом; 3) использование радиоактивно меченого специфического элиситора как маркера для выделения рецептора и реконструкции кодирующего гена по структуре его продукта. Первыми были исследованы гены устойчивости N (Nicotiana sylvestris/ВТМ), L 6, M (Linum sativum/Melampsora lini), RPPS (Arabidopsis thaliana/Peronospora parasitica), Cf 2, Cf 4, Cf 5, Cf 9 (Lycopersicum tomatum/Cladosporium fulvum), Xa 21 (Oryza sativa/Xanthomonas oryzae pv. оryzae), Pto (Lycopersicum tomatum/Pseudomonas savastanoi pv. tomato), RPM 1 (Arabidopsis thaliana/Pseudomonas savastanoi pv. maculicola), Mi 1 (Lycopersicum tomatum/Melodoidyginea sp. ) и др. n


Продукты исследованных R генов (R белки) имеют в своем составе несколько характерных структур. 1. Крупный С концевой участок. Содержит большое число повторяющихся последовательностей с высоким содержанием аминокислоты лейцина ( Leucine rich repeats – LRR). Каждый повтор состоит из 23 -24 аминокислот. Эта структура встречается во многих белках эукариот, осуществляет межбелковые взаимодействия, т. е. служат рецептором, связыва-ющимся с лигандом – белковым или гликопротеиновым элиситором патогена. LRR-домен имеет большие возможности для генетических реорганизаций, рекомбинаций, что приводит к изменению рецепторных свойств молекулы. Экспериментально показано, что многие мутации, меняющие реакцию на заражение авирулентными расами патогенов, картированы в этой части генной структуры. 2. Участок, связывания с нуклеотидами (Nucleotide binding sites – NBS), состоит из трех под-участков: n - киназы 1 а – петли, связывающей фосфат (P loop), n - киназы 2 а, связывющей ион металла, необходимого для реакции переноса фосфата, n - киназы 3 а, аргинин которой обеспечивает взаимодействие с пуриновыми основаниями АТФ. n NBS – сигнальная область, связывающаяся с АТФ и ГТФ, вследствие чего она может активировать киназы и сигнальные G белки. Отметим, что NBS-область R-белков растений гомологична генам Ced 4 червя Caenohabolitis elegans и Apaf 1 человека, являющихся регуляторами активности протеиназы – каспазы, которая является важным фактором программированной клеточной смерти (апоптоза). n По современным представлениям реакция сверхчувствительного некроза растений при взаимодействии с авирулентной расой патогена аналогична реакции апоптоза у животных. n

3. Участок лейциновой «застежки» (Leuzine zipper region – LZR). Этот участок способствует формированию спирализованных структур, обеспечивающих димеризацию белковых молекул или их специфическое взаимодействие с другими белками. Известно, что R-белки, находящиеся в незараженной клетке в виде мономеров, призаражении с участием своих LZдоменов могут формировать гомодимеры или олигодимеры, взаимодействующие с элиситором, что может проявляться в виде «окаймленных» ямок на плазмалемме, либо, наоборот, при заражении происходит диссоциация ранее имевшихся олигомеров. Возможны также гетероди- (и поли-) меризация R-белка с другими белками. 4. Участок гомологии с цитоплазматическим доменом Toll белка дрозофилы и рецепторои интерлейкина (IL 1) млекопитающих и человека, названный TIR (Toll–Interleukin 1 Resistance). n Известно, что рецепторный белок Toll контролирует дорзо-вентральную поляризацию эмбрионов дрозофилы, а также играет роль в ядерной локализации фактора Dif (Dorsal related immunity factor), который активирует защитные свойства жирового тела. В частности, белок Toll регулирует синтез антигрибного пептида дрозофилы – дрозомицина. n Интерлейкин 1 – один из важнейших цитокинов (т. е. межклеточных передатчиков иммунной системы высших животных и человека), активирующих иммунокомпетентные клетки, благодаря взаимодействию с находящимися на поверхности этих клеток рецепторами. Связывание обоих рецепторных белков сопровождается активацией серин/треониновых киназ. Возможно, что и TIRучастки растительных R-белков несут сходные функции. 5. Участок серин/треониновых фосфокиназ (Protein kinase – PK)обнаружен у некоторых R-белков. Он обладает отчетливыми сигнальными свойствами и является фактором активации транскрипции. PK-участок R-белков, как правило, находится на цитоплазматической стороне плазмалеммы и может быть связан или не с участками R-белков, расположенными в или под поверхностью плазматической мембраны. У многих R-белков PK-участок отсутствует.

n n n R-белки 1 группы имеют внеклеточный LRR-гликопротеиновый домен, заякоренный в плазматической мембране С-концом. Как вытекает из сказанного, N-концевой участок молекулы R -белков – их свободный LRR-конец, может быть непосредственным сайтом связывания элиситоров, но он не способен выполнять (по крайней мере, полностью) функцию передачи сигнала с поверхности на внутрицитоплазматические домен и далее на ядро. Возможно, LRR-участки ассоциируются с мембранными протеинкиназами вне молекулярной структуры R-белков: в частности, их короткий С-концевой домен на внутренней стороне плазмалеммы может при каких-то условиях взаимодействовать с киназами. R-белки 2 группы, такие как продукт гена Pto, напротив, являются внутриклеточными серин/треониновыми киназами, но они не способны к выполнению рецепторной роли, т. к. у них отсутствует экстраплазматический участок. Таким образом, двудоменная структура R-белков томатов (Cf и Pto) – экстра- и интра-цитоплазматическая, соответственно, т. е. она как бы разделена между факторами устойчивости к двум разным паразитам. Тем не менее, в устойчивой фитопатосистеме Avr. Pto/RPto их продукты после автофосфорилирования Pto-белка могут взаимодействовать.

n n Каким образом происходит доставка элиситора Avr. Pto в цитоплазму растительной клетки долгое время было неясно, пока не был открыт так называемый III тип секреции у бактериальных патогенов. Именно благодаря ему обеспечивается «впрыскивание» через узкий канал в стенке и плазмалемме белка Avr в цитоплазму растительной клетки. Интересно также, что ген Pto сцеплен с геном Prf, который, по-видимому, необходим Pto. Продукт Prf-гена имеет участок LRR, NBS, LZ, а также длинную область с двумя прямыми повторами, негомологичную известным белкам, но все они находятся под поверхностью плазмалеммы. Возможно, что действие белков Pto и Prf в клетке скоординировано. Комбинация генов Pto и Prf, предположительно необходимая для работы R-гена, позволила de Wit’у предложить двухкомпонентную систему защиты растений из взаимодействующих Avr/Rгенов посредством гена активатора.



n n n R-белки 3 группы – например, белок риса Ха 21 – единственный из изученных R-белков, который полностью соответствует требуемым функциональным (рецепторным и сигнальным) параметрам. В нем наружу выдвинута рецепторная LRR-часть, а внутри клетки находится участок, имеющий структуру серин/треониновой протеин-киназы, – т. е. способный к внутриклеточной трансдукции сигнала. R-белки из 4 и 5 групп имеют рецепторные области и области трансдукции сигнала, но внутриклеточная (полностью) локализация этих белков не соответствует представлениям о над- или внутри- и под-мембранной локализации рецепторных и иных участков. Особенностью R-генов злаков и других однодольных является то, что у них TIR-домен практически не обнаруживается, а если и выявляется, то вне связи со структурой LRR–NBS. В некоторых случаях TIR-домен у однодольных замещается многоузелковым участком (CC – Coiled coile).

n n n Поскольку, кроме уже упоминавшегося гена устойчивости риса к Xanthomonas oryzae Xa 21, имеющего экстраплазматический участок, все другие R-белки однодольных таких участков не имеют, то есть основания думать, что процесс распознавания Avr-белков патогена происходит у них внутри протоплазмы. Пути доставки Avr-белка через плазматическую мембрану клетки хозяина пока не известны. Возможно, здесь участвуют III тип секреции бактериальных патогенов и некий аналог этого пути грибных патогенов. Что касается последних, то предполагают, что это происходит в период формирования гаусториев, которые вступают в прямой контакт с плазматической мембраной клетки растенияхозяина, но детали всего механизма пока не ясны. Однако существуют экспериментально обоснованные указания на участие процессов экзо- и эндоцитоза в акте распознавания грибного патогенна протоплазмой растительной клетки.





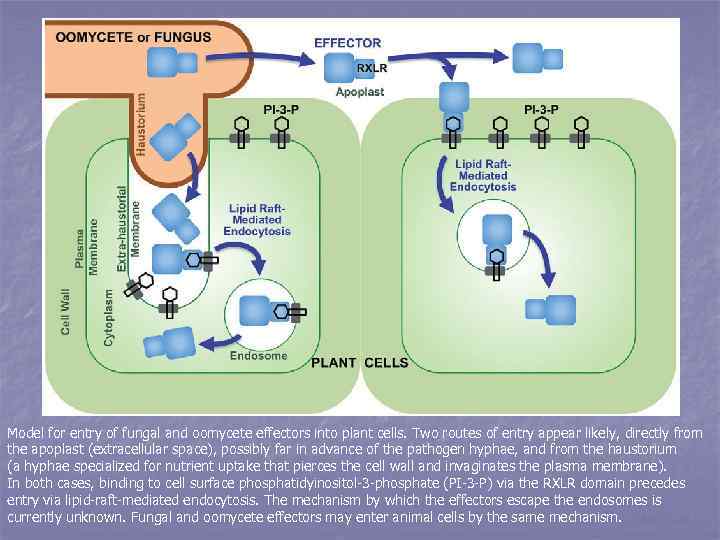
Model for entry of fungal and oomycete effectors into plant cells. Two routes of entry appear likely, directly from the apoplast (extracellular space), possibly far in advance of the pathogen hyphae, and from the haustorium (a hyphae specialized for nutrient uptake that pierces the cell wall and invaginates the plasma membrane). In both cases, binding to cell surface phosphatidyinositol-3 -phosphate (PI-3 -P) via the RXLR domain precedes entry via lipid-raft-mediated endocytosis. The mechanism by which the effectors escape the endosomes is currently unknown. Fungal and oomycete effectors may enter animal cells by the same mechanism.


n Этот процесс представляется следующим образом. Взаимодействие элиситоров (напр. , Avr-белков патогена) с Rрецепторами на плазмалемме растения вызывает связывание – «кэппизация» и втягивание этих рецепторов в ямках на плазматической мембране вглубь цитоплазмы, где они, замыкаясь в везикулы, сливаются с другими налипающими пузырьками, содержащими мономерные и полимерные углеводы, фенольные соединения различной степени сложности и структуры, гидролитические и окислительные ферменты и другие вещества, и одновременно – активация связывающих Avr-белки рецепторов плазмалеммы, сопровождаемая выделением K+ и H+ (и подкислением экстраплазматического пространства), входом кальция в цитоплазму, где ионы Ca 2+ активируют расположенные на цитоплазматической стороне плазмалеммы протеинкиназы в результате сложного ступенчатого каскада фосфорилирования белков и, если этому процессу не мешают развиваться, он приводит к передаче сигнала с поверхности плазматической мембраны на ядро, активации определенных участков хроматина и включению программы сверхчувствительного некроза инфицируемой клетки – программы ее быстрого самоуничтожения.

n n n Однако в акте распознавания на цитоплазматической стороне плазмалеммы кроме рецепторов, непосредственно взаимодействующих с элиситорами, принимают участие и некоторые соседние белки–такие как EDS 1/EDR 1 (EDS 1 обладает каталитической активностью липазы); RAR 1/NDR 1 (RAR 1 играет роль якоря для групп гликозилфосфатидилинозитола (GPI) и требуется, в частности, для запуска Mla 1– гена устойчивости злаков к мучнистой росе и NDR 1 – гена нерасоспецифической болезнеустойчивости; SGT 1/SKP 1 (SGT 1 – суппрессор G 2 -аллеля SKP 1, явдяющегося связанным белком S-фазы киназы); PAD 4/Hsp (PAD – фитоалексин-дефицитный белок с липазной активностью, Hsp – белок теплового шока, шаперон, или белок -компаньон). Эти и некоторые другие белки вносят свой вклад непосредственно в рецепцию элиситора патогена, а также в передачу сигнала с плазмалеммы на ядро, могут снижать силу стимула, сдерживать скорость передачи сигнала по цепи фосфокиназ и таким образом регулировать ответную реакцию клетки растения от типичной сверхчувствительной устойчивости (resistance, immunity) до разных степеней и типов восприимчивости (susceptibility). Таким образом, элиситор патогена при связывании с рецептором растения запускает в клетках последнего сторожевой механизм, или «будильник» (guard) для активации программы устойчивости. Если для вирусов, белки которых синтезируются внутри клеток хозяина, внутриклеточная локализация продуктов R-генов еще понятна, то бактериальные клетки переносят свои Avr-белки под стенку и плазмалемму, где узнаются соответствующими R-белками, с помощью механизма харпинов или III типа секреции.


n У фитопатогенных грибов (таких как Cladosporium fulvum, Phytophthora infestans, Tiletia caries, Uromyces fabae) подобного механизма не обнаружено. Полагают, что у томата имеется неспецифический рецептор, связывающий внеклеточные белки патогенна без индукции сверхчувствительного некроза. Активация клеточного сигнала происходит, вероятно, после взаимодействия элиситора с гетеродимером, состоящим из R-белка и неспецифического рецептора или, что более вероятно, из R -белка и протеинкиназы (т. к. с плазматической мембраной связано несколько типов киназ).

Относительно других возможных функций R генов растений. Гомологичные R-белки описаны у растений разных порядков; они придают последним специфическую устойчивость к вирусам, бактериям, грибам, нематодам, тлям и т. п. Это говорит о том, что, ● во-1 -х, они возникли давно, до расхождения растений по современным таксонам, и, ● во-2 -х, они первично выполняли не защитные, а некие иные внутриклеточные функции. Поскольку основной формой проявления активности R-генов является программируемая клеточная гибель, которая часто встречается в развивающихся растениях и животных, то можно предполагать, что характерные для R-генов эффекты могли также происходить и играть ключевую роль в разных аспектах нормального онтогенеза растений, в частности, при возникновении внутри массы малодифференцированных паренхимных клеток клеточных групп со специализацией на передаточно-транспортной, механической и защитной функциях.

■Молекулярно-генетическими исследованиями последних лет обнаружены взаимосвязи R-генов устойчивости к мучнистой росе с генами CLAVATA, контролирующими меристематическую активность и процессы развития в тканях растений. Следует обратить внимание на ряд аспектов взаимосвязи генов фитоустойчивости и развития. ■Гены устойчивости томатов к Cladosporium fulvum активируются при снижении концентрации аминного азота в межклеточной среде, гены восприимчивости растений к микоризным грибам – при понижении фосфат -ионов в окружающей среде, гены сверхчувствительного некроза и апоптоза (программируемой клеточной гибели) – при появлении в межклеточной среде перекиси водорода и недостаточном поступлении питательных веществ и часто сопровождаются так называемым окислительным и лизосомальным взрывом в самой растительной клетке. ■В подобных случаях погибающая в результате апоптоза клетка животных используется для питания соседними клетками, в к-рых активируются процессы фагоцитоза, само-переваривания и реутилизации веществ. ■В растениях же погибающая клетка опустошается внутри и лигнифицируется снаружи – превращаясь в прототип сосуда, облегчающего передаточную функцию между другими живыми клетками. ■В клетках, соседних с гибнущей, активируется вторичный метаболизм, вырабатываются вещества, имеющие защитную и сигнальную функцию, индуцируется меристематическая активность и может развиваться краевая перидерма вокруг очага окислительных и гидролитических процессов. ■ Т. о. , возникают предпосылки для цитодифференцировки, гисто и органогенеза.

Уст. , что белок Pto томата гомологичен цитоплазматическому домену SRK – продукта гена гаметофитной несовместимости капусты. Внеклеточный LRR-участок белка Ха 21 риса подобен продуктам генов erecta и clavata растения Arabidopsis, которые определяют формы и размеры цветков и участвуют в гистодифференцировке растительных клеток, в частности, ее трахеид и сосудов (трахей) ксилемы. При их образовании наблюдают все признаки апоптоза, чрезвычайно сходного со сверхчувствительным некрозом. В обоих случаях наблюдается взрыв окислительной и лизосомальной активности в клетке, и клеточные стенки лигнифицируются либо в области папилл, либо по всей поверхности, и тогда клетки могут превращаться в сосуды.



n n n Показано, что белок Pto томата гомологичен цитоплазматическому домену SRK – продукта гена гаметофитной несовместимости капусты. Внеклеточный LRR-участок белка Ха 21 риса подобен продуктам генов erecta и clavata растения Arabidopsis, которые определяют формы и размеры цветков и участвуют в гистодифференцировке растительных клеток, в частности, ее трахеид и сосудов (трахей) ксилемы. При их образовании наблюдаются все признаки апоптоза, чрезвычайно сходного со сверхчувствительным некрозом. В обоих случаях наблюдается взрыв окислительной и лизосомальной активности в клетке, и клеточные стенки лигнифицируются либо в области папилл, либо по всей поверхности, и тогда клетки могут превращаться в сосуды. Сверхчувствительный некроз растений в ответ на инфекцию был описан американским фитопатологом Стэкменом при заражении пшеницы несовместимой расой возбудителя стеблевой ржавчины в начале 20 в. Впоследствии реакцию сверхчувствительности стали рассматривать как основное и наиболее типичное проявление высокой устойчивости растений к вирусной, бактериальной, грибной или нематодной инфекции, т. е. как наиболее характерный стандарт иммунности сорта. В восприимчивых сортах подобные изменения, если и наступают, то в конце инфекционного периода, т. е. с гораздо меньшей скоростью. Кроме того, имеются некротрофные патогены, у которых первая фаза внедрения в растение может индуцировать у него также сверхчувствительную ответную реакцию, которая полностью или частично останавливает развитие фитопатогена в сверчувствительно некротизированных клетках.

n. Как отличать сверхчувствительный некроз (апоптозе) от некроза, вызываемого токсинами, ксенобиотиками и другими причинами. n. При апоптозе (сверхчувствительном некрозе) клетка уменьшается, ее ядро сжимается тоже, плазмалемма сохраняет целостность долго, но протоплазма может «съеживаться» , висеть на стенке на нитях Гехта или фрагментироваться, ядра в этих клетках темнеют (пикноз), в них происходит конденсация хроматина и разрыв на нуклеосомные фрагменты, дающие на электрофореграммах «лесенку» , повышается активность Са 2+-зависимой эндонуклеазы, в митохондриях в наружной мембране падает мембранный электрический потенциал и появляются гигантские поры, ч-з которые выходят протеиназы (прокаспазы), хлоропласты продуцируют активные формы кислорода с одним электроном (О-), содержимое протоплазмы темнеет и распадается по апоптозным фрагментам и везикулам, плазмодесмы разрываются, клеточная стенка лигнифицируется, кремнефицируется, вокруг очага поражения иногда образуется перидерма (вследствие приобретения здоровыми клетками меристематической активности). n. При некрозе объем клетки увеличивается, клеточная стенка разрыхляется, увеличивается проницаемость плазматической и внутриклеточных мембран, в них появляются поры, разрывы, цитоплазма вакуолизируется, вскоре повреждается и тонопласт (практически одновременно с плазмалеммой), органеллы набухают и распадаются, ядро увеличивается и лизирует, в конце концов, останки деградирующей цитоплазмы могут выходить в межклеточное пространство. n. Главное же то, что при некрозе не происходит активация генетической программы самоуничтожения клетки, которая запускается при сверхчувствительном некрозе (апоптозе).
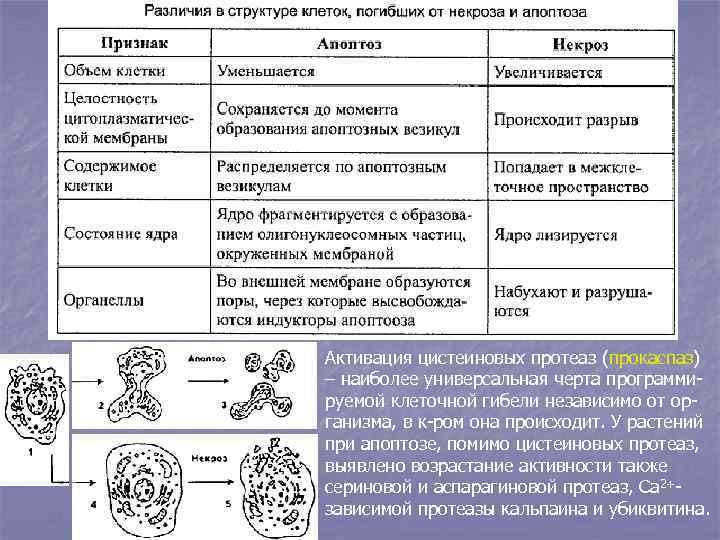
Активация цистеиновых протеаз (прокаспаз) – наиболее универсальная черта программируемой клеточной гибели независимо от организма, в к-ром она происходит. У растений при апоптозе, помимо цистеиновых протеаз, выявлено возрастание активности также сериновой и аспарагиновой протеаз, Са 2+зависимой протеазы кальпаина и убиквитина.

n Устойчивость растений к патогенам выработалась в ходе длительной совместной эволюции, что закрепилось в геномах этих организмов. Согласно M. Heath, первой линией обороны растения является видоспецифическая нехозяинная устойчивость, позволяющая разделять патогены на настоящие и непатогены (потенциальные патогены. По-видимому, эта устойчивость является смесью пассивных и активных защитных реакций и полигенна (ее еще называют горизонтальной). Эта нехозяиная (видоспецифическая) устойчивость растений эволюционно более древняя, чем расо-сорто-специфическая, и т. о. при взаимодействии патогена с растением она проявляется раньше, чем расо-сорто-специфическая (моногенная, верикальная) устойчивость, проявляющаяся позже. n Иными словами, к расо сорто специфическому взаимодействию предполагающему взаимодействие ген на ген), патоген и растение смогут перейти только после преодоления патогеном первой нехозяинной (или видоспецифическй, базисной) устойчивости. n По современным представлениям эта базисная (видоспецифическая или нехозяинная) устойчивость есть не что иное, как врожденный иммунитет (innate immunity). Он вызывается неспецифическими элиситорами патогенов, воспринимаемыми клетками растений как чужеродные молекулы − PAMPs (Pathogen-associated molecular patterns). Аналогичное восприятие чужеродности имеется и у животных, которые воспринимают как несвои такие молекулы как белок жгутиков флагелин, липополисахариды (грам-негативных бактерий), пептидо-гликаны (грам-позитивных бактерий), гликопротеины, белки, глюканы, маннаны, хитозан и хитин (грибных организмов), метилированные ДНК-фрагменты (бактерий и вирусов) и т. д.
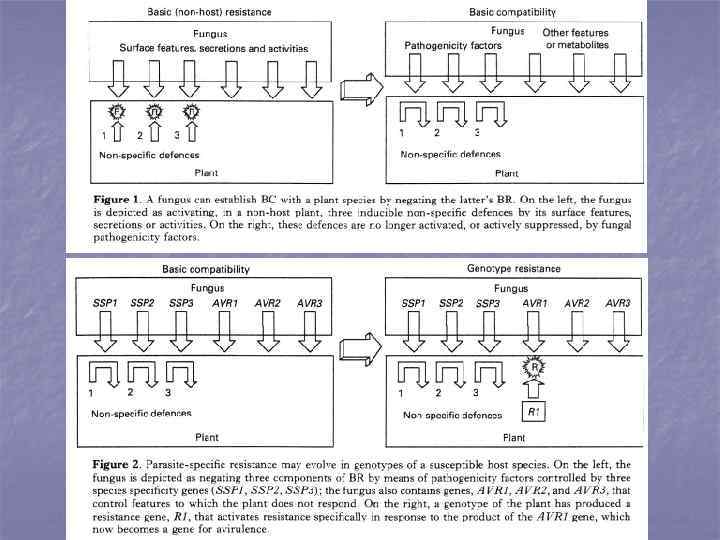

n n n Связывание и распознавание молекул PAMPs на рецепторах плазматических мембран в клетках растений вызывает в них защитный ответ, включающий окислительный всплеск, образование антипатогенных ферментов (главным образом, оксидаз и гидролаз), образование РRбелков, папилл, актвцию фенил-пропаноидных метаболических путей, др. защитные проявления, в т. ч. реакции, напоминающие сверчувств-е. Если эти защитные реакции и скорость их осуществления в клетках не останавливает рост и развитие патогена, то он вводит во взаимодействие с растением свои эффекторы – суппрессоры защитных реакций – Avr-белки. У бактерий эти эффекторные белки могут доставляться в растительную цитоплазму с помощью систем секреции III типа (у грамнегативных бактерий), II типа (обнаруженным у Erwinia и используемым для выделения ферментов, вызывающих разложение пектиновых и гемиполисахаридных компонентов растительных клеточных стенок и мягкую гниль), IV типа (осуществляющего перенос белка и ДНК у Agrobacterium). Патогеные грибы, по-видимому, также секретируют свои эффекторные белки – через гаустории (в экстрагаусториальный матрикс – периплазматическое пространство вокруг гаусториев, но как они проходят в цитоплазму растительной клетки и там оказывают действие – пока не ясно. Таким образом, в начале взаимодействия в системе хозяин-патоген в клетках растений происходит видоспецифическая индукция защитных реакций, а затем – расо-сорто-специфичесая активация/суппрессия этого ответа с помощью Avr-белков патогенна (активация сверхчувствительности – если Avr- и R-гены оба в доминантном комплементарном сочетании).



Фитоиммунитет: двухтактный рабочий механизм Растения обладают врожденным иммунитетом, который позволяет им обнаруживать на поверхности потенциально патогенных организмов и преодолевать исходящую от них угрозу. Главная особенность этой линии системы защиты является наличие рецепторов, существующих на поверхности клеток растений , комплементарных к важнейшим молекулам патогенов и микроорганизмов вообще (т. е. PAMPs – pathogenassociated molecular patterns и MAMPs – microbe-associated molecular patterns) Чтобы обеспечить защиту против патогенов, если первая, неспецифическая линия обороны, преодолевается, растения имеют еще вторую линию обороны, создаваемую рецепторами, комплементарными к определенным эффекторам патогенов. В отличие от PRRs, которые узнают эволюционно консервативные молекулы MAMPs, эти рецепторные белки воспринимают специфические эффекторы патогена и содержат кроме LRR-домена еще NB-домен, а потому их часто называют NB-LRRбелками; на С-конце они могут содержать также TIR- или CC-домен. LRR-домен NB-LRR-белков находится над плазмалеммой не всегда, в большинстве случаев мишенью эффекторов бывают внутрицитоплазматические NB-LRR-белки. Эти R-белки могут взаимодействовать с эффекторами либо прямо (как например, в патосистеме Linum–Melampsora lini), либо с участием посредников, как в системе Arabidopsis–Pseudomonas syringae). Непрямое действие часто связано с TIR- или CC -доменами в NB-LRR-белке.



В настоящее время утвердилось представление, что видо-специфическая (нехозяинная) устойчивость есть не что иное, как врожденная, или врожденный иммунитет (innate immunity) и вызывается неспецифическими элиситорами патогенов, воспринимаемыми растениями как чужеродные молекулы. Также показано, что сверхчувствительность одинаковым образом развивается у растения как в ответ на элиситоры непатогенного микроорганизма, так и авирулентной расы патогена. Строгих качественных различий между видовым и сортовым иммунитетом и формами их проявления нет, имеются лишь некоторые количественные особенности: специфическая устойчивость проявляется несколько быстрее, сильнее, отчетливее и часто сопровождается гибелью клеток, окружающих инфицированную в реакции сверхчувствительности. Оба ответа PTI и ETI качественно сходны. Приводя к сходному конечному результату, специфическая и неспецифическая системы защиты, используют разные сигнальные пути – первая, в основном, действует через активизацию фенольного метаболизма и использует в кач ве универсального посредника салициловую кислоту, вторая – через липооксигеназный путь с образованием другого универсального мессенджера – жасмоновой кислоты.

Узнавание и защитный ответ связывают каскады сигнальных ередач, гл. обр. через вторичные мессенджеры, которые у укариот консервативны. Обнаружены изменения уровня Са 2+, еактивных форм кислорода, NO, серии митоген-активируемых иназ, которые аналогичны у растений и животных. У растений обнаружены изменения уровней этилена, жасмоновой и салициловой кислот, которые вовлечены в идо- и расоспецифические формы устойчивости растений. В астности, показано участие жасмоновой к ты в ехозяинной нехозяинной устойчивости Arabidopsis к Alternaria brassicola, абака – к Pythium (к некро трофам), тогда как нехозяинная видоспецифическая) устойчивость Арабидопсиса к ржавчине romyces Uromyces vignae (биотрофу) зависит от салициловой к ты. В настоящее время установлено, что биотрофные патогены например, возбудители мучнистой росы) должны либо не ключать, либо подавлять образование этилена / жасмоновой ислоты в своих сигнальных механизмах фитопатогенеза, спользуя, главным образом, жасмоновую кислоту и этилен.

Долгое время вызывал споры вопрос: что специфично в влениях распознавания патогена растениями – устойчивость ли восприимчивость? Однако лишь после того как удалось понять значение неспецифических элиситоров (PAMP’s) и специфических эффекторов Avr’s), из которых первые выступают в роли индукторов, а торые – в роли суппрессоров защитных реакций, но могут воими ролями меняться, эти научные споры потеряли остроту. Многими экспериментами показано, что специфичность могут пределять и элиситоры и суппрессоры. Причем даже одни и те же продукты паразитов, в зависимости от идов и сортов растений-хозяев (или даже в зависимости от онцентрации), могут выступать в качестве элиситоров или уппрессоров.

n. В качестве примеров можно привести след. факты. из клеточных стенок Phytophthora infestans в восприимчивых сортах ослабляют защитные реакции, а в устойчивых – усиливают их. Специфичный для сортов овса с геном Pc 2 токсин викторин в пико-граммовых концентрациях является специфическим элиситором защитных реакций к Helminthosporium victoriae, а в нано-граммовых – суппрессором их. n. Глюканы n. Продукты бактерий – Hrp-белки (харпины) в нехозяинных видах растений действуют как элиситоры сверхчувствительных реакций, а в клет-ках растений-хозяев – как суппрессоры этих реакций.

n. Еще методами классической генетики и цитогенетики начали проводить локализацию генов на хромосомах, что получило название «картирование хромосом» . n. Были установлены места расположения многих генов на определенных участках растительных хромосом. В числе этих генов были и многие гены устойчивости растений к болезням или же связанных с фитоустойчивостью функций: например, генов пероксидазы. n. Анализ хромосомных карт обнаружил, что гены устойчивости растений, контролирующие синтез R-белков, расположены на хромосомах не случайно, а чаще всего в неких группах – кластерах. n. Возникновение кластеров сцепленных генов, функционально и, вероятно, структурно сходных, обусловлено внутри- или межгенными обменами участков ДНК, имеющих прямые (a, b, c, d −`a, `b, `c, `d) или инвертированные повторяющиеся последовательности (a, b, c, d −`d, `c`, b, `a). n. Нити ДНК родителей в мейозе могут спариваться по гомологичным последовательностям, к-рые находятся в негомологичных участках хромосом. n. Это приводит к неравному кроссинговеру. В результате у одного родителя участок хромосомы теряется (делетирует), а у другого удваивается (дуплицирует), т. е. вместо одного гена появляется два сцепленных.



Широко распространены три типа локализации генов: 1) одиночное диаллельное (один локус с двумя аллелями, контролирующими восприимчивость и устойчивость, которая, как правило, доминантна; 2) одиночное мультиаллельное (один локус с множеством ко-доминантных аллелей, контролирующих устойчивость к разным расам и видам патогена); 3) сцепленное (большое число ди- и мультиаллельных локусов сцеплены и образуют блок фенотипически сходных генов, контролирующих устойчивость к одной или неск. болезням. n С этой точки зрения наибольший интерес представляют LRR-области R-генов с многочисленными повторяющимися последовательностями (десятки раз). Благодаря точковым мутациям, делециям, инверсиям такая структура обеспечивает генетическую реорганизацию – прежде всего, участков R-генов, контролирующих взаимодействие с элиситорами – многочисленными и изменяющимися. Большую роль в увеличении генетического разнообразия семейства генов устойчивости могут играть разрывы кодирующей части ДНК, вызванные внедрением мобильных генетических элементов. Так, у риса в локусе R -гена Xa 21 обнаружены транспозоны Truncator и Retrofit, приводящие к разрывам и образованию самостоятельных рамок считывания. Этот белок ( Xa 21) сочетает свойства двух белков томата – мембранного рецептора и протеинкиназы. Вероятно, возникновение R-генов Cf 9 и Pto обусловлено разрывом гена-предшественника, аналогичного рисовому Xa 21. n

n Каждая часть смыслового комплекса R белков, включающего комплекс белков LRR–NBS–LZ, обеспечивающих не только взаимодействие с элиситором и с молекулами-мишенями (в частности, с ДНК), но также и передачу сигналов на другие молекулы – протеинкиназы, белки-посредники, циклические нуклеотиды и др. И каждая часть смыслового комплекса R-белков может подвергаться изменениям, описанным для LRR-участка. n Как правило, случайные генетические вариации сохраняются в геноме, образуя груз – неиспользуемую часть генома. n Исследования генома Arabidopsis и др. растений обнаружили, что почти 70% материала ДНК хромосом – это дубликаты, повторы, они расположены на всех хромосомах. n Одна из важнейших находок – значительная часть (~¼) этих участков содержит структуру R генов. Но зачем арабидопсису, имеющему всего 5 хромосом, чтобы 23% их объема занимали R гены? n Возникало логичное предположение, не является ли это повторение абзацов генома растительным аналогом систе мы гистосовместимости: как известно, система гистосов мести у человека и высших животных (млекопитающих) включает много дуплицированных генов. n Т. к. функции R генов растений заключаются в узнавании эффекторных Avr белков патогена, то увеличенное число повторов может вызываться давлением отбора – готовностью узнавать новые расы патогена на основе изменений существующего генетического материала.

n. Альтернативная возможность возникла из того, что пока же, несмотря на очевидную простоту и легкую допустимость предположения о существовании у многоклеточных растительных организмов системы распознавания своего, своих молекул, своих клеток при их контакте существуют экспериментальные доказательства о распознавании клетками растений только чужеродного генетического материала и нет данных о распознавании своего, кроме данных о бóльшей совместимости близкородственных растительных геномов прививках, чем генетически далеких. n. Кроме того, основанием для допущения у растений системы гистосовместимости служит сходство автофаговых явлений. n. У растений не обнаружен механизм гистосовместимости , подобный MHC – Major Hystocompatibility Complex животных, представляющая антигенные фрагменты чужого и missing self (ошибочного своего) как чужого на лимфоциты в межклеточную циркуляционную жидкость, тем не менее, определенные параллели в функционировании MHC животных и R-генной клеточной системы растений все же просматриваются. Главн. препятствием является вероятно наличие у растений клеточ. стенок, мешающих поступлению в цитоплазму белков.



ЛОКАЛЬНАЯ И СИСТЕМНАЯ ПРИОБРЕТЕННАЯ УСТОЙЧИВОСТЬ В местах развития инфекции происходят активные процессы, основанные на обмене сигнальными молекулами. При взаимодействии между партнерами активируется комплекс механизмов иммунитета, приводящих к несовместимости между растением и патогеном. Однако р-я растения не исчерпывается подавлением локального патогена. Установлено, что в месте инфекции развиваются более длительные процессы, получившие название индуцированной устойчивости. Первоначально для обозначения этих процессов был использован термин «иммунизация» . Иммунизация специфична, но приводит к общему повышению устойчивости растений к различным типам патогенов. Было показано, что активные защитные механизмы индуцируются различными элиситорами. Обнаружено, что растения способны развивать генерализованную (общую) индуцированную устойчивость к заболеваниям и вредителям в ответ на предварительное воздействие рядом факторов. К таким факторам относят: - заражение авирулентными патогенами; инокуляция непатогенными бактериями; обработка определенными микробными элиситорами и химическими веществами; повреждение органов растений грызущими вредителями.

Индуцированная устойчивость может иметь локальный характер, развиваясь вокруг места первичного внедрения патогена, выполняющего роль иммунизатора. Этот тип устойчивости называется локальной приобретен ной устойчивостью (local acquired resistance – LAR ). В некоторых случаях устойчивость распространяется на другие существующие и вновь образованные части растения, что приводит к формированию системной индуцированной устойчивости (induced systemic resistance – ISR). Явление индуцированной устойчивости изучали ученые разных научных школ (в частности, Kuč J. e. a. ), и исторически сложились 2 сходных названия: ● системная приобретенная устойчивость (systemic acquired resistance – SAR) и ● индуцированная системная устойчивость (induced systemic resistance – ISR).

На I Международном симпозиуме по индуцированной устойчивости растений к болезням (Корфу, 2000) ведущие исследователи пришли к общему мнению, что термин «индуцированная устойчивость» является общим. Для описания частных случаев возможно употребление обоих названий (SAR и ISR). Термин «индуцированная системная устойчивость» (ISR) употребляют гл. обр. при описании системной устойчивости, вызванной взаимодействием с симбиотическими бактериями рода Rhizobium. Индуцированная устойчивость неспецифична. Это значит, что ответ, развившийся в результате предварительной иммунизации растения, эффективен не только по отношению к исходному иммунизирующему виду, но и к > или < широкому кругу фитопатогенов, включая возбудителей болезней и вредителей.

Локальная индуцированная устойчивость была описана ранее по отношению к вирусам. Специфической формой индуцированной устойчивости является так называемая перекрестная защита. Она выражается в том, что предварительное заражение растений штаммом вируса, вызывающим слабые симптомы (или бессимптомным), предохраняет растение от последующего заражения штаммами, способными вызывать сильные симптомы поражения. Размножение второго вируса в клетках подавляется, хотя из клеток он не исчезает. Позже был выявлен другой тип локальной индуцированной уст-ти к вирусам, связанный с проявлением реакции сверхчувствительности В настоящее время показано, что LAR может быть индуцирована введением бактерий или фрагментов бактериальных оболочек, а также предварительной инокуляцией авирулентными грибами. При развитии локальной индуцированной устойчивости ткани, примыкающие к инфекционному месту и даже расположенные на противоположной стороне листа, приобретают устойчивость к внедрению и распространению различных патогенов.

Биохимической основой для развития LAR являются образование активных форм окислителей, биосинтез защитных PR-белков, фитоалексинов, а также укрепление клеточных стенок в результате действия комплекса ферментов и окислительного взрыва. Благодаря высокой концентрации антимикробных в-в предотвращается внедрение или распространение патогенов при повторной инфекции. Происхождение LAR стало понятным после расшифровки молекулярной основы событий, происходящих в зоне развития возбудителей заболеваний. В несовместимых комбинациях при узнавании патогена формируется внутриклеточный сигнал, активирующий защитные механизмы в пораженной и соседних клетках растения.


Системная приобретенная устойчивость (SAR) проявляется в удаленных от места первичной инфекции частях растения и снижает интенсивность проявления болезней, вызываемых разными микроорганизмами, а также повреждений вредителями при повторном контакте. Действие SAR неспецифично по отн. к разным видам патогенов. Пионером в изучении SAR была школа америк. фитопатологов под руководст. Дж. Куча, активно изучавшая это явление на примере растений сем. Тыквенные и Бобовые. Оказалось, что огурцы, дыни и арбузы могут быть системно защищены от многих заболеваний путем иммунизации – инокуляции их первого настоящего листа Предварительная иммунизация листьев возбудителем антракноза или вирусом некроза табака защищала растения, по крайней мере, от 13 видов микроорганизмов (облигатно- и факультативно-паразитических грибов, вирусов и бактерий). Такие же результаты были получены не только в тепличных, но и в полевых условиях – что весьма немаловажно для с. х.

Неспецифическая устойчивость к широкому кругу патогенов возникала, как прав. , при инфицировании микроорганизмами, вызывающими р-ю сверхчувствительности, но не механическими и химическими повреждениями. Позже было обнаружено, что индукция устойчивости может осуществляться и без р-и сверхчувствительности. Системная устойчивость проявлялась через 48. . . 72 ч после инокуляции листа-индуктора, затем через несколько суток достигала своего максимума, причем этот период совпадал с появлением симптомов на листе-индукторе. 1 -кратная индукция SAR защищала огурец от патогенов на 4. . . 6 нед. , а повторная инокуляция (ч-з 2. . . 3 нед. ) способствовала приобретению сезонной устойчивости к кругу патогенов.


Устан. , что SAR распространяется по растению снизу вверх. Так, прививка дыни или арбуза на подвой огурца, содержащего лист-индуктор, вызывала устойчивость в привое. Выяснилось, что для SAR-генов характерна экспрессия генов PR-белков. Экспрессия РR-генов начиналась ч-з 3. . . 6 ч и совпадала с началом формирования активного иммунного ответа в месте первичной инфекции. Кроме того, через некот. время продолжительная системная активация SAR-генов наблюдалась в удаленных частях растения. Значимость PR-белков определяется их участием во многих иммунных механизмах. Например, PR 6 – ингибиторы протеиназ, которые нарушают метаболизм грибных и бактериальных патогенов, а также защищают от грызущих насекомых. PR 9 – пероксидазы участвующие в укреплении кл. стенки через образование отложений лигнина. Др. белки принимают участие в укреплении стенки клеток хоз. и образовании папилл. В некот. патосистемах для SAR-генов характерна индукция активн. липоксигеназ: эти ферменты обр. производные жирных к-т с высокой антимикробной активн-ю.

Помимо накопления защитных белков в иммунизированных растениях наблюдаются синтез фитоалексинов и укрепление клет. стенки. Эти механизмы связаны с увеличением активности окислительных ферментов, а также синтезом терпеноидных или ароматических предшественников. Активность пероксидаз возрастает системно и вызывает сильную лигнификацию после иммунизации. Интересные данные были получены при индукции SAR у картофеля. Обработка раст-й картофеля элиситорами, выделенными из клеточ. стенок Ph. infestans, оказывает двойное действие на гриб. С одной стороны, индуцируется синтез сесквитерпеноидных фитоалексинов ришитина и любимина, сдерживающих развитие мицелия; с другой стороны, сокращается синтез стеринов растения, т. к. для них используются те же предшественники, что и для синтеза фитоалексинов. Поскольку оомицеты не способны к самостоятельному синтезу стеринов (являются ауксотрофами по отношению к стеринам), нарушается процесс образования спор. В результате иммунизация защищает картофель от повторного заражения и снижает интенсивность развития болезни. В наст. время доказано, что в индукции SAR в кач-ве мобильных сигналов участвуют салициловая, жасмоновая к-ты, этилен, абсцизовая к-та, поли-пептид системин и, возможно, др. в-ва.


Выявлены различные пути активации индуцированной устойчивости против определенных групп патогенов. Обнаружено существование двух различных путей сигнальной трансдукции для двух возбудителей заболеваний ячменя: мучнистой росы (Blumeria graminis f. sp. hordei) и корневой гнили (Bipolaris sorokiniana). Установлено, что салициловая к-та (СК) индуцирует устойчивость к облигатному паразиту В. graminis, в то время как жасмоновая к-та (ЖК) вызывает системную уст-ть к некротрофу Bipolaris sorokiniana. Формирование системной приобретенной устойчивости приводит к согласованной активации большого спектра генов, обеспечивающих комплекс иммунных ответов растений. Совокупность механизмов иммун-та обеспечивает неспецифическую устойчивость к различным вредным орг-ам. Проявления и регуляция индуцированной устойчивости имеют особенности для иммунизации био- и некротрофными патогенами, а также при поранениях и при повреждении грызущими насекомыми. Предполагается, что взаимодействие путей сигнальной трансдукции ведет к созданию сетевой структуры, к-рая адекватно реагирует на различные внешние сигналы. На I Международ. симпозиуме по индуцированной устойчивости растений к болезням (Корфу, 2000) многими ведущими учеными было высказано мнение, что именно индуцированная устойчивость лежит в основе неспецифической (горизонтальной) устойч-ти раст-й к болезням и вредителям.
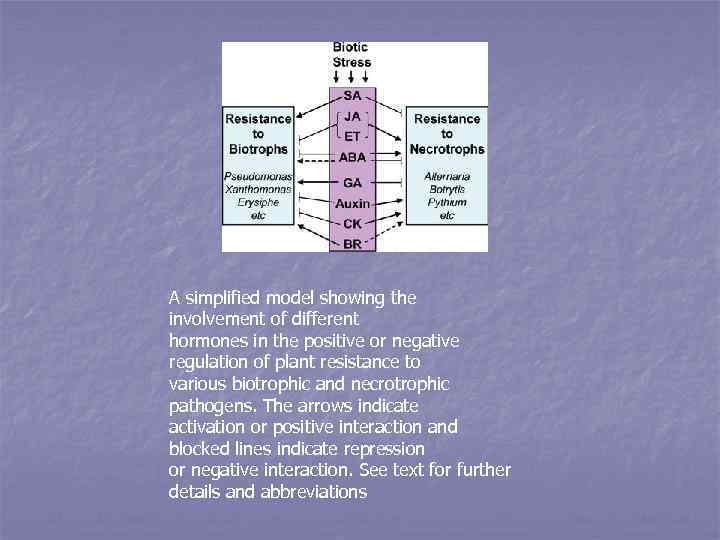
A simplified model showing the involvement of different hormones in the positive or negative regulation of plant resistance to various biotrophic and necrotrophic pathogens. The arrows indicate activation or positive interaction and blocked lines indicate repression or negative interaction. See text for further details and abbreviations


Прогнозируется, что использов-е ключевых регуляторов индуцированной устойчивости приведет к созд-ю сортов с длительной устойчивостью широкого спектра действия. Это мнение уже подтверждено эксперимент. данными. Так, обнаружены мутанты с более сильным выражением ключевого гена сигнальной трансдукции NPR 1. Трансгенные растения с этим геном проявляли неспецифическую устойчивость широкого профиля. Другим подтверждением этой гипотезы стало обнаружение химич. в-в, индуцирующих системную устойчивость. Такие вещества используют как эффективные пестициды нового поколения, особенности их применения описаны. Так, первоначально в качестве индуктора системной приобретенной устойчивости испытывали салициловую кислоту (СК).



Позже для индукции SAR были применены производные изоникотиновой к-ты (INA) и бензотиазола (ВТН). Эти химические индукторы включаются в цепь сигнальной трансдукции SAR, а также индуцируют дополнительные гены. Показано, что INA запускает путь сигнальной трансдукции, действуя на те же самые сайты, что и CK, или на сайты, идущие за ними. Салициловую и изоникотиновую к-ты считают настоящими SAR-индукторами. Они индуцируют экспрессию тех же самых генов, что и патогены. В 1996 г. в кач-ве коммерческого препарата для индукции SAR был изучен Бензотиазол (CGA-245704); на рынке в США он представлен под названием ‘Actigard’, в Европе ‘BION’ и в РФ «Бион» . Можно прогнозировать, что понимание механизмов индуцированной устойчивости даст возможность построить эффективную интегрированную систему защиты растений, использующую как сорта с повышенным уровнем неспецифической устойчивости, так и эффективные и экологически безвредные пестициды.

Благодаря обнаружению феномена индукции SAR у растений с помощью симбиотических бактерий рода Rhizobium (а также микоризообразующих грибов) в перспективе можно будет развивать экологически безопасные формы защиты растений от патогенных микроорганизмов и вредителей. В частности, в экспериментах по бактеризации семян редьки и огурца для закрытого грунта была получена 50%-ная прибавка урожая в результате снижения заболеваний. Индукцию ISR с помощью ризобий стали использовать для разработки системы биологического контроля болезней овощей, передающихся векторно с помощью насекомых. Результаты показали, что при обработке ризобиями у растений повысилась уст-ть к грызущим жукам и к бактериальному вилту огурцов.

Рассматривая иммунитет как общебиологический феномен, имеющий эволюционно выработанные особенности у двух основных царств многоклеточных живых существ – животных и растений, мы должны остановиться на понятии «иммунная система организма» . Известно, что организмы животных и растений состоят примерно из 10 млн. генотипически идентичных клеток, к-рые в целом комплексе могут возникнуть и существуют при одном обязательном условии – наличии специальной системы распознавания и элиминации чужеродных или собственных мутировавших клеток и молекул. Такую функцию надзора за генотипическим и химико-функциональным постоянством совокупности соматических клеток несет иммунная система. Иммунологический контроль над внутренним постоянством многоклеточной популяции организма – это и есть главная функция иммунитета. У человека и высших животных центральной фигурой иммунной системы является лимфоцит. Иммунная система – совокупность всех лимфоидных органов и скоплений лимфоидных клеток тела. Лимфоидная система организма в этом случае представляет собой морфологический синоним иммунной системы.

Растения как многоклеточные организмы на интервенцию патогена отвечают не только «выстрелом в него из каждой отдельной атакованной клетки» , но также вовлекают во взаимодействие соседние и даже дистанционно удаленные клетки. Для этого они используют клеточные стенки, межклетники и всю сеть внепротоплазматического пространства – апопласт. Клеточные стенки, основу которых составляют переплетения целлюлозных фибрилл, обеспечивают диффузию молекул с той или иной скоростью в зависимости от их размера и физико-химических свойств подобно хроматографической бумаге. Некоторые сигнальные молекулы достигают сосудов флоэмы и перемещаются по ним далеко от очага инфекции. Известно, что патогены бактериальной и грибной природы, за исключением вирусов, не проникают внутрь растительной протоплазмы, – в том числе и гаустории биотрофных грибов: они, вторгаясь в клетку хозяина, вдавливаются в его протоплазму, но находятся за пределами инвагинированной плазмалеммы. Для грибных и бактериальных патогенов зоной оккупации в организме растения всегда является некоторая часть внепротоплазматического пространства. В случае неэффективности антиинфекционного действия выделяемых в межклеточное пространство растительными протоплазмами лизосомальных гидролаз и оксидаз мембрана вакуоли разрывается и из гибнущей клетки на патогена обрушивается комплекс заключенных в главной лизосоме гидролаз и токсичных вторичных метаболитов.

Апопласт, по которому перемещаются в том или ином направлении вода, ионы, гормоны, физиологически активные вещества, токсины патогенов и т. п. соединения, представляет собой специфическую, но очень важную часть гомеостатической системы растений. Поскольку поддержание функционального равновесия в организме – атрибут иммунной системы, хорошо выраженный у высших животных и человека, то можно сказать, что система внепротоплазматического пространства (апопласт), наряду с внутрипротоплазматической лизосомально-вакуолярной (эндо-мембранной) системой – две главные составные части структурной организации специфической иммунной системы растений. Хотя у растений в процессе эволюции не получила развития система гуморального иммунитета – накопление специфических пептидов – антител в ответ на появление высокомолекулярных соединений паразита – антигенов, как это произошло у животных, у них имеются белки, связанные с патогенезом (Pathogenesis-related proteins – PR-белки), а также ферменты синтеза вторичных метаболитов, кодируемые семейством сцепленных R-генов и выполняющих функции защиты, аналогичные функциям, выполняемым множественным иммуноглобулинам млекопитающих. Несмотря на различные молекулярные основы и пути их происхождения у животных и растений в обоих случаях высокая вариабельность генопродуктов позволяет быстро реагировать на заражение новыми вирулентными расами и видами паразитов как в очаге инвазии, так и на удалении от него.

Вышесказанное определяет наше понимание структурной организации системы иммунитета растений, включающей апопласт и лизосомально-вакуолярную (эндомембранную) систему как ее основные составные части. Данное представление о структурной организации системы фитоиммунитета объясняет механизмы функционирования как врожденного (клеточного) иммунитета, так и индуцированной устойчивости всего многоклеточного организма и является существенным дополнением и углублением получившей признание концепции J. Jones, J. Dangle (2006). Наше дополнение никоим образом не отвергает и не умаляет вклад ученых, исследовавших значение экстра- и интрапротоплазматических рецепторных белков растений и механизмы восприятия и передачи сигнала на ядерный геном.

n. Приведем аргументы в подтверждение этого тезиса. n. Как показали наши исследования, межклеточное пространство мезофилла листа злаков содержит всегда некоторый уровень гидролитических ферментов: хитинах, фосфатаз, пероксидазы и других оксидаз. Однако после вторжения в межклеточное пространство мезофилла патогенного гриба, − будь то возбудитель ржавчины или сетчатого гельминтоспориоза, − уровень активности этих ферментов повышается, если только сами патогены не подавляют эту гидролитическую активность в апопласте листа. Апопласт, включая экстрагаусториальную капсулу, является местом паразитического существования патогенных грибов и бактерий. Выявленные нами явления в апопласте листьев при инфицировании свидетельствуют о том, что апопласт, т. е. система межклетников и контактирующих клеточных стенок является, во-1 -х, местом процессинга и гидролиза крупных биомолекул и появления их фрагментов ( элиситоров) и, во-2 -х, одновременно выполняет функцию поддержания физиологического равновесия (гомеостаза) ткани, органа и растения в целом. n. Таким образом, апопласт, по которому могут диффундировать в том или ином направлении вода, ионы, гормоны, физиологическиактивные в-ва, токсины патогенов и т. п. соединения, представляет собой специфическую, но очень важную часть гомеостатической системы растений. Поскольку поддержание функционального равновесия в организме – атрибут иммунной системы, хорошо выраженный у высших животных и человека, то можно сказать, что система внепротоплазматического пространства (апопласт), наряду с внутрипротоплазматической лизосомальновакуолярной системой – две главные составные части структурной организации весьма специфической иммунной системы растений.





n n n Поскольку основной формой проявления активности R-генов является программируемая клеточная гибель, которая часто встречается в развивающихся растениях и животных, то можно предполагать, что характерные для R-генов эффекты могли также происходить и играть ключевую роль в разных аспектах нормального онтогенеза растений, в частности, при возникновении внутри массы малодифференцированных паренхимных клеток клеточных групп со специализацией на передаточно-транспортной, механической и защитной функциях. Молекулярно-генетическими исследованиями последних лет обнаружены взаимосвязи R-генов устойчивости к мучнистой росе с генами CLAVATA, контролирующими меристематическую активность и процессы развития в тканях растений. Следует обратить внимание на некоторые стороны взаимосвязи генов фитоустойчивости и развития. Гены устойчивости томатов к Cladosporium fulvum активируются при снижении концентрации аминного азота в межклеточной среде, гены восприимчивости растений к микоризным грибам – при понижении фосфат-ионов в окружающей среде, гены сверхчувствительного некроза и апоптоза (программируемой клеточной гибели) – при появлении в межклеточной среде перекиси водорода и недостаточном поступлении питательных веществ и часто сопровождаются так называемым окислительным и лизосомальным взрывом в самой растительной клетке. В подобных случаях погибающая в результате апоптоза клетка животных используется для питания соседними клетками, в которых активируются процессы фагоцитоза, самопереваривания и реутилизации веществ. В растениях же погибающая клетка опустошается внутри и лигнифицируется снаружи – превращаясь в прототип сосуда, облегчающего передаточную функцию между другими живыми клетками. Кроме того, в соседних с гибнущей клетках активируются процессы вторичного метаболизма, вырабатываются вещества, имеющие защитную и сигнальную функцию, индуцируется меристематическая активность и может развиваться краевая перидерма вокруг очага окислительных и гидролитических процессов. Т. о. , возникают предпосылки для цитодифференцировки, гисто- и органогенеза. Благодаря молекулярным исследованиям стало ясно, что в процессах, обеспечивающих жизнедеятельность клетки и ее взаимодействие с окружающей средой, между простейшими, дрожжами, эукариотами, и человеком гораздо больше общего, чем специфического. Поэтому не удивительно наличие общих механизмов в защите от инфекционных болезней, которые начали формироваться еще при переходе от одноклеточной к многоклеточной форме существования. Переход от более примитивных механизмов иммунитета у растений к более совершенным, присущим позвоночным, заключается, видимо, в разделении функций.

n n n У растений (почти как у одноклеточных форм) каждая клетка способна к синтезу молекул, узнающих «чужое» , к трансдукции сигнала в ядерный аппарат, токсическому действию на паразита, подавлению его внедрения, изоляции и т. д. Сигнальные молекулы действуют внутриклеточно, обеспечивая локальную иммунную реакцию. Хотя в ответ на заражение может возникнуть и системная приобретенная устойчивость (System Acquired Resistence – SAR), она не абсолютна и проявляется лишь в снижении восприимчивости к повторному заражению неинфицированных участков растения. SAR, Systemic acquiered resistance: снижения степени поражения после повторного заражения, но без признаков сверхчувствительного некроза. В функционировании SAR роль сигнала, распространяющегося по флоэме растения снизу вверх при биотрофном патогенезе играет салициловая кислота, а при некротрофном – жасмоновая кислота, продукт действия липоксигеназы на ненасыщенные жирные кислоты клеточных мембран. Интерес представляет также то, что устойчивость передается также растениям-регенерантам через культуру ткани. У животных иммунные функции разделены между рядом клеток – Т- и В -лимфоцитами, макрофагами и др. Сигнальные молекулы передают информацию между клетками, что обеспечивает усиление сигнала и его системное распространение. Этот механизм обусловил возникновение семейства сигнальных молекул – цитокинов (интерлейкинов, ФНО и др. ) и их рецепторов на поверхности иммунокомпетентных клеток.

n n n У растений возникновение такого механизма маловероятно и по структурным соображениям – наличию клеточных оболочек, препятствующих межклеточным обменам. С появлением функционально различных, способных к автономному размножению и системному распространению клеток связано и другое принципиальное различие между иммунными системами растений и животных. У животных главные защитные механизмы − антитела, высокоспецифичные к определенным видам и даже штаммам патогенных микроорганизмов. Такая специфичность требует, во-1 -х, огромного разнообразия в строении иммунных молекул, которое может быть обеспечено только белками и, во-2 -х, механизма преимущественного размножения только того клона, который продуцирует нужное антитело. Каждая клетка растения, несущая иммунные функции, не может обеспечить такую сложную систему защиты. Поэтому основные защитные молекулы растений низкомолекулярны (фенолы, сапонины, терпеноиды, алкалоиды) и неспецифичны, т. е. токсичны по отношению к большому числу видов патогенных грибов, бактерий и растений. Специфичен, и то относительно, лишь их синтез в ответ на инфекцию. И хотя в зараженной клетке растения обычно образуется семейство близких по строению вторичных метаболитов (например, фитоалексинов), все они неспецифичны и отличаются лишь степенью токсичности к штаммам и чувствительностью к их ферментам.

n n Т. о. , у растений имеются белки (так называемые PR-белки), а также ферменты синтеза вторичных метаболитов, которые кодируются семейством сцепленных R-генов и выполняющих функции защиты, аналогичные функциям, выполняемым множественным иммуноглобулинам млекопитающих. Несмотря на различные основы их происхождения в обоих случаях высокая вариабельность генопродуктов позволяет быстро реагировать на заражение новыми вирулентными расами и видами паразитов. В последние годы меняется отношение фитопатологов и к практическому использованию приобретенного иммунитета. Однако в отличие от животных, иммунизация которых основана на заражении ослабленными штаммами паразитов, вызывающими размножение требуемого клона лимфоцитов, иммунизацию растений проводят химическими соединениями, индуцирующими синтез неспецифических форм защиты (абиотическими элиситорами). Сейчас многие фирмы производят такие соединения для практического использования: предпосевной обработки семян или клубней, летнему опрыскиванию вегетирующих растений и т. д.

n Итак, мы теперь знаем, что биологическая эволюция шла в направлении от одноклеточных организмов к многоклеточным, и таким же образом происходила эволюция иммунитета. В многоклеточном организме возникает система защиты: она включает уже некоторые пространственно расположенные и специализированные (ткане-дифференцированные) клетки, более других выполняющие функции защиты – например, эпидермис, вторичные покровы. В поддержании фитоиммунитета очень важны и тонкие слои меристем, препятствующие проникновению патогенов в них или через них, т. к. паразитизм патогенов поддерживают только завершившие деление клетки, растущие и приобретшие черты специализации (патогены, парализующие токсинами сократительные белки делящегося ядра и использующие содержимое таких клеток для питания встречаются редко). С этим связано использование меристем для оздоровления растений. Важную перестройку в переходе от одноклеточного к многоклеточному состоянию и в поддержании иммунитета претерпевает эндоплазматический ретикулум, связывающий ядерную мембрану с плазматической, но цитофизиологические детали этого перехода пока слабо изучены. Совершенно очевидно также, что в проявлениях фитоиммунитета важнейшую роль играет система клеточных стенок и межклетников, одновременно являющаяся и нишей, в которой развиваются фитопатогены (даже образующие гаустории). Однако, у растений нет специфических белковых гуморальных факторов и циркулирующей по организму жидкости, используемой для защиты, хотя обнаружены их аналоги – небелковые вторичные метаболиты и так называемые патогенезозависимые белки (PR-белки), ответственные за окислительный взрыв, папиллобразование и лигнификацию клеточных стенок в инфицированных тканях, а через 48 -72 ч во всем растении – явление, получившее название системной приобретенной устойчивости (SAR).

n. В проявлениях иммунитета у растений, в отличие от человека и животных, нет типичного механизма гистосовместимости (его работе, в частности, свободному перемещению крупных молекул антигенов мешают клеточные стенки), но есть распознавание «чужого» (клеток бактерий, гиф и гаусториев грибов, молекул токсинов и ферментов), а также, по-видимому, и «ошибочного своего» , которое происходит несмотря на наличие у растений клеточных стенок. А вот распознавания «своего» – наиболее простого и жизненно необходимого, пока не доказано. Генетическая тотипотентность протоплазм на протяже-нии жизни растения без сбоев обеспечивает построение его тела из большого числа однотипных клеток без случайного попадания в клеточную массу «чужаков» , а проникновение «чужеродных» клеток из многочисленных фитопатогенов и потенциальных фитопатогенов, населяющих почву или надземное пространство, становится терпимым паразитизмом или взаимовыгодным сожительством (у микориз или лишайников). n. Способность распознавать чужеродное не кончается уровнем клеток, но обнаруживаются в форме абортации «чужих» хромосом при аллополиплоидизации и межвидовом и межродовом скрещивании (например, Triticum и Secale). Митохондрии и хлоропласты, которые считаются позже включенными в растительные протоплазмы, при поражении растительных клеток гаусториями или токсинами патогенов, как предполагают, должны реагировать на них иным образом, чем древняя часть клетки – ядро и цитоплазма. На практике эти особенности реакции растительных клеток на структуры или молекулы патогена не столь выражены.

n. У водорослей же инфицирование фитопатогенами, эволюционно адаптированными к высшим растениям, чаще всего просто невозможно вследствие слабой адгезии клеток патогена, отсутствия дифференциации инфекционных структур, их проникновения и физиологической недоступности, но не из-за отсутствия в клетках водорослей нужных патогенам питательных веществ. n. Водоросли представляют источник пищи для насекомых, животных и человека, т. к. токсичные вторичные метаболиты у водорослей почти не образуются. n. Общность врожденного иммунитета человека и растений и их реакции на инфекцию (Ausubel, Plotnikova) предполагает новые возможности влияния на иммунные реакции растений и человека, в том числе разработку биотехнологического способа получения сывороточных белков и др. лекарств из растений после заражения патогенами человека, а также после вставки генов иммунобелков человека в геном растений


Ученые, внесшие наибольший вклад в изучение фитоиммунитета Мечников ИИ. Комаров ВЛ. Палладин ВИ. Дунин МС. Вавилов НИ. Страхов ТД. Вердеревский ДД. Рубин БА. Федотова ТИ. Сухоруков КТ. Метлицкий ЛВ. Токин БП. Купревич ВФ. Горленко МВ. Эфроимсон ВП. Серова ЗЯ. Андреев ЛН. Тарчевский ИА. Тютерев CЛ. Дьяков ЮТ. Озерецковская ОЛ. Плотникова ЛЯ. Ward M. Pfeffer W. Bernard N. Massee G. Chester KS. Offord T. Müller K. Börger H. Cruickshank I. Tatcher FS. Show M. Walton JD. Uritani I. Tomiyama K. Garber ED. Stakman EC. Van der Plank J. Flor H. Loegering WQ. Van Loon H. Aist J. Keen NT. Ouchi H. de Wit P. Yarwood CE. Show M. Bushnell WR. Heath MC. Mendgen K. Boller T. Kuć J. Kiraly Z. Jonson JGD. Ausubel F. Plotnikova JM. Наhn M.

n n n n n Литература: Дьяков Ю. Т. Пятьдесят лет теории ген-на-ген //Успехи совр. биологии. 1996. Т. 116, вып. 3. С. 293– 305. Дьяков Ю. Т. , Озерецковская О. Л. , Джавахия В. Г. , Багирова С. Ф. Общая и молекулярная фитопатология. – М. : изд. об-ва фитопатол. , 2001. – 302 с. Дьяков Ю. Т. На пути к общей теории иммунитета //Ж. общей биологии. 2005. Т. 66, № 6. С. 451– 458. Шкаликов В. А. , Дьяков Ю. Т. , Смирнов и др. Иммунитет растений. – М. : Колос. С, 2005. – 190 с. Карпук В. В. Структурные основы системы иммунитета злаков. //Ботаника. – Мн. : ИЭБ, 2014. – 58 с. ( в печ. ). De Wit P. J. G. M. Pathogen avirulence and plant resistance: a key role for recognition. //Trends in Plant Science. 1997. V. 2, N 12/ P. 452 -458. Schulze-Lefert P. Plant immunity: the origami of receptor activation //Current Biology. 2004. V. 14, N 1. R 22 – 24. Bent A. F. Plant disease resistance genes: function meets structure //Plant Cell. 1996. V. 8, N 19. 1757– 1771. Wisser R. J. , Balint-Kurti P. J. , Nelson R. J. The genetic architecture of disease resistance in maize: a synthesis of published studies. //Phytopathology. 2006. V. 96, N 10. 120– 129. Rahme L. G. , Ausubel F. M. , Cao H. e. a. Plants and animals share functionally common bacterial virulence factors //PNAS. 2000. V. 97, N 16. 8815– 8821. Hahn M. , Mendgen K. Characterization of in planta-induced rust genes isolated from a haustorium-specific c. DNA library //Mol. Plant-Microbe Interactions. 1997. V. 10, N 4. 427 – 437. Parker J. E. , Coleman M. J. Molecular intimacy between proteins specifying plant-pathogen recognition //Trends in Biochem. Science. 1997. V. 22, N 8. 291– 296. Michelmore R. W. , Meyers B. C. Clusters of resistance genes in plants evolve by divergent selection and a birthand-death process //Genome Research. 1998. V. 8. 1113 – 1130. Heath M. C. Evolution of plant resistance and susceptibility to fungal parasites //The Mycota. Vol. V, part B: Plant Relationships /Carroll and Tudzynski, eds. – Berlin, Heidelberg: Springer-Verlag, 1997. P. 257 – 276. Jones D. A. , Takemoto D. Plant innate immunity – direct and indirect recognition of general and specific pathogen-associated molecules //Current Opinion in Immunology. 2004. V. 16, N 1. 48 – 62. Innes R. W. Guarding the goods. New insights into the central alarm system of plant //Plant Physiology. 2004. V 135. 695– 701. Staskawicz B. J. Genetic of plant-pathogen interactions specifying plant disease resistance //Plant Physiology. 2001. V. 125, N 1. 73– 76. Staskawicz B. J. , e. a. Common and contrasting themes of plant and animal diseases //Science. 2001. V. 292, N 5525. 2285– 2289.


СПАСИБО ЗА ВНИМАНИЕ !
+Лек1,2.Фитоиммунитет-2014.pptx