Bioenergetics 3lection 2012.ppt
- Количество слайдов: 50

Мышцы, пиво Енергетика цтк, белков, судьба метаболитов
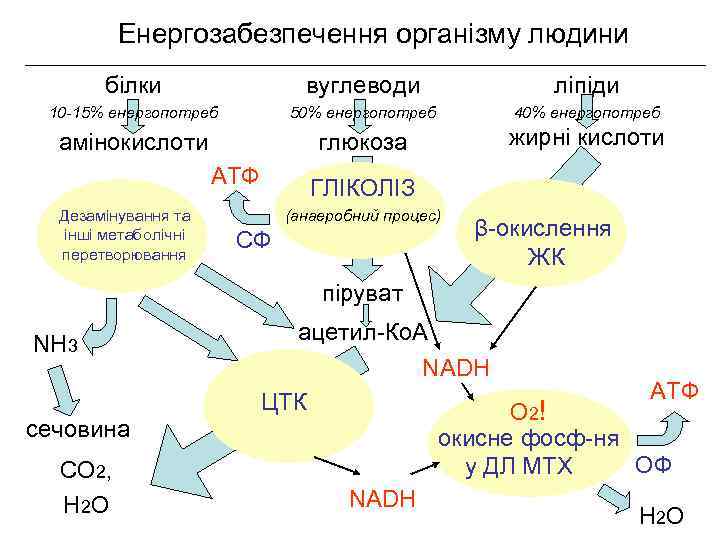
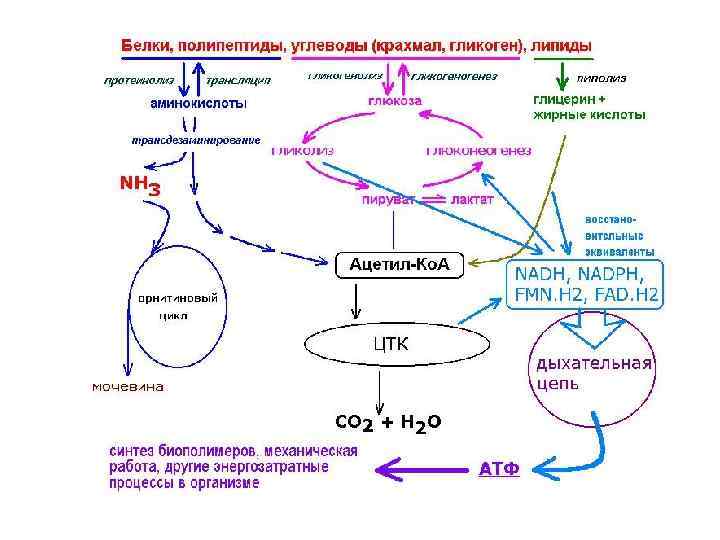
Енергозабезпечення організму людини білки вуглеводи ліпіди 10 -15% енергопотреб 50% енергопотреб 40% енергопотреб амінокислоти глюкоза жирні кислоти АТФ Дезамінування та інші метаболічні перетворювання ГЛІКОЛІЗ (анаеробний процес) СФ β-окислення ЖК піруват NH 3 сечовина СО 2, Н 2 О ацетил-Ко. А NADH АТФ ЦТК О 2! окисне фосф-ня ОФ у ДЛ МТХ NADH Н 2 О
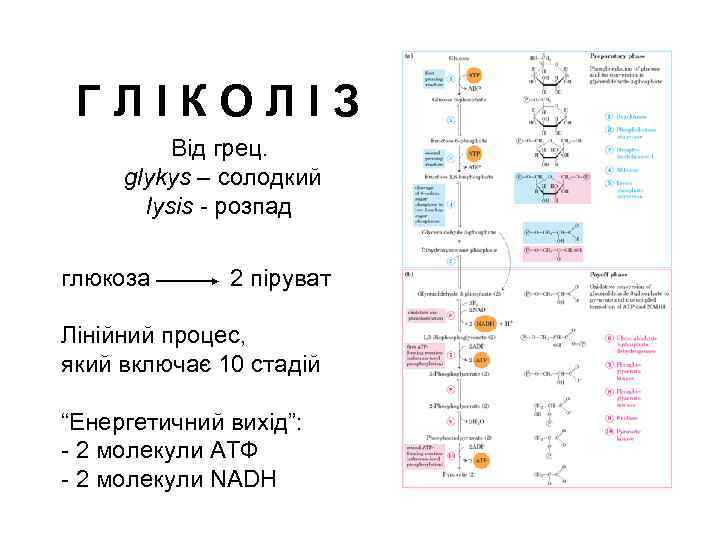
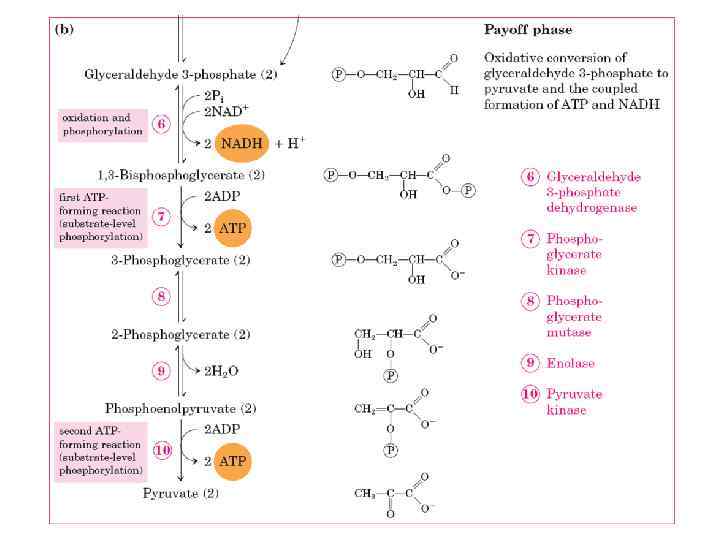
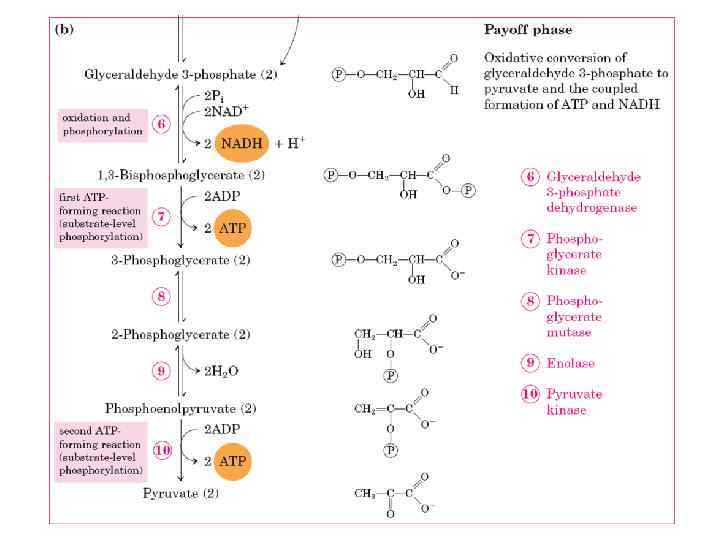
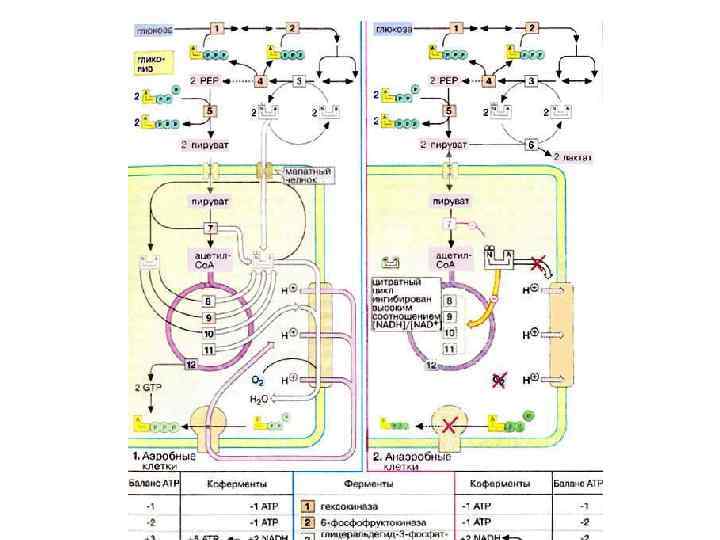
ГЛІКОЛІЗ Від грец. glykys – солодкий lysis - розпад глюкоза 2 піруват Лінійний процес, який включає 10 стадій “Енергетичний вихід”: - 2 молекули АТФ - 2 молекули NADH
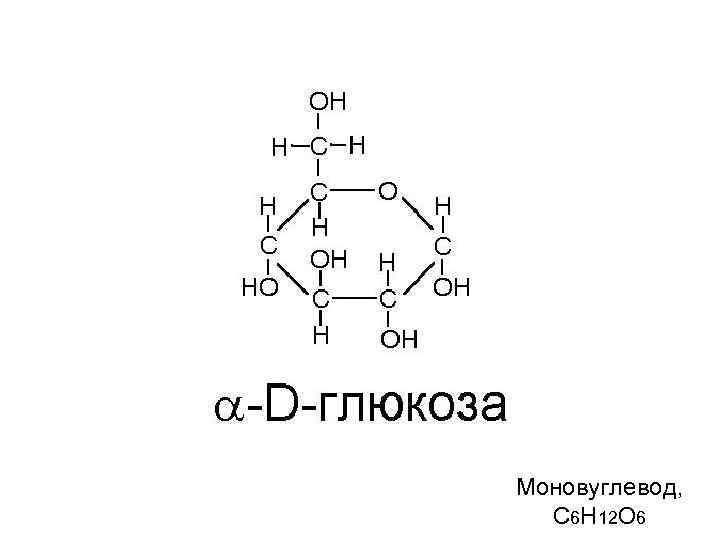
Моновуглевод, С 6 Н 12 О 6
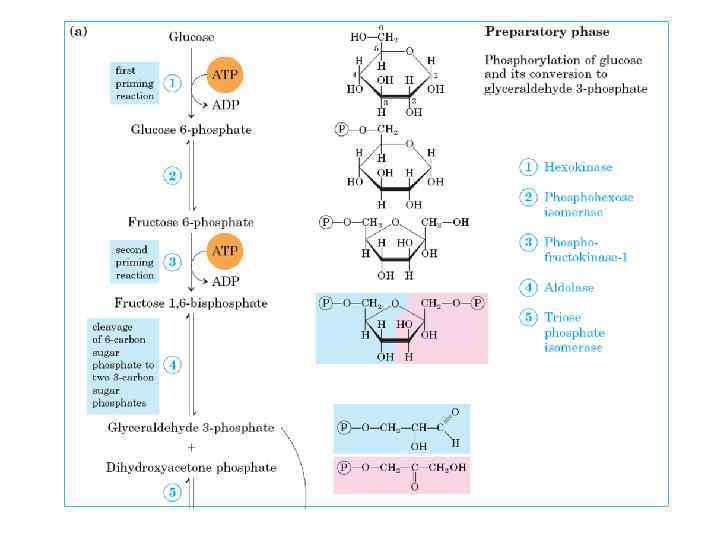

Макроергічні сполуки (грец. makros великий + ergon робота) містять зв’язки з високою негативною енергією гідролізу (<20. 9 к. Дж/моль або <30. 5 к. Дж/моль) реакція ∆Go, , к. Дж/моль ATФ + H 2 O АДФ + Ф -30, 6 AДФ + H 2 O АМФ + Ф -30, 6 ATФ + H 2 O АМФ + ФФ -30, 6 (-31, 5) ФФ + H 2 O 2 Ф -30, 6 (-33, 1) фосфоенолпіруват + H 2 O піруват + Ф -61, 9 1, 3 -діфосфогліцерат + H 2 O 3 -фосфогліцерат + Ф -49, 3 креатинфосфат + H 2 O креатин + Ф -42, 7 Ацетилфосфат + H 2 O ацетил + Ф -43, 1 AМФ + H 2 O Аденозин + Ф -14, 6

• Глюкоза 2 лактат ∆Go, = -196, 9 к. Дж/моль • АДФ АТФ ∆Go, = 30, 6 к. Дж/моль • КПД - 31% ! • (при фізіологічних концентраціях продуктів та субстратів реакцій 50 -55%)

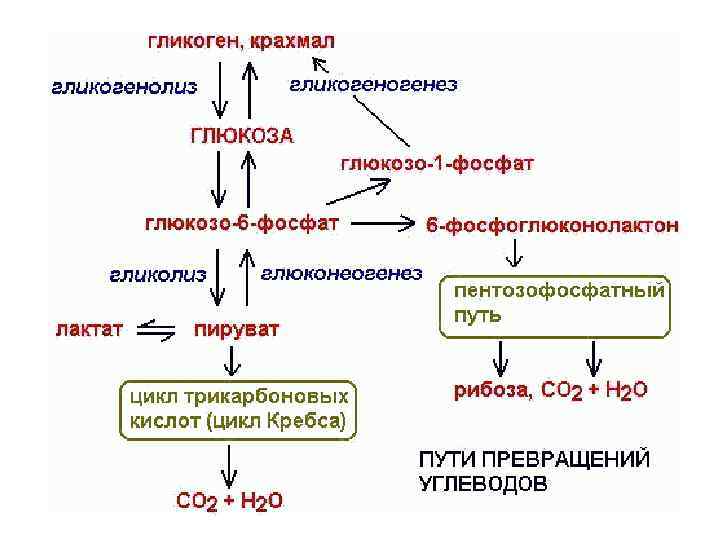
• Глюкоза 6 СО 2+Н 2 О ∆Go, = -2870 к. Дж/моль • Глюкоза 2 лактат ∆Go, = -196, 9 к. Дж/моль • Використовується лише близько 7% !
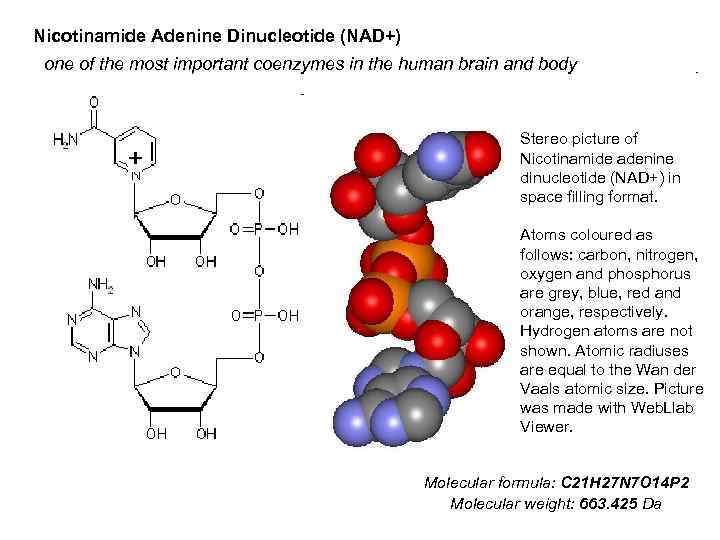
Nicotinamide Adenine Dinucleotide (NAD+) one of the most important coenzymes in the human brain and body Stereo picture of Nicotinamide adenine dinucleotide (NAD+) in space filling format. Atoms coloured as follows: carbon, nitrogen, oxygen and phosphorus are grey, blue, red and orange, respectively. Hydrogen atoms are not shown. Atomic radiuses are equal to the Wan der Vaals atomic size. Picture was made with Web. Llab Viewer. Molecular formula: C 21 H 27 N 7 O 14 P 2 Molecular weight: 663. 425 Da
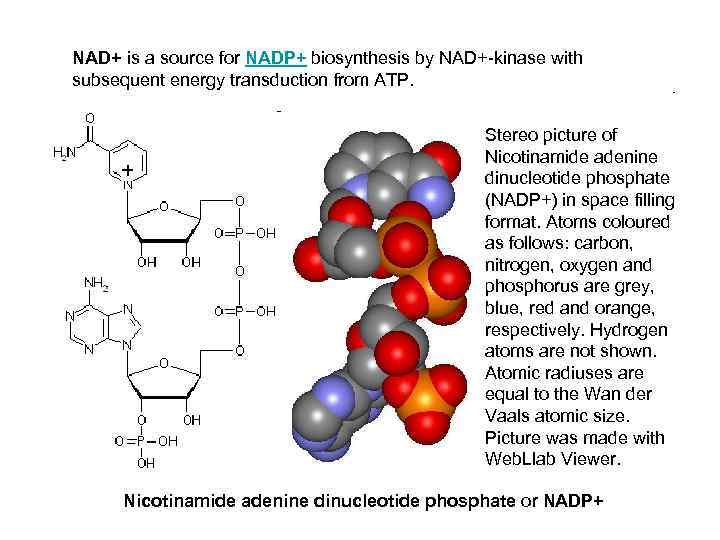
NAD+ is a source for NADP+ biosynthesis by NAD+-kinase with subsequent energy transduction from ATP. Stereo picture of Nicotinamide adenine dinucleotide phosphate (NADP+) in space filling format. Atoms coloured as follows: carbon, nitrogen, oxygen and phosphorus are grey, blue, red and orange, respectively. Hydrogen atoms are not shown. Atomic radiuses are equal to the Wan der Vaals atomic size. Picture was made with Web. Llab Viewer. Nicotinamide adenine dinucleotide phosphate or NADP+
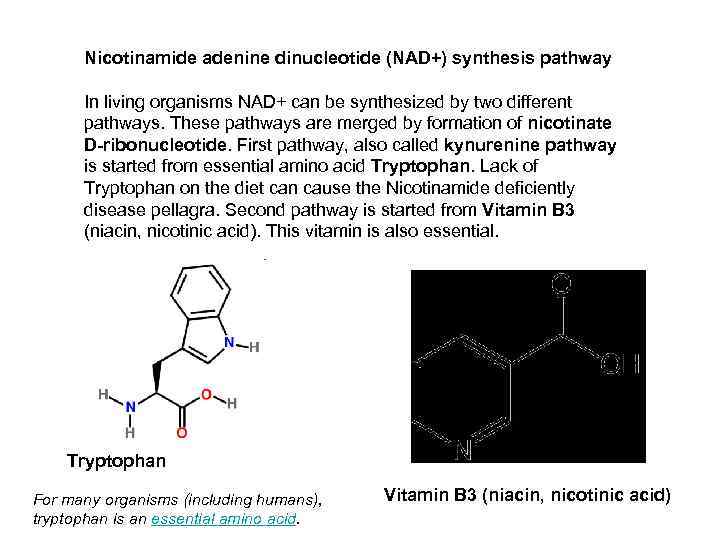
Nicotinamide adenine dinucleotide (NAD+) synthesis pathway In living organisms NAD+ can be synthesized by two different pathways. These pathways are merged by formation of nicotinate D-ribonucleotide. First pathway, also called kynurenine pathway is started from essential amino acid Tryptophan. Lack of Tryptophan on the diet can cause the Nicotinamide deficiently disease pellagra. Second pathway is started from Vitamin B 3 (niacin, nicotinic acid). This vitamin is also essential. Tryptophan For many organisms (including humans), tryptophan is an essential amino acid. Vitamin B 3 (niacin, nicotinic acid)
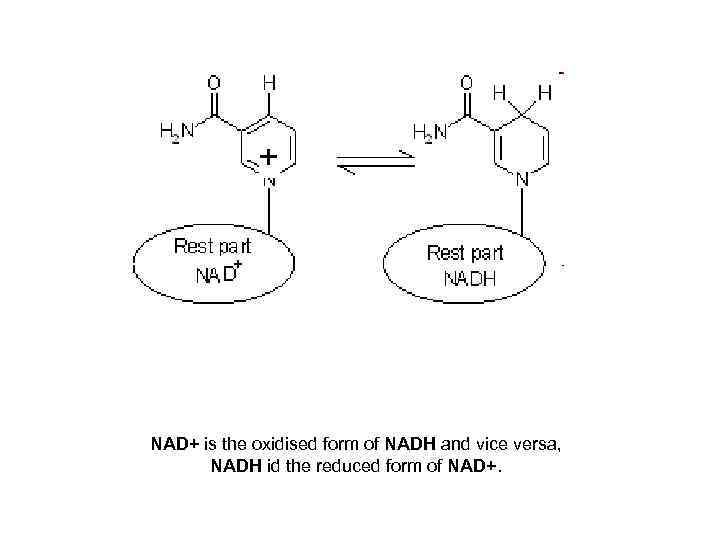
NAD+ is the oxidised form of NADH and vice versa, NADH id the reduced form of NAD+.

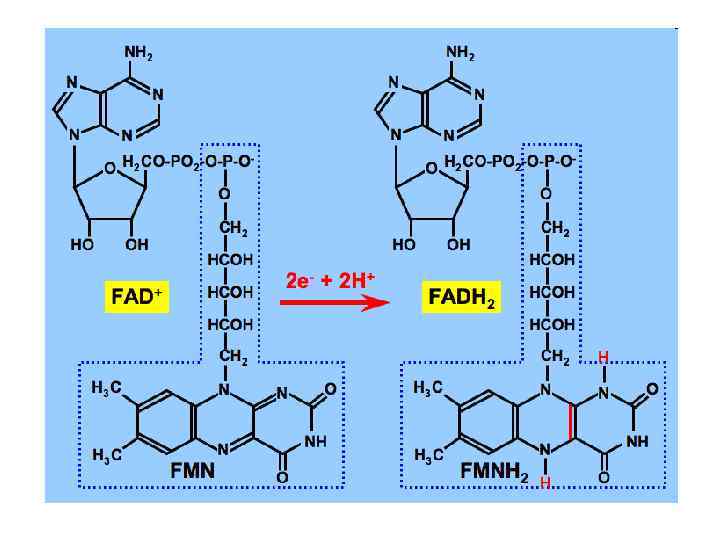
• The structure shown on the left is for FAD and is similar to NAD+ in that it contains a vitamin-riboflavin, adenine, ribose, and phosphates. As shown it is the diphosphate, but is also used as the monophosphate (FMN). • In the form of FMN it is involved in the first enzyme complex 1 of the electron transport chain. A FMN (flavin adenine mononucleotide) as an oxidizing agent is used to react with NADH for the second step in the electron transport chain. The simplified reaction is: • NADH + H+ + FMN -----> FMNH 2 + NAD+ Red. Ag. Ox. Ag. • Note the fact that the two hydrogens and 2 e- are "passed along" from NADH to FFMN. Also note that NAD+ as a product is back to its original state as an oxidizing agent ready to begin the cycle again. The FMN has now been converted to the reducing agent and is the starting point for the third step.
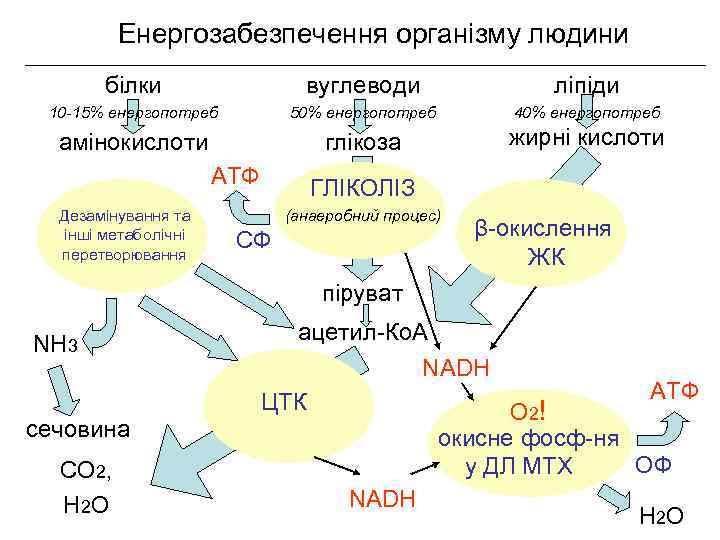
Енергозабезпечення організму людини білки вуглеводи ліпіди 10 -15% енергопотреб 50% енергопотреб 40% енергопотреб амінокислоти глікоза жирні кислоти АТФ Дезамінування та інші метаболічні перетворювання ГЛІКОЛІЗ (анаеробний процес) СФ β-окислення ЖК піруват NH 3 сечовина СО 2, Н 2 О ацетил-Ко. А NADH АТФ ЦТК О 2! окисне фосф-ня ОФ у ДЛ МТХ NADH Н 2 О
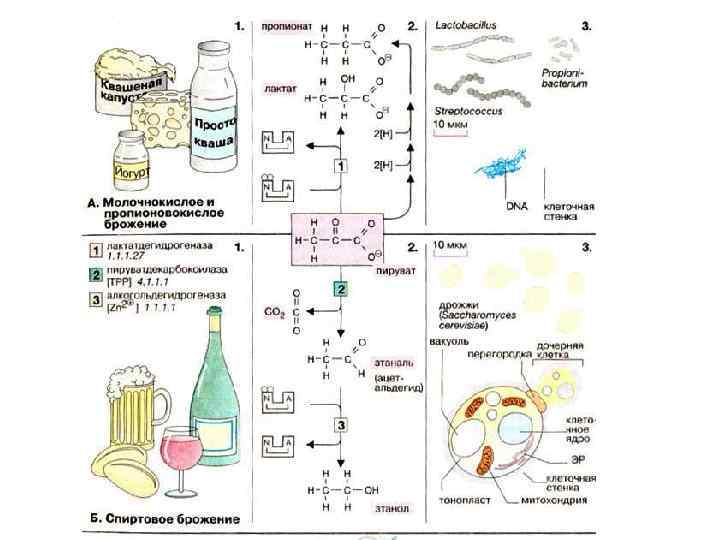
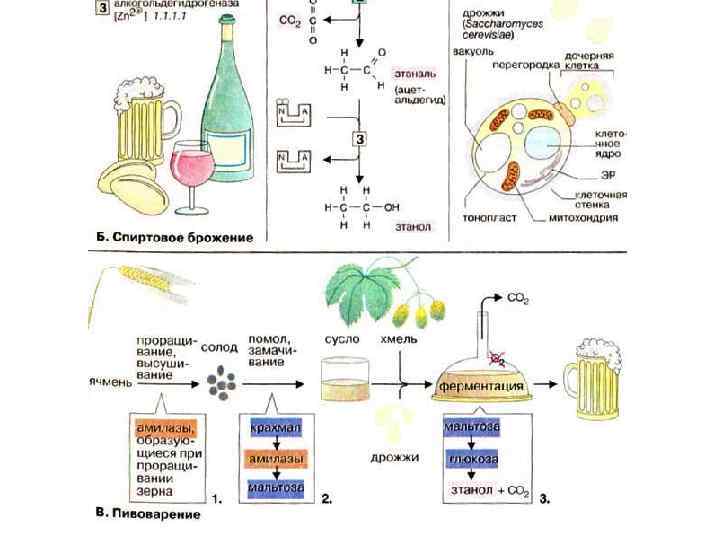
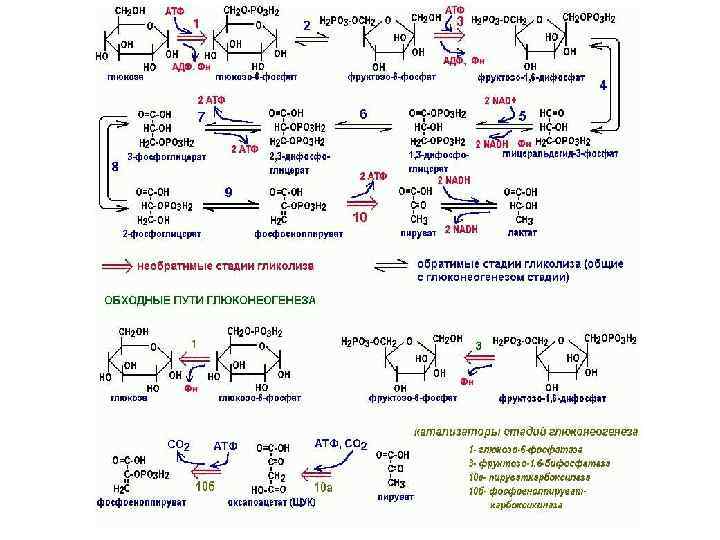

• Глюкоза 6 СО 2+Н 2 О ∆Go, = -2870 к. Дж/моль • Глюкоза 2 лактат ∆Go, = -196, 9 к. Дж/моль • Використовується лише близько 7% !
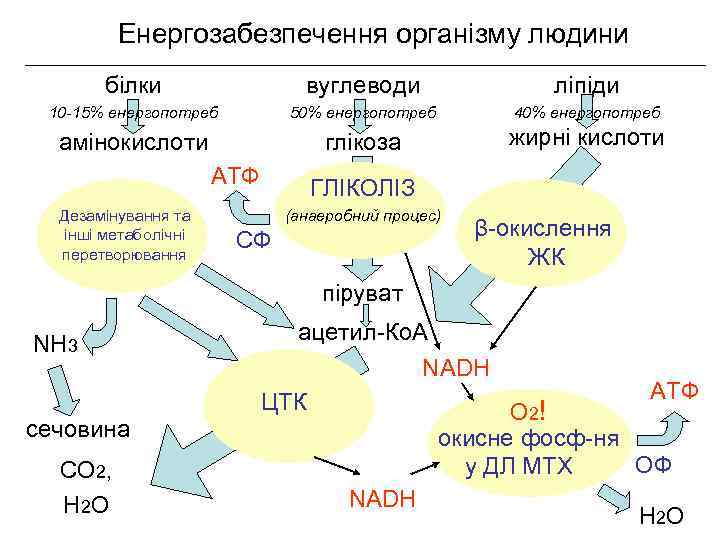
Енергозабезпечення організму людини білки вуглеводи ліпіди 10 -15% енергопотреб 50% енергопотреб 40% енергопотреб амінокислоти глікоза жирні кислоти АТФ Дезамінування та інші метаболічні перетворювання ГЛІКОЛІЗ (анаеробний процес) СФ β-окислення ЖК піруват NH 3 сечовина СО 2, Н 2 О ацетил-Ко. А NADH АТФ ЦТК О 2! окисне фосф-ня ОФ у ДЛ МТХ NADH Н 2 О
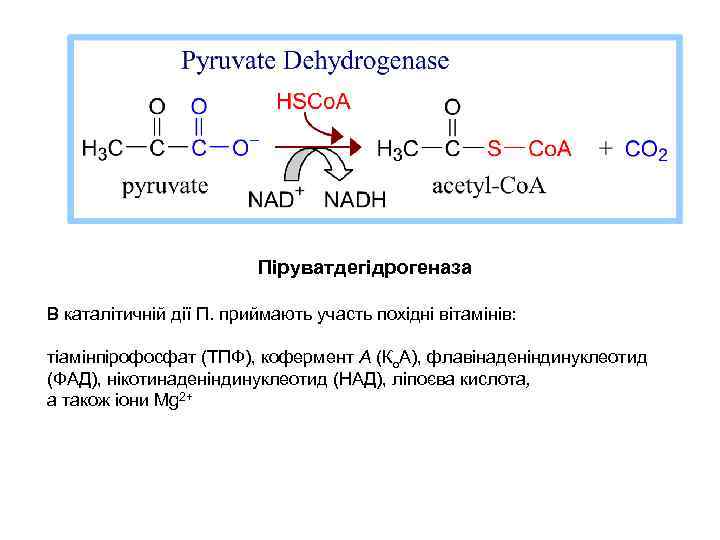
Піруватдегідрогеназа В каталітичній дії П. приймають участь похідні вітамінів: тіамінпірофосфат (ТПФ), кофермент А (Ко. А), флавінаденіндинуклеотид (ФАД), нікотинаденіндинуклеотид (НАД), ліпоєва кислота, а також іони Mg 2+
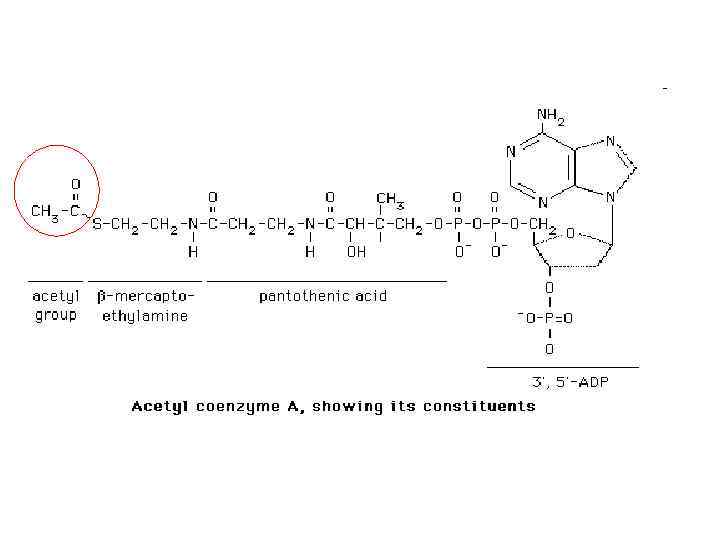
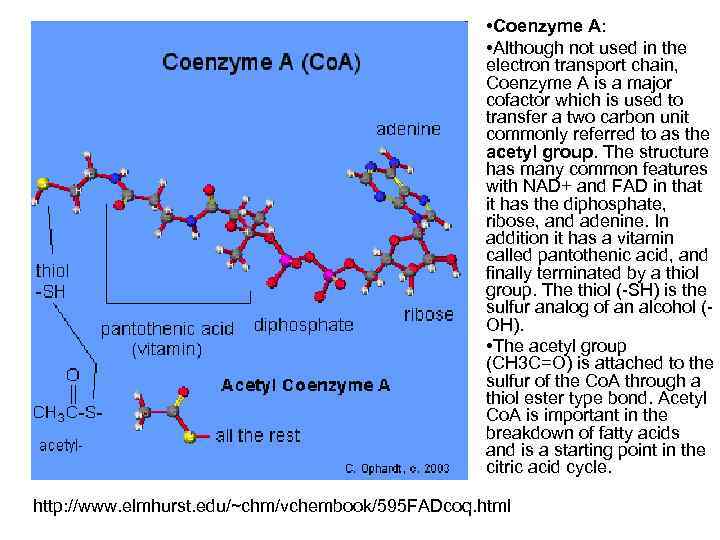
• Coenzyme A: • Although not used in the electron transport chain, Coenzyme A is a major cofactor which is used to transfer a two carbon unit commonly referred to as the acetyl group. The structure has many common features with NAD+ and FAD in that it has the diphosphate, ribose, and adenine. In addition it has a vitamin called pantothenic acid, and finally terminated by a thiol group. The thiol (-SH) is the sulfur analog of an alcohol (OH). • The acetyl group (CH 3 C=O) is attached to the sulfur of the Co. A through a thiol ester type bond. Acetyl Co. A is important in the breakdown of fatty acids and is a starting point in the citric acid cycle. http: //www. elmhurst. edu/~chm/vchembook/595 FADcoq. html

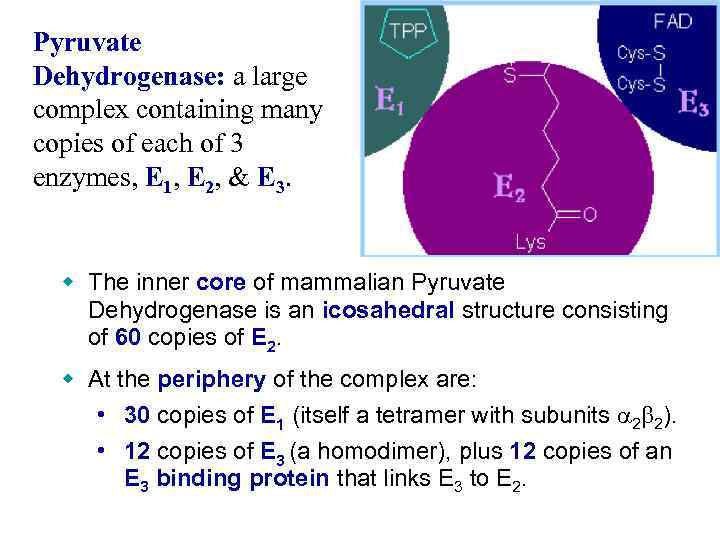
Pyruvate Dehydrogenase: a large complex containing many copies of each of 3 enzymes, E 1, E 2, & E 3. w The inner core of mammalian Pyruvate Dehydrogenase is an icosahedral structure consisting of 60 copies of E 2. w At the periphery of the complex are: • 30 copies of E 1 (itself a tetramer with subunits a 2 b 2). • 12 copies of E 3 (a homodimer), plus 12 copies of an E 3 binding protein that links E 3 to E 2.
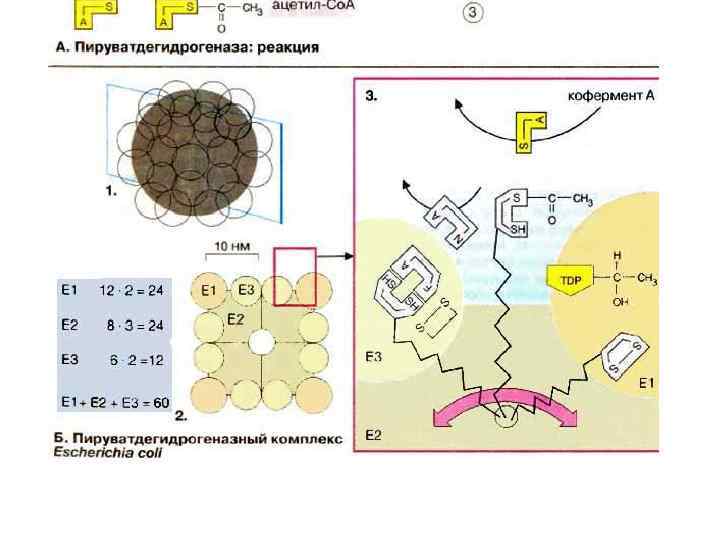

http: //www. brookscole. com/chemistry_d/tem plates/student_resources/shared_resource s/animations/pdc. html

Цикл трикарбонових кислот Цикл Кребса або цикл лимонної кислоти (1953 р. НП) - циклічний (1937 р. ) процес, який включає 8 стадій “Енергетичний вихід”: 3 молекули NADH (або 2 NADH + 1 NADPH) 1 молекула FADH+H+ 1 молекула ГТФ
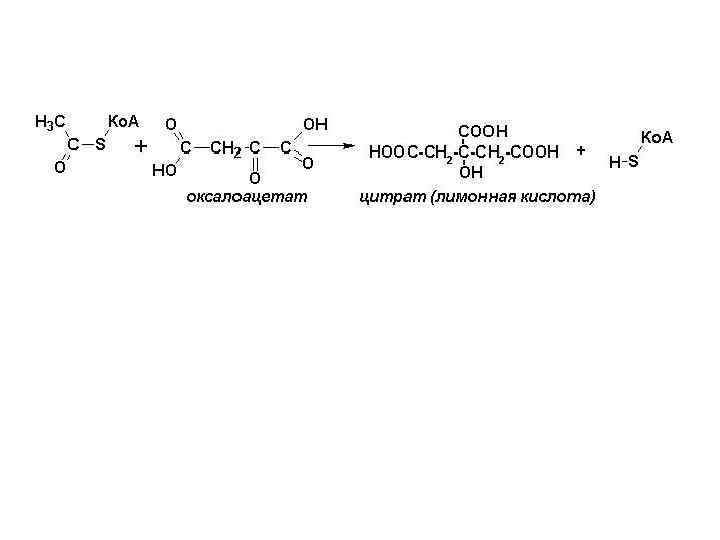
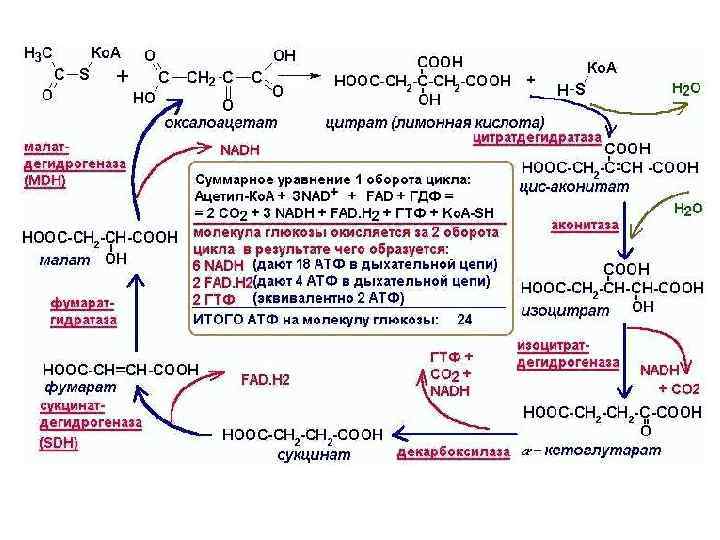
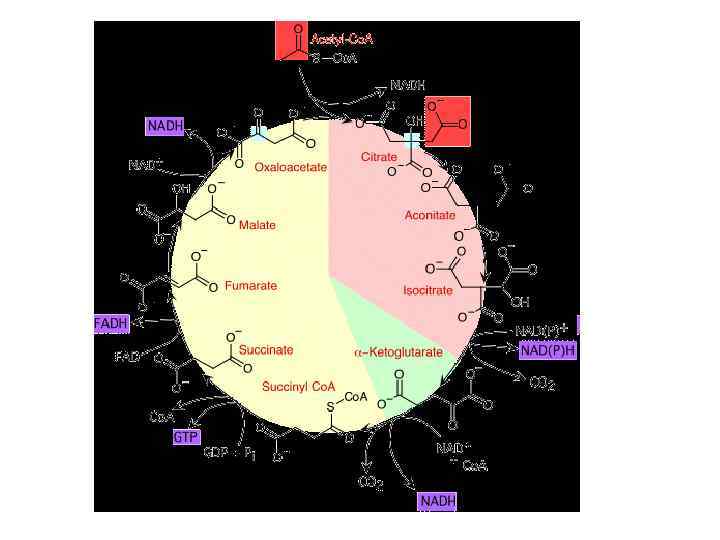
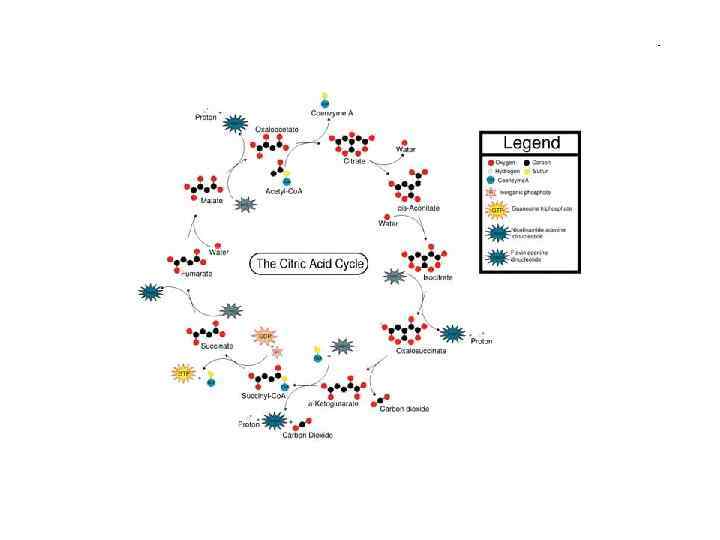

Цикл трикарбонових кислот При метаб. перетворенні 1 молекули ацетил Ко. А: 3 молекули NADH --------- 3 * 3 АТФ (або 2 NADH + 1 NADPH) 1 молекула FADH+H+------- 1 * 2 АТФ 1 молекула ГТФ ---------- 1 ______________ 12 АТФ + 1 молекула NADH -------- 3 АТФ При окисленні ацетилу виділяється 899 к. Дж. моль КПД - 40%
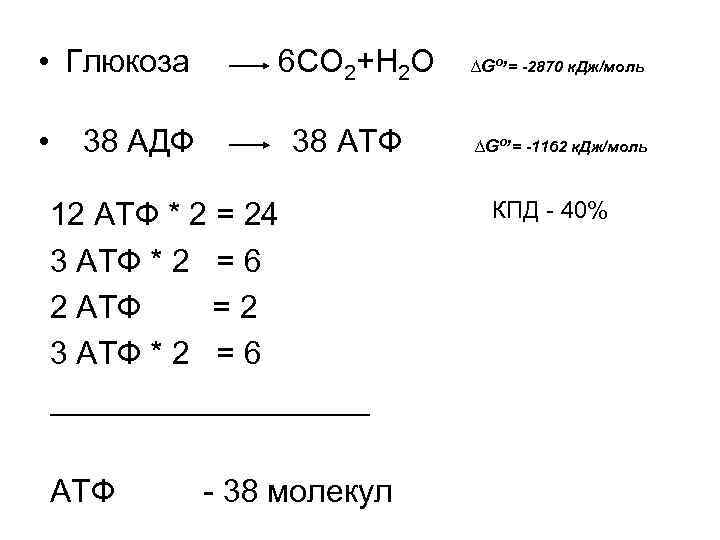
• Глюкоза 6 СО 2+Н 2 О ∆Go, = -2870 к. Дж/моль • 38 АДФ 38 АТФ ∆Go, = -1162 к. Дж/моль 12 АТФ * 2 = 24 3 АТФ * 2 = 6 2 АТФ = 2 3 АТФ * 2 = 6 _________ АТФ - 38 молекул КПД - 40%
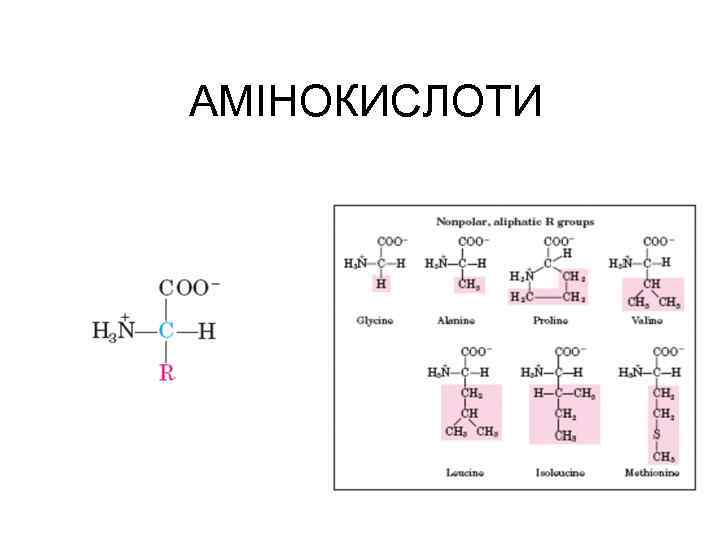
АМІНОКИСЛОТИ
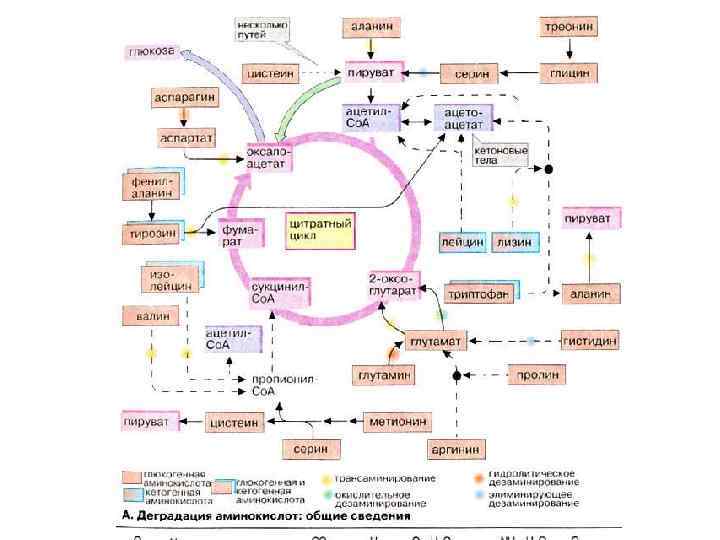
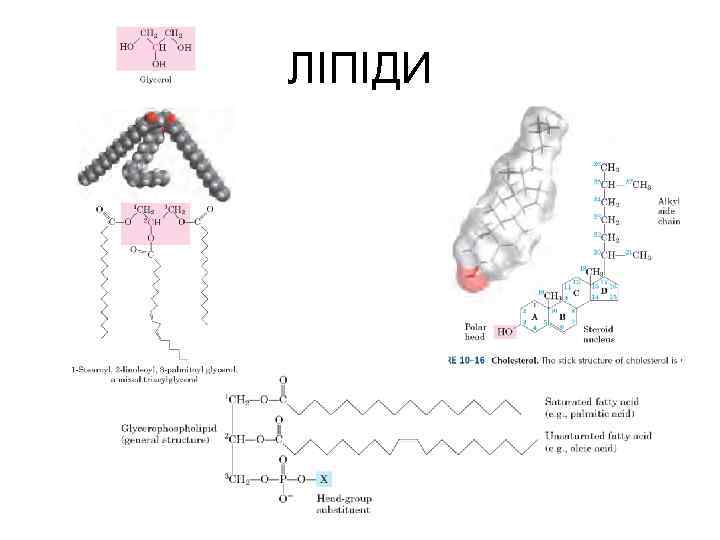
ЛІПІДИ
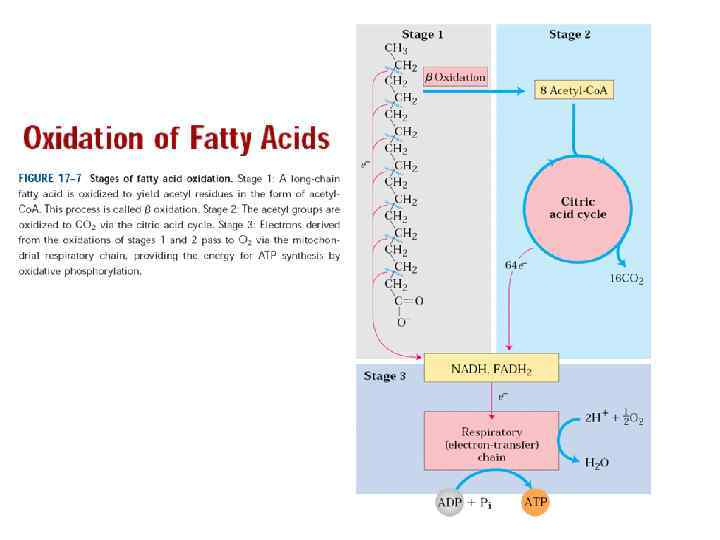
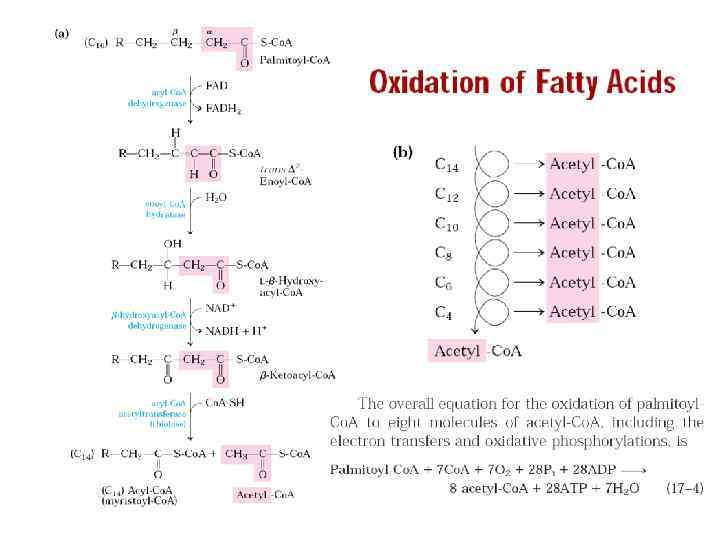
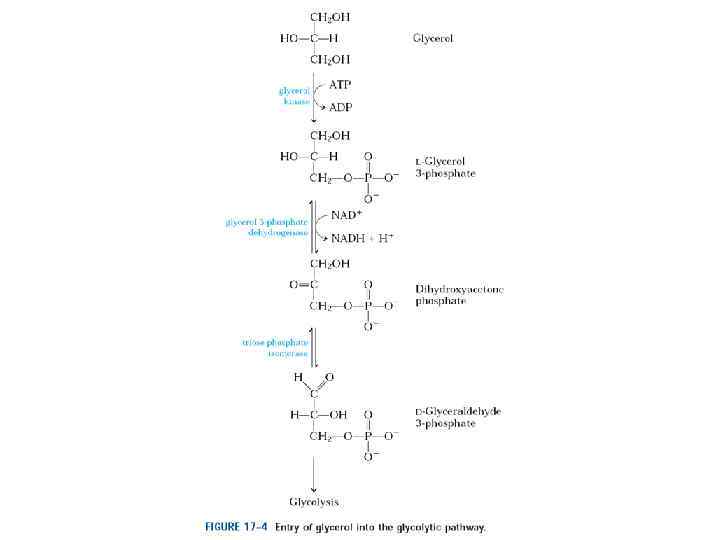

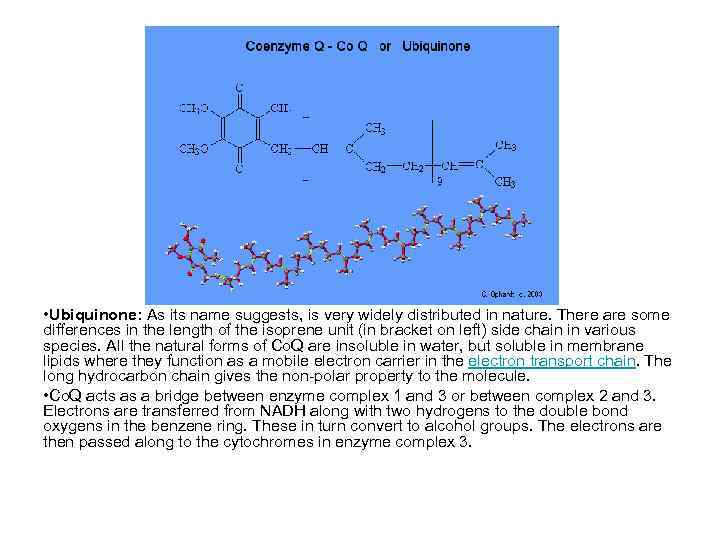
• Ubiquinone: As its name suggests, is very widely distributed in nature. There are some differences in the length of the isoprene unit (in bracket on left) side chain in various species. All the natural forms of Co. Q are insoluble in water, but soluble in membrane lipids where they function as a mobile electron carrier in the electron transport chain. The long hydrocarbon chain gives the non-polar property to the molecule. • Co. Q acts as a bridge between enzyme complex 1 and 3 or between complex 2 and 3. Electrons are transferred from NADH along with two hydrogens to the double bond oxygens in the benzene ring. These in turn convert to alcohol groups. The electrons are then passed along to the cytochromes in enzyme complex 3.
Bioenergetics 3lection 2012.ppt